母乳中含有复杂的微生物群落,其中常见的菌属包括链球菌属(Streptococcus)、乳杆菌属(Lactobacillus)、双歧杆菌属(Bifidobacterium)等,可作为筛选益生菌的重要来源[1-2]。20世纪中期以来,微生态制剂在食品、医药、畜牧等多个行业的发展日益成熟,Datalntelo上发布的报告中提出,预测到2032年,全球微生态制剂市场规模将由2023年的75亿美元增长至145亿美元,预测年复合增长率可达7.5%,发展前景较好。母乳源双歧杆菌作为国内外快速发展的微生态制剂中的主要菌种之一,其在影响脂肪代谢改善肥胖、增加肠道内短链脂肪酸缓解关节炎、改善免疫因子增强免疫力等方面的作用已经被证实[3-5]。
我国拥有自主知识产权且发展成熟的母乳源双歧杆菌较少,其在科研成果转化与实际应用方面仍存在不足。造成这一现象的主要原因为以下2点:a)母乳源双歧杆菌分离、培养手段有限,菌种资源匮乏。目前开发成熟的母乳源双歧杆菌仅有4株,其中3株来源于中国,分别是动物双歧杆菌乳亚种Probio-M8(中国内蒙古农业大学)、动物双歧杆菌乳亚种CP-9(中国锦旗生物公司)、青春双歧杆菌DB2458(中国台湾地区中兴大学)[6];b)受菌株特异性限制,母乳源双歧杆菌发酵水平普遍偏低,无法满足后续开发利用需求[7]。
动物双歧杆菌乳亚种IMAU12344 (Bifidobacterium animalis subsp.lactis IMAU12344)是分离自内蒙古呼和浩特市健康妇女母乳中的一株具有完全自主知识产权的菌株。前期研究表明该菌株具有良好的人工胃肠液耐受性,经人工模拟胃液(pH 2.5)处理3 h、人工模拟肠液(pH 8.0)处理8 h后,其存活率可达75%以上,但该菌株在改良MRS培养基中活菌数较低。因此探索适合该菌株的高密度发酵培养基及生长条件,对于其工业化生产具有重要意义。
本研究旨在针对内蒙古母乳源动物双歧杆菌乳亚种IMAU12344生长特性及营养需求,通过单因素试验、复配实验、Plackett-Burman实验、最陡爬坡实验及响应面试验多种方法联用确定该菌株的最优培养基配方。在最优培养基的基础上,对其最佳静态培养条件(初始pH值、培养温度、接种量)进行优化,最后进行高密度发酵验证,以有效提升其发酵水平,为该菌株工业化生产提供数据和理论支持。
1 材料与方法
1.1 材料与试剂
动物双歧杆菌乳亚种IMAU12344由国家饲料微生物种质资源库(内蒙古)提供。
D-葡萄糖、D-乳糖、D-麦芽糖、D-棉子糖、D-蔗糖,山东丰泰生物科技有限公司;酵母膏、牛肉膏、酵母提取粉、大豆蛋白胨、酵母蛋白胨、酵母浸出粉、牛肉浸粉、牛肝浸粉,安琪酵母股份有限公司;水解乳蛋白、蛋白胨、鱼蛋白胨、月示蛋白胨、酪蛋白胨、胰蛋白胨,广东环凯微生物科技有限公司;磷酸氢二钠、磷酸二氢钠、氢氧化钠、柠檬酸、磷酸氢二钾、柠檬酸钠、无水乙酸钠、磷酸二氢钾,青岛海信生物化学有限公司;ZnSO4·7H2O、CuSO4·5H2O、MgSO4·7H2O、MnSO4·5H2O、FeSO4·7H2O,昌乐鼎博化工有限公司;维生素B1、维生素B5、维生素B6、维生素B2、叶酸、生物素、烟酸,国药集团化学试剂有限公司;鸟嘌呤、胸腺嘧啶、尿嘧啶、腺嘌呤、次黄嘌呤、β-胸苷、苏氨酸、色氨酸、苯丙氨酸、精氨酸、脯氨酸、半胱氨酸、缬氨酸、组氨酸、丙氨酸、酪氨酸、异亮氨酸、亮氨酸、丝氨酸、赖氨酸、天门冬氨酸,北京Solarbio科技有限公司。
1.2 仪器与设备
ZHJH-C1112C无菌工作台,智城分析仪器有限公司;SX-700高压蒸汽灭菌锅,日本Tomy Digital Biology公司;SpectraMax M2酶标仪,美国Molecular Devices公司;LIT-700 W生化培养箱,一恒科学仪器有限公司;BX-53光学显微镜,日本OLYMPUS公司。
1.3 实验方法
1.3.1 菌株活化
将保藏于-80 ℃超低温冰箱中的动物双歧杆菌乳亚种IMAU12344菌种管取出,以2%(体积分数)的接种量接种于改良MRS培养基,37 ℃厌氧培养(24±0.5) h。连续活化3代后,4 ℃保存备用。
1.3.2 活菌数及菌体密度的测定
按10倍稀释法,选取合适梯度将培养液稀释,吸取1 mL稀释液注入改良MRS琼脂培养基培养皿中,37 ℃厌氧培养(72±0.5) h后计菌落总数。
选取合适梯度稀释培养液,利用酶标仪测定菌株在600 nm波长下的菌体密度。
1.3.3 培养基配方优化
将活化3代后的IMAU12344培养液,吸取至API 50CHL碳水化合物鉴定试剂条中,无菌液体石蜡封口,37 ℃恒温厌氧培养72 h后记录结果。根据碳水化合物代谢特性研究结果,挑选出可被IMAU12344利用的碳源代替改良MRS培养基中的碳源,保持其他成分不变。菌株以2%(体积分数)的接种量接种至培养基中,37 ℃厌氧培养24 h,测定菌体密度及活菌数,确定最优碳源。而后在其他成分不变的基础上,分别添加总量为2.5%(质量分数)的植物氮源、动物氮源、微生物氮源等14种氮源,进行最优氮源筛选。在上述实验基础上,对培养基中碳氮源的总量(1%~15%)及比例(1∶3、1∶2、1∶1、2∶1、3∶1)进行优化。最后依次对缓冲盐体系(磷酸氢二钠-磷酸二氢钠、磷酸二氢钾-氢氧化钠、磷酸氢二钠-柠檬酸、柠檬酸-柠檬酸钠、磷酸二氢钾-磷酸二氢钠、柠檬酸-无水乙酸钠- K2HPO4)、微量元素(ZnSO4·7H2O、CuSO4·5H2O、MgSO4·7H2O、MnSO4·5H2O、FeSO4·7H2O)、生长因子(维生素B1、维生素B5、维生素B6、维生素B2、叶酸、生物素、烟酸、鸟嘌呤、胸腺嘧啶、尿嘧啶、腺嘌呤、次黄嘌呤、β-胸苷、苏氨酸、色氨酸、苯丙氨酸、精氨酸、脯氨酸、L-半胱氨酸、缬氨酸、组氨酸、丙氨酸、酪氨酸、异亮氨酸、亮氨酸、丝氨酸、赖氨酸、天门冬氨酸)等进行优化。
在上述优化的基础上使用Design Expert 12.0软件设计Plackett-Burman实验,确定培养基中主要因素及其效应,在Plackett-Burman实验结果的基础上设计最陡爬坡实验确定主要因素的中心点。最后设计响应面优化实验,确定最优培养基配方。
1.3.4 培养条件优化
在最优培养基配方基础上,选取不同体积分数接种量(2%、4%、6%、8%)、初始pH(5.0、5.5、6.0、6.5、7.0、7.5、8.0)及培养温度(25、30、37、42 ℃)进行单因素试验确定最佳静态培养条件。
1.3.5 高密度发酵优化验证
参考胡殿庚[8]乳双歧杆菌V9高密度发酵生产工艺,采用恒温37 ℃、初始pH值6.5、恒值pH 5.9、中和剂25%(质量分数)氨水、保压气体氮气、搅拌速率200 r/min的工艺,每隔1 h测定菌体密度,前后菌体密度差异不显著时终止发酵,取发酵液活菌计数进行高密度发酵培养验证。
1.4 数据处理
所有实验均设置3组重复,采用Excel 2019和SPSS 22.3软件分析处理数据,结果以“平均值±标准差”的形式表示。各组间的比较采用单因素方差分析,采用LSD法分析差异显著性,P<0.05为差异显著。
2 结果与分析
2.1 培养基配方的优化
2.1.1 碳源优化
培养基中的碳源不仅是主要能源物质,还参与培养物细胞的构成。受菌株特异性影响,不同菌株对碳源的利用存在差异。本研究通过API 50 CHL碳水化合物鉴定试剂条(法国bio Merieux公司)对IMAU12344可利用碳源种类进行研究,明确其碳源谱,结果如表1所示。可被IMAU12344利用的碳源共12种,考虑到工业化低成本生产原则,选取D-葡萄糖、D-麦芽糖、D-乳糖、D-蔗糖和D-棉子糖进行下一步优化实验。
表1 菌株碳水化合物代谢实验结果
Table 1 Results of carbohydrate metabolism test of the strains

序号底物成分反应结果序号底物成分反应结果0阴性对照 -25七叶灵(柠檬酸铁) +1丙三醇 -26水杨苷 +2赤藓糖醇 -27 D-纤维二糖 -3D-阿拉伯糖 -28D-麦芽糖 +4L-阿拉伯糖 -29D-乳糖 +5D-核糖 +30D-蜜二糖 +6D-木糖 -31D-蔗糖 +7L-木糖 -32D-海藻糖 -8D-核糖醇 -33菊粉 -9甲基-β-D-吡喃木糖苷 -34D-松三糖 -10D-半乳糖 -35D-棉子糖 +11D-葡萄糖 +36淀粉 -12D-果糖 -37糖原 -13D-甘露糖 -38木糖醇 -14L-山梨糖 -39D-龙胆二糖 +15L-鼠李糖 -40D-土伦糖 +16卫矛醇 -41D-来苏糖 -17肌醇 -42D-塔格糖 -18甘露醇 -43D-岩藻糖 -19山梨醇 -44L-岩藻糖 -20甲基-α-D-吡喃甘露糖苷 -45D-阿拉伯醇 -21甲基-α-D-吡喃葡萄糖苷 -46L-阿拉伯醇 -22N-乙酰葡萄糖胺 -47葡萄糖酸钾 -23苦杏仁苷 +482-酮基葡萄糖酸钾 -24熊果苷 -495-酮基葡萄糖酸钾 -
注:“+”表示可利用碳源,“-”表示不可利用碳源。
如图1所示,当碳源为D-乳糖时,IMAU12344活菌数和菌体密度分别可达(1.60±0.01)×109 CFU/mL、3.26±0.02,优于其他碳源。这是由于双歧杆菌在代谢乳糖的过程中可通过β-半乳糖苷酶代谢产生短链脂肪酸(short chain fatty acid,SCFA),SCFA可进一步促进双歧杆菌生长[9]。徐显睿等[10]对乳双歧杆菌Z-1最适高密度发酵培养基进行优化时发现,选取乳糖作为碳源时,乳双歧杆菌Z-1的活菌数最高,可达1.9×109 CFU/mL,优于其他碳源。这与本研究结果一致,因此选择D-乳糖进行下一步优化实验。
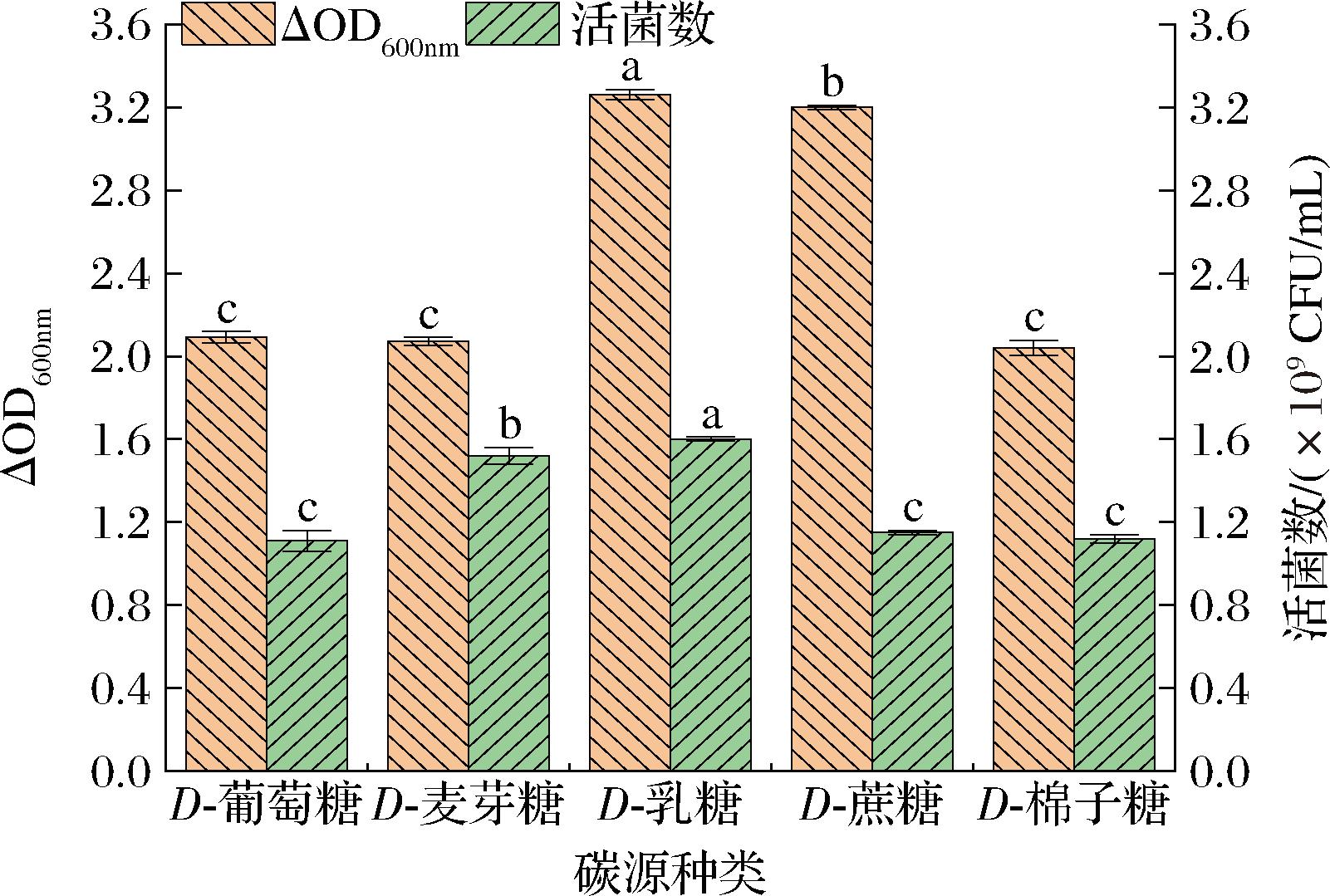
图1 不同碳源对菌株菌体密度及活菌数的影响
Fig.1 The effect of different carbon on the density and viable count of strains
注:不同小写字母表示IMAU12344在不同培养基中菌体密度及活菌数的差异显著(P<0.05)(下同)。
2.1.2 氮源优化
由于不同菌株蛋白质分解代谢能力差异巨大,因此其所需的最适氮源也不尽相同[11]。本研究选取植物源、动物源、微生物源等14种氮源代替改良MRS培养基中的复合氮源,进行优化,结果如图2所示。添加酵母蛋白胨为氮源时,IMAU12344菌体密度最高,达到3.52±0.02。而酵母提取粉、蛋白胨、酵母浸出粉、鱼蛋白胨、牛肉膏等5种氮源对菌体密度的影响无显著性差异(P>0.05),均高于改良MRS中的复合氮源。
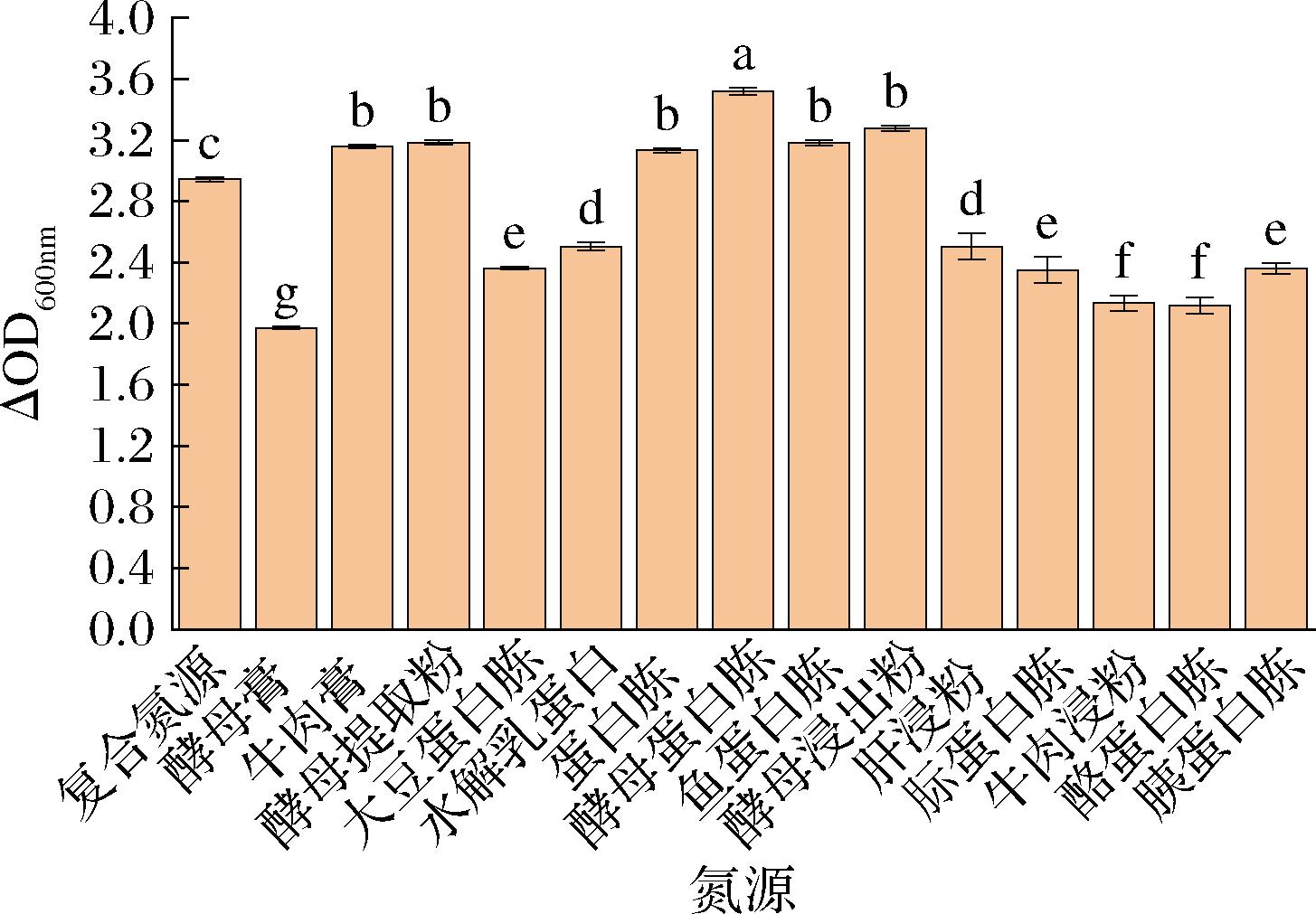
图2 不同氮源对菌株菌体密度的影响
Fig.2 The effect of different nitrogen sources on the density of strains
为进一步验证其培养效果,对含上述氮源的培养基进行计数,结果如表2所示。当氮源为酵母蛋白胨时,IMAU12344活菌数最高,可达(2.22±0.04)×109 CFU/mL,是改良MRS培养基的2倍。这是因为酵母蛋白胨中含有大量的双歧杆菌生长促进因子(如含氮化合物、维生素、嘌呤碱和嘧啶碱等),这些物质可使双歧杆菌生长更加旺盛[12]。
表2 不同氮源对菌株活菌数的影响
Table 2 The effects of different nitrogen sources on the number of viable count of the strain
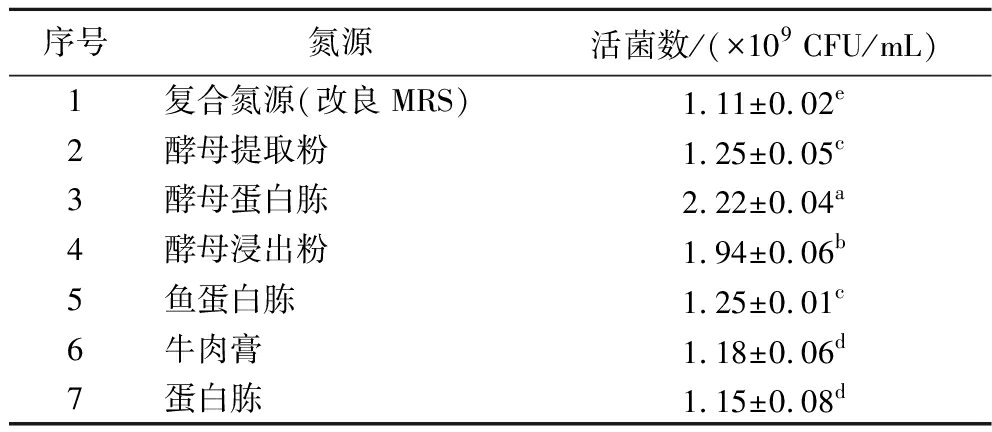
序号氮源 活菌数/(×109 CFU/mL) 1复合氮源(改良MRS)1.11±0.02e2酵母提取粉1.25±0.05c3酵母蛋白胨2.22±0.04a4酵母浸出粉1.94±0.06b5鱼蛋白胨1.25±0.01c6牛肉膏1.18±0.06d7蛋白胨1.15±0.08d
注:不同小写字母表示IMAU12344在不同培养基中活菌数的差异显著(P<0.05)(下同)。
复配氮源对菌株生长的影响是否优于单一氮源,是高密度发酵的研究热点之一。谢为天等[13]认为对比单一氮源,将不同氮源以不同比例复配更适合作为培养基的最终氮源。而高欣伟等[14]认为菌株对氮源的利用程度取决于氮源是否富含生长因子和自身对氮源的偏好性,而不是复配氮源一定强于单一氮源。
在上述研究的基础上,本研究选取酵母提取粉、酵母浸出粉及鱼蛋白胨3种氮源与酵母蛋白胨以1∶1的质量比复配实验,结果如表3所示。当酵母蛋白胨与酵母浸出粉以1∶1的质量比复配时,其活菌数与酵母蛋白胨单独作为氮源时无显著差异(P>0.05),说明酵母蛋白胨即可满足IMAU12344的生长需要。
表3 不同复配氮源对菌株活菌数的影响
Table 3 The effect of different nitrogen source compounding ratios on the viable count of strains

序号氮源 活菌数/(×109CFU/mL) 1酵母蛋白胨 2.22±0.04a2酵母蛋白胨+酵母浸出粉 2.12±0.05a3酵母蛋白胨+酵母提取粉 1.85±0.01b4酵母蛋白胨+鱼蛋白胨 1.64±0.02c
2.1.3 碳氮总量及比例优化
碳源、氮源的总量及比例,对菌株细胞壁的合成、核酸的产生和代谢的稳定均有一定的影响[15]。本研究在上述优化条件基础上,设置不同的碳氮总量(1%~15%)及比例(1∶3、1∶2、1∶1、2∶1、3∶1)进行优化。如图3所示,碳氮总量对菌株的菌体密度具有显著影响(P<0.05),随着碳氮总量的增加,菌体密度迅速增加。当碳氮总量达到8%时,菌体密度改为缓慢上升。此外,当碳氮比为1∶1时IMAU12344可获得较高的菌体密度。
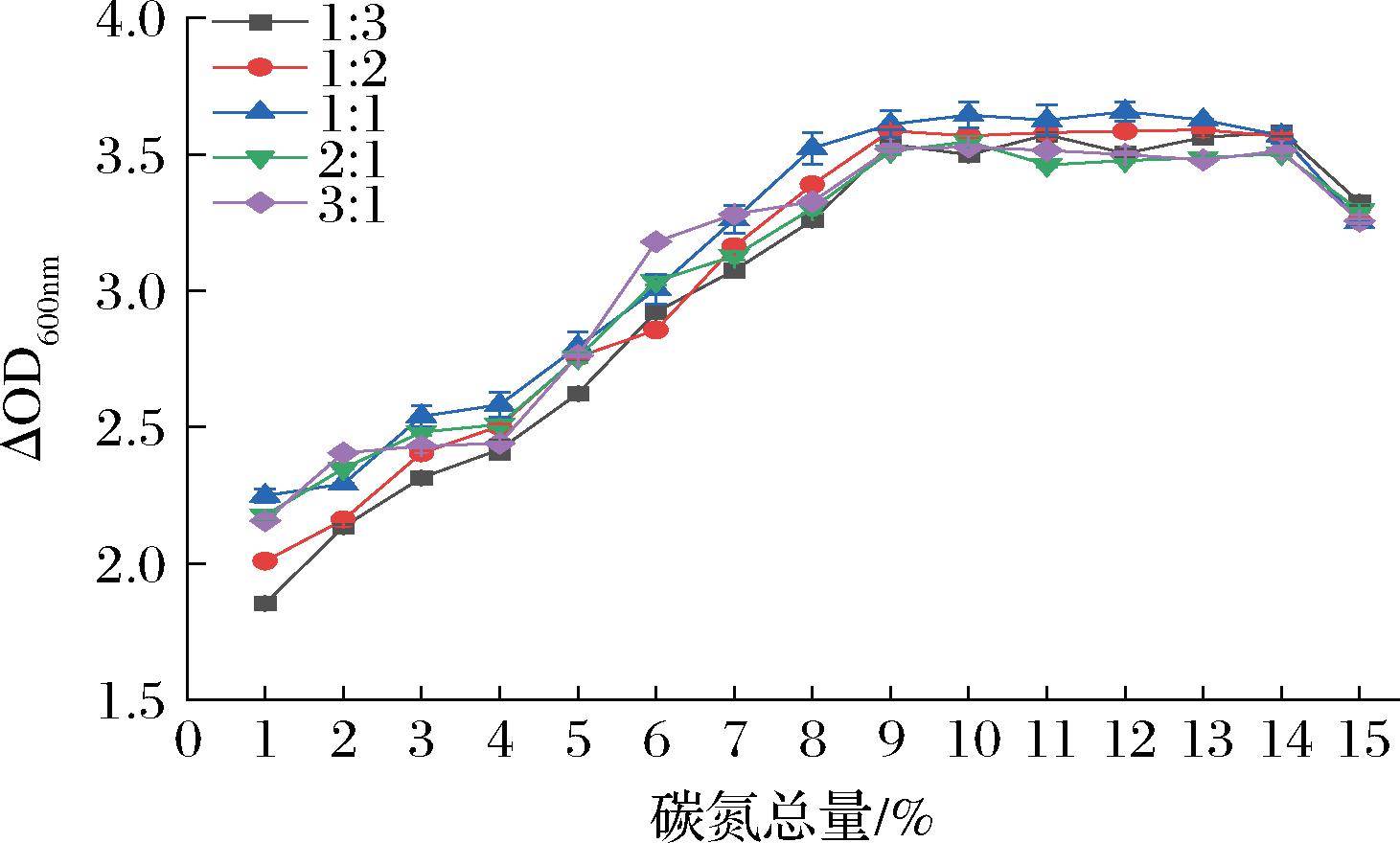
图3 不同碳氮总量及比例对菌株菌体密度的影响
Fig.3 The effect of different concentration and proportions on the density of strains
为进一步验证,本研究选取菌体密度较高的4组进行活菌计数,结果如表4。当碳氮总量为12%、碳氮比为1∶1时,活菌数达到最高,为(3.08±0.06)×109 CFU/mL,因此选取该组进行下一步实验。
表4 不同碳氮总量对菌株活菌数的影响
Table 4 The effect of different concentration on the viable count of strains
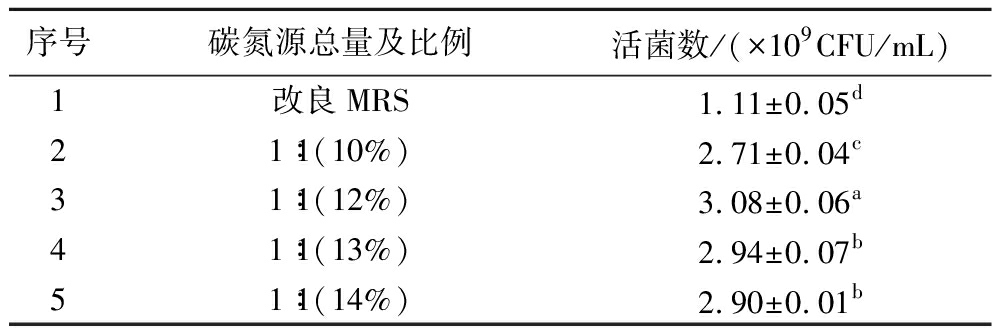
序号碳氮源总量及比例 活菌数/(×109CFU/mL) 1改良MRS1.11±0.05d21∶1(10%)2.71±0.04c31∶1(12%)3.08±0.06a41∶1(13%)2.94±0.07b51∶1(14%)2.90±0.01b
2.1.4 缓冲盐体系优化
双歧杆菌在发酵过程中会利用碳水化合物生成大量酸性物质,造成环境pH值快速降低,影响菌体生长繁殖,而适量的缓冲盐体系可以通过中和酸性物质调节培养环境pH值。因此本研究选取6种不同的缓冲盐体系进行优化实验。结果如图4所示,随着培养基中缓冲盐体系浓度的增加,IMAU12344菌体密度呈下降趋势。
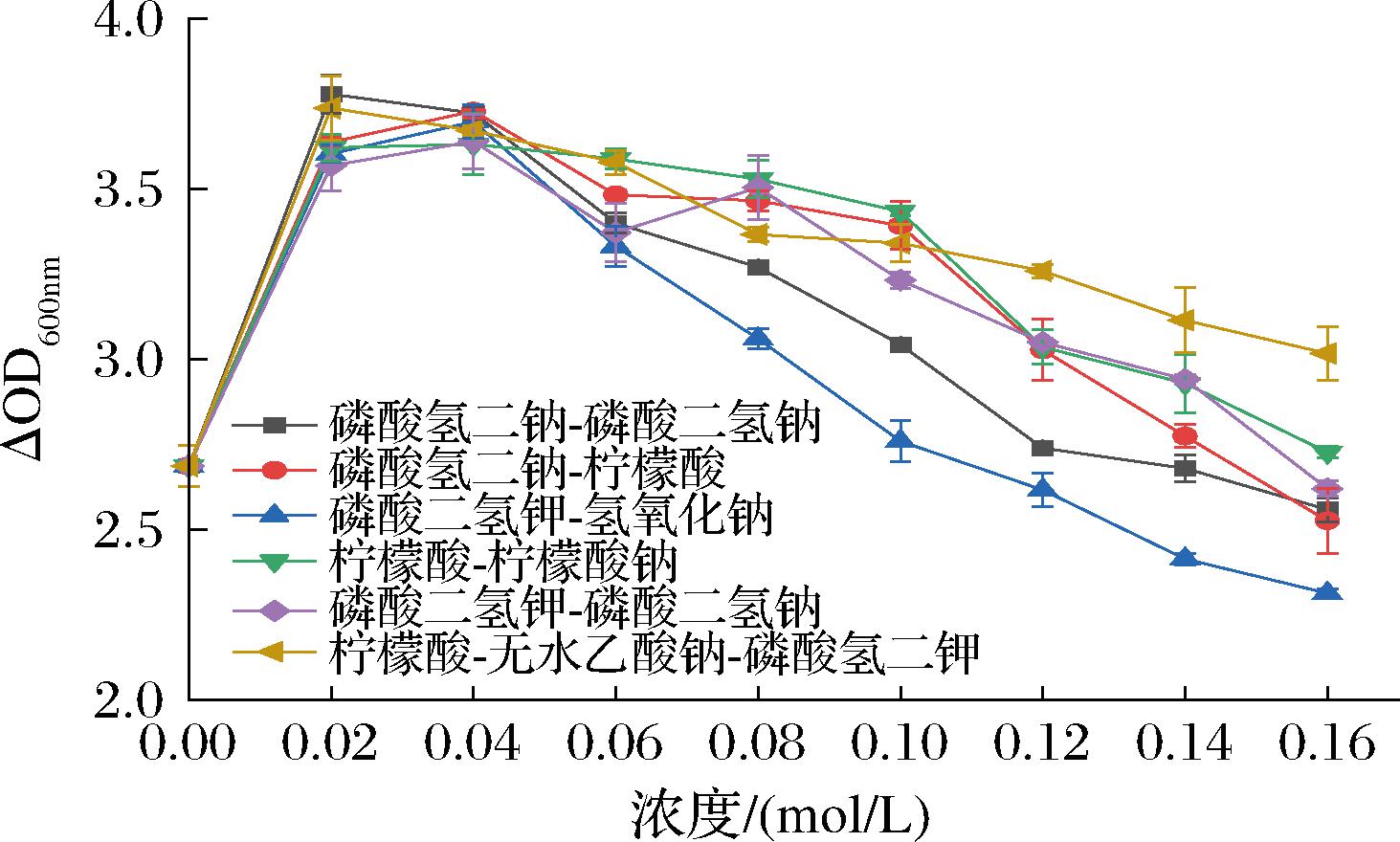
图4 不同缓冲盐体系对菌株菌体密度的影响
Fig.4 The effect of different buffer salts on the density of strains
为进一步确定最适缓冲盐体系,选取菌体密度较高的4组(0.04 mol/L磷酸氢二钠-柠檬酸、0.02 mol/L磷酸氢二钠-磷酸二氢钠、0.04 mol/L磷酸氢二钠-磷酸二氢钠、0.02 mol/L柠檬酸-无水乙酸钠-磷酸氢二钾)进行活菌计数并与空白对照组进行比较。结果如表5所示,当添加0.04 mol/L磷酸氢二钠-磷酸二氢钠为缓冲盐体系时,IMAU12344活菌数最高,为(3.57±0.03)×109 CFU/mL,显著高于其他组(P<0.05)。
表5 不同缓冲盐体系对菌株活菌数的影响
Table 5 The effect of different buffer salts on the viable count of strains
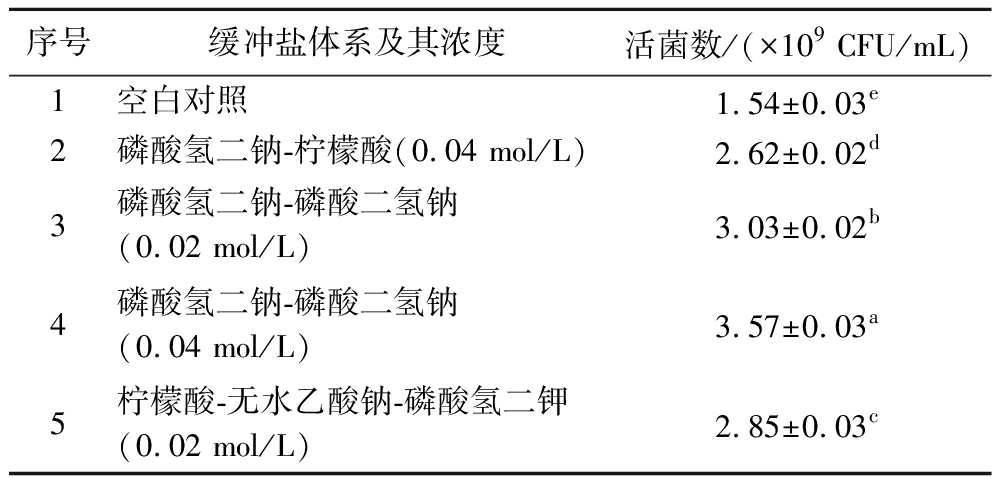
序号 缓冲盐体系及其浓度 活菌数/(×109 CFU/mL) 1空白对照1.54±0.03e2磷酸氢二钠-柠檬酸(0.04 mol/L)2.62±0.02d3磷酸氢二钠-磷酸二氢钠(0.02 mol/L)3.03±0.02b4磷酸氢二钠-磷酸二氢钠(0.04 mol/L)3.57±0.03a5柠檬酸-无水乙酸钠-磷酸氢二钾(0.02 mol/L)2.85±0.03c
2.1.5 微量元素优化
微量元素既能够参与菌体细胞的构成,也能够为菌体提供生物活性物质,还有着提高菌株酸碱耐受度、温度耐受度的功效[16]。本研究参考马琳[17]的研究,选取5种不同微量元素,并设置不同浓度进行微量元素优化。结果如图5所示,添加MnSO4·5H2O的组别,菌体密度显著高于其他组别(P<0.05)。添加160 mg/L MnSO4·5H2O时菌体密度最高。这是由于Mn2+可作为辅助因子与活性位点结合,促进菌株细胞内酶的催化。如双歧杆菌中的果糖-6-磷酸酮糖酶、乙酸激酶、转酮醇酶等酶,均需要Mn2+作为辅助因子帮助其发挥作用[18-19]。
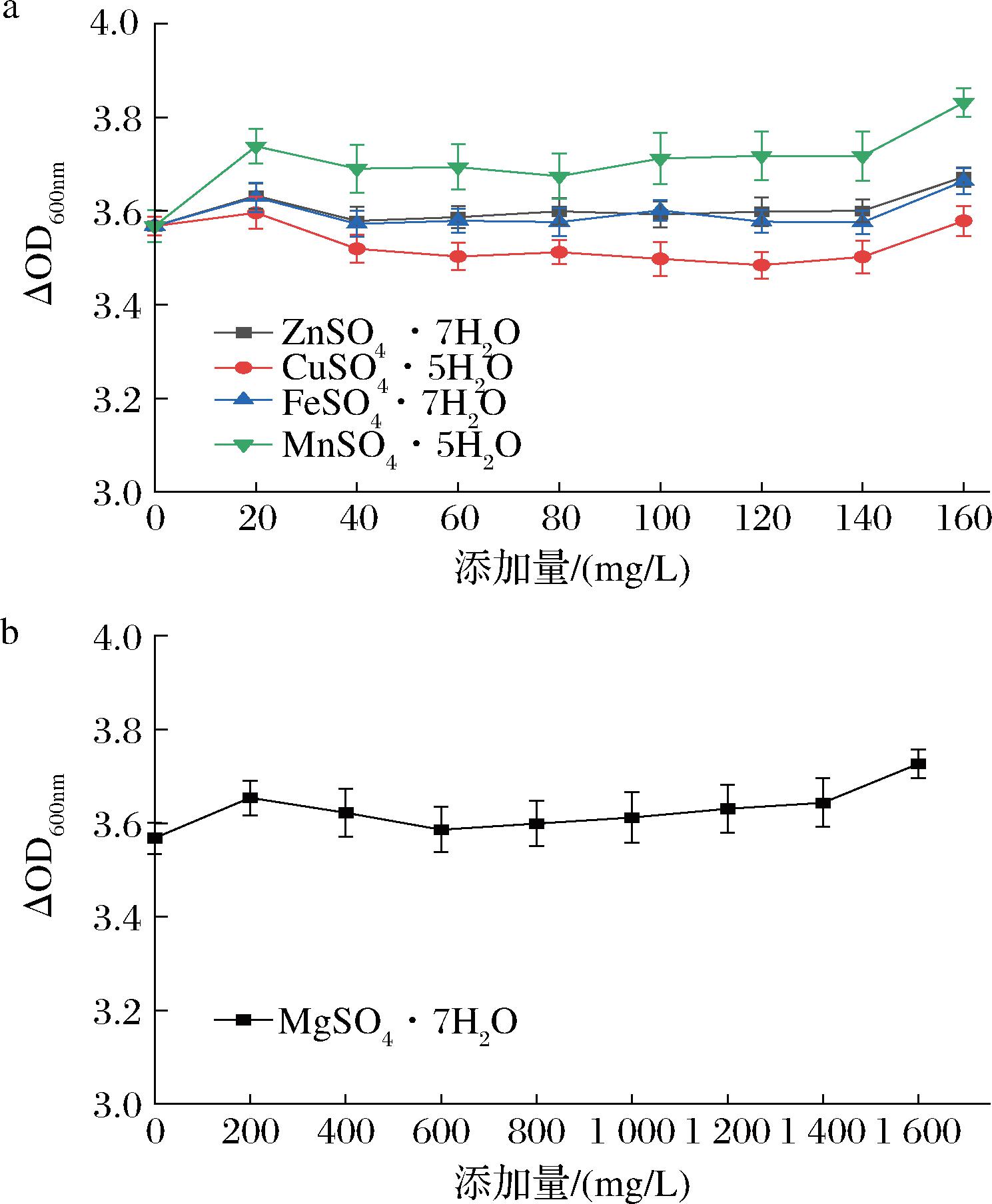
a-ZnSO4·7H2O、CuSO4·5H2O、FeSO4·7H2O、MnSO4·5H2O添加量对菌体密度的影响;b-MgSO4·7H2O添加量对菌体密度的影响
图5 不同微量元素对菌株菌体密度的影响
Fig.5 The effect of different trace elements on the density of strains
考虑到添加160 mg/L MnSO4·5H2O后菌体密度仍呈上升趋势,本研究选取不同质量浓度(120、140、160、180、200 mg/L)MnSO4·5H2O进行进一步优化,并与空白对照组进行比较,结果如表6所示。当添加160 mg/L MnSO4·5H2O时IMAU12344活菌数达到最高,为(3.75±0.25)×109 CFU/mL,显著高于其他组别(P<0.05)。因此选择该组进行后续实验。
表6 不同浓度MnSO4·5H2O对菌株活菌数的影响
Table 6 The effect of different concentrations MnSO4·5H2O on the viable count of strains

序号微量元素及其浓度 活菌数/(×109 CFU/mL) 1空白对照1.59±0.01f2MnSO4·5H2O (120 mg/L)2.41±0.28e3MnSO4·5H2O (140 mg/L)2.98±0.12d4MnSO4·5H2O (160 mg/L)3.75±0.25a5MnSO4·5H2O (180 mg/L)3.26±0.16b6MnSO4·5H2O (200 mg/L)3.15±0.07c
2.1.6 生长因子优化
生长因子是指微生物难以自身合成的,对其生长具有促进意义的物质,常见的生长因子包括一些核苷酸、氨基酸、维生素类物质[20]。本实验通过查阅文献选取28种不同生长因子进行优化实验,结果如图6所示。IMAU12344对各生长因子的利用趋势相同,均呈现先下降后上升的趋势,当添加L-半胱氨酸盐酸盐为生长因子时,IMAU12344的菌体密度显著高于其他组别(P<0.05)。这是由于L-半胱氨酸盐酸盐可去除环境中的游离氧降低氧化还原电势,为厌氧菌提供一个还原性环境促进其生长[21]。
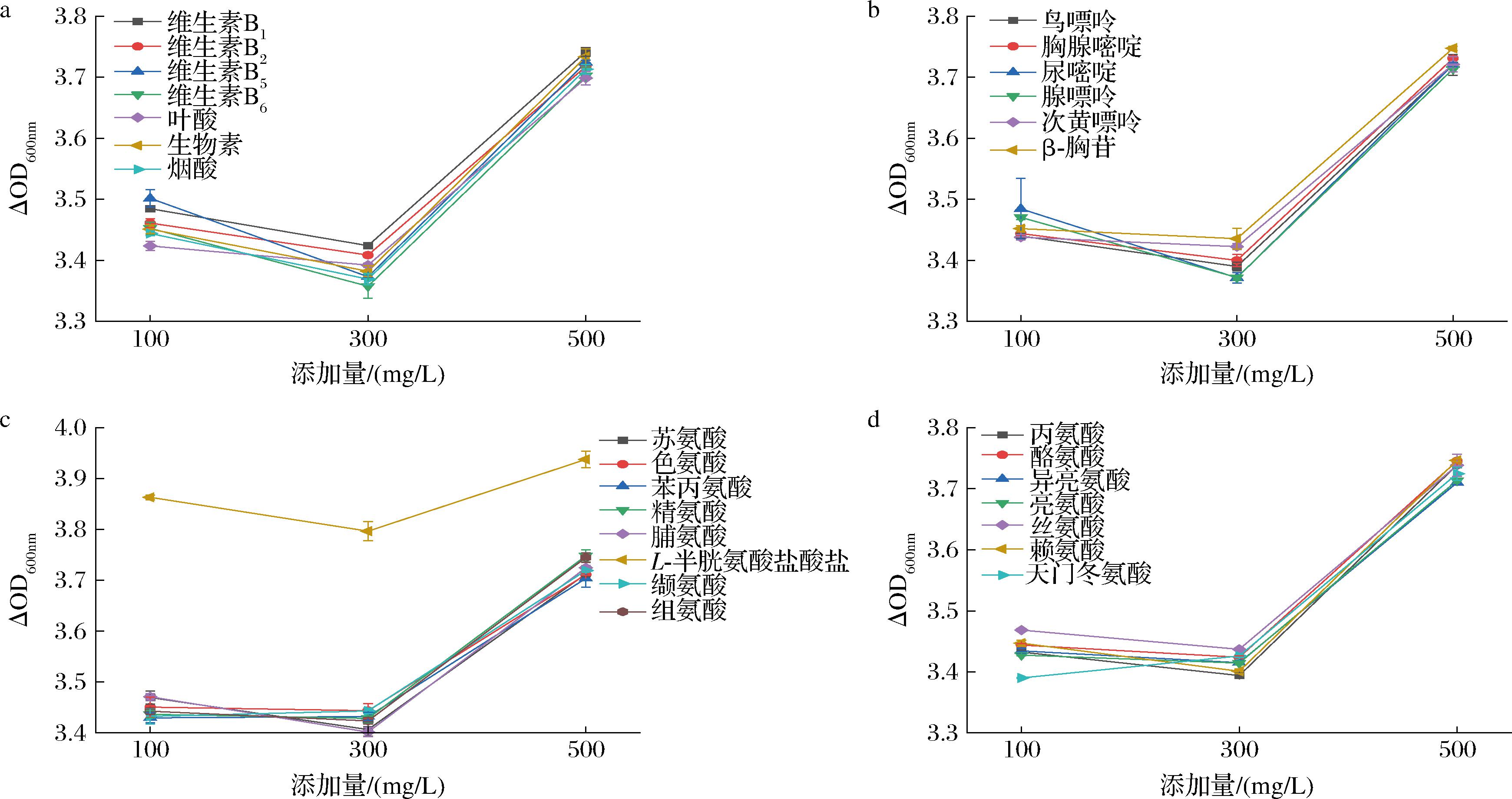
a-维生素类生长因子对菌体密度的影响;b-核苷酸类生长因子对菌体密度的影响;c-氨基酸类生长因子对菌体密度的影响;d-氨基酸类生长因子对菌体密度的影响
图6 不同生长因子对菌株菌体密度的影响
Fig.6 The effect of different growth factors on the density of strains
由于在添加500 mg/L L-半胱氨酸盐酸盐后菌体密度仍呈现上升趋势,因此实验选取不同质量浓度的L-半胱氨酸盐酸盐(100、300、500、700、900 mg/L)进行活菌计数,并与不添加生长因子的空白对照组进行比较进行进一步筛选。由表7可知,当添加500 mg/L的L-半胱氨酸盐酸盐为生长因子时,IMAU12344的活菌数达到最高,为(4.48±0.08)×109 CFU/mL,故选择此添加量进行下一步实验。
表7 不同浓度L-半胱氨酸盐酸盐对菌株活菌数的影响
Table 7 The effects of different concentrationsL- cysteine hydrochloride on the viable count of strains
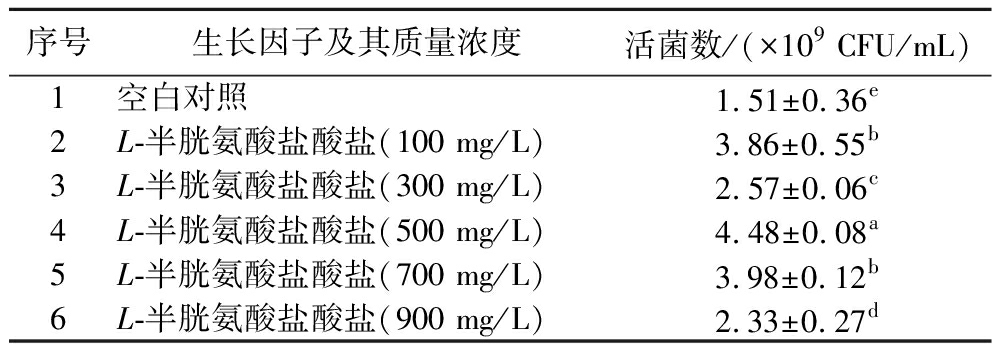
序号生长因子及其质量浓度 活菌数/(×109 CFU/mL) 1空白对照1.51±0.36e2L-半胱氨酸盐酸盐(100 mg/L)3.86±0.55b3L-半胱氨酸盐酸盐(300 mg/L)2.57±0.06c4L-半胱氨酸盐酸盐(500 mg/L)4.48±0.08a5L-半胱氨酸盐酸盐(700 mg/L)3.98±0.12b6L-半胱氨酸盐酸盐(900 mg/L)2.33±0.27d
2.1.7 Plackett-Burman实验
根据以上优化结果,利用Design-Expert 12.0软件进行影响因子数N=5的Plackett-Burman设计,每个因子按优化结果取高水平、低水平,以菌体密度为响应值(Y)进行实验。结果如表8所示,碳源添加量为70 g/L,缓冲盐体系添加量为0.05 g/L的组菌体密度与其他组相比较低,推测这2个因素能显著影响IMAU12344菌体密度。
表8 Plackett-Burman实验结果
Table 8 Results of Plackett-Burman experiment
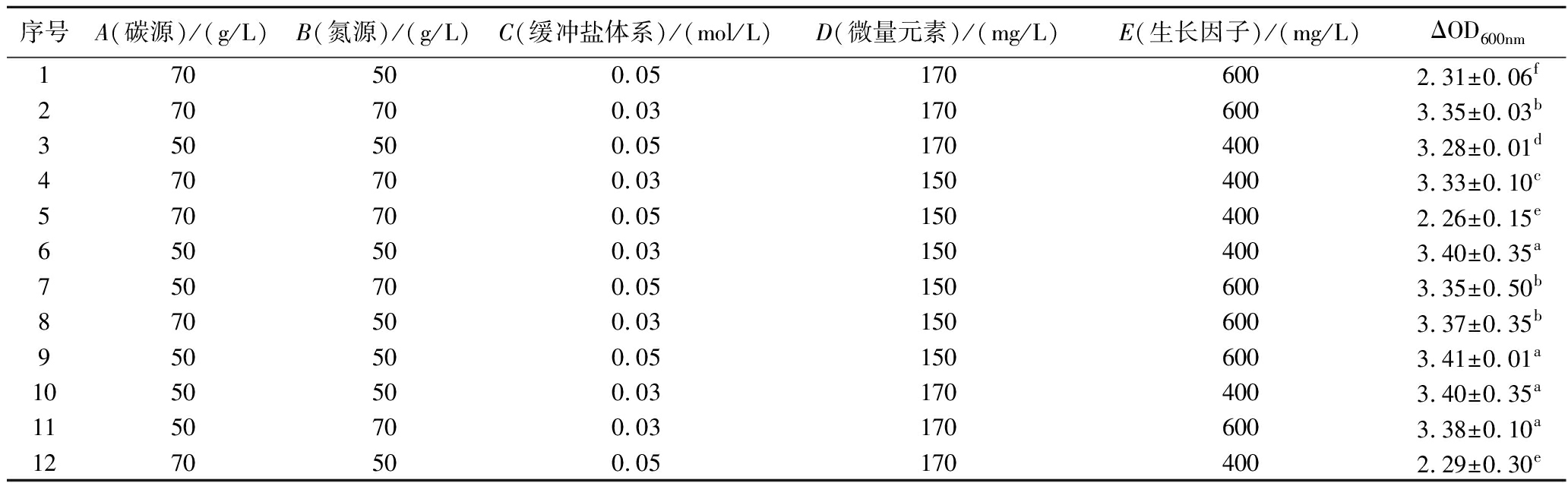
序号A(碳源)/(g/L)B(氮源)/(g/L)C(缓冲盐体系)/(mol/L)D(微量元素)/(mg/L)E(生长因子)/(mg/L)ΔOD600nm170500.051706002.31±0.06f270700.031706003.35±0.03b350500.051704003.28±0.01d470700.031504003.33±0.10c570700.051504002.26±0.15e650500.031504003.40±0.35a750700.051506003.35±0.50b870500.031506003.37±0.35b950500.051506003.41±0.01a1050500.031704003.40±0.35a1150700.031706003.38±0.10a1270500.051704002.29±0.30e
注:不同小写字母表示IMAU12344在不同培养基中菌体密度的差异显著(P<0.05)(下同)。
为进一步确定5个因素对菌体密度影响的显著性,使用Design-Expert 12.0软件对其分析。如表9所示,该模型P<0.05,R2=0.975,模型显著且相关性较好。5个影响因素中除微量元素外均能显著影响IMAU12344的菌体密度。贡献度分析表明,碳源、氮源、缓冲盐体系3个因素对于促进IMAU12344生长的贡献度较高,分别为21.252%、8.823%、25.236%。因此选择碳源、氮源、缓冲盐体系3个因素进行下一步实验。
表9 Plackett-Burman实验结果显著性分析
Table 9 Significance test of the results of Plackett-Burman test
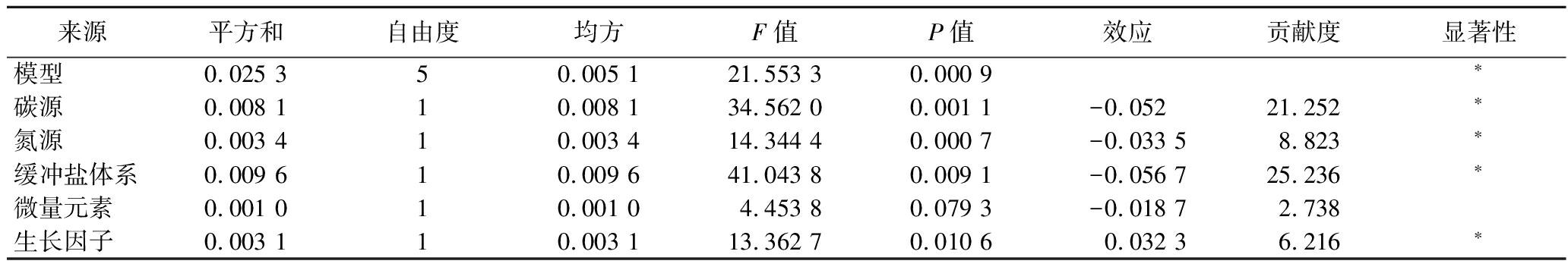
来源平方和自由度均方F值P值效应贡献度显著性模型0.025 3 50.005 1 21.553 3 0.000 9 ∗碳源0.008 1 10.008 1 34.562 0 0.001 1 -0.05221.252∗氮源0.003 4 10.003 4 14.344 4 0.000 7 -0.033 58.823∗缓冲盐体系0.009 6 10.009 6 41.043 8 0.009 1 -0.056 725.236∗微量元素0.001 0 10.001 0 4.453 8 0.079 3 -0.018 72.738生长因子0.003 1 10.003 1 13.362 7 0.010 6 0.032 36.216∗
注:P<0.05为水平差异显著,用*表示。
2.1.8 最陡爬坡实验
由表10可知,碳源、氮源、缓冲盐体系三因素对IMAU12344菌体密度的影响均为负效应,因此设计最陡爬坡实验时应减少因素的水平。具体设计及结果如表10所示,与其他组相比,第3组的活菌数及菌体密度均最高,因此选择该组作为实验中心点进行后续实验。
表10 最陡爬坡实验设计及结果
Table 10 Design and results of the steepest climbing experiment
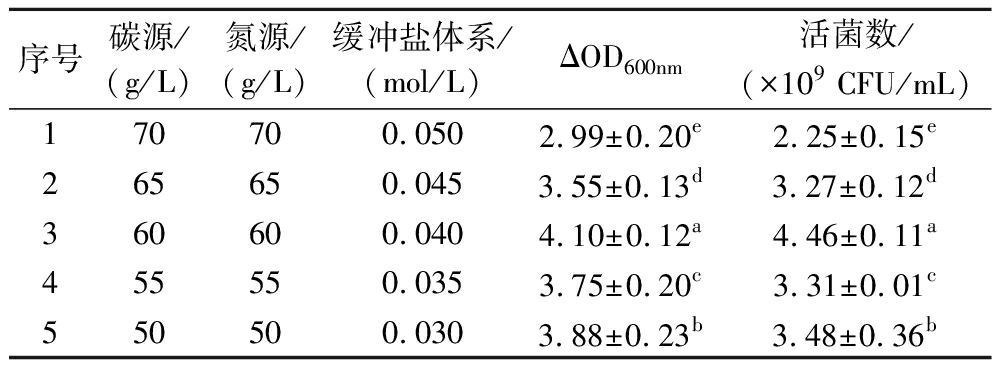
序号碳源/(g/L)氮源/(g/L)缓冲盐体系/(mol/L)ΔOD600nm活菌数/(×109 CFU/mL)170700.0502.99±0.20e2.25±0.15e265650.0453.55±0.13d3.27±0.12d360600.0404.10±0.12a4.46±0.11a455550.0353.75±0.20c3.31±0.01c550500.0303.88±0.23b3.48±0.36b
2.1.9 响应面试验
以Plackett-Burman实验和最陡爬坡实验的结果为基础,设计Box-Behnken实验,确定3个因素的最佳水平及其相互间的作用,探究其对IMAU12344生长的影响。如表11所示,IMAU12344菌体密度受三因素水平变化影响较大,因素水平越靠近中心点的组菌体密度越高。
表11 响应面设计及结果
Table 11 Response surface design and results
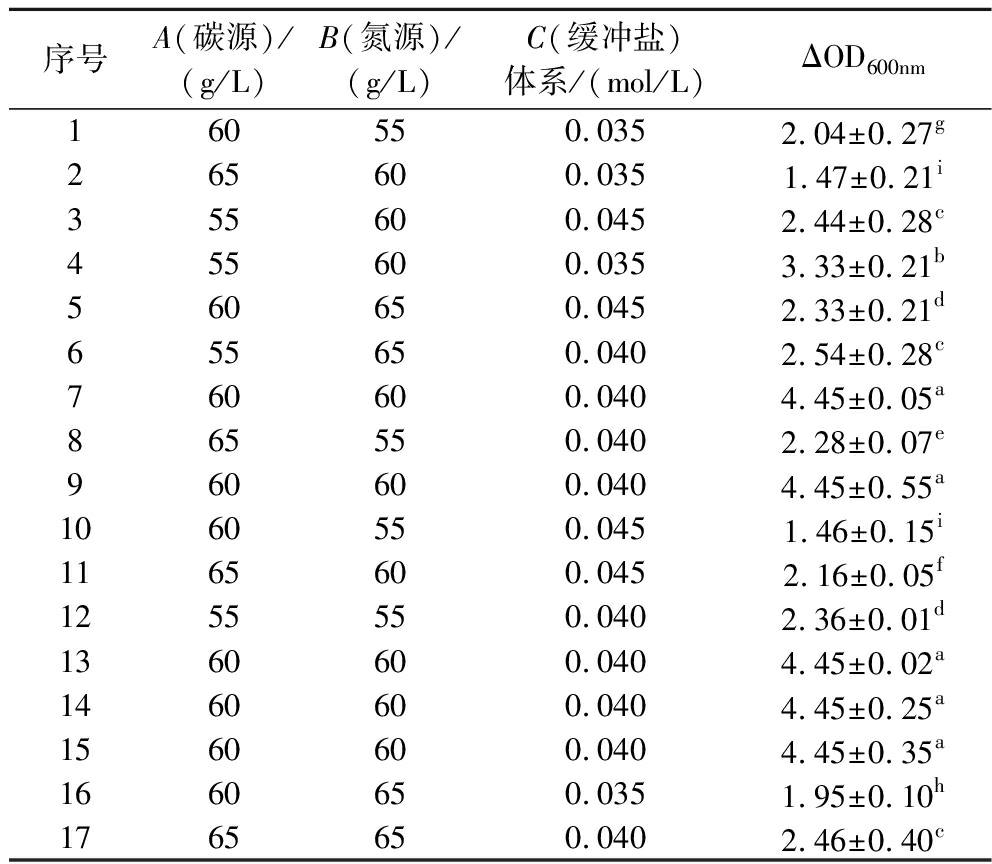
序号A(碳源)/(g/L)B(氮源)/(g/L)C(缓冲盐)体系/(mol/L)ΔOD600nm160550.0352.04±0.27g265600.0351.47±0.21i355600.0452.44±0.28c455600.0353.33±0.21b560650.0452.33±0.21d655650.0402.54±0.28c760600.0404.45±0.05a865550.0402.28±0.07e960600.0404.45±0.55a1060550.0451.46±0.15i1165600.0452.16±0.05f1255550.0402.36±0.01d1360600.0404.45±0.02a1460600.0404.45±0.25a1560600.0404.45±0.35a1660650.0351.95±0.10h1765650.0402.46±0.40c
基于此结果进行方差分析,结果如表12所示该模型整体极显著(P<0.01);失拟项不显著(P>0.05);模型![]() 方程与实验拟合度高,可用作预测动物双歧杆菌乳亚种IMAU12344的生长情况。模型回归方程系数显著性表明,二次项A2、B2、C2均对动物双歧杆菌乳亚种IMAU12344菌体密度有极显著影响(P<0.01)。一次项A、交叉项AC有显著影响(P<0.05)。
方程与实验拟合度高,可用作预测动物双歧杆菌乳亚种IMAU12344的生长情况。模型回归方程系数显著性表明,二次项A2、B2、C2均对动物双歧杆菌乳亚种IMAU12344菌体密度有极显著影响(P<0.01)。一次项A、交叉项AC有显著影响(P<0.05)。
表12 二次多项式模型的系数及其方差分析
Table 12 Coefficients and ANOVA for the developed quadratic polynomial model
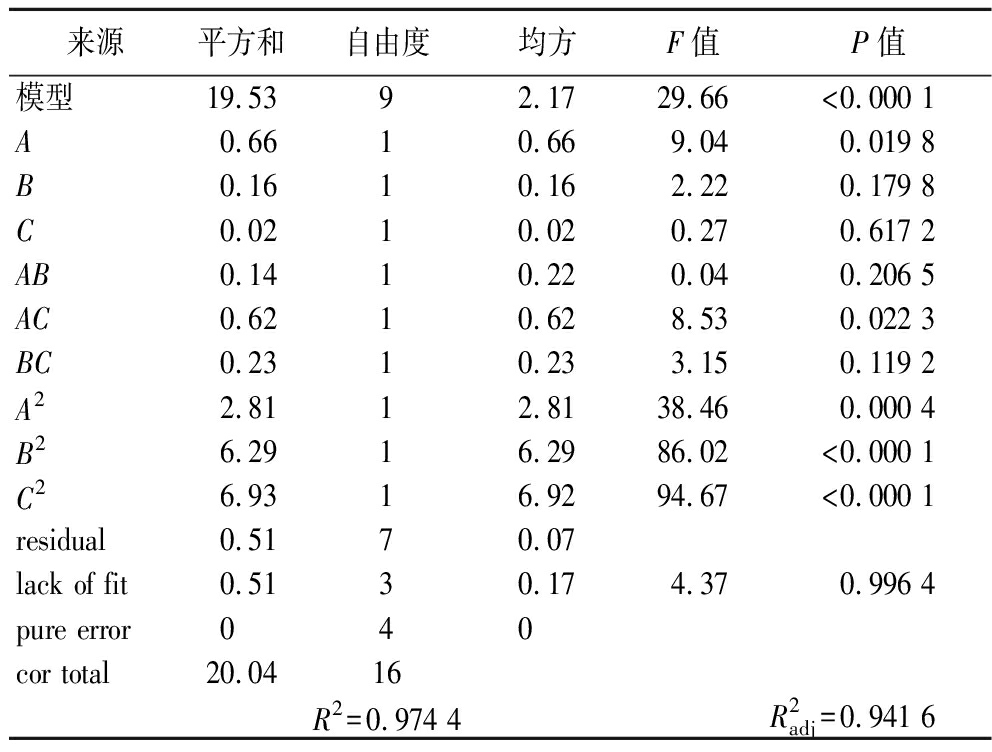
来源 平方和 自由度 均方 F值 P值 模型19.5392.1729.66<0.000 1A0.6610.669.040.019 8B0.1610.162.220.179 8C0.0210.020.270.617 2AB0.1410.220.040.206 5AC0.6210.628.530.022 3BC0.2310.233.150.119 2A22.8112.8138.460.000 4B26.2916.2986.02<0.000 1C26.9316.9294.67<0.000 1residual0.5170.07lack of fit0.5130.174.370.996 4pure error040cor total20.0416R2=0.974 4R2adj=0.941 6
注:表中P<0.05表示差异显著,P<0.01表示差异极显著。
结合以上研究结果,绘制等高线图及响应面图确定回归模型最大值。结果如图7所示,两两因素间的交互响应面曲率明显,等高线均呈椭圆形,说明其对IMAU12344菌体密度的改变有交互作用,且各因素间存在显著性差异。
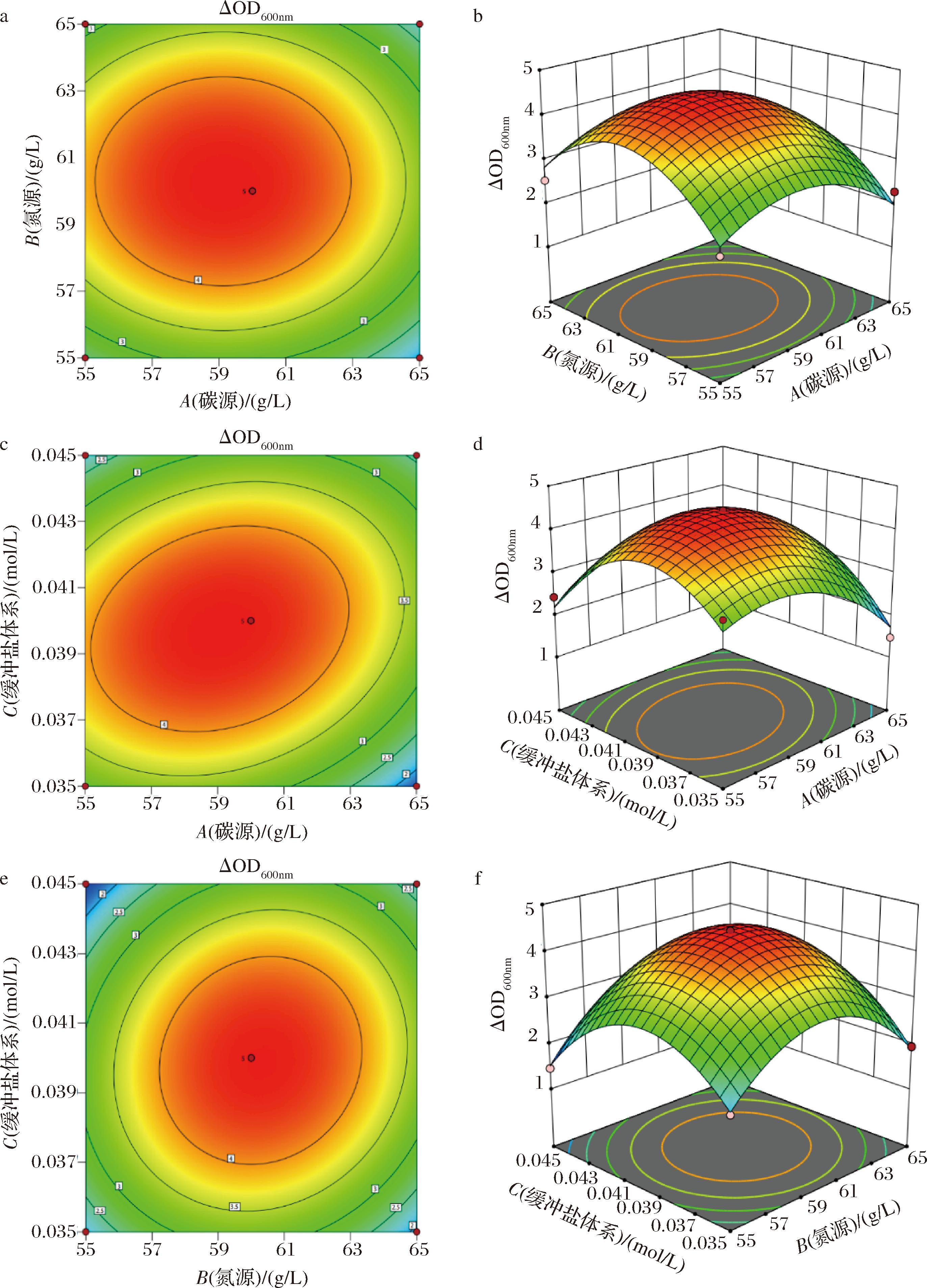
a-碳源和氮源交互等高线;b-碳源和氮源交互响应面;c-碳源和缓冲盐体系交互等高线;d-碳源和缓冲盐体系交互响应面;e-氮源和缓冲盐体系交互等高线;f-氮源和缓冲盐体系交互响应面
图7 因素交互作用响应面图及相应的等高线图
Fig.7 Response surface plot and contour map of interactive effects of various factors
通过Box-Behnken实验,最后得出最优添加量为:碳源59.56 g/L、氮源60.76 g/L,缓冲盐体系20.56 g/L。该配方下预测IMAU12344最大菌体密度值4.46,实测为4.51,与预测值差异不显著,数据可信度较高。
2.2 静态培养条件优化
2.2.1 接种量优化
适宜体积分数的接种量有助于促进发酵液中菌株活菌数的增长。接种量过小时,培养基中营养物质不能被充分利用。而接种量过大时,将产生较多的代谢产物积累,不利于菌株生长[22]。本研究选取不同体积分数的接种量(2%、4%、6%、8%)进行优化。结果如图8所示。动物双歧杆菌乳亚种IMAU12344的接种量在2%时效果最佳,其活菌数显著高于其他组别(P<0.05)。因此选择此接种量进行下一步实验。
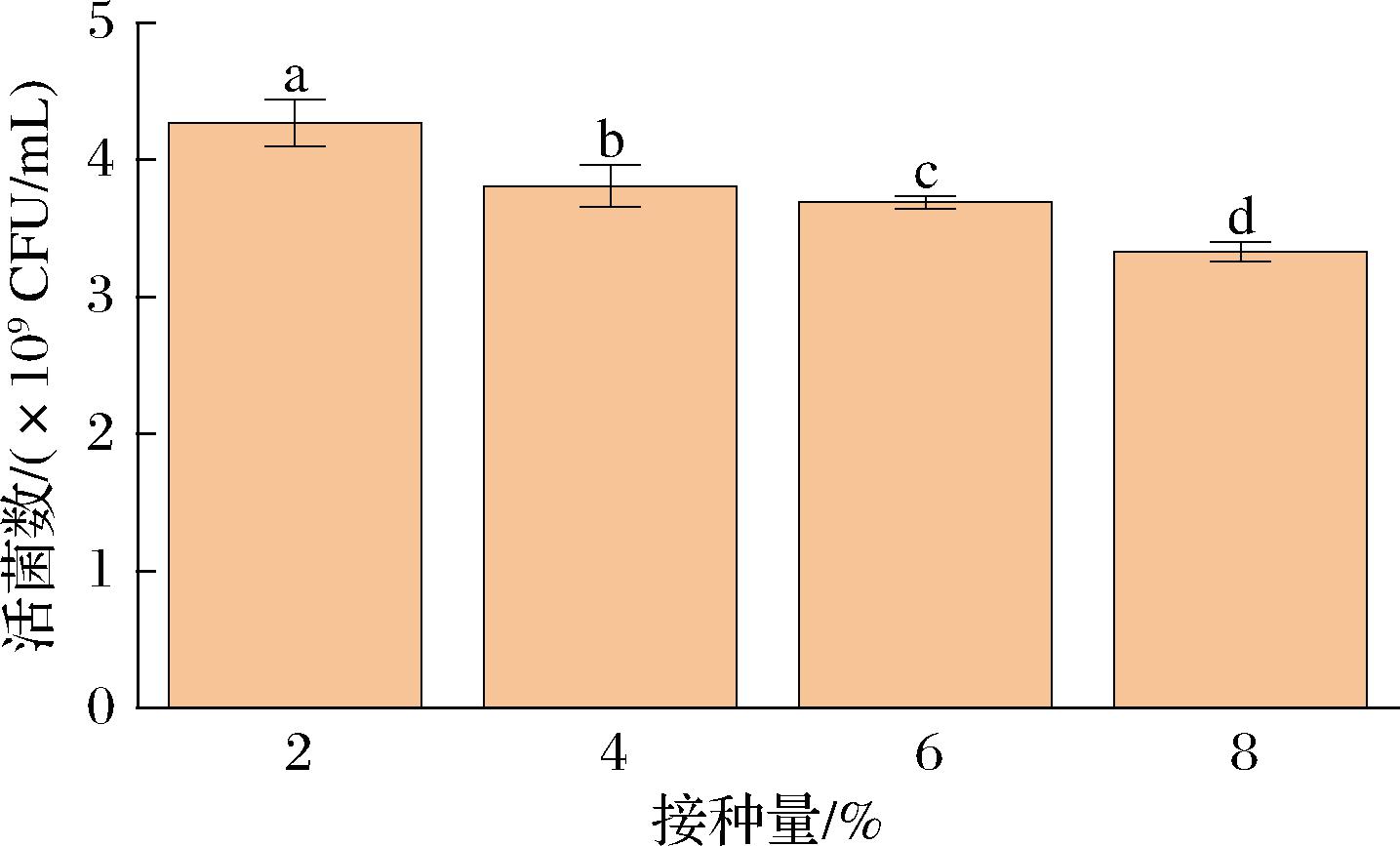
图8 不同接种量对菌株活菌数的影响
Fig.8 The effect of different inoculation amount on the viable count of strains
注:不同小写字母表示IMAU12344在不同接种量下活菌数的差异显著(P<0.05)。
2.2.2 初始pH值的优化
适宜的初始pH值有利于保持微生物细胞膜的完整性,过酸或过碱均会对其产生不良的影响[23]。在最适接种量的基础上,本研究通过查阅文献,选取不同的初始pH值展开实验。结果如图9所示。IMAU12344在初始pH 5.0~8.0均能生长,随着pH值的升高,活菌数呈先上升后下降趋势。在初始pH值为6.5时活菌数达到最大,因此选择该pH值进行下一步实验。
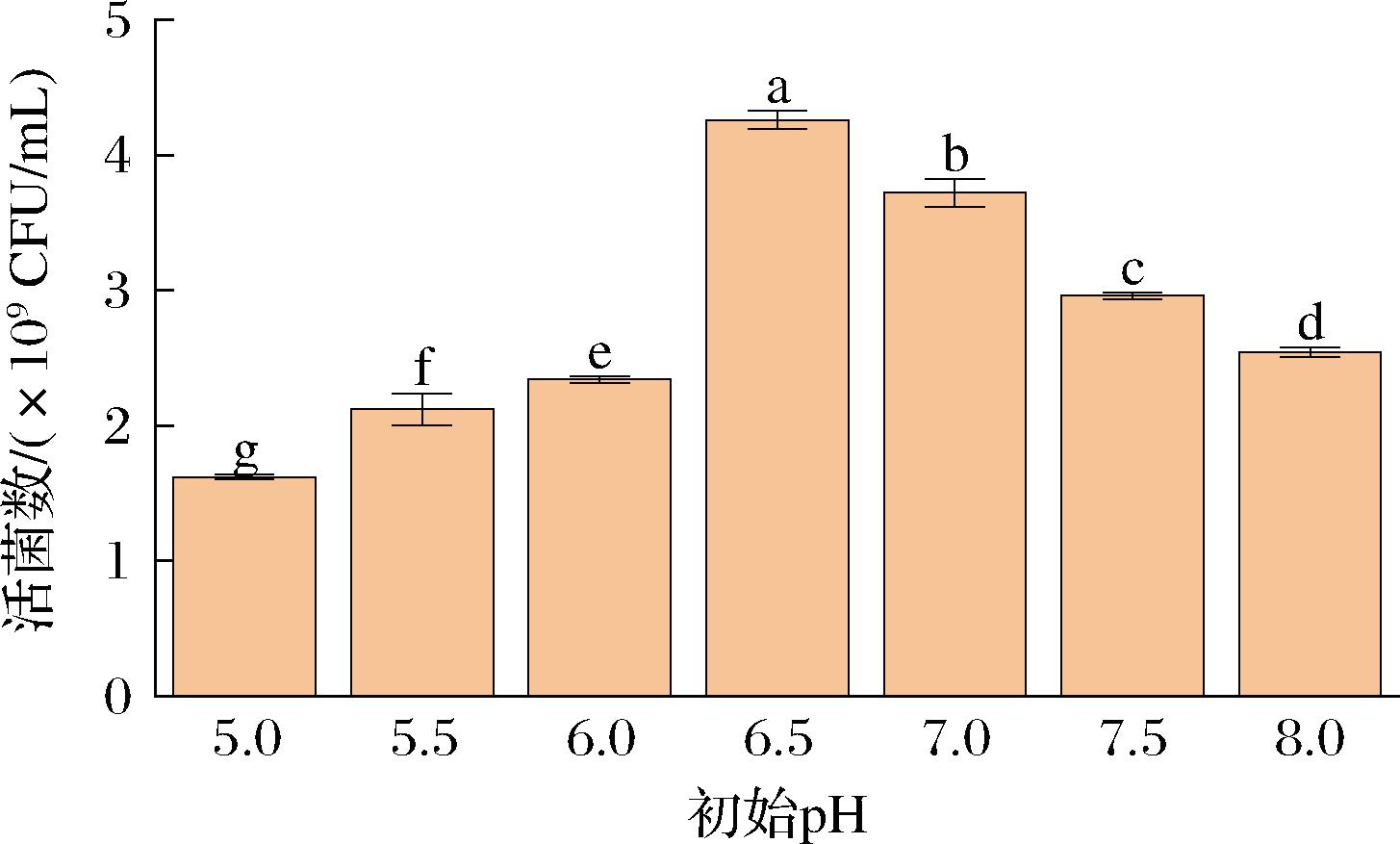
图9 不同初始pH对菌株活菌数的影响
Fig.9 The effect of different initial pH on the viable count of strains
注:不同小写字母表示IMAU12344在不同初始pH下活菌数的差异显著(P<0.05)。
2.2.3 培养温度的优化
培养温度影响着菌株对营养物质利用水平的高低[24]。在上述优化基础上选取25、30、37、42 ℃温度进行优化。结果如图10所示,当培养温度为37 ℃时,IMAU12344的活菌数显著高于其他组别。因此选取该温度作为最适培养温度。
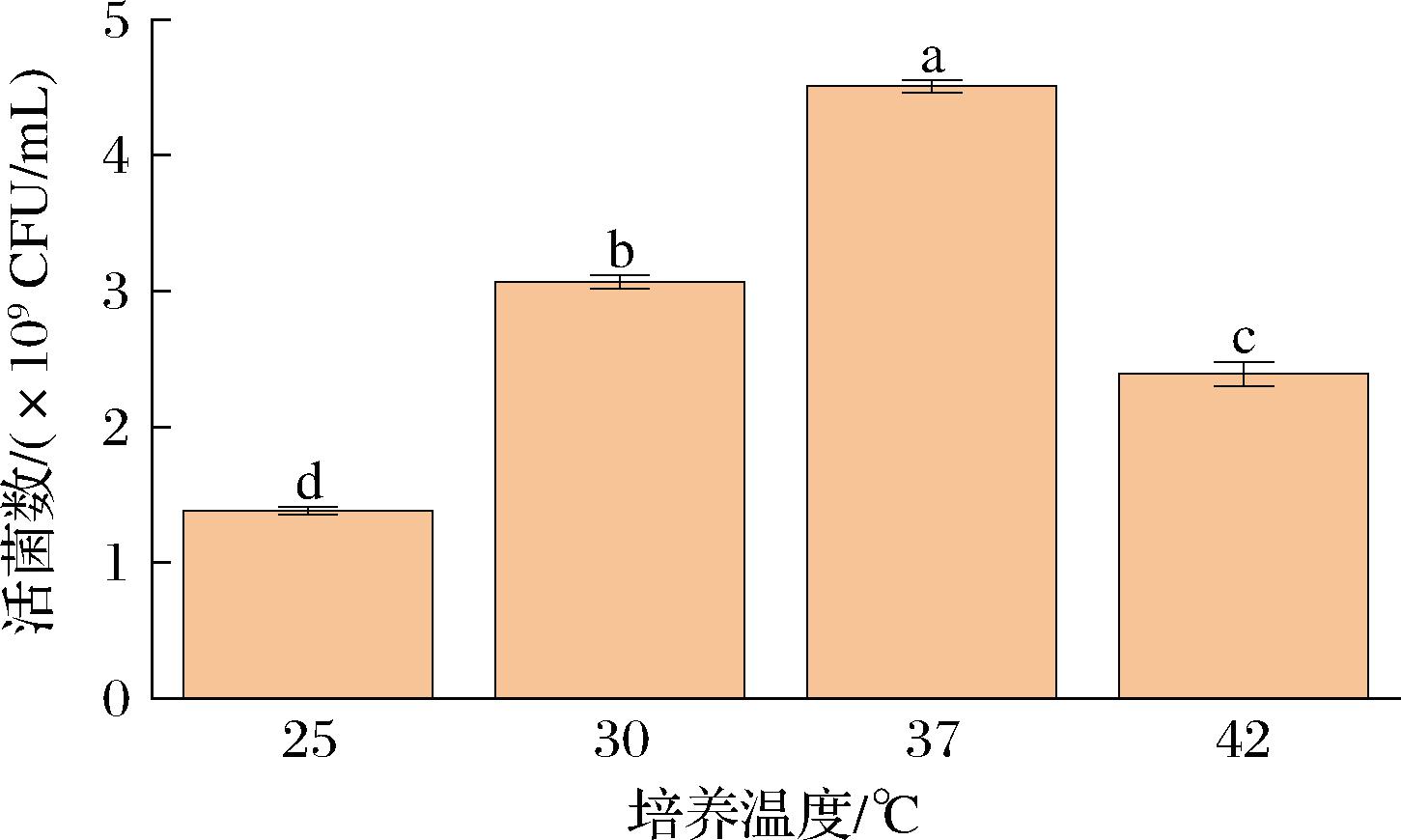
图10 不同温度对菌株活菌数的影响
Fig.10 The effect of different temperature on the viable count of strains
注:不同小写字母表示IMAU12344在不同温度下活菌数的差异显著(P<0.05)。
2.3 高密度发酵培养验证
根据以上结果,采用最佳培养基配方及最佳静态培养条件对动物双歧杆菌乳亚种IMAU12344进行培养并计数,其活菌数可达(4.50±0.05)×109 CFU/mL,较改良MRS培养基提高了3.06倍。采用已有动物双歧杆菌乳亚种高密度发酵工艺,进行动态发酵验证,最终发酵液活菌数为(1.51±0.14)×1010 CFU/mL,较改良MRS培养基提高了12.60倍。
胡殿庚[8]对乳双歧V9最佳高密度培养基及培养条件优化后,活菌数可达8.9×109 CFU/mL。徐显睿等[10]应用响应面法对乳双歧杆菌Z-1进行高密度培养基优化后,活菌数可达1.05×1010 CFU/mL。与之相比,本研究中内蒙古地区母乳源动物双歧杆菌乳亚种IMAU12344在优化后的活菌数更高。
3 结论
本研究对内蒙古地区母乳源动物双歧杆菌乳亚种IMAU12344高密度发酵培养基配方及培养条件进行优化。确定其最优培养基配方为:乳糖59.56 g/L、酵母蛋白胨60.76 g/L、磷酸氢二钠14.32 g/L、磷酸二氢钠6.24 g/L、MnSO4·5H2O 0.16 g/L、吐温-80 1 mL/L、L-半胱氨酸盐酸盐0.5 g/L。最优静态培养条件为:体积分数2%的接种量、初始pH值为6.5、培养温度37 ℃。在此条件下静态培养活菌数可达(4.50±0.05)×109CFU/mL,较改良MRS培养基提高了3.06倍,动态高密度发酵培养活菌数可达(1.51±0.14)×1010 CFU/mL,发酵水平大幅度提升,可为后续研发及生产提高参考数据。
[1] ARCHACKA M, ![]() E, BIA
E, BIA AS W.Techno-economic analysis for probiotics preparation production using optimized corn flour medium and spray-drying protective blends[J].Food and Bioproducts Processing, 2020, 123:354-366.
AS W.Techno-economic analysis for probiotics preparation production using optimized corn flour medium and spray-drying protective blends[J].Food and Bioproducts Processing, 2020, 123:354-366.
[2] LIU W J, CHEN M X, DUO L N, et al.Characterization of potentially probiotic lactic acid bacteria and bifidobacteria isolated from human colostrum[J].Journal of Dairy Science, 2020, 103(5):4013-4025.
[3] SUNG H K, YOUN S J, CHOI Y, et al.Body fat reduction effect of Bifidobacterium breve B-3:A randomized, double-blind, placebo comparative clinical trial[J].Nutrients, 2022, 15(1):28.
[4] LI B W, DING M F, LIU X M, et al.Bifidobacterium breve CCFM1078 alleviates collagen-induced arthritis in rats via modulating the gut microbiota and repairing the intestinal barrier damage[J].Journal of Agricultural and Food Chemistry, 2022, 70(46):14665-14678.
[5] 许晓林, 王斯栌, 陈菲, 等.利用2′-岩藻糖基乳糖生长的两歧双歧杆菌BD-1免疫调节功能评价[J].中国微生态学杂志, 2024, 36(7):745-752;760.XU X L, WANG S L, CHEN F, et al.Evaluation of the immunomodulatory function of Bifidobacterium bifidum BD-1 grown with 2′-fucosyllactose[J].Chinese Journal of Microecology, 2024, 36(7):745-752;760.
[6] 梅丽亚, 郑雪丽, 李佳豪, 等.母乳源乳酸菌调节肠道稳态的研究进展及产业化应用[J].食品与发酵工业, 2025,51(12):424-432.
MEI L Y, ZHENG X L, LI J H, et al.Research progress and industrial application of breast milk-derived lactic acid bacteria in regulating intestinal homeostasis[J].Food and Fermentation Industry, 2025,51(12):424-432.
[7] 赵丽霞, 刘文俊.母乳中乳酸菌多样性及益生菌开发利用研究进展[J].食品与生物技术学报, 2024, 43(4):25-34.ZHAO L X, LIU W J.Research progress on diversity of lactic acid bacteria and probiotics exploitation in breast milk[J].Journal of Food Science and Biotechnology, 2024, 43(4):25-34.
[8] 胡殿庚. 乳双歧杆菌V9的高密度培养研究[D].呼和浩特:内蒙古农业大学, 2016.HU D G.The study on high cell density culture of Bifidobacterium lactis V9[D].Hohhot:Inner Mongolia Agricultural University, 2016.
[9] JANSSENDUIJGHUIJSEN L, LOOIJESTEIJN E, VAN DEN BELT M, et al.Changes in gut microbiota and lactose intolerance symptoms before and after daily lactose supplementation in individuals with the lactase nonpersistent genotype[J].The American Journal of Clinical Nutrition, 2024, 119(3):702-710.
[10] 徐显睿, 李翠凤, 张宗博, 等.响应面法优化乳双歧杆菌Z-1高密度发酵培养基[J].食品工程, 2020(3):39-47.XU X R, LI C F, ZHANG Z B, et al.Response surface design optimizing high cell density medium of Bifidobacterium lactis Z-1[J].Food Engineering, 2020(3):39-47.
[11] HU M Y, WANG D Y, TANG X, et al.Improving the utilization efficiency of nitrogen source through co-culture of Lactobacillus strains with different nitrogen source metabolisms[J].LWT, 2024, 191:115701.
[12] PONOMAROVA O, GABRIELLI N, SÉVIN D C, et al.Yeast creates a niche for symbiotic lactic acid bacteria through nitrogen overflow[J].Cell Systems, 2017, 5(4):345-357.
[13] 谢为天, 徐春厚, 冯晓杰.鼠李糖乳杆菌LT22发酵培养基优化[J].安徽农业科学, 2012,40(12):7155-7156;7239.XIE W T, XU C H, FENG X J.Optimization of the growth medium for a Lactobacillus rhamnosus LT22 strain[J].Journal of Anhui Agricultural Sciences, 2012,40(12):7155-7156;7239.
[14] 高欣伟, 崔树茂, 唐鑫, 等.长双歧杆菌的最适底物解析和高密度发酵工艺优化[J].食品与发酵工业, 2021, 47(19):12-20.GAO X W, CUI S M, TANG X, et al.Optimization of substrate in high-density fermentation of Bifidobacterium longum[J].Food and Fermentation Industries, 2021, 47(19):12-20.
[15] HAYEK S A, GYAWALI R, ALJALOUD S O, et al.Cultivation media for lactic acid bacteria used in dairy products[J].Journal of Dairy Research, 2019, 86(4):490-502.
[16] 孔洁, 张涵, 李亭玉, 等.矿物质复合微量元素对乳酸菌生长及生物学特征的影响[J].延边大学农学学报, 2018, 40(2):76-81.KONG J, ZHANG H, LI T Y, et al.The effects of minerals microelement compound on the growth and biological characteristics of lactic acid bacteria[J].Agricultural Science Journal of Yanbian University, 2018, 40(2):76-81.
[17] 马琳. 短双歧杆菌高密度发酵工艺的优化[D].呼和浩特:内蒙古农业大学, 2024.MA L.Optimization of high cell density cultivation processing of Bifidobacterium brevis[D].Hohhot:Inner Mongolia Agricultural University, 2024.
[18] WEGKAMP A, DE VOS W M, SMID E J.Folate overproduction in Lactobacillus plantarum WCFS1 causes methotrexate resistance[J].FEMS Microbiology Letters, 2009, 297(2):261-265.
[19] GULBINSKY J S, CLELAND W W.Kinetic studies of Escherichia coli galactokinase[J].Biochemistry, 1968, 7(2):566-575.
[20] DONG Z X, GU L, ZHANG J, et al.Optimisation for high cell density cultivation of Lactobacillus salivarius BBE 09-18 with response surface methodology[J].International Dairy Journal, 2014, 34(2):230-236.
[21] 王似锦, 江志杰, 牛振东, 等.保健食品双歧杆菌和乳酸菌计数中4种稀释液的比较[J].中国卫生检验杂志, 2015(16):2700-2702.WANG S J, JIANG Z J, NIU Z D, et al.Comparison of 4 diluents for enumeration of Bifidobacteria and lactic acid bacteria in health food[J].Chinese Journal of Health Laboratory Technology, 2015(16):2700-2702.
[22] 陈园园. 德氏乳杆菌保加利亚亚种QH38-1高密度发酵工艺的优化[D].呼和浩特:内蒙古农业大学, 2023.CHEN Y Y.Optimization of high density cultivation process of Lactobacillus delbrueckii subsp.bulgaricus QH38-1[D].Hohhot:Inner Mongolia Agricultural University, 2023.
[23] 左梦楠, 刘伟, 张菊华, 等.发酵乳杆菌BLHN3的高密度培养优化[J].食品与机械, 2022, 38(12):181-189.ZUO M N, LIU W, ZHANG J H, et al.Optimization of high density culture of Lactobacillus fermentum BLHN3[J].Food and Machinery, 2022, 38(12):181-189.
[24] 沙玉杰, 杨平平, 何培青, 等.响应面法优化嗜热菌Bacillus sp.BⅡ-5产琼胶酶的发酵培养基条件[J].中国酿造, 2013, 32(5):31-35.SHA Y J, YANG P P, HE P Q, et al.Optimization of medium composition and culture conditions for agarase production by Bacillus sp.BⅡ-5[J].China Brewing, 2013, 32(5):31-35.