氧化应激是机体病理生理过程中的核心环节,其本质是氧化与抗氧化系统失衡,导致活性氧等分子过度产生与蓄积[1]。这些高活性分子可攻击细胞内生物大分子,引发脂质过氧化、蛋白质氧化修饰及DNA损伤,进而破坏细胞结构与功能,甚至诱发细胞凋亡或癌变等严重后果[2-5]。应对氧化应激的传统策略主要包括生活方式干预、外源性抗氧化补充和药物/医疗干预[6]。尽管直接补充抗氧化剂有效,但其作用常局限于直接清除自由基。近年来,一种更深入的策略日益受到关注:通过调节肠道微生态等内源性保护机制,从整体上增强机体的抗氧化能力。这种“由内而外”的协同增效方式,正展现出巨大的应用潜力[7]。
氧化应激研究常用动物模型包括全身性诱导模型、器官特异性毒物模型、转基因/基因敲除模型及快速老化模型四大类[8]。D-半乳糖(D-galactose,D-gal)是一种全身性诱导模型,以慢性、全身、低强度但多器官氧化应激损伤为核心,兼具周期短、成本低、表型丰富、可重复性强等优势;用该模型可在最短时间内获得肝、肾、心、脾、脑、肠等多个器官的氧化损伤数据,因此被广泛应用于氧化应激损伤研究中。臭氧吸入是对肺部和呼吸系统造成直接且强烈的氧化损伤,因此该模型常用于研究呼吸系统疾病中氧化损伤;γ-射线/全身辐照会直接破坏生物大分子,其损伤路径远比普通氧化应激复杂,因此该模型常用于研究特定器官或基因突变导致的疾病中氧化损伤;转基因/基因敲除和快速老化小鼠模型不仅价格昂贵,而且由于其基因缺陷可能干扰测定结果,并且该模型常用于年龄老化相关疾病中氧化损伤[6,8]。综上所述,D-gal诱导大鼠氧化应激损伤模型通过长期给药,在动物体内模拟了一个慢性、全身性、以氧化应激为核心特征的状态。这与可长期服用的和具有全身性保护作用的天然抗氧化剂的定位高度契合。
麦角硫因(ergothioneine,ERGO)是一种天然存在的氨基酸衍生物,主要富集于食用菌等天然食物来源中[9-10]。其核心生物活性不仅体现在抗氧化活性上,还展现出调节肠道菌群、增加短链脂肪酸(short-chain fatty acids, SCFAs)生成等益生元样功效[9-10]。ERGO的系统性保护作用可能超越其直接的自由基清除能力,它还可能通过重塑肠道菌群结构、上调SCFAs生成菌的丰度,从而增加丁酸、丙酸等具有抗炎和肠道屏障保护功能的代谢产物,协同放大其抗氧化与抗炎功效。这一双重作用机制不仅深化了对ERGO多靶点药理活性的认识,也为开发基于“抗氧化-肠道微生态调控”协同策略的新型功能性食品或治疗药物提供了重要理论依据。
然而,将ERGO、肠道菌群、SCFAs与D-gal诱导的氧化应激损伤四者关联的系统性研究尚属空白。ERGO能否通过重塑紊乱的肠道菌群、调节SCFAs谱图来协同其直接抗氧化作用,进而发挥保护功效,是亟待阐明的关键科学问题。为此,本研究旨在系统探讨ERGO对D-gal诱导大鼠氧化应激损伤的保护作用及其与肠道菌群-SCFAs轴的内在联系。研究将首先确证其体内抗氧化功效,进而通过16S基因测序和超高效液相色谱-串联质谱技术,分别解析肠道菌群结构变化与粪便中关键SCFAs含量。本研究期望阐明ERGO“直接抗氧化”与“肠道菌群-SCFAs轴调控”的双重保护机制,为其开发新型多靶点功能性食品或药物前体,提供更全面深入的科学依据。
1 材料的方法
1.1 材料与试剂
ERGO(批号:CMJ2503002),联邦制药(内蒙古)有限公司;D-gal(批号:C14971408),上海麦克林生化科技股份有限公司;还原型谷胱甘肽(reduced glutathione,GSH)测定试剂盒(批号:20250619)、超氧化物歧化酶(superoxide dismutase,SOD)测定试剂盒(批号:20250619)、丙二醛(malondialdehyde,MDA)测定试剂盒(批号:20250620)、过氧化氢酶(catalase,CAT)测定试剂盒(批号:20250617)、蛋白质羰基(protein carbonyl,PC)测定试剂盒(批号:20250625),南京建成生物科技研究所;大鼠IL-1β ELISA科研试剂盒(批号:A301B31021),联科生物技术股份有限公司;大鼠IL-6(批号:202412)和大鼠TNF-α ELISA检测试剂盒(批号:202412),上海凡科维有限公司;生理盐水(批号:L25021401),四川科伦药业股份有限公司。
1.2 仪器与设备
TU-1810紫外可见分光光度计,北京普析通用有限责任公司;MultiSkan FC酶标仪,赛默飞世尔科技(中国)有限公司;Synergy HT多功能酶标仪,美国伯腾仪器有限公司;1-15PK高速冷冻离心机,德国Sigma;LCMS-8050超高效液相串联三重四极杆质谱,日本岛津公司。
1.3 实验方法
1.3.1 实验动物
SPF级健康SD雄性大鼠,体质量约250 g,购自斯贝福(北京)生物技术有限公司,实验动物生产许可合格证号:SCXF(京)2019-0010。本研究已通过实验动物伦理委员会批准,批准号为BUCM-4-2022061501-2061。大鼠饲养于昼夜节律光照条件下,温度(26±2) ℃, 相对湿度60%~70%,实验前适应性饲养7 d,自由进水,给予普通维持饲料。
1.3.2 灌胃溶液制备、动物分组与给药
实验动物选用50只SD雄性大鼠,采用随机区组设计分为5组(n=10):对照组(仅接受生理盐水处理)、D-gal诱导模型组、ERGO低剂量组(ERGO-L,1.25 mg/kg)、ERGO中剂量组(ERGO-M,2.50 mg/kg)、ERGO高剂量组(ERGO-H,5.0 mg/kg)。模型建立采用腹腔注射D-gal(200 mg/kg/d),持续6周;对照组与模型组同步腹腔注射等体积生理盐水。ERGO用去离子水溶解后,各给药组在造模期间同步接受ERGO灌胃给药,而对照组与模型组则同步灌胃给予等体积去离子水作为溶剂对照,给药周期为4周。
1.3.3 ERGO对大鼠体质量和脏器指数的影响
在大鼠造模实验开始后,每天对各组大鼠进行一般状态观察,包括其活动性、生存状况和毛发状况等。每5 d测量一次大鼠的体质量。实验的最后一天,大鼠需禁食过夜,并测量最终体质量。在处死所有大鼠后,立即取出每只大鼠的心脏、肝脏、脾脏和肾脏,用冰冷的生理盐水清洗,然后在滤纸上吸干并称重。脏器指数的计算方式如公式(1)所示[11]:
脏器指数![]()
(1)
每只大鼠的肝脏被冷冻在液氮中,并在-80 ℃的条件下保存,以用于生化指标的测定。
1.3.4 ERGO对大鼠氧化应激水平的影响
大鼠腹主动脉采集血样至采血管中,然后将采集到的血液在4 ℃条件下,以1 400×g的离心力离心15 min,分离出的血清在-80 ℃下贮存,用于后续分析[9]。根据试剂盒说明书,分别测定大鼠血清、肝脏、肾脏和脾脏中的MDA、PC和GSH的含量以及SOD和CAT的活性。
1.3.5 粪便中菌群16S基因测序
取各组大鼠粪便约80 mg,采用DNA提取试剂盒提取总DNA,经琼脂糖凝胶电泳和NanoDrop检测DNA完整性,使用特异性引物进行PCR扩增,纯化后构建文库,使用Illumina NovaSeq 6 000 测序平台进行测序。所得原始数据经质控、去噪和拼接后,使用QIIME2软件进行生物信息学分析。
1.3.6 SCFAs测定
1.3.6.1 粪便匀浆与上清制备
称取各组大鼠粪便样本约100 mg,加入1 mL超纯水后以4 260 r/min匀浆1 min。匀浆液于4 ℃、16 000×g条件下离心5 min,收集上清液作为待测样品。
1.3.6.2 衍生化反应
以盐酸吡啶溶液(0.54 mL浓盐酸、0.86 mL吡啶及8.6 mL超纯水混合而成)为溶剂,分别配制1 mol/L的1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐[1-ethyl-3-(3-dimethylaminopropyl)carbodiimide hydrochloride, EDC]溶液和1 mol/L的3-叔丁基-4-羟基苯甲醚(3-tert-butyl-4-hydroxyanisole,O-BHA)溶液。精密移取20 μL粪便上清液,依次加入10 μL含内标(D7-丁酸)的乙腈溶液、10 μL EDC溶液及10 μL O-BHA溶液,每加入一种试剂均需涡旋混匀。将混合物在室温下以1 000 r/min振荡孵育20 min完成衍生化。
1.3.6.3 SCFAs的萃取与浓缩
衍生化反应结束后,向样本中加入等体积超纯水涡旋混匀,再加入400 μL乙酸乙酯,剧烈涡旋萃取2 min。萃取液在4 ℃、离心力5 000×g条件下离心5 min,小心移取约200 μL上层有机相(乙酸乙酯层),于真空下浓缩至干。残留物用50 μL 50%(体积分数)甲醇溶液复溶,经4 ℃、离心力16 000×g离心15 min后,取上清液用于分析。
1.3.6.4 液相色谱-质谱联用分析条件
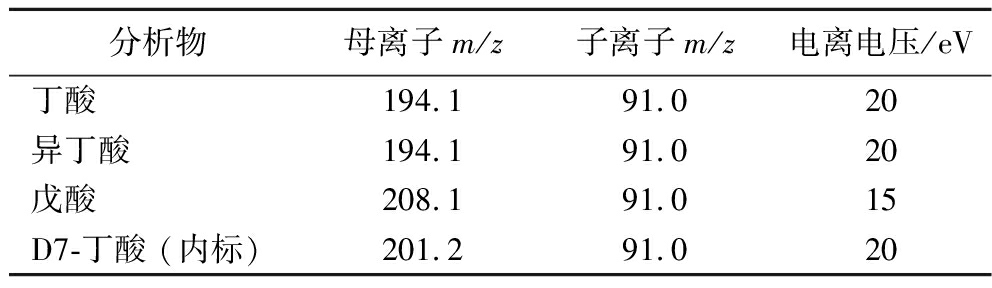
Waters XSelect HSS T3色谱柱(50 mm×2.1 mm,2.5 μm),柱温:40 ℃。流动相A[0.1%(体积分数)甲酸溶液],流动相B(甲醇),流速:0.25 mL/min。采用梯度洗脱程序:0~1 min,B相由5%线性升至22%;1~5 min,B相由22%升至45%;5~5.5 min,B相由45%升至60%;5.5~6 min,B相由60%升至75%;6~6.5 min,B相保持75%。进样体积为3 μL。质谱检测在电喷雾离子源正离子模式下进行,采用多反应监测模式采集数据。离子源参数设置如下:雾化气、干燥气、加热气流量分别为2、10、10 L/min;接口温度、脱溶剂管温度和加热块温度分别为300、526、400 ℃。各目标分析物及内标的多反应监测(multiple reaction monitoring,MRM)离子对、碰撞能量等参数详见表1。
表1 SCFAs及内标的MRM参数
Table 1 MRM monitoring parameters for SCFAs and internal standards
分析物母离子m/z子离子m/z电离电压/eV丁酸194.191.020异丁酸194.191.020戊酸208.191.015D7-丁酸 (内标)201.291.020
1.4 统计数据处理
实验数据以“平均值±标准差”表示。使用GraphPad Prism 8.0.1软件(美国GraphPad软件公司)通过单因素方差分析进行统计分析。P<0.05认为具有统计学显著性差异。
2 结果与分析
2.1 ERGO对大鼠体质量和脏器指数的影响
在大鼠造模实验开始后,对照组大鼠的体质量持续稳定增长,其自然反应、行为活动、生存状态和毛发状况均表现正常,且进食量保持正常水平。随着实验的进行,与对照组相比,模型组大鼠的毛发逐渐变黄且易于脱落,活动范围减小,体质量增长速度减慢。相比之下,各给药组在这些方面的表现有显著性改善。ERGO给药对大鼠体质量的具体影响如图1所示。
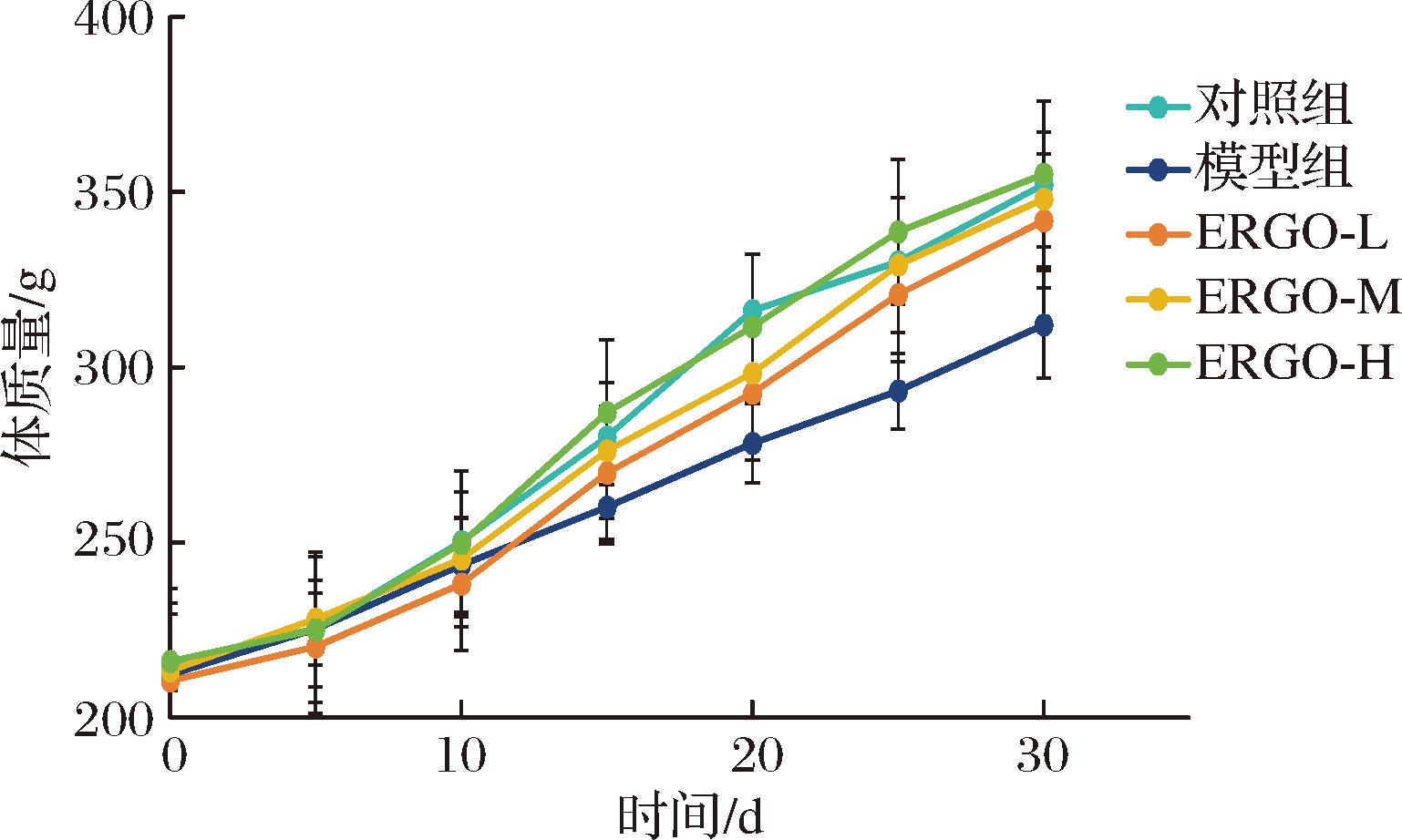
图1 给药对大鼠体质量的影响
Fig.1 Effects of administration on the weight of rats
实验初期,各组的体质量没有明显差异。在D-gal给药造模后,对照组和ERGO剂量组的体质量增长没有显著差异,而模型组的体质量增长明显较低,显著低于其他4组。
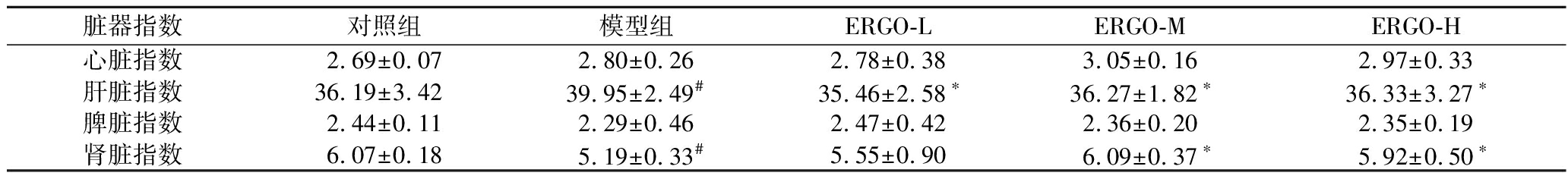
如表2所示,与对照组大鼠相比,模型组大鼠的肝脏指数显著升高(P<0.05),而肾脏指数显著降低(P<0.05)。心脏和脾脏指数未见显著差异。相较于模型组,各个剂量组的肝脏指数均显著降低(P<0.05),而中、高剂量组大鼠的肾脏指数显著升高(P<0.05),低剂量组大鼠的肾脏指数也呈现升高趋势。实验结果证实,ERGO对D-gal引起的脏器指数变化具有一定的恢复作用。
表2 ERGO对大鼠脏器指数的影响
Table 2 Effects of ERGO on organ index in rats
脏器指数对照组模型组ERGO-LERGO-MERGO-H心脏指数2.69±0.072.80±0.262.78±0.383.05±0.162.97±0.33肝脏指数36.19±3.4239.95±2.49#35.46±2.58∗36.27±1.82∗36.33±3.27∗脾脏指数2.44±0.112.29±0.462.47±0.422.36±0.202.35±0.19肾脏指数6.07±0.185.19±0.33#5.55±0.906.09±0.37∗5.92±0.50∗
注:和对照组相比,#表示P<0.05;和模型组相比,*表示P<0.05。
2.2 ERGO对氧化应激损伤大鼠抗氧化活性的影响
MDA和PC是细胞膜中多不饱和脂肪酸和细胞内蛋白质过氧化后氧化应激损伤的关键标志物,其含量上升通常与氧化损伤程度呈正相关[12]。GSH是细胞内至关重要的抗氧化分子,对于维持细胞内氧化还原平衡、清除自由基、保护细胞免受氧化应激损伤具有核心作用。GSH含量下降通常意味着抗氧化防御能力减弱[13]。SOD和CAT是人体内重要的抗氧化酶,能够清除自由基、抗氧化,从而保护细胞免受过氧化氢的氧化损伤[14]。D-gal诱导的大鼠氧化应激会导致一系列生化指标发生显著变化,这些变化共同构成了D-gal诱导氧化应激的生化特征。这些指标的变化是评估ERGO对D-gal诱导氧化应激损伤保护作用的重要依据。
表3显示了ERGO对氧化应激损伤大鼠中MDA、PC和GSH含量以及SOD和CAT活性变化的影响。与对照组相比,模型组的上述5个生化指标在所有检测器官(血清、肝脏、肾脏和脾脏)中显示出显著变化(P<0.01)。除了ERGO-L组在脾脏中MDA含量、血清和肾脏中的PC含量、血清中GSH含量之外,其他ERGO剂量组在所有检测器官的MDA、PC和GSH含量均显著高于模型组(P<0.05或P<0.01)。除了ERGO-L组在肾脏中SOD活性、血清、肾脏和脾脏中CAT活性之外,其他ERGO剂量组在所有检测器官的SOD和CAT活性均高于模型组(P<0.05或P<0.01)。ERGO中、高剂量组均显著性降低了所有检测器官中的MDA、PC和GSH含量(P<0.05),并显著性增加了这些检测器官中SOD和CAT的活性。有些氧化应激生化指标未呈现线性量效关系可能源于3方面因素:饱和效应(低剂量即可饱和关键靶点);组织特异性响应(不同器官氧化还原网络差异);多靶点机制复杂性(直接抗氧化与肠道菌群调控双重机制交互作用)。但总体上,ERGO对氧化应激损伤大鼠具有显著的抗氧化活性是明确的。
表3 ERGO对大鼠血清和主要脏器中氧化应激生化指标的影响
Table 3 Effects of ERGO on oxidative stress biochemical indicators in rats serum and major organs

生化指标脏器对照组模型组ERGO-LERGO-MERGO-HMDA水平/(nmol/mL)血清4.62±1.2210.15±1.41##5.72±1.81∗∗8.98±1.86∗∗5.57±1.28∗∗肝脏3.65±0.857.67±1.58##5.09±1.01∗∗5.01±0.96∗∗3.88±0.95∗∗肾脏5.95±1.8311.90±2.38##7.92±1.68∗∗6.47±1.15∗∗8.18±2.46∗∗脾脏14.77±1.1324.22±2.75##24.09±3.5917.63±2.72∗∗16.68±1.88∗∗PC水平/(nmol/mg)血清6.03±1.59 8.66±1.00##8.80±1.32 4.80±1.11∗∗5.98±1.24∗∗肝脏85.91±10.99130.30±13.20##99.66±23.10∗127.53±21.67∗∗91.88±12.48∗∗肾脏66.02±8.1895.23±7.51##90.23±10.4576.88±13.66∗∗69.85±6.80∗∗脾脏59.22±10.60118.23±8.38##86.73±10.32∗∗82.28±7.35∗∗74.17±13.66∗∗SOD水平/(U/mL)血清13.90±1.03 7.23±0.39##16.24±2.20∗∗ 14.19±2.02∗∗ 13.48±1.80∗∗ 肝脏10.18±1.243.76±0.79##10.41±1.99∗∗6.79±1.91∗∗8.70±0.83∗∗肾脏28.18±2.4515.43±3.43##18.76±2.6822.50±4.20∗∗26.61±4.91脾脏16.82±4.309.62±1.38##11.71±1.61∗12.45±0.77∗∗14.67±1.77∗∗CAT水平/(U/mg)血清7.94±1.15 3.07±0.85##2.79±0.31 5.08±1.15∗∗ 6.57±0.95∗∗ 肝脏11.32±1.677.07±0.96##12.31±1.81∗∗13.27±2.58∗∗11.14±0.41∗∗肾脏16.11±3.38 8.358±1.06##9.54±0.67 12.06±2.00∗∗ 14.95±2.48∗∗ 脾脏10.40±1.69 6.44±1.65## 7.21±1.30 8.85±1.09∗ 9.89±1.87∗∗GSH水平/(nmol/mg)血清26.62±3.19 11.21±3.67## 14.02±2.48 16.29±3.51∗ 20.41±2.99∗∗ 肝脏389.25±39.88217.45±22.82##408.90±29.14∗∗417.51±27.23∗∗413.25±24.66∗∗肾脏451.48±25.01265.91±43.75##398.07±33.05∗∗387.67±24.99∗∗473.74±65.82∗∗脾脏231.35±14.81137.09±13.43##167.65±24.75∗161.69±15.90∗203.31±10.35∗∗
注:和对照组相比,##表示P<0.01;和模型组相比,*和**分别表示P<0.05和P<0.01(下同)。
2.3 ERGO对氧化应激损伤大鼠血清炎症因子水平的影响
在D-gal诱导的大鼠氧化应激模型中,体内氧化剂与抗氧化剂之间的失衡引发了细胞损伤,进而激活了炎症反应,导致炎症细胞因子的过度释放,这与之前的报道一致[15]。其中,IL-1β、IL-6和TNF-α作为关键的炎症因子,其水平的高低直接反映了氧化应激的严重程度。如图2所示,经过D-gal处理的大鼠模型组血清中,IL-1β、IL-6和TNF-α的水平与对照组相比显著升高(P<0.01),这表明大鼠体内氧化应激损伤显著。相比之下,除了低剂量组的IL-1β水平无显著性降低外,其他剂量组的IL-1β、IL-6和TNF-α的水平均显著性降低(P<0.05或0.01),显示出ERGO对氧化应激损伤具有保护作用。
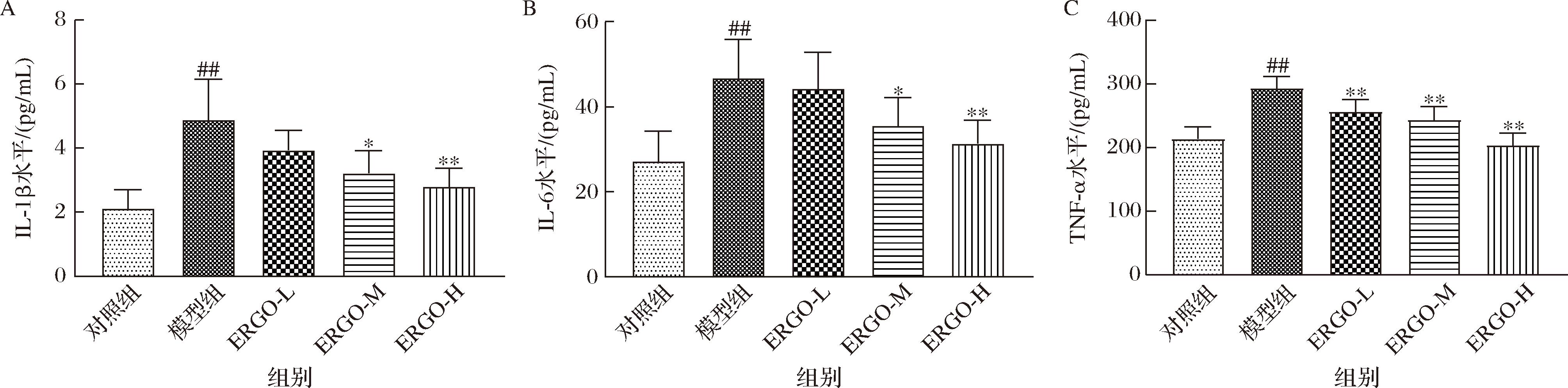
A-IL-1β水平;B-IL-6水平;C-TNF-α水平
图2 ERGO对氧化应激损伤大鼠血清炎症因子水平的影响
Fig.2 Effects of ERGO on serum inflammatory factor levels in rats with oxidative stress injury
注:和对照组相比,##表示P<0.01;和模型组相比,*和**分别表示P<0.05和P<0.01(下同)。
2.4 ERGO对氧化应激损伤大鼠粪便中肠道菌群和SCFAs的影响
2.4.1 肠道菌群Alpha多样性分析
在肠道菌群研究中,Alpha多样性分析是评估物种多样性的重要指标。如表4所示,与对照组相比,模型组的系统发育多样性(phylogenetic diversity whole tree,PD whole tree)指数、Chao1指数、观测物种数及基于丰度的覆盖度估计量(abundance-based coverage estimator,ACE)指数均显著降低(P<0.01),表明D-gal诱导的氧化应激对肠道菌群的多样性与丰富度产生了明显的抑制作用。而与模型组相比,ERGO-H组的上述指数显著回升,提示ERGO能够有效改善模型大鼠肠道菌群的多样性与丰富性,从而可能通过调节肠道微生态平衡发挥其保护作用。
表4 肠道菌群Alpha多样性分析统计表
Table 4 Statistical table of Alpha diversity analysis of gut microbiota

组别系统发育多样性指数Chao1指数观测物种物数ACE指数对照组28.16±1.50423.06±27.82422.27±27.41424.15±25.95模型组23.54±0.99##279.71±36.77##298.27±23.33##299.43±24.46##ERGO-H27.44±0.57∗∗381.39±8.10∗∗380.63±7.18∗∗381.85±9.92∗∗
2.4.2 ERGO对肠道菌群的调控作用
线性判别分析效应大小(linear discriminant analysis effect size,LEfSe)分析如图3所示,LEfSe结果揭示了不同组别肠道菌群组成的关键差异。对照组的代表物种共有21个,主要包括厚壁菌门(Firmicutes)、毛螺菌科(Lachnospiraceae)和毛螺菌目(Lachnospirales)等;模型组的代表物种减少至13个,以鼠杆菌科(Muribaculaceae)、乳杆菌目(Lactobacillales)和乳杆菌科(Lactobacillaceae)为主;而ERGO-H组的代表物种为12个,显著富集了普雷沃氏菌科(Prevotellaceae)、拟杆菌门(Bacteroidota)和拟杆菌纲(Bacteroidia)等菌群。已有文献报道,普雷沃氏菌属(Prevotella)属相关物种(如Prevotellaceae)是膳食纤维分解的关键菌群,能够通过代谢产生丁酸等SCFAs,从而增强肠道屏障功能[16]。相比之下,模型组中显著富集的鼠杆菌科(Muribaculaceae)虽属于拟杆菌门,但其部分亚群可能与能量吸收过剩或炎症反应相关[17]。本研究表明,ERGO通过降低Muribaculaceae的丰度,有助于恢复肠道菌群的健康平衡。这些发现提示,ERGO可能通过选择性调节肠道菌群组成,促进有益菌群的增殖并抑制潜在有害菌群的过度生长,从而在改善氧化应激损伤中发挥重要作用。

图3 ERGO对氧化应激损伤大鼠肠道菌群组成差异的影响
Fig.3 Effects of ERGO on the differences in gut microbiota composition in rats with oxidative stress injury
2.4.3 肠道菌群与SCFAs差异分析
如图4所示,与对照组相比,模型组中3种肠道菌属普雷沃氏菌科(Prevotellaceae)、梭菌纲 vadinBB60 群(Clostridia vadinBB60 group)以及瘤胃球菌科(Ruminococcaceae)的相对丰度显著降低,差异具有统计学意义(P<0.01)。经ERGO干预后,这3种菌属的相对丰度均显著回升,且差异更为显著(P<0.01)。上述结果表明,ERGO能够有效增加有益菌的相对丰度,优化肠道菌群结构,从而可能通过调节肠道微生态平衡来改善机体的氧化应激状态。这一发现进一步支持了ERGO在保护肠道健康及缓解氧化应激损伤中的潜在作用机制。
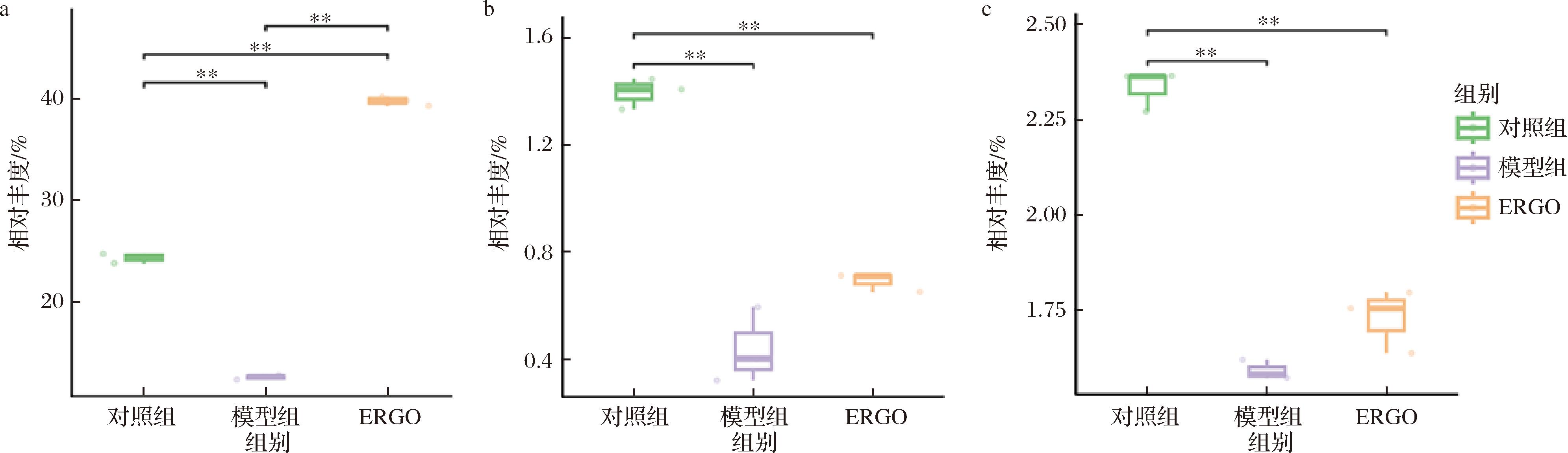
a-Prevotellaceae;b-Clostridia_vadinBB60_group;c-Ruminococcaceae
图4 ERGO对氧化应激损伤大鼠肠道菌群相对丰度变化的影响
Fig.4 Effects of ERGO on the relative abundance of gut microbiota in rats with oxidative stress injury
进一步测定大鼠粪便中的SCFAs含量(图5),结果显示与对照组相比,模型组中丁酸、异丁酸和戊酸的水平显著降低(P<0.01)。经ERGO干预后,各给药组的上述SCFAs水平均显著回升,且差异具有统计学意义(P<0.01)。已有研究证实,丁酸、异丁酸和戊酸作为重要的SCFAs,能够通过增强抗氧化防御系统缓解氧化应激,其机制包括减少活性氧的过量生成并修复氧化损伤,从而保护细胞免受氧化应激的侵害[18]。结果表明,ERGO能够有效提升肠道中这3种SCFAs的含量,这可能是其发挥抗氧化活性的重要机制之一。这一发现进一步支持了ERGO通过调节肠道菌群代谢产物来改善氧化应激损伤的假设。
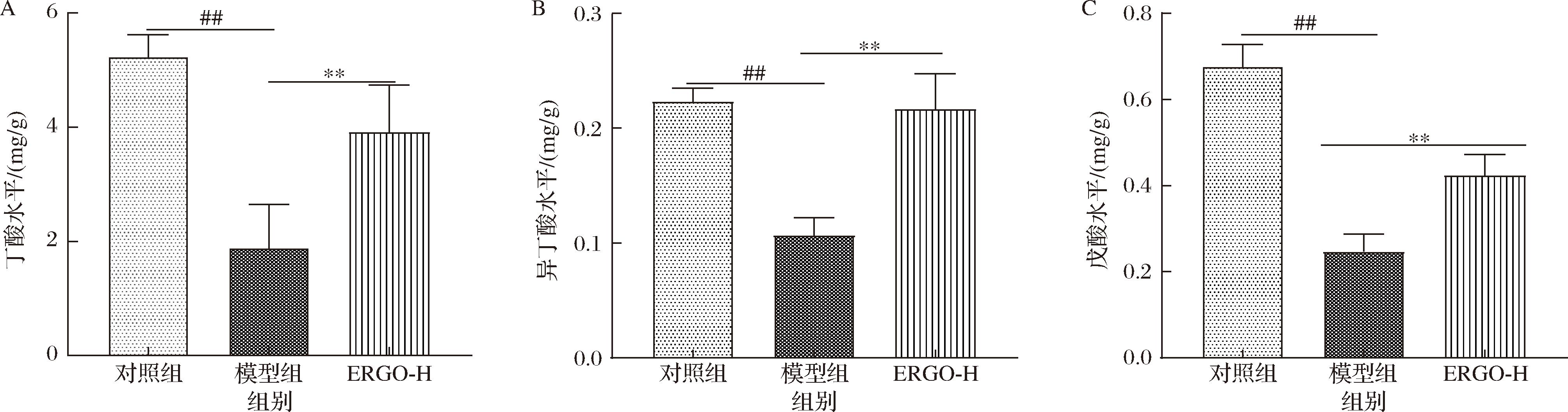
A-丁酸水平;B-异丁酸水平;C-戊酸水平
图5 ERGO对氧化应激损伤大鼠肠道SCFAs含量的影响
Fig.5 Effects of ERGO on the content of SCFAs in the gut of rats with oxidative stress injury
3 讨论
氧化应激是一种生物体内促氧化剂与抗氧化剂系统失衡的现象,导致自由基过量产生和抗氧化防御系统功能下降,从而使生物体更易发生氧化反应[1]。这种现象与多种慢性健康问题密切相关, 补充天然抗氧化剂是控制氧化应激的有效策略之一。ERGO是一种具有抗氧化特性的天然产物[9-10]。尽管已有多个研究评估了其抗氧化活性,但这些研究大多基于体外测量[19],而体外抗氧化活性很难准确预测其在体内的效果。也有研究采用了疾病动物模型,如糖尿病和非酒精性脂肪性肝病模型等测定了抗氧化活性[20-21],但这些体内研究主要是观测ERGO对疾病中氧化应激反应的影响,并未在非疾病状态动物模型中系统地从氧化应激损伤标志物含量、抗氧化酶活性及抗氧化分子水平等多个层面对ERGO的抗氧化活性进行评估。D-gal诱导的大鼠模型作为一种显示氧化应激和活性氧种类紊乱的非疾病状态的动物模型,具有操作简便和结果稳定的优点。因此,本文采用此模型来研究ERGO在体内的抗氧化活性。
研究发现,D-gal给药会导致氧化应激损伤动物体质量下降,这一趋势与文献研究报道相一致[9],但其具体机制尚需进一步探究。在本研究中,与对照组相比,ERGO各个剂量组大鼠体质量没有显著的变化。然而值得注意的是,作为维持脂质稳态的关键器官,模型组的肝脏指数显著低于对照组。这一现象可能是由于D-gal处理引起的脂质代谢紊乱所致,研究中肝脏的苏木精-伊红染色结果进一步证实了这一点,显示模型小鼠出现了肝脏病变[22]。此外,本研究还发现D-gal处理组的肾脏指数显著低于空白对照组,但其具体机制仍有待明确。
本研究结果表明,ERGO能够显著降低D-gal诱导的大鼠血清、肝脏、肾脏和脾脏中MDA和PC的含量,同时提高SOD和CAT的活性以及GSH的水平。这些数据表明,ERGO具有直接的抗氧化作用,能够有效清除自由基,减轻氧化应激对细胞膜、蛋白质等生物大分子的损伤,从而维护细胞结构和功能的完整性。这些研究结果证实ERGO是一种高效的自由基清除剂,能够与多种自由基,如超氧阴离子自由基、羟自由基和过氧自由基等反应,从而减轻氧化应激造成的损伤。
IL-1β、IL-6和TNF-α可促进炎症反应和活性氧生成,与氧化应激损伤密切相关。它们之间的相互作用形成了一个复杂的网络,共同加剧机体的氧化损伤[15]。本实验结果表明,ERGO可显著降低氧化应激损伤大鼠血清中IL-1β、IL-6和TNF-α水平,提示ERGO通过控制氧化应激反应和降低炎症因子水平以达到抗氧化活性。
氧化应激损伤后,肠道菌群和炎症形成了一个复杂的相互作用网络:氧化应激导致菌群失衡,菌群失调破坏肠道屏障并影响免疫反应,进而加剧炎症,而炎症又会进一步促进氧化应激,形成由氧化应激-菌群失调-炎症加剧-再氧化应激构成的恶性循环。Prevotellaceae、Clostridia vadinBB60 group以及Ruminococcaceae是肠道中重要的菌群,与SCFAs的产生密切相关[23]。Prevotellaceae菌属能够通过发酵膳食纤维产生SCFAs,如乙酸和丙酸,这些代谢产物不仅为肠道细胞提供能量,还能通过调节氧化应激相关通路,发挥抗氧化作用[24]。Clostridia vadinBB60 group是肠道菌群中一类重要的厌氧菌,其代谢活动同样促进SCFAs的生成,尤其是丁酸,这种SCFAs在维持肠道屏障功能和抑制炎症反应方面具有显著作用,从而间接减轻氧化应激损伤。Ruminococcaceae菌属则是丁酸的主要生产者之一,丁酸作为重要的SCFAs,能够通过激活抗氧化酶系统(如SOD和谷胱甘肽过氧化物酶),直接中和自由基,减轻氧化应激对机体的损害。此外,这些SCFAs还能通过抑制TLR4/NF-κB等炎症信号通路,减少IL-1β、IL-6和TNF-α等促炎因子的产生[25]、减少活性氧的过量生成并修复氧化损伤,从而保护细胞免受氧化应激的侵害[18]。本研究初步结果表明,ERGO 干预能够改善肠道菌群结构,显著增加有益菌丰度(如Prevotellaceae、Clostridia vadinBB60 group以及Ruminococcaceae),并促进 SCFAs 的生成。因此ERGO的抗氧化活性可能与调节道菌群组成和提高肠道有益菌增加SCFAs含量有关。
4 结论
本研究系统探讨了ERGO对D-gal诱导的大鼠氧化应激损伤的保护作用及其潜在机制,重点考察了ERGO对肠道菌群和SCFAs的影响。研究结果表明,ERGO能显著减轻D-gal诱导的氧化应激损伤,多个剂量组均能有效改善氧化应激大鼠血清、肝脏、肾脏和脾脏中的5个关键氧化应激生化指标。同时,ERGO显著降低了氧化应激损伤大鼠血清中IL-1β、IL-6和TNF-α等炎症因子的水平,展现了良好的抗炎效果。在肠道微生态调节方面,ERGO能显著增加有益菌Prevotellaceae、Clostridia vadinBB60 group以及Ruminococcaceae的相对丰度,并提高肠道中丁酸、异丁酸和戊酸等SCFAs的含量。其作用机制可能与ERGO的直接抗氧化效应及其对肠道菌群的调节作用,进而促进SCFAs生成密切相关。未来研究需进一步阐明ERGO对肠道菌群的具体调节机制,以及肠道菌群在ERGO抗氧化作用中的确切角色,为开发基于“抗氧化-肠道微生态调控”协同策略的新型功能性食品或治疗药物提供更为深入的科学依据。
[1] SELVARAJ N R, NANDAN D, NAIR B G, et al.Oxidative stress and redox imbalance:Common mechanisms in cancer stem cells and neurodegenerative diseases[J].Cells, 2025, 14(7):511.
[2] LIU H J, JIN L H, WANG X Y, et al.Reactive oxygen species in polycystic ovary syndrome:Mechanistic insights into pathogenesis and therapeutic opportunities[J].Redox Biology, 2025, 85:103776.
[3] GUPTA N, VERMA K, NALLA S, et al.Free radicals as a double-edged sword:The cancer preventive and therapeutic roles of curcumin[J].Molecules, 2020, 25(22):5390.
[4] ZHENG Y X, SUN J L, LUO Z T, et al.Emerging mechanisms of lipid peroxidation in regulated cell death and its physiological implications[J].Cell Death &Disease, 2024, 15:859.
[5] CHANDIMALI N, BAK S G, PARK E H, et al.Free radicals and their impact on health and antioxidant defenses:A review[J].Cell Death Discovery, 2025, 11:19.
[6] MORÉN C, DESOUZA R M, GIRALDO D M, et al.Antioxidant therapeutic strategies in neurodegenerative diseases[J].International Journal of Molecular Sciences, 2022, 23(16):9328.
[7] MCBETH A, MILLER E A, THOMPSON B, et al.Balancing oxidative stress:How the gut microbiome supports redox homeostasis and mitochondrial health[J].Journal of Restorative Medicine, 2025, 15(1):4-19.
[8] MANFUL C F, FORDJOUR E, IKUMOINEIN E, et al.Therapeutic strategies targeting oxidative stress and inflammation:A narrative review[J].BioChem, 2025, 5(4):35.
[9] KUMARI M, DASRIYA V L, NATARAJ B H, et al.Lacticaseibacillus rhamnosus-derived exopolysaccharide attenuates D-galactose-induced oxidative stress and inflammatory brain injury and modulates gut microbiota in a mouse model[J].Microorganisms, 2022, 10(10):2046.
[10] 葛珈铭, 弓思涵, 韩翠婷, 等.麦角硫因的药理作用研究进展[J].现代药物与临床, 2023, 38(8):2093-2099.GE J M, GONG S H, HAN C T, et al.Progress on pharmacological effects of ergothioneine[J].Drugs &Clinic, 2023, 38(8):2093-2099.
[11] 刘晶晶, 金红宇, 胡晓茹, 等.基于肠道菌群-短链脂肪酸途径的人参改善运动性疲劳作用机制探索[J].中国现代中药, 2024, 26(11):1930-1937.LIU J J, JIN H Y, HU X R, et al.Mechanism of Panax ginseng in improving exercise fatigue based on gut microbiota-short-chain fatty acid pathway[J].Modern Chinese Medicine, 2024, 26(11):1930-1937.
[12] AL-HAKEIM H K, AL-RUBAYE H T, AL-HADRAWI D S, et al.Long-COVID post-viral chronic fatigue and affective symptoms are associated with oxidative damage, lowered antioxidant defenses and inflammation:A proof of concept and mechanism study[J].Molecular Psychiatry, 2023, 28(2):564-578.
[13] KWON D H, CHA H J, LEE H, et al.Protective effect of glutathione against oxidative stress-induced cytotoxicity in RAW264.7 macrophages through activating the nuclear factor erythroid 2-related factor-2/heme oxygenase-1 pathway[J].Antioxidants, 2019, 8(4):82.
[14] JOMOVA K, ALOMAR S Y, ALWASEL S H, et al.Several lines of antioxidant defense against oxidative stress:Antioxidant enzymes, nanomaterials with multiple enzyme-mimicking activities, and low-molecular-weight antioxidants[J].Archives of Toxicology, 2024, 98(5):1323-1367.
[15] RAJENDRAN P, AL-SAEEDI F J, BEN AMMAR R, et al.Geraniol attenuates oxidative stress and neuroinflammation-mediated cognitive impairment in D galactose-induced mouse aging model[J].Aging, 2024, 16(6):5000-5026.
[16] LIU P Y, WANG Y B, YANG G, et al.The role of short-chain fatty acids in intestinal barrier function, inflammation, oxidative stress, and colonic carcinogenesis[J].Pharmacological Research, 2021, 165:105420.
[17] ZHAO Y Y, SOKOL H, CAO Q, et al.Systemic inflammatory response to daily exposure to microcystin-LR and the underlying gut microbial mechanisms[J].Journal of Hazardous Materials, 2024, 480:135855.
[18] FERRER M, BUEY B, GRASA L, et al.Protective role of short-chain fatty acids on intestinal oxidative stress induced by TNF-α[J].Cell Stress and Chaperones, 2024, 29(6):769-776.
[19] 黄政皖, 唐毓萍, 彭振刚.麦角硫因与7种抗氧化剂组合的抗氧化作用[J].香料香精化妆品, 2025(1):109-114.HUANG Z W, TANG Y P, PENG Z G.Combined antioxidant effect of ergothioneine with seven antioxidants[J].Flavour Fragrance Cosmetics, 2025(1):109-114.
[20] LAM-SIDUN D, PETERS K M, BORRADAILE N M.Mushroom-derived medicine? preclinical studies suggest potential benefits of ergothioneine for cardiometabolic health[J].International Journal of Molecular Sciences, 2021, 22(6):3246.
[21] CHEAH I K, TANG R, YE P, et al.Liver ergothioneine accumulation in a guinea pig model of non-alcoholic fatty liver disease.A possible mechanism of defence?[J].Free Radical Research, 2016, 50(1):14-25.
[22] ZHOU Y, XU Q, DONG Y, et al.Supplementation of mussel peptides reduces aging phenotype, lipid deposition and oxidative stress in D-galactose-induce aging mice[J].The Journal of Nutrition, Health and Aging, 2017, 21(10):1314-1320.
[23] RENDON-ROSALES M A, MÉNDEZ-ROMERO J I, HERN NDEZ-MENDOZA A, et al.Gut microbiota response to consumption of milks fermented with specific strains of Lactococcus lactis with hypocholesterolemic effect[J].Food Production, Processing and Nutrition, 2024, 6(1):58.
NDEZ-MENDOZA A, et al.Gut microbiota response to consumption of milks fermented with specific strains of Lactococcus lactis with hypocholesterolemic effect[J].Food Production, Processing and Nutrition, 2024, 6(1):58.
[24] MAZHAR M, ZHU Y, QIN L K.The interplay of dietary fibers and intestinal microbiota affects type 2 diabetes by generating short-chain fatty acids[J].Foods, 2023, 12(5):1023.
[25] GE S H, ZHANG S L, SHE L J, et al.Synergistic therapy of Chinese herbal medicine and gut microbiota modulation for post-stroke cognitive recovery:Focus on microbial metabolite and immunoinflammation[J].Frontiers in Microbiology, 2025, 16:1623843.