随着人们对健康、低热量食品的需求不断增长,新型甜味剂的开发与应用得到了广泛关注。作为目前应用最广泛的天然甜味剂之一,甜菊糖苷具有高甜度、低热量、不被人体直接代谢吸收等优点,已广泛应用于食品和饮料行业。其中,莱鲍迪苷D(rebaudioside D,Reb D)是一种从甜叶菊中提取的高甜度天然产物,其甜度约为蔗糖的250~350倍,且回味较短、苦味较弱,被认为是理想的蔗糖替代品[1]。然而,甜叶菊中Reb D的天然含量较低,难以通过直接提取满足工业化生产需求,因此亟需借助化学合成或生物催化途径实现高效制备[2]。相比之下,酶法转化因其绿色环保、立体选择性强和反应条件温和等优势,已成为Reb D合成的主要手段。
生物催化法主要依赖糖基转移酶催化甜菊糖苷类底物的糖基化反应,通过特定酶的作用将糖基选择性转移至目标位点,从而实现Reb D的高效合成[3]。目前,该方法多以Reb A为底物,已报道出可催化该反应的糖基转移酶如下:来源于甜叶菊的UGT91D2[4]、番茄的UGTSL2[5]、枯草芽孢杆菌的YojK[3]、马铃薯的StUGT[6]以及人参的PgUGT[7]。其中部分酶经蛋白质工程改造后,其催化性能显著提升(表1)。近年来,结构建模、分子对接、分子动力学模拟和能量分析等方法被广泛应用于解析酶的三维结构特征、底物识别机制及催化过程,为酶的理性改造提供了理论依据[8]。蛋白质三维结构的获得对于研究Reb D生物催化作用机制的解析至关重要。例如,YAGI等[9]利用AlphaFold预测人类糖基转移酶结构,探讨其附加结构域的功能多样性。分子对接和分子动力学模拟技术常用来探究目标蛋白和底物之间的作用机制。例如,XIA等[10]通过分子对接分析拟南芥尿苷二磷酸葡萄糖醛酸转移酶(uridine diphosphate glucuronosyltransferase,UGT)与对羟基苄醇之间的相互作用。此外,YANG等[11]结合分子对接与100 ns分子动力学模拟,利用均方根偏差(root-mean-square error,RMSD)与均方根波动(root mean square fluctuation,RMSF)分析发现,核心堆积增强、表面电荷重排以及环刚性增加导致UGT76G1突变体热稳定性显著提升。
表1 不同生物来源的糖基转移酶活性提高的实例
Table 1 Examples of increased glycosyltransferase activity from different biological sources
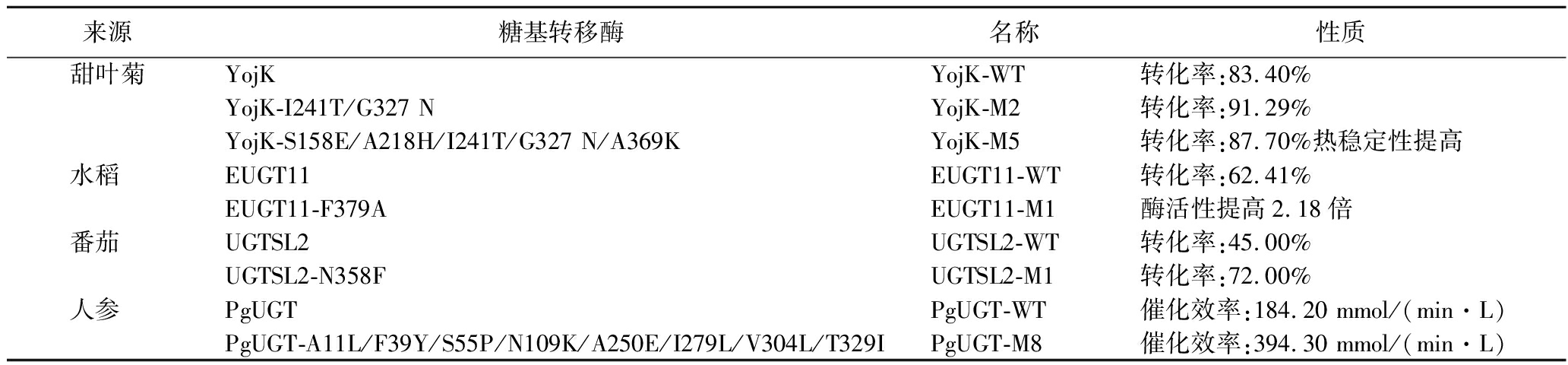
来源糖基转移酶名称性质甜叶菊YojKYojK-WT转化率:83.40%YojK-I241T/G327 NYojK-M2转化率:91.29%YojK-S158E/A218H/I241T/G327 N/A369KYojK-M5转化率:87.70%热稳定性提高水稻 EUGT11EUGT11-WT转化率:62.41%EUGT11-F379AEUGT11-M1酶活性提高2.18倍番茄 UGTSL2UGTSL2-WT转化率:45.00%UGTSL2-N358FUGTSL2-M1转化率:72.00%人参 PgUGTPgUGT-WT催化效率:184.20 mmol/(min·L)PgUGT-A11L/F39Y/S55P/N109K/A250E/I279L/V304L/T329IPgUGT-M8催化效率:394.30 mmol/(min·L)
尽管已有研究在糖基转移酶改造方面取得一定进展,但针对催化Reb D合成相关酶的性能提升机制尚缺乏系统性分析。为此,本文首先通过序列与结构分析,阐明了催化Reb A生成Reb D的糖基转移酶的保守性特征及结构基础,进一步对催化性能提高的突变体开展分子动力学模拟,结合构象变化与能量分析,系统解析突变对酶-底物稳定性及结合模式的影响。本研究有助于深入理解酶的结构功能关系,为优化糖基转移酶的催化性能及高效合成Reb D提供理论支持和策略参考。
1 材料与方法
1.1 分子模型构建
从PDB数据库(https://www.rcsb.org/)得到糖基转移酶YojK的结构(PDB号:7VM0)。为了补充该结构中的缺失loop,使用Modeller软件进行了结构重建。本研究采用了Alphafold2[12]构建糖基转移酶EUGT11、UGTSL2、PgUGT的三维模型。使用Discovery Studio[13]软件进一步构建了相关突变体的结构。对于底物尿苷二磷酸葡萄糖(uridine diphosphate glucose,UDPG)和Reb A,首先从PubChem网站(https://pubchem.ncbi.nlm.nih.gov/)下载了二级结构数据,通过Chembio 3D[14]软件进行结构优化。
1.2 分子模拟
1.2.1 分子对接
Auto Dock和Auto Dock Vina软件用于获得糖基转移酶复合体的构象[15]。在YojK晶体结构中,尿苷二磷酸(uridine diphosphate,UDP)已与糖基转移酶结合,因此在本研究中将UDP替换为UDPG。随后,使用AutoDock Vina对YojK-UDPG复合体与Reb A进行对接,选取能量最低的构象用于后续的分子动力学模拟。已有研究表明,YojK与UDPG结合的关键氨基酸位点包括:N16、T240、Y288、H304、E312、D328和Q329。为了提高对接精度,将YojK与糖基转移酶EUGT11、UGTSL2和PgUGT进行序列和结构比对,并依据这些糖基转移酶对应的保守氨基酸位点设置对接盒子。随后,使用AutoDock Vina对这些糖基转移酶-UDPG复合体与Reb A进行对接,得到初始模拟构象。
1.2.2 分子动力学模拟
利用GROMACS 2022进行分子动力学模拟[16],Gromos 54A7[17]联合原子力场被应用。以蛋白配体复合物为中心建立正方体盒子,放其边缘距盒子的最小距离为1.50 nm。随后,向盒子中添加相应的水分子,选择SPC/E水分子。为保持溶液的中性条件,溶液中相应数量的水分子被替换为Cl离子。能量最小化采用最速下降法,最大步数50 000,截断半径设为1.2 nm,使用PME处理长程电荷,施加三维周期性边界条件。NVT与NPT平衡模拟均使用Leap-frog积分器(步长2 fs,共5 000步),温度控制采用V-rescale方法,NPT阶段启用Parrinello-Rahman压强耦合。所有键通过LINCS算法约束。生产模拟时长100 ns,步长2 fs,每50 ps输出1次轨迹,其他参数与平衡阶段一致。
1.3 数据分析
利用gmx trjconv命令处理轨迹,通过gmx rms命令计算蛋白、配体的RMSD[18],gmx rmsf计算蛋白质各个残基的RMSF[19-20],揭示其动态特性。gmx distance计算催化原子之间的距离,分别是d(H27-NE2--O8-Reb A):Reb A的C-19位羧酸基团共价连接的葡糖基的2位羟基氧原子与催化残基组氨酸中NE2氮原子;d(UDPG-C1--O8-Reb A):Reb A的C-19位羧酸基团葡萄糖的2位羟基氧原子与糖基供体UDPG中葡糖基1位碳原子C-1。VMD软件被用来计算Reb A不同部位与蛋白质之间氢键。设定供体与受体原子之间的距离小于0.35 nm,并且角度小于40°,编写Python脚本统计氢键的占用度(occupancy)。利用gmx_covar和gmx_anaeig命令,获得了协方差矩阵、特征向量和特征值。使用gmx_sham模块,进一步构建了自由能景观(free energy landscape,FEL)。
2 结果与分析
2.1 糖基转移酶的结构特征
2.1.1 糖基转移酶保守位点分析
保守氨基酸在酶的催化活性、底物结合及分子识别中具有至关重要的作用[21]。对催化生成Reb D的糖基转移酶的序列进行比对,发现以下氨基酸残基G13、H14、P17、L82、D102、I105、D107、G211、G239、P280、F284、R286、P290、Q291、I294、L295、F301、H304、G306、S309、E312、F316、P319、D328、Q329(以YojK为标准)在不同的糖基转移酶序列中高度保守(图1)。结构映射结果显示,这些保守残基主要集中于C端Rossmann折叠结构域,少数分布于N端。其中D102、G211、G239、P280、P290、H304、G306和P319位于柔性较大的loop区。值得注意的是,G13、P17位于活性残基附近,可能与底物的催化过程密切相关。此外,D328和Q329是参与UDPG中葡糖基识别和结合的重要残基。
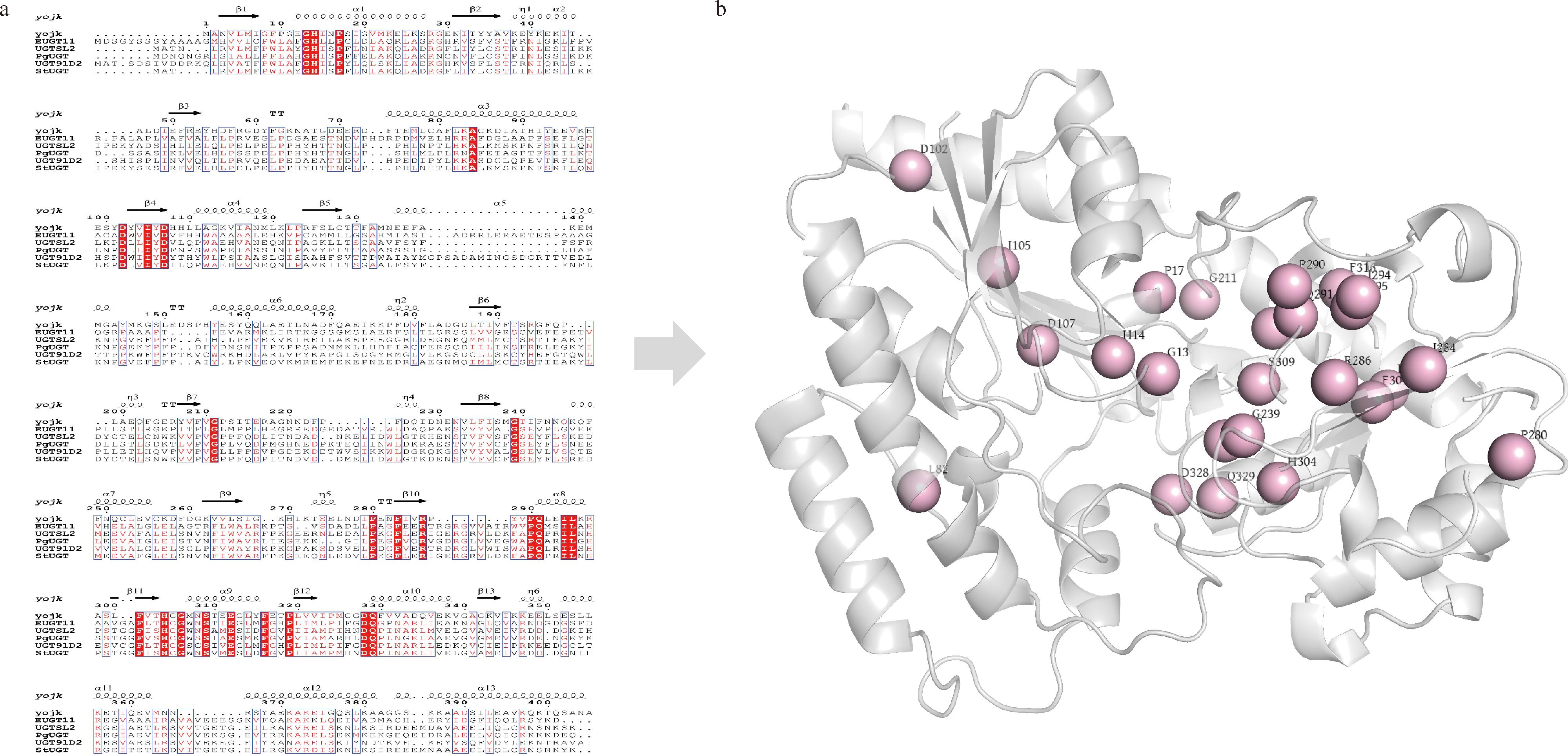
a-糖基转移酶多序列比对结果;b-保守位点投射在YojK结构中
图1 保守位点分析
Fig.1 Analysis of conserved residues
2.1.2 糖基转移酶结构分析
对催化Reb A转化为Reb D的糖基转移酶的结构进行分析,以识别和对比他们的结构特征。结构比对发现见电子版增强出版附图1(https://doi.org/10.13995/j.cnki.11-1802/ts.044006,下同),这些糖基转移酶都有相似的Rossmann结构域,并且β-sheet叠合的较好,但α螺旋和loop区域数量有差异,是整体结构难以完全叠合的主要原因。此外,YojK与其他糖基转移酶在整体结构上的保守性相对较低。相比蛋白整体结构,活性中心的构象对催化反应的影响更为显著[22],因此本研究进一步聚焦于活性中心的结构差异。选取催化残基H14和D107周围5Å范围内的氨基酸作为活性中心,分别与Yojk进行比对,结果如图2所示。YojK与EUGT11整体结构的RMSD为4.64,而活性中心的RMSD为4.53,二者差异较小。YojK与UGT91D2的整体结构和活性中心的RMSD分别为4.96和3.03,表明活性中心的结构相似度高于整体蛋白。此外,YojK与PgUGT、UGTSL2、StUGT活性中心的结构差异显著小于整体结构,RMSD值分别为1.05、0.80和0.90。这些数据表明,尽管蛋白的整体结构差异较大,但活性中心的相似性较高。从整体到局部系统地分析结构差异,可以更全面地理解催化机制。
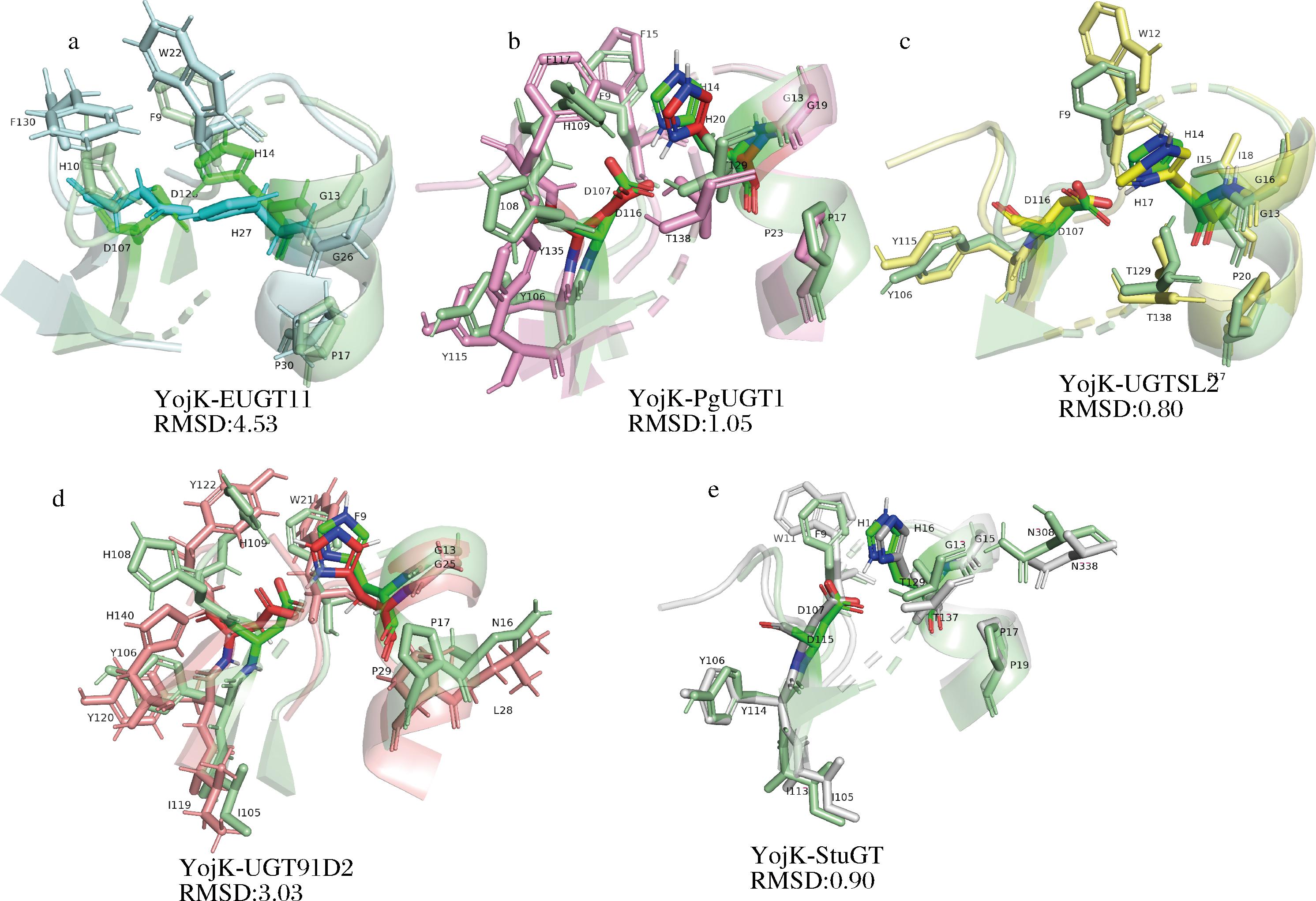
a-YojK与EUGT11活性中心结构比对;b-YojK与PgUGT活性中心结构比对;c-YojK与UGTSL2活性中心结构比对;d-YojK与UGT91D2活性中心结构比对;e-YojK与StUGT活性中心结构比对
图2 糖基转移酶活性中心结构比对
Fig.2 Active site structural alignment of glycosyltransferase
为直观展示不同糖基转移酶活性中心中保守残基的空间分布,采用棒状模型标示结构中保守性较高的残基。结果显示,YojK与EUGT11相比(图2-a),其G13/G26与P17/P30在序列和空间位置上高度保守;催化残基H14/H27上方的F9/W22虽具体位置略有偏移,但均含有芳香环结构,显示出一定的功能类同性;此外,H10/F130的侧链亦均为环状结构。与PgUGT、UGTSL2、UGT91D2及StUGT比对发现(图2-b~图2-e),F9、G13、P17、Y106、T129等关键位点在多个酶中均表现出较高保守性,尤其是F9位点,在PgUGT中为F,其余酶则为W,均为疏水性芳香族氨基酸,认为该类氨基酸在活性中心中可能具有重要的结构或功能作用。为进一步验证上述规律,分别对EUGT11、PgUGT、UGTSL2、UGT91D2和StUGT的活性中心区域进行了两两结构比对(附图2)。结果表明,尽管其氨基酸组成存在一定差异,但活性中心区域的二级结构相对一致,且均在相应位置保留了疏水性芳香环侧链残基,显示出高度的空间构象保守性。这一结果支持了活性中心中疏水环状氨基酸在催化功能中具有关键作用的推测。
2.1.3 活性中心理化性质分析
为进一步揭示不同糖基转移酶的催化特性,对其活性中心的理化性质进行了分析(表2)。结果显示,所有酶的等电点集中在5.08~6.25,表明在中性或碱性环境下呈负电荷,更易与带正电荷的底物或蛋白质发生相互作用。PgUGT和UGT91D2表现出较高的芳香性,活性中心疏水性强,利于与疏水性底物结合。调用Protein Analysis来计算不稳定性指数,通过综合氨基酸的稳定性评分和氨基酸对的组合效应,评估蛋白质的稳定性。StUGT和UGTSL2的活性中心不稳定性指数较高,表明活性中心区域不稳定,容易发生构象变化,帮助蛋白质适应不同底物的结合。EUGT11和UGT91D2的疏水性较强,而YojK疏水性最低,显示其活性中心更趋亲水。上述理化性质揭示了各糖基转移酶在底物识别和催化适应性方面的差异,为深入理解其催化机制提供了理论依据。
表2 糖基转移酶活性中心理化性质
Table 2 Physicochemical properties of the active sites of glycosyltransferases
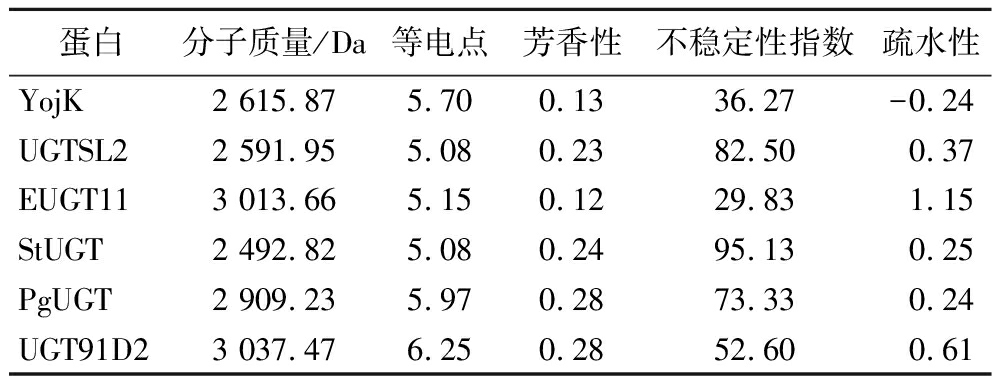
蛋白分子质量/Da等电点芳香性不稳定性指数疏水性YojK2 615.875.700.1336.27-0.24UGTSL22 591.955.080.2382.500.37EUGT113 013.665.150.1229.831.15StUGT2 492.825.080.2495.130.25PgUGT2 909.235.970.2873.330.24UGT91D23 037.476.250.2852.600.61
2.2 糖基转移酶催化效率提升的分子机制
2.2.1 蛋白结构稳定性对催化效率的影响
通过分析RMSD和RMSF值的变化,评估糖基转移酶突变前后的结构稳定性。图3-a显示,YojK-M2的RMSD始终低于野生型(YojK-WT),表明其结构更稳定,YojK-M5在前期RMSD低于WT,50 ns后则高于WT,可能与突变引起的局部构象变化或柔性增加有关。RMSF分析显示(图3-b),两突变体在40-50区段的柔性均增强,YojK-M5在60-70区段的柔性提升尤为明显。即突变主要影响局部动态行为,未显著改变整体结构稳定性。图3-c显示,EUGT11突变后RMSD明显下降,30 ns后稳定在约0.5 nm,表明整体稳定性增强。RMSF分析发现(图3-d),突变导致161-172、256-258和312-322区段的柔性提高,但未对蛋白整体稳定性造成不利影响。
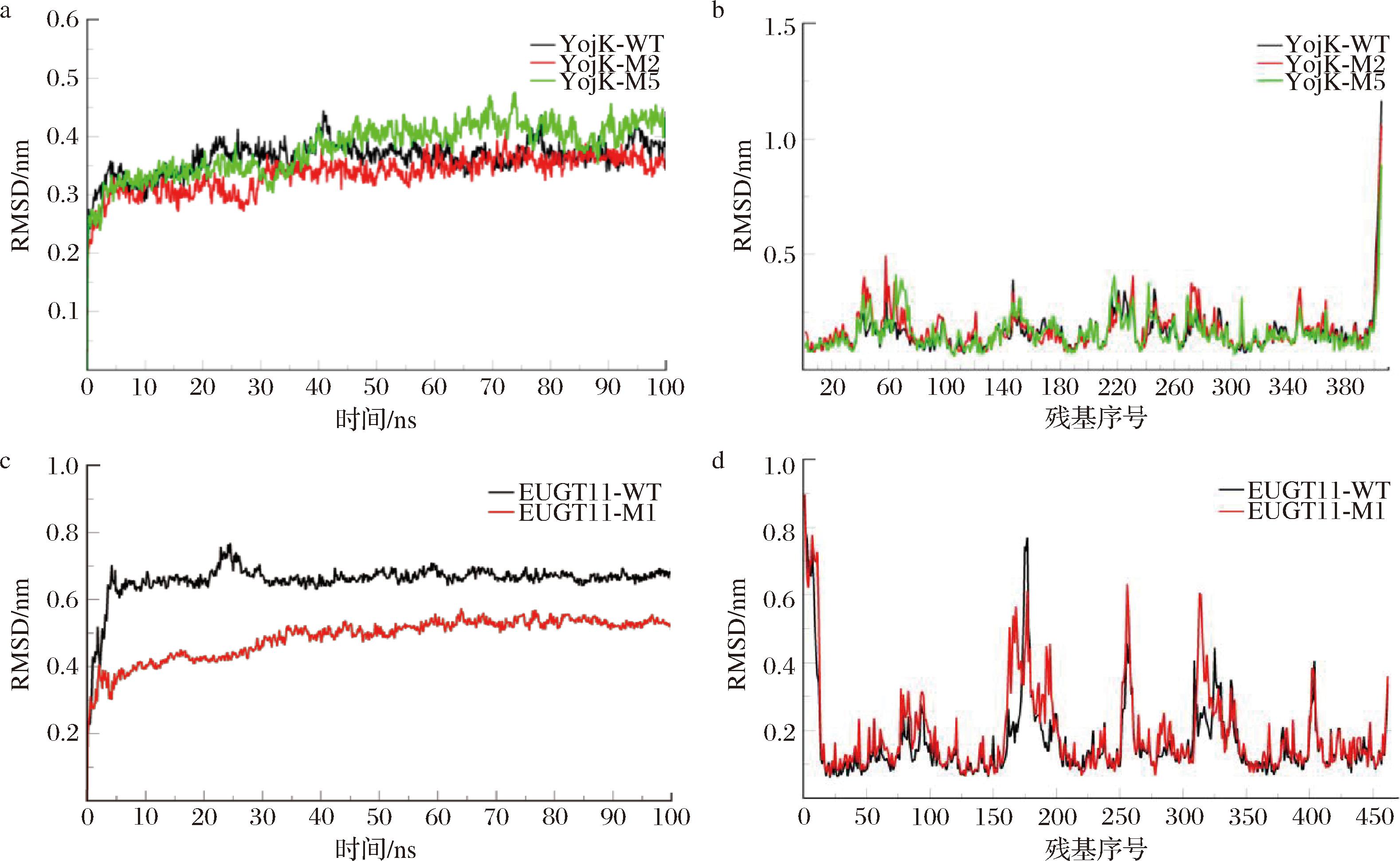
a-YojK的RMSD;b-YojK的RMSF;c-EUGT11的RMSD;d-EUGT11的RMSF
图3 模拟期间糖基转移酶的RMSD、RMSF值变化
Fig.3 RMSD and RMSF of glycosyltransferases during simulation
对糖基转移酶UGTSL2突变前后的稳定性变化进行分析,结果见附图3。模拟平衡后,UGTSL2-M1的RMSD值较野生型高出约0.05 nm,变化较小。突变后大部分氨基酸的RMSF值与野生型相似。然而,氨基酸片段179~194的RMSF值显著增高(附图3-b)。尽管整体结构变化较小,局部区域的柔性增强可能影响蛋白功能或与底物的结合。如附图3-c、附图3-d所示,PgUGT突变后整体稳定性下降,60-65、155-165和290-300片段柔性明显增强。进一步分析发现,突变位点S55P和A250E反而增强了所在区域的刚性,而柔性增强的区域并未直接包含突变位点,说明突变对非突变区域产生了间接结构影响。因此,尽管整体结构稳定性变化有限,突变引发的局部柔性调控为催化效率提升提供了结构基础。
2.2.2 底物稳定性变化分析
进一步分析了模拟过程中糖基供体UDPG和糖基受体Reb A的稳定性变化。图4-a显示,在YojK的模拟体系中,突变体的Reb A的RMSD值均低于野生型,表明突变增强了Reb A在活性位点中的稳定性。这一结果意味着突变通过优化Reb A的构象,促进了其与糖基转移酶的结合和稳定性。相反,在EUGT11(图4-b)、UGTSL2(图4-c)和PgUGT(图4-d)模拟体系中,突变后的Reb A的RMSD值普遍高于野生型,显示出Reb A的稳定性有所下降。
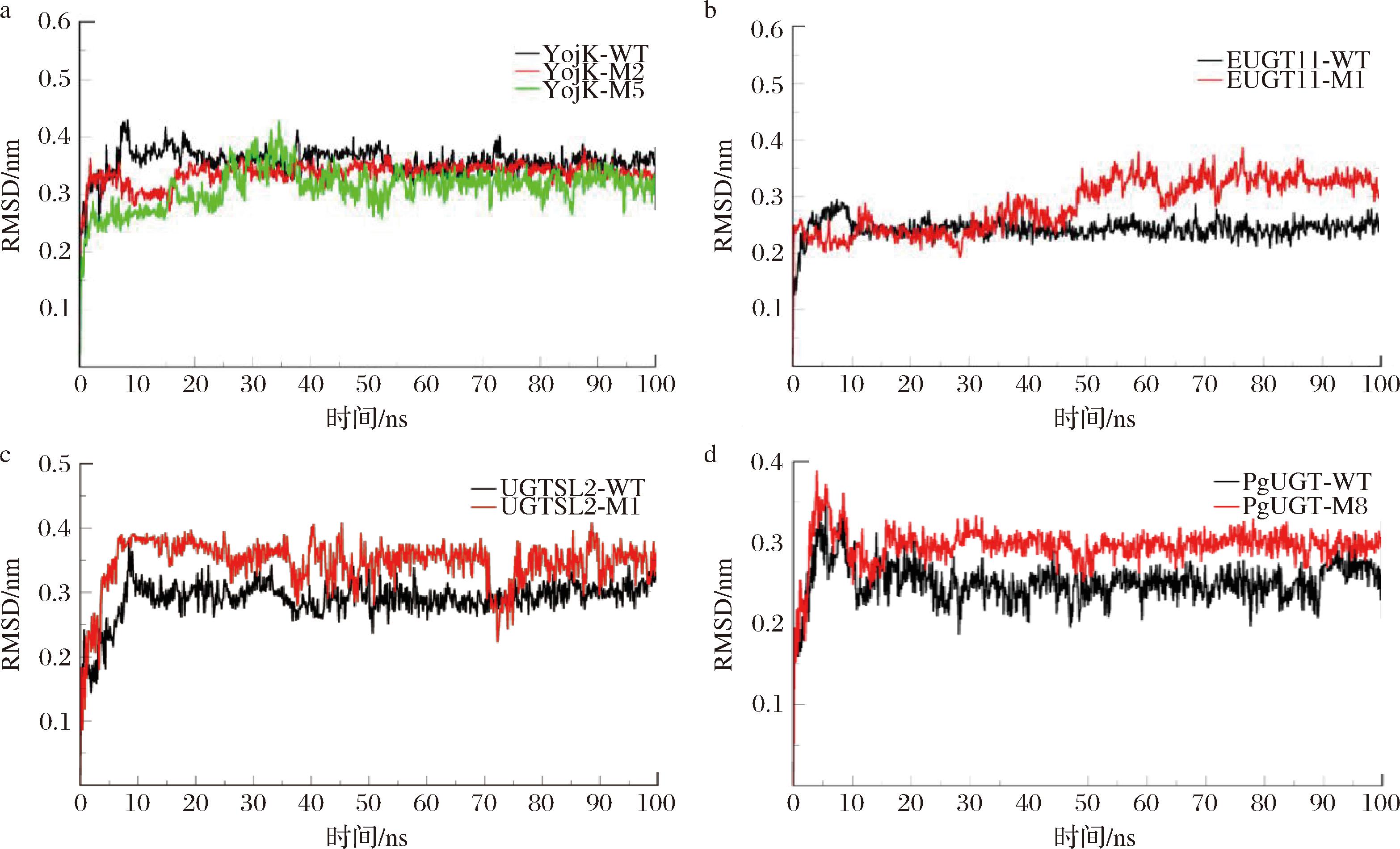
a-YojK复合体中Reb A的RMSD值变化;b-EUGT11复合体中Reb A的RMSD值;c-UGTSL2复合体中Reb A的RMSD值;d-PgUGT复合体中Reb A的RMSD值变化
图4 模拟期间糖基转移酶复合体中Reb A的RMSD值变化
Fig.4 RMSD variations of Reb A in the glycosyltransferase complexes during the simulation
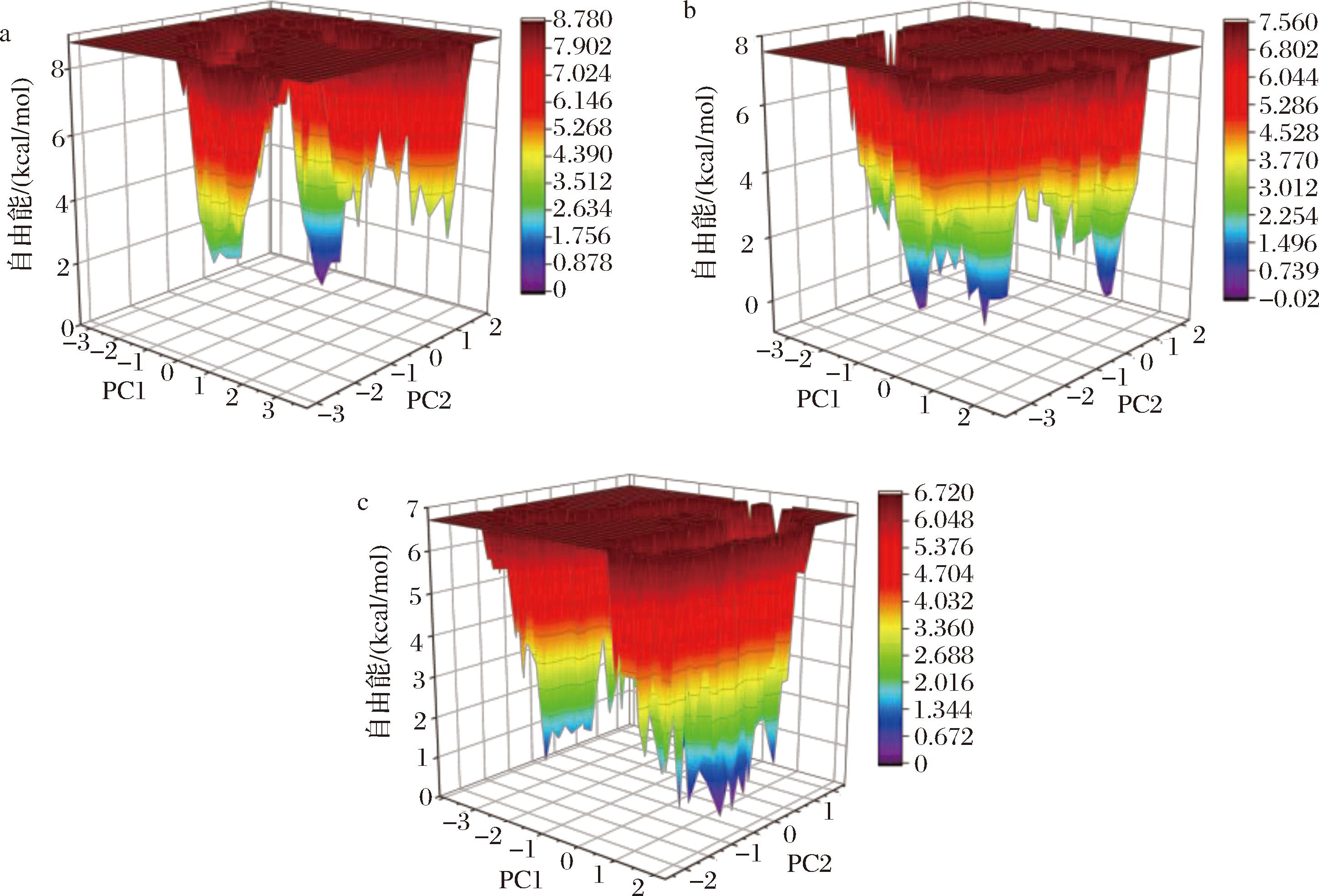
a-YojK-WT;b-YojK-M2;c-YojK-M5
图5 YojK野生型和突变体的自由能形貌图
Fig.5 Free energy landscapes of YojK wild type and mutants
如附图4所示,UDPG在不同糖基转移酶体系中的稳定性变化趋势与Reb A明显不同。在YojK体系中,2种突变体的UDPG在模拟后期均表现出比野生型更高的稳定性(附图4-a)。其中,YojK-M2突变体中UDPG的RMSD稳定在约0.2 nm,而YojK-M5在约90 ns后RMSD显著下降,反映其结构稳定性在模拟后期明显提升。在EUGT11体系中(附图4-b),EUGT11-M1突变体同样展现出优于野生型的UDPG稳定性,表示该突变有助于维持供体底物的构象稳定性。相比之下,附图4-c与附图4-d表明,在UGTSL2和PgUGT的突变体中,UDPG在活性位点中的稳定性显著降低。通过对底物稳定性分析发现,糖基转移酶的催化效率不仅取决于底物的结合稳定性,还需要考虑双底物之间的协同作用。
2.2.3 构象空间变化与结构灵活性分析
主成分分析(principal component analysis,PCA)常用于蛋白质折叠与解折叠的分子动力学轨迹降维和运动模式分析[23]。本研究对糖基转移酶及其突变体的轨迹进行PCA,统计前40个本征向量对应的本征值。如附图5所示,前2个本征向量的本征值较高,突变体在这2个向量上的本征值高于野生型,表明突变体沿主要运动模式的协同运动更为剧烈。基于此,选取PC1和PC2构建糖基转移酶的自由能景观图。YojK的自由能景观图如图5所示,只有1个局部极小值,而突变体有多个极小值。表明突变体在功能上具备更多的潜力和灵活性,即更高的催化效率或对不同底物的适应性更强。YojK-M2和YojK-M5具有更崎岖和更丰富的构象态,存在更多的自由能最小化区域,说明这些构象态之间的转换所需的能量屏障较低。这意味着突变体在不同构象态之间转换更容易,使酶的催化循环更加高效。
如附图6-a和附图6-b所示,EUGT11-WT只有1个较大体积的能量盆地和1个极小值,EUGT11-M1有2个能量盆地,并且其中1个存在2个极小值。表明分子在这一能量盆地中有2个稳定的构象状态,可以在这些构象之间动态转换。突变丰富了EUGT11的构象态,有助于降低构象转换的能量屏障,导致蛋白结构更加灵活。如附图6-c和6-d所示,糖基转移酶UGTSL2突变后,能量盆地的数量减少,表明蛋白质的构象灵活性降低,而其构象稳定性增加。通过分析突变后2个极小值之间的能垒高度,可以推断出构象切换的难度增加。糖基转移酶PgUGT突变后具有2个盆地,其中一个呈平坦状,底部区域几乎没有明显的极小值或能量差异(附图6-e和6-f)。这表示体系在这一区域内处于相对均匀的平衡状态,且各构象之间能量差异不大,处于非特异性的状态。另一个盆地出现2个局部最小值,这些极小值代表2种相对稳定的构象。
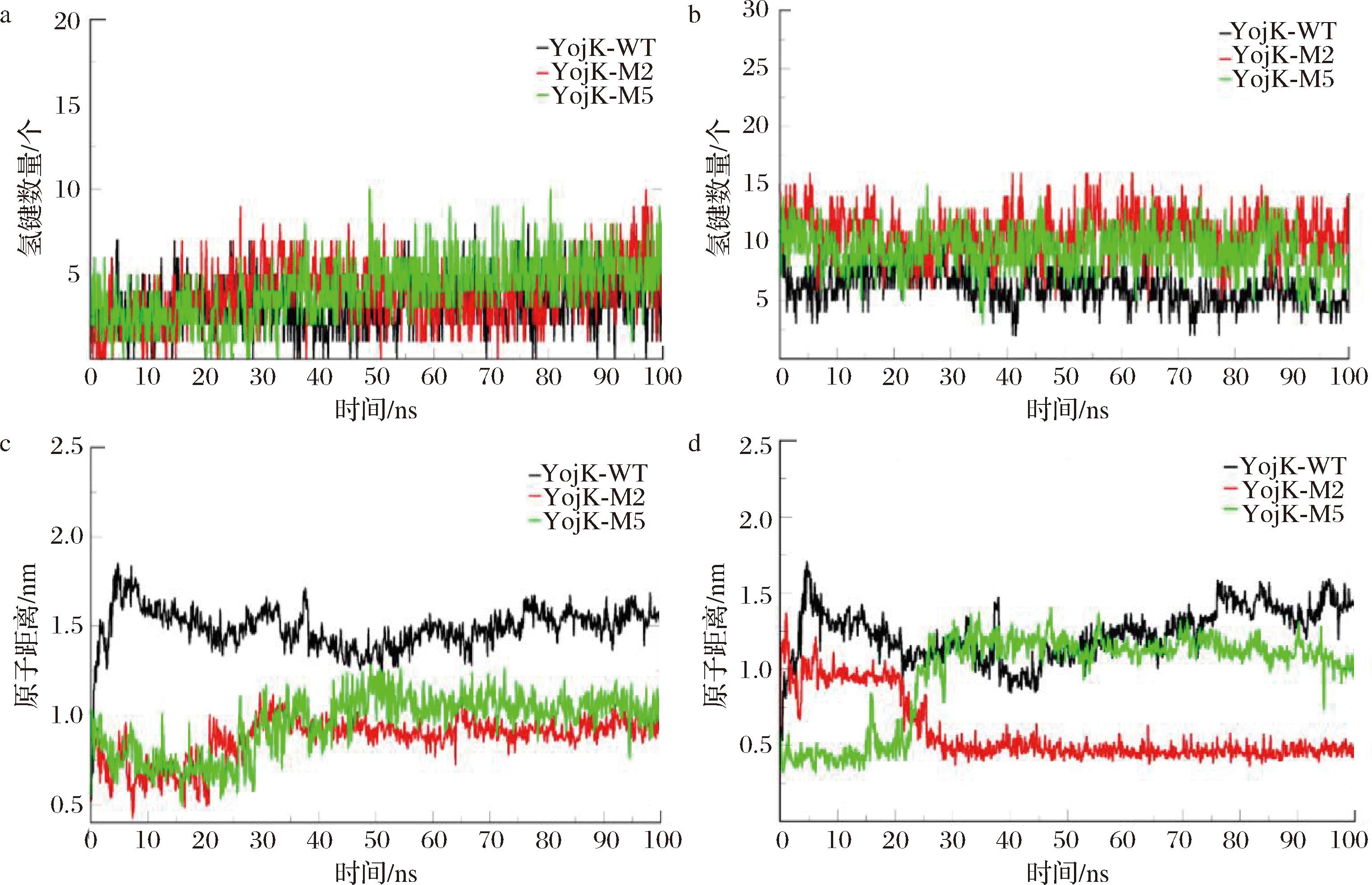
a-YojK与Reb A的氢键数量;b-YojK与UDPG的氢键数量;c-YojK与Reb A的关键原子距离;d-UDPG与Reb A的关键原子距离
图6 模拟期间YojK与底物的氢键数量和关键原子距离
Fig.6 Number of hydrogen bonds and key atomic distances between YojK and the substrate during the simulation
2.2.4 氢键作用与关键原子距离对催化效率的影响
计算氢键数量的变化有助于揭示糖基转移酶与底物之间的相互作用强度和稳定性,比较催化原子之间的距离有助于分析催化活性的差异,从而为理解催化机制和优化酶性能提供重要信息[24]。图6-a和图6-b显示,突变后YojK-M2、YojK-M5与底物Reb A、UDPG之间氢键数量增加,氢键相互作用增强。相较于野生型,模拟期间突变体的催化残基H14与Reb A之间的距离均减小(图6-c)。同样的,突变体的Reb A与UDPG关键原子之间的距离小于野生型,特别是YojK-M2,在20 ns之后距离保持在0.5 nm左右(图6-d)。综上,YojK突变体中增强的氢键作用及催化关键原子之间距离的减小,共同促进了底物转化率的提升。
分析糖基转移酶EUGT11和Reb A之间的氢键相互作用,发现平衡后突变体与Reb A、UDPG之间的氢键数量均略高于野生型(附图7-a和附图7-b)。对关键原子之间的距离进行比较,发现突变后d(H27-NE2--O8-Reb A)的值在25 ns之后开始减小,在90~95 ns期间又增大,之后与野生型保持一致。从附图7-c中可以看出在模拟的大部分时间中,突变体的d(H27-NE2--O8-Reb A)小于野生型,即有利于反应发生。同样的,突变后d(UDPG-C1--O8-Reb A)在8 ns后均小于野生型(附图7-d),即突变使UDPG的葡萄糖基更容易与Reb A结合生成Reb D。综上,突变体通过优化关键原子之间的空间距离和氢键相互作用提升了催化效率。
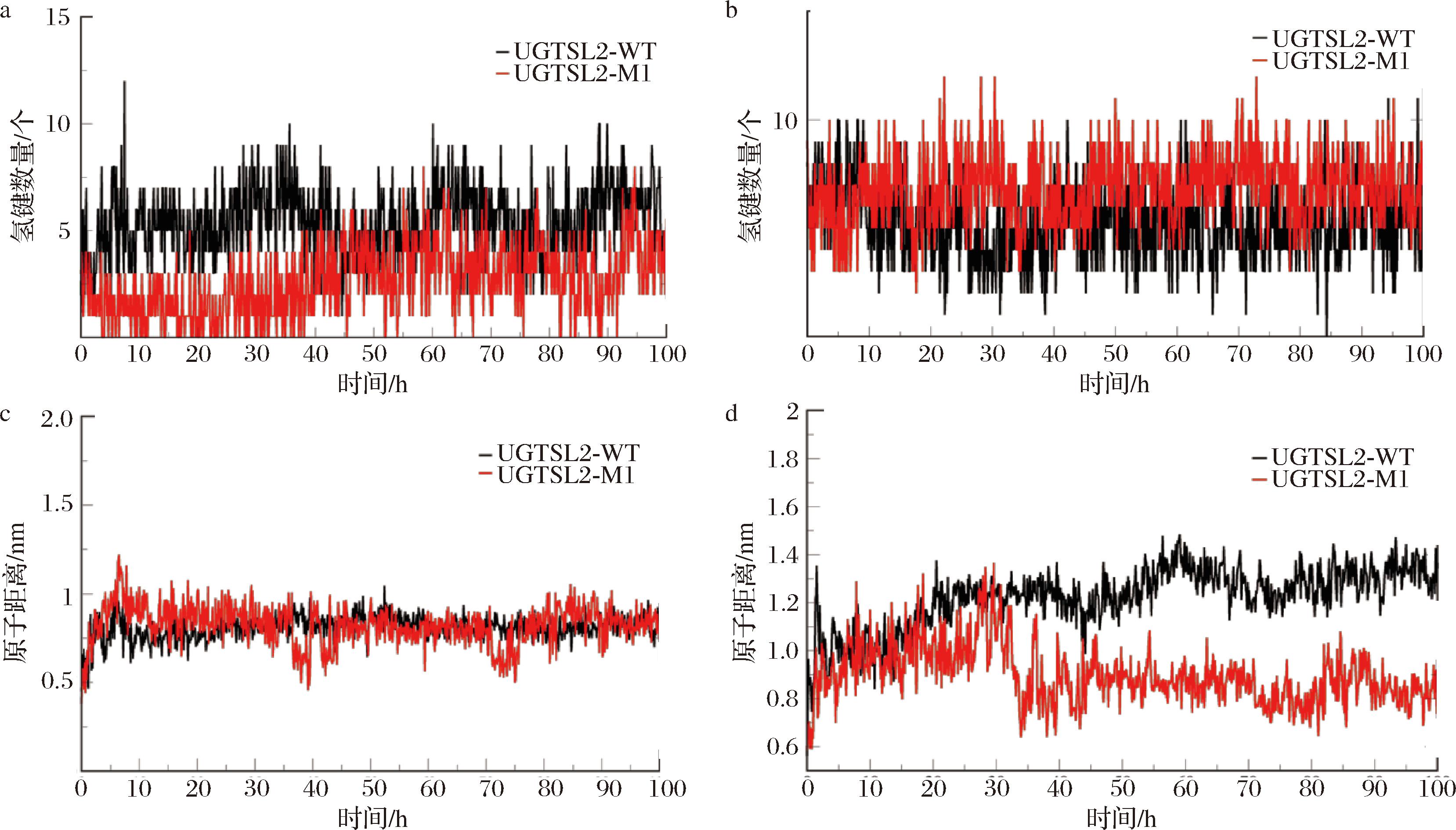
a-UGTSL2与Reb A的氢键数量;b-UGTSL2与UDPG的氢键数量;c-UGTSL2与Reb A的关键原子距离;d-UDPG与Reb A的关键原子距离
图7 模拟期间UGTSL2与底物的氢键数量和关键原子距离
Fig.7 Number of hydrogen bonds and key atomic distances between UGTSL2 and the substrate during the simulation
接下来分析了糖基转移酶UGTSL2突变对蛋白和配体之间相互作用的影响。发现UGTSL2-M1与Reb A之间形成的氢键数量减少(图7-a)。前面的研究发现Reb A在活性中心的稳定性降低,表明突变导致蛋白与配体之间氢键相互作用的减弱,进而无法有效稳定Reb A结合在活性中心。相反,UGTSL2-M1和UDPG之间的氢键作用增强,使UDPG更稳固的定位于活性位点(图7-b)。这种增强的氢键作用在某种程度上补偿了Reb A结合稳定性的下降,从而维持了酶的催化活性。图7-c和图7-d显示,突变后催化残基和Reb A关键原子之间的距离没有明显变化,Reb A与UDPG之间距离明显降低。该突变在活性位点对不同配体的影响反映了底物识别或催化机制中的细微调控作用,这为进一步优化糖基转移酶提供了线索。
最后分析了糖基转移酶PgUGT和配体之间的相互作用。发现突变后PgUGT和Reb A之间的氢键数量增加,氢键作用力增强(附图8-a)。PgUGT和UDPG之间的氢键作用变化不明显(附图8-b)。附图8-c显示,突变后d(H27-NE2--O8-Reb A)值增大,这意味着增强的氢键作用力不利于蛋白精准的和底物Reb A反应。然而Reb A和UDPG之间的关键原子之间距离减小,突变使UDPG的葡萄糖基更容易与Reb A结合生成Reb D。以上结果表明,尽管糖基转移酶与底物之间的氢键数量表现出不同的变化,Reb A和UDPG之间的距离均有所减小,表明在这些突变体中,底物间的相对位置更为紧密,这有利于增强两者之间的协同作用,并促进糖基转移反应的顺利进行。
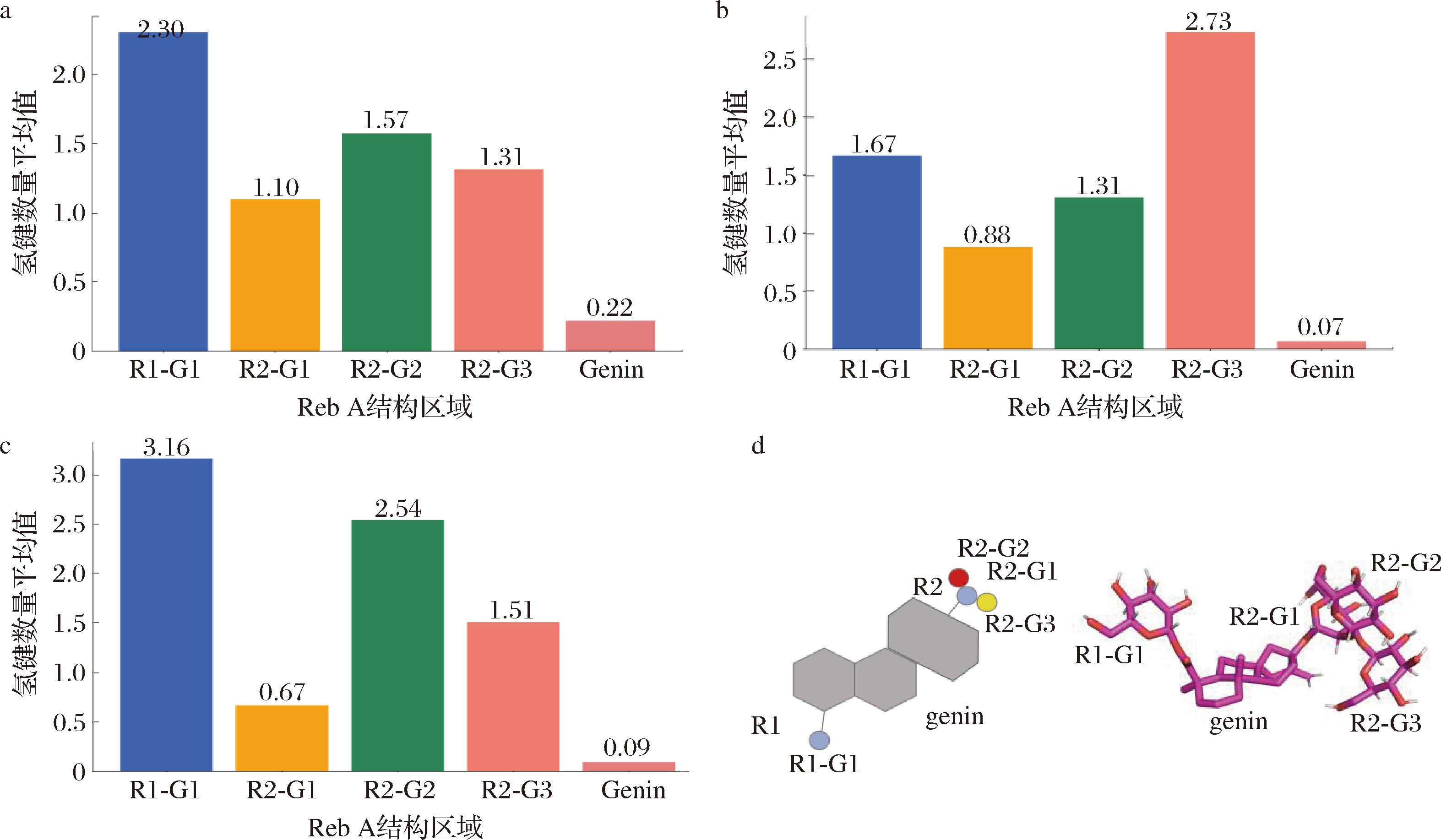
a-YojK-WT与Reb A不同部位之间氢键的平均值;b-YojK-M2与Reb A不同部位之间氢键的平均值;c-YojK-M5与Reb A不同部位之间氢键的平均值;d-Reb A结构示意图
图8 模拟期间YojK与Reb A不同部位之间氢键的平均值
Fig.8 Average number of hydrogen bonds between YojK and different regions of Reb A during the simulation
2.2.5 结合能分析
为评估糖基转移酶与底物Reb A的结合能力,利用g_mmpbsa计算了各酶与底物的结合自由能(表3)。结果显示,YojK-M2的结合能降低至(-245.54±21.38) kJ/mol,优于野生型(-221.01±28.40) kJ/mol,主要由于范德华作用增强。YojK-M5结合能变化不大。整体看,疏水作用是YojK结合的主要驱动力。EUGT11-M1突变后结合能为(-214.61±20.33) kJ/mol,较野生型弱,主要由于范德华能降低所致,静电能差异不大,突变减弱了疏水相互作用,导致结合稳定性下降。UGTSL2-M1同样显示出较弱的范德华和静电能,导致结合能减弱。在PgUGT-M8中,范德华作用力减弱,静电能增强,但结合能升高至(-202.78±23.75) kJ/mol,表明虽然静电相互作用增强,疏水作用减弱仍主导了结合稳定性降低。分析发现以上糖基转移酶与Reb A的结合主要由疏水相互作用驱动,尤其是范德华能贡献显著,非极性作用在结合中也起关键作用。尽管静电能在不同酶中差异较大,但也对结合稳定性具有一定调节作用。
表3 不同模拟体系中Reb A与糖基转移酶的结合能
Table 3 Binding energies between Reb A and glycosyltransferases in different simulation systems
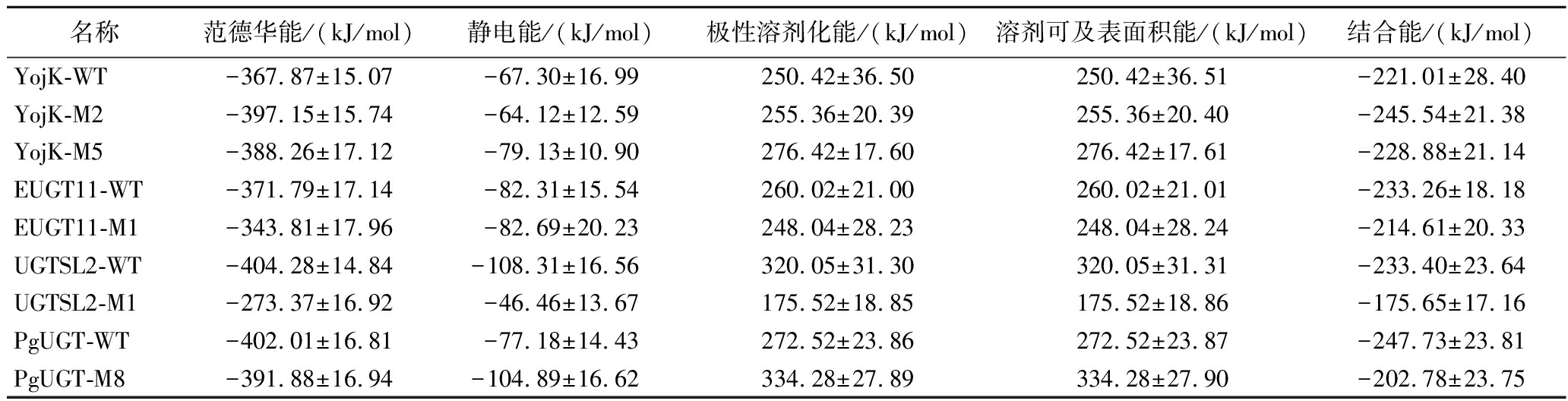
名称范德华能/(kJ/mol)静电能/(kJ/mol)极性溶剂化能/(kJ/mol)溶剂可及表面积能/(kJ/mol)结合能/(kJ/mol)YojK-WT-367.87±15.07-67.30±16.99250.42±36.50250.42±36.51-221.01±28.40YojK-M2-397.15±15.74-64.12±12.59255.36±20.39255.36±20.40-245.54±21.38YojK-M5-388.26±17.12-79.13±10.90276.42±17.60276.42±17.61-228.88±21.14EUGT11-WT-371.79±17.14-82.31±15.54260.02±21.00260.02±21.01-233.26±18.18EUGT11-M1-343.81±17.96-82.69±20.23248.04±28.23248.04±28.24-214.61±20.33UGTSL2-WT-404.28±14.84-108.31±16.56320.05±31.30320.05±31.31-233.40±23.64UGTSL2-M1-273.37±16.92-46.46±13.67175.52±18.85175.52±18.86-175.65±17.16PgUGT-WT-402.01±16.81-77.18±14.43272.52±23.86272.52±23.87-247.73±23.81PgUGT-M8-391.88±16.94-104.89±16.62334.28±27.89334.28±27.90-202.78±23.75
2.3 动态氢键网络分析
Reb A中不同位置的葡糖糖基与酶活性位点之间的氢键作用形成了一个氢键网络,这一网络在催化过程中不断变化,优化底物的结合亲和力和稳定性。为了深入理解各个糖基区域对催化反应的不同影响,将底物Reb A的葡糖糖基按照位置和糖苷键的不同划分为R1-G1、R2-G1、R2-G2、R2-G3(图8-d),并分别分析苷元和不同葡萄糖基与糖基转移酶的氢键作用动态变化。
对糖基转移酶YojK与Reb A之间的氢键平均值(图8-a~图8-c)和氢键数量变化(附图9)进行了统计分析。结果显示,在野生型和突变体中,葡萄糖基与糖基转移酶之间的氢键相互作用强于苷元部分,说明两端糖基通过氢键维持构象。突变体YojK-M2和YojK-M5在R2-G1处氢键虽减少但稳定性增强,且YojK-M2在R2-G3处氢键数量增加。此外,YojK-M5在R1-G1和R2-G2处的氢键数量增加。总体而言,YojK-M2与R1-G1、R2-G1氢键作用减弱,和R2-G3的氢键作用增强;YojK-M5与R1-G1、R2-G2、R2-G3氢键作用增强,R2-G1稳定性提高。
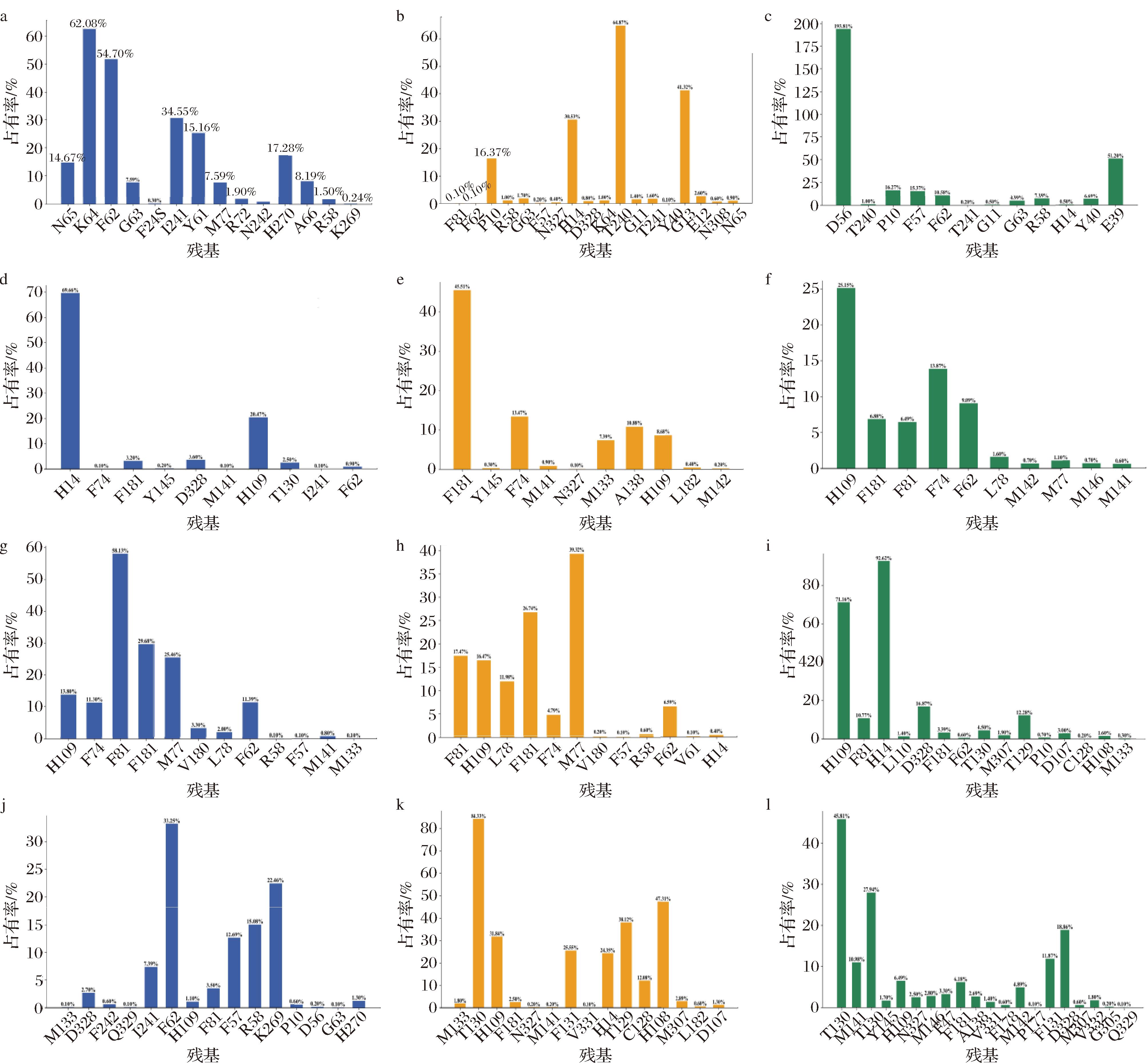
a-YojK-WT与R1-G1;b-YojK-M2与R1-G1;c-YojK-M5与R1-G1;d-YojK-WT与R2-G1;e-YojK-M2与R2-G1;f-YojK-M5与R2-G1;g-YojK-WT与R2-G2;h-YojK-M2与R2-G2;i-YojK-M5与R2-G2;j-YojK-WT与R2-G3;k-YojK-M2与R2-G3;i-YojK-M5与R2-G3
图9 模拟期间YojK野生型与突变体与Reb A不同部位形成氢键的氨基酸
Fig.9 Amino acids forming hydrogen bonds with different regions of Reb A by YojK wild type and mutants during the simulation
对与Reb A形成氢键的氨基酸残基分析表明,突变改变了氢键作用的关键残基。图9-a~图9-c显示,R1-G1糖基在YojK-WT中主要与K64、F62、I241、Y61形成氢键,而YojK-M2主要与H14、T240、G13作用,YojK-M5则与D56、E39形成氢键,突变增强了R1-G1与催化残基H14及T240的相互作用。R2-G1糖基的氢键作用较弱,YojK-WT中主要与H14形成氢键,突变后增强,YojK-M2主要与F181、F74作用,YojK-M5则与F74、H109作用,说明F74在2个突变体中都起重要作用(图9-d~图9-f)。R2-G2(图9-g~图9-i)和R2-G3(图9-j~图9-l)的关键残基变化明显,H14在YojK-M2中与R2-G3形成氢键,在YojK-M5中则与R2-G2频繁相互作用。总的来说,无论是野生型还是突变体,葡萄糖基部分与糖基转移酶之间的氢键作用明显强于苷元部分。在突变体中,YojK-M2和YojK-M5的不同糖基部分氢键作用发生了显著变化。
进一步分析其他糖基转移酶的氢键变化规律。对EUGT11氢键网络分析(附图10~附图12)显示,突变后R1-G1端氢键作用增强,关键残基由F379转变为与A379、D381、Q382形成更稳定网络。R2-G1与F130、F208保持稳定,R2-G2和R2-G3氢键模式呈现更分散的相互作用。UGTSL2分析(附图13~附图15)表明,两端糖基氢键强于中间糖苷。M1突变增强R1-G1氢键稳定性,减弱R2端氢键,关键氢键残基由R151、F148转向D359,整体优化了底物与活性位点匹配。PgUGT分析(附图16~附图18)显示,糖苷部分氢键较弱且不稳定,突变后氢键进一步减弱,两端糖基R1-G1、R2-G2、R2-G3氢键增强。氨基酸层面分析显示,突变显著改变了氢键残基及占比:R1-G1由N118等转为与D359、L82结合,R2-G1新增K157残基作用,R2-G2与N178、D177形成更强氢键。PgUGT-M8突变减弱了糖苷中部的结合力,增强了两端糖基的氢键网络,提升了其催化Reb A转化为Reb D的能力。综上,突变通过重构糖基与蛋白之间的氢键网络,尤其是增强R1端结合能力并优化R2端氢键分布,提升了底物与酶的构象适配性,从而增强催化效率。
通过前面的结合能分析可知,糖基转移酶主要通过疏水相互作用与底物Reb A结合,通过调节与底物糖基部分的氢键作用,从而影响产物的生成。由此推断,在糖基转移酶催化过程中,苷元与酶的非极性相互作用是主要的结合驱动力,起到“锚定”底物的作用,使得糖基正确地定位于酶的活性中心,而糖基部分的不稳定氢键相互作用则改变了糖基的位置,进而生成不同的糖苷键。
3 结论与讨论
随着催化Reb A生成Reb D的糖基转移酶被陆续鉴定,利用甜叶菊中含量高的Reb A通过酶催化制备Reb D已经成为一种可行的方案。部分糖基转移酶的理性改造经过分析,揭示了突变体催化效率提升的潜在原因。例如,EUGT11的F379A突变被发现改善了糖受体的结合能力,从而提高了该酶的催化活性[25]。然而,该研究的模拟时间较短,分析较为片面。UGTSL2的通道分析发现N358F突变通过微调酶的通道和空腔,有助于更好地结合底物,但该研究仅分析了UDPG的结合,忽视了Reb A的结合[5]。综上,已有研究未能全面阐述糖基转移酶催化性能提升的机制。
相比之下,本研究结合生物信息学分析与分子模拟方法,对相关糖基转移酶进行了系统而深入的机制探讨。首先分析了催化合成Reb D的糖基转移酶的序列结构特征。序列比对发现,氨基酸残基G13、H14、P17等高度保守,保守位点主要分布于C端Rossmann结构域,其中D102、G211、G239、P280、P290、H304、G306和P319位于柔性较大的loop区。结构分析发现,活性中心结构保守性高于蛋白整体结构,且活性中心中疏水环状氨基酸在催化功能中具有关键作用。理化性质分析表明,多数酶在中性至碱性环境下带负电,利于与正电底物作用,芳香性和疏水性差异影响其底物选择性与结合能力。
进一步通过对多种酶突变体进行分子动力学模拟,系统探讨催化性能提升机制。结果表明,虽然突变对蛋白整体结构稳定性、底物稳定性及氢键数量的影响有差异,但在所有突变体中,Reb A与UDPG关键原子的距离均减小,表明催化效率的提升更依赖于底物的构象适配性而非整体结构稳定性。PCA发现,YojK、EUGT11突变体蛋白构象灵活性增加,PgUGT、UGTSL2突变体构象稳定性提升,突变通过改变构象空间分布进而影响了其催化功能和底物适应性。结合能和动态氢键网络进一步分析表明,酶与Reb A的结合主要由非极性作用主导,突变优化了糖基端的作用力,重塑了与蛋白之间的氢键网络。基于上述发现,本研究提出了底物结合模式:苷元部分通过稳定的疏水相互作用主导结合,而糖基部分则通过氢键相互作用辅助调节活性位点关键原子的位置。本研究系统性地揭示了突变对糖基转移酶结构灵活性、稳定性以及底物适应性的影响,为糖基转移酶的工程改造及优化提供了理论依据。
[1] MORISSETTE A, DE WOUTERS D’OPLINTER A, ANDRE D M, et al.Rebaudioside D decreases adiposity and hepatic lipid accumulation in a mouse model of obesity[J].Scientific Reports, 2024, 14(1):3077.
[2] SONG F W, WANG S D, MAO Y H, et al.Enhancing rebaudioside M synthesis via introducing sulfur-mediated interactions between glycosyltransferase UGT76G1 and rebaudioside D[J].Journal of Agricultural and Food Chemistry, 2025, 73(1):667-677.
[3] GUO B D, HOU X D, ZHANG Y, et al.Highly efficient production of rebaudioside D enabled by structure-guided engineering of bacterial glycosyltransferase YojK[J].Frontiers in Bioengineering and Biotechnology, 2022, 10:985826.
[4] ZHANG S S, YANG Y S, LYU C C, et al.Identification of the key residues of the uridine diphosphate glycosyltransferase 91D2 and its effect on the accumulation of steviol glycosides in Stevia rebaudiana[J].Journal of Agricultural and Food Chemistry, 2021, 69(6):1852-1863.
[5] CHEN L L, CAI R X, WENG J Y, et al.Production of rebaudioside D from stevioside using a UGTSL2 Asn358Phe mutant in a multi-enzyme system[J].Microbial Biotechnology, 2020, 13(4):974-983.
[6] MA S Y, MA Y Y.A sustainable strategy for biosynthesis of Rebaudioside D using a novel glycosyltransferase of Solanum tuberosum[J].Biotechnology Journal, 2024, 19(2):e2300628.
[7] CHEN M Q, SONG F W, QIN Y X, et al.Improving thermostability and catalytic activity of glycosyltransferase from Panax ginseng by semi-rational design for rebaudioside D synthesis[J].Frontiers in Bioengineering and Biotechnology, 2022, 10:884898.
[8] TALEVI A.Computer-aided drug discovery and design:Recent advances and future prospects[J].Methods in Molecular Biology 2024, 2714:1-20.
[9] YAGI H, TAKAGI K, KATO K.Exploring domain architectures of human glycosyltransferases:Highlighting the functional diversity of non-catalytic add-on domains[J].Biochimica et Biophysica Acta-General Subjects, 2024, 1868(10):130687.
[10] XIA H, ZHANG Z H, DING J, et al.A glycosyltransferase from Arabidopsis thaliana enables the efficient enzymatic synthesis of gastrodin[J].Catalysis Letters, 2024, 154(4):1558-1566.
[11] YANG M L, YANG S, DENG Z W, et al.Improving the thermostability of glycosyltransferase UGT76G1 by computer-aided target analysis for highly efficient biosynthesis of rebaudioside M[J].Food Bioscience, 2023, 56:103119.
[12] SARAIVA A, CARRASCOSA C, RAMOS F, et al.Agave syrup:Chemical analysis and nutritional profile, applications in the food industry and health impacts[J].International Journal of Environmental Research and Public Health, 2022, 19(12):7022.
[13] CHEN Y X, XIE Y N, AJUWON K M, et al.Xylo-oligosaccharides, preparation and application to human and animal health:A review[J].Frontiers in Nutrition, 2021, 8:731930.
[14] SIDDIQUI H, SAMI F, HAYAT S.Glucose:Sweet or bitter effects in plants-a review on current and future perspective[J].Carbohydrate Research, 2020, 487:107884.
[15] FORLI S, HUEY R, PIQUE M E, et al.Computational protein-ligand docking and virtual drug screening with the AutoDock suite[J].Nature Protocols, 2016, 11(5):905-919.
[16] ASSAREH E, MEHRNEJAD F, ASGHARI S M.Structural studies on an anti-angiogenic peptide using molecular modeling[J].Iranian Journal of Biotechnology, 2020, 18(4):e2553.
[17] HUANG W, LIN Z X, VAN GUNSTEREN W F.Validation of the GROMOS 54A7 force field with respect to β-peptide folding[J].Journal of Chemical Theory and Computation, 2011, 7(5):1237-1243.
[18] SARGSYAN K, GRAUFFEL C, LIM C.How molecular size impacts RMSD applications in molecular dynamics simulations[J].Journal of Chemical Theory and Computation, 2017, 13(4):1518-1524.
[19] CHOI J M, VUPPALA S, PARK M J, et al.Computer simulation approach to the identification of visfatin-derived angiogenic peptides[J].PLoS One, 2023, 18(6):e0287577.
[20] WANG B, KENNEDY M A.Principal components analysis of protein sequence clusters[J].Journal of Structural and Functional Genomics, 2014, 15(1):1-11.
[21] AHARONOVSKY E, TRIFONOV E N.Protein sequence modules[J].Journal of Biomolecular Structure and Dynamics, 2005, 23(3):237-242.
[22] CAMPITELLI P, MODI T, KUMAR S, et al.The role of conformational dynamics and allostery in modulating protein evolution[J].Annual Review of Biophysics, 2020, 49:267-288.
[23] KARNATI K R, WANG Y X.Structural and binding insights into HIV-1 protease and P2-ligand interactions through molecular dynamics simulations, binding free energy and principal component analysis[J].Journal of Molecular Graphics and Modelling, 2019, 92:112-122.
[24] MAGUIRE J B, BOYKEN S E, BAKER D, et al.Rapid sampling of hydrogen bond networks for computational protein design[J].Journal of Chemical Theory and Computation, 2018, 14(5):2751-2760.
[25] LIN M, WANG F, ZHU Y S.Modeled structure-based computational redesign of a glycosyltransferase for the synthesis of rebaudioside D from rebaudioside A[J].Biochemical Engineering Journal, 2020, 159:107626.