果胶是一类存在于植物细胞壁中的复杂多糖,主要由α-1,4-连接的D-半乳糖醛酸单元组成,广泛存在于水果、蔬菜等植物组织中[1]。作为一种重要的天然生物高分子,果胶具有良好的生物相容性、可降解性和优异的凝胶特性,在食品工业中被广泛应用于果酱制备、果汁澄清、乳制品稳定等领域[2]。此外,果胶还具有降低胆固醇、促进消化和预防结肠癌等多种生理活性,在功能性食品和药物载体系统中也有潜在应用价值[3]。然而,天然果胶自身的抗氧化和抑菌活性相对有限,这在一定程度上限制了其在功能性材料和健康产品领域的应用潜力。
多糖的分子修饰与功能化改性已成为提升其性能和拓展应用范围的重要策略。其中,将具有特定功能的小分子接枝到多糖骨架上,是赋予多糖新功能的有效途径[4]。没食子酸,又被称为棓酸,作为一种天然酚酸类化合物,广泛存在于茶叶、葡萄、石榴等植物中,因其分子结构中含有3个邻位酚羟基,表现出优异的抗氧化、抑菌和抗炎活性[5-6]。将没食子酸接枝到果胶分子上,有望赋予果胶增强的生物活性,创造出具有多功能特性的新型生物材料。
传统的多糖分子修饰通常需要使用有机溶剂和化学试剂,不仅产生环境污染问题,还可能导致产物的安全性隐患。例如,现有文献报道的脂肪酶催化没食子酸-果胶酯化反应需要在四氢呋喃等有机溶剂中进行[4-5],限制了其在食品领域的实际应用。相比之下,酶催化反应具有专一性强、反应条件温和、环境友好等显著优势[7]。漆酶作为一种含铜氧化还原酶,能在温和条件下催化酚类化合物的氧化,生成活性自由基中间体,这些自由基可与多糖上的官能团发生偶联反应[8]。因此,漆酶催化接枝为果胶功能化改性提供了一种绿色、高效的新途径[9]。
本研究采用漆酶催化接枝法制备了具有增强抗氧化和抑菌活性的没食子酸-果胶共聚物。通过多种光谱技术确认产物结构并评价其生物活性,为果胶功能化改性提供新思路,所得产物在食品防腐、功能包装和生物医药领域具有潜在应用价值。
1 材料与方法
1.1 材料与试剂
果胶(半乳糖醛酸值>72%,酯化度56.7%)、没食子酸,上海阿拉丁试剂公司(中国);漆酶(来源于白腐真菌,活性≥12 U/mg),源叶生物科技有限公司;ABTS、DPPH、β-胡萝卜素、Trolox,上海麦克林生化科技有限公司;抗菌活性测试所用的大肠杆菌(ATCC 25922)、金黄色葡萄球菌(ATCC 6538)菌株,中国微生物菌种保藏中心;肉汤培养基,北京陆桥技术有限公司;其他试剂均为分析纯。
1.2 仪器与设备
MultiSkan Go全波长酶标仪、NICOLET IS 10傅里叶变换红外光谱(Fourier transform infrared spectroscopy, FTIR)仪,美国赛默飞世尔有限责任公司;BRUKER 400M核磁共振波谱仪,德国布鲁克有限责任公司。
1.3 实验方法
1.3.1 没食子酸-果胶共聚物的制备
称取5.0 g果胶(标记为Na-Pe)溶于100 mL磷酸盐缓冲液(0.1 mol/L,pH 6.5)中,室温搅拌4 h至完全溶解。将没食子酸(2.55 g或5.10 g)溶于20 mL无水乙醇中,缓慢滴加到果胶溶液中并持续搅拌30 min。随后,加入50 mg漆酶(预先溶于5 mL磷酸盐缓冲液中),在40 ℃条件下搅拌反应8 h。反应结束后,将反应液加热至80 ℃保持10 min以灭活酶,冷却至室温。向反应液中加入3倍体积的无水乙醇沉淀产物,4 ℃静置过夜。通过离心(8 000 r/min,10 min)收集沉淀,并用70%(体积分数)乙醇溶液洗涤3次以去除未反应的没食子酸。所得产物经冷冻干燥46 h后,得到没食子酸-果胶共聚物(分别标记为Ga1-Pe和Ga2-Pe),于干燥器中避光保存备用。
1.3.2 结构表征
紫外-可见光谱(ultraviolet-visible spectroscopy, UV-Vis)分析:将样品溶于磷酸盐缓冲液(0.1 mol/L,pH 6.5)配制成1 mg/mL的溶液。使用紫外-可见分光光度计在200~400 nm范围内进行扫描,扫描间隔为1 nm,以缓冲液为空白对照。通过没食子酸标准曲线(线性范围0.01~0.1 mg/mL,相关系数R2=0.999 6)计算接枝度,如公式(1)所示:
接枝率![]()
(1)
式中:C1,改性果胶中没食子酸浓度,mg/L;C2,果胶浓度,mg/L。
1.3.3 姜黄素-果胶共聚物的结构表征
核磁共振光谱(nuclear magnetic resonance spectroscopy,1HNMR)分析:将样品(20 mg)溶于0.7 mL重水(D2O)中,室温下溶解24 h后,使用400 MHz核磁共振波谱仪进行测定,以四甲基硅烷为内标。
FTIR分析:将干燥样品与溴化钾按1∶50的质量比混合研磨,压片后使用傅里叶变换红外光谱仪在4 000~400 cm-1范围内进行扫描,分辨率为8 cm-1,扫描次数32次。
1.3.4 抗氧化活性评价
ABTS阳离子自由基清除能力测定[10-11]:将7 mmol/L ABTS与2.45 mmol/L过硫酸钾等体积混合,避光反应16 h生成ABTS溶液。使用磷酸盐缓冲液将ABTS溶液稀释至734 nm处吸光度为0.70±0.02。将0.1 mL样品溶液(1 mg/mL)与3.9 mL稀释后的ABTS溶液混合,避光反应6 min后,于734 nm处测定吸光度。以Trolox为标准品建立标准曲线,结果表示为清除率(%)。
DPPH自由基清除能力测定[10-11]:将0.1 mL样品溶液(1 mg/mL)与3.9 mL DPPH乙醇溶液(0.1 mmol/L)混合,避光反应30 min后,于517 nm处测定吸光度。以Trolox为标准品建立标准曲线,结果表示为清除率(%)。
β-胡萝卜素漂白抑制率测定[11]:将2 mg β-胡萝卜素溶于10 mL氯仿中,取1 mL该溶液与20 μL亚油酸和200 mg吐温80混合。使用旋转蒸发仪在40 ℃下除去氯仿,加入50 mL去离子水重新分散制成β-胡萝卜素-亚油酸乳液。取4.8 mL该乳液与0.2 mL样品溶液(1 mg/mL)混合,50 ℃水浴中保温,每15 min于470 nm处测定吸光度,共120 min。抑制率的计算如公式(2)所示:
β-胡萝卜素漂白抑制率![]()
(2)
式中:![]() 和
和![]() 分别表示空白样在加热前后的吸光度,
分别表示空白样在加热前后的吸光度,![]() 和
和![]() 分别表示花色苷样品在加热前后的吸光度。
分别表示花色苷样品在加热前后的吸光度。
还原力测定[11]:将1 mL样品溶液(1 mg/mL)与1 mL磷酸盐缓冲液(0.2 mol/L,pH 6.6)和1 mL铁氰化钾溶液(10 g/L)混合,50 ℃水浴中反应20 min。加入1 mL三氯乙酸溶液(100 g/L)终止反应,离心(3 000 r/min,10 min)。取2 mL上清液与2 mL去离子水和0.4 mL氯化铁溶液(1 g/L)混合,于700 nm处测定吸光度。以抗坏血酸为标准品建立标准曲线,结果表示为还原能力(%)。
1.3.5 抑菌活性评价
采用微量稀释法测定样品对大肠杆菌(革兰氏阴性菌)和金黄色葡萄球菌(革兰氏阳性菌)的抑菌活性[12]。将待测菌株于37 ℃营养肉汤中培养16 h至对数生长期,稀释至约1×106 CFU/mL。在96孔板中,每孔加入100 μL菌液和100 μL不同浓度的样品溶液(0.5~8.0 mg/mL),37 ℃培养24 h。使用酶标仪于600 nm处测定吸光度,计算抑菌率。抑菌率的计算如公式(3)所示:
抑菌率![]()
(3)
式中:A1,加入样品组的吸光度,A0,阴性对照组(仅含菌液和磷酸盐缓冲液)的吸光度。
1.4 数据处理
所有实验均重复3次,结果以“平均值±标准差”表示。使用SPSS 23.0软件进行单因素方差分析(ANOVA)和Duncan多重比较,P<0.05表示差异具有统计学显著性。
2 结果与分析
2.1 UV-Vis分析
图1展示了天然果胶(Na-Pe)与不同接枝程度的没食子酸改性果胶(Ga1-Pe和Ga2-Pe)的UV-Vis吸收光谱及接枝度。由图1-a可见,天然果胶在240~400 nm范围内未出现特征吸收峰,而改性果胶Ga1-Pe和Ga2-Pe则在272 nm附近表现出明显的吸收峰。这一峰归因于没食子酸芳香环的π→π*电子跃迁,证实了没食子酸成功接枝于果胶分子结构中[13-14]。
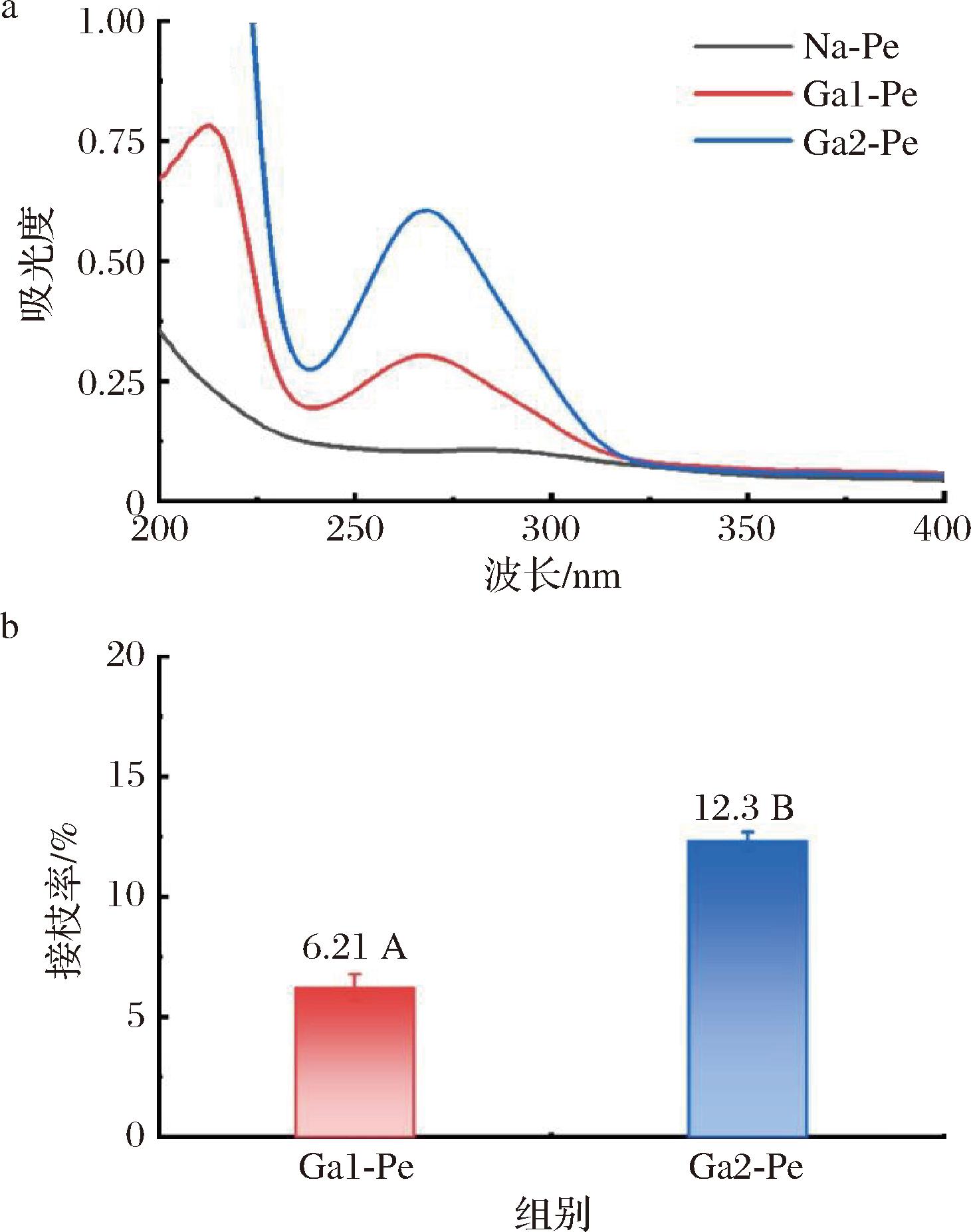
a-UV-Vis光谱图;b-接枝率
图1 天然果胶和改性果胶的UV-Vis光谱图和接枝率
Fig.1 UV-Vis spectra and grafting ratio of native and modified pectin
注:不同字母表示差异显著(P<0.05)(下同)。
进一步依据272 nm处的吸收峰,通过分光光度法测得没食子酸接枝率。Ga1-Pe和Ga2-Pe分别为6.21%和12.3%,表明随没食子酸添加量的提高,接枝率显著提升。这可能是由于没食子酸浓度增加,有利于生成更多的酚氧自由基,促进与果胶分子上的偶联反应。综上,UV-Vis分析结果验证了没食子酸成功接枝到果胶分子,并表明增加没食子酸添加量可显著提升接枝效率。
2.2 1HNMR分析
图2展示了天然果胶(Na-Pe)与不同接枝度没食子酸改性果胶(Ga1-Pe、Ga2-Pe)的1HNMR。天然果胶的特征氢信号主要分布在5.20~1.17 ppm区间,其中4.98、3.72、3.91、4.37、4.87、3.60 ppm处的峰分别对应半乳糖醛酸甲酯分子C1~C5、C7位上的氢原子。
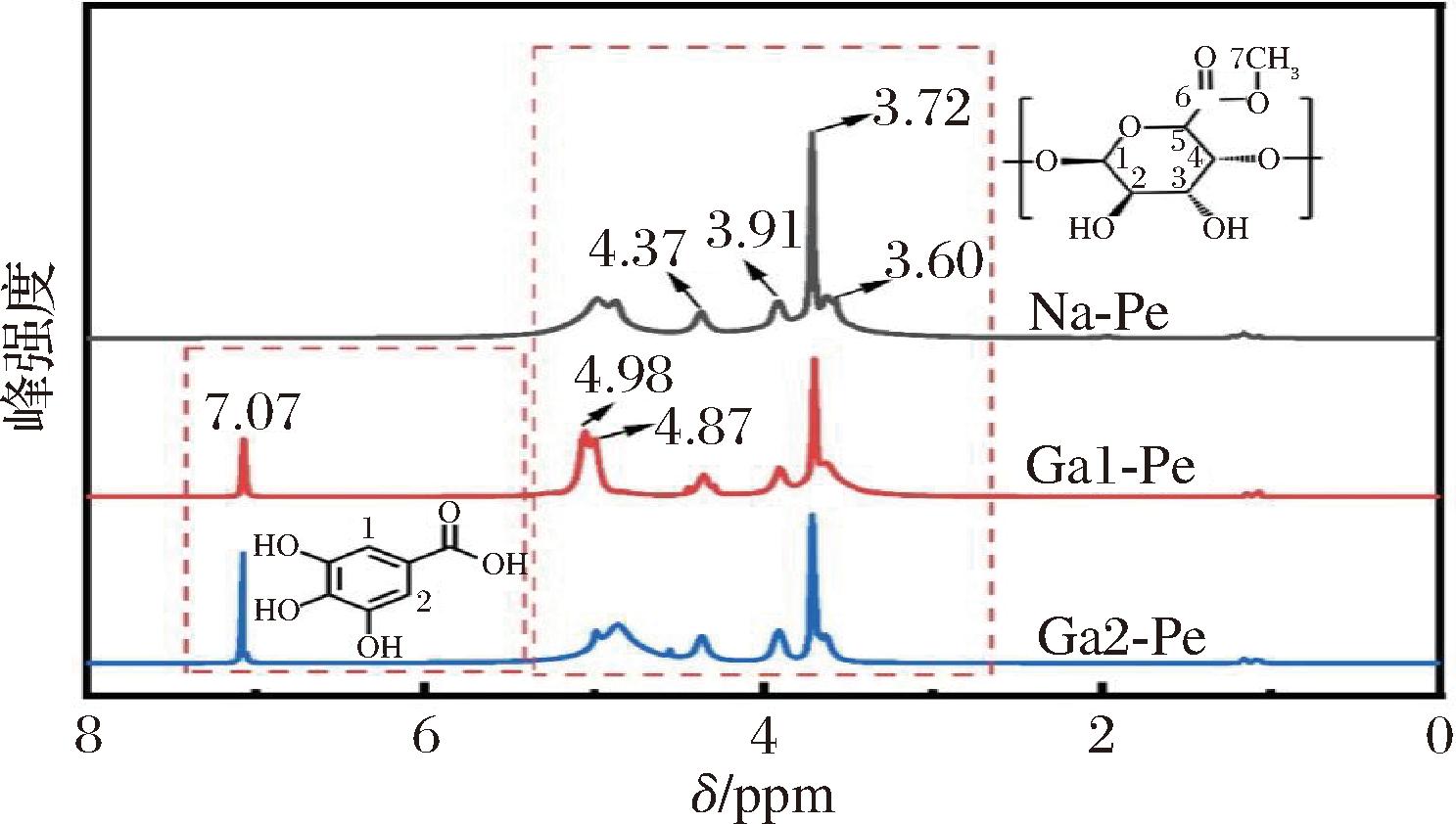
图2 天然果胶和改性果胶的1HNMR光谱图
Fig.2 1HNMR spectra of native and modified pectin
与天然果胶相比,改性果胶在7.07 ppm处出现了明显的新特征峰,且随着接枝度增加(Ga1-Pe到Ga2-Pe),该峰的强度显著增强。这一特征峰归属于没食子酸分子芳香环上对称结构的2个氢原子[15-16],进一步证实了没食子酸成功接枝到果胶分子骨架上,并且峰强度与接枝程度呈正相关关系,与UV-Vis分析结果相互印证。
2.3 FTIR分析
图3展示了天然果胶与没食子酸改性果胶的FTIR。如图3-a所示,所有样品在3 391 cm-1处均呈现宽而强的吸收峰,归属于果胶及没食子酸分子中丰富羟基的伸缩振动及其形成的氢键;在2 939 cm-1处的吸收峰则对应—CH3和—CH2基团的伸缩振动。图3-b的局部放大图显示,天然果胶在1 749 cm-1和1 644 cm-1处的特征峰分别对应果胶分子中—COOC—和—COOH的伸缩振动。而改性果胶样品在1 693 cm-1处出现了新的吸收峰,这可能源于果胶分子上的羧基与没食子酸分子上的羟基发生的酯化反应[17]。此外,改性果胶在1 537 cm-1处出现的新特征峰可归因于没食子酸分子中苯环的骨架振动[18-19]。
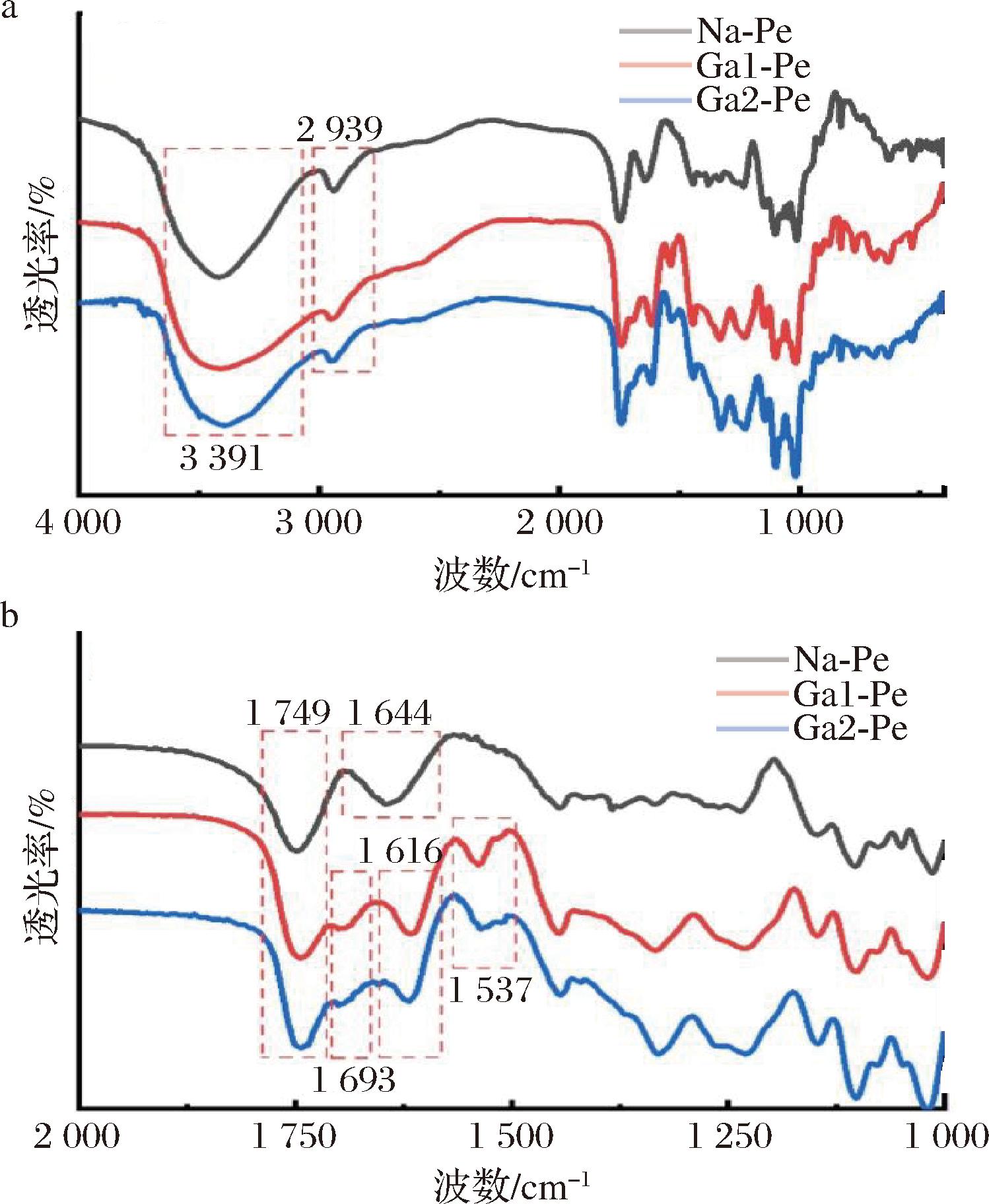
a-全谱扫描(4 000~400 cm-1);b-局部放大图(2 000~1 000 cm-1)
图3 天然果胶和改性果胶的FTIR光谱图
Fig.3 FTIR spectra of native and modified pectin
上述结果进一步证实,在漆酶催化条件下,没食子酸通过酯化反应成功接枝到果胶分子链上,形成了结构稳定的改性产物。
2.4 抗氧化活性分析
图4展示了天然果胶与没食子酸改性果胶的抗氧化活性评价结果,采用了ABTS阳离子自由基和DPPH自由基清除能力、β-胡萝卜素漂白抑制率及还原力4种互补测定方法进行综合评价。结果表明,在ABTS阳离子自由基清除能力测定中,Na-Pe仅表现出3.4%的清除率,而Ga2-Pe达到了76.3%;在DPPH自由基清除能力测定中,Na-Pe和Ga2-Pe分别为4.2%和68.8%,显示出显著差异。类似地,β-胡萝卜素漂白抑制率测定中,Ga2-Pe(85.6%)比Na-Pe(13.8%)高出约6倍;还原力测定也呈现相似趋势。
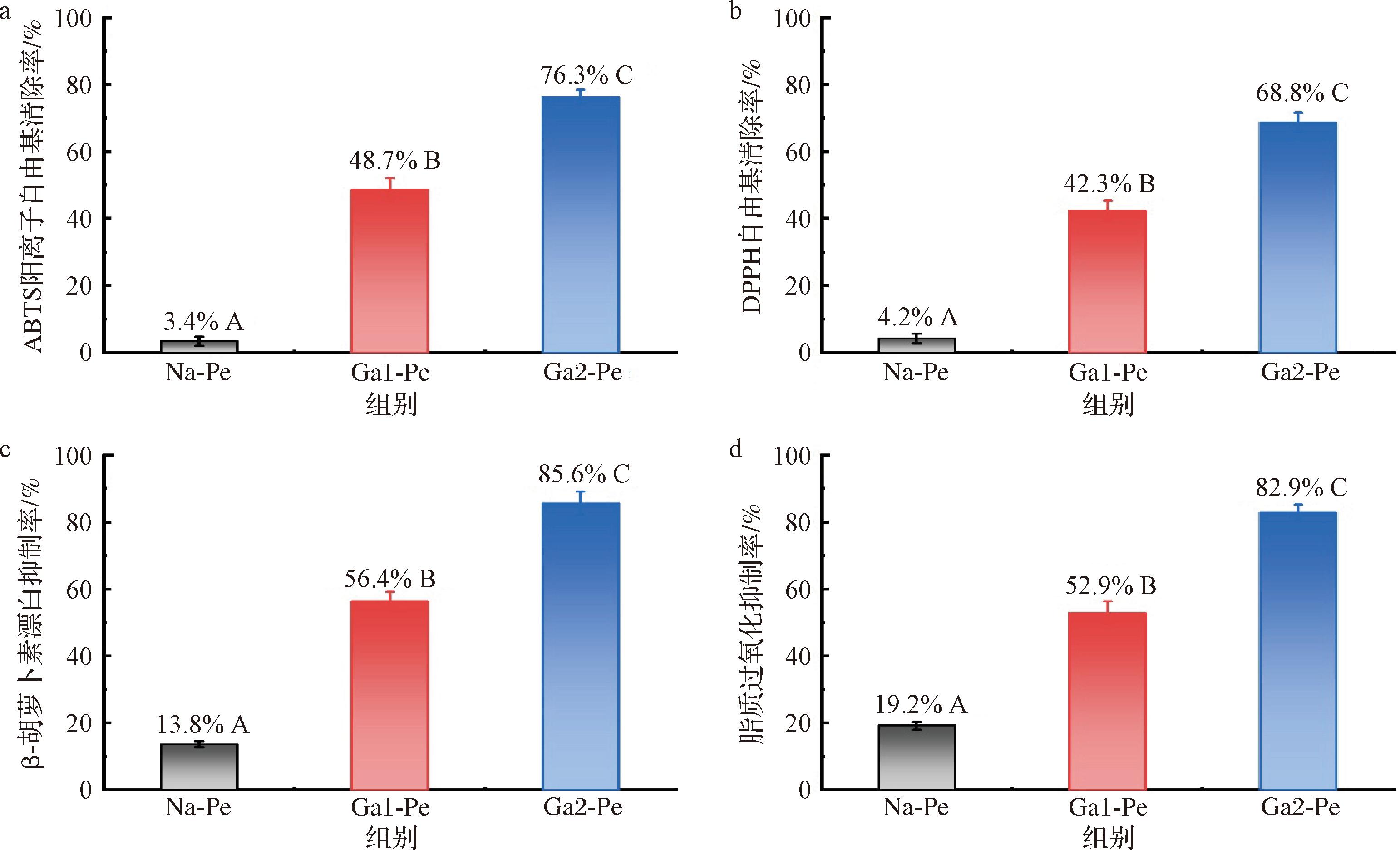
a-ABTS阳离子自由基清除能力;b-DPPH自由基清除能力;c-β-胡萝卜素漂白抑制率;d-脂质过氧化抑制率
图4 天然果胶和改性果胶的抗氧化活性
Fig.4 Antioxidant activities of native and modified pectin
抗氧化活性的增强与接枝度呈正相关关系,这主要归因于接枝的没食子酸分子中含有的邻三羟基结构。该结构具有强大的电子供体能力,可通过单电子转移机制有效捕获自由基,形成相对稳定的半醌式结构[20-21]。这些结果证实,通过漆酶催化接枝没食子酸可以有效改善果胶的抗氧化活性,为开发功能性果胶衍生物提供了可行途径。
2.5 抑菌活性分析
图5展示了天然果胶与改性果胶对大肠杆菌和金黄色葡萄球菌的抑菌活性。如图5所示,天然果胶对2种测试菌株几乎不具备抑菌活性,抑菌率均低于5%。而没食子酸接枝后的果胶表现出显著增强的抑菌能力,且抑菌效果与接枝度呈正相关关系。对大肠杆菌(图5-a),Ga1-Pe和Ga2-Pe在相同测试浓度下的抑菌率分别达到37%~67%和58%~84%;对金黄色葡萄球菌(图5-b),抑菌率分别达到48%~78%和62%~92%。结果表明,接枝度较高的Ga2-Pe对2种病原菌均表现出优异的抑菌活性,且对革兰氏阳性菌(金黄色葡萄球菌)的抑制效果略优于革兰氏阴性菌(大肠杆菌)。
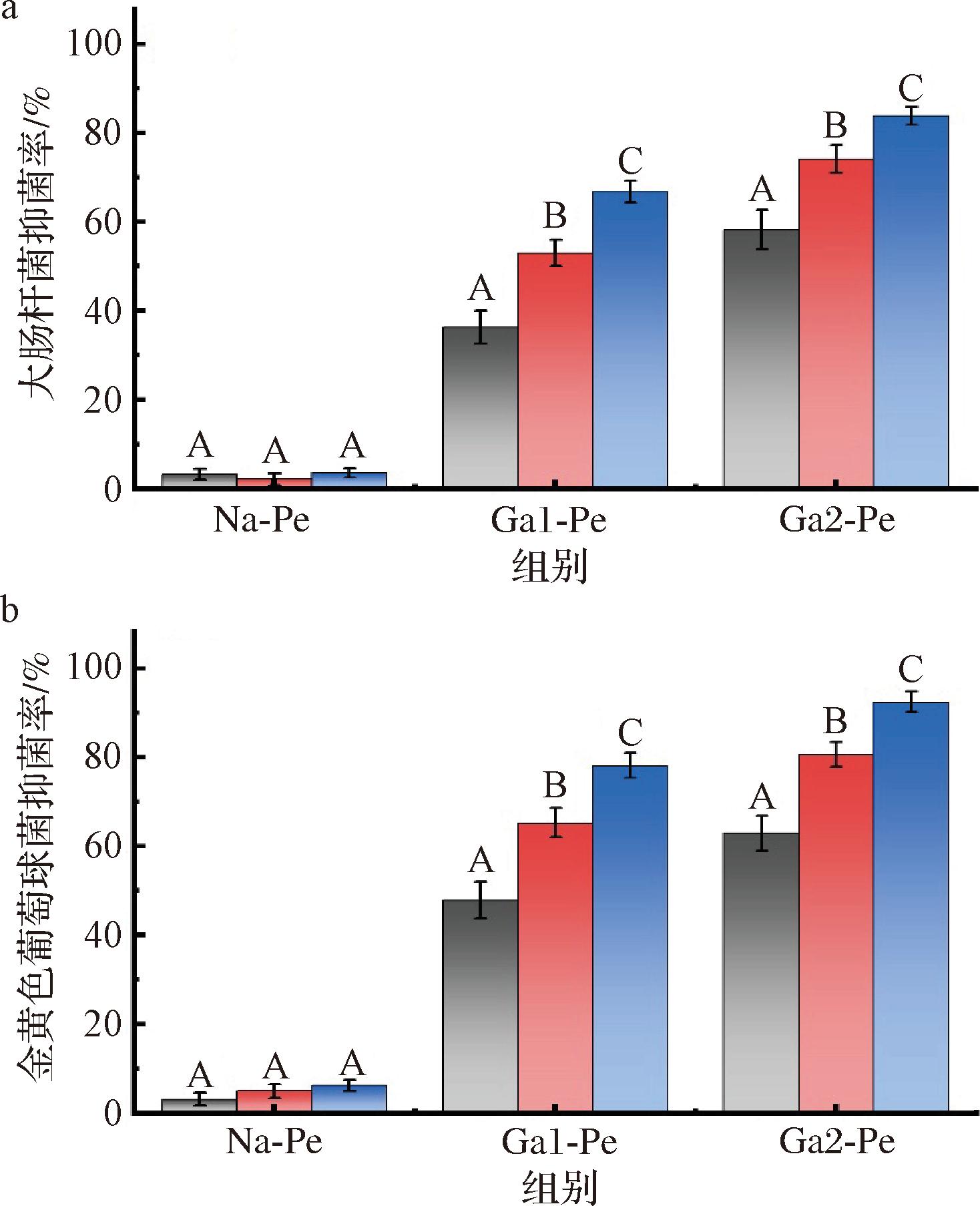
a-大肠杆菌;b-金黄色葡萄球菌
图5 天然果胶和改性果胶的抑菌活性
Fig.5 Antibacterial activities of native and modified pectin against Escherichia coli and Staphylococcus aureus
没食子酸接枝果胶的抑菌机制可能包括以下几方面:一方面,没食子酸分子中的酚羟基可与细菌细胞壁和细胞膜上的蛋白质结合,破坏其结构完整性,导致细胞内容物泄漏[22-23];另一方面,没食子酸可能通过螯合细菌生长所必需的金属离子,干扰细菌正常代谢[24-25]。此外,接枝后果胶分子的空间结构变化也可能有助于增强其与细菌细胞表面的相互作用。对革兰氏阴性菌和阳性菌的差异抑制效果可能与两类细菌细胞壁结构的差异有关。革兰氏阴性菌外膜的存在可能部分阻碍了改性果胶与细胞的接触,从而降低了抑菌效率。
这些结果进一步证实了没食子酸-果胶共聚物作为潜在天然防腐剂的应用价值,特别是在开发功能性食品包装材料和生物医用材料方面具有广阔前景。
3 结论
本研究成功开发了一种以漆酶为催化剂将没食子酸接枝到果胶分子上的生物催化方法,通过UV-Vis光谱、1HNMR和FTIR分析证实了接枝反应的成功进行及产物结构。结果表明,没食子酸-果胶共聚物表现出显著增强的生物活性,与天然果胶相比,改性产物在ABTS阳离子自由基、DPPH自由基清除、β-胡萝卜素漂白抑制及还原力等多种抗氧化评价体系中均展现出优异性能,同时对革兰氏阳性菌和阴性菌均表现出良好抑制效果(抑菌率达60%~90%)。这些功能特性与接枝度呈正相关关系,且理论上可改善果胶的凝胶强度和热稳定性等理化特性,为产品性能优化提供了理论依据。从产业化角度分析,该方法原料来源丰富,工艺条件温和,无需有机溶剂,适合工业化放大,虽然成本略高于传统化学防腐剂,但其天然属性和抗氧化、抑菌双重功能使其在功能性食品包装材料和天然防腐剂等领域具有较高市场价值和广阔应用前景。
[1] ZHENG C M, ZHANG Z G, DING N S, et al.Synthesis of amidated pectin with amino acid using ultra-low temperature enzymatic method and its evaluation of fat mimic characteristics[J].Food Hydrocolloids, 2022, 125:107454.
[2] ZHANG W L, CAO J K, JIANG W B.Effect of different cation in situ cross-linking on the properties of pectin-thymol active film[J].Food Hydrocolloids, 2022, 128:107594.
[3] 卢泳强, 周朝曦, 张丽丽, 等.苹果果胶的理化特性、抗氧化及降血脂作用研究[J].食品与发酵工业, 2024, 50(7):61-68.LU Y Q, ZHOU Z X, ZHANG L L, et al.Physicochemical properties, antioxidant, and hypolipidemic effects of pectin from Malus pumila[J].Food and Fermentation Industries, 2024, 50(7):61-68.
[4] HUANG B Q, ZHANG Z G, DING N S, et al.Investigation of the pectin grafting with gallic acid and propyl gallate and their antioxidant activities, antibacterial activities and fresh keeping performance[J].International Journal of Biological Macromolecules, 2021, 190:343-350.
[5] 张泽宏, 郭苏童, 李奕雅, 等.没食子酸-果胶共聚物的酶法制备:溶剂效应及功能特性研究[J].食品与发酵工业,2024, 50(17):156-161.ZHANG Z H, GUO S T, LI Y Y, et al.Enzymatic synthesis of gallic acid-pectin conjugates:Solvent effects and functional properties[J].Food and Fermentation Industries, 2024, 50(17):156-161.
[6] FU L L, XIAO Q, RU Y, et al.Bio-based active packaging:Gallic acid modified agarose coatings in grass carp (Ctenopharyngodon idellus) preservation[J].International Journal of Biological Macromolecules, 2024, 255:128196.
[7] LIU N, NI S Z, GAO H L, et al.Laccase-catalyzed grafting of lauryl gallate on chitosan to improve its antioxidant and hydrophobic properties[J].Biomacromolecules, 2021, 22(11):4501-4509.
[8] LIN H, YU Z J, WANG Q, et al.Application of laccase catalysis in bond formation and breakage:A review[J].Catalysts, 2023, 13(4):750.
[9] YANG X D, WANG K, ZHONG Y A, et al.Synthesis, characterization and application of sugar beet pectin-ferulic acid conjugates in the study of lipid, DNA and protein oxidation[J].International Journal of Biological Macromolecules, 2025, 307:141358.
[10] FARRAG A F S, OTIFY A M, KHEDR A I M, et al.Unveiling metabolome heterogeneity in seed and husk from three cardamom species for quality control and valorization purposes of its waste products via NMR-based metabolomics in relation to in vitro biological effects[J].Food Chemistry, 2025, 480:143687.
[11] PIRES C, MARTINS N, CARVALHO A M, et al.Phytopharmacologic preparations as predictors of plant bioactivity:A particular approach to Echinacea purpurea (L.) Moench antioxidant properties[J].Nutrition, 2016, 32(7-8):834-839.
[12] ROMANESCU M, OPREAN C, LOMBREA A, et al.Current state of knowledge regarding WHO high priority pathogens:Resistance mechanisms and proposed solutions through candidates such as essential oils:A systematic review[J].International Journal of Molecular Sciences, 2023, 24(11):9727.
[13] KHAINSKAYA K, HILEUSKAYA K, NIKALAICHUK V, et al.Chitosan-gallic acid conjugate with enhanced functional properties and synergistic wound healing effect[J].Carbohydrate Research, 2025, 553:109496.
[14] HUWAIMEL B, ALQARNI S.DFT and QTAIM insights into Al- and Zn-doped C20 fullerenes for H2S sensing:Asthma biomarker and environmental pollutant[J].Chinese Journal of Physics, 2025, 96:1453-1469.
[15] SOBEH M, EL-RAEY M, REZQ S, et al.Chemical profiling of secondary metabolites of Eugenia uniflora and their antioxidant, anti-inflammatory, pain killing and anti-diabetic activities:A comprehensive approach[J].Journal of Ethnopharmacology, 2019, 240:111939.
[16] MUCCILLI V, CARDULLO N, SPATAFORA C, et al.α-Glucosidase inhibition and antioxidant activity of an oenological commercial tannin.Extraction, fractionation and analysis by HPLC/ESI-MS/MS and 1H NMR[J].Food Chemistry, 2017, 215:50-60.
[17] LIU J N, WANG T L, HUANG B Q, et al.Pectin modified with phenolic acids:Evaluation of their emulsification properties, antioxidation activities, and antibacterial activities[J].International Journal of Biological Macromolecules, 2021, 174:485-493.
[18] LU H S, LI Q F, LIU W F, et al.Enhanced solar interfacial evaporation through lignin-polyaniline composite coatings on Balsa wood substrates[J].International Journal of Biological Macromolecules, 2024, 281:136382.
[19] YANG C, GE C Z, LI X L, et al.Does soluble starch improve the removal of Cr(VI) by nZVI loaded on biochar?[J].Ecotoxicology and Environmental Safety, 2021, 208:111552.
[20] HALDER A, DAS S, OJHA D, et al.Highly monodispersed gold nanoparticles synthesis and inhibition of herpes simplex virus infections[J].Materials Science and Engineering:C, 2018, 89:413-421.
[21] KHAN M R, VOLPE S, SALUCCI E, et al.Active caseinate/guar gum films incorporated with gallic acid:Physicochemical properties and release kinetics[J].Journal of Food Engineering, 2022, 335:111190.
[22] CUI L, ZHAO J, WANG Y R, et al.Multifunctional polyvinyl alcohol/gallic acid functionalized chitosan hydrogels prepared by freeze-thaw method for potential application as wound dressings[J].Reactive and Functional Polymers, 2024, 197:105866.
[23] AHMED A S, MOODLEY N, ELOFF J N.Bioactive compounds from the leaf extract of Bauhinia galpinii (Fabaceae) used as antidiarrhoeal therapy in southern Africa[J].South African Journal of Botany, 2019, 126:345-353.
[24] FAN X T, GURTLER J B, MATTHEIS J P.Possible sources of Listeria monocytogenes contamination of fresh-cut apples and antimicrobial interventions during antibrowning treatments:A review[J].Journal of Food Protection, 2023, 86(6):100100.
[25] DUBE E.Antibacterial activity of engineered nanoparticles against fish pathogens[J].Aquaculture Reports, 2024, 37:102240.