神经退行性疾病是一类以中枢神经系统进行性损伤为特征的慢性疾病,主要包括阿尔茨海默病、帕金森病及额颞叶痴呆等[1-2]。这类疾病不仅严重影响患者的生活质量,也给家庭和社会带来沉重的医疗与经济负担[3],已成为全球公共卫生与生物医学研究领域亟待解决的重大挑战。已有研究表明,活性氧(reactive oxygen species, ROS)是细胞内重要的信号分子[4],然而其过度积累会引发氧化应激(oxidative stress, OS),进而对细胞结构和功能造成广泛损伤[5]。在大脑中,持续的OS可激活炎症通路和诱导神经元凋亡,从而促进多种神经退行性疾病的发生与发展[6]。因此,研发具有神经保护功能的抗氧化活性物质,已成为防治神经退行性疾病的重要策略之一。
蛹虫草(Cordyceps militaris)作为一种营养丰富且具有药用潜力的食药用真菌,因其多样的生物活性受到广泛关注[7]。其富含多种功能成分,如多糖、蛋白质、虫草素、腺苷和麦角甾醇等[8],在免疫调节、抗炎、抗氧化、降血脂及降血糖等方面表现出显著活性[9]。近年来,蛹虫草蛋白质及其酶解产物的抗氧化潜力逐渐成为研究热点。例如,宗静[10]通过酶解与分离纯化技术,从蛹虫草子实体中获得了具有显著抗氧化活性的多肽组分;陈梦霏等[11]则通过模拟胃肠消化处理蛹虫草蛋白质,发现其酶解产物的抗氧化能力显著高于原始蛋白质。这些研究提示,蛹虫草蛋白质可作为制备高活性抗氧化多肽的理想前体,并为开发具备神经保护作用的功能性食品提供了新思路。
基于上述背景,本研究以蛹虫草蛋白质为原料,采用模拟胃肠消化法制备其酶解产物,并利用谷氨酸(Glu)诱导的PC12细胞损伤模型评估该酶解液的神经保护效应。进一步通过分离纯化与结构鉴定,筛选潜在的活性多肽单体,初步探讨其生物活性及相关作用机制。本研究旨在为开发基于蛹虫草的功能性健康产品提供数据支持。
1 材料与方法
1.1 材料与试剂
蛹虫草购自福东海健康产业科技(广东)有限公司,粉碎后备用。
硫酸铵、胰酶和谷氨酸,Sigma-Aldrich(上海)贸易有限公司;胃蛋白酶,上海源叶生物技术有限公司;BCA蛋白浓度测定试剂盒,碧云天生物技术有限公司;PC12细胞(大鼠肾上腺嗜铬细胞瘤细胞株),中科院上海细胞库;DMEM(Dulbecco’s modified Eagle’s medium)细胞培养基、胎牛血清、双抗(青霉素-链霉素)溶液、0.05%(体积分数)胰酶、PBS,赛默飞世尔生物化学制品有限公司;CCK-8 试剂盒,上海翊圣生物科技有限公司;多肽单体由吉尔生化有限公司合成;浓硫酸、盐酸和氢氧化钠均为分析纯,国药集团化学试剂有限公司。
1.2 仪器与设备
90-1B恒温磁力搅拌器,上海司乐仪器有限公司;DK-S24电热恒温水浴锅,精宏仪器设备有限公司;LyoQuest-85Plus真空冷冻干燥机,TELSTAR公司;160i 细胞培养箱,美国赛默飞世尔科技公司;K9860全自动凯氏定氮仪,山东海能科技仪器有限公司;CLARIOstar Plus酶标仪,BMG LABTECH公司。
1.3 实验方法
1.3.1 蛹虫草中蛋白质的测定和提取
参考GB 5009.5—2025《食品安全国家标准 食品中蛋白质的测定》测定蛹虫草中蛋白质含量。
根据WU等[12]方法采用水提-硫酸铵沉淀法提取蛹虫草蛋白质。将蛹虫草干粉配制成15 g/mL悬液,25 ℃下搅拌3 h,随后8 500×g离心15 min获得上清液。上清液加入硫酸铵至75%(质量分数)饱和度进行沉淀(15 h),离心(8 500×g,15 min)后收集沉淀。沉淀复溶,并通过透析袋透析24 h。透析液经过冷冻干燥后获得蛋白质,于-80 ℃保存待用。
1.3.2 蛹虫草蛋白质酶解液的制备
参考先前研究成果采用模拟胃肠消化(胃蛋白酶-胰酶)方法制备酶解液[9]。配制10 mg/mL的蛋白质溶液,按4%(质量分数)加酶量,使用胃蛋白酶(37 ℃,pH值至2.00±0.02)模拟胃消化2 h,沸水浴灭酶10 min。再按4%加酶量,使用胰酶(37 ℃,pH值至7.00±0.02)模拟肠道消化2 h,沸水浴灭酶10 min。离心(7 000×g,15 min),收集上清液。将上清液过0.22 μm滤膜后,得到蛹虫草蛋白质酶解液。
1.3.3 蛹虫草蛋白质酶解液的细胞毒性和生物活性
参照王曙光[13]建立的Glu诱导神经损伤PC12细胞模型,并稍作修改,用以评估蛹虫草蛋白质酶解液的细胞毒性和生物活性。
酶解液的细胞毒性:PC12细胞按1×104个/孔的密度于96孔板中贴壁生长24 h后,通过完全培养基配制不同浓度的酶解液(25、50、100 μg/mL),样品处理组每孔添加样品液100 μL,空白组则添加100 μL完全培养基。孵育12 h后。随后通过CCK-8试剂盒测定细胞存活率。
细胞存活率![]()
(1)
式中:A1,样品处理组OD值;A2,空白对照组的OD值。
酶解液的生物活性:PC12细胞按1×104个/孔的密度于96孔板中贴壁生长24 h,随后样品组每孔添加100 μL由完全DMEM培养基配制的不同浓度酶解液(25、50、100 μg/mL)孵育12 h,空白对照组则添加100 μL完全DMEM培养基。最后,除空白对照组外,其余各组使用20 mmol/L的Glu(每孔100 μL)损伤24 h。损伤后,CCK-8试剂盒测定细胞存活率,计算如公式(1)所示。实验中所有换液步骤均使用1×PBS清洗2遍。
1.3.4 不同分子质量蛹虫草蛋白质酶解液的生物活性
蛹虫草蛋白质酶解液(10 mg/mL)使用3 kDa和10 kDa的超滤离心管进行分离,得到<3 kDa、3~10 kDa和>10 kDa 3个分子质量的酶解液。将不同分子质量的酶解液按1.3.3节中确定的最适保护浓度配制后,通过Glu诱导损伤的PC12细胞模型,评估蛹虫草蛋白质及其不同分子质量酶解液的神经保护活性,并筛选出活性最优的组分。
1.3.5 蛹虫草蛋白质酶解液最优活性组分分析
将1.3.4节获得的活性最优组分通过UPLC-MS/MS进行分析。色谱柱使用德国麦克色谱柱(Acclaim PepMap100 C18,150 μm×150 mm,1.9 μm)。洗脱程序为梯度洗脱:0~5 min,6%~9% B;5~20 min,9%~14% B;20~50 min,14%~30% B;50~58 min,30%~40% B;58~60 min,40%~95% B。流动相A和B分别为超纯水[含0.1%(体积分数)甲酸和2%(体积分数)乙腈]和80%的乙腈(含0.1%甲酸)。电喷雾-组合型离子阱质谱仪结果通过限定蛹虫草物种进行数据库检索分析,获得多肽序列信息。
1.3.6 蛹虫草活性多肽的筛选
获得多肽序列信息后,在“Bioware”(http://bioware.ucd.ie/~compass/biowareweb/)平台上使用peptideRanker和CPPpred两个模块预测其生物活性和细胞穿透能力。将离子强度最高的30条多肽、生物活性得分最高的30条多肽,以及细胞穿透能力得分最高的30条多肽取交集,初步筛选可能具有生物活性的候选多肽。最终再选择其中分子质量最小的3条多肽进行下一步探究。
1.3.7 蛹虫草多肽单体的生物活性
采用Glu损伤的PC12细胞模型测定3条活性多肽的活性,并筛选出最好活性的多肽单体。
1.3.8 蛹虫草多肽单体的DPPH自由基清除能力
参照文献中DPPH测定方法略有修改,测定蛹虫草多肽单体的自由基清除能力[11]。将多肽单体依次配制成1、2、3、4 mg/mL的梯度浓度溶液。于96孔板中,分别取多肽溶液与0.225 mL的0.1 mmol/L DPPH溶液混合,充分振荡混匀后,于室温下避光静置反应30 min。随后在517 nm测定各孔吸光值,代入公式(2)计算DPPH自由基清除率。
清除率![]()
(2)
式中:B0为0.225 mL DPPH和0.225 mL超纯水混合反应的OD值;B1为待测样品与DPPH溶液混合反应的OD值。
1.3.9 蛹虫草多肽单体与Keap 1蛋白的分子对接
为探究蛹虫草多肽单体激活Keap1-Nrf2通路的潜力,采用分子对接分析蛹虫草多肽单体与Keap 1蛋白相互作用的结合模式。多肽单体的三维结构通过ChemBioDraw绘制并转化为空间3D结构;Keap1的晶体结构从Protein Data Bank (PDB ID:2FLU)获取。采用薛定谔软件包,首先对蛋白受体、多肽配体进行能量优化。随后,使用Grid模块执行分子对接分析[14]。
1.4 数据处理
所有实验平行测量3次,采用SPSS 软件进行单因素方差分析,结果为“平均值±标准差”,P<0.05为统计学上有显著性差异。使用Graphpad Prism 10.1.2进行绘图。
2 结果与分析
2.1 蛹虫草蛋白质酶解液的生物活性分析
测定结果显示,干基蛹虫草蛋白质含量为(22.83±1.34)%,表明其可作为优质的膳食蛋白质来源。天然蛋白质经摄入后,常在胃肠消化过程中被降解为多肽,其中不少多肽已经被报道具备多种功能活性[15-16]。同时,PC12细胞通过适当诱导可分化为神经样细胞,而过高浓度的细胞外Glu可诱导OS,导致神经元损伤。Glu损伤PC12细胞是被广泛用于神经元相关研究的重要细胞模型[12-13]。因此,本研究通过模拟胃肠消化法制备蛹虫草多肽,并评估其对PC12细胞的毒性及在Glu损伤模型中的神经保护作用。结果如图1所示,不同浓度酶解液处理均无明显细胞毒性(图1-a)。在Glu损伤PC12细胞模型中,模型组细胞存活率降至(41.05±1.73)%,而酶解液干预有效降低了Glu引起的细胞凋亡(图1-b)。其中,50 μg/mL和100 μg/mL酶解液的保护效果尤为显著,与模型组相比均具有统计学差异,细胞存活率分别提高至(59.62±1.54)%和(66.73±3.56)%。上述结果表明,蛹虫草蛋白质在模拟胃肠消化过程中可释放出具有改善神经元损伤的活性多肽组分。基于100 μg/mL酶解液表现出最佳保护效果,后续细胞实验中均选用该浓度作为上样浓度。
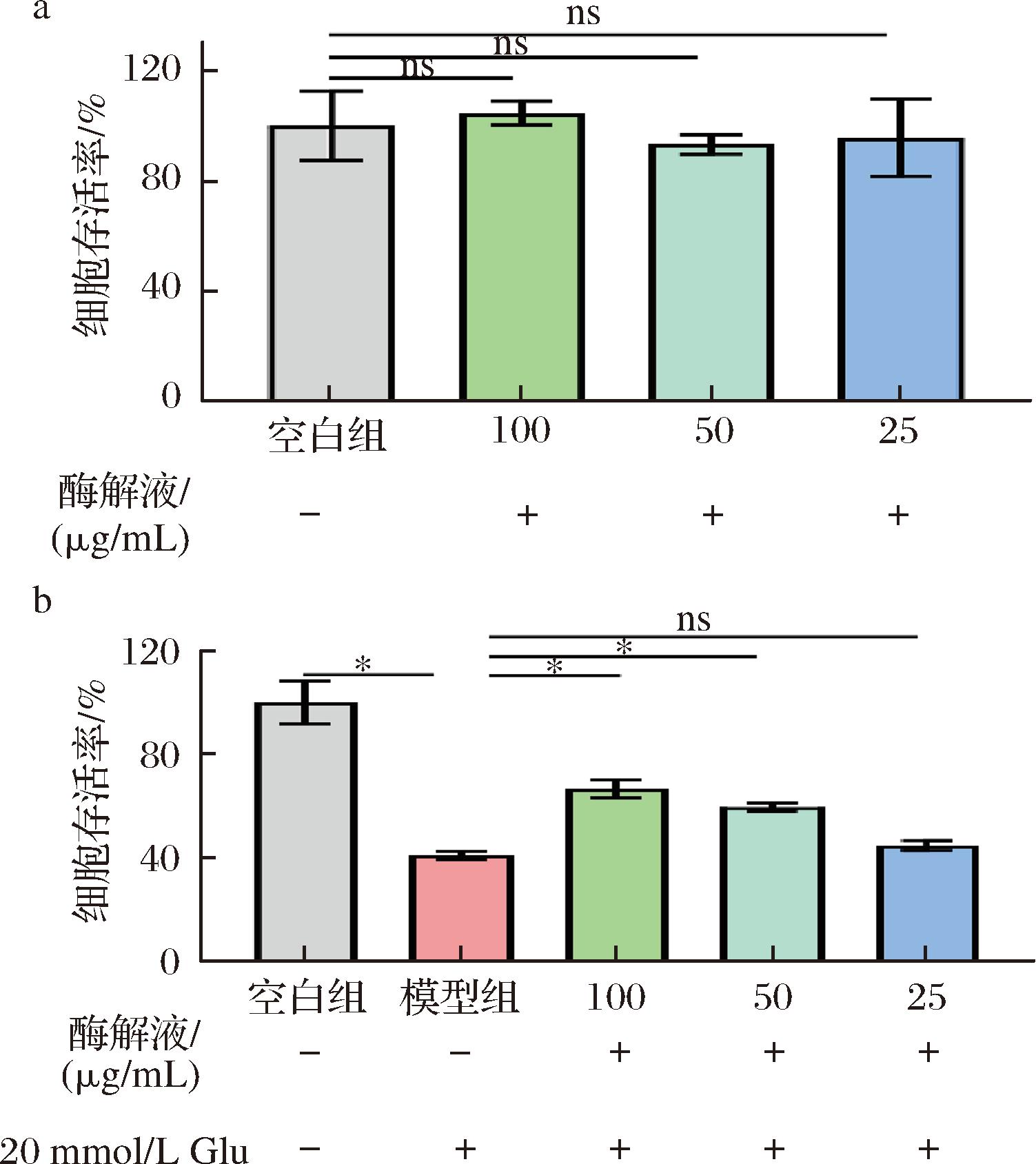
a-不同浓度酶解液处理PC12细胞存活率;b-不同浓度酶解液处理Glu损伤PC12细胞的细胞存活率
图1 蛹虫草蛋白质酶解液对Glu损伤PC12细胞的保护效果
Fig.1 Protective effect of hydrolysate obtained fromC.militaris protein on Glu-injured PC12 cell model
注:“+”表示添加该物质,“-”表示无;*,组间具有统计学差异
(P<0.05);ns,无显著性差异(P>0.05)(下同)。
2.2 不同分子质量酶解液的活性组分筛选
采用超滤法分离蛹虫草蛋白质酶解液,获得<3 kDa、3~10 kDa和>10 kDa 3个不同分子质量的酶解液。不同分子质量的酶解液和原始蛹虫草蛋白质对PC12细胞的毒性及保护效果如图2所示。结果显示,蛹虫草蛋白质、酶解液和不同分子质量酶解液均无明显细胞毒性(图2-a)。在Glu损伤PC12细胞模型中,模型组细胞存活率仅为(39.87±3.48)%,而酶解液和<3 kDa组分均对Glu损伤PC12细胞展现出保护效果,细胞存活率分别提高至为(48.84±2.49)%和(57.43±5.35)%(图2-b)。多项研究指出,膳食蛋白质酶解后所产生的多肽具有较母蛋白更高的生物活性[11]。例如,DAI等[17]与CHO[18]也均通过模拟胃肠消化获得了抗氧化活性显著提高的酶解液。此外,多项研究报道,来源于膳食蛋白的<3 kDa小分子质量蛋白酶解液具有较好抗炎抗氧化等生物活性[19-22],这类多肽不仅稳定性较高,也更容易进一步被吸收,从而有效地发挥其功能活性[23]。综上可知,模拟胃肠消化能够有效增强蛹虫草蛋白质的生物活性,并且<3 kDa组分可能是其发挥神经保护作用的关键活性组分。
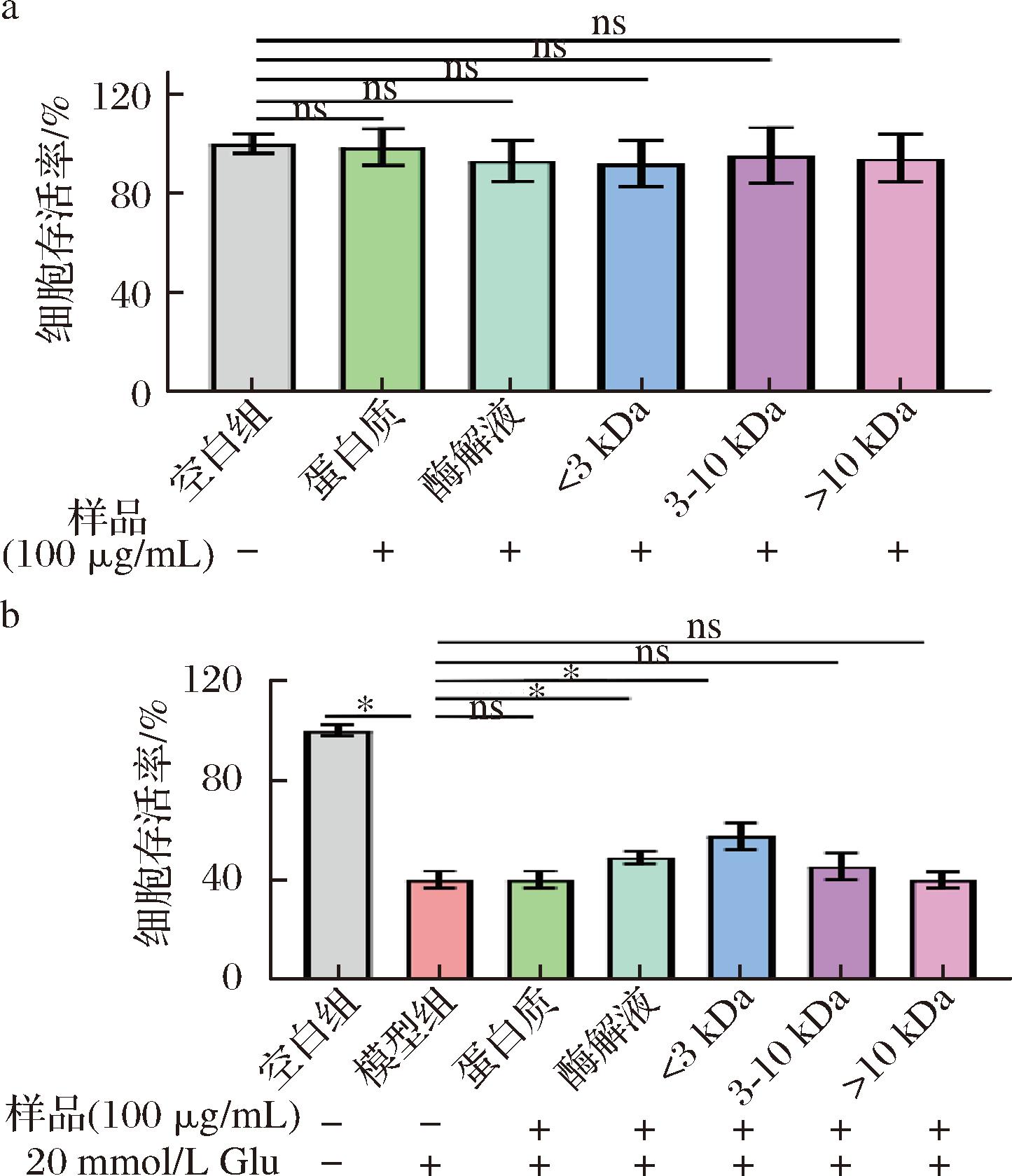
a-各组分对PC12细胞的细胞毒性;b-各组分处理Glu损伤PC12细胞的细胞存活率
图2 蛹虫草蛋白质和不同分子质量酶解液组分对Glu损伤PC12细胞的保护效果
Fig.2 Protective effect of C.militaris proteins and hydrolysate fractions with different molecular weights on Glu-injured PC12 cells
2.3 酶解液最优活性组分的多肽序列分析
酶解液的生物活性与其所含多肽的分子质量和序列特征密切联系[15,24]。为进一步探究活性最佳的<3 kDa组分,采用LC-MS/MS分析其多肽组成,共鉴定到2 288条多肽。其中,离子强度最高的76条多肽的相对含量占总量的50%以上(图3-a),提示这些多肽可能是该组分发挥功能活性的主要成分。进一步分析76条多肽的氨基酸组成,结果显示其肽链长度为3~25个氨基酸,其中约85%为3~15个氨基酸组成的小分子多肽(图3-b),可知,蛹虫草蛋白质经模拟胃肠消化产生的酶解液中,这些小分子多肽是其具有生物活性的重要结构基础。
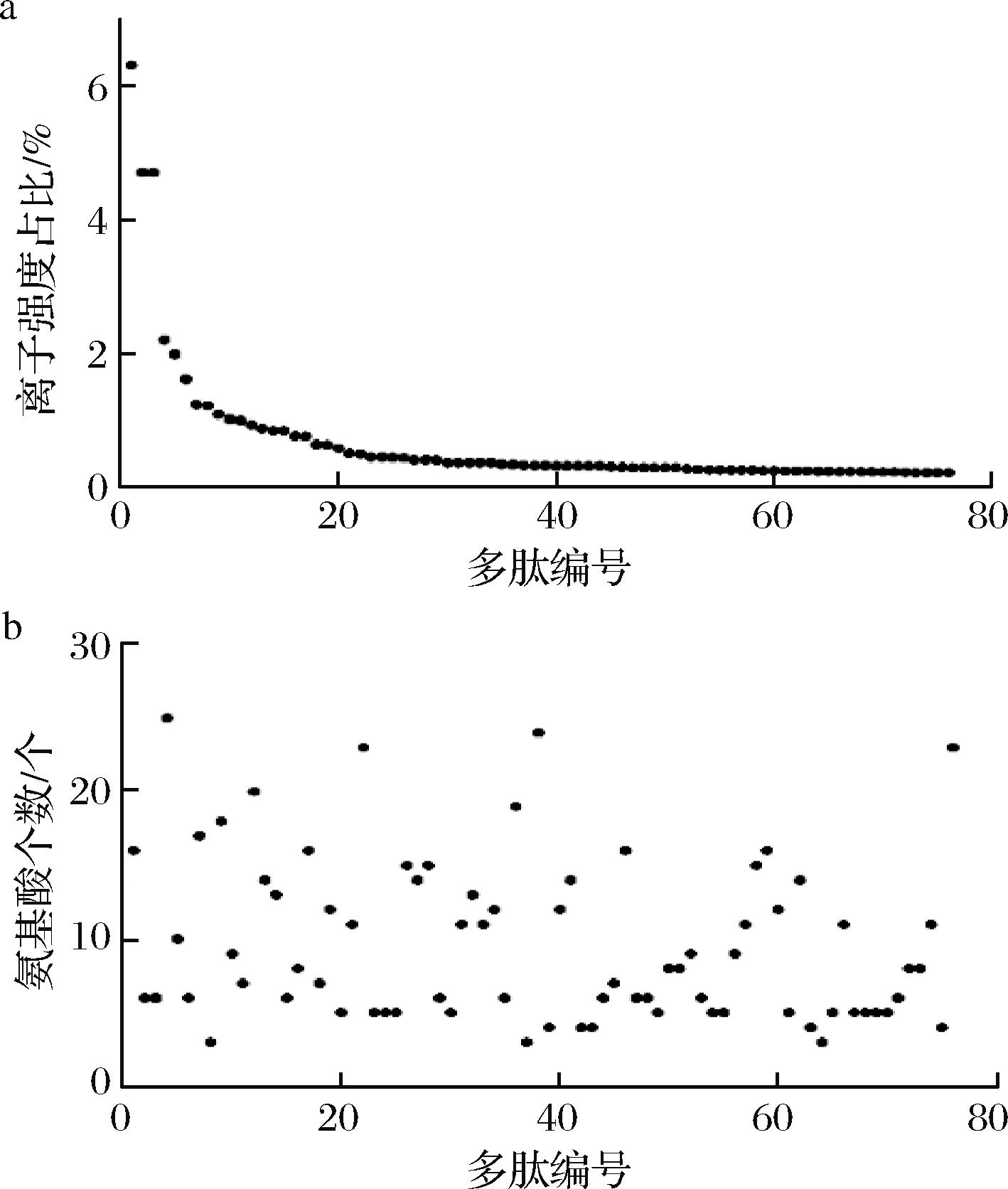
a-<3 kDa组分中离子强度最高的76条多肽;b-76条肽的氨基酸个数分布
图3 <3 kDa组分的多肽组成分析
Fig.3 Analysis of peptides in <3 kDa fractions
许多研究表明了蛋白酶解液和多肽的生物活性可能归因于其特定的氨基酸组成,尤其是疏水性氨基酸和芳香族氨基酸的贡献[12]。对76条多肽的分析表明(图4),所有多肽均含有疏水性氨基酸,其占比为25%~100%,平均含量达到51.78%(图4-a)。此外,61.84%(47条)多肽含有芳香族氨基酸,其余38.16%(29条)则无该类氨基酸(图4-b)。据报道,富含疏水性氨基酸的酶解液和多肽可通过氢原子转移和单电子转移机制清除自由基[25],高比例的疏水性氨基酸与较强抗氧化活性相关[26];同时,具有疏水性氨基酸的多肽更容易与细胞膜相互作用,促进其内化吸收,从而发挥功能活性[27]。另一方面,芳香族氨基酸能够通过提供质子来稳定缺乏电子的自由基,以及通过共振结构保持自身的稳定性,进而增强自由基清除能力[28-29]。综上,<3 kDa组分中高含量的小分子多肽,且这些多肽含有较高的疏水性氨基酸和芳香族氨基酸,这些可能是其发挥生物活性的分子基础。
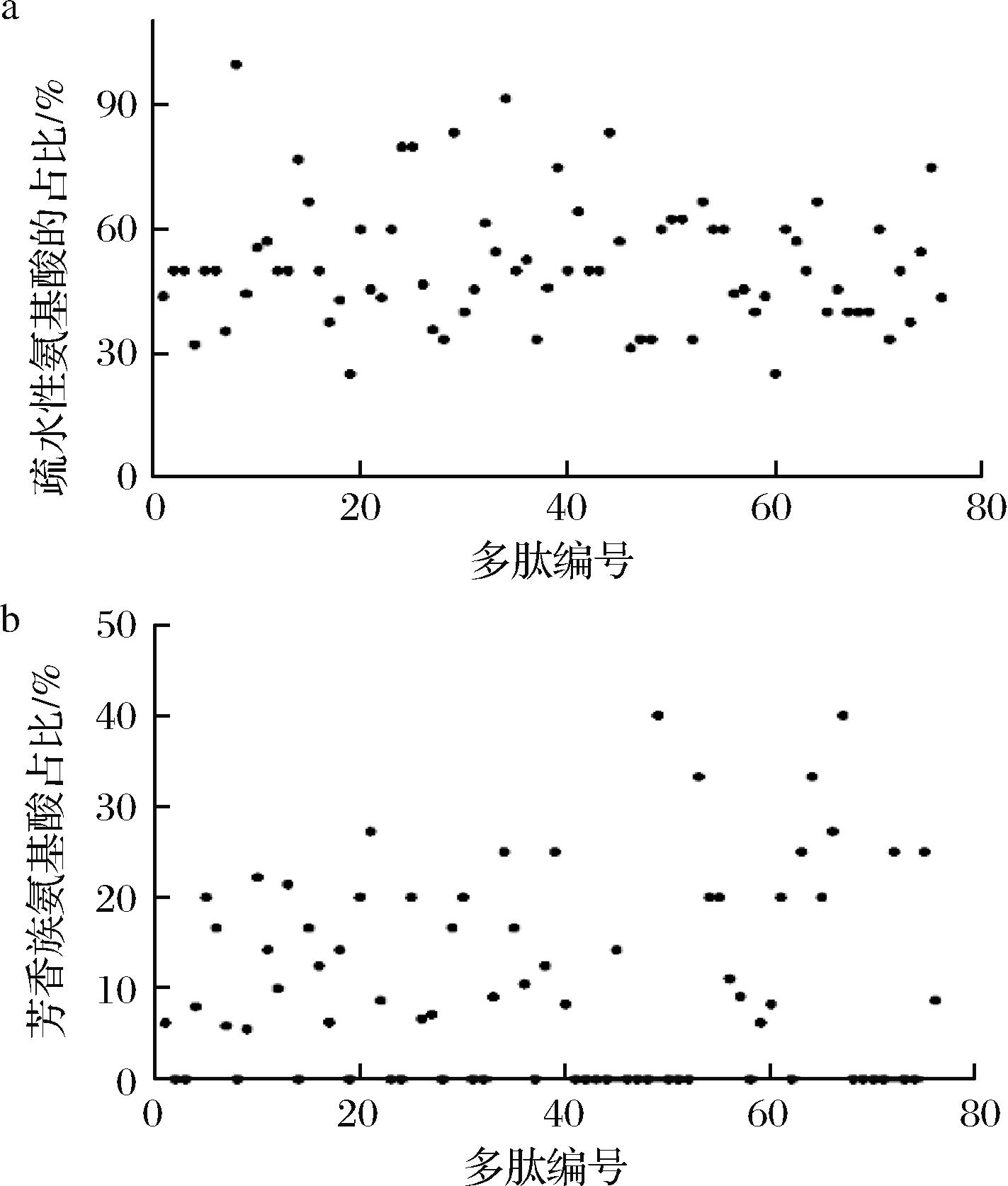
a-76条多肽的疏水性氨基酸的占比;b-76条多肽的芳香族氨基酸占比
图4 76条多肽的氨基酸组成分析
Fig.4 Amino acids composition of 76 peptides
2.4 蛹虫草活性多肽单体的筛选及其生物活性分析
通过对离子强度、活性预测分数和细胞穿透能力分数中各排名前30的多肽进行交集分析,从76条多肽中共筛选出5条潜在活性多肽,分别为IGGAQAVSGWNSAACGTCWR(1 195.2 Da)、KKPPVTPPPPPPP(1 251.6 Da)、NWVPGD(686.30 Da)、HAGPGGPGAGGPG(988.0 Da)和SGPCCSGNCHCP(1 164.4 Da)。由于小分子多肽通常更易通过胞吞作用进入细胞发挥作用,且具有更高的生物活性[27]。本研究从中选择分子质量较小的3条活性多肽[NWVPGD(记为P1)、HAGPGGPGAGGPG(记为P2)、SGPCCSGNCHCP(记为P3)]进一步在Glu诱导神经损伤的PC12细胞模型中评估其神经保护作用。如图5所示,3条多肽均未表现出明显细胞毒性(图5-a)。在Glu损伤PC12细胞模型中,模型组细胞存活率为(48.71±4.23)%,仅P1处理组细胞存活率显著提高至(62.48±2.06)%,而P2和P3未观察到明显保护效果(图5-b)。WU等[12]研究发现,秀珍菇蛋白质酶解液可将H2O2诱导氧化损伤的PC12细胞存活率提升约25%;王曙光等[13]研究报道了,核桃蛋白质酶解液经Sephadex G-15分离获得的各组分可将Glu诱导神经损伤的PC12细胞存活率提升5%~30%。相较而言,本研究从蛹虫草中分离得到的<3 kDa酶解液和单体多肽P1,分别在Glu损伤PC12细胞模型中可将细胞存活率提升了约18%和14%。虽然P1在数值略低于部分文献报道的粗提物或混合组分,但这可能正反映了P1作为一个高纯度单一成分的特性。上述结果表明,本研究成功从蛹虫草中鉴定出一条具有神经保护作用的六肽P1,其序列为Asn-Trp-Val-Pro-Gly-Asp,分子质量为686.30 Da,来源于蛹虫草中A0A2H4SP79蛋白(图6和表1)。
表1 蛹虫草多肽P1的信息
Table 1 Information of P1 from C.militaris
序列缩写长度分子质量/Da母蛋白Asn-Trp-Val-Pro-Gly-AspNWVPGD6686.30A0A2H4SP79
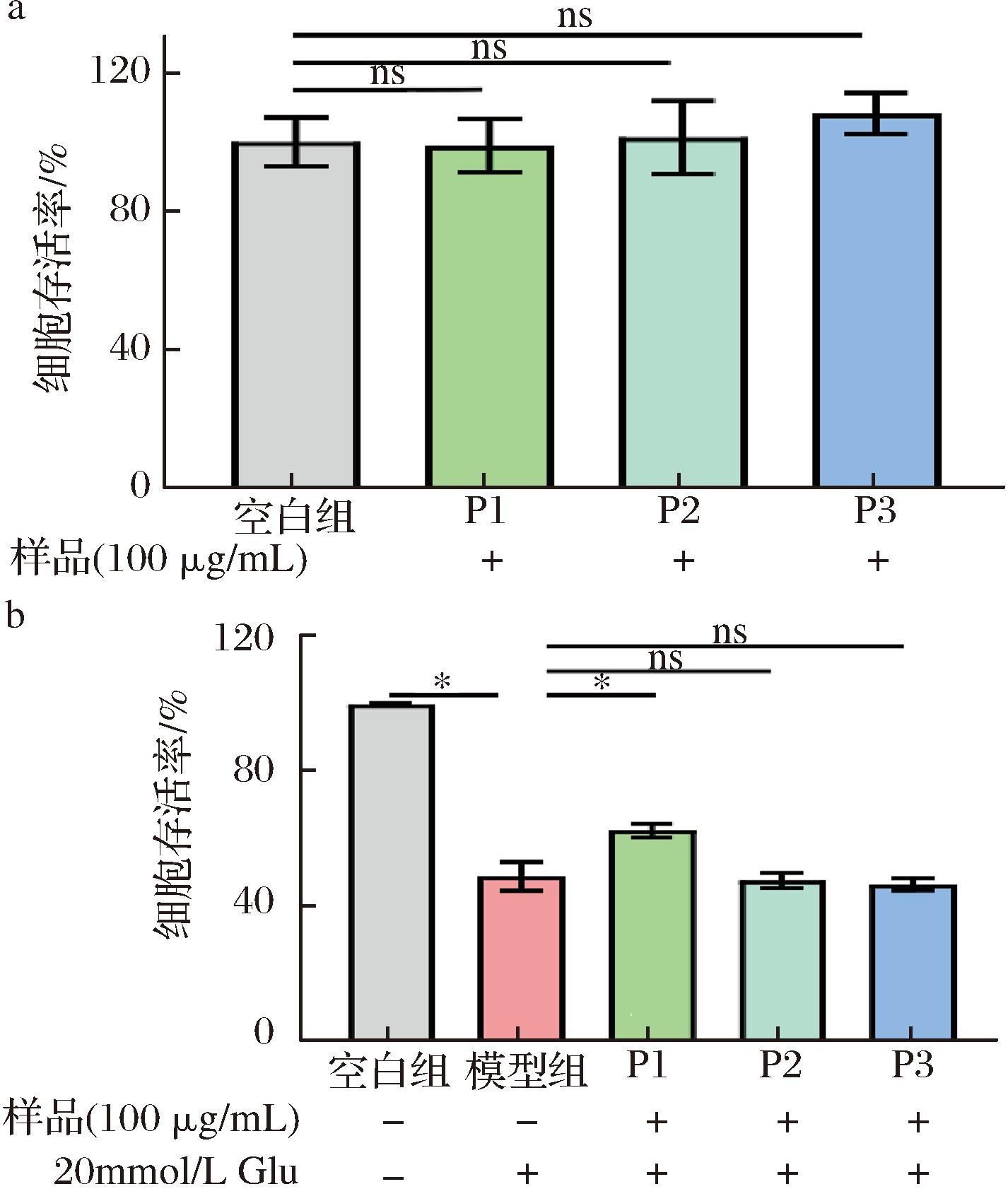
a-蛹虫草多肽PC12细胞的细胞毒性;b-蛹虫草多肽处理Glu损伤PC12细胞的细胞存活率
图5 蛹虫草多肽对Glu损伤PC12细胞保护效果
Fig.5 Protective effect of C.militaris peptide on Glu-injured PC12 cell model
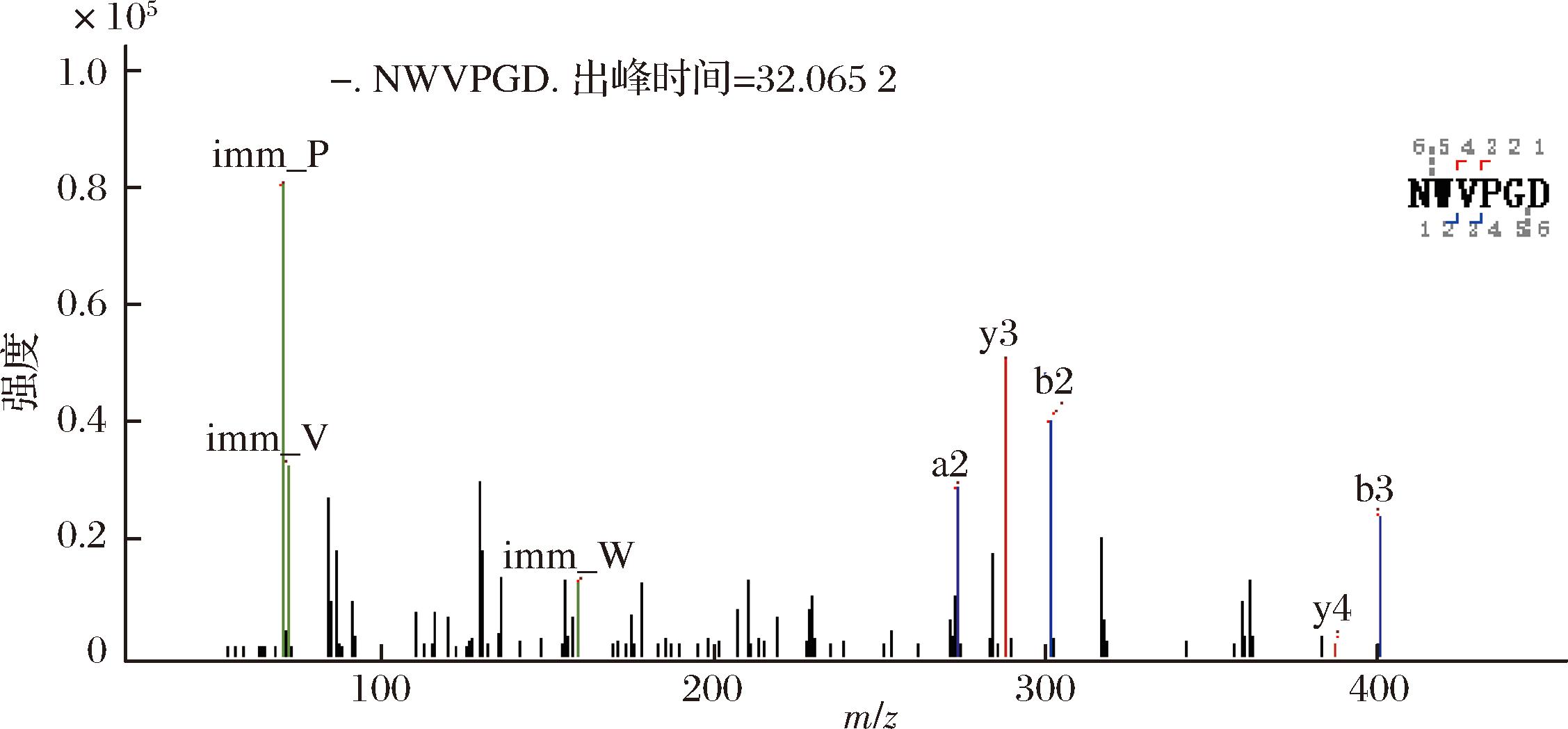
图6 蛹虫草多肽P1的二级质谱图
Fig.6 Secondary ion mass spectrometry of P1
2.5 蛹虫草活性多肽NWVPGD的抗氧化能力分析
Glu作为一种重要兴奋性神经递质,其在细胞外过量累积可导致细胞内抗氧化防御机制失衡,表现为谷胱甘肽减少、ROS增加和过氧化氢积累,最终引起神经元损伤及相关神经紊乱[13]。因此,Glu诱导的OS是引起PC12细胞神经损伤的重要因素之一。在此背景下,NWVPGD的抗氧化活性可能在其神经保护功效中发挥关键作用。为进一步阐明其抗氧化机制,本研究从自由基清除能力和激活机体抗氧化系统两方面进行评估(图7)。如图7-a所示,NWVPGD具有明显的DPPH自由基清除能力,在1 mg/mL质量浓度下的清除率达到(50.14±4.06)%,此后随质量浓度增加清除率进入平台期,表明其在该体系中具有一定的自由基清除饱和效应。此外,在调控细胞内抗氧化防御系统方面,重点关注了Keap1-Nrf2-ARE通路。正常情况下,核因子红细胞2相关因子2(Nrf2)与细胞质中的Keap 1蛋白结合,处于低活性状态。OS时,Nrf2被Keap1释放并进入细胞核,进而激活抗氧化反应元件(Nrf2-ARE)通路调控抗氧化基因表达,从而增强抗氧化活性[30]。NWVPGD与Keap1的分子对接结果如图7-b~图7-d所示,NWVPGD可与Keap1中Asp389、Ser431、Gly433和Ser508残基形成稳定氢键。同时,NWVPGD还可竞争性结合Nrf2在Keap1上的关键结合位点,包括Arg380、Arg415、Arg483和Ser555。这些结果表明,NWVPGD与Keap 1之间有较高的亲和活性与结合稳定性,可通过干扰Keap1-Nrf2相互作用,促进Nrf2的释放及其后续通路激活。综上所述,NWVPGD不仅具备直接清除自由基的能力,还可激活Keap1-Nrf2通路的内源性抗氧化防御系统,这两方面可能是其缓解OS诱导神经损伤的潜在作用机制,值得进一步研究。
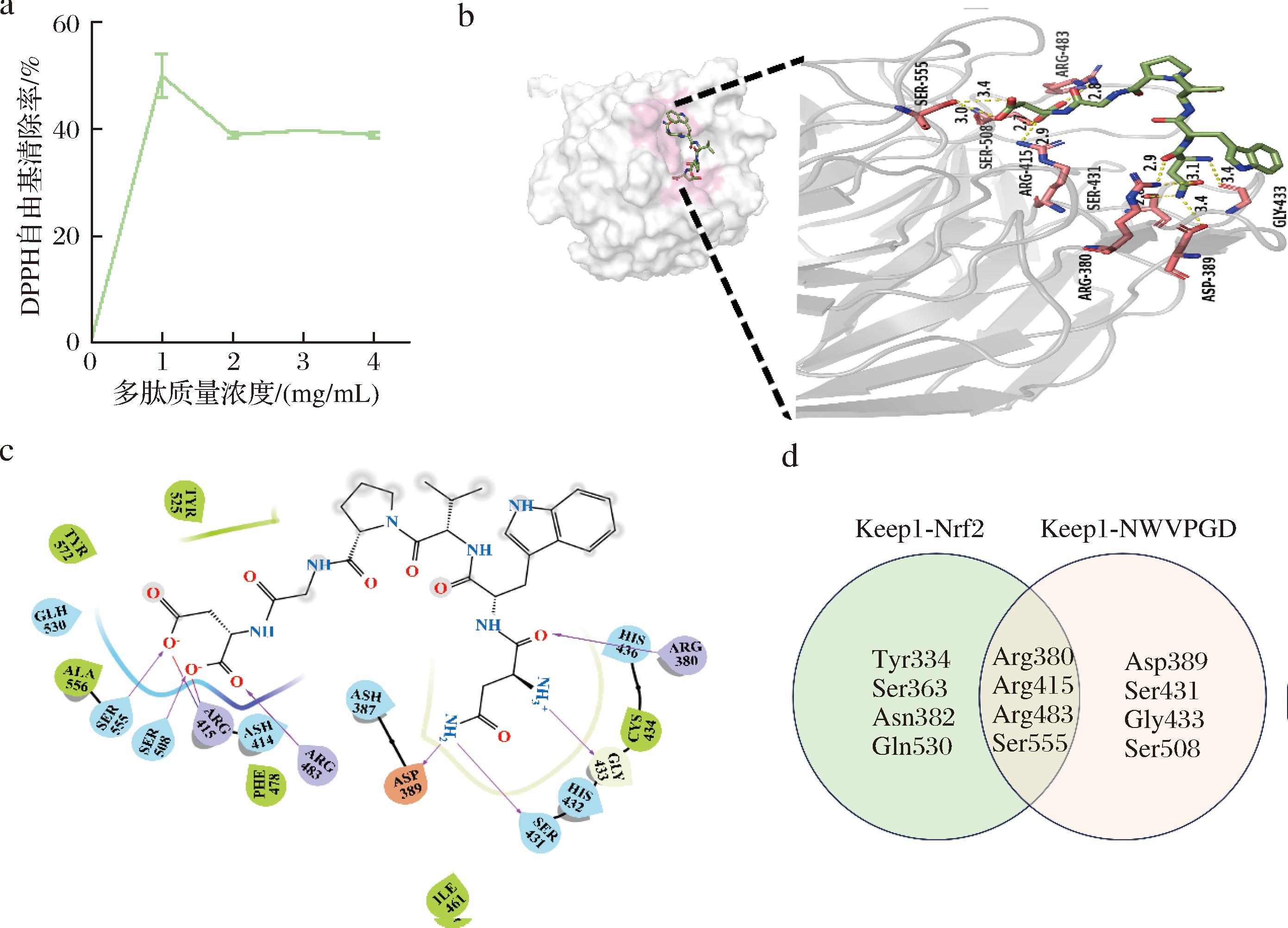
a-DPPH自由基清除能力;b,c-NWVPGD与Keap1的分子对接示意图;d-NWVPGD和Nrf2分别与Keap1对接靶点的Venn图
图7 NWVPGD的抗氧化能力
Fig.7 Antioxidants of NWVPGD
3 结论与讨论
本研究从蛹虫草中提取蛋白质,经模拟胃肠消化法获得具有神经损伤保护作用的酶解液组分。其中,<3 kDa酶解液对PC12细胞无明显毒性且有效提高Glu诱导神经损伤的PC12细胞存活率(P<0.05)。该组分的生物活性可能源于其所含的76个小分子肽,这些多肽含有较高比例的疏水性氨基酸或芳香族氨基酸。进一步筛选发现一条序列为NWVPGD的多肽单体,在Glu损伤PC12细胞模型中表现出明确的神经保护作用。该多肽单体不仅具备良好的自由基清除能力,还具有激活Keap1-Nrf2-ARE抗氧化通路的潜力,提示其抗氧化活性可能在神经保护作用机制中发挥关键作用。综上所述,蛹虫草多肽在预防神经退行性疾病方面展现出良好的功能性食品开发前景。后续研究应深入探讨其构效关系,并在体内模型中进一步验证其活性与作用机制。
[1] RADI E, FORMICHI P, BATTISTI C, et al. Apoptosis and oxidative stress in neurodegenerative diseases[J]. Journal of Alzheimer’s Disease, 2014, 42(Suppl 3): S125-S152.
[2] LI P, FENG D, YANG D C, et al. Protective effects of anthocyanins on neurodegenerative diseases[J]. Trends in Food Science &Technology, 2021, 117:205-217.
[3] WOLFE M S. Solving the puzzle of neurodegeneration[M]. The Molecular and Cellular Basis of Neurodegenerative Diseases. Amsterdam: Elsevier, 2018:1-22.
[4] DE ARA JO BOLETI A P, DE OLIVEIRA FLORES T M, MORENO S E, et al. Neuroinflammation: An overview of neurodegenerative and metabolic diseases and of biotechnological studies[J]. Neurochemistry International, 2020, 136:104714.
JO BOLETI A P, DE OLIVEIRA FLORES T M, MORENO S E, et al. Neuroinflammation: An overview of neurodegenerative and metabolic diseases and of biotechnological studies[J]. Neurochemistry International, 2020, 136:104714.
[5] SONG K, LI Y Y, ZHANG H L, et al. Oxidative stress-mediated blood-brain barrier (BBB) disruption in neurological diseases[J]. Oxidative Medicine and Cellular Longevity, 2020, 2020(1):4356386.
[6] 吴书建. 富硒蛹虫草硒多肽预保护缓解神经炎症的效果及机制研究[D]. 暨南大学, 2022.WU S. The pre-protection effect of Se-peptides obtained from Se-enrich Cordyceps militaris on mitigating neuroinflammation and the underlying mechanism [D]. Jinan University, 2022.
[7] 刘晴, 刘梦潜, 王芬, 等. 我国东北及山东部分地区野生蛹虫草资源采集及观察[J]. 菌物学报, 2022, 41(11):1761-1771.LIU Q, LIU M Q, WANG F, et al. Collection and observation of wild Cordyceps militaris resources in partial areas of Northeast China and Shandong Province[J]. Mycosystema, 2022, 41(11):1761-1771.
[8] 彭志苹, 张景艳, 李建喜. 蛹草有效成分及其药理作用[J]. 中兽医医药杂志, 2022, 41(2):51-55.PENG Z P, ZHANG J Y, LI J X. Chemical constituents and pharmacological activities of Cordyceps militaris[J]. Journal of Traditional Chinese Veterinary Medicine, 2022, 41(2):51-55.
[9] WU S J, WU Q P, WANG J, et al. Novel selenium peptides obtained from selenium-enriched Cordyceps militaris alleviate neuroinflammation and gut microbiota dysbacteriosis in LPS-injured mice[J]. Journal of Agricultural and Food Chemistry, 2022, 70(10):3194-3206.
[10] 宗静. 蛹虫草子实体活性多肽的提取分离方法及其部分生物活性的研究[D]., 2012.Zong J. Studies on extraction and separation and some biological activities of peptides from fruiting bodies of Cordyceps militaris [D]. Southwest University, 2012.
[11] 陈梦霏, 周娟娟, 吴书建, 等. 模拟胃肠消化提高蛹虫草蛋白的体外抗氧化活性[J]. 现代食品科技, 2020, 36(2):70-77.CHEN M F, ZHOU J J, WU S J, et al. Simulated gastrointestinal digestion increase the in vitro antioxidant activity of Cordyceps militaris proteins[J]. Modern Food Science and Technology, 2020, 36(2):70-77.
[12] WU S J, CHEN M F, LIAO X Y, et al. Protein hydrolysates from Pleurotus geesteranus obtained by simulated gastrointestinal digestion exhibit neuroprotective effects in H2O2-injured PC12 cells[J]. Journal of Food Biochemistry, 2022, 46(4): e13879.
[13] 王曙光. 核桃肽改善睡眠剥夺诱导大鼠记忆障碍及其对PC12细胞神经保护作用机制研究[D]. 华南理工大学, 2019.WANG S. Study on improving sleep deprivation-induced memory impairment in rat by walnut (Juglans regia) peptides and its neuroprotective mechanisms in PC12 cells [D]. South China University of Technology, 2019.
[14] 成翠, 兰乾敏, 王婷玉, 等. 基于网络药理学与分子对接探讨杜仲雄花多肽抗氧化机制[J]. 食品与发酵工业, 2025, 51(24):253-260.CHENG C, LAN Q M, WANG T Y, et al. Exploring antioxidant mechanism of peptides from Eucommia ulmoides male flowers based on network pharmacology and molecular docking[J]. Food and Fermentation Industries, 2025, 51(24):253-260.
[15] WU S J, BEKHIT A E A, WU Q P, et al. Bioactive peptides and gut microbiota: Candidates for a novel strategy for reduction and control of neurodegenerative diseases[J]. Trends in Food Science &Technology, 2021, 108:164-176.
[16] ZHOU J J, CHEN M F, WU S J, et al. A review on mushroom-derived bioactive peptides: Preparation and biological activities[J]. Food Research International, 2020, 134:109230.
[17] DAI C H, ZHANG W W, HE R H, et al. Protein breakdown and release of antioxidant peptides during simulated gastrointestinal digestion and the absorption by everted intestinal sac of rapeseed proteins[J]. LWT, 2017, 86:424-429.
[18] CHO S J. Changes in the antioxidant properties of rice bran protein isolate upon simulated gastrointestinal digestion[J]. LWT, 2020, 126:109206.
[19] TIM N M L, PARRA V, OTTE J, et al. Identification of radical scavenging peptides (<3 kDa) from Burgos-type cheese[J]. LWT-Food Science and Technology, 2014, 57(1):359-365.
N M L, PARRA V, OTTE J, et al. Identification of radical scavenging peptides (<3 kDa) from Burgos-type cheese[J]. LWT-Food Science and Technology, 2014, 57(1):359-365.
[20] SHEN D Y, BEGUM N, SONG H L, et al. In vitro and in vivo antioxidant activity and umami taste of peptides (1 kDa) from porcine bone protein extract[J]. Food Bioscience, 2021, 40:100901.
[21] WANG J Y, GUO M T, WANG Q L, et al. Antioxidant activities of peptides derived from mutton ham, Xuanwei ham and Jinhua ham[J]. Food Research International, 2021, 142:110195.
[22] PENG L, KONG X Y, WANG Z M, et al. Baijiu vinasse as a new source of bioactive peptides with antioxidant and anti-inflammatory activity[J]. Food Chemistry, 2021, 339:128159.
[23] SINGH B P, VIJ S. In vitro stability of bioactive peptides derived from fermented soy milk against heat treatment, pH and gastrointestinal enzymes[J]. LWT, 2018, 91:303-307.
[24] PEIGHAMBARDOUST S H, KARAMI Z, PATEIRO M, et al. A review on health-promoting, biological, and functional aspects of bioactive peptides in food applications[J]. Biomolecules, 2021, 11(5): 631.
[25] ESFANDI R, WALTERS M E, TSOPMO A. Antioxidant properties and potential mechanisms of hydrolyzed proteins and peptides from cereals[J]. Heliyon, 2019, 5(4): e01538.
[26] ZOU T B, HE T P, LI H B, et al. The structure-activity relationship of the antioxidant peptides from natural proteins[J]. Molecules, 2016, 21(1): 72.
[27] XU Q B, HONG H, WU J P, et al. Bioavailability of bioactive peptides derived from food proteins across the intestinal epithelial membrane: A review[J]. Trends in Food Science &Technology, 2019, 86:399-411.
[28] QIAN Z J, JUNG W K, KIM S K. Free radical scavenging activity of a novel antioxidative peptide purified from hydrolysate of bullfrog skin, Rana catesbeiana Shaw[J]. Bioresource Technology, 2008, 99(6):1690-1698.
[29] SARMADI B H, ISMAIL A. Antioxidative peptides from food proteins: A review[J]. Peptides, 2010, 31(10):1949-1956.
[30] WU S J, LIAO X Y, ZHU Z J, et al. Antioxidant and anti-inflammation effects of dietary phytochemicals: The Nrf2/NF-κB signalling pathway and upstream factors of Nrf2[J]. Phytochemistry, 2022, 204:113429.