氧化淀粉是变性淀粉的主要品种之一,是淀粉与氧化剂在一定温度、pH等条件下作用所得产品,因其流动性好、糊液稳定性高、黏度低、成膜性好等被广泛用于造纸工业中的涂料黏合剂和表面施胶剂,纺织工业的上浆剂及食品工业的添加剂等产品中[1]。
目前,制备氧化淀粉常用的氧化剂有高碘酸盐、重铬酸盐、次氯酸盐、高锰酸盐和过氧化氢等[2]。其中,过氧化氢成本低廉,绿色环保,越来越受到人们的重视[3]。工艺上,湿法工艺产生废水多,对环境污染大[4];而干法、半干法工艺用水量少,流程短,能耗低,已被广泛用于氧化淀粉制备中[5-9]。
并且加入一个价格低廉的过渡金属作为催化剂,可以促进反应进行[10];在我国,许多学者选用0.02%~0.2%硫酸铜为催化剂[4,11-12]。但是,含金属催化剂的应用会产生废水,造成环境污染,同时难以从产品中除去。所以,应当降低金属催化剂用量[2,13]。同时,氧化时通常需要加热,微波因其加热效率高、穿透能力强、均匀性强、对环境无害等优点,已作为一种新型能源广泛用于变性淀粉制备中[6]。此外,MAACHE等[14]研究表明瞬时控制压降处理会引起淀粉结构和物理化学特性变化,BAHRANI等[15]发现真空处理过的玉米淀粉颗粒结构变得脆弱。然而,真空辅助微波法用于氧化淀粉制备未见报道。
本试验根据前人的研究,从快速、节能、减排及降耗考虑,以玉米淀粉为原料,过氧化氢为氧化剂,加入少量催化剂(低于0.02%),引入真空处理辅助微波半干法制备氧化淀粉,并通过正交试验优化氧化条件,为环境友好制备变性淀粉提供理论与实际应用的支撑。
1 材料与方法
1.1 原料与试剂
玉米淀粉(水分含量13.66%),金平云鹏生物淀粉糖业有限责任公司;体积分数30%的过氧化氢(分析纯),成都市科龙化工试剂厂;CuSO4·5H2O(分析纯),重庆吉元化学有限公司;HCl(分析纯),成都市科龙化工试剂厂;NaOH(分析纯),成都市科龙化工试剂厂。
1.2 仪器与设备
DZ600/2S型真空包装机,上海人民包装股份有限公司;MAS-Ⅱ型微波快速制样系统,上海新仪化学科技有限公司;DHG-9070A型电热恒温鼓风干燥箱,上海齐欣科学仪器有限公司;YB-750A型多功能粉碎机,浙江永康市速锋工贸有限公司;NDJ-5S 型旋转黏度计,上海越平仪器有限公司;Spectrum 100红外光谱仪,美国Perkin Elmer公司;Olympus BX43生物显微镜,日本奥林巴斯公司;S-4800场发射扫描电子显微镜,日本日立公司。
1.3 试验方法
1.3.1 氧化淀粉的制备
真空氧化淀粉的制备:参照李芳良[6]的方法并适当改进,向混合器中加入一定量的淀粉,边搅拌边依次加入适量的过氧化氢、去离子水、硫酸铜,充分搅拌待混合均匀后,倒入聚乙烯袋中于真空包装机抽真空一定时间。然后将其破空并送入微波反应器中,在一定温度下反应一定时间。最后用质量分数10%亚硫酸钠溶液终止反应,经洗涤、烘干、粉碎得样品。
未真空氧化淀粉的制备:参照真空氧化淀粉制备方法,但不进行真空处理。比较其与真空氧化淀粉性能及结构的差异。
1.3.2 黏度测定
称取一定量的样品于150 mL烧杯内,加水配成质量浓度10%的淀粉乳,沸水中糊化30 min,并不断搅拌。待淀粉糊冷却到常温(25 ℃)后,测定其粘度(1号转子,12 r/min)。
1.3.3 氧化淀粉制备单因素试验
本试验主要考察过氧化氢用量、加水量、硫酸铜用量、真空处理时间、微波反应温度、微波反应时间对淀粉黏度的影响,试验以方法1.3.1制备氧化淀粉,以方法1.3.2测定其黏度,以黏度作为评价指标。
1.3.3.1 过氧化氢用量对黏度的影响
固定加水量30%(以淀粉干基计,下同),硫酸铜用量0.013 6%,50 ℃下微波反应6 min,分别在真空处理10 s和未真空处理下考察过氧化氢用量为4%、6%、8%、10%、12%时氧化淀粉黏度的变化。
1.3.3.2 加水量对黏度的影响
固定过氧化氢用量10%,硫酸铜用量0.013 6%,50 ℃下微波反应6 min,分别在真空处理10 s和未真空处理下考察加水量为22%、26%、30%、34%、38%时对氧化淀粉黏度的影响。
1.3.3.3 催化剂用量对黏度的影响
固定过氧化氢用量10%,加水量34%,50 ℃下微波反应6 min,分别在真空处理10 s和未真空处理下考察硫酸铜用量为0.010 4%、0.012 0%、0.013 6%、0.015 2%、0.016 8%时对氧化淀粉黏度的影响。
1.3.3.4 反应温度对黏度的影响
固定过氧化氢用量10%,加水量34%,硫酸铜用量0.013 6%,微波反应6 min,分别在真空处理10 s和未真空处理下考察反应温度为30、40、50、60、70 ℃时对氧化淀粉黏度的影响。
1.3.3.5 反应时间对黏度的影响
固定过氧化氢用量10%,加水量34%,硫酸铜用量0.013 6%,50 ℃下微波反应,分别在真空处理10 s和未真空处理下考察反应时间为3、4、5、6、7 min时氧化淀粉黏度的变化。
1.3.3.6 真空时间对黏度的影响
固定过氧化氢用量10%,加水量34%,硫酸铜用量0.013 6%,50 ℃下微波反应6 min,考察真空处理0、10、20、30、40 s时对氧化淀粉黏度的影响。
1.4 羧基含量的测定
采用淀粉糊滴定法[15],称取5.0 g样品于150 mL烧杯中,加入25 mL 0.1 mol/L的HCl溶液,样品在30 min内不断被摇动搅拌,过滤后用去离子水洗至无氯离子为止。将样品转移到500 mL烧杯中,加入300 mL去离子水,加热煮沸5~7 min,趁热以酚酞作指示剂,用0.1 mol/L的NaOH标准溶液滴定到终点,其消耗的体积为V1。
空白样:将原淀粉置于500 mL的烧杯中,加入300 mL蒸馏水糊化,用NaOH标准溶液趁热滴定至酚酞变色,消耗的体积为V2。按下式计算羧基含量:
![]()
(1)
式中:Y,羧基含量,%;c,NaOH标准溶液的浓度,mol/L;m,淀粉样品质量,g。
1.5 氧化淀粉结构表征
红外光谱分析:采用KBr压片法,以空气为对照,在400~4 000 cm-1区间扫描。
偏光十字:使用生物显微镜在偏振光镜下测定淀粉粒子的偏光十字,以去离子水作分散剂。
扫描电镜分析:用导电胶将干燥样品粘在样品台上,离子溅射金膜后用扫描电镜观察并拍照。
2 结果与分析
2.1 氧化淀粉制备单因素试验
2.1.1 过氧化氢用量对黏度的影响
过氧化氢用量对黏度的影响如图1所示,随着过氧化氢用量增加,氧化淀粉的黏度降低;当过氧化氢含量超过10%,黏度变化趋于平缓;且真空氧化淀粉黏度明显低于未真空氧化淀粉。这是因为过氧化氢用量增加,淀粉分子周围可利用的过氧化氢分子增多,因而淀粉氧化程度增大[5];而真空处理可能导致淀粉颗粒膨胀,结构更脆碎,过氧化氢更容易与淀粉接触,从而增加反应速率,增大氧化程度,使其黏度明显低于未真空氧化淀粉的黏度[16]。因此,过氧化氢较佳用量为10%。
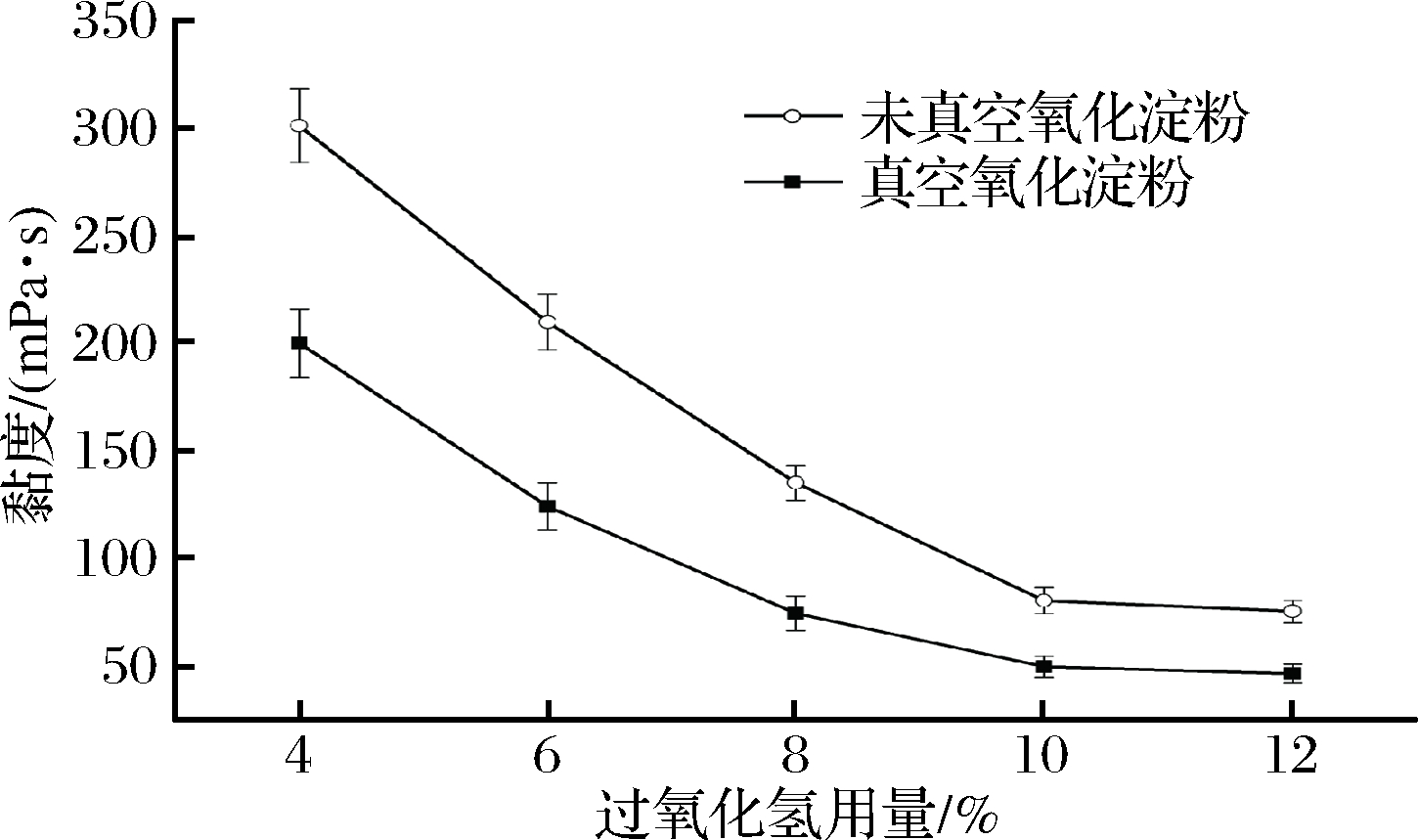
图1 过氧化氢用量对氧化淀粉黏度的影响
Fig.1 The effect of hydrogen peroxide dosage on viscosity of oxidized starch
2.1.2 加水量对黏度的影响
图2是加水量对黏度的影响情况,当水量从22%增加到30%时,氧化淀粉黏度急剧降低;当水量超过30%,黏度降幅变缓;且真空氧化淀粉黏度明显低于未真空氧化淀粉,最低为未真空氧化淀粉黏度的1/2。这是因为水量过少,反应试剂不易在淀粉中扩散渗透;水量增加,反应试剂渗透能力增强,淀粉颗粒充分膨胀,氧化程度增大,从而黏度降低。但是,水量过多会降低试剂浓度,使反应速率降低,加速淀粉糊化,使反应体系发黏,导致黏度降幅变缓[17]。而真空处理可能导致淀粉颗粒膨胀,使反应试剂更易在淀粉中扩散渗透,从而增大淀粉氧化程度,使其黏度明显低于未真空氧化淀粉的黏度。因此,加水量以34%为宜。

图2 加水量对氧化淀粉黏度的影响
Fig.2 The effect of water addition on viscosity of oxidized
starch
2.1.3 催化剂用量对黏度的影响
图3是硫酸铜用量对黏度的影响情况。氧化淀粉黏度随硫酸铜用量的增加而降低;当硫酸铜用量超过0.013 6%,黏度逐渐增大。一是铜离子与氧化剂反应生成羟基自由基,增强氧化反应;二是铜离子能破坏淀粉颗粒结构,使氧化剂更好地与淀粉分子接触,改善氧化效果[18]。但是硫酸铜用量过多,由于氧化淀粉对铜离子有一定的络合作用,核心离子被禁锢,催化效果下降,因而黏度增大[19]。此外,相同硫酸铜用量下,真空氧化淀粉黏度低于未真空氧化淀粉,如硫酸铜用量为0.008 8%时,真空氧化淀粉的黏度为210 mPa·s,与未真空氧化淀粉的黏度319.8 mPa·s有极显著性差异(p<0.01)。因此,真空处理可能破坏了淀粉颗粒结构,从而提高淀粉氧化程度。故选择硫酸铜用量在0.013 6%为宜。
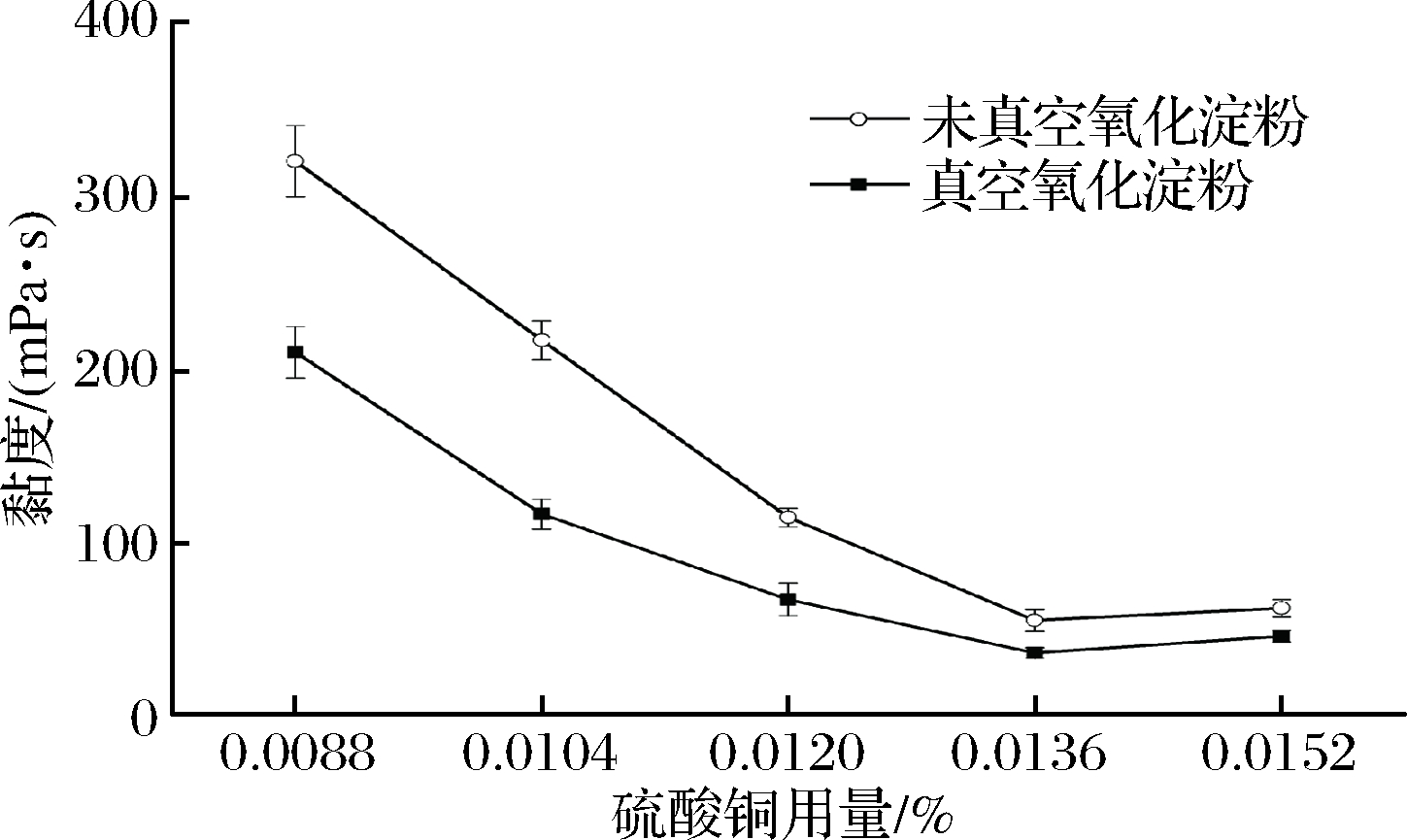
图3 硫酸铜用量对氧化淀粉黏度的影响
Fig.3 The effect of copper sulfate dosage on viscosity of oxidized starch
2.1.4 反应温度对黏度的影响
反应温度对黏度的影响如图4所示。
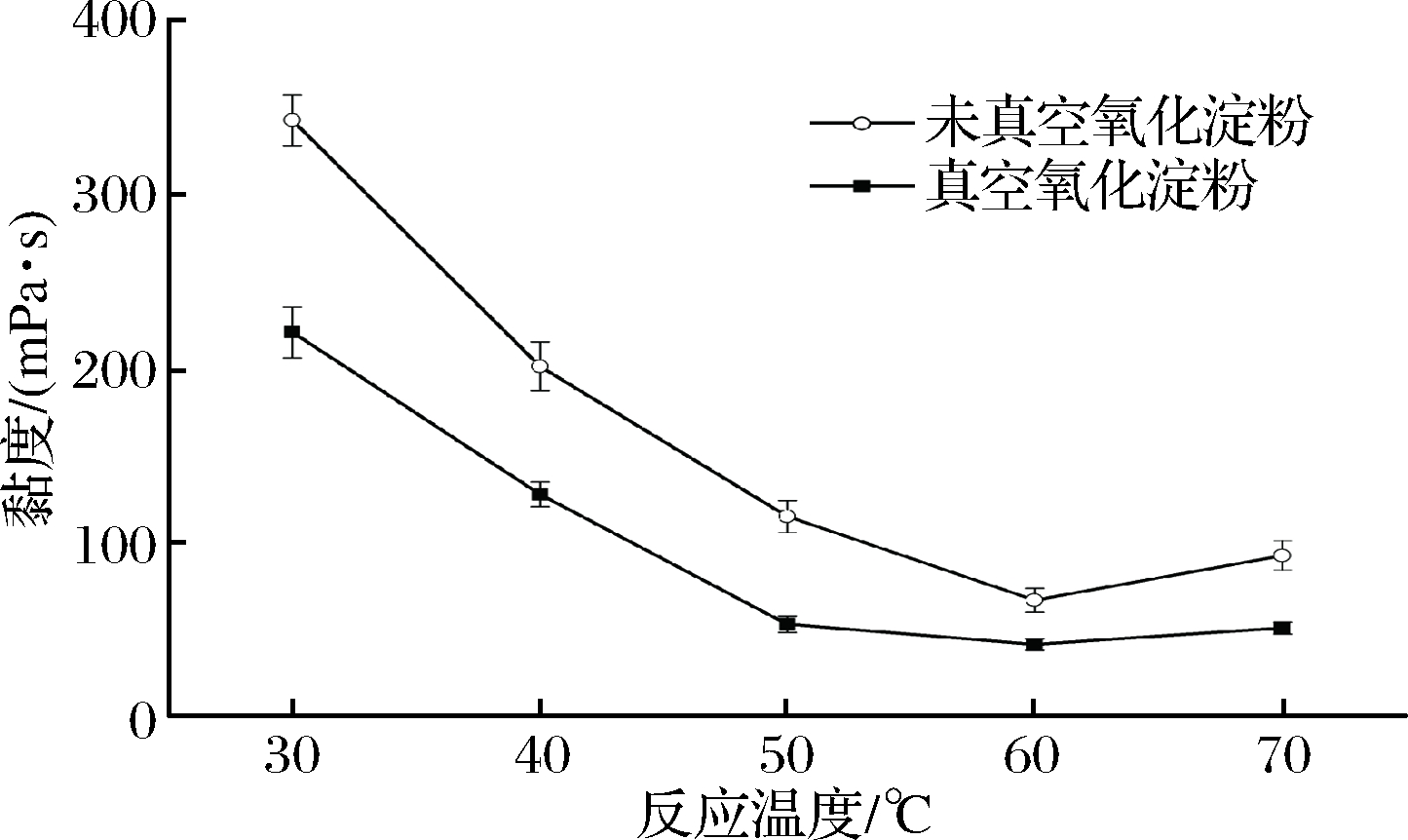
图4 反应温度对氧化淀粉黏度的影响
Fig.4 The effect of reaction temperature on viscosity of oxidized starch
反应温度增加,氧化淀粉黏度随之降低,当温度高于60 ℃时,黏度升高。这是因为温度升高,满足反应所需的活化能,同时淀粉颗粒膨胀程度增加,氧化剂更易渗透到膨胀淀粉颗粒中,反应速率加快,从而氧化程度提高,黏度降低。但是,温度过高,过氧化氢分解速率加快,浓度降低,氧化程度降低,因而黏度增加[20]。在相同温度下,真空氧化淀粉黏度低于未真空氧化淀粉;且随着温度的增加,相同温度变化下真空氧化淀粉黏度降幅高于未真空氧化淀粉,如当温度从40 ℃升到50 ℃时,真空氧化淀粉黏度由127.5 mPa·s降到53 mPa·s,下降了58%;未真空氧化淀粉由201 mPa·s降到114.8 mPa·s,下降了43%。可能是因为真空处理使淀粉结构疏松,易于氧化剂渗透,故黏度降低显著。同时,温度过高会引起淀粉糊化。所以,选择温度在60 ℃为宜。
2.1.5 反应时间对黏度的影响
反应时间对黏度的影响如图5所示,反应时间不足6 min,黏度随反应时间延长而迅速降低,反应时间继续增加,黏度降低变缓;6 min以后,黏度降低趋势平缓;且真空氧化淀粉黏度明显低于未真空氧化淀粉。这是因为反应前期氧化剂浓度较高,氧化容易,随着反应的进行,氧化剂被消耗,没有足够的氧化剂参与反应,降解和氧化反应逐渐停止导致反应效率降低[21]。故最佳的反应时间为6 min。
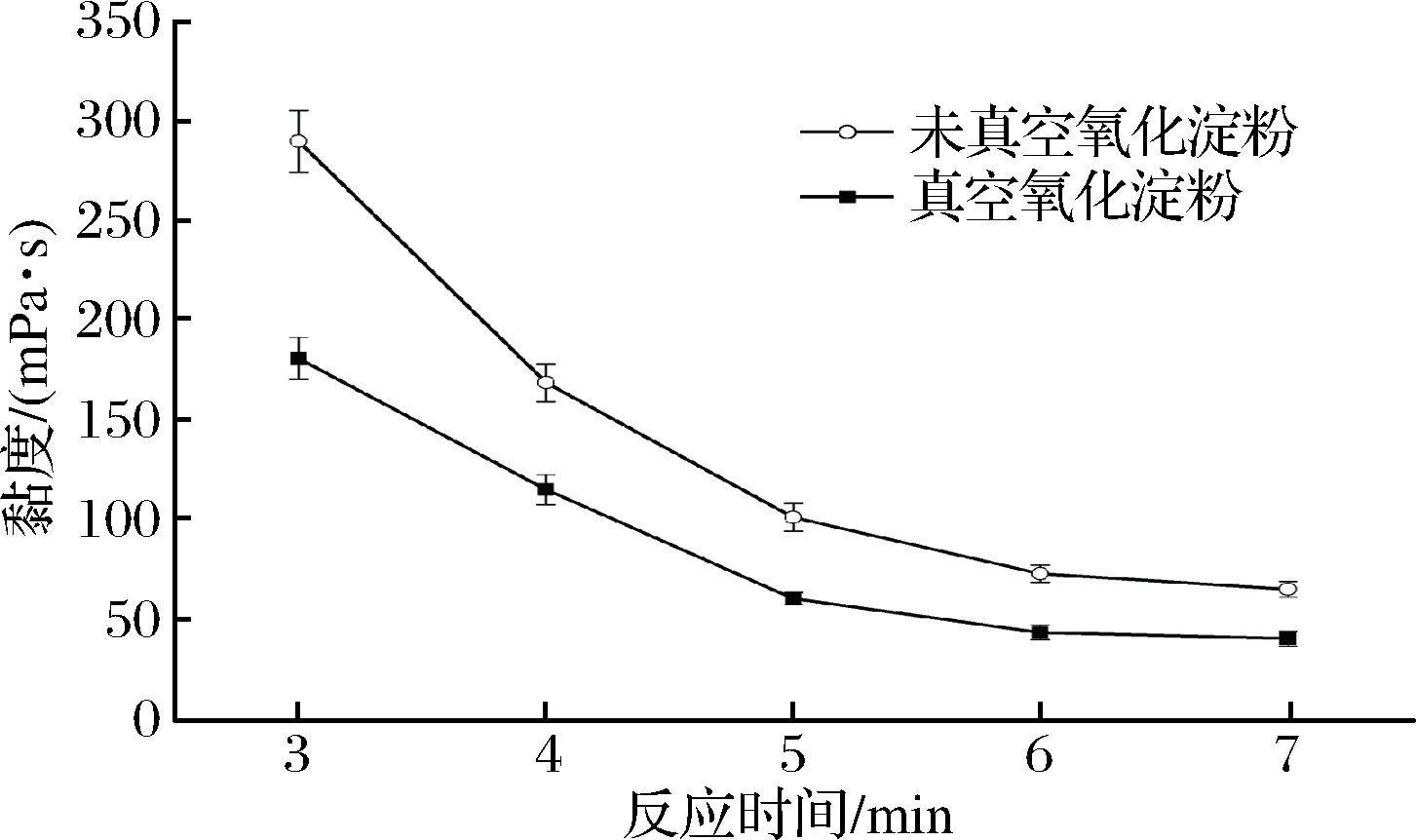
图5 反应时间对氧化淀粉黏度的影响
Fig.5 The effect of reaction time on viscosity of oxidized starch
2.1.6 真空处理时间对黏度的影响
图6为真空处理时间对黏度的影响情况,未真空处理时氧化淀粉黏度为82.5 mPa·s;当真空处理10 s时,黏度大大降低,为51.8 mPa·s;随着真空处理时间的增加,黏度继续降低;30 s后,黏度减势趋缓,这可能是是因为真空处理时,淀粉颗粒内部的压力高于外部压力,导致淀粉颗粒膨胀,结构变脆,处理时间长,颗粒膨胀更严重[16],氧化剂分子更易与淀粉颗粒反应。
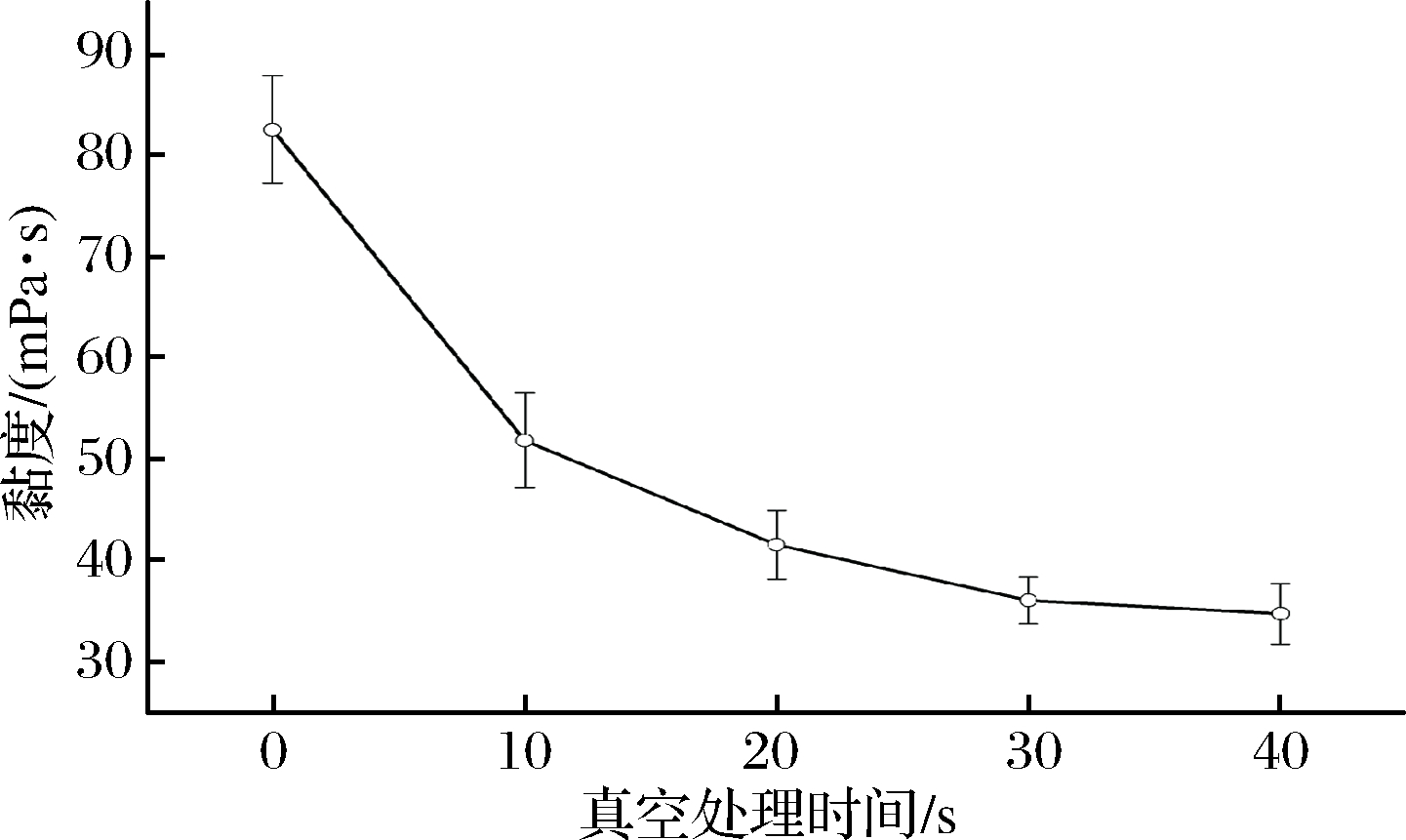
图6 真空处理时间对氧化淀粉黏度的影响
Fig.6 The effect of vacuum treatment time on viscosity of oxidized starch
2.2 正交试验
根据单因素试验结果,固定过氧化氢用量为10%,反应时间为6 min,设计催化剂用量、加水量、反应温度、真空处理时间进行4因素3水平正交试验(见表1),采用L9(34) 正交表对工艺条件进行优化。试验结果及分析见表2。
表1 L9(34)正交试验因素水平表
Table 1 Orthogonal test design table of the L9(34)
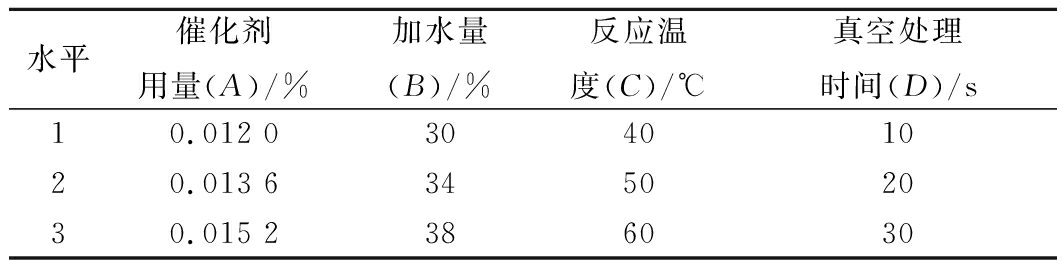
表2 正交试验结果表
Table 2 Results of orthogonal test

本试验以氧化淀粉黏度为评价指标,黏度越低,淀粉氧化程度越大。由表2中极差分析可知,各因素对黏度的影响大小次序为:催化剂用量>反应温度>真空处理时间>加水量。由于试验结果最优组合A3B1C3D2与K值分析最优组合A2B1C3D2不一致,故分别进行了3次验证试验,结果表明组合A2B1C3D2制得产品黏度低于组合A3B1C3D2制得产品黏度,因此确定A2B1C3D2为较佳工艺条件,即催化剂用量0.013 6%,加水量30%,反应温度60 ℃,真空处理时间20 s。在此条件下产品黏度为11.8 mPa·s。
2.3 黏度及羧基含量
由于原淀粉10%的淀粉乳太黏稠而未测出其黏度,故测得其2%浓度下黏度。淀粉黏度及羧基含量见表3,真空氧化淀粉黏度11.8 mPa·s显著(p<0.05)低于未真空氧化淀粉21.8 mPa·s;且真空氧化淀粉羧基含量显著(p<0.05)高于未真空氧化淀粉,说明真空氧化反应较未真空氧化反应更剧烈,可能是真空处理导致淀粉颗粒结构变化,使氧化剂分子进入淀粉内部引起淀粉更高程度的解聚,产生更多的羧基,同时引起黏度降低[16]。与已有研究报道相比,氧化效果相当,如彭佳莹等[7]以微波干法制备出黏度(浓度为6%)为4 mPa·s,羧基含量为0.586%的氧化淀粉;王亚龙等[22]以微波湿法制备出黏度(浓度为15%)最低为23.4 mPa·s,羧基含量最高为0.275%的氧化淀粉。
表3 黏度及羧基含量
Table 3 Viscosity and carboxyl content

注:同列字母不同表示差异显著(p<0.05)。
2.4 氧化淀粉黏度与羧基含量的关系
氧化淀粉的黏度是其应用的重要指标,且大小与氧化程度相关。改变试剂用量制得不同羧基含量的真空氧化淀粉,观察羧基含量不同时黏度的变化,结果如图7所示。由图7可知,氧化淀粉黏度随其羧基含量增大而降低。因为在氧化过程中,淀粉分子链被切断,导致淀粉分子质量变小,聚合度降低,溶解度增大,抗剪切力稳定性减弱,从而黏度下降。羧基含量越高,表明淀粉被氧化程度越深,分子降解程度越大,导致黏度越小[23]。
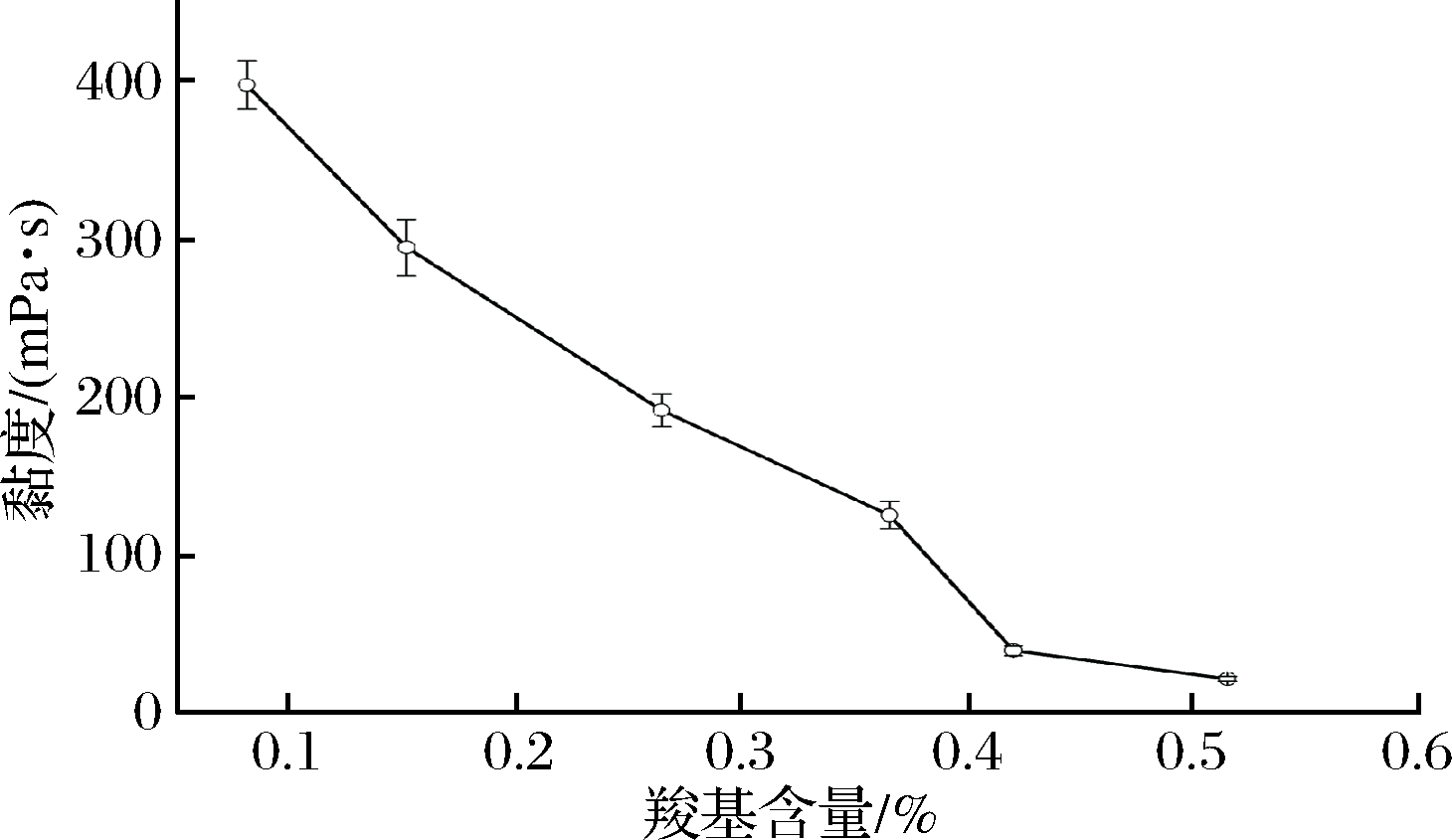
图7 氧化淀粉黏度与羧基含量的关系
Fig.7 The effect of carboxyl content on viscosity of oxidized
starch
2.5 氧化淀粉结构表征
2.5.1 红外光谱分析
淀粉被氧化后,其分子上的羟基可转化为羰基和羧基,这些变化可用红外光谱鉴定,如图8所示。原淀粉在3 410.5和2 929 cm-1处的吸收峰分别为—OH和—CH2的伸缩振动特征峰[21];1 645 cm-1的吸收峰是典型的H—O—H的弯曲振动吸收峰;1 151、1 080和1 018 cm-1处吸收峰为C—O—C键的伸缩振动峰[2];1 400~800 cm-1的区域为C—C和C—O键的伸缩振动[24]。与原淀粉相比,真空氧化淀粉和未真空氧化淀粉分别在1 615与1 616 cm-1出现羧基的特征吸收峰[25-26],说明淀粉被成功氧化。
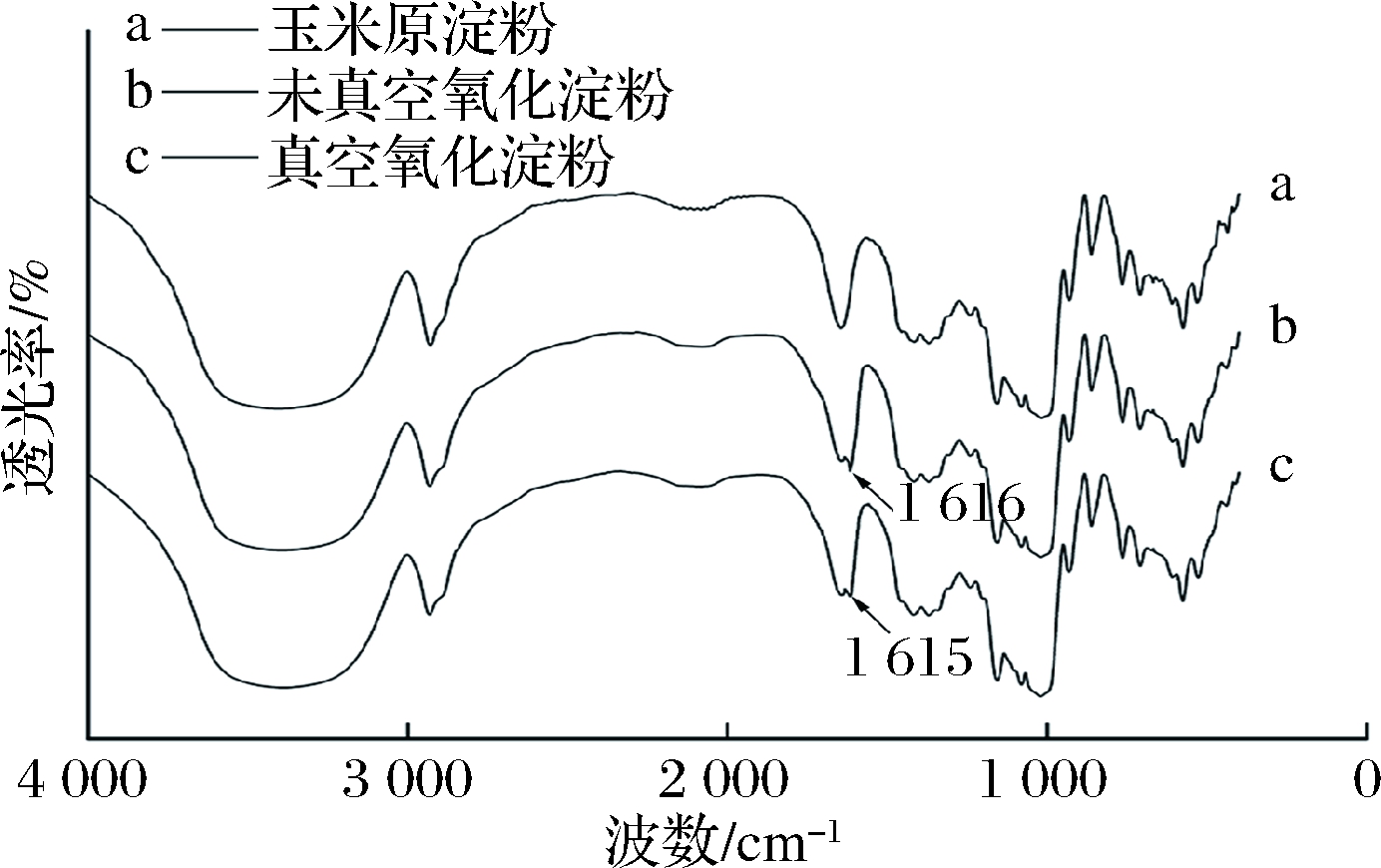
图8 原淀粉、未真空氧化淀粉、真空氧化淀粉的红外光谱图
Fig. 8 FTIR patterns of native, non-vacuum oxidized and vacuum oxidized starches
2.5.2 偏光十字
图9为淀粉的偏光显微镜图,从图9可以看出,玉米淀粉颗粒外观为圆形和多边型。图9-a中玉米原淀粉颗粒的偏光十字明显,叉点位于颗粒中心,呈现垂直十字交叉;未真空氧化淀粉(图9-b)和真空氧化淀粉(图9-c)依然显示出清晰的偏光十字,说明氧化反应没有改变淀粉的晶体结构,反应发生在淀粉的无定型区[27]。
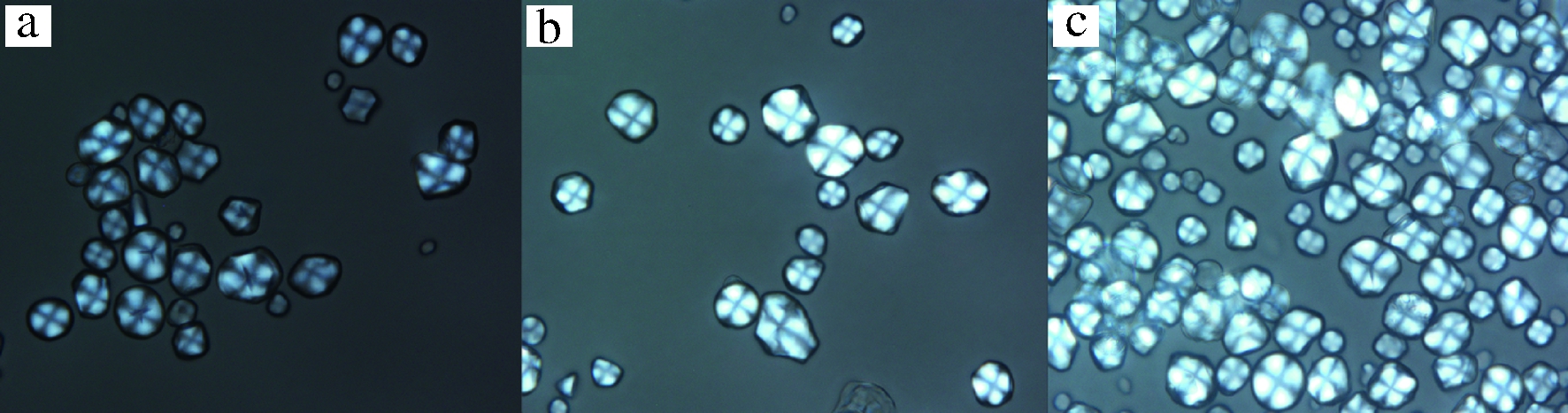
a-玉米原淀粉(400×);b-未真空氧化淀粉(400×);c-真空氧化淀粉(400×)
图9 原淀粉、未真空氧化淀粉、真空氧化淀粉的偏光显微镜图
Fig.9 Polarized light micrographs of native, non-vacuum oxidized and vacuum oxidized starches
2.5.3 扫描电镜
淀粉扫描电镜图如图10所示,由图10-a中可以看出玉米原淀粉呈椭圆形或不规则多边形,其颗粒分散,棱角光滑,形貌规整,表面光滑;由图10-b和图10-c可以看出氧化淀粉仍为颗粒状,其大小未变,但表面粗糙,且某些颗粒表面出现裂缝,这是由于过氧化氢与淀粉反应,造成淀粉表面损伤,说明氧化反应发生在淀粉表面[28]。

a-玉米原淀粉(2000×);b-未真空氧化淀粉(2000×);c-真空氧化淀粉(2000×)
图10 原淀粉、未真空氧化淀粉、真空氧化淀粉的扫描电镜图
Fig.10 Scanning electron microscopy images of native,non-vacuum oxidized and vacuum oxidized starches
3 结论
(1)同样条件下,真空处理下氧化淀粉的黏度明显低于未真空条件下氧化淀粉的黏度,表明真空处理可以促进氧化,将其运用到淀粉氧化改性是有效的。同时,微波加热能大大加快反应的进行,反应只需6 min就可制得低黏度氧化淀粉;真空处理辅助微波半干法制备氧化淀粉可以减少催化剂及水用量,同时缩短反应时间,达到快速高效、节能、减排及降耗的目的。
(2)真空处理制备氧化淀粉的优化试验条件为:过氧化氢用量10%,催化剂用量0.0136%,加水量30%,反应温度60 ℃,真空处理时间20 s,微波反应时间为6 min;在此条件下可制得黏度为11.8 mPa·s,羧基含量为0.556%的氧化淀粉;而同等条件下,未真空处理制得氧化淀粉黏度增加,羧基含量降低,分别为21.8 mPa·s,0.414%。
(3)采用红外光谱、偏光十字、电子显微镜对原淀粉、真空氧化淀粉、非真空氧化淀粉进行表征,结果表明:淀粉被成功氧化,氧化反应发生在淀粉的无定型区。
参考文献
[1] 曹晶晶,杨益琴.TEMPO/NaBr/NaClO体系下氧化淀粉的制备及其结构性能表征[J].南京林业大学学报(自然科学版),2011,35(2):88-92.
[2] SHENG Ye,WANG Qiu-hua,XU Xue-chun,et al.Oxidation of cornstarch using oxygen as oxidant without catalyst[J].LWT-Food Science and Technology, 2011, 44(1):139-144.
[3] 王春艳,钟耕,李大勇.双氧水氧化玉米淀粉的制备及其性质研究[J].粮食与饲料工业,2007(8):26-27.
[4] 李芳良,麻昌爱,韦群兰.室温半干法制备木薯氧化淀粉的研究[J].农产品加工(学刊),2008(1):51-53.
[5] 刘冠军,董海洲,侯汉学,等.干法制备氧化淀粉的工艺研究[J].食品与发酵工业,2005(11):71-74.
[6] 李芳良,童张法,黄祖强,等.微波干法制备氧化淀粉的研究[J].化工技术与开发,2007(2):13-17.
[7] 彭佳莹,周露,杨椰,等.新型氧化剂微波干法制备氧化淀粉及其性能研究[J].中国粮油学报,2012,27(5):39-43,59.
[8] 文玉萍,覃学江.半干法生产纺织用氧化淀粉工艺探讨[J].化工技术与开发,2014,43(6):37-39.
[9] 孙小凡,朱明霞,高友君.小麦氧化淀粉制备工艺及性质研究[J].食品科技,2012,37(3):175-177,186.
[10] 丁龙龙,张彦华,顾继友,等.高羧基含量氧化淀粉的制备与表征[J].林产化学与工业,2014,34(2):108-112.
[11] 李芳良,童张法,麻昌爱,等.木薯交联氧化淀粉的制备及性能研究[J].现代食品科技,2009,25(2):157-161.
[12] 韦艳枝,黄祖强,胡华宇,等.氧化淀粉的机械活化木薯淀粉干法制备[J].湖北农业科学,2012,51(24):5 752-5 755.
[13] LUKASIEWICZ M,BEDNARZ S,PTASZEK A.Environmental friendly polysaccharide modification-microwave-assisted oxidation of starch[J].Starch-Stärke,2011,63(5):268-273.
[14] MAACHE-REZZOUG Z,ZARGUILI I,LOISEL C,et al.Structural modifications and thermal transitions of standard maize starch after DIC hydrothermal treatment[J].Carbohydrate Polymers,2008,74(4):802-812.
[15] 丁龙龙,张彦华,顾继友,等.傅里叶变换红外测定氧化淀粉的羧基含量初探[J].光谱学与光谱分析,2014,34(2):401-404.
[16] BAHRANI S A, LOISEL C, REZZOUG S A,et al. Role of vacuum steps added before and after steaming treatment of maize starch. Impact on pasting,morphological and rheological properties[J].Carbohydrate Polymers,2012, 89(3):810-820.
[17] 谭义秋,农克良.正交试验法优化马铃薯氧化淀粉制备工艺[J].粮食与油脂,2009(9):16-18.
[18] ABANOWSKA M,BIDZNSKA E,PIETRZYK S,et al.Influence of copper catalyst on the mechanism of carbohydrate radicals generation in oxidized potato starch[J].CarbohydratePolymers,2011,85(4):775-785.
[19] 谭义秋,黄祖强,王茂林,等.机械活化木薯淀粉干法制备氧化淀粉的研究[J].食品科技,2008(6):32-36.
[20] 王丽萍,李祥,师春兰.高羧基含量氧化淀粉的制备[J].食品科技,2015,40(10):206-210.
[21] ZHANG Yu-rong,WANG Xiu-liu,ZHAO Guo-ming,et al.Preparation and properties of oxidized starch with high degree of oxidation[J].Carbohydrate Polymers,2012,87(4):2 554-2 562.
[22] 王亚龙,张宏伟.微波湿法氧化淀粉的制备及其性质研究[J].食品科技,2010,35(2):183-186.
[23] 谭义秋.马铃薯氧化淀粉性质及表征[J].粮食与油脂,2011(2):10-12.
[24] TANG Hong-tao,TANG Hong-bo,LI Yang-ping.Synthesis,optimization,characterization and property of oxidized hydroxypropyl mung bean starch[J].Journal of Food Processing and Preservation,2017,41(1):e12 763.
[25] ZHANG Shui-dong,ZHANG Yu-rong,WANG Xiu-li,et al.High carbonyl content oxidized starch prepared by hydrogen peroxide and its thermoplastic application[J].Starch-Stärke, 2009, 61(11): 646-655.
[26] 卢鑫. 氧化蜡质玉米淀粉的制备及性质研究[D].哈尔滨:哈尔滨商业大学,2015.
[27] KUAKPETOON D, WANG Y J. Locations of hypochlorite oxidation in corn starches varying in amylose content[J].Carbohydrate Research,2008,343(1):90-100.
[28] SANGSEETHONG K, TERMVEJSAYANON N, SRIROTH K. Characterization of physicochemical properties of hypochlorite-and peroxide-oxidized cassava starches[J].Carbohydrate Polymers, 2010, 82(2):446-453.