天然虾青素是一种具有强抗氧化特性的叶黄素类胡萝卜素,其抗氧化性分别是VE和番茄红素的550倍和55倍,被誉为“超级维生素E”,广泛应用于功能食品和制药行业[1-3]。天然虾青素可从细菌、原生动物、真菌以及甲壳类动物中获得[4],而雨生红球藻(H. pluvialis)因其生长周期短、培养条件易控制且虾青素含量高,被认为是天然虾青素的最佳来源[5-6]。
胁迫条件下,当雨生红球藻中叶绿素及初生类胡萝卜素不足以保护细胞免受损伤时,虾青素会大量合成。然而,环境胁迫同时也会增加细胞内活性氧的水平,使得细胞的生长受到阻碍[7-9]。雨生红球藻细胞内存在两套清除活性氧的防御体系:一类为酶促系统(短期机制);另一类为非酶促系统(长期机制),主要产物为虾青素。在胁迫条件下,作为信号分子的ROS迸发,激活雨生红球藻两套抗氧化系统进行防御[10],但ROS水平的急剧增加可能会影响抗氧化酶的活性。β-胡萝卜素酮醇酶(β-carotenoid ketolase, BKT)是虾青素合成过程中一个关键酶,催化β-胡萝卜素形成β-胡萝卜素衍生物角黄质,然后进一步被催化形成虾青素[11],bkt基因表达量的提高可以有效提高β-胡萝卜素转化为角黄质的效率,从而提高虾青素的合成效率。有报道指出,在胁迫条件下虾青素的积累与脂质合成密切相关[12]。ω-3脂肪酸去饱和酶(fatty acid desaturase,FAD)酶基因fad作为脂质合成途径上的一个关键酶基因,其表达量水平也会间接影响虾青素的积累。
褪黑素(melatonin, MLT),是一种甲氧基吲哚胺,是色氨酸的衍生物[13-14],已有研究证明外源褪黑素处理能够增强植物抵御逆境的能力[15]。徐向东等[16]在高温胁迫条件下向黄瓜幼苗叶面喷施褪黑素,发现黄瓜幼苗叶片H2O2和丙二醛(MDA)的积累被有效抑制,抗氧化物质改性树脂(ASA)和谷胱甘肽(GSH)含量及抗坏血酸代谢相关酶——抗坏血酸过氧化物酶(APX)、单脱氢抗坏血酸还原酶(MDHAR)、脱氢抗坏血酸还原酶(DHAR)和谷胱甘肽还原酶(GR)活性被提高。虾青素作为雨生红球藻应对环境胁迫的主要次生代谢产物, MLT对其合成的调控作用和作用机理方面的研究鲜有报道。
该试验以雨生红球藻 H. pluvialis LUGU为对象,在高光照联合缺氮条件下,研究外源MLT诱导对其生长、虾青素积累和油脂积累的影响以及对抗氧化酶SOD, CAT和POD活性的影响,同时分析了MLT对虾青素和油脂合成相关酶基因表达量的影响。为提高虾青素的产量及MLT诱导其合成机制提供了理论依据。
1 材料和方法
1.1 雨生红球藻的培养和诱导
雨生红球藻H. pluvialis LUGU为云南省高原淡水湖泸沽湖水样中分离纯化所得[17]。以BBM为基础培养基,在鼓泡式光生物反应器(直径0.2 m,高0.3 m,容积3 L)中培养,(其中含2 L BBM培养基),并以0.1 vvm/min的速度通入无菌空气,光照强度为2800 lx,室内恒温(25±1)℃,培养到对数后期(大约9.0×105 cells/mL)。
采用3 800×g离心5 min,无菌水洗涤两次,以去除残留的营养物质。将所获的藻液沉淀,并重新悬浮至缺氮的BBM(500 mL锥形瓶,其中含360 mL培养基)培养基中,最初的细胞浓度调整为2×105 cells/mL。用二甲基亚砜(DMSO)溶解MLT作为母液,添加同样体积MLT至缺氮BBM培养基中,使MLT最终浓度为10 μmol/L,每组设3个平行样。以0.4 vvm/min的速度通入无菌空气,光照10 000 lx,温度保持在(27±1) ℃,室内培养13 d。每隔1天进行取样,测定H. pluvialis LUGU生物量、虾青素含量及油脂含量。
1.2 雨生红球藻细胞生物量浓度、虾青素和脂质含量的测定
为测定H. pluvialis LUGU的干细胞重量(DCW),每隔1天取10 mL的诱导藻液,在3 800×g离心5 min,所获沉淀用蒸馏水洗涤2次,收集沉淀,置于EP管中,储存于-20 ℃,冷冻干燥并称重。
利用高效液相色谱(HPLC)测定虾青素含量。取各干燥样品10 mg,充分研磨,然后用丙酮:氯仿(1∶1,体积比)溶液提取干藻粉中的虾青素, 4 ℃条件下,12 000 r/min离心5 min。多次重复此过程,至藻细胞变为白色。将提取后的溶液置于45 ℃真空干燥箱完全干燥。随后用1 mL甲醇:二氯甲烷(3∶1,体积比)溶液溶解干燥的提取物,HPLC上样检测。其中,HPLC条件为:流动相A为丙酮,流动相B是体积比为9∶1的甲醇∶水溶液。洗脱梯度为:B,80%~20%,25 min; B,20%,10 min; B,20%~80%,15 min;进样量20 μL,流速为1.25 mL/min;光谱扫描波长范围为250~700 nm,检测波长为476 nm。用液相色谱标准曲线计算虾青素质量浓度ρ(mg/L),虾青素含量为:
P(mg/g)=ρ(mg/L)/ DCW(g/L)
(1)
收集干藻粉,称取干藻粉-石英砂(1∶ 2, 质量比),研磨30 min,然后取1.0 g研磨好的干藻粉加入氯仿-甲醇(2∶ 1, 体积比),室温下振荡20 min。3 000 r/min离心10 min,收集上清,沉淀再用氯仿-甲醇(2∶1, 体积比)重复提取2~3次,然后合并多次提取有机相,40 ℃旋蒸,70 ℃干燥2 h,冷却至室温后称重。油脂含量按公式(2)计算:
油脂含量![]()
(2)
式中:WL,提取的总脂质量,g;WA,藻粉干质量,g。
1.3 ROS、酶活及MDA的测定
利用2′,7′-二氯荧光素二乙酸酯(DCFH-DA)测定雨生红球藻细胞内ROS含量[18]。DCFH-DA作为荧光探针,本身不具有荧光性,透过雨生红球藻细胞膜被细胞内的酯酶水解成非荧光的二氯荧光黄(DCFH),当ROS存在时, DCFH被氧化为不能透过细胞膜的绿色荧光物质DCF。
取微藻培养液5 mL,调整细胞浓度为1×106 cells/mL,离心后弃去上清液,将1 mL 10 μmol/L CFH-DA添加至培养基中,避光于37 ℃摇床中振荡反应30 min,离心弃上清液,使用PBS缓冲液洗涤2次以除去未反应的DCFH-DA,使用荧光分光光度计进行测量,激发波长488 nm,发射波长500~600 nm,测定细胞内ROS水平。
用总超氧化物歧化酶测定试剂盒(beyotime,China)测定超氧化物歧化酶(SOD)的活性,CAT和POD的活性分别利用过氧化氢酶试剂盒(beyotime,China)和过氧化物酶试剂盒(Beyotime,China)进行测定。脂质过氧化产物(MDA)的含量是根据Heath和Parker的研究方法进行测定[19]。
1.4 RNA提取和实时荧光定量PCR(qRT-PCR)扩增
使用Trizol试剂提取总RNA。首先液氮研磨微藻样品,刮1~2勺研磨好的藻粉到已加入1 mL Trizol的1.5 mL EP管中,盖好盖子,摇晃均匀,室温下静置5 min,然后在4 ℃,12 000 r/min条件下离心10 min;将上清液转移到新的EP管中,加0.2 mL氯仿,剧烈摇晃15 s,室温放置2~3 min,在4 ℃,12 000 r/min条件下离心15 min,并吸取上清液至新的EP管中;加入等体积的异丙醇,轻轻混匀,室温静置培养10 min,然后在4 ℃,12 000 r/min条件下离心10 min,离心后将除管底白色固体外的液体用枪吸除,加入1 mL 75%的乙醇,涡旋振荡2~3 min,在4 ℃,12 000 r/min条件下离心5 min,再次将除管底白色固体外的液体用枪吸除,剩余晾干;晾干后加入30~50 μL Rnase-free水,用枪轻轻吹打混匀,将57 μL水加入PCR管中,再加入3 μL RNA,以备RNA浓度测定,将原RNA液体放置于-80℃待逆转录。然后用RT-PCR试剂盒(Takara)对1 μg RNA进行反转录,再进行qRT-PCR扩增,使用ABI 7500荧光定量仪分析bkt和fad相对转录水平。表1为内参基因18 S、bkt、fad的荧光定量引物。其中内参基因的作用即作为内标以调节RNA的用量和循环数,使内标基因在诱导条件下的表达丰度一致。qRT-PCR数据结果用2-ΔΔCt的方法进行分析。
表1 酶基因荧光定量引物

1.5 统计分析
每组试验设置3个平行,采用ANOVA(SPSS 20.0)一步法分析所得试验数据。最小显著性差异进行多重比较,检验调查不同试验的组间差异,当p<0.05时具有显著性意义,p<0.01具有极显著性意义。
2 结果与讨论
2.1 MLT对H.pluvialis生物量及虾青素含量的影响
环境胁迫条件下,雨生红球藻细胞生物量会受到影响。图1-a显示,随着培养时间的延长,对照组和褪黑素诱导组的生物量浓度均逐渐增加,但增长缓慢,至第13 d分别达到最大值0.61和0.59 g/L,外源MLT并不能促进藻细胞的生长。此外,李大菲等[20]也得到相同的结果,褪黑素对单针藻Monoraphidium sp. QLY-1细胞生长未表现出积极作用。
雨生红球藻在胁迫条件下会大量积累虾青素。如图1-b所示,在13 d的诱导过程中,对照组虾青素含量逐步增加并最终达到最大值14.36 mg/g。而褪黑素作为一种信号分子和抗氧化剂,其外源添加显著促进了雨生红球藻虾青素含量的提高。随着培养时间的延长,褪黑素处理组虾青素含量逐渐升高,且相对于对照组来说,增长速率也在不断提高,至第13天虾青素含量达到最大值32.37 mg/g,是对照组的2.25倍。由此可知,胁迫条件下,添加外源MLT虽然对微藻生长没有促进作用,但可以显著提高雨生红球藻中虾青素积累。这与先前报道的诱导策略相比,如添加H2O2、叔丁基羟基茴香醚(BHA)诱导或采用不同光照强度,获得了更高的虾青素积累量[21-22]。
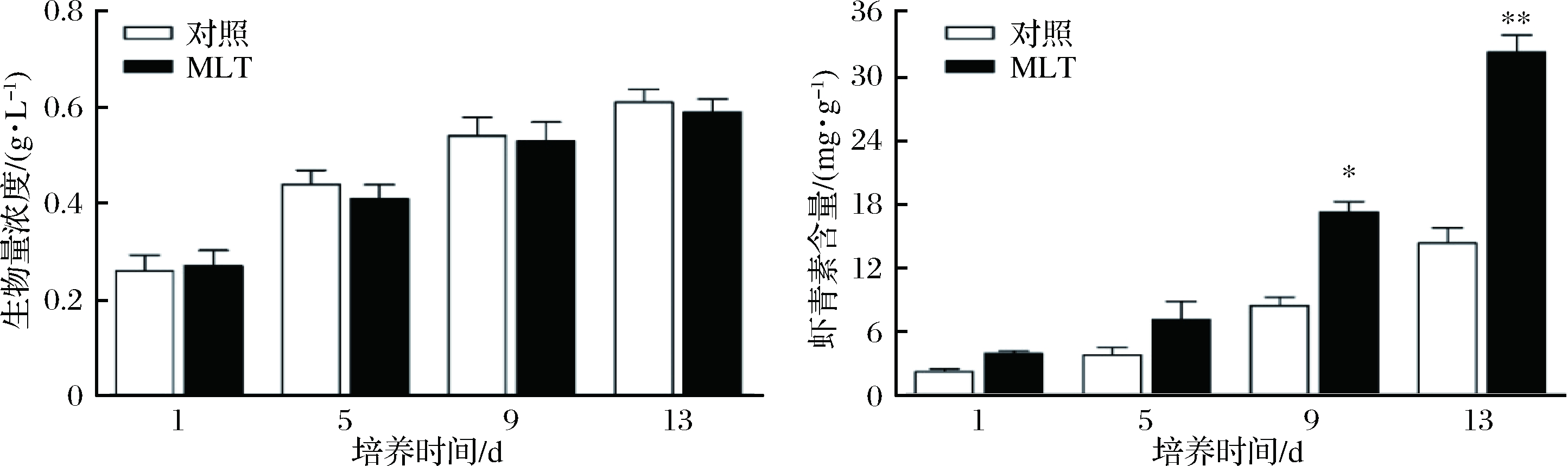
图1 (a)MLT对雨生红球藻生长的影响;(b)MLT对雨生红球藻虾青素含量的影响
Fig.1 (a)Effect of MLT on the growth of H. pluvialis;(b)Effects of MLT on astaxanthin content of H. pluvialis 注:*表示同一时间与其他组差异显著(p<0.05); **表示同一时间与其他组差异极显著(p<0.01。
2.2 MLT对H.pluvialis LUGU脂质含量的影响
KARSTEN[12]研究发现,在高等植物代谢过程中,类胡萝卜素主要储存在叶绿体等质体内,而雨生红球藻合成的 95%的虾青素与脂肪酸发生酯化反应,储存在富含有甘油三酯的脂囊泡中[23]。因此雨生红球藻虾青素的积累与脂质合成密切相关。外源MLT对H. pluvialis脂质含量的影响如图2所示。在13 d的诱导过程中,脂质含量逐渐增加,且与虾青素积累量增加的趋势一致。MLT诱导组中,脂质最高含量达到42.84%,是对照组(35.19%)的1.22倍。结果表明,褪黑素诱导促进了脂质的生物合成。这可能是由于褪黑素作为一种诱导剂,增加了脂质的合成,从而促进了虾青素的酯化存储,减轻了游离虾青素的产物抑制作用[23];另外,作为一种抗氧化剂,褪黑素可以防止脂质过氧化反应,并维持雨生红球藻细胞生物膜的正常功能,保持了细胞正常代谢活性[24]。
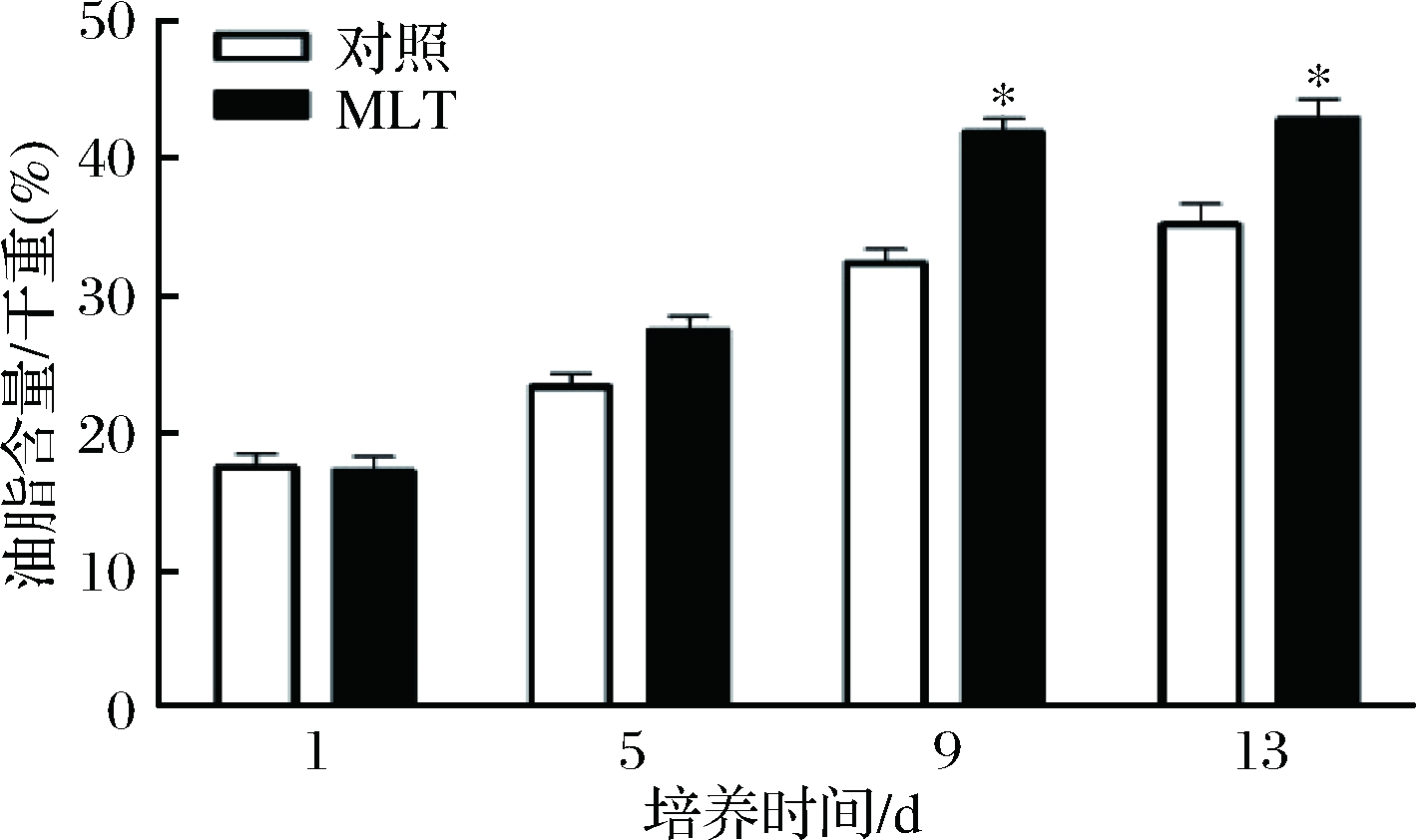
图2 MLT对雨生红球藻脂质含量的影响
Fig.2 Effects of MLT on lipid content of H. pluvialis 注:*为同一时间与其他组差异显著(p<0.05); **为同一时间与其他组差异极显著(p<0.01)。
2.3 MLT对H.pluvialis LUGU细胞内ROS水平、抗氧化酶活及MDA含量的影响
ROS是在多种生物细胞中均存在的一种重要的信号分子,其对雨生红球藻虾青素合成的促进作用已经被证明[25]。然而,ROS能与细胞内DNA、脂质和蛋白质等一些主要的大分子发生反应,导致细胞损伤[26-27]。雨生红球藻细胞中存在酶系和非酶系两套自由基清除系统,以应对生物或非生物胁迫产生的有毒化合物[28]。
如图3-a所示,在缺氮和高光胁迫条件下,对照组和褪黑素诱导组,培养初期ROS水平均表现为逐渐升高趋势;但两组相互比较发现,在13 d的培养过程中,褪黑素组ROS水平均低于对照组,这可能是由于MLT作为一种抗氧化剂,可以清除藻细胞内产生的ROS,抑制ROS水平的升高。从第5天起,ROS水平开始急剧下降,这可能由于培养前期ROS水平的升高激活了藻细胞的酶促抗氧化防御系统,抗氧化酶活性的增强抑制了ROS水平的持续升高。该研究测定了SOD、CAT和POD 3种重要抗氧化酶的活性。如图3-b所示,SOD活性在第5天时达到最高,同样的,CAT与POD活性也在第5 d时达到最高,这与ROS水平在培养至第5 d时开始急剧下降相一致。然而, SOD、CAT和POD的活性在第9 d和第13 d出现了降低。这可能是由于藻细胞中酶系防御体系会对ROS的增加产生快速应答反应,但ROS造成的细胞损伤也是广泛的,随着时间的推移,蛋白质会被降解,因此酶活性降低;另外,细胞内ROS水平的升高通常会触发细胞自噬,这也使得部分细胞成分被降解[29]。
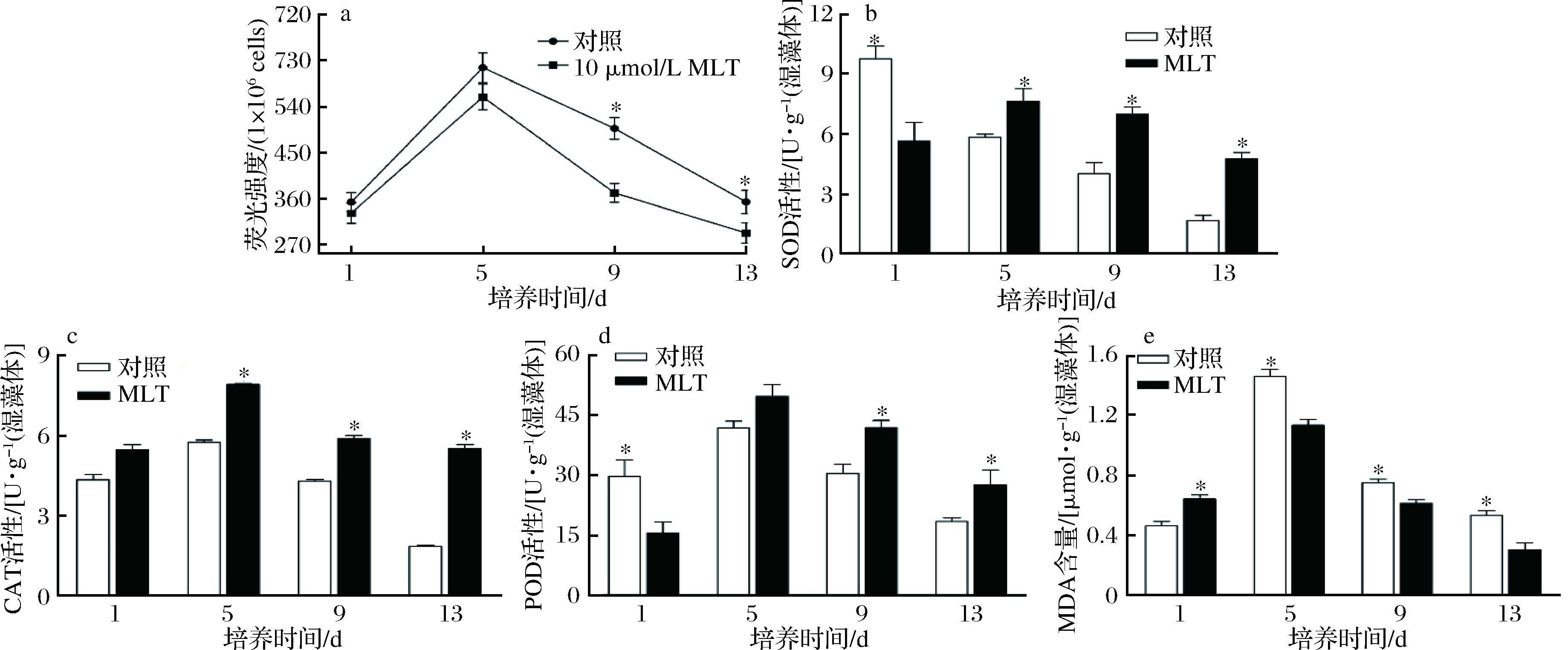
*为同一时间与其他组差异显著(p<0.05); **为同一时间与其他组差异极显著(p<0.01)
图3 (a) MLT对雨生红球藻细胞内ROS水平的影响(b) MLT对雨生红球藻细胞内SOD活性的影响(c)MLT对雨生 红球藻细胞内CAT 活性的影响(d)MLT对雨生红球藻细胞内POD活性的影响(e) MLT对雨生红球藻 细胞内MDA含量的影响
Fig.3 (a)Effects of MLT on ROS level in H. pluvialis cells (b) Effects of MLT on SOD activity in H. pluvialis cells (c) Effects of exogenous addition of MLT on CAT activity in H. pluvialis cells (d) Effects of MLT on POD activity in H. pluvialis cells (e) Effects of MLT on MDA content in H. pluvialis cells
MDA是细胞脂质过氧化反应的指标。图3-e显示,当雨生红球藻处于胁迫条件下时,MDA的含量升高,同时,对照组MDA含量比褪黑素诱导组表现出更快的增长,但在抗氧化酶及抗氧化物质的作用下,MDA的含量自第5 d起逐渐下降,并与ROS水平的下降和抗氧化酶活性的升高趋势保持一致。以上结果表明,褪黑素作为诱导剂,提高了抗氧化酶活性,显著升高了雨生红球藻抗氧化物—虾青素含量,对增强微藻应对氧化应激具有显著作用。
2.4 MLT对H.pluvialis LUGU虾青素合成相关基因及油脂合成相关基因表达的影响
非生物胁迫条件下外源添加化学调节剂或植物激素可上调微藻中与虾青素和脂质生物合成相关酶基因的表达水平,从而促进虾青素和油脂的合成[22]。为了确定褪黑素对雨生红球藻虾青素积累和脂质合成相关基因的相对转录水平的影响,在缺氮和高光胁迫条件下外源添加褪黑素诱导5 d和13 d后,对虾青素合成途径中关键基因bkt和脂质生物合成途径中关键基因fad表达量进行了测定。
如图4-a所示,外源添加褪黑素提高了bkt的转录水平。在第5 d,褪黑素诱导组中bkt基因表达量相比对照组提高了0.37倍;而在第13 d,bkt达到最大转录水平,为对照组的1.55倍。此外,如图4-b显示,外源添加褪黑素同样提高了fad的转录水平。在诱导第5 d, fad表达水平比对照组提高了2.54倍;第13 d,提高了1.52倍。这些结果与虾青素积累量和脂质合成水平的增长趋势是一致的。
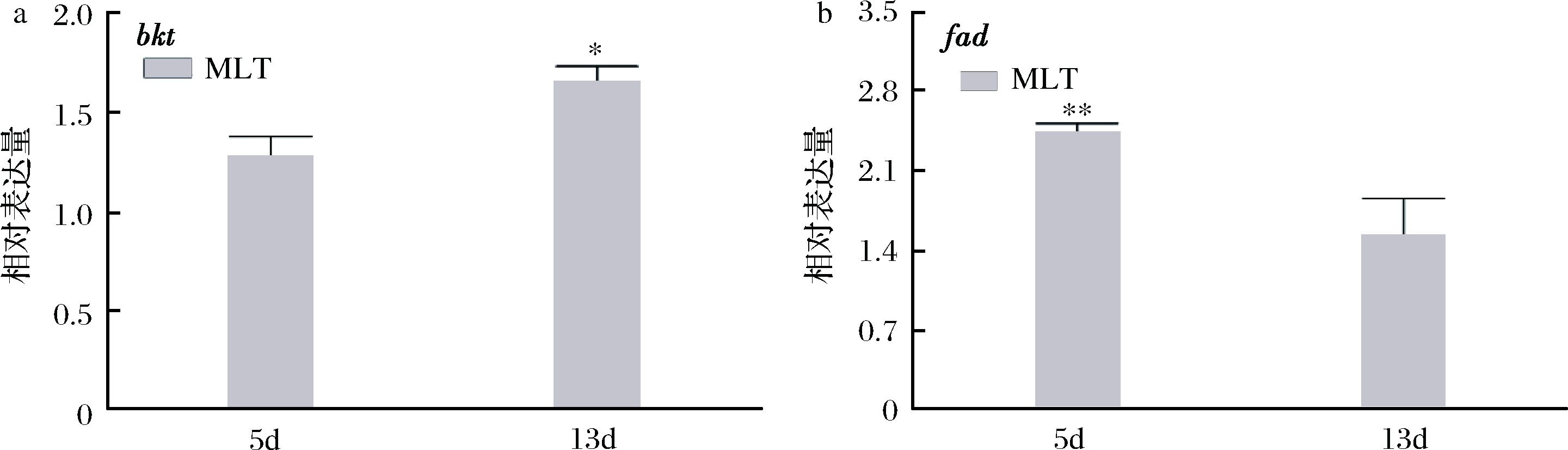
图4 (a)MLT对雨生红球藻虾青素合成关键基因bkt的影响(b)MLT对雨生红球藻脂质合成关键基因fad的影响
Fig.4 (a) Effects of MLT on the key gene bkt of astaxanthin synthesis in H. pluvialis cells (b) Effects of MLT on the key gene fad of lipid synthesis in H. pluvialis cells 注:*为同一时间与其他组差异显著(p<0.05); **为同一时间与其他组差异极显著(p<0.01)。
高政权[30]等的研究表明,外源添加植物激素SA(水杨酸)和JA(茉莉酸),均能显著提高虾青素合成途径中关键酶基因bkt的转录水平,从而促进虾青素的合成。LI[31]等研究也表明,褪黑素能够通过提高Monoraphidium中脂质合成相关基因的表达水平来增加细胞内脂质含量。本研究也得到了同样的结果,外源MLT可以显著提高H. pluvialis虾青素积累与脂质积累关键基因的表达水平,从而提高虾青素与油脂的积累量。
3 结论
在高光照联合缺氮胁迫条件下,外源添加MLT对雨生红球藻的生长无显著影响,但显著提高了虾青素积累量和油脂合成水平。另外,MLT抑制了细胞内信号分子ROS的水平,并提高了抗氧化酶SOD、CAT和POD的活性;虾青素积累相关酶基因bkt和油脂合成相关酶基因fad表达量提高。这些变化均与藻细胞中虾青素的积累密切相关。作为抗氧化剂和信号分子,虽然MLT诱导增加了雨生红球藻虾青素生物合成,但其作为信号分子,对藻细胞虾青素合成相关信号转导途径的作用还有待进一步深入研究。
参考文献
[1] 魏东,严小君. 天然虾青素的超级抗氧化活性及其应用[J]. 中国海洋药物, 2001, 20(4):45-50.
[2] 殷青青. 胰岛素抵抗大鼠脑组织损伤机制以及番茄红素的保护作用研究[D]. 济南:山东大学, 2015.
[3] HIGUERA-CIAPARA I, FELIX-VALENZUELA L, GOYCOOLEA F M. Astaxanthin: a review of its chemistry and applications[J]. Critical Reviews in Food Science and Nutrition, 2006, 46(2): 185-196.
[4] 张晓燕,刘楠,周德庆. 天然虾青素来源及分离的研究进展[J]. 食品与机械, 2012, 28(1):264-267.
[5] POONKUM W, POWTONGSOOK S, PAVASANT P. Astaxanthin induction in microalga H. pluvialis with flat panel airlift photo bioreactors under indoor and outdoor conditions[J]. Preparative Biochemistry & Biotechnology, 2015, 45(1): 1-17.
[6] NAGUIB Y M A. Antioxidant activities of astaxanthin and related carotenoids[J]. Journal of Agricultural and Food Chemistry, 2000, 48(4): 1 150-1 154.
[7] WU Y H, YANG J, HU H Y, et al. Lipid-rich microalgal biomass production and nutrient removal by Haematococcus pluvialis in domestic secondary effluent[J]. Ecological Engineering, 2013, 60: 155-159.
[8] HAGEN C, ![]() K,
K, ![]() M, et al. Effect of cultivation parameters on growth and pigment biosynthesis in flagellated cells of Haematococcus pluvialis[J]. Journal of Applied Phycology, 2001, 13(1): 79-87.
M, et al. Effect of cultivation parameters on growth and pigment biosynthesis in flagellated cells of Haematococcus pluvialis[J]. Journal of Applied Phycology, 2001, 13(1): 79-87.
[9] SU Y, WANG J, SHI M, et al. Metabolomic and network analysis of astaxanthin-producing Haematococcus pluvialis under various stress conditions[J]. Bioresource Technology, 2014, 170: 522-529.
[10] LEMOINE Y, SCHOEFS B. Secondary ketocarotenoid astaxanthin biosynthesis in algae: A multifunctional response to stress[J]. Photosynthesis Research, 2010, 106(1-2): 155-177.
[11] GAO Z Q, MENG C X, CHEN Y C, et al. Comparison of astaxanthin accumulation and biosynthesis gene expression of three Haematococcus pluvialis strains upon salinity stress[J]. Journal of Applied Phycology, 2015, 27(5): 1853-1860.
[12] HOLTIN K, KUEHNLE M, REHBEIN J, et al. Determination of astaxanthin and astaxanthin esters in the microalgae Haematococcus pluvialis by LC-(APCI) MS and characterization of predominant carotenoid isomers by NMR spectroscopy[J]. Analytical and Bioanalytical Chemistry, 2009, 395(6): 1 613-1 622.
[13] LEMER A B, CASE J D, TAKAHASHI Y, et al. Isolation of melatonin, the pineal gland factor that lightens melanocyteS1[J]. Journal of the American Chemical Society, 1958, 80(10): 2 578-2 587.
[14] WANG Y P, REITER R J, CHAN Z L-long. Phytomelatonin: A universal abiotic stress regulator[J]. Journal of Experimental Botany, 2017, 69(5): 963-974.
[15] 姜超强,祖朝龙. 褪黑素与植物抗逆性研究进展[J]. 生物技术通报, 2015, 31(4): 47-55.
[16] 徐向东,孙艳,郭晓芹,等. 褪黑素对高温胁迫下黄瓜幼苗抗坏血酸代谢系统的影响[J]. 应用生态学报, 2010, 21(10):2 580-2 586.
[17] ZHAO Y T, SHANG M M, XU J W, et al. Enhanced astaxanthin production from a novel strain of Haematococcus pluvialis using fulvic acid[J]. Process Biochemistry, 2015, 50(12): 2 072-2 077.
[18] CHE R Q, DING K, HUANG L, et al. Enhancing biomass and oil accumulation of Monoraphidium sp. FXY-10 by combined fulvic acid and two-step cultivation[J]. Journal of the Taiwan Institute of Chemical Engineers, 2016, 67: 161-165.
[19] HEATH R L, PACKER L. Photoperoxidation in isolated chloroplasts: I. Kinetics and stoichiometry of fatty acid peroxidation[J]. Archives of Biochemistry and Biophysics, 1968, 125(1): 189-198.
[20] 李大菲,赵永腾,余旭亚. 褪黑素对单针藻油脂积累的影响[J]. 水生生物学报, 2018, 42: 423-429.
[21] YU X H, NIU X F, ZHANG X Q, et al. Identification and mechanism analysis of chemical modulators enhancing astaxanthin accumulation in Haematococcus pluvialis[J]. Algal Research, 2015, 11: 284-293.
[22] MA R, THOMAS-HALL S R, CHUA E T, et al. Gene expression profiling of astaxanthin and fatty acid pathways in Haematococcus pluvialis in response to different LED lighting conditions[J]. Bioresource Technology, 2018, 250: 591-602.
![]() K, HIRSCHBERG J, HAGEN C. Ketocarotenoid biosynthesis outside of plastids in the unicellular green alga Haematococcus pluvialis[J]. Journal of Biological Chemistry, 2001, 276(8): 6 023-6 029.
K, HIRSCHBERG J, HAGEN C. Ketocarotenoid biosynthesis outside of plastids in the unicellular green alga Haematococcus pluvialis[J]. Journal of Biological Chemistry, 2001, 276(8): 6 023-6 029.
[24] 刘月,寇从贤,付桂萍,等. 褪黑素对大豆幼苗盐害的缓解效应及机理研究[J]. 中国油料作物学报, 2017, 39(6):813-819.
[25] ANDREEV I M. The vacuolar symplast: Does it really exist in plants? (comments on publications of G A Velikanov et al. in Russian Journal of Plant Physiology)[J]. Russian Journal of Plant Physiology, 2008, 55(6):843-845.
[26] IP P F, CHEN F. Employment of reactive oxygen species to enhance astaxanthin formation in Chlorella zofingiensis in heterotrophic culture[J]. Process Biochemistry, 2005, 40(11): 3 491-3 496.
[27] ZHENG Y H, LI Z, TAO M, et al. Effects of selenite on green microalga Haematococcus pluvialis: Bioaccumulation of selenium and enhancement of astaxanthin production[J]. Aquatic Toxicology, 2017, 183: 21-27.
[28] LI Y T, SOMMERFELD M, CHEN F, et al. Consumption of oxygen by astaxanthin biosynthesis: aprotective mechanism against oxidative stress in Haematococcus pluvialis (Chlorophyceae)[J]. Journal of Plant Physiology, 2008, 165(17): 1 783-1 797.
[29] ZHANG Z, SUN D Z, CHENG K W, et al. Inhibition of autophagy modulates astaxanthin and total fatty acid biosynthesis in Chlorella zofingiensis under nitrogen starvation[J]. Bioresource Technology, 2018, 247: 610-615.
[30] 高政权,孟春晓,高宏正,等. 多种植物生长调节剂诱导雨生红球藻高效生产虾青素的研究[D]. 淄博:山东理工大学, 2015.
[31] ZHAO Y T, LI D F, XU J W, et al. Melatonin enhances lipid production in Monoraphidium sp. QLY-1 under nitrogen deficiency conditions via a multi-level mechanism[J]. Bioresource Technology, 2018, 259: 46-53.