热凝胶(curdlan)又称凝胶多糖、可德兰胶、可得然胶等,是一种由微生物产生的胞外多糖,以β-1,3-糖苷键连接而成的直链大分子,分子式为![]() 热凝胶不溶于水、乙醇和大多数有机试剂,可以溶解在pH>12的氢氧化钠、磷酸三钠等碱性溶液中;具有独特的热成胶性,60 ℃下加热能形成可逆的低固定胶,80 ℃下加热下能形成不可逆的高固定胶[3]。此外,热凝胶还具有抗脱水性[4]、持水性[5]、稳定性、成膜性,因此被广泛应用于食品、医药行业。但热凝胶在提取过程中易发生强度损失,加热后形成的凝胶也存在着脆性大,弹性小等问题。
热凝胶不溶于水、乙醇和大多数有机试剂,可以溶解在pH>12的氢氧化钠、磷酸三钠等碱性溶液中;具有独特的热成胶性,60 ℃下加热能形成可逆的低固定胶,80 ℃下加热下能形成不可逆的高固定胶[3]。此外,热凝胶还具有抗脱水性[4]、持水性[5]、稳定性、成膜性,因此被广泛应用于食品、医药行业。但热凝胶在提取过程中易发生强度损失,加热后形成的凝胶也存在着脆性大,弹性小等问题。
黄原胶是食品工业中主要的商业微生物聚合物之一,可溶于热水或冷水,分子质量可达到6 MDa,即使在非常低的浓度下也能产生高黏度溶液;对酶促降解具有很强的抵抗力,并且在很宽的pH和温度范围内都很稳定[6];能够与其他树胶(例如结冷胶、瓜尔胶和刺槐豆胶)协同相互作用[7-9]。因此,将黄原胶和次级多糖组合使用,在食品工业中运用广泛[10-11]。
由于各种食品胶的来源、生产工艺和结构的差异,他们各自具有不同的性质和功能。但是单一的食品胶应用具有局限性,实际应用中通常需将2种胶体复配,达到协同作用以弥补各自的缺陷。热凝胶加热后形成的凝胶弹性小,脆性大,黄原胶常与其他胶体协同互用且价格低廉。目前的胶体复配研究仅限于成品之间的复配,且大多是机械的混匀,所产生的结合胶结构可能不稳定,并且不能大规模生产,在实际应用中存在局限性。本文研究一种新型凝胶的生产工艺,在热凝胶酸碱提取工艺[12]的碱溶这一步骤,添加黄原胶,通过对黄原胶添加比例、碱溶浓度和碱溶搅拌时间3个方面进行优化,确定提取工艺,为新型凝胶的工业化生产奠定理论基础。
1 材料与方法
1.1 材料与仪器
热凝胶发酵沉淀,实验室通风发酵所得;黄原胶,食品级;其他试剂均为分析纯,上海国药基团。
85-2数显恒温磁力搅拌器,金坛市良友仪器公司;T18数显型高速均质机,德国IKA公司;Haake Mars Ⅲ流变仪,美国赛默飞世尔科技;TA.XT Plus质构仪,英国SMS公司;SC-25型电热恒温水浴锅,宁波新芝科技股份有限公司;Quanta 200扫描电子显微镜,荷兰Fei公司;NEXUS傅里叶变换红外光谱仪,美国Nicolet公司。
1.2 新型凝胶的提取工艺及优化方法
工艺流程如图1所示。
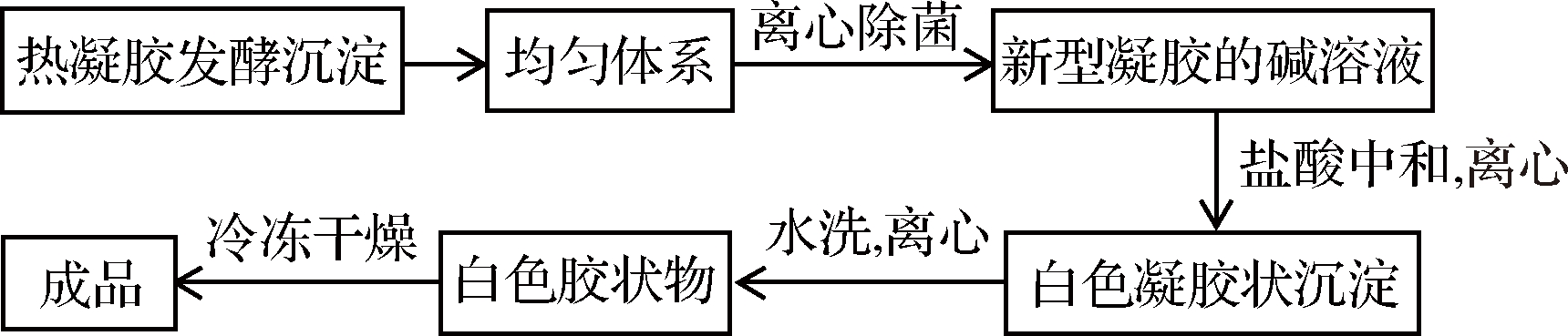
图1 新型凝胶提取工艺图
Fig.1 New gel extraction process diagram
从黄原胶添加比例、碱溶浓度和碱溶搅拌时间3个方面进行优化。将热凝胶与黄原胶的总质量浓度设为2 g/L,热凝胶与黄原胶的质量比分别为1∶0、2∶1、4∶1、6∶1、8∶1,碱溶浓度均为0.2 mol/L,搅拌时间均为6 h;碱溶浓度分别为0.2、0.4、0.6、0.8 mol/L,热凝胶与黄原胶质量比均为4∶1,搅拌时间均为6 h;搅拌时间分别为6、8、10、12 h,热凝胶与黄原胶比例均为4∶1,碱溶浓度均为0.2 mol/L。
1.3 分析方法
1.3.1 流变特性检测
动态黏弹性频率扫描方法参照蔡路军等[13]和CHANDRA等[14]的方法,并略做修改。将冷冻干燥后的产品配制成2%的均匀乳液,抽真空。在动态模式测试中,应变在1 Hz的恒定频率下从0.01%增加到10%,以确定线性黏弹区。确定线性黏弹区后,按照样品板温度25 ℃,转子型号P60 Ti L,间隙d=1 mm,应变为2%,频率f为1%~100%,进行动态频率扫描。
1.3.2 凝胶制备及质构特性检测
取冷冻干燥后产品,参照国家标准GB 28304—2012[15],制备凝胶。质构分析方法参照叶剑等[16]方法,并略作修改。采用TA.XT plus质构分析仪的压缩模式测定热凝胶的机械性能。探头型号为P/0.5R,测试前速度、测试时速度、测试后速度均为2 mm/s,目标模式为应变,压缩形变量为50%,测试时间5 s,触发力为2 g,得到全质构曲线[17-18]。
1.3.3 扫描电镜观察
扫描电镜观察参照WU[19]的方法,并略作修改。将提取得到的冻干样品固定至样品台,离子溅射仪镀膜,然后采用Quanta 200扫描电子显微镜进行显微观察并拍照,加速电压10.0 kV。
1.3.4 傅里叶红外光谱扫描
傅里叶红外光谱扫描参照文献[20]的方法,并略作修改。称取1~2 mg冷冻干燥样品与100 mg左右干燥的KBr粉末混合,在红外灯的照射下于玛瑙研钵中细细研磨至颗粒直径低于3 nm,然后将粉末经压片机压成薄片后上机测定。扫描波数范围4 000~400 cm-1,分辨率2.0 cm-1,采集样品的红外光谱图。
1.3.5 实验数据
采用Origin 8.5作图软件进行处理分析。
2 结果与讨论
2.1 提取条件对新型热凝胶流变性质的影响
2.1.1 热凝胶和黄原胶比例的影响
对凝胶体施加一个扭摆力矩,使胶体分子在此力矩下发生运动。当扭摆力矩的频率从低到高变化时,分子链的运动也会发生相应的变化,测其黏弹性。G′反应凝胶分子随外力的改变而发生的形变能力,G″反应凝胶分子随外力改变分子链内或分子之间拉伸导致的能力损耗[21-22]。图2显示了热凝胶和黄原胶比例对新型凝胶流变性质的影响。
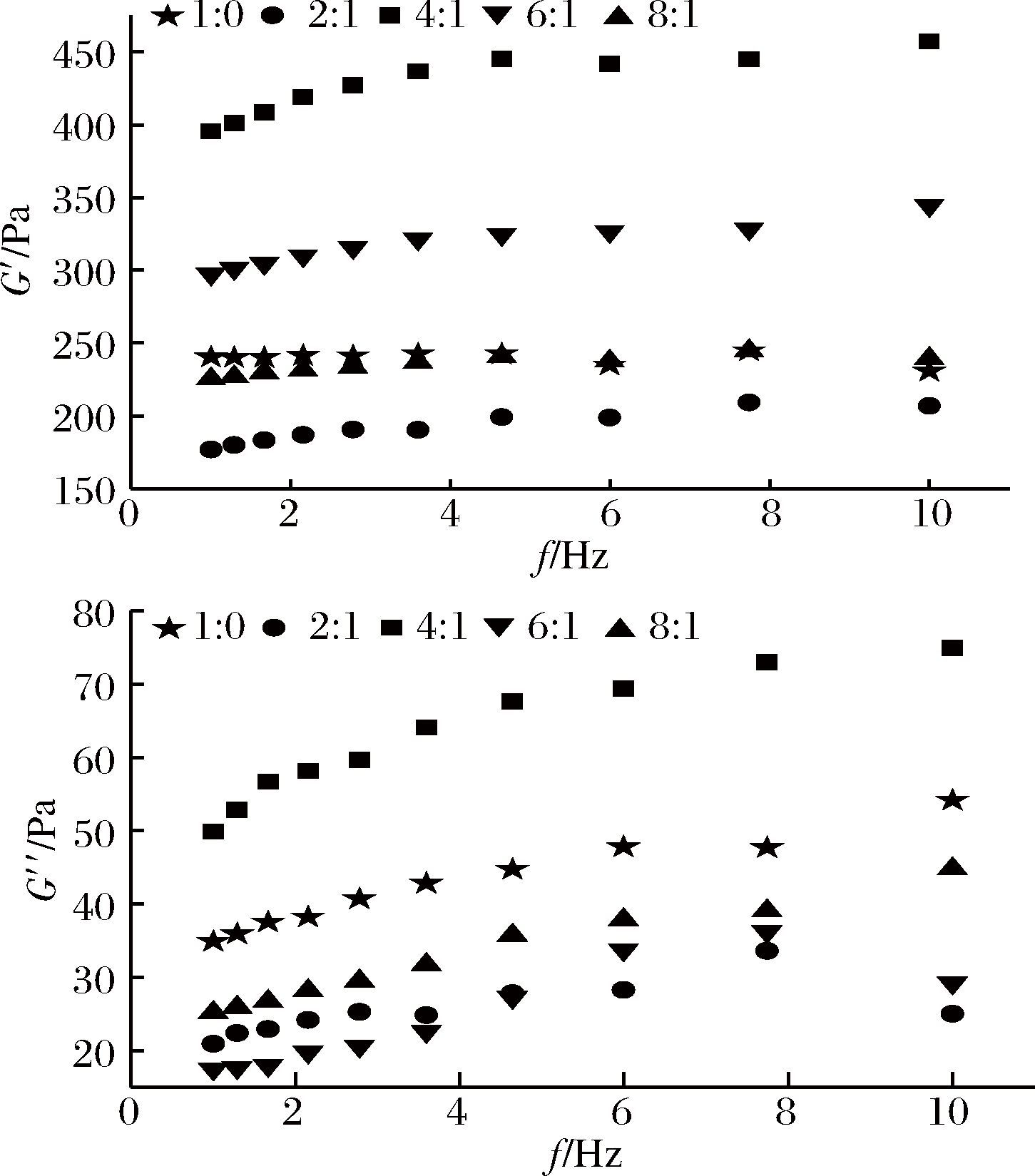
图2 不同黄原胶添加比例对新型凝胶的流变性质影响
Fig.2 Effect of different proportion of xanthan gum on rheological properties of new gels
如图2所示,新型凝胶储能模量G′随黄原胶添加量的增加呈现先增大后减小趋势,当热凝胶与黄原胶质量比为4∶1时,新型凝胶的储能模量G′达到最大,与未添加黄原胶的对照组相比,新型凝胶的G′增加了1倍,新型凝胶损耗模量G″随黄原胶添加量的增加呈现先减小后增大再减小的趋势,当热凝胶与黄原胶比例为4∶1时,新型凝胶损耗模量G″达到最大,与未添加黄原胶的对照组相比,G″几乎增加了3倍,即新型凝胶的黏性和弹性增加。说明此比例下添加的黄原胶与热凝胶存在协同增效作用,黄原胶分子与热凝胶分子之间结合效果最佳,产生了交联,形成了较稳定的网络结构,导致凝胶性能改善[23]。
从图2可知,在整个频率扫描过程中,G′和G″的变化趋势相同,G′始终是大于G″,体系一直以凝胶状态存在,不受黄原胶添加量的影响。
2.1.2 碱溶浓度的影响
图3显示了不同碱溶浓度对新型凝胶的流变性质影响。随着碱溶浓度的增加,新型凝胶的储能模量G′与损耗模量G″呈现先增加后减小的趋势,在碱溶浓度为0.4 mol/L条件下,新型凝胶的黏弹性最佳,与其他碱溶浓度所得新型凝胶相比,储能模量G′高5~8倍,损耗模量G″高5~10倍,这无疑给工业化生产提取时选取碱溶浓度提供了参考指标。
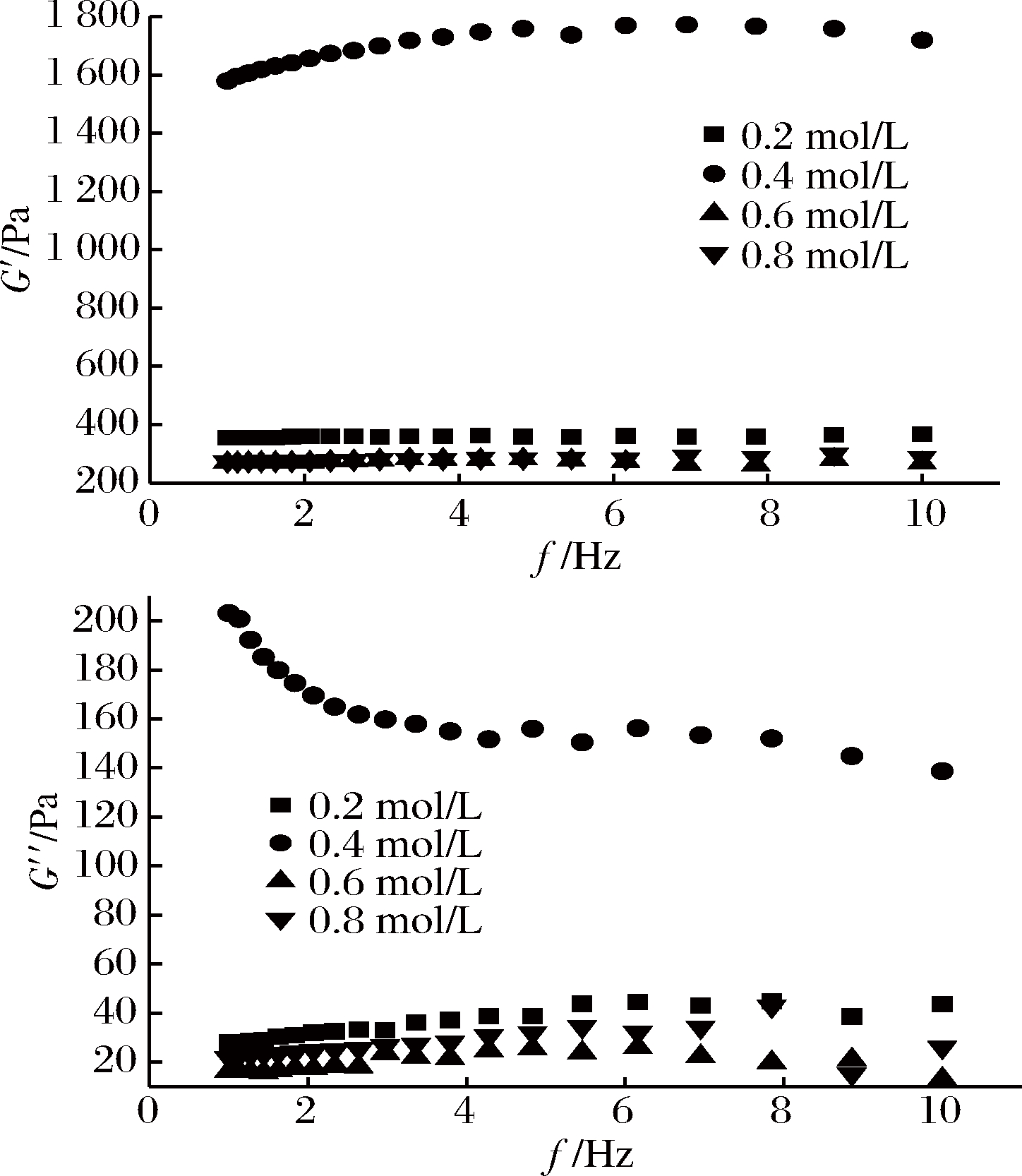
图3 不同碱溶浓度对新型凝胶流变性质的影响
Fig.3 Effect of different alkali soluble concentrations on the rheological properties of new gels
整个扫描过程中,G′和G″的变化趋势相同,G′始终大于G″,新型凝胶以弹性为主。G′随扫描频率增加略有变化,G″随扫描频率变化较大,说明扫描频率对新型凝胶的弹性影响较小,对其黏性影响较大。
2.1.3 搅拌时间的影响
图4显示了不同搅拌时间对新型凝胶的流变性质影响。随着搅拌的进行,新型凝胶的储能模量G′和损耗模量G″呈现明显先增大后减小的趋势,搅拌10 h,新型凝胶的储能模量G′和损耗模量G″达到最大,黏弹性质最佳,10 h后新型热凝胶的储能模量G′和损耗模量G″减小,黏弹性质下降。随着搅拌时间的进行,黄原胶与热凝胶氢键逐渐增加,当达到10 h后氢键数量趋于饱和,同时搅拌时间增长,搅拌所带来的机械力对凝胶本身具有破坏作用,这是导致上述结果的原因。
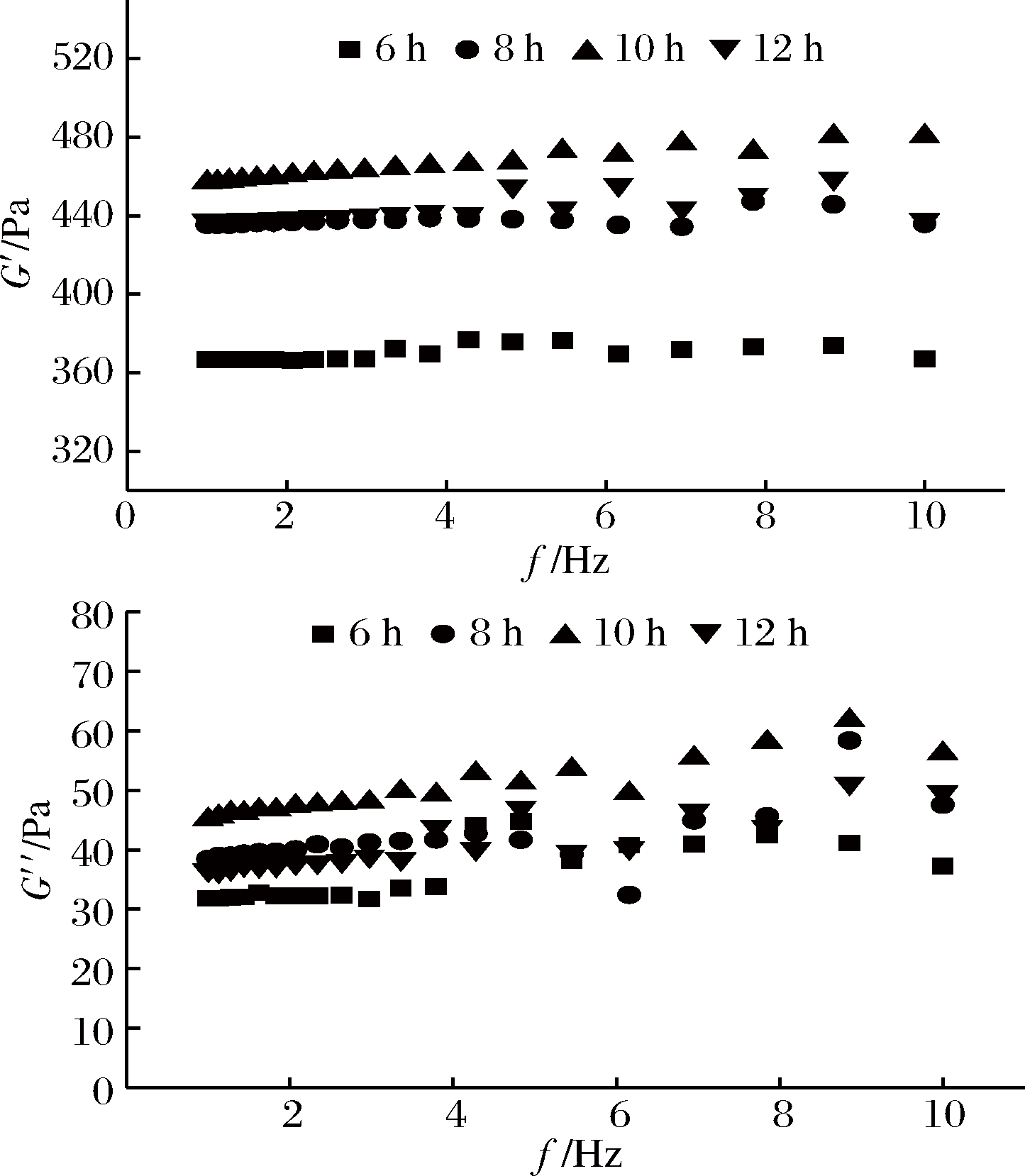
图4 不同搅拌时间对新型凝胶流变性质的影响
Fig.4 Effect of different mixing time on rheological properties of new gels
2.2 提取条件对新型凝胶质构性质的影响
2.2.1 热凝胶和黄原胶比例的影响
为了保证新型凝胶独特的热凝胶性,将黄原胶的添加量控制在50%以内,且碱溶浓度为0.2 mol/L,搅拌时间为6 h,热凝胶与黄原胶比例对新型凝胶的质构性质影响,如图5所示。

图5 热凝胶和黄原胶比例对新型凝胶的质构性质影响
Fig.5 Effect of thermal gel and xanthan gum ratio on texture properties of new gels
新型凝胶的硬度随黄原胶的添加量增加呈先增大后减小的趋势,当热凝胶与黄原胶的质量比为4∶1时,硬度达到最大,与对照组相比提升了1.4倍。新型凝胶的黏性随黄原胶添加量的增加呈现先减小后增大的趋势,当添加比例为4∶1时,黏性达到最大。新型凝胶的弹性随黄原胶添加量的变化无显著性变化,但相比对照组,都略有提升。另外新型凝胶的内聚性、回复性和咀嚼性随黄原胶添加量的增加呈现先减小后增大的趋势,当添加比例为4∶1时,3项性质达到最大。黄原胶添加质量比为4∶1时,所得到的新型凝胶其各项质构性质与对照组相比都有提升且达到最大值,黄原胶与热凝胶发生了交联反应,产生了稳定的网络结构,导致新型凝胶的质构性质增强,电镜结果也证实了这一结论。
2.2.2 碱溶浓度的影响
NaOH溶液是一种强烈的氢键破坏试剂,热凝胶溶于NaOH溶液后其分子由氢键连接而形成的有序结构被破坏,NaOH浓度越高对氢键破坏越严重,热凝胶分子的构象也随之发生相应的变化,其结构变化类似于蛋白质的变性过程,碱浓度越高,其螺旋结构越松散,最终会形成无规则卷曲的线性分子[24-25]。这也是选择在碱溶这一提取步骤添加黄原胶的原因,期望被碱溶成线性分子的热凝胶与黄原胶发生分子交联形成新型凝胶。结果如图6所示,当热凝胶与黄原胶的质量比为4∶1,搅拌时间6 h时,新型凝胶的硬度随着碱浓度增加呈下降趋势,这与叶剑等[16]研究热凝胶硬度随碱浓度增加线性下降的结论相似。但是在0.8 mol/L NaOH溶液浓度下,新型凝胶硬度有所回升,这是因为在高碱浓度下热凝胶的结构螺旋结构打开彻底,与黄原胶分子发生交联产生了较为稳定的网络结构使其凝胶强度回升。随着碱溶浓度的提高,黏性和弹性均无显著性变化,受碱溶浓度影响较小。另外咀嚼性与回复性随碱溶浓度提高呈下降趋势,但在0.6 mol/L NaOH溶液浓度下咀嚼性与回复性与0.2 mol/L NaOH溶液浓度相比有较大提升且此浓度下其内聚性也有较大提升。从上述结果发现碱溶浓度较高时,其硬度会降低,但咀嚼性、内聚性和回复性在0.6 mol/L NaOH溶液浓度下有较大提升,且在0.8 mol/L NaOH溶液浓度下,其硬度回升。选取0.2 mol/L NaOH溶液浓度为最佳提取碱溶浓度。

图6 碱溶浓度对新型凝胶的质构性质影响
Fig.6 Effect of alkali concentration on the texture properties of new gels
2.2.3 搅拌时间的影响
发酵液中的热凝胶是一种弱晶体,它的微粒结构为环形,和淀粉颗粒类似[26]。在溶解过程中搅拌可以加速微粒的扩散和断裂,使氢键更加快速和彻底地断裂,从而加速热凝胶的溶解,搅拌时间也是影响热凝胶质构性质的重要原因之一。如图7所示,当热凝胶与黄原胶的质量比为4∶1,碱溶浓度为0.2 mol/L时,新型凝胶的质构性质随搅拌时间发生规律性变化,随搅拌时间增加,新型热凝胶的硬度和黏性呈显著性增强趋势,当搅拌时间为10 h时硬度和黏性达到最大,分别提升了1.8倍和2倍,当搅拌时间为10 h后,硬度和黏度降低。弹性在搅拌时间10 h内无显著性变化,10 h后,弹性降低。另外咀嚼性和内聚性在搅拌时间为10 h时达到最大,回复性随搅拌时间增加呈显著性增强趋势。搅拌时间为10 h时,新型凝胶的综合质构性质最佳,随搅拌时间增加热凝胶的螺旋结构慢慢打开,此时黄原胶与热凝胶分子发生交联,在10 h时形成了稳定的网络结构使其质构性能达到最佳。

图7 搅拌时间对新型凝胶的质构性质影响
Fig.7 Effect of mixing time on the texture properties of new gels
2.3 扫描电镜结果分析
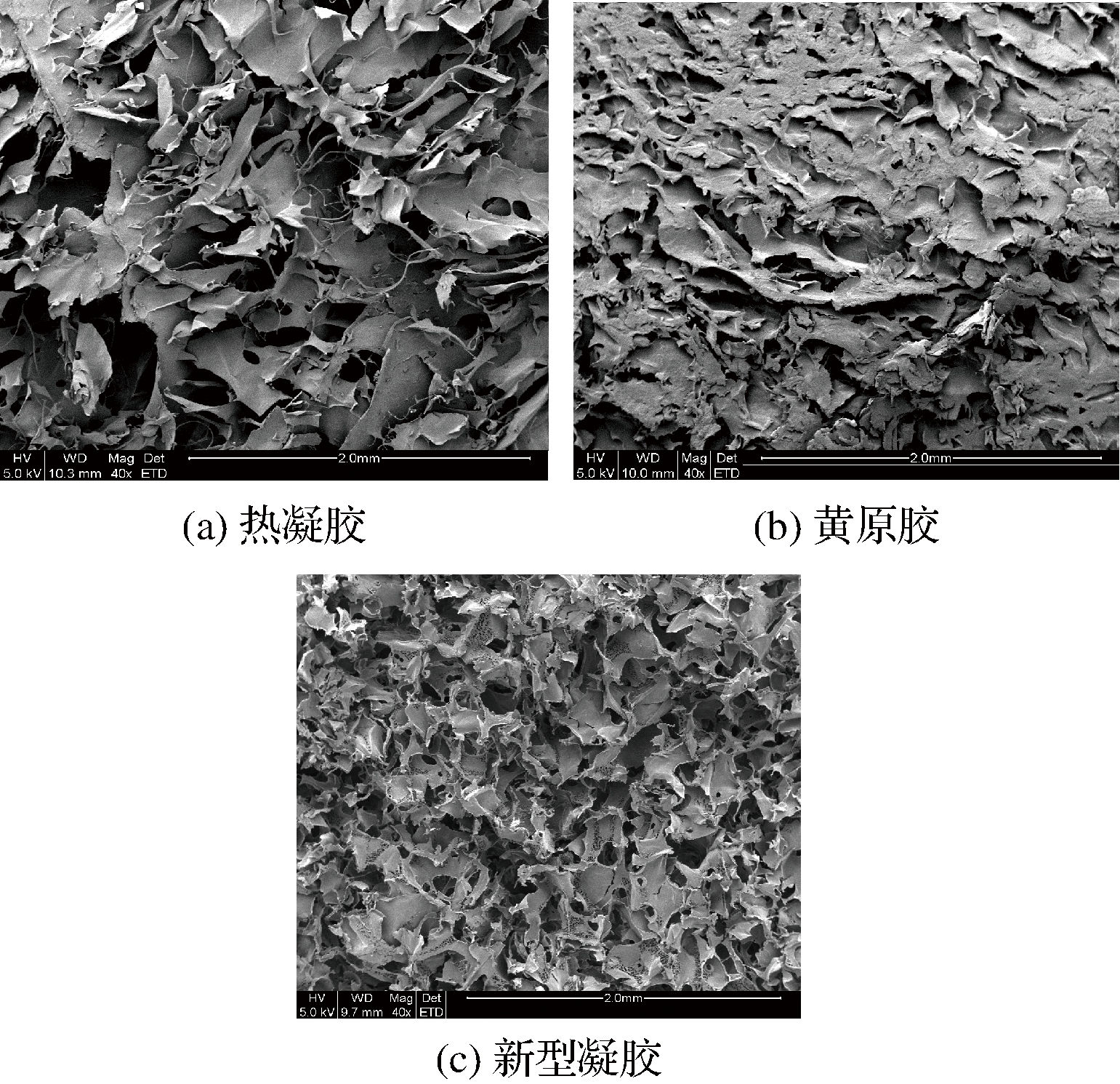
图8 热凝胶、黄原胶和新型热凝胶冻干后扫描电镜图
Fig.8 Scanning electron micrograph of curdlan, xanthan gum and new thermal gel after lyophilization
热凝胶、黄原胶和新型凝胶的扫描电镜结果如图8所示。从图8-a可观察到,热凝胶的微观结构呈现不规则的孔状结构,孔径较大,孔壁光滑较薄;图8-b黄原胶的微观结构也呈现不规则的孔状结构,但孔径较小,孔壁较厚;图8-c是在提取工艺条件为:m(热凝胶)∶m(黄原胶)=4∶1、碱溶浓度0.2 mol/L,搅拌时间10 h条件下所得到的新型凝胶微观结构图,与对照组相比,出现了致密性的网状结构,孔径变小,这一结构特征与新型凝胶质构,流变性质改善相一致。结果说明在提取过程中添加黄原胶,可以极大地改变热凝胶的性质。
2.4 红外光谱结果分析
热凝胶、黄原胶和新型凝胶的红外光谱如图9所示。热凝胶的羟基伸缩振动峰为3 295.12 cm-1,黄原胶的羟基伸缩振动峰为3 282.22 cm-1,新型凝胶的羟基振动峰分别为3 281.93 cm-1。采用优化的工艺[m(热凝胶)∶m(黄原胶)为4∶1,碱溶浓度0.2 mol/L,搅拌时间为10 h]得到的新型凝胶羟基伸缩振动峰波数最低,说明黄原胶分子与热凝胶分子发生交联,产生了协同增效作用,并形成了稳定的网络结构,这与上述的质构、流变和扫描电镜结果相吻合。
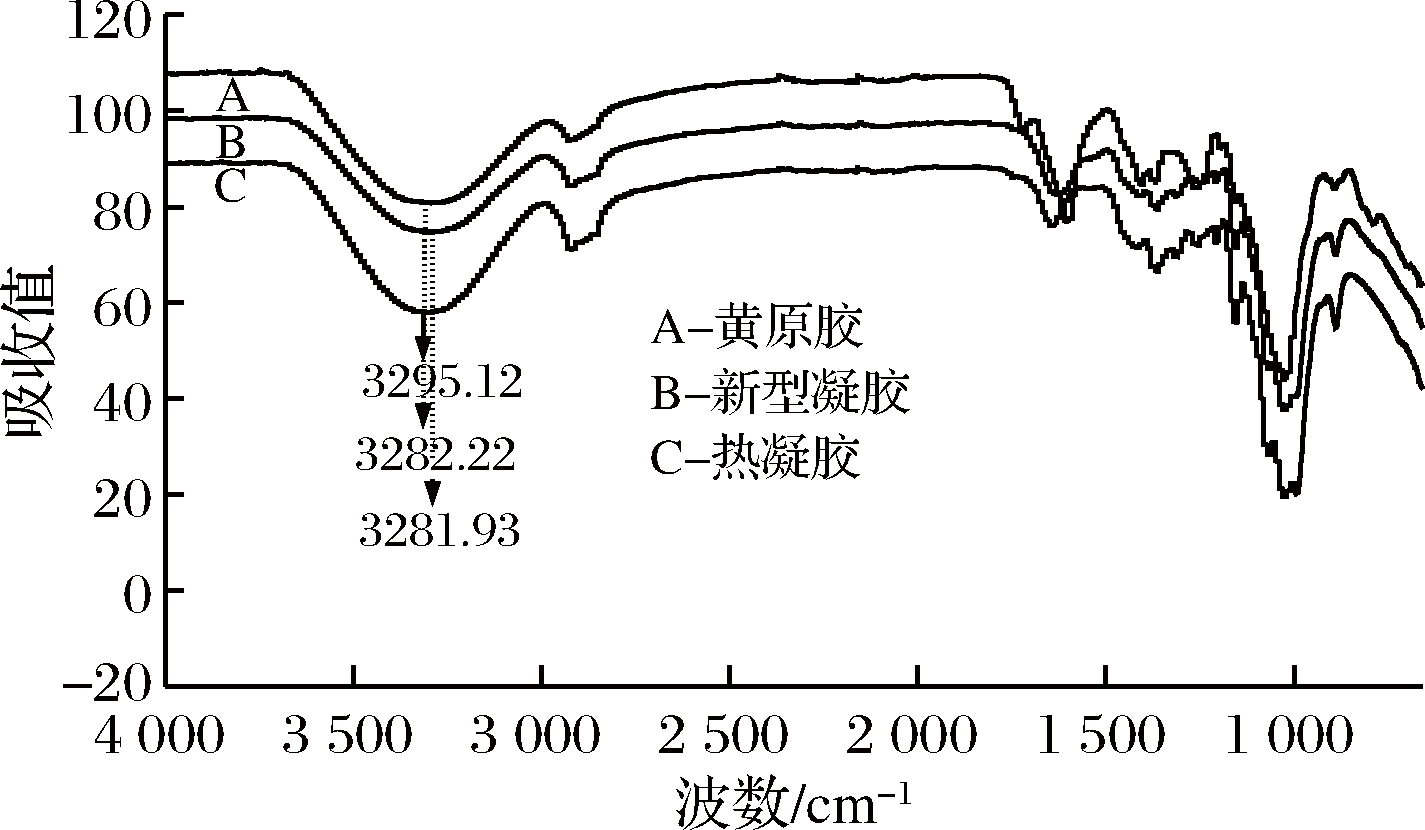
图9 热凝胶,黄原胶和新型凝胶冻干后红外光谱图
Fig.9 Infrared spectrum of curdlan, xanthan gum and new gel after lyophilization
3 结论
本文根据热凝胶在酸碱提取法碱溶这一步骤,三螺旋结构打开这一特点添加黄原胶,以质构和流变性质为考察指标,从黄原胶添加比例、碱溶浓度和搅拌时间3个方面进行优化,通过质构和流变性质分析,确定最佳生产工艺为:m(热凝胶)∶m(黄原胶)为4∶1,碱溶质量浓度0.2~0.4 mol/L,搅拌时间10 h。并利用扫描电镜和红外光谱对其结构分析,证实了最佳工艺下得到的新型凝胶形成了稳定的网络结构,黄原胶与热凝胶产生了协同增效作用。
[1] HARADA T, MASADA M, FUJIMORI K, et al. Production of a firm, resilient gel-forming polysaccharide by a mutant of Alcaligenes faecalis var. myxogenes 10C3 [J]. Journal of the Agricultural Chemical Society of Japan, 2008, 30(2): 196-198.
[2] HARADA T, YOSHIMUKA T, HIDAKA H, et al. Production of a new acidic polysaccharide, succinoglucan by Alcaligenes faecalis var. myxogenes [J]. Journal of the Agricultural Chemical Society of Japan, 1965, 29(8): 757-762.
[3] KANAMARU T, KIMURA H, SHIBATA M, et al. New thermo gelable polysaccharide containing foodstuffs: US, US 3754925 A[P]. 1973.
[4] ISHIDA K I, TAKEUCHI T. Starch to repress syneresis of curdlan gel[J]. Journal of the Agricultural Chemical Society of Japan, 1981, 45(6):1 409-1 412.
[5] KIMURA H, MORITAKA S, MISAKI M. Polysaccharide 13140: A new thermo-gelable polysaccharide[J]. Journal of Food Science, 2010, 38(4):668-670.
[6] PALANIRAJ A, JAYARAMAN V. Production, recovery and applications of xanthan gum by Xanthomonas campestris[J]. Journal of Food Engineering, 2011, 106(1):1-12.
[7] 朱桂兰, 陶思远,童群义. 结冷胶与黄原胶复配体系流变与凝胶特性[J]. 食品与发酵工业, 2013, 39(3):56-60.
[8] 朱慧, 吴伟都,潘永明,等. 黄原胶与阴离子瓜尔胶复配溶液的流变特性研究[J]. 中国食品学报, 2014, 14(5):55-62.
[9] 魏燕霞, 谢瑞,郭肖,等. 刺槐豆胶与黄原胶复配体系的流变性[J]. 食品科学, 2017, 38(1):149-153.
[10] WILLIAMS P D, OZTOP M H, MCCARTHY M J, et al. Characterization of water distribution in xanthan-curdlan hydrogel complex using magnetic resonance imaging, nuclear magnetic resonance relaxometry, rheology, and scanning electron microscopy[J]. Journal of Food Science, 2011, 76(6):7.
[11] SANDOLO C, CHIARA D, BULONE M R, et al. Synergistic interaction of locust bean gum and xanthan investigated by rheology and light scattering[J]. Carbohydrate Polymers, 2010, 82(3):733-741.
[12] 马立伟. 微生物多糖热凝胶高生产强度发酵工艺研究[D]. 无锡:江南大学, 2008.
[13] 蔡路昀, 冯建慧,聂小华,等. 草鱼皮明胶-可得然胶共混体系流变特性及作用机理的研究[J]. 食品工业科技, 2017,38(1):49-53.
[14] CHANDRA M V, SHAMASUNDAR B A. Rheological properties of gelatin prepared from the swim bladders of freshwater fish Catla catla[J]. Food Hydrocolloids, 2015, 48:47-54.
[15] 中华人民共和国卫生部.GB 28304—2012,食品安全国家标准食品添加剂可得然胶[S].2012.
[16] 叶剑,郑志永,詹晓北,等. 热凝胶在碱溶过程的流变学和质构学行为分析[J].食品与发酵工业,2018,44(11):82-88.
[17] 李里特. 食品物性学[M]. 北京:中国农业出版社, 2001.
[18] SINGH V, GUIZANI N, AL-ALAWI A, et al. Instrumental texture profile analysis (TPA) of date fruits as a function of its physico-chemical properties[J]. Industrial Crops & Products, 2013, 50(10):866-873.
[19] WU C, PENG S, WEN C, et al. Structural characterization and properties of konjac glucomannan/curdlan blend films[J]. Carbohydrate Polymers, 2012, 89(2):497-503.
[20] KUAN Y H, NAFCHI A M, HUDA N, et al. Effects of sugars on the gelation kinetics and texture of duck feet gelatin[J]. Food Hydrocolloids, 2016,58(7):267-275.
[21] VITURAWONG Y, ACHAYUTHAKAN P, SUPHANTHARIKA M. Gelatinization and rheological properties of rice starch/xanthan mixtures: Effects of molecular weight of xanthan and different salts[J]. Food Chemistry, 2008, 111(1):106-114.
[22] SEOK L J, KIM Y S, SONG K.Transient rheological behavior of natural polysaccharide xanthan gum solutions in start-up shear flow fields: An experimental study using a strain-controlled rheometer[J].Korea-Australia Rheology Journal, 2015, 27 (3):227-239.
[23] 朱桂兰,叶银杉,葛洁,等.低酰基结冷胶-果胶复配体系的性能[J].食品科学,2017,38(13):66-70.
[24] SAIT H. Conformation, dynamics, and gelation mechanism of gel-state (1→3)-β-D-glucans revealed by C-13 NMR[C] American Chemical Society, 1981:125-147
H. Conformation, dynamics, and gelation mechanism of gel-state (1→3)-β-D-glucans revealed by C-13 NMR[C] American Chemical Society, 1981:125-147
[25] TADA T, MATSUMOTO T, MASUDA T. Influence of alkaline concentration on molecular association structure and viscoelastic properties of curdlan aqueous systems[J]. Biopolymers, 2015, 42(4):479-487.
[26] KOREEDA A, HARADA T, OGAWA K, et al. Study of the ultrastructure of gel-forming (1→3)-β-D-glucan (curdlan-type polysaccharide) by electron microscopy[J]. Carbohydrate Research, 1974, 33(2):396-399.