鱿鱼俗称枪乌贼、柔鱼,营养价值高,可食用部分达到体质量的80%左右[1]。目前鱿鱼主要靠远洋运输,捕捞上来后为了减少品质的下降基本都会对鱿鱼进行冻结处理再冻藏。众所周知,冻结速率会影响通过最大冰晶生成带的时间、冰晶的大小和分布情况,进而影响蛋白质的变性程度[2]。因此,研究不同的冻结方式对鱿鱼品质的影响意义重大。
目前,已有大量关于冻结方式对鱼类品质影响研究。于刚等[3]研究了液氮冻结、冷冻液冻结、-18 ℃冰箱冻结和-80 ℃超低温冰箱冻结冻藏对黄鳍金枪鱼品质的影响;胡亚芹等[4]为了提高带鱼的品质,在冻藏前分别用液氮冻结、冰箱冻结和平板冻结新鲜的带鱼;方林等[5]研究了-40 ℃速冻、-20 ℃乙醇液体冻结和-20 ℃冰箱冻结对草鱼不同部位品质的影响。研究显示,冻结前对样品进行预处理会对鱼类品质有影响。AUBOURG等[6]曾用加高压的方法辅助大西洋鲭鱼的冻结。目前对水产品冻结方式的研究,主要集中在冰箱冻结、液氮冻结和平板冻结,而螺旋式速冻机和超低温冷库对水产品的冻结研究鲜有报道,但这2种速冻方式在现实生活、生产中却是很普遍的。
本实验以鱿鱼为实验对象,分别用-20 ℃冰箱、-30 ℃平板冻结、-35 ℃螺旋冻结、-60 ℃超低温冷库冻结4种冻结方式对鱿鱼样品进行冻结保鲜,并运用低场核磁共振技术(low field-nuclear magnetic resonance, LF-NMR)结合理化指标分析鱿鱼的品质变化。
1 材料与方法
1.1 材料与试剂
新鲜的鱿鱼购于上海市浦东新区芦潮港水产批发市场。选取同一批次且规格大体一致的产品,单体质量(420±30)g,用碎冰处理后置于泡沫箱中,运至实验室待处理。
二甲苯、KCl(分析纯)、无水乙醇、10%的福尔马林、苏木精染色液、伊红染色液、改良型Bradford法蛋白浓度测定试剂盒,生工生物工程(上海) 股份有限公司;丙二醛(malondialdehyde, MDA)测试盒,南京建成生物工程研究所。
1.2 仪器与设备
UV-1102型紫外可见分光光度计,上海天美仪器有限公司;H-2050R型台式高速冷冻离心机,湖南湘怡实验室仪器开发有限公司;CR-400型色彩色差计,日本柯尼卡美能达公司;TMS-Pro型质构仪,美国FTC公司;Fluke 2640A网络型多点温度采集仪,美国福禄克电子仪器仪表公司;Ellab热力验证系统,ETA10;螺旋式速冻机、平板速冻机,烟台冰轮股份有限公司;超低温速冻机[7](单机双级压缩系统);KK25F55TI型冰箱,德国西门子股份公司;testo 425热线风速仪,德图集团。
1.3 方法
1.3.1 原料的预处理
对照组使用新鲜的鱿鱼。用流动冷却水洗去鱼体表面杂质,对新鲜鱿鱼进行指标测定;在待冻结的鱿鱼几何中心位置插入测温探头后,分别放入-20 ℃冰箱、-30 ℃平板速冻机、-35 ℃螺旋速冻机(风速6.67 m/s)和-60 ℃超低温冷库(风速1.33 m/s)中进行速冻。速冻鱿鱼的几何中心温度达到-18 ℃时,立即取出样品,分装于标记好的自封袋中,放到-18 ℃的冰箱中贮藏(7 d),20 ℃流水解冻后进行指标测定。
1.3.2 冻结曲线的测定
在-20 ℃冰箱、-30 ℃平板冻结和-60 ℃超低温冷库冻结鱿鱼时,分别把热电偶的探头插入鱼样的中心位置,通过多点温度采集仪实时记录样品温度的变化,螺旋式冻结方式采用热力验证系统测温。
1.3.3 保水性指标的测定
冻结损失按公式(1)计算:
冻结损失![]()
(1)
式中:m1,冻前鱿鱼质量;m2,冻结之后的鱿鱼质量。
持水力的测定按公式(2)计算[8]:
持水力![]()
(2)
式中:m3,鱿鱼碎块离心前的质量;m4,鱿鱼碎块离心后的质量。
蒸煮损失率的测定:取鱿鱼样品(2 cm×2 cm×2 cm),在85 ℃的水浴锅中加热20 min后取出并冷却至室温,用吸水纸吸干鱿鱼表面的水分,按公式(3)计算鱿鱼的蒸煮率损失:
蒸煮损失率![]()
(3)
式中:m5,蒸煮前的鱿鱼样品质量;m6,蒸煮后鱿鱼样品的质量。
每组样品重复3次。
1.3.4 色泽的测定
用色差计测定解冻后鱿鱼的色差值L*,a*和b*,在鱼品测定前进行白板校正。每组重复3次取平均值。再根据公式(4)计算白度值:
W=100-[(100-L*)2+a*2+b*2]1/2
(4)
1.3.5 质构的测定
参考文献[9]的方法。
1.3.6 pH的测定
准确称取2 g鱿鱼样品,加入18 mL蒸馏水后机械匀浆,然后在1 000 r/min下离心10 min,用pH计测定上清液的pH值。每组重复3次,取平均值。
1.3.7 肌原纤维蛋白的提取
参考文献[10]的方法。
1.3.8 肌原纤维蛋白浓度
改良型Bradford法试剂盒测定蛋白浓度。
1.3.9 丙二醛(MDA)的测定
取解冻后鱿鱼2 g,按照1∶9(g∶mL)加入18 mL生理盐水,机械匀浆,以7 500 r/min离心10 min。采用丙二醛(MDA)测试盒法。
1.3.10 低场核磁共振实验
参考王硕等[11]的方法
1.3.11 微观结构观察
参考文献[12]的方法。
1.4 数据处理
各项指标均使用origin 8.5软件进行处理及绘图,使用SPSS 19.0软件进行分析。
2 结果与分析
2.1 鱿鱼在冻结过程中温度的变化
图1为鱿鱼在不同冻结方式下,从20 ℃到-18 ℃的温度变化曲线。通过最大冰晶生成带(-1~-5 ℃)的时间越短,生成的冰晶越小且越均匀,对冻品的品质影响越小[13]。
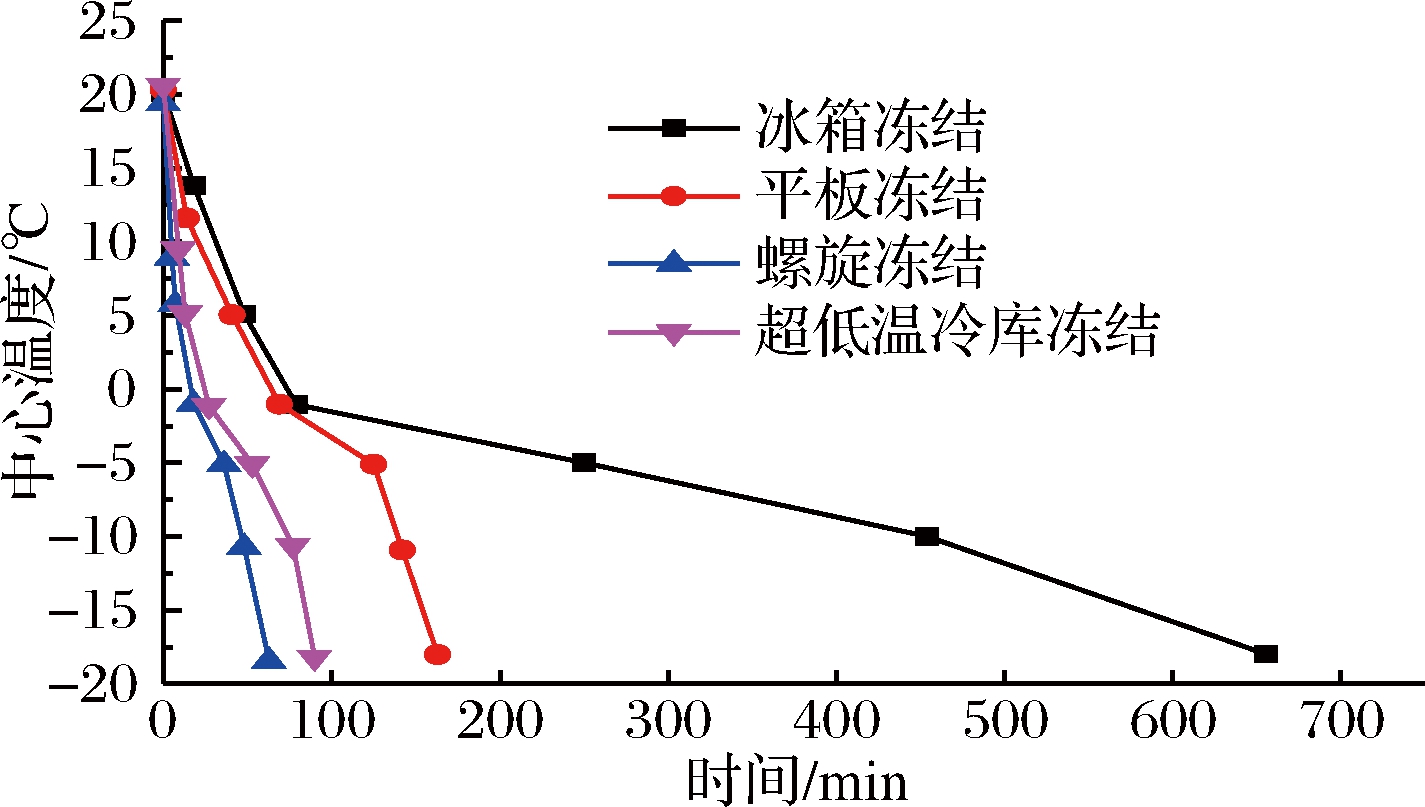
图1 不同冻结条件下鱿鱼的冻结曲线
Fig.1 Freezing curve of squid under different freezing methods
由图1可知,冰箱冻结、平板冻结、超低温冷库冻结和螺旋冻结的鱿鱼通过最大冰晶生成带的时间分别为171、56、26和18 min。超低温冷库冻结的温度比螺旋冻结温度低25 ℃,螺旋速冻机内部的风速是超低温冷库中的5倍,同时由于螺旋速冻传送带为网孔状,因此上下两侧都有空气流动,而超低温冷库为上侧强制对流换热,与搁架接触的为导热。平板冻结是将放在鱼盘内的鱿鱼压在两块导热板之间,靠导热的热传递方式使鱼冻结,而且平板速冻是先放置鱼样后开启制冷机组,与其他冻结方式先开启制冷机组,温度到达要求后再放入鱼样的操作不同,所以鱿鱼用平板冻结,通过最大冰晶生成带的时间也较长,同时冻结时中心温度达到-18 ℃所需的时间较长,为163 min。
2.2 鱿鱼在冻结过程中保水性的变化
鱿鱼在冻结过程中,体内的水分会逐渐形成冰晶,小冰晶的数量会因不断升华而减少,而大冰晶会逐渐长大,损伤肌肉组织结构,造成水分流失[14]。胡亚芹[4]认为,冰箱冻结时间长,冻结速率慢,形成的冰晶大,对肌肉组织结构的破坏大,比平板冻结的持水能力弱,这与表1显示的结论不一致,可能是因为在平板冻结过程中,由于鱿鱼受到挤压,表面的水分会被挤压出来,直接体现在冻结损失率(2.13%)上。同时肌肉组织结构由于挤压而受到破坏,也会对鱿鱼的持水能力造成影响,可以从表1中的持水力(64.98%)和蒸煮损失(45.81%)看出鱿鱼在平板冻结后保水性最差。
表1 不同冻结方式对鱿鱼保水性的影响
Table 1 Effect of different freezing methods on water holding capacity of squid
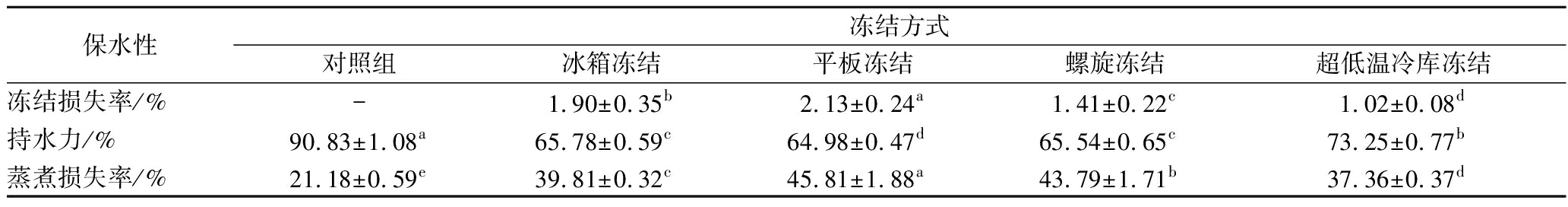
保水性冻结方式对照组冰箱冻结平板冻结螺旋冻结超低温冷库冻结冻结损失率/%-1.90±0.35b2.13±0.24a1.41±0.22c1.02±0.08d持水力/%90.83±1.08a65.78±0.59c64.98±0.47d65.54±0.65c73.25±0.77b蒸煮损失率/%21.18±0.59e39.81±0.32c45.81±1.88a43.79±1.71b37.36±0.37d
干耗现象是由于食品中水分蒸发或者升华造成的结果,合理的空气流速及分布可以减少干耗[15]。螺旋冻结过程中,由于风速较大,表面的水分会发生蒸发或者升华。同时食品在速冻过程中表面的冰层会阻碍内部冻结的体积膨胀,产生内应力,内应力还会因温度的不均而逐渐升高,到一定程度之后冻品的内部间隙或者薄弱部分会发生低温断裂现象,破坏细胞结构的完整性,在加热和离心下,水分流失更加明显,保水性更差[16]。LIU等[17]在研究海鲈鱼冻结过程中指出,速冻造成的低温断裂会降低水分含量,破坏细胞结构,影响食品品质。鱿鱼经超低温冷库冻结后在持水能力上与对照组最接近。
2.3 鱿鱼冻结后色泽的变化
鱿鱼在冻结过程中,色泽会因脂肪的氧化和色素的降解等一系列反应发生改变,影响消费者的可接受度。从图2可以看出,新鲜鱿鱼经过冻结处理后白度值升高,这是因为鱼肉在冻结过程中有冰晶生成,解冻之后肌肉组织中的游离水增加,鱼肉表面的反射光增强导致白度值的升高。随着冻结速率加快,L*值增加,a*和b*减少,白度值W越高[18],鱿鱼经螺旋速冻后的时间最短,白度值最大(67.16)。肌肉表面的色泽变化还与肌肉的保水性有关[19]。虽然平板冻结的速率远大于冰箱冻结,但是平板冻结的保水性最差,在这2种冻结方式下,鱿鱼的白度值差异不明显(P>0.05)。

图2 不同冻结方式对鱿鱼白度值的影响
Fig.2 Effect of different freezing methods on whiteness of squid
注:不同小写字母表示差异显著(P<0.05),下同。
2.4 鱿鱼在冻结过程中pH值的变化
pH值是衡量鱼肉品质的一个重要指标。通常情况下,水产品会因冻结和解冻导致蛋白质变性,pH值降低[20]。而鱿鱼随着贮藏时间的延长,pH值会呈现上升的趋势[21]。由图3可知,对照组的pH值是6.41,鱿鱼经过冻结和冻藏之后pH值会升高,但是经不同冻结方式后,鱿鱼pH值差异不明显,这与董佳等[22]的研究结论相似。可能是因为鱿鱼在冻结过程中生成冰晶破坏蛋白质,呈碱性的物质增加,pH值升高。球蛋白ATP酶和微生物的活性在低温条件下降低,蛋白质不能被分解成氨类物质,导致pH值变化不明显,而且pH值的变化与冻藏时间没有相关性[21,23]。
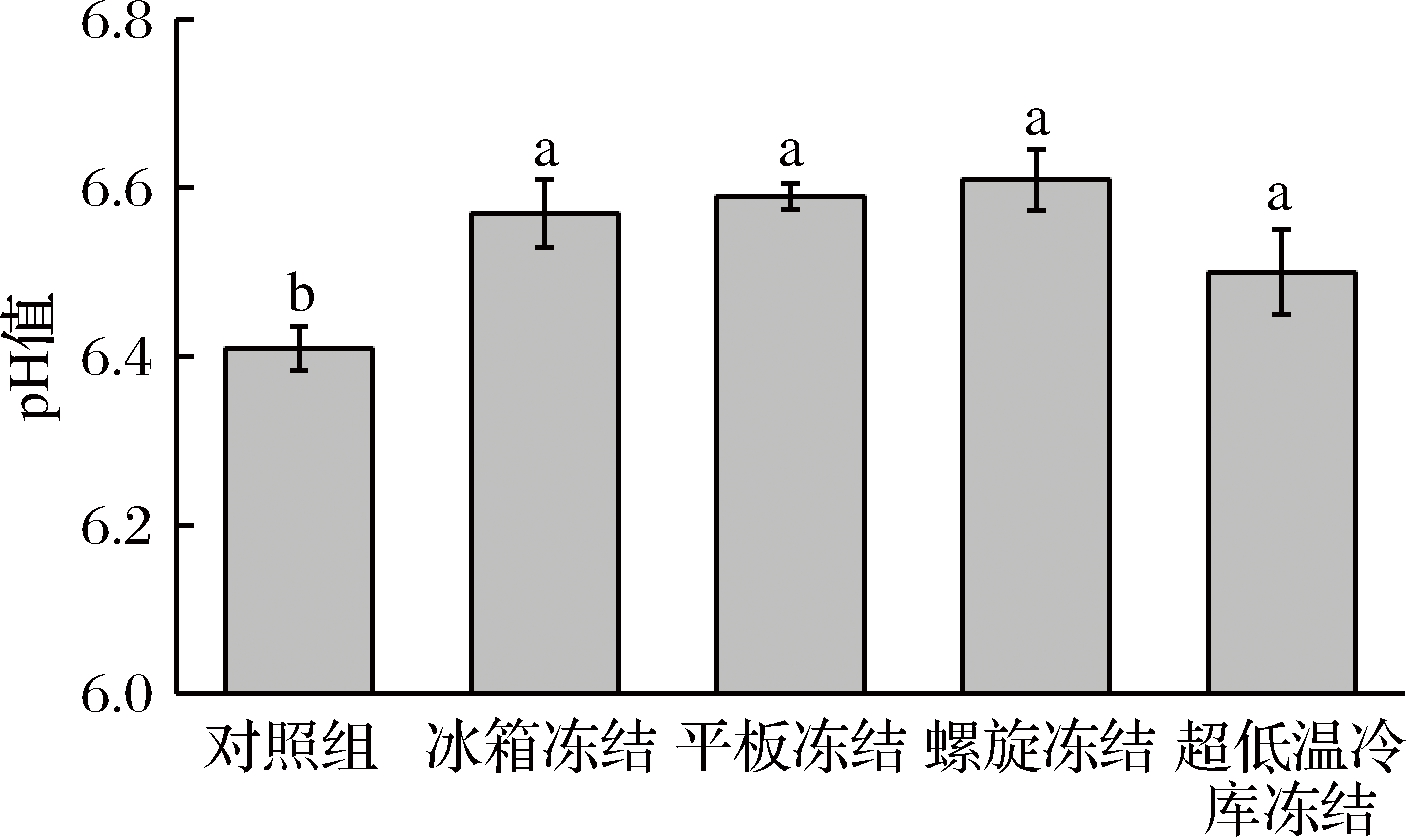
图3 不同冻结方式对鱿鱼pH值的影响
Fig.3 Effect of different freezing methods on pH value of squid
2.5 鱿鱼在冻结过程中质构的变化
通过质构仪测得的硬度、咀嚼性、弹性和胶黏性等质构参数,可以用来反映不同冻结方式对鱿鱼的品质的影响。硬度是肉发生形变所需要的能量,咀嚼性是咀嚼到吞咽这个过程中所消耗的能量,两者指标的变化应该是一致的。胶黏性是鱼肉在剪切时所产生的抵抗力,反映鱼肉细胞间结合力的大小程度。由表2可知,样品经不同冻结处理后,对硬度、咀嚼性和胶黏性影响大小的顺序均为:对照组>螺旋冻结>超低温冷库冻结>冰箱冻结>平板冻结,表明冻结速度越快,冻结后的这3种质构参数更接近对照组。平板冻结因为是接触式传热,为了冻结效果所以在冻结过程中鱿鱼之间尽可能紧密,相互挤压导致质构数据最差。弹性是表示鱼肉撤掉外力之后,鱼肉恢复形状的程度。胶黏性越好越有利于弹性的保持[16],但是在弹性上冰箱冻结组更接近对照组,可能是由于鱼肉因冻结速度过快而产生的内应力导致了低温断裂的发生,破坏蛋白质的二级结构,因此细胞间的结合力会下降[24]。
表2 不同冻结方式对鱿鱼硬度、咀嚼性、胶黏性及弹性的影响
Table 2 Effect of different freezing methods on hardness, chewiness, gumminess and springiness of squid
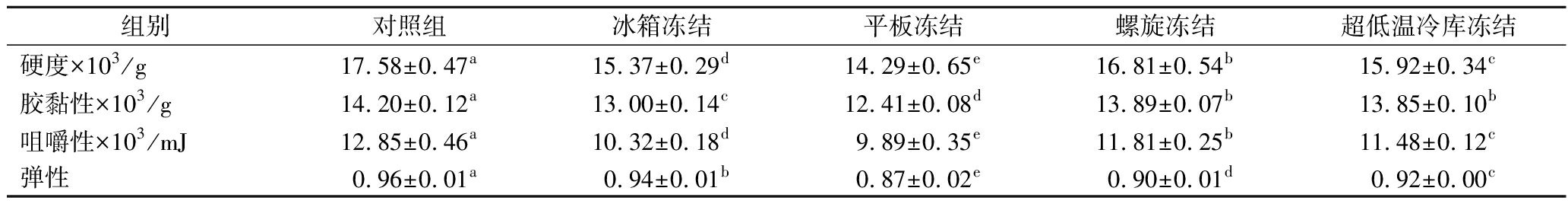
组别对照组冰箱冻结平板冻结螺旋冻结超低温冷库冻结硬度×103/g17.58±0.47a15.37±0.29d14.29±0.65e16.81±0.54b15.92±0.34c胶黏性×103/g14.20±0.12a13.00±0.14c12.41±0.08d13.89±0.07b13.85±0.10b咀嚼性×103/mJ12.85±0.46a10.32±0.18d9.89±0.35e11.81±0.25b11.48±0.12c弹性0.96±0.01a0.94±0.01b0.87±0.02e0.90±0.01d0.92±0.00c
2.6 鱿鱼在冻结过程中脂肪氧化的变化
在温度很低的条件下,鱼类脂肪会发生氧化[25]。在冻结过程中,鱼肉组织中自由水不断减少,可溶性物质浓度不断增大,脂肪氧化速度加剧[2]。而且鱿鱼经不同的冻结方式后形成的冰晶大小和形状不同,对组织的机械损伤也有差异,导致与空气的接触面积大小不一,影响脂肪的氧化程度。新鲜鱿鱼的脂肪含量较一般水产品低,如图4所示,对照组的MDA含量是0.07 nmol/mg,这与路钰希[21]的实验结论一致。从图4可以看到,鱿鱼经过不同冻结方式后,MDA含量之间存在差异性,其中螺旋冻结的MDA含量与新鲜样品最为接近,达到0.133 nmol/mg,可能是因为螺旋冻结速度最快,冰晶最小,对组织的机械损伤最小。虽然平板冻结的速率比冰箱快,但是在冻结过程中因为挤压的关系对鱼肉组织有损伤影响。从表1看出,平板冻结的冻结损失率最大,导致组织液浓度增大,氧化速度加快。
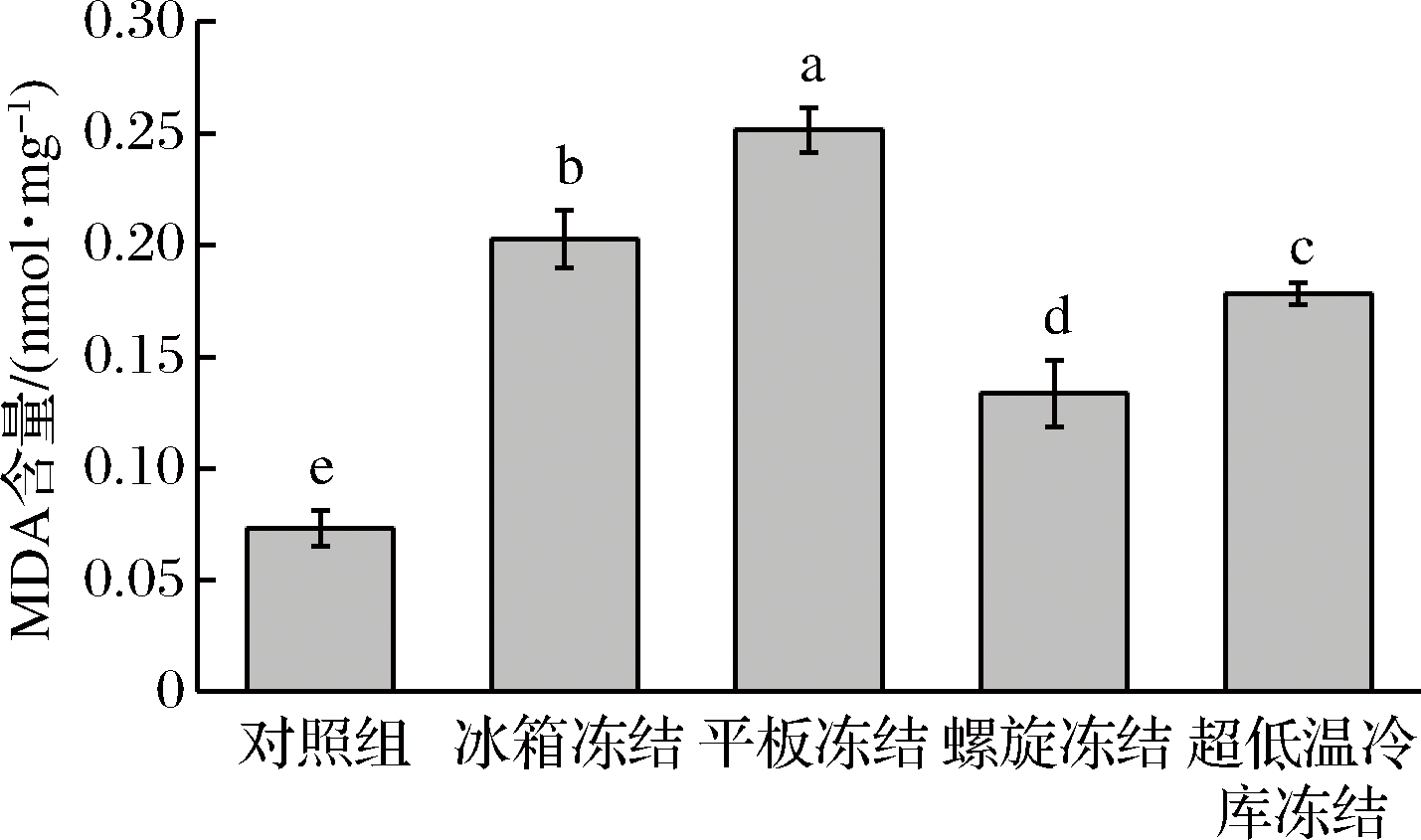
图4 不同冻结方式对鱿鱼MDA含量的影响
Fig.4 Effect of different freezing methods on MDA content of squid
2.7 鱿鱼在冻结过程中水分状态的变化
鱿鱼在冻结过程中,冰晶会使非极性基团周围的水发生凝聚,导致三维网状结构和疏水性残基发生改变使水的结合力变弱,同时冻结后食品发生干耗从而造成食品的表面呈现多孔层,这也会导致持水能力的下降[26]。弛豫时间越长代表水分的流动性越好,T21、T22、T23所代表的的弛豫时间分别是结合水、不易流动水和自由水。由图5可知,不同冻结方式对鱿鱼的结合水变化不明显,结合水的流动性本来就很差,冻结过程中这部分水没有形成结晶,基本维持在稳定状态。相比对照组的T23值,冻结组在冻结过程中会由于低温断裂和静电斥力等原因,多肽链间隔增加,蛋白质网状结构空间扩大,最终都有较大的T22、T23值,水分自由度增加。T22这部分水分会经历2种变化:向内迁移和向外蒸发,超低温冷库冻结的T22值(62.94 ms)与对照组最接近,其他3种冻结方式的T22值都是67.48ms。螺旋冻结和超低温冷库冻结的T23值都是1 084.36 ms,与对照组T23值(1 011.63 ms)最接近,自由水流动性较低。
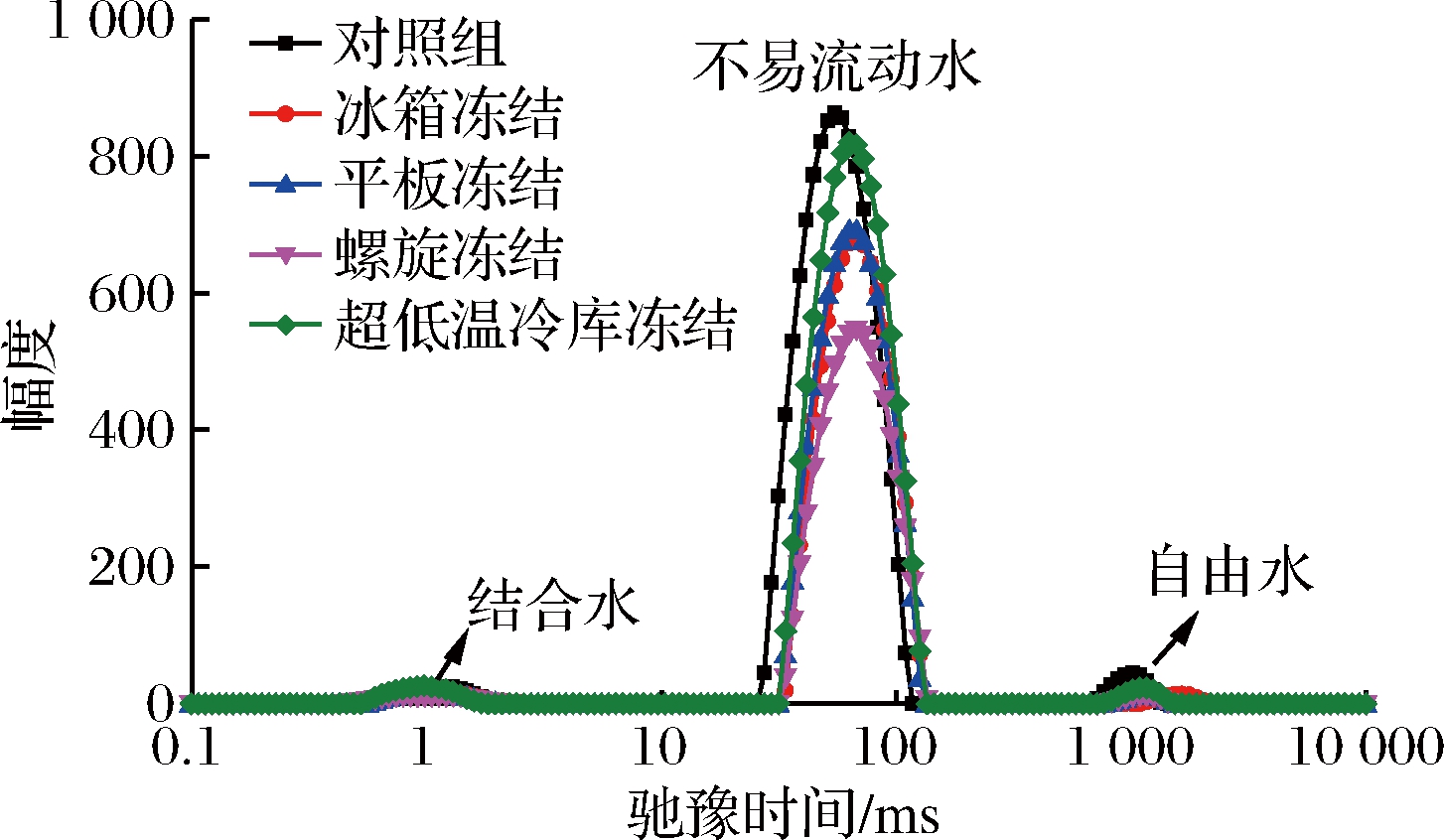
图5 不同冻结方式对鱿鱼T2弛豫时间的影响
Fig.5 Effect of different freezing methods onT2 relaxation timeof squid
由图6可知,约93%~97%的水在T21弛豫时间表征的不易流动水上,即水分主要存在肌原纤维蛋白结构中,这与朱文慧等[27]的实验结果一致。与对照组相比,冻结组的不易流动水含量较低,自由水含量较高,表明新鲜的鱿鱼有更多的水分截留在肌原纤维蛋白结构中[28]。超低温冷库冻结和螺旋冻结的自由水含量比冰箱冻结低,可能是因为冻结速度快,产生的内应力使蛋白质网状结构空间扩大,不易流动水被截留下来。平板冻结的自由水含量最高,在离心或蒸煮等外部条件下这部分水分很容易流失,这与保水性的研究结果相一致。
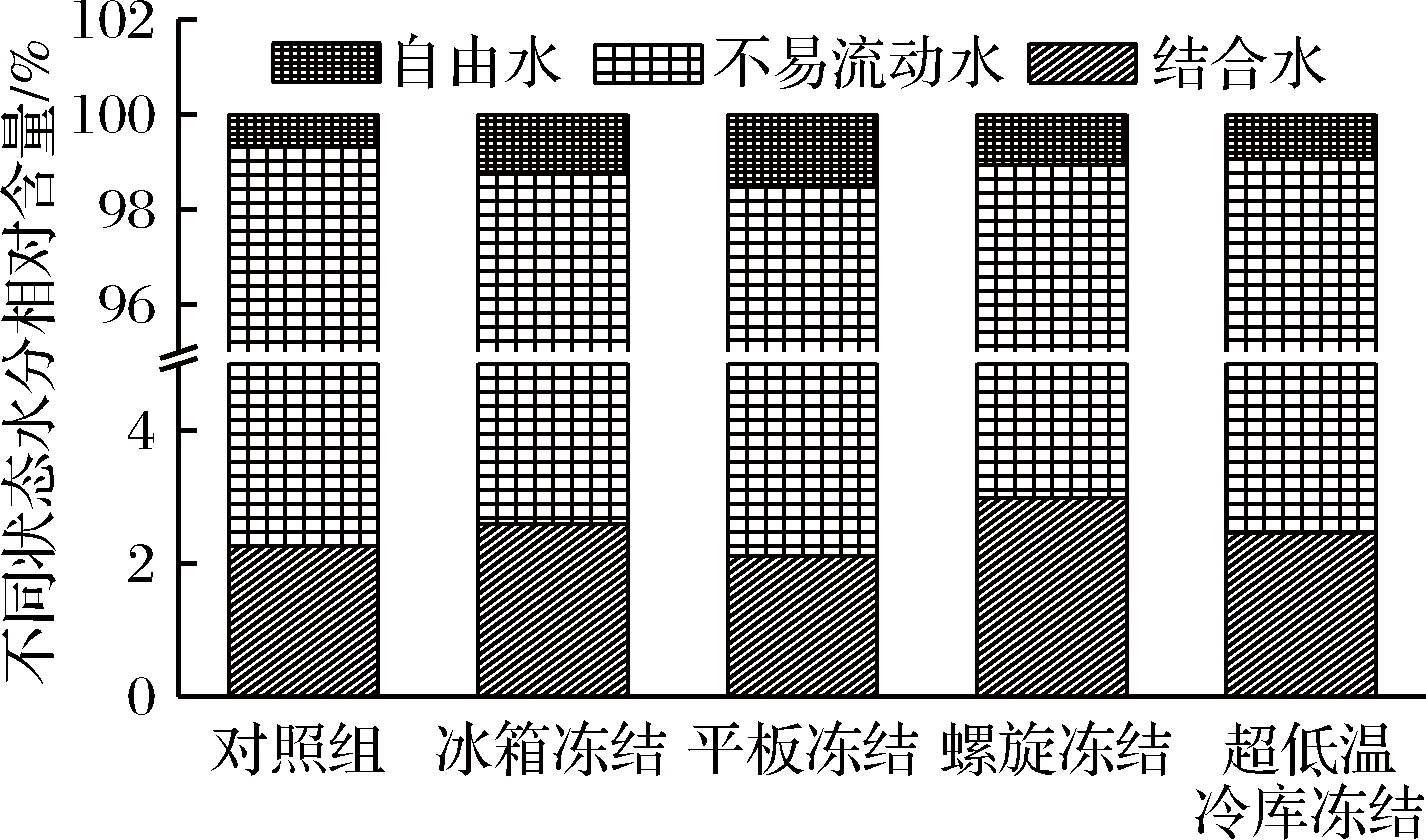
图6 不同冻结方式对鱿鱼各状态水分含量的变化
Fig.6 Changes of different freezing methods on water population of different status of squid
核磁共振成像(MRI)是一门可以获得肌肉中水、脂肪等MRI成像的技术,能够直观反映水产品加工过程中的水分分布及迁移[29]。通常情况下,MRI图亮度越强,质子密度越高,越趋于红色,表明鱼肉该部分的水分含量越高。从图7中可以看出,MRI图亮度由高到低依次为对照组、螺旋冻结、超低温冷库冻结、冰箱冻结、平板冻结。超低温冷库冻结处理质子密度加权像的亮度和螺旋冻结差异不明显,但是前者的亮度分布较为均匀,表明冻结方式对鱿鱼水分分布的位置有影响。冰箱冻结和平板冻结的亮度较弱,表明鱿鱼经冻结、解冻后的失水较多。

图7 不同冻结方式下鱿鱼的核磁共振成像图
Fig.7 MRI of different freezing methods on squid
2.8 鱿鱼在冻结过程中组织微观结构的变化
鱼肉在冻结过程中生成的冰晶大小和分布都会影响组织微观结构的完整性[30]。可以通过肌纤维束的间隙大小和分布情况来间接反映不同冻结方式对鱿鱼品质的影响。由图8可知,新鲜鱿鱼的肌纤维束排列紧密,肌内膜完整,而鱼肉经不同冻结方式后的微观结构有显著性差异。在肌纤维完整性上,螺旋冻结最好,冰箱冻结和平板冻结较差,这可能是因为冻结速率越快,冰晶越小、分布越规则,对肌纤维的机械损伤越小[31]。鱿鱼在平板冻结过程中鱼肉被挤压,肌纤维可能会被撕裂,间隙增大,在组织微观结构上的表现是最差的。所以,螺旋冻结能够较好维持鱿鱼的组织结构的紧密性、完整性。

A-对照组;B-螺旋冻结;C-超低温冷库冻结;D-冰箱冻结;E-平板冻结
图8 不同冻结方式对鱿鱼微观结构的影响(×100)
Fig.8 Effect of different freezing methods on microstructure of squid(×100)
3 结论
本文为了研究冻结方式对鱿鱼的品质影响,采用4种不同冻结方式进行分析。结果表明,冰箱冻结、平板冻结、超低温冷库冻结和螺旋冻结的鱿鱼通过最大冰晶生成带的时间分别为171、56、26和18 min。在冻结过程中,螺旋冻结的冻结速度虽然比超低温冷库冻结快,但是因为其风速较快,表面的水分会发生蒸发或者升华,保水性较差。低场核磁共振结果也表明,与其他冻结方式比较,超低温冷库冻结和螺旋冻结的自由水含量和流动性较低,且超低温冷库冻结的水分分布最为均匀。螺旋冻结在色差、脂肪氧化和微观结构上与新鲜鱿鱼的值最为接近,在质构方面,其硬度、咀嚼性和胶黏性维持最好,但是冰箱冻结的弹性最好。鱿鱼经过冻结之后pH值会升高,但是鱿鱼经不同冻结方式后其pH值差异性不明显。平板冻结因挤压的缘故对鱿鱼品质的维持效果最差,所以在用螺旋冻结工艺冻结水产品时,为了更好地维持冻品的品质,应考虑风速对冻品的保水性的影响或者采用加湿的方式进行处理。
[1] CHEN X, LIU B, CHEN Y. A review of the development of Chinese distant-water squid jigging fisheries[J].Fisheries Research, 2008, 89(3):211-221.
[2] 彭欢欢, 刘小莉,张金振,等.不同冷冻方式对斑点叉尾鮰鱼片品质的影响[J].食品研究与开发, 2017, 38(8):177-182.
[3] 于刚,杨少玲,张慧,等.不同冻结方式对黄鳍金枪鱼品质变化的比较研究[J].食品工业科技,2015,36(10):325-329.
[4] 胡亚芹,胡庆兰,杨水兵,等.不同冻结方式对带鱼品质影响的研究[J].现代食品科技,2014,30(02):23-30.
[5] 方林,施文正,刁玉段,等.冻结方式对不同部位草鱼呈味物质的影响[J].食品科学,2018,39(12):199-204.
[6] AUBOURG S P, TORRES J A, SARAIVA J A, et al.Effect of high-pressure treatments applied before freezing and frozen storage on the functional and sensory properties of Atlantic mackerel (Scomber scombrus)[J]. LWT-Food Science and Technology, 2013, 53(1):100-106.
[7] 汪磊,谢晶,王金锋,等.船用超低温R404A单机双级制冷系统的试验研究[J].食品与机械,2018,34(3):103-107.
[8] JIANG Qingqing, JIA Ru, NAKAZAWA N, et al. Changes in protein properties and tissue histology of tuna meat as affected by salting and subsequent freezing[J].Food Chemistry,2019,271: 550-560.
[9] 刘妙,杨宪时,张小伟,等.复配保鲜剂对反复冻融鱿鱼品质的影响[J].食品与发酵工业,2016,42(5):140-145.
[10] BENJAKUL S, SEYMOUR T A, MORRISSEY M T, et al. Physicochemical changes in Pacific whiting muscle proteins during iced storage[J]. Journal of Food Science, 2010, 62(4):729-733.
[11] 王硕,谢晶,杨凯,等.三文鱼冷链流通过程中质构、鲜度及感官品质变化规律与水分迁移相关性[J].中国食品学报,2018,18(5):173-184.
[12] 曹荣, 王凤玉,赵玲,等. 日本枪乌贼(Loligo japonica)不同温度冻藏过程中的品质变化[J].渔业科学进展, 2016, 37(4):97-103.
[13] XU B, ZHANG M, BHANDARI B, et al. Effect of ultrasound immersion freezing on the quality attributes and water distributions of wrapped red radish[J].Food and Bioprocess Technology, 2015, 8(6): 1 366-1 376.
[14] 江杨阳,杨水兵,余海霞,等.不同冻结方式对红虾肌肉品质的影响[J].现代食品科技,2017,33(10):142-148;116.
[15] 华泽钊, 李云飞,刘宝林.食品冷冻冷藏原理与设备[M].北京:机械工业出版社, 1999.
[16] 廖媛媛,欧昌荣,汤海青,等.三种冻结方式对大黄鱼品质的影响[J].现代食品科技,2014,30(7):218-223;186.
[17] LIU Shi, TAO Yang, XIONG Guangquan,,et al.Influence of frozen storage temperature on the microstructures and physicochemical properties of pre-frozen perch (Micropterus salmoides) [J].LWT,2018,92:471-476.
[18] KONO S, KON M, ARAKI T,et al. Effects of relationships among freezing rate, ice crystal size and color on surface color of frozen salmon fillet[J].Journal of Food Engineering, 2017, 214:158-165.
[19] THANONKAEW A, BENJAKUL S, VISESSANGUAN W, et al. The effect of metal ions on lipid oxidation, colour and physicochemical properties of cuttlefish (Sepia pharaonis) subjected to multiple freeze-thaw cycles[J].Food Chemistry, 2006, 95(4):591-599.
[20] LEYGONIE C, BRITZ T J, HOFFMAN L C.Oxidative stability of previously frozen ostrich M.iliofibularis packaged under different modified atmosphere conditions[J].International Journal of Food Science&Technology, 2011, 46 (6):1 171-1 178.
[21] 路钰希, 林玉海,李学英,等.冻藏温度对鱿鱼品质的影响[J].食品与发酵工业, 2015, 41 (3):105-111.
[22] 董佳,胡嘉杰,王庆,等.液体浸渍冷冻对鲟鱼贮藏过程中品质的影响[J].食品科学,2017,38(5):281-287.
[23] 迟海,李学英,杨宪时,等.南极磷虾冻藏温度下的品质变化及其货架期分析[J].水产学报,2012,36(1):153-160.
[24] BOONSUMREJ S, CHAIWANICHSIRI S, TANTRATIAN S, et al.Effects of freezing and thawing on the quality changes of tiger shrimp (Penaeus monodon) frozen by air-blast and cryogenic freezing[J].Journal of Food Engineering, 2007, 80(1):292-299.
[25] 赵巧灵, 廖明涛,刘书臣,等. 蓝鳍金枪鱼脂肪氧化和鱼肉色泽的变化研究[J].中国食品学报, 2014, 14(7):79-86.
[26] 林晶晶,林向阳,吴佳,等.利用核磁共振技术研究鱼糜制品在储藏过程中的水分变化[J].食品科学,2011,32(19):46-49.
[27] 朱文慧,宦海珍,步营,等. 不同解冻方式对秘鲁鱿鱼肌肉保水性和蛋白质氧化程度的影响[J].食品科学,2017,38(11):6-11.
[28] SHAO J H, DENG Y M, JIA N, et al.Low-field NMR determination of water distribution in meat batters with NaCl and polyphosphate addition[J].Food Chemistry, 2016, 200:308-314.
[29] MARCONE M F, WANG S, ALBABISH W, et al.Diverse food-based applications of nuclear magnetic resonance (NMR) technology[J].Food Research International, 2013, 51(2):729-747.
[30] NERI L, HERNANDO I, PÉREZMUNUERA I, et al.Mechanical properties and microstructure of frozen carrots during storage as affected by blanching in water and sugar solutions.[J].Food Chemistry, 2014, 144(2):65-73.
[31] 史咏梅,李勇勇,吴迪迪,等.不同冻结方式对南美白对虾品质的影响[J].食品与发酵工业,2019,45(5):87-93.