白酒是中国统发酵食品。浓香型白酒以窖香浓郁、绵柔甘冽、入口绵甜、香味协调及尾净余长等酒体风格而享有盛名,是我国白酒的基本香型之一,占据了70%的市场份额。目前市场上浓香型白酒的品牌主要有泸州老窖、五粮液、剑南春等。河南省出产的白酒以浓香型为主,并以杜康、宋河、张弓(皇封)、林河和仰韶等为典型代表[1-4]。
中国浓香型白酒的发酵过程是与窖池中庞大微生物区系在酒醅固、液、气三相的复杂物质能量代谢紧密相连的。酒醅是白酒酿造的主体,也是微生物生长代谢的基质。伴随着酒醅发酵的进行,窖池微生物群落不断地发生着有序的消长变化[5-6],酒醅中的各种物质形态不断地产生和消失,通过窖池内物质链的传递形式体现能量代谢的变化,最终形成浓香型白酒与众不同的成分构成和风味特征[7-10]。
本文通过跟踪研究发酵过程中酒醅理化指标的动态变化,解析浓香型白酒的酿造机制,以丰富浓香型白酒酿造的科学理论,提高白酒酿造的工艺控制水平和白酒品质。
1 材料与方法
1.1 样品来源及采样方法
实验样品取自洛阳汝阳杜康酒厂2-3班中排3号窖。该窖池出产的酒的品质一直较稳定,具有较好的代表性。取样时间2017年4~6月。发酵酒醅按上、中、下分层,同一层面又分为中心部和周边部,取样后混合均匀作为1个样品。发酵过程按0(入窖)、10、20、30、40、50、60 d(出窖)采样。
1.2 主要实验仪器
GZX-9420MBE电热恒温鼓风干燥箱,上海博讯实业有限公司医疗设备厂;THZ-82A恒温振荡器,常州朗越仪器制造有限公司;UV7500紫外可见分光光度计,上海博讯实业有限公司医疗设备厂;J-110001电子天平,上海精密科学仪器有限责任公司;K9840自动凯氏定氮仪,山东欧莱德仪器有限公司;pH计,北京华科仪科技股份有限公司;HH-6水浴锅,巩义市予华仪器有限公司。
1.3 实验方法
对发酵酒醅的分析包括水分、pH值、总酸、还原糖、粗淀粉、酒精含量、总酯、氨态氮、有效磷和粗蛋白等。其中水分、总酸、还原糖、粗淀粉、酒精含量、总酯、氨态氮和有效磷含量的测定方法参考《白酒生产技术全书》 [7, 11-12]。pH值采用pH计测定。粗蛋白的含量采用自动凯氏定氮仪测定。
2 结果与分析
2.1 水分的变化
水分是固态发酵酒醅的主要控制指标之一。窖池中水分适宜,不仅可以参与糖化过程,保证窖池中微生物的生长代谢,并为其代谢产物(醇、醛、酸、酯等)提供有效溶剂,还可以稀释酸度,调节窖池内的发酵温度,保证酒醅的缓慢发酵[8, 12]。酒醅发酵过程中的水分含量及其变化趋势如图1所示。
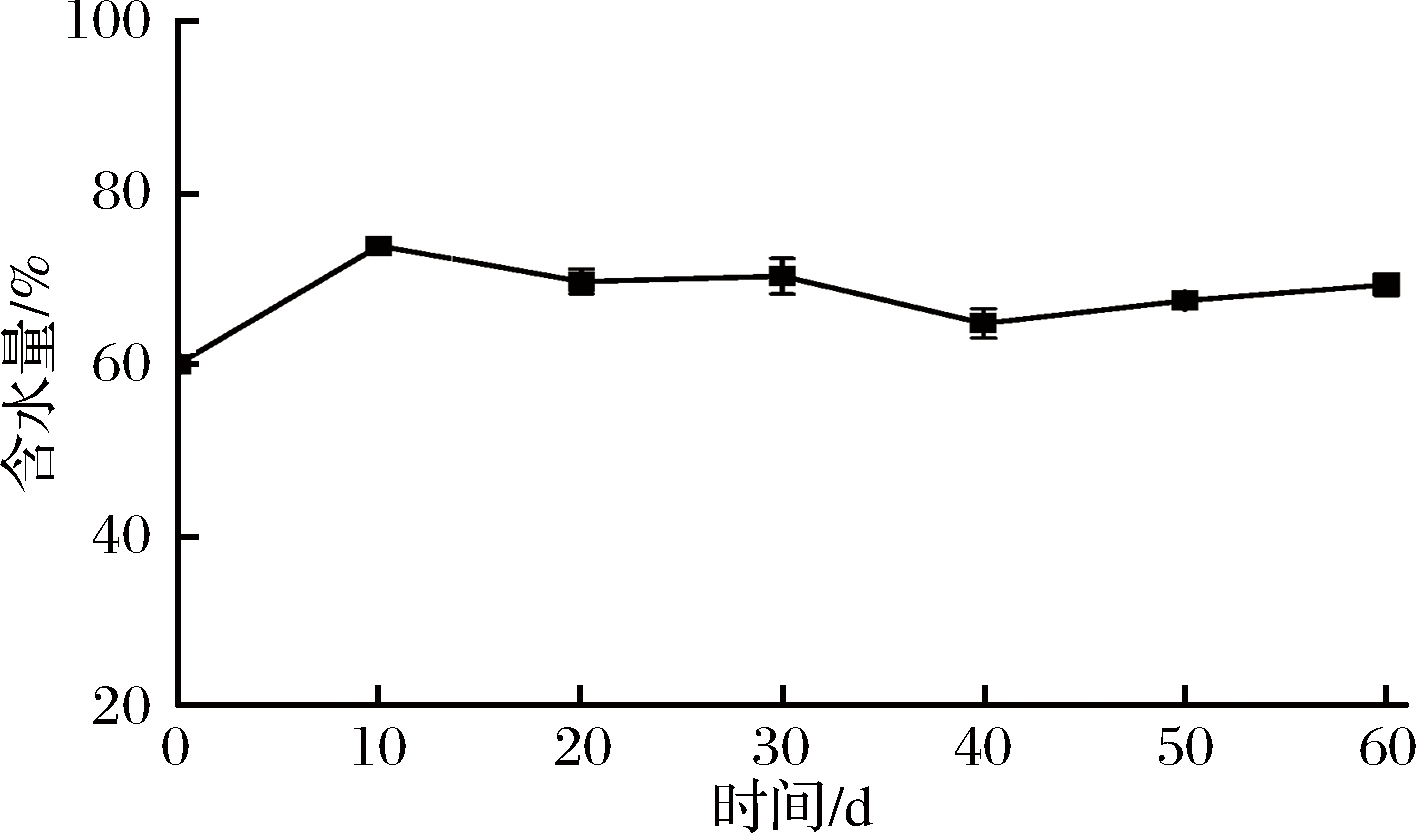
图1 酒醅发酵过程中水分含量随时间的变化趋势
Fig.1 The change trend of moisture in the fermented grains during the fermentation
酒醅初始含水量为59.97%,在发酵前10 d内急剧上升,可能由于初期酒醅中营养物质丰富且含氧充足,酵母菌和霉菌等好氧微生物快速生长繁殖,进行有氧呼吸代谢产生大量的水,第10天达最高值73.70%;自第10天后含水量呈现波动下降,可能是由于水分达到饱和状态,多余的水向下移动在窖池底部沉积,成为黄水的主要成分[7],这期间也有通过酯化反应生成的水,但由于水的生成速度略小于水的沉降速度,所以才呈现波动下降的趋势,直到发酵后期,水分含量略有所上升。
2.2 pH值和总酸的变化
发酵过程中pH值是微生物在特定环境下代谢活动的综合指标,是一项重要的发酵参数,它对微生物的生长及代谢产物的形成有重要的影响。酒醅发酵过程中的pH值及其变化趋势如图2所示。整个发酵过程中pH值一直在3.6~3.9之间。pH值在前10 d内略微上升,而后又呈现下降趋势。整个发酵过程pH值由初始的3.86下降至最终的3.60。发酵过程中的总酸含量及其变化趋势如图3所示。总酸含量在发酵前10 d内略微下降,由0.63 g/100 g酒醅下降至0.53 g/100 g酒醅,而后急剧上升,含量达到1.15 g/100 g酒醅,之后趋于平稳并略有上升,正好与pH值的变化趋势相反。
导致这种变化趋势的原因是由于发酵初期霉菌和酵母是微生态系统中的优势菌,产酸菌的活性受到抑制,同时酒醅中的乙醇和有机酸通过酯化反应相结合,导致初期有机酸含量的减少,使得pH值略微升高,同时有机酸也可以作为碳源和能源物质被消耗[13]。当酒醅颗粒间隙中的氧气近乎消耗殆尽,以及产物的抑制作用让霉菌和酵母活性减弱,产酸菌开始大量生长繁殖,总酸含量快速上升,pH值开始下降。之后酯类的生成开始加强,并且有机酸作为碳源和能源物质被微生物利用,有机酸的产生和消耗处于动态平衡中[14-16]。

图2 酒醅发酵过程中pH值随时间的变化趋势
Fig.2 The change trend of pH values in the fermented grains during the fermentation
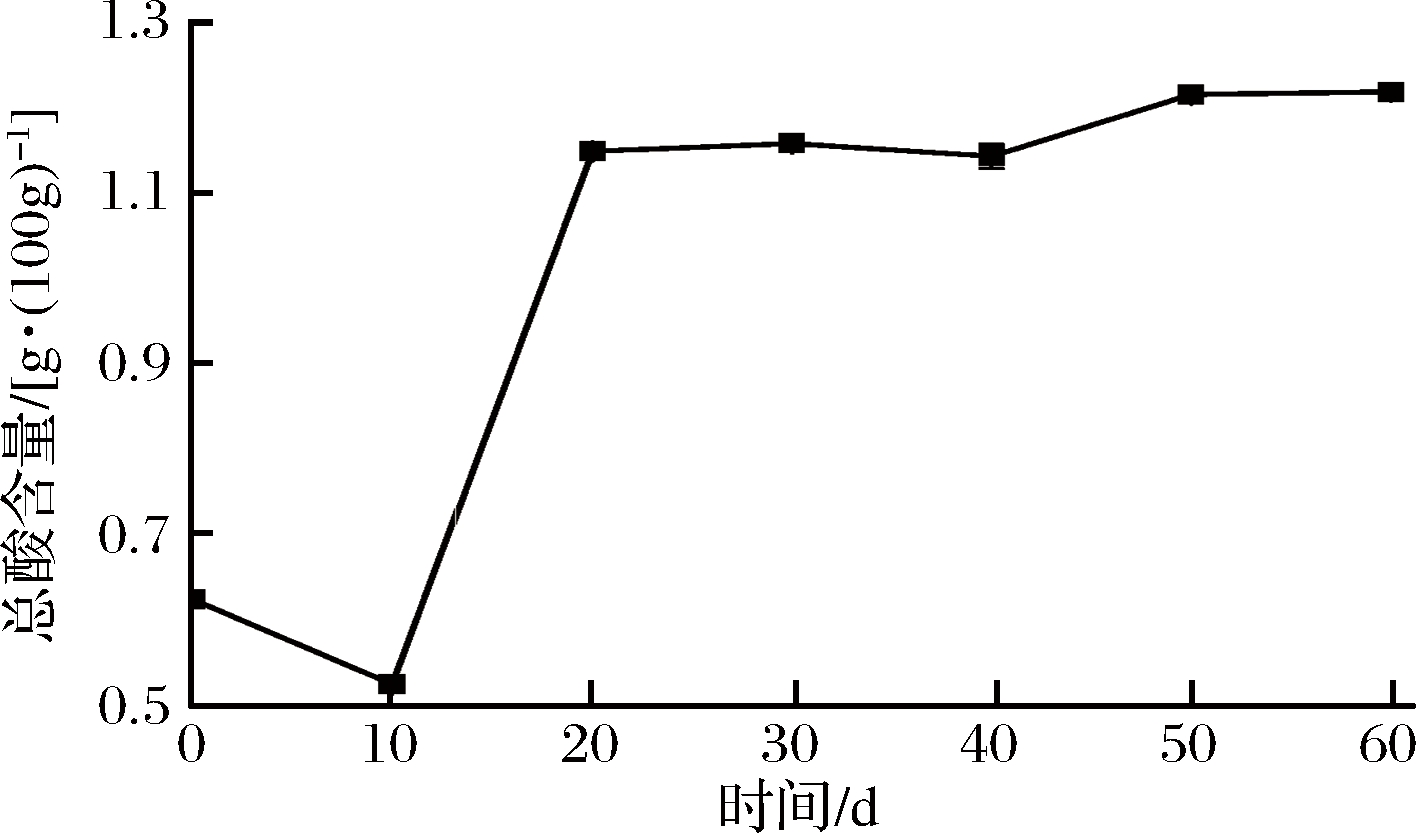
图3 酒醅发酵过程中总酸含量随时间的变化趋势
Fig.3 The change trend of total acid in the fermented grains during the fermentation
2.3 还原糖和粗淀粉的变化
发酵过程中还原糖的含量呈下降趋势(图4),其含量由初始1.42 g/100 g(酒醅)下降至0.04 g/100 g。在发酵前20 d下降速度较快,发酵20~60 d下降幅度逐渐减缓,主要是由于发酵过程中微生物代谢导致还原糖分解生成乙醇和乳酸等物质,而发酵中后期随着酸度的升高,抑制了淀粉酶的活性,使得还原糖在消耗的同时没有得到有效的补充,还原糖作为整个发酵过程中的主要能源物质和主要碳源,逐渐被微生物利用消耗殆尽[17-18]。
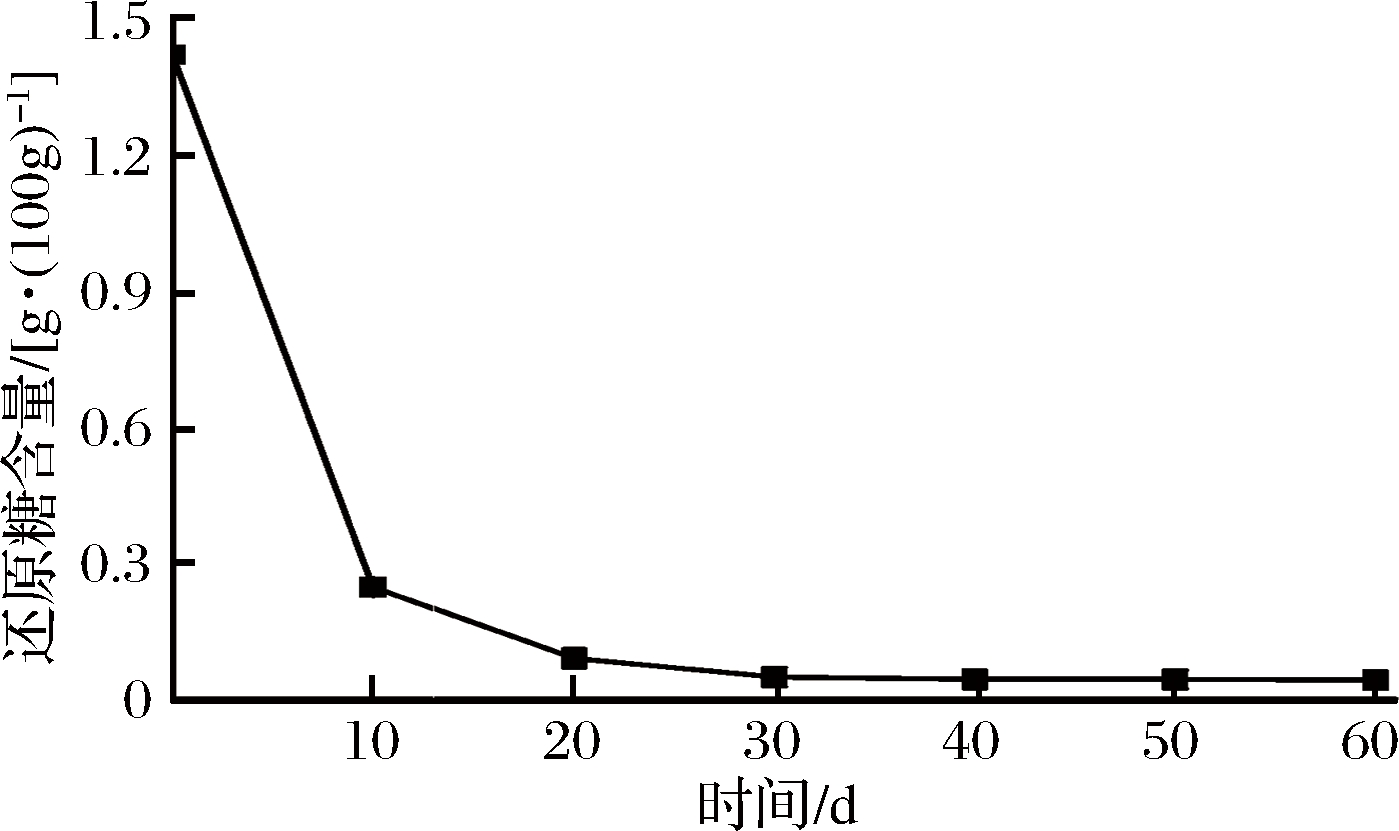
图4 酒醅发酵过程中还原糖含量随时间的变化趋势
Fig.4 The change trend of reducing sugar content in the fermented grains during the fermentation
酒醅发酵过程中淀粉含量的变化如图5所示,淀粉含量在发酵前10 d小幅度上升,可能是由于发酵初期,还原性糖、纤维素等其他固体原料成分消耗较快,粗淀粉利用率很低,使粗淀粉所占酒醅的质量比例增高。淀粉含量在发酵第10~20天快速下降至9.40 g/100 g(酒醅),发酵第20~60天保持平稳且略微下降。这是由于发酵前期霉菌和酵母菌生长代谢旺盛,是酒醅整个微生态系统中的优势菌,产生大量的淀粉酶,使淀粉水解产生单糖,因而前期淀粉含量下降较快[18-19],中后期逐渐趋于平稳是由于随着有机酸的产生,酒醅中的较高酸度抑制了淀粉酶的活性,使淀粉几乎不再分解的缘故。
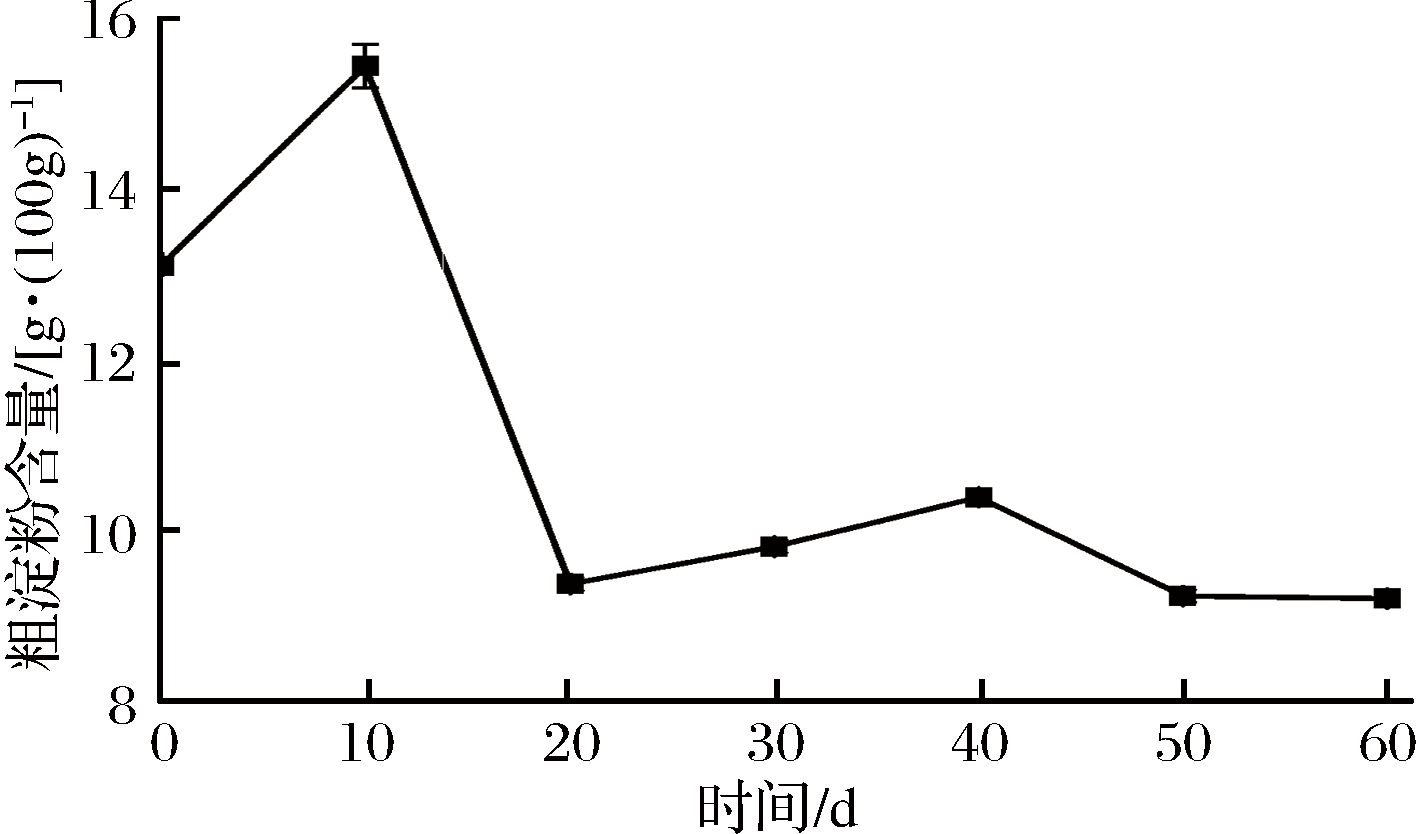
图5 酒醅发酵过程中淀粉含量随时间的变化趋势
Fig.5 The change trend of starch in the fermented grains during the fermentation
2.4 酒精含量的变化
发酵过程中的酒精含量及其变化趋势如图6所示。酒精含量的变化在发酵前10 d呈现快速上升趋势,并在第10天达到最高值94.68 mg/g(酒醅),之后酒精含量变化较为平稳,略有下降。基本维持在78.90~94.68 mg/g(酒醅)。呈现这种变化趋势的原因可能是发酵初期酵母发酵分解糖类产生大量的酒精,20 d以后发酵进入了产酸和产酯为主的阶段,酒精发酵减弱,同时酯化作用和呼吸作用都会消耗乙醇,酒精含量便处于一个动态平衡之中[16, 20]。
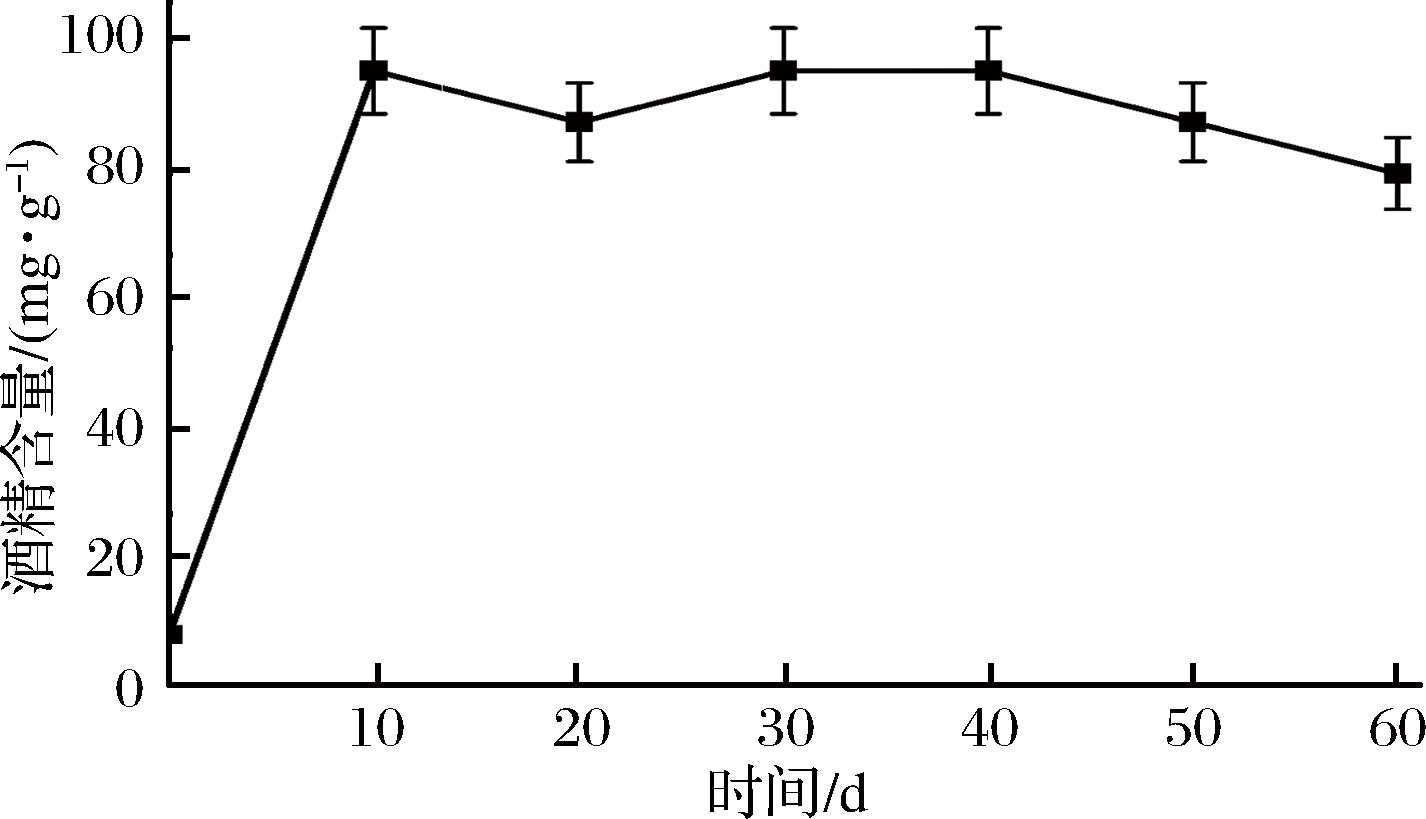
图6 酒醅发酵过程中酒精含量随时间的变化趋势
Fig.6 The change trend of alcohol content in the fermented grains during the fermentation
2.5 其他参数的变化
2.5.1 总酯的变化
发酵过程中的总酯含量及其变化趋势如图7所示。总酯含量的变化在发酵初期快速上升,在第10天达到最高值8.34 g/100 g(酒醅),而后逐渐下降并趋于平稳,维持在4.0 g/100 g(酒醅)左右。从发酵开始,原料的分解伴随乙醇和各种有机酸的产生,酯类开始合成,含量逐渐升高。在发酵中后期的厌氧阶段,由于微生物对底物的分解作用减弱,代谢反应从以酯分解为主逐步过渡到以酯合成为主,总酯的合成速度近似于总酯的分解速度,最终处于动态平衡之中并趋于稳定[21]。
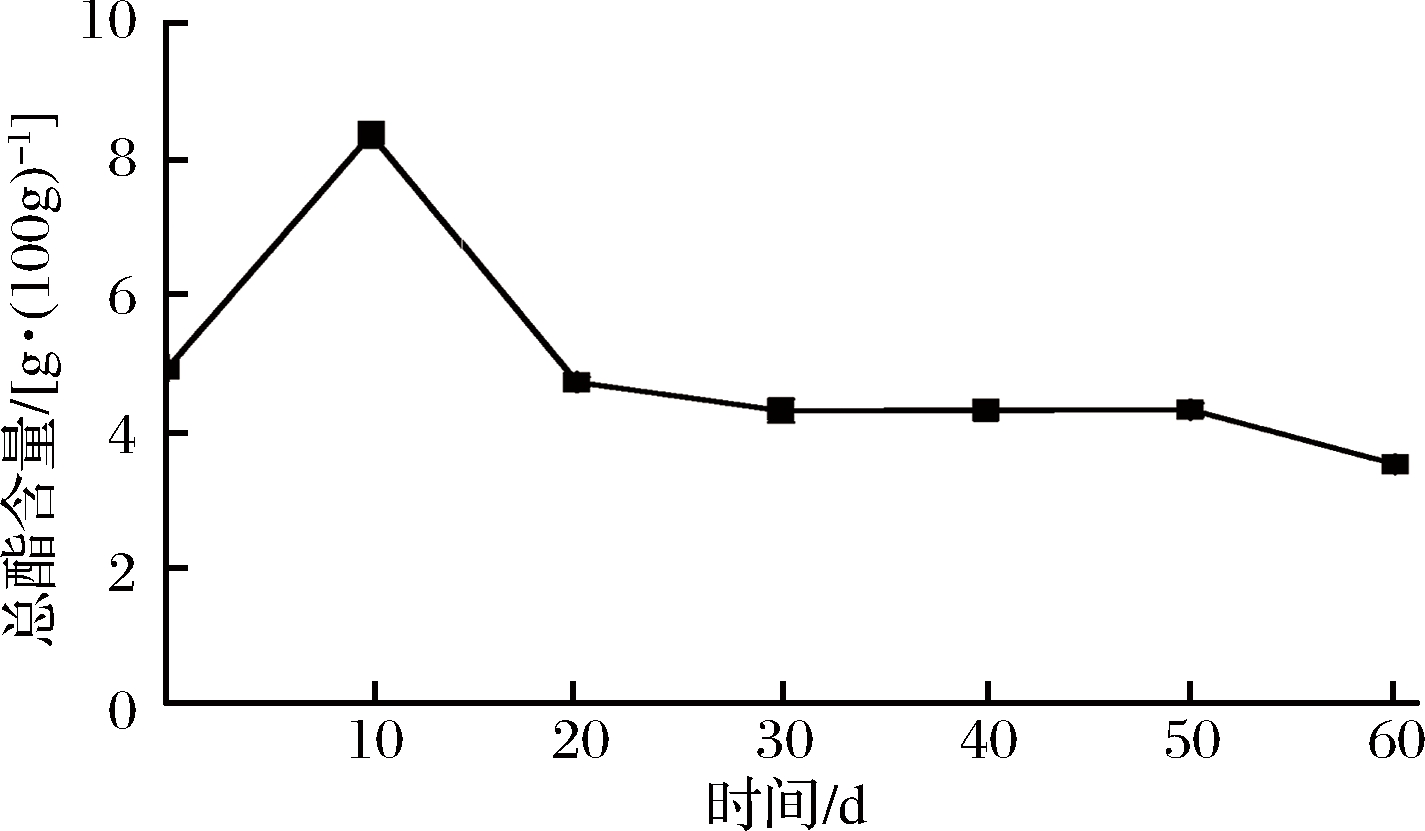
图7 酒醅发酵过程中总酯含量随时间的变化趋势
Fig.7 The change trend of total ester in the fermented grains during the fermentation
2.5.2 氨态氮和有效磷的变化
酒醅发酵过程中的氨态氮含量及其变化趋势如图8所示。氨态氮在发酵的前10 d快速下降,由1.71 g/100 g(酒醅)下降至1.25 g/100 g(酒醅),而后下降速度趋于平缓,第30天之后又快速上升,至第50天达到最高值1.77 g/100 g(酒醅),发酵最后10 d又有所下降。产生这种变化趋势的原因可能是,发酵前期原料中的蛋白质降解而成的氨基酸,被微生物大量利用,导致酒醅中氨态氮含量下降。而随着发酵过程中酸度的升高,以及酒精的产生,酵母菌和霉菌等活性受到抑制,菌体开始自溶,释放出氨基酸等物质,使得氨态氮含量又有所升高。产酸菌的持续利用使氨态氮在最后10 d又有所下降[8]。

图8 酒醅发酵过程中氨态氮含量随时间的变化趋势
Fig.8 The change trend of ammonia nitrogen content in the fermented grains during the fermentation
酒醅发酵过程中的有效磷含量及其变化趋势如图9所示。有效磷是细胞核的组成成分,是微生物生长繁殖的必需物质,因此其含量的变化与酒醅中微生物的生长繁殖密切相关。发酵前20 d有效磷含量呈缓慢下降的趋势,由初始值53.70 mg/100 g(酒醅)下降至最低46.28 mg/100 g(酒醅),之后快速上升,在第30天时达到最高值64.88 mg/100 g(酒醅),发酵的30~60 d有效磷含量趋于平稳略有下降。导致这种变化趋势的原因可能是发酵前期霉菌和酵母菌快速生长,合成菌体消耗了有效磷导致含量下降,而发酵中期,由于产物的抑制作用,霉菌和酵母数量逐渐减少,菌体自溶使得含量再次升高。此外有效磷的来源还包括原料的分解。
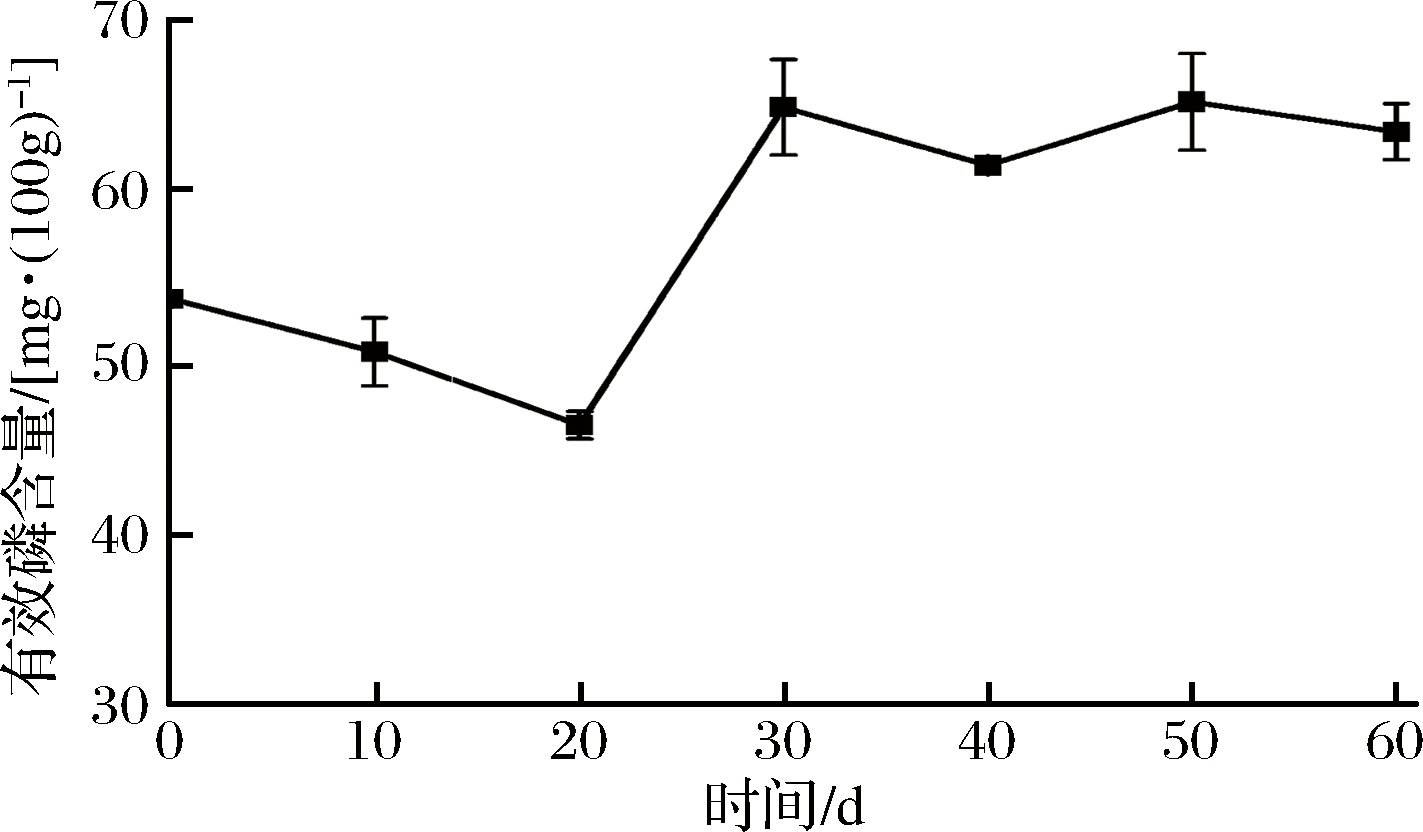
图9 酒醅发酵过程中有效磷含量随时间的变化趋势
Fig.9 The change trend of available phosphorus in the fermented grains during the fermentation
2.5.3 粗蛋白的变化
酒醅发酵过程中的粗蛋白含量及其变化趋势如图10所示,发酵过程中粗蛋白含量呈波动性上升趋势。随发酵的进行,其含量由初始11.54 g/100 g(酒醅)逐渐上升至出窖时的15.39 g/100 g(酒醅),在发酵第50天酒醅的粗蛋白含量达到最高值的16.41 g/100 g(酒醅)。这主要是由于菌体的大量生长,某些固氮菌的作用以及糖类物质的消耗造成蛋白质相对含量的升高。
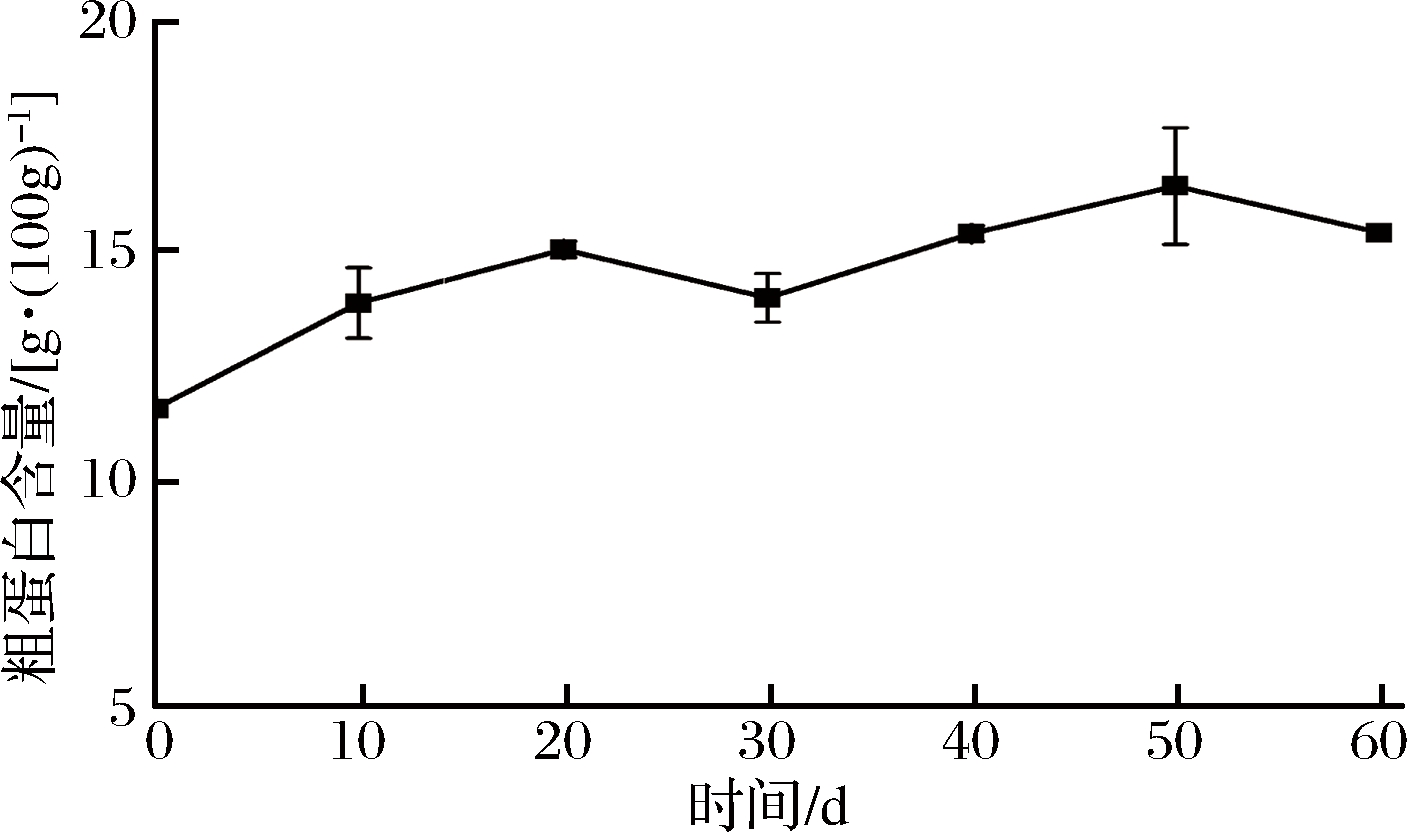
图10 酒醅发酵过程中粗蛋白含量随时间的变化趋势
Fig.10 The change trend of protein in the fermented grains during the fermentation
3 结论
本研究对浓香型杜康白酒发酵酒醅进行了分析,测定了其水分、pH值、总酸、还原糖、粗淀粉、酒精含量、总酯、氨态氮、有效磷和粗蛋白等理化指标的变化规律。其中,主要的变化趋势表现为:
(1)水分含量在初始时最低,为59.97%,在发酵前10 d上升至73.70%,之后呈现波动下降。
(2)pH值和总酸含量的变化具有密切相关性,总酸含量在发酵前10 d内略微下降,第10~20天又急剧上升至1.15 g/100 g,之后趋于平稳并略有上升。pH值则在前10 d上升至最高3.89,而后逐渐下降至发酵结束。
(3)还原糖和淀粉含量随发酵的进行都逐渐下降,尤其在前20 d下降最为剧烈,分别由初始1.42和13.12 g/100 g(酒醅)下降至发酵完成时0.04和9.23 g/100 g(酒醅)。
(4)酒精含量在发酵前10 d快速上升至94.68 mg/g(酒醅),之后变化较为平稳,略有下降。
(5)总酯含量在前10 d内快速上升至最高值8.34 g/100 g(酒醅),第10~20天急剧下降,之后趋于平稳,维持在4.0 g/100 g(酒醅)左右。
(6)氨态氮随着发酵的进行,前30 d内表现为下降的趋势,第30~50天逐渐升高到最高值1.77 g/100 g(酒醅),之后下降直至发酵结束。
(7)有效磷在发酵前20 d逐渐下降至46.28 mg/100 g酒醅,第20~30天快速升高,之后趋于平稳。
(8)粗蛋白的含量随发酵的进行逐渐上升。
发酵过程中化学物质的变化原因与酒醅中各种微生物的繁殖代谢密切相关。发酵初期,由于酵母、霉菌等好氧微生物在微生态系统中占主体地位,利用酒醅颗粒间隙中的空气进行有氧呼吸,产生的酶分解淀粉和蛋白质等大分子物质,利用葡萄糖和氨基酸等小分子物质进行分解代谢以及合成菌体,产生大量的水和乙醇,在此期间释放出大量的热量致使发酵初期温度急剧升高。同时己酸菌和乳酸菌等功能微生物代谢产生的有机酸同乙醇酯化生成酯类,使己酸乙酯、乳酸乙酯等酯类含量开始升高[22-24]。当接近发酵中期,由于酒醅间隙中的氧气几乎消耗殆尽,同时代谢产物的抑制作用使酵母菌和霉菌等菌体数量减少,产酸菌逐渐成为酒醅中的主体微生物,发酵开始进入产酸阶段,通过代谢产生各种有机酸,如乙酸、丁酸等,导致窖池产生高酸度,有机酸又和乙醇通过酯化反应产生各种芳香物质,直到发酵后期各种化学物质的含量才基本趋于稳定,预示着发酵的完成[25-27]。
白酒发酵非常复杂,各个发酵参数的变化受多种因素的影响。通过跟踪研究发酵过程中酒醅理化指标的动态变化,对于传统白酒酒醅发酵质量的判断和生产过程控制具有较大的参考价值,对解析浓香型白酒的酿造机制,为浓香型白酒发酵的机械化和可控化提供理论支持。
[1] 张健,高海燕,赵镭,等.白酒理化指标及其与香气品质的关系[J].食品科学,2010,31(10):283-286.
[2] 王进明,刘忠军.浓香型白酒产质量与工艺操作的关系[J].酿酒科技,2012(4):86-87;91.
[3] 李丹,张文学,李东,等.我国白酒产业发展方向探讨[J].食品安全质量检测学报,2015,6(7):2 633-2 638.
[4] 李大和.曲药、窖池、工艺操作与浓香型酒产质量的关系[J].酿酒,2008,35(4):3-9.
[5] HUANG Yuhong,YI Zhuolin,JIN Yanling,et al.Metatranscriptomics reveals the functions and enzyme profiles of the microbial community in Chinese Nong-flavor liquor starter[J].Frontiers in Microbiology,2017,8:1747.
[6] XU Youqiang,SUN Baoguo,FAN Guangsen,et al.The brewing process and microbial diversity of strong flavour Chinese spirits:a review[J].Journal of the Institute of Brewing,2017,123(1):5-12.
[7] YAN Shoubao,WANG Shunchang,WEI Guoguang,et al.Investigation of the main parameters during the fermentation of Chinese Luzhou-flavour liquor[J].Journal of the Institute of Brewing,2015,121(1):145-154.
[8] 张文学,岳元媛,向文良,等.浓香型白酒酒醅中化学物质的变化及其规律性[J].四川大学学报(工程科学版),2005,37(4):44-48.
[9] ZHANG Yanyan,ZHU Xiaoyu,LI Xiangzhen,et al.The process-related dynamics of microbial community during a simulated fermentation of Chinese strong-flavored liquor[J].BMC Microbiology,2017,17(1):196.
[10] HAN Sihai,ZHANG Weiwei,LI Peiyan,et al.Characterization of aromatic liquor by gas chromatography and principal component analysis[J].Analytical Letters,2017,50(5):777-786.
[11] 沈怡方.白酒生产技术全书[M].北京:中国轻工业出版社,2007.
[12] 周新虎,陈翔,杨勇,等.浓香型白酒窖内参数变化规律及相关性研究(I):理化参数[J].酿酒科技,2012(4):39-43.
[13] WANG Xueshan,DU Hai,XU Yan.Source tracking of prokaryotic communities in fermented grain of Chinese strong-flavor liquor[J].International Journal of Food Microbiology,2017,244:27-35.
[14] 张会敏.古井贡酒微生物群落结构及其与主要风味物质的关联研究[D].哈尔滨:哈尔滨工业大学,2017.
[15] 陆其刚,甘广东,张广松,等.浓香型白酒酒醅发酵体系参数变化相互关系的分析研究[J].酿酒科技,2016(10):45-47;52.
[16] 黄治国,刘燕梅,卫春会,等.浓香型酒醅微生物群落与理化指标的相关性分析[J].现代食品科技,2014,30(11):38-42.
[17] 张献敏.杜康酒酿造过程中化学物质的变化及其规律[J].中国酿造,2011,30(2):93-95.
[18] 黄治国,侯海波,罗惠波,等.浓香型白酒酒醅发酵过程中淀粉和还原糖的变化规律研究[J].中国酿造,2012,31(7):107-110.
[19] 赵爽,杨春霞,徐曼,等.浓香型白酒生产中酿酒微生物研究进展[J].食品与发酵科技,2012,48(1):24-29.
[20] 周瑞平,游玲,陈云宗,等.多粮浓香型白酒发酵过程中糟醅生物及非生物因子的变化规律[J].食品与发酵工业,2012,38(8):53-57.
[21] 甄攀.汾酒发酵过程之酒醅化学成分变化规律[J].酿酒,2016,43(1):83-86.
[22] 唐贤华,杨官荣,黄志瑜,等.传统浓香型白酒窖池发酵糟醅研究现状及其展望[J].酿酒,2014,41(3):14-17.
[23] 王媚.浓香型白酒糟醅窖内外发酵动态因子的初步研究[D].贵阳:贵州大学,2015.
[24] 王涛,姚韬,李涛,等.浓香型白酒酿造相关酵母发酵糟醅产己酸乙酯的研究[J].食品与发酵工业,2013,39(1):41-45.
[25] LI Xiaoran,MA Enbo,YAN Liangzhen,et al.Bacterial and fungal diversity in the traditional Chinese liquor fermentation process[J].International Journal of Food Microbiology,2011,146(1):31-37.
[26] ZHANG Wenxue,QIAO Zongwei,SHIGEMATSU TORU,et al.Analysis of the bacterial community in Zaopei during production of Chinese Luzhou-flavor liquor[J].Journal of the Institute of Brewing,2005,111(2):215-222.
[27] ZHANG Wenxue,QIAO Zongwei,TANG Yueqin,et al.Analysis of the fungal community in Zaopei during the production of Chinese Luzhou-flavour liquor[J].Journal of the Institute of Brewing,2007,113(1):21-27.