表1 不同解冻方式解冻条件
Table 1 Thawing conditions for different thawing methods
解冻方式解冻条件空气解冻金枪鱼鱼肉放置在洁净托盘置于恒温恒湿箱内,环境温度为28 ℃静止水解冻金枪鱼鱼肉放入恒温水中浸泡,水温28 ℃流水解冻水流均匀冲刷金枪鱼鱼肉表面,水流速度为0.94 m/s, 微波解冻将金枪鱼鱼肉放置在洁净无菌托盘上,置于NN-GD568M型微波炉中,解冻功率为500 W,频率为2 400 MHz
金枪鱼广泛分布于大西洋、太平洋,富含丰富的蛋白质、不饱和脂肪酸等营养物质,食用价值和商用价值极高[1-3]。金枪鱼属于高度洄游性鱼类,通过高速游动过程中,水流经鳃部进行呼吸,维持氧气供给,捕捞后的新鲜金枪鱼一旦停止游动将会逐渐窒息死亡。为了保持新鲜度,金枪鱼通常在被捕捞后立即进行超低温速冻冻结贮藏[4]。市面上所售的金枪鱼在加工和食用之前必须进行解冻处理,金枪鱼的食用品质与解冻方式密切相关。
李念文等[5]通过比较空气解冻、微波解冻、真空解冻和超声波解冻4种方式发现,微波解冻和超声波解冻虽然能显著缩短解冻时间,但在维持鱼肉品质方面效果一般,真空解冻作为新型的外部解冻方法,解冻方式温和,在持水力和盐溶性蛋白含量上要优于其余解冻方式。刘燕等[6]比较自然空气解冻、冷藏库解冻、温盐水组合解冻和静止水解冻发现,冷藏库解冻对金枪鱼的色泽有很好地保护作用,但其余指标不甚理想,温盐水组合解冻能更好的保持金枪鱼的口感圆润、色泽鲜亮且肉质富有弹性,但存在解冻时间过长的缺陷。TOLGA等[7]比较了冷藏解冻、水解冻和微波解冻3种方法分别对凤尾鱼、沙丁鱼和海鲷品质的影响,结果表明,不同解冻方式对凤尾鱼pH值影响较为接近,但冷藏解冻对沙丁鱼和海鲷的pH值影响最大;微波解冻后鱼肉的TVB-N值最低,但对鱼肉色泽影响最大;水解冻对pH值影响最小,感官评定得分最高,是最为理想的解冻方式。
目前,对金枪鱼及副产品加工工艺研究较多,对金枪鱼解冻方式的研究多集中在空气解冻、静水解冻等传统解冻方式,且对于解冻过程中的水分迁移和肌肉组织结构研究较少。因此,本文综合比较空气解冻、静止水解冻、流水解冻和微波解冻4种方式下金枪鱼鱼肉持水力、色差、蛋白质溶解度等指标,结合低磁场核磁共振技术,通过光镜对解冻后金枪鱼鱼肉的组织结构进行观察,旨在获得能维持金枪鱼较好新鲜度的解冻方式,为金枪鱼解冻方式的研究提供参考与理论依据。
实验采用的是捕捞后超低温速冻切割,真空包装后贮藏于-55 ℃冰箱中的大目金枪鱼鱼块,购自浙江丰汇远洋渔业有限公司。
二甲苯、无水乙醇、10%的福尔马林、苏木精染色液、伊红染色液、改良型Bradford法蛋白浓度测定试剂盒、10×PBS缓冲液,生工生物工程(上海) 股份有限公司。
H-2050R型台式高速冷冻离心机,湖南湘仪实验室仪器开发有限公司;F2640A型福禄克多路采集热电偶NN.GD567M型微波炉,上海松下微波炉有限公司;MWS.8型微波工作站,加拿大FISO公司;UV-2100型紫外可见分光光度计,尤尼柯(上海)仪器有限公司;FA25型高剪切分散乳化机,上海FLUKO型弗鲁克流体机械制造有限公司;F2640A型福禄克多路采集热电偶,美国FLUKE公司;Leica CM1100冰冻切片机,德国徕卡测量系统有限公司;Eclipse E200生物显微镜,日本尼康仪器有限公司;PB-10精密数显酸度计,赛多丽斯科学仪器有限公司;PQ001台式脉冲核磁共振分析仪,上海纽迈公司。
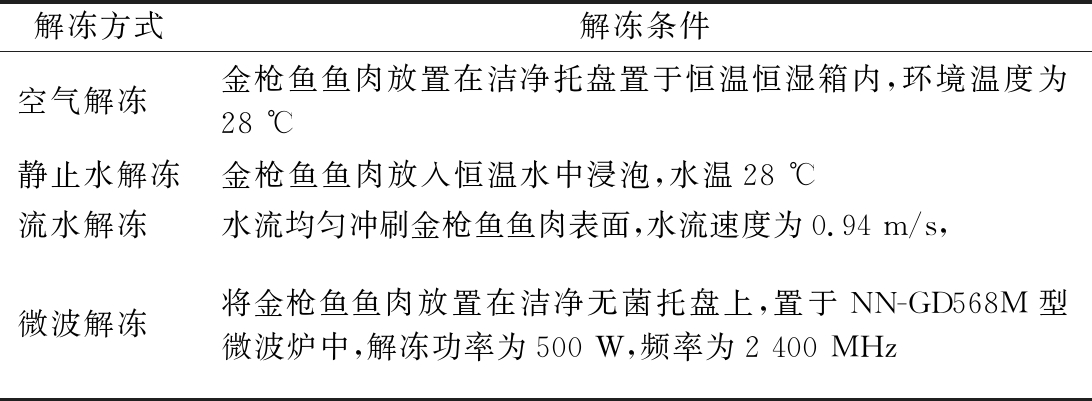
将金枪鱼鱼块从-55 ℃冰箱中取出,分别通过空气解冻、静止水解冻、流水解冻和微波解冻4种方式进行解冻,以金枪鱼鱼块中心温度作为解冻温度测量点,解冻终温为5 ℃(表1)。
表1 不同解冻方式解冻条件
Table 1 Thawing conditions for different thawing methods

解冻方式解冻条件空气解冻金枪鱼鱼肉放置在洁净托盘置于恒温恒湿箱内,环境温度为28 ℃静止水解冻金枪鱼鱼肉放入恒温水中浸泡,水温28 ℃流水解冻水流均匀冲刷金枪鱼鱼肉表面,水流速度为0.94 m/s, 微波解冻将金枪鱼鱼肉放置在洁净无菌托盘上,置于NN-GD568M型微波炉中,解冻功率为500 W,频率为2 400 MHz
1.4.1 解冻时间
空气解冻、流水解冻和静止水解冻采用多路热电偶测定温度,微波解冻采用光纤测温仪测定温度,将多个探头插入鱼体中心部位,每秒记录1次数据,金枪鱼鱼肉解冻至5 ℃时记录停止,从-55 ℃升温至5 ℃ 所需要的时间即为解冻时间。
1.4.2 解冻损失率
参考HONIKEL[8]的方法。解冻前的金枪鱼鱼肉在天平称重,记录质量为m1,解冻完成后,将解冻后流失掉的汁液倒掉,用吸水纸将金枪鱼肉表面汁液吸干,再次称重,称重并记录质量为m2,汁液损失率按照公式(1)计算。
![]()
(1)
1.4.3 持水力
参照ÖZOGUL等[9]的方法测定。称取2 g左右解冻后的金枪鱼鱼肉,质量记为m1,用滤纸包好,4 ℃, 5 000 r/min冷冻离心后去掉滤纸,称量纸称量并记质量为m2,冷冻离心,重复试验3次取平均值。按公式(2)计算。
![]()
(2)
1.4.4 质构
参考李念文等[10]的方法进行部分修改。将解冻后的鱼块切成1 cm×1 cm×2 cm的方块,每组实验各取6份样品,重复测定取平均值,对样品进行2次压缩测试,测定指标包括黏聚性、弹性、咀嚼度、硬度等。
1.4.5 核磁
参考李欣等[11]的方法,将金枪鱼鱼肉切成规格为2 cm×1 cm×2 cm的方块,放入磁场中心位置的射频线圈中心,使用CPMG序列,设置参数为:采样宽带SW=100 kHz,重复采样时间为4 000 ms,回波时间TE=0.500,回波个数Nech=8 000,重复采样次数2次,使用CPMG序列,采用分析软件进行迭代反演。
1.4.6 色差
将解冻后的金枪鱼鱼肉切块(1 cm×1 cm×2 cm),采用色差仪测定正反两面色差值,每面测定2次,采用红度指标(a*/b*)作为肉色变化的判定依据[12]。每次实验进行3次取平均值减小误差。
1.4.7 高铁肌红蛋白
称取2 g金枪鱼鱼肉碎肉,加入20 mL浓度为 0.02 mol/L的PBS溶液,均质匀浆1 min,冷冻离心10 min(10 000×g匀浆,4 ℃),吸取上清液,采用分光度计分别测A525 nm、A545 nm、A565 nm、A572 nm。高铁肌红蛋白(metmyoglobin, MetMb)的含量按照公式(3)计算。
MetMb/%=
![]()
(3)
1.4.8 pH
取5 g解冻后的金枪鱼鱼肉,均质后加入50 mL的蒸馏水静置20 min,取上清液测定pH值。
1.4.9 蛋白质溶解度
金枪鱼肌肉中的可溶性蛋白质主要分为水溶性的肌浆蛋白和盐溶性的肌原纤维蛋白,其测定参考JOO等[13]和NIU等[14]的方法并稍作修改。
肌浆蛋白的含量测定:称取2 g的金枪鱼鱼肉,加入40 mL预冷的磷酸钾缓冲液(浓度0.1 mol/L)均质(14 000 r/min,1 min)后将溶液冷冻离心20 min(10 000 r/min,4 ℃),取上清液测定蛋白质的溶解度。
肌原纤维蛋白的含量测定:称取2 g的金枪鱼肉,加入18 mL蒸馏水,均质(14 000 r/min,1 min)后将溶液冷冻离心10 min(10 000 r/min,4 ℃),过滤获得沉淀,再次加入18 mL质量分数为3%的NaCl溶液,均质离心后取上清液。
蛋白质含量均采用Bradford试剂盒检测,每组实验均重复3次。
分别采用空气解冻、静止水解冻、流水解冻和微波解冻4种方法在相同温度条件下对金枪鱼鱼肉进行解冻,不同解冻方式的解冻时间差异显著,如图1所示。空气解冻在中心温度到达5 ℃后的解冻速率变化平缓,微波解冻速度最快且解冻过程中的温度变化速率均匀,但是由于鱼肉内部极性分子分布不均匀,会导致金枪鱼鱼肉不同部位吸收热量差异较大[15],随着解冻的进行,解冻生成的水分会吸收更多的热量,最终可能会导致鱼肉部分熟化,严重影响金枪鱼鱼肉的品质与商业价值。静止水解冻相对于空气解冻,解冻时间较短,这是由于水和空气相比,比热容较大,能够迅速传导热量,大大缩短解冻时间,解冻速率也较为平缓。采用流水解冻,会加剧热量的交换,提高解冻效率,比静止水解冻缩短近一半的解冻时间,但流水解冻对金枪鱼鱼肉表面冲刷,解冻速率会有一定的波动。
不同解冻方式的汁液损失率如图2所示。可以看出,4种解冻方式中,流水解冻的解冻损失率为13.52%,在4种解冻方式中解冻损失率最高。

a-空气解冻;b-静止水解冻;c-流水解冻;d-微波解冻
图1 不同解冻方式解冻曲线
Fig.1 Thawing curves with different thawing methods
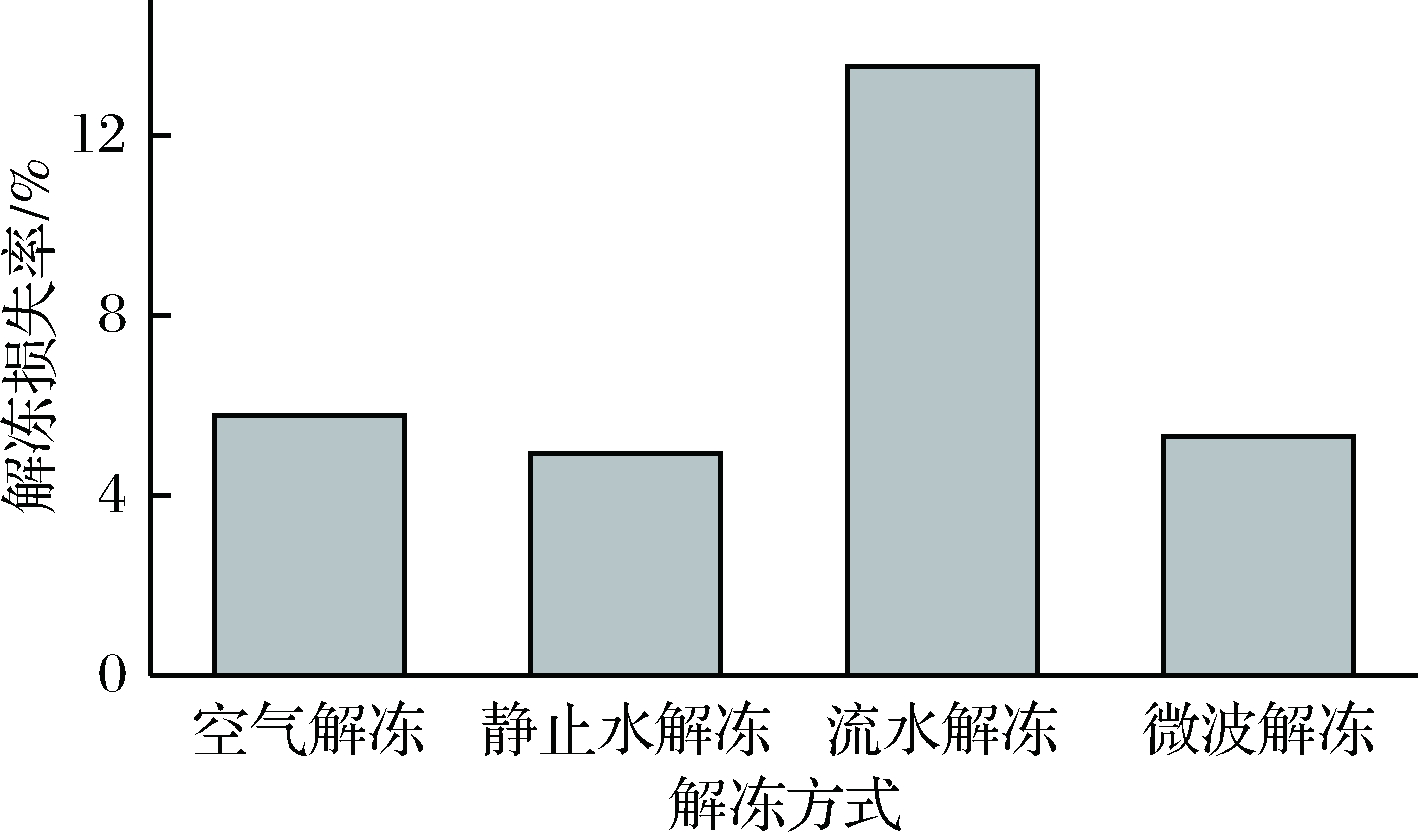
图2 不同解冻方式解冻损失率对比
Fig.2 Comparison of juice loss rate in different thawing methods
这是因为流水解冻过程中,冻结金枪鱼鱼肉直接和水分进行接触,部分可溶性蛋白通过鱼肉切面直接溶入水中,与静止水解冻相比,提高了将近一半的解冻速率。空气解冻的解冻损失率其次,为5.78%,这是因为空气解冻过程中,虽然不易流动水会转化成自由水损失,但空气解冻时间较长,减缓了金枪鱼肉解冻过程中的汁液损失。微波解冻的解冻损失率要大于静止水解冻的解冻损失率,这是因为鱼肉是多相非均匀的物质,在解冻加热的过程中,金枪鱼鱼肉各部分对热量的吸收程度不同,微波加热速率较快,使得金枪鱼鱼肉部分熟化,加速了水分的损失,且微波解冻对蛋白质破坏较大,冰晶融化后的水分子不能重新和蛋白质分子重新结合,造成较大的解冻损失率。通过对解冻时间和解冻损失率的比较,发现解冻时间和解冻损失率呈非线性关系,这与余小领等[16]用不同解冻方式对猪肉的研究结果相一致。
持水力是指在肌肉受到外力作用时,肌肉组织通过物理方式保持水分的能力。肌肉中的水分主要存在于细胞内部,解冻过程中蛋白质的变性以及细胞的损伤破裂都会影响到持水力的变化。由图3可知,空气解冻的持水力最大,微波解冻的持水力最小。这可能是因为空气解冻时间较长,自然对流解冻可以缩小金枪鱼鱼肉表面和中心温度之间的温差,且空气解冻在干燥的环境下,避免了细胞吸水涨破而使水分损失;微波解冻后的pH值为5.56,接近肌球蛋白的等电点,此刻蛋白质有相等的正负电荷,彼此吸引,对水分的吸引力减小,且微波解冻过程中,金枪鱼鱼肉内部温度较高,肌球蛋白头部变性,致使持水力下降。经流水解冻和静止水解冻后的金枪鱼鱼肉,持水力差异不显著,同空气解冻相比,用时较短,可快速通过-5~0 ℃ 这一最大冰晶溶解带,有效减小蛋白质的变性和细胞的损伤,较好的维持金枪鱼鱼肉的持水力。
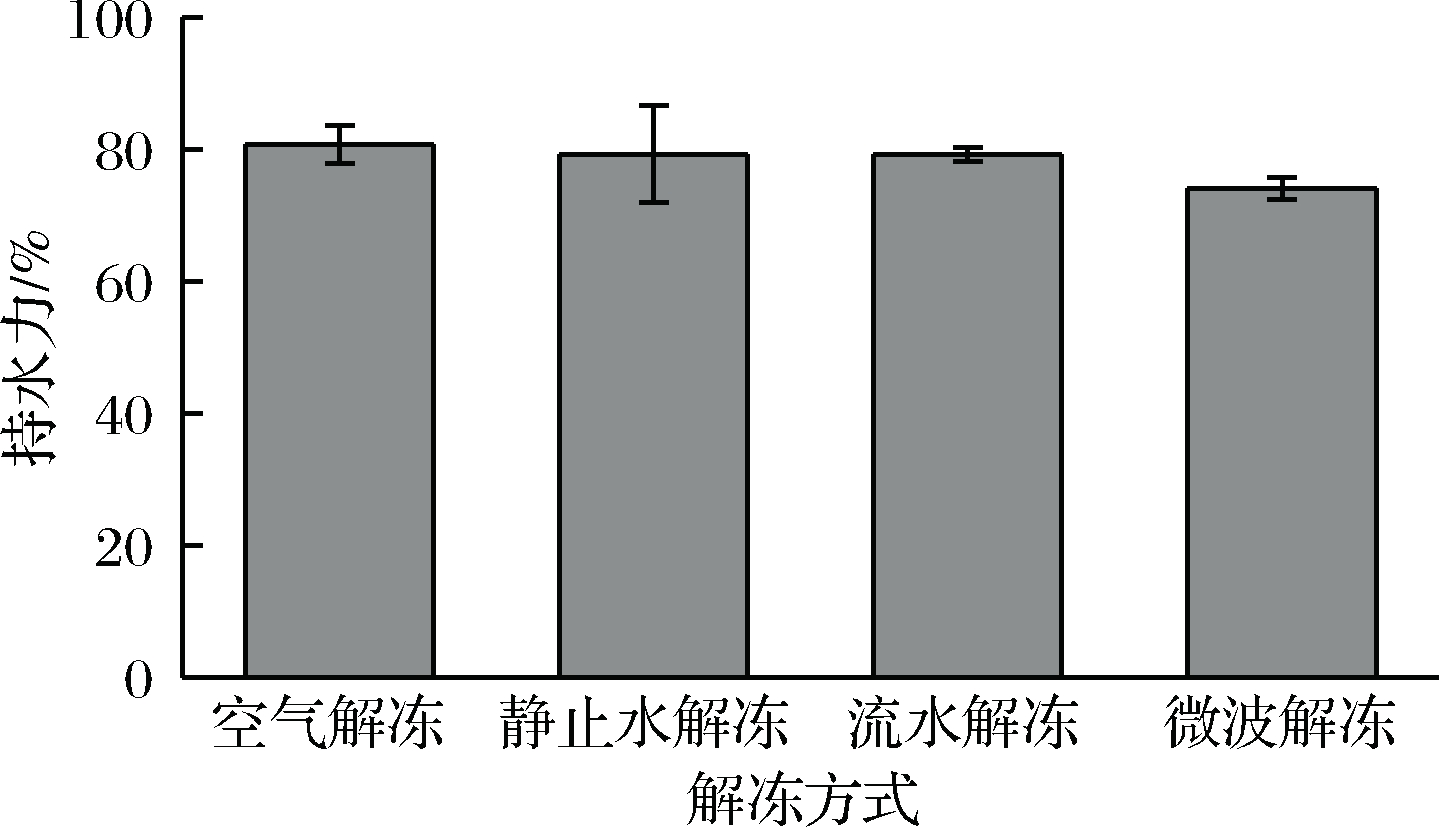
图3 不同解冻方式持水力对比
Fig.3 Hydraulic comparison of different thawing methods
金枪鱼鱼肉在解冻过程中,蛋白质变性引起H+的释放,新鲜金枪鱼鱼肉pH值一般维持在7.0~7.3,随着解冻过程中水分的损失,H+浓度逐渐增加,4种解冻方式中,金枪鱼鱼肉的pH值均有所降低,如图4所示,空气解冻后金枪鱼鱼肉pH值为6.86, 静止水解冻后金枪鱼鱼肉pH值为6.03,流水解冻后金枪鱼鱼肉pH值为5.81,微波解冻后金枪鱼鱼肉pH值为5.56,可以看出4组鱼肉pH值均维持在6.0左右。静止水解冻后金枪鱼鱼肉pH值与6.0最为接近,能最大程度地保持金枪鱼鱼肉解冻后的新鲜程度[17]。
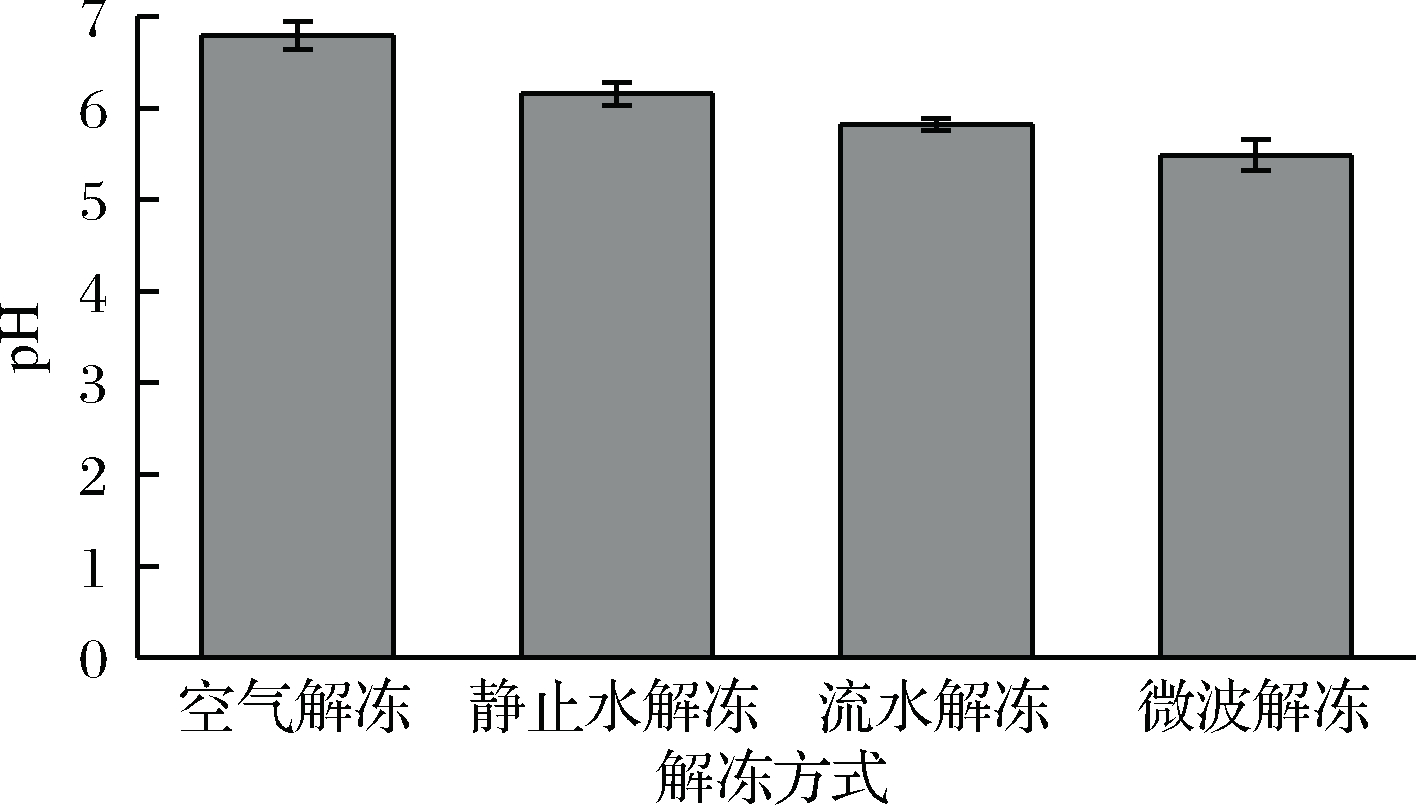
图4 不同解冻方式pH值对比
Fig.4 Comparison of pH values for different thawing methods
金枪鱼鱼肉肌肉生理学、生物化学和微生物学综合作用的结果可以直观反映在肉色上[18]。虽然金枪鱼鱼肉的色泽对其营养价值和风味没有任何影响,却是消费者在购买金枪鱼鱼肉时重要的判断标准[19]。新鲜的金枪鱼鱼肉由于富含氧合肌红蛋白,呈现鲜红色,当氧合肌红蛋白进一步氧化形成高铁肌红蛋白时则鱼肉呈现出暗红色,相比单独使用a*值或b*值,红度值(a*/b*)则能更好地反映出肉色的感官评价[12]。不同解冻方式下金枪鱼鱼肉的红度值变化如图5所示,静止水解冻的金枪鱼鱼肉红度值最高,颜色最好,这是由于静止水解冻过程中金枪鱼鱼肉的解冻速度较快,且与空气隔绝,有效降低了氧合肌红蛋白的氧化程度,最大限度地保证了金枪鱼鱼肉的品质。微波解冻的金枪鱼鱼肉颜色变化最大,这是由于微波加热迅速,导致金枪鱼鱼肉蛋白质变性,红度值随之降低。流水解冻与静止水解冻虽然同属于水解冻,但水在流经鱼肉表面时,会携带大量气泡,气泡中所含氧气加快了金枪鱼鱼肉氧合肌红蛋白的氧化程度,使鱼肉发生褐变。
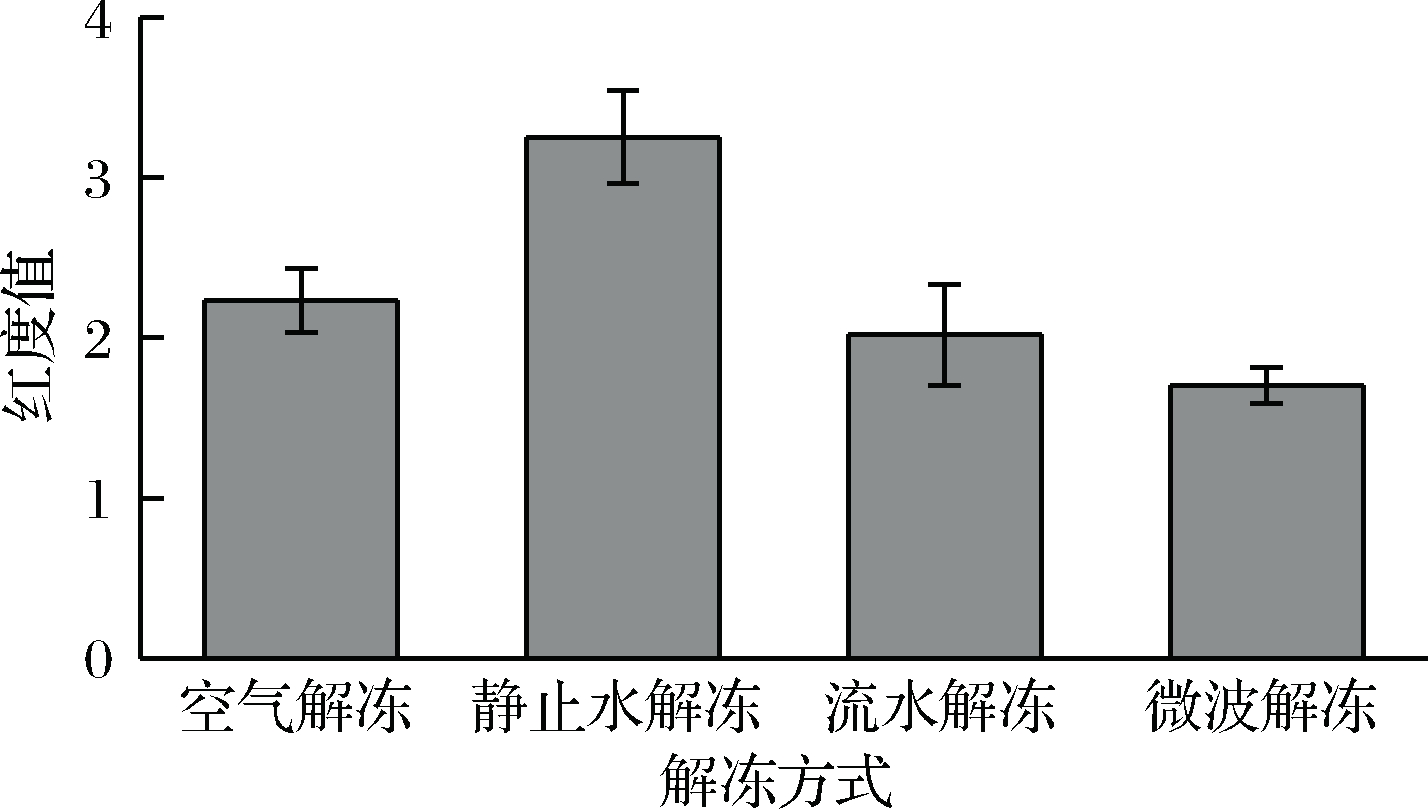
图5 不同解冻方式红度值对比
Fig.5 Color contrast of different thawing methods
高铁肌红蛋白的含量与金枪鱼鱼肉的色泽密切相关。在贮藏及解冻过程中,肌红蛋白、氧合肌红蛋白、高铁肌红蛋白三者的比例决定了金枪鱼鱼肉的肉色变化,变色程度取决于高铁肌红蛋白的生成率[20]。金枪鱼鱼肉中高铁肌红蛋白含量在20%以下时呈现鲜红色,升至30%时呈现暗红色,大于50%时呈现红褐色,70%以上呈现褐色。新鲜的金枪鱼鱼肉中含有大量丰富的酶[21],通过将金枪鱼鱼肉还原并与氧气结合形成氧合肌红蛋白,便能使鱼肉保持鲜亮的血红色。如图6所示,4种解冻过程中,流水解冻的金枪鱼鱼肉MetMb含量最高,空气解冻其次,这是因为流水解冻的汁液损失率最为严重,金枪鱼鱼肉中的酶会随着汁液而大量损失,而空气解冻过程中O2含量充足,更有利于高铁肌红蛋白的形成。微波解冻后的金枪鱼鱼肉中MetMb含量低于20%,但在实际操作中,微波使鱼肉部分熟化,造成金枪鱼鱼肉色泽不均匀,因此,相比与其余3种解冻方式,静止水解冻能更好的保持金枪鱼鱼肉的外观品质。
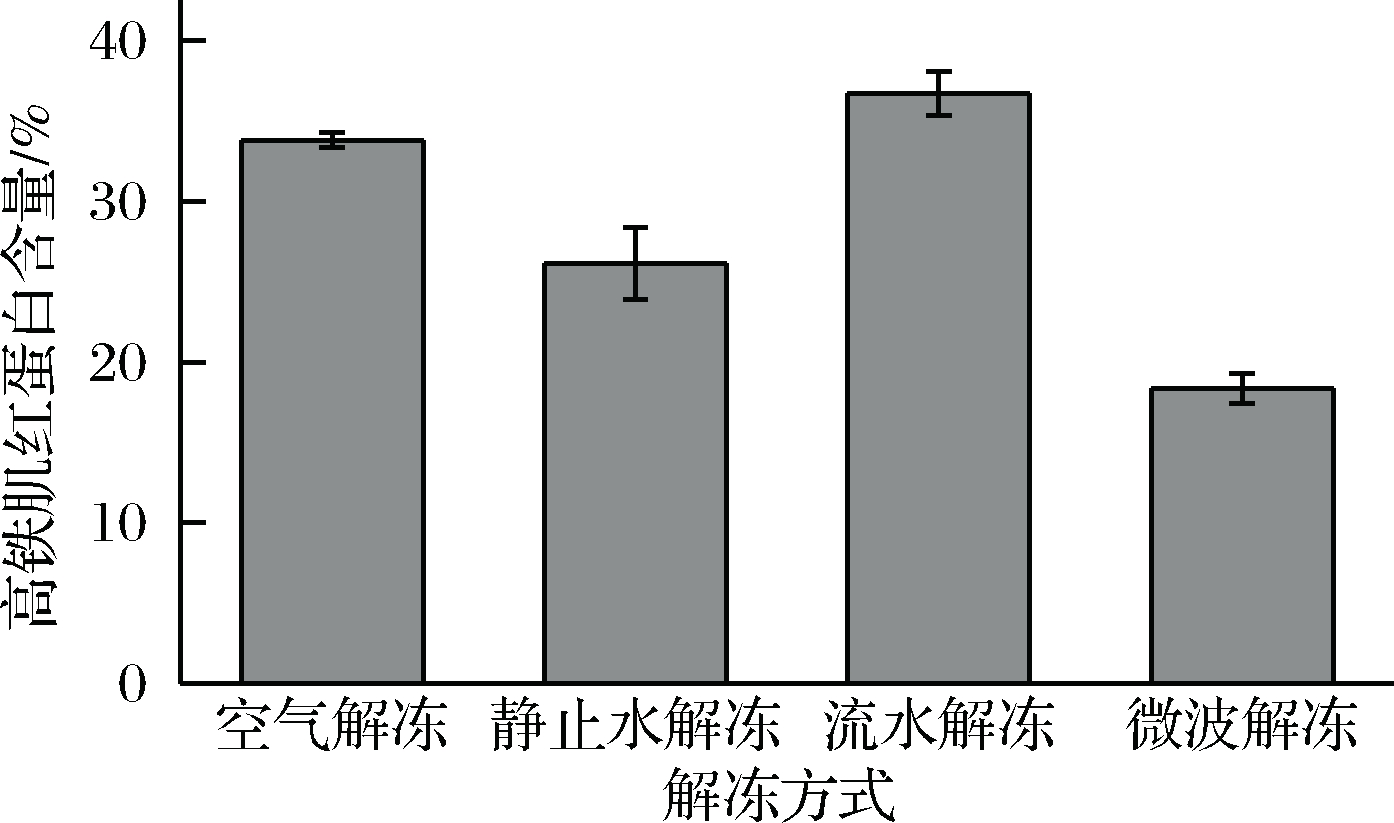
图6 不同解冻方式高铁肌红蛋白含量对比
Fig.6 Comparison of different levels of thawing myoglobin in different thawing methods
根据肌肉中蛋白质的溶解性质不同,金枪鱼肌肉中的蛋白质可以分为水溶性的肌浆蛋白、盐溶性的肌原纤维蛋白以及不可溶解的基质蛋白。其中肌原纤维蛋白在鱼体中占50%~70%,肌浆蛋白占20%~50%,而基质蛋白只占极少部分。肌原纤维蛋白和肌浆蛋白是金枪鱼鱼肉中的重要营养成分,鱼肉品质的好坏和蛋白质的溶解程度紧密相关。金枪鱼鱼肉在解冻过程中,蛋白质含量受外界条件的影响,导致不同程度的结构损伤和蛋白质变性,从而影响到金枪鱼鱼肉的新鲜度和营养价值。如图7所示,不同的解冻方式对金枪鱼鱼肉中的蛋白质含量有着不同程度的影响,微波解冻速度最快,可溶性蛋白含量最低;流水解冻方式下肌浆蛋白和肌原纤维蛋白的含量最高,效果最好。这可能是由于微波解冻的过程中,极性分子的迅速受热导致大量蛋白质变性。在解冻过程中,不饱和脂肪酸氧化生成自由基,会与蛋白质相结合,也会引起蛋白含量的降低[22]。因此,静止水解冻、空气解冻和流水解冻3种解冻方式的蛋白含量与解冻时间具有一定的相关性。流水和静止水解冻时间短,蛋白质变性程度不明显,对金枪鱼肉的品质影响相对较小。空气解冻由于解冻时间过长,肌原纤维蛋白和肌浆蛋白含量较低,影响鱼肉的品质。
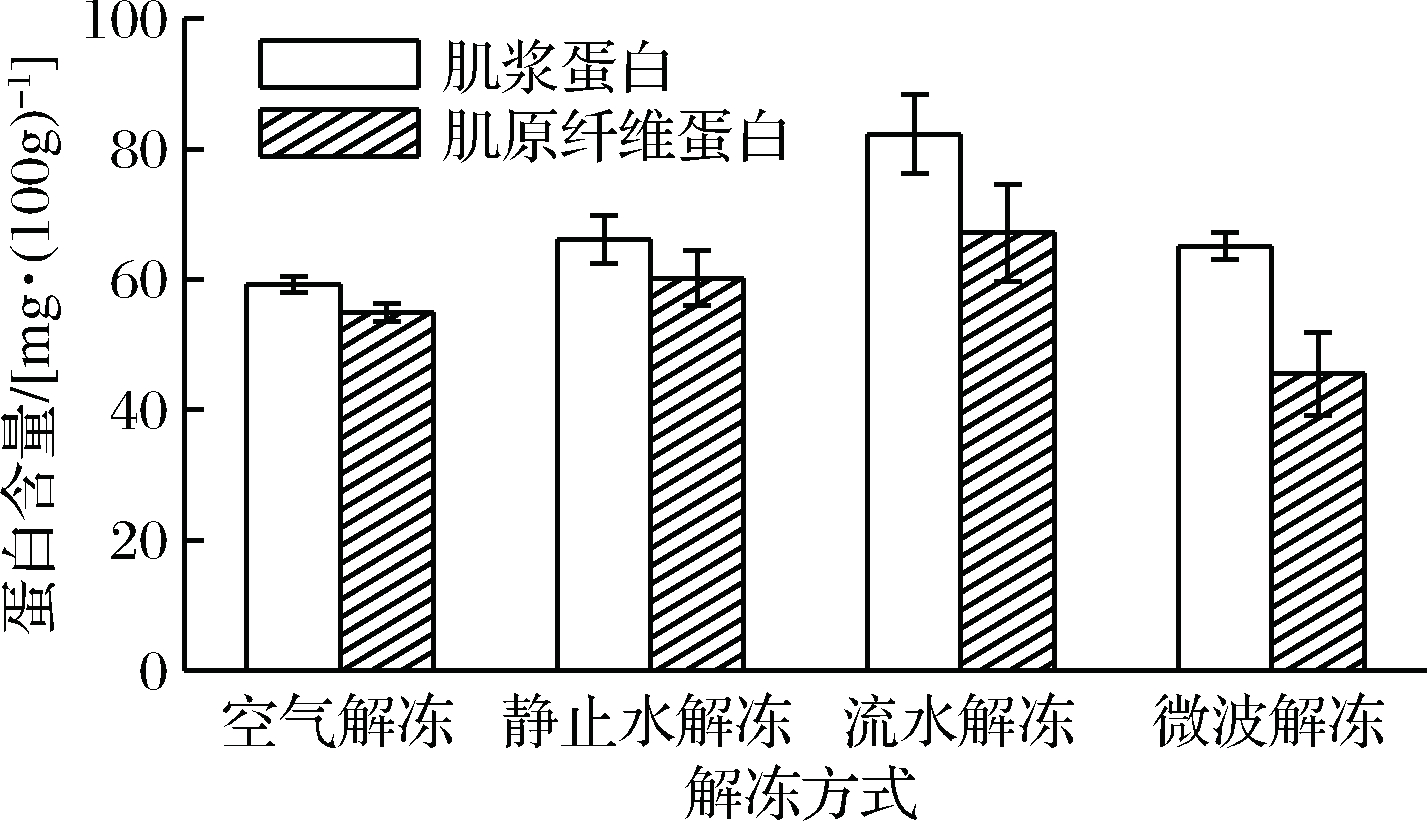
图7 不同解冻方式肌肉全蛋白含量对比
Fig.7 Comparison of total protein content of muscle in different thawing ways
质构包括硬度、恢复力、咀嚼度、胶着性、黏附性等,是评价食品物理特性的重要手段。鱼肉进入自溶阶段以后,蛋白质会逐渐分解,弹性、硬度以及咀嚼性等随之降低,鱼肉的口感变差,食用品质遭到破坏。本文选取了硬度、黏附性、弹性、内聚性、胶着性、咀嚼度和恢复力等几个指标对不同解冻方式下金枪鱼鱼肉的品质进行评价。如图8所示,不同解冻方式对各个质构指标的影响基本一致。
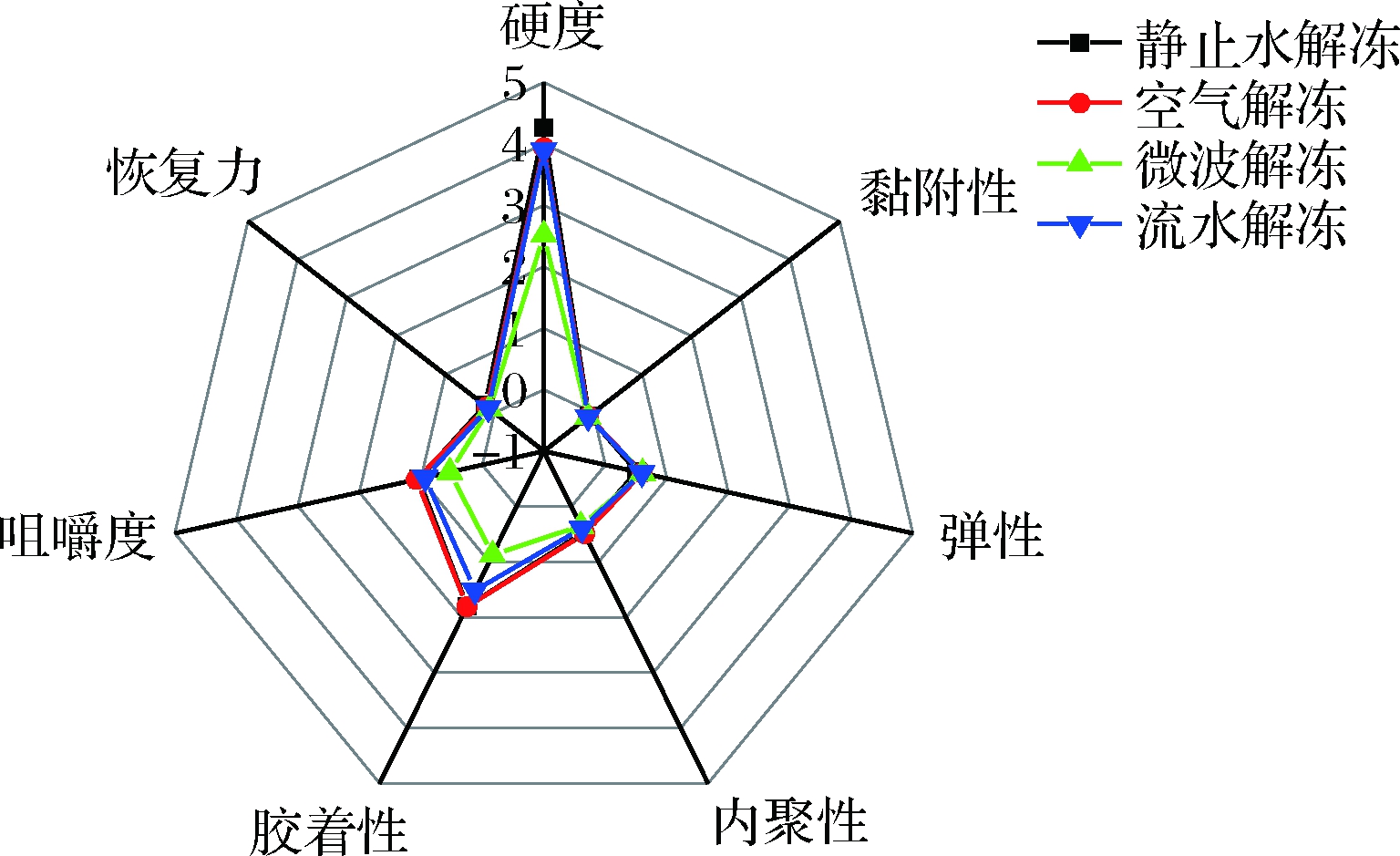
图8 不同解冻方式对质构的影响
Fig.8 Effects of different thawing methods on texture
其中,金枪鱼鱼肉的内聚性、黏附性、恢复力和弹性等指标受不同解冻方式的影响相对较小;硬度、咀嚼度和胶着性受解冻方式的影响较大。静止水解冻下的金枪鱼鱼肉硬度、胶着性和咀嚼度最高,微波解冻后的金枪鱼鱼肉硬度等较小,这与李天翔等[23]的结论相符合。由于不同解冻方式对金枪鱼鱼肉中蛋白质变性程度的影响不同,使得金枪鱼鱼肉的质构特性的下降程度也不尽相同。微波解冻过程中,由于鱼肉中蛋白质的变性以及肌肉组织纤维的破坏,因此,微波解冻的硬度咀嚼度和胶着性都明显少于其他几种解冻方式。空气解冻和水解冻的金枪鱼质构指标较好,其中静止水解是有最硬度和胶着性。
金枪鱼的冻结过程中伴随着冰晶的生成与长大,对细胞的完整性具有一定的破坏性。解冻过程中,冰晶融化速率不同,不同的解冻方式均会对金枪鱼的肌肉组织造成不同程度的机械损伤,使微观结构产生不同程度的劣变。不同解冻方式下金枪鱼鱼肉组织结构变化如图9所示。
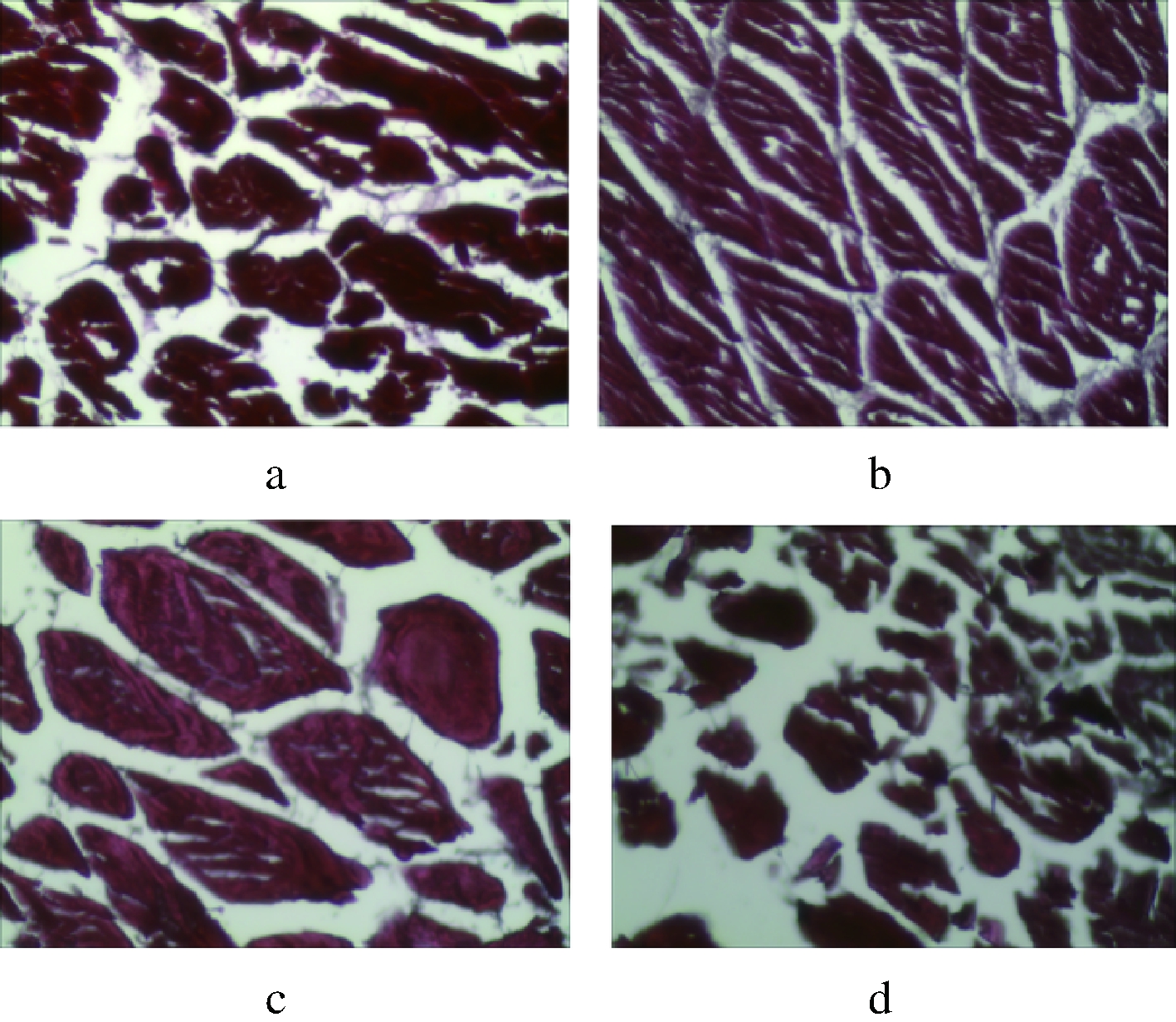
a-空气解冻;b-静止水解冻;c-流水解冻;d-微波解冻
图9 不同解冻方式对组织结构的影响
Fig.9 Effects of different thawing methods on tissue structure
微波解冻的金枪鱼肉肌纤维间隙最大,结缔组织破坏也较为严重,这是因为微波解冻不同于其余3种解冻方式,对金枪鱼鱼肉直接进行加热,温度最高,解冻迅速,使蛋白质遭到大量的破坏。空气解冻的金枪鱼肉也有较大的肌纤维间隙,这可能是因为空气解冻时间较长,金枪鱼鱼肉组织直接暴露在空气中,导致微生物的大量繁殖,分解了鱼肉组织中的蛋白质,使得肌肉组织的完整性遭到破坏,鱼肉组织失去了原本的致密性。相比于流水解冻,静止水解冻的金枪鱼鱼肉间隙较小,肌束结合更为紧密,这是因为采用静止水解冻,速率更为均匀,流水解冻时,与水流直接接触的部分冰晶先行融化,解冻更为迅速,由于液体水蒸气的气压大于冰晶的水蒸气压[24],冰晶融化的液相水向低压处的组织纤维间隙处聚集,增大了金枪鱼鱼肉的组织间隙,金枪鱼鱼肉肉质变得松散。
2.10 肌肉含水量及分布状态
肌肉中的水分主要以结合水、不易流动水和自由水这3种形式存在,结合水存在于细胞内部,与分子相互作用;不易流动水存在于肌纤维以及网状组织之间;自由水则可以自由流动,存在于细胞以外[25]。目前食品中的含水状态广泛采用低场核磁共振技术(low field nuclear magnetic resonance,LF-NMR)测定[26],通过对1H质子的横向弛豫时间(T2)在肉制品中的衰减规律来测定3种不同水分的含量[27],以T21、T22、T23所对应的峰面积所占比率来表示。测定结果如图10所示,弛豫时间最短0~10 ms的峰(T21)代表了结合水,弛豫时间在10~150 ms的峰(T22)代表了不易流动水,弛豫时间为150~1 245 ms的峰(T23)表示存在于外肌纤维空间的自由水。T21、T22、T23所对应的峰面积表示了3种状态的相对含量,3种水分状态可以互相转换,迁移率与水分子和大分子之间的氢键自由能的变化相关。
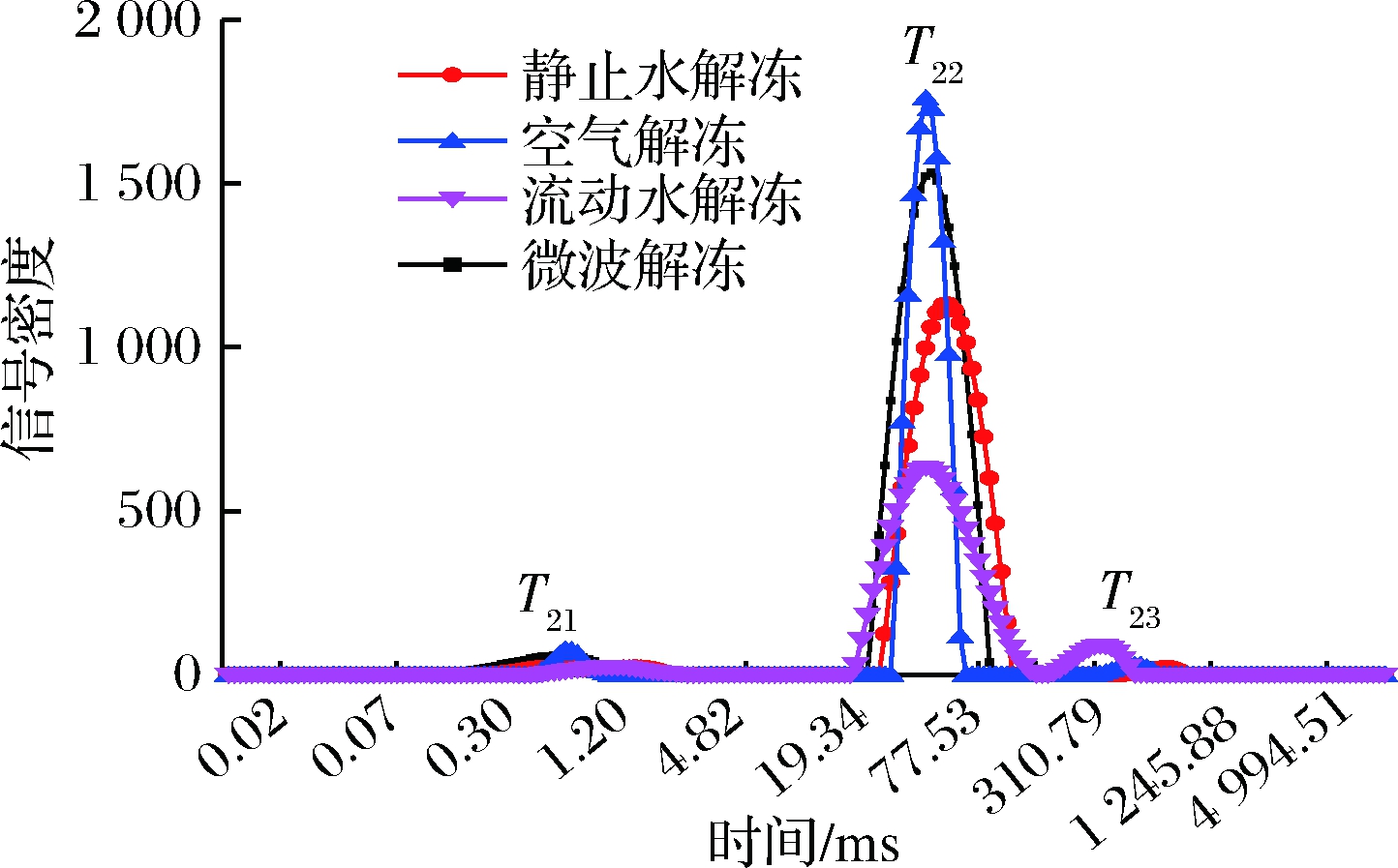
图10 不同解冻方式对横向弛豫时间的影响
Fig.10 Effect of different thawing methods on transverse relaxation time
由图11可以看出,在3种水状态含量对比中,不易流动水占到90%以上,微波解冻的总峰面积最大,含水量最高,结合水含量比例最高,这是由于微波解冻时间短,速度快,结合水转化较少。
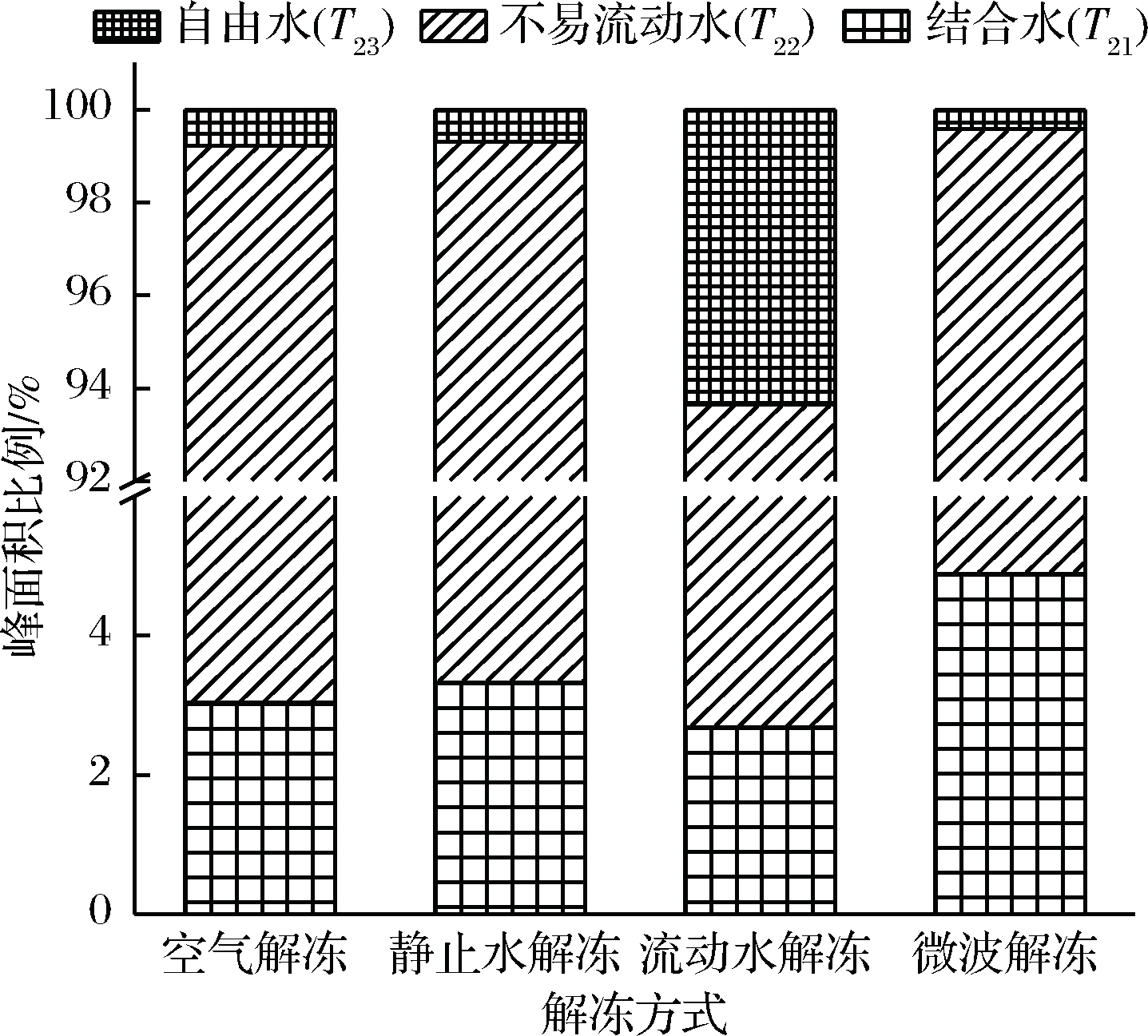
图11 不同解冻方式对峰面积比例
Fig.11 Peak area ratio of different thawing methods
空气解冻组的解冻时间最长,随着蛋白质的变性,结合水转化为不易流动水,导致不易流动水含量增加,汁液损失率增加,总含水量也最小。流动水解冻组中自由水的含量占比最高,不易流动水含量较低,这是由于流动水对组织结构造成破坏,导致肌纤维组织间的不易流动水转换成为自由水。
利用LF-NMR技术还可以直观观测到水分分布情况,通过样品所反射出的信号强度与水分含量成正比。如图12所示为不同解冻方式后鱼肉中水分分布情况,其中颜色越亮,表示该部分含水率越高,颜色越暗,表示样品的含水量越低[28]。微波解冻更多的呈现黄红色,表示1H质子含量较高,说明微波解冻水分含量较高,能够较好地保存水分含量,能够有效降低汁液损失率。
2.11 相关性
为了揭示指标间的关联关系,对比不同解冻方式的解冻效果,实验数据采用SPSS软件进行相关性分析,分析结果如表2所示。
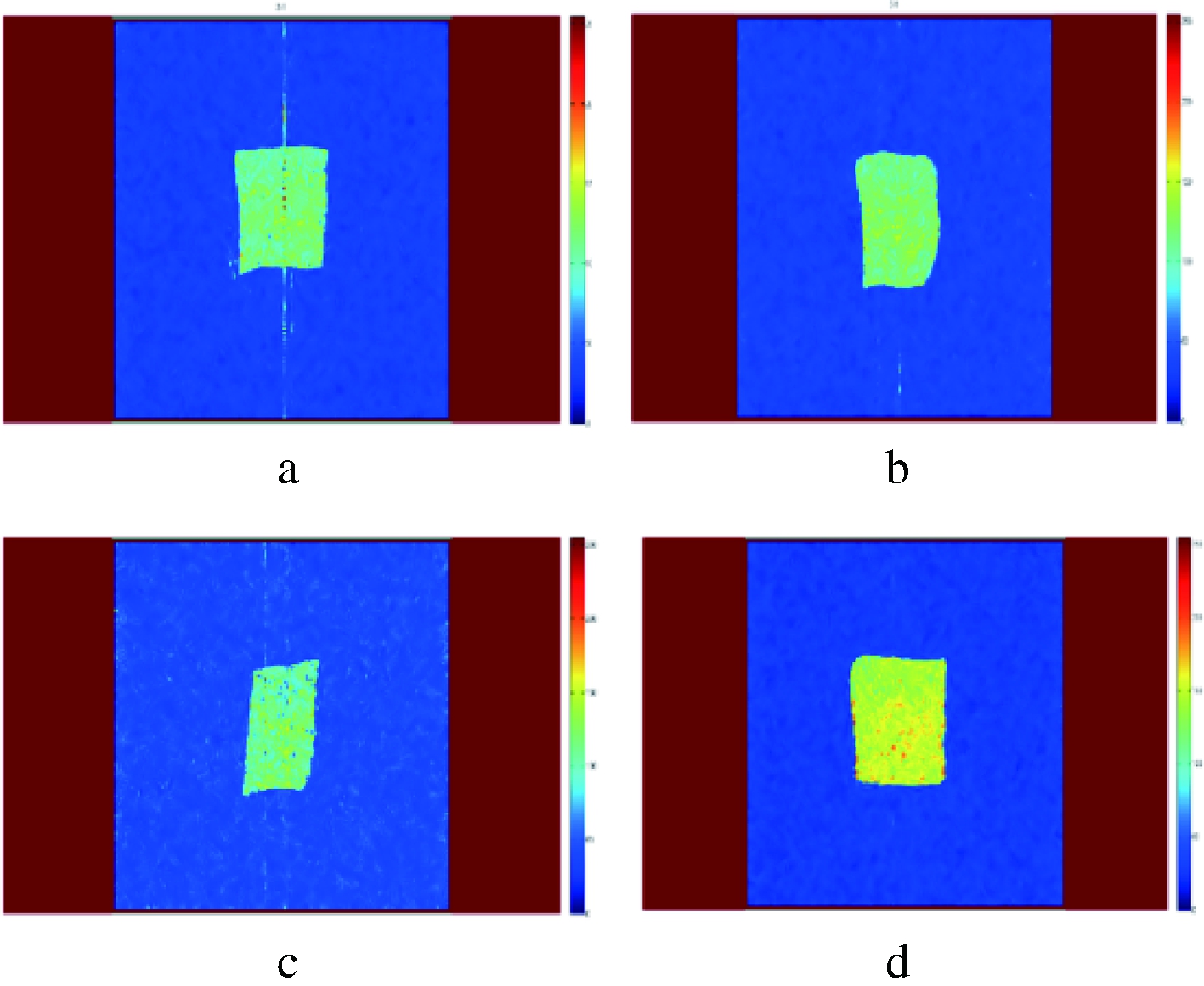
a-空气解冻;b-静止水解冻;c-流水解冻;d-微波解冻
图12 不同解冻方式对核磁图像
Fig.12 Different thawing methods for NMR images
表2 解冻指标相关性分析
Table 2 Correlation analysis of thawing indexes
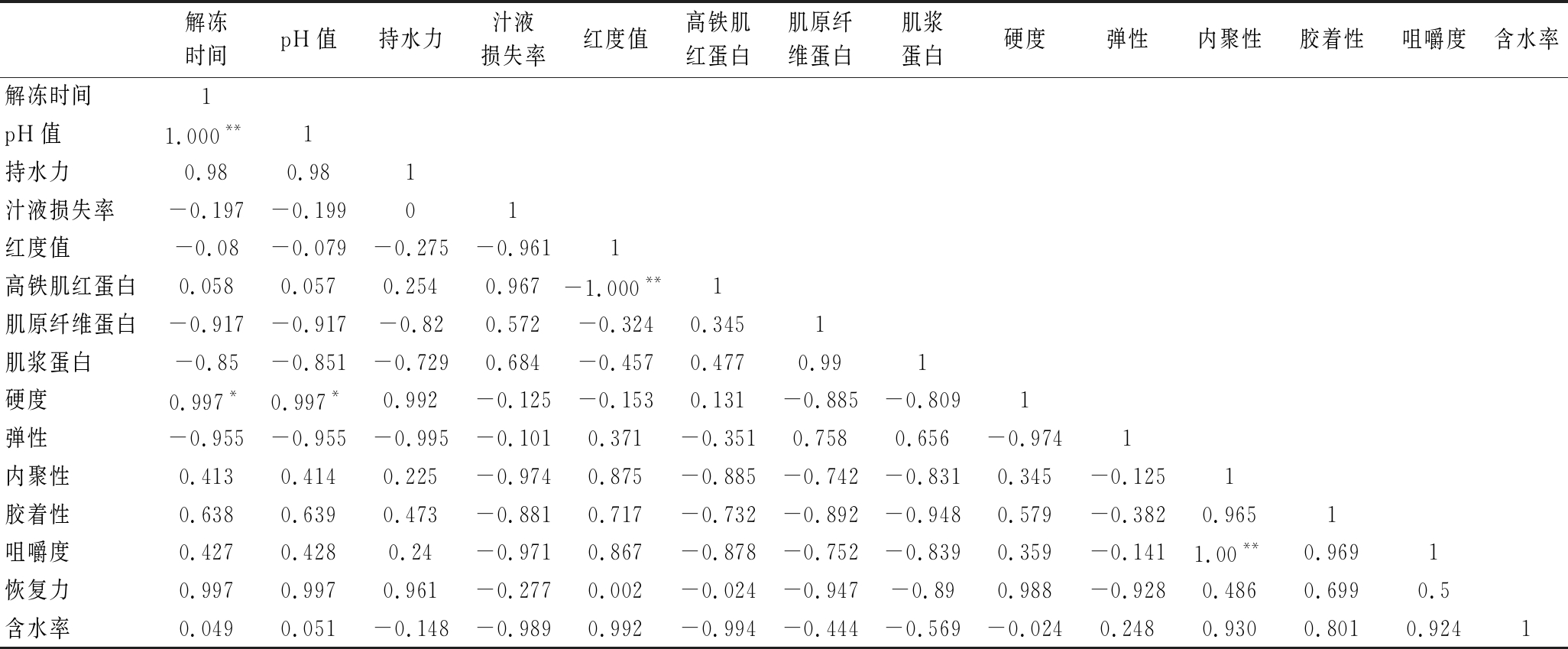
解冻时间pH值持水力汁液损失率红度值高铁肌红蛋白肌原纤维蛋白肌浆蛋白硬度弹性内聚性胶着性咀嚼度含水率解冻时间1pH值1.000**1持水力0.980.981汁液损失率-0.197-0.19901红度值-0.08-0.079-0.275-0.9611高铁肌红蛋白0.0580.0570.2540.967-1.000**1肌原纤维蛋白-0.917-0.917-0.820.572-0.3240.3451肌浆蛋白-0.85-0.851-0.7290.684-0.4570.4770.991硬度0.997*0.997*0.992-0.125-0.1530.131-0.885-0.8091弹性-0.955-0.955-0.995-0.1010.371-0.3510.7580.656-0.9741内聚性0.4130.4140.225-0.9740.875-0.885-0.742-0.8310.345-0.1251胶着性0.6380.6390.473-0.8810.717-0.732-0.892-0.9480.579-0.3820.9651咀嚼度0.4270.4280.24-0.9710.867-0.878-0.752-0.8390.359-0.1411.00**0.9691恢复力0.9970.9970.961-0.2770.002-0.024-0.947-0.890.988-0.9280.4860.6990.5含水率0.0490.051-0.148-0.9890.992-0.994-0.444-0.569-0.0240.2480.9300.8010.9241
注:“**”表示相关性极显著(P<0.05);“*”表示相关性显著(0.01<P<0.05)。
由表2可知,不同指标之间存在着一定的相关性,解冻时间与pH值、硬度呈正相关,与肌浆蛋白含量和弹性呈负相关。4种解冻方式中,空气解冻时间最长,pH值和鱼肉硬度最高,鱼肉的弹性较差,肌浆蛋白和肌原纤维蛋白变性程度较大,影响鱼肉的口感和品质。pH值和持水力变化相比较,发现二者呈正相关,这与CHOW等[29]的研究相一致。高铁肌红蛋白含量和红度值存在极显著负相关(P<0.05),新鲜的金枪鱼呈鲜红色,解冻后,高铁肌红蛋白的含量越高,红度值越低,肉色褐变越严重。咀嚼度、内聚性、胶着性和含水率之间呈正相关,与汁液损失率成负相关。因此,不同解冻方式中,汁液损失率越大,含水率越低,质构指标下降越明显,这也与刘欢等[30]所得到的结论具有一致性。
本文采用4种不同解冻方式分别对金枪鱼鱼肉块进行解冻,测定了持水力、色差、质构等指标并通过低磁场核磁共振手段分析了水分迁移。结果表明,空气解冻组解冻时间最长,蛋白含量较低,氧化生成的高铁肌红蛋白较多,且高铁肌红蛋白和红度值呈正相关,因此鱼肉的色泽和品质较差。持水力和pH值也呈正相关,微波解冻组解冻时间最短,持水力和pH值最低,鱼肉含水量较高,当冰晶解冻成液态水后,鱼肉出现了严重的受热不均的情况,使鱼肉的蛋白含量降低,组织结构变得稀松,降低了鱼肉的口感和商品价值。静止水解冻和流水解冻对鱼肉的硬度、内聚性和胶着性等影响较小,解冻后的金枪鱼蛋白含量较高,但流水解冻组汁液损失率较高,含水率较低。4种解冻方式中,静止水解冻组汁液损失率最低、红度值和硬度最好,pH值、含水率、蛋白含量也较高,对肌纤维组织结构的影响最小,是最适金枪鱼的解冻方式。
[1] 全晶晶, 蔡江佳, 郑平安, 等. 鲣鱼肌肉品质改良研究[J]. 中国食品学报, 2013, 13(7):122-129.
[2] 苏阳,章超桦,曹文红,等.南海产3种金枪鱼普通肉、暗色肉营养成分分析与评价[J].广东海洋大学学报,2015,35(3):87-93.
[3] NAKAMURA Y N, ANDO M, SEOKA M, et al. Changes of proximate and fatty acid compositions of the dorsal and ventral ordinary muscles of the full-cycle cultured Pacific bluefin tuna Thunnus orientalis, with the growth[J]. Food Chemistry, 2007, 103(1):234-241.
[4] 于刚, 杨少玲, 张慧,等. 不同冻结方式对黄鳍金枪鱼品质变化的比较研究[J]. 食品工业科技, 2015, 36(10):325-329.
[5] 李念文, 谢晶, 周然,等. 大目金枪鱼外部与内部解冻法的品质变化[J]. 食品工业科技, 2013, 34(16):84-87.
[6] 刘燕, 王锡昌, 刘源. 黄鳍金枪鱼块常用解冻方法的比较[J]. 食品科学, 2010, 31(15):8-12.
[7] DINSER T, CADVNC, CAKLI, et al. Effects of different thawing methods on the freshness quality of fish[J]. Journal of Fisheries & Aquatic Sciences, 2015,26(4)253-256.
[8] HONIKEL K O . Reference methods for the assessment of physical characteristics of meat[J]. Meat Science, 1998, 49(4):447-457.
[9]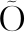 ZOGUL Y,
ZOGUL Y,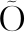 ZYURT G,
ZYURT G,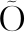 ZOGUL F, et al. Freshness assessment of European eel (Anguilla anguilla) by sensory, chemical and microbiological methods[J]. Food Chemistry, 2005, 92(4):745-751.
ZOGUL F, et al. Freshness assessment of European eel (Anguilla anguilla) by sensory, chemical and microbiological methods[J]. Food Chemistry, 2005, 92(4):745-751.
[10] 李念文, 谢晶, 周然,等. 真空解冻工艺对金枪鱼品质的影响[J]. 食品工业科技, 2013, 34(23):84-87.
[11] 李欣, 苏珊珊, 马俪珍, 等. 利用LF-NMR研究牛肉粒微波干燥过程中水分迁移和分布变化[J]. 食品科技, 2013(1):145-149.
[12] 廖明涛,冻藏条件下蓝鳍金枪鱼鱼由色泽变化的研究[D].杭州:浙江工商大学,2013.
[13] JOO S T, KAUFFMAN R G, KIM B C, et al. The relationship of sarcoplasmic and myofibrillar protein solubility to colour and water-holding capacity in porcine longissimus muscle[J]. Meat Science, 1999, 52(3):291-297.
[14] NIU L, RASCO B A, TANG J, et al. Relationship of changes in quality attributes and protein solubility of ground beef under pasteurization conditions[J]. LWT - Food Science and Technology, 2015, 61(1):19-24.
[15] 崔瑾. 冷冻鱼的微波解冻方法研究[D].大连:大连工业大学, 2012.
[16] 余小领, 李学斌, 闫利萍, 等.不同冻结和解冻速率对猪肉保水性和超微结构的影响[J]. 农业工程学报, 2007(08):261-265.
[17] 福田裕. 冷冻金枪鱼的质量评价法[R]. 上海: 金枪鱼的鲜度保持与加工技术国际研讨会,2009.
[18] 路昊, 包建强. 黄鳍金枪鱼肉在不同冻藏温度下品质变化的动力学研究[J]. 现代食品科技, 2007, 23(2):11-13.
[19] LAGERSTEDT ,ENF
,ENF LT L,JOHANSSON L,et al. Effect of freez-ing on sensory quality,shear force and water loss in beefMlongissimus dorsi[J].Meat Science, 2008, 80 ( 2 ) :457-461.
LT L,JOHANSSON L,et al. Effect of freez-ing on sensory quality,shear force and water loss in beefMlongissimus dorsi[J].Meat Science, 2008, 80 ( 2 ) :457-461.
[20] 冯志哲.食品冷藏学[M].北京:中国轻工业出版社, 2001.
[21] RODE T M, HOVDA M B . High pressure processing extend the shelf life of fresh salmon, cod and mackerel[J]. Food Control, 2016, 70:242-248.
[22] 李天翔, 包海蓉, 王锡昌,等. 不同解冻方式对鲣鱼鱼肉蛋白及组胺变化的影响[J]. 食品与发酵工业, 2017, 43(3):180-185.
[23] LEYGONIE C, BRITZ T J, HOFFMAN L C. Meat quality comparison between fresh and frozen/thawed ostrichM.iliofibularis[J]. Meat Science, 2012, 91(3):364-368.
[24] 金剑雄,贺志军.鱼在冻藏中的冻结晶与肌纤维变化的研究[J].浙江海洋学院学报(自然科学版),2000,19(2):118-121.
[25] 夏天兰, 刘登勇, 徐幸莲,等. 低场核磁共振技术在肉与肉制品水分测定及其相关品质特性中的应用[J]. 食品科学, 2011, 32(21):253-256.
[26] PEARCE K L, ROSENVOLD K, ANDERSEN H J, et al. Water distribution and mobility in meat during the conversion of muscle to meat and ageing and the impacts on fresh meat quality attributes — A review[J]. Meat Science, 2011, 89(2):111-124.
[27] BROWN R J, CAPOZZI F, CAVANI C, et al. Relationships between 1H NMR relaxation data and some technological parameters of meat: A chemometric approach[J]. Journal of Magnetic Resonance, 2000, 147(1):89-94.
[28] MIKLOS R, MORA-GALLEGO H, LARSEN F H, et al. Influence of lipid type on water and fat mobility in fermented sausages studied by low-field NMR[J]. Meat Science, 2014, 96(1):617-622.
[29] CHOW C JEN,OCHLAI Y,WATABE S,et al. Autoxidation of bluefin tuna myoglobin associated with freezing and thawing [J]. Journal of Food Science,1987,52(3):589-591.
[30] 刘欢,陈雪,宋立玲,等.不同解冻方式对鲐鱼鲜度及品质的影响[J].食品科学, 2016, 37(10):259-265.