可食用膜是指食品最初包装的薄层,一般是由可食用的成分制成的。可食用膜可阻止氧气、水分和食品成分之间的交换,从而延长食品的保质期。可食用膜一般用多糖、蛋白质、脂类等天然大分子制成[1]。这些可食用膜材料最大的优点是在食用过程中可以和食品一起被消化,不需要对其进行额外的处理,所以不仅有效地节约了能源,同时也避免了环境污染。近年来,大量的研究工作都集中于两种或多种成分制成的复合膜[2-3],这样可以结合各种成膜材料的优点改善单一材料的性能,进而获得具有多种优良性能的可食用性膜,也可以降低成本。
结冷胶是一种线性的细胞外多糖,可降解且无毒。结冷胶在金属离子的存在下可形成性能优良的凝胶,从而被广泛应用于食品行业中[4-6]。结冷胶还具有良好的成膜性能,YANG等[7-8]研究了结冷胶可食用膜,发现其具有良好的机械性能和阻水性能,已应用于果蔬保鲜中[9]。后来,学者们又将结冷胶与魔芋胶[10]、明胶[11]、卡拉胶[12]、普鲁兰[13]等制成了复合膜,发现结冷胶具有良好的复配性能。
可食用膜可通过携带和释放各种活性物质(例如抗氧化剂和抗菌化合物),来延长食品的保质期,降低病原微生物在食品表面生长的风险[14]。天然酚类化合物(例如植物精油和植物提取物)应用于可食用膜中,可改善膜的阻隔性能[15]。茶多酚是茶叶中多酚类物质及衍生物的总称,具有很强的抗氧化活性和抑菌性能[16]。同时,茶多酚含有多羟基,具有和聚合物形成稳定氢键的能力,从而改变聚合物的网络结构[17]。近年来,茶多酚因其低成本,无毒以及良好的生物相容性,而结合多糖、蛋白等制成可食用膜已广泛应用于食品保鲜中[18-19]。DOU等研究了茶多酚对明胶-海藻酸钠可食性薄膜发现随着茶多酚浓度的增加,生物活性增加,拉伸强度,接触角和交联度增加[20]。LEI等研究了果胶和魔芋胶结合茶多酚共混制备食品活性包装膜,研究发现添加适量的茶多酚后复合膜的分子间作用力更强且结构更致密,力学性能和阻隔性能均有一定提升,同时具备良好的抗菌和抗氧化等功能活性[21]。
本文以结冷胶为成膜材料、甘油为增塑剂,添加茶多酚制作可食用复合膜以增强抑菌作用,研究结果可为这类食品活性包装膜的研发提供重要的参考依据,也扩大了结冷胶、茶多酚等食品添加物在可食用膜中的应用及开发。
1 材料与方法
1.1 材料与试剂
茶多酚(食品级,纯度≥98%):上海兴隆食品科技有限公司;结冷胶(食品级):河南安锐生物科技有限公司;其他试剂均为国产分析纯。
1.2 仪器与设备
TA-XT plus型物性测试仪,英国Stable Micro System公司;HAAKE旋转流变仪,塞默飞世尔科技有限公司。
1.3 实验方法
1.3.1 复合膜膜液流变性能测定
将1g的结冷胶溶于100 mL蒸馏水中,90 ℃完全溶解后,加入0.5 g甘油混匀。再加入0.1、0.2、0.3、 0.4、0.5 g的茶多酚分别制成1、2、3、4、5 g/L的结冷胶-茶多酚复合膜液,脱气后备用。
静态流变性:探头P35TiL;温度30 ℃;剪切速率0.1~100 s-1。
动态黏弹性:探头P35TiL;扫描应变1%;测试温度30 ℃,扫描频率0.1~100 Hz。
在复合膜液的频率扫描的线性黏弹区域,储能模量和损耗模量随角频率的变化选用公式(1)、(2)进行拟合:
G′=K′(w)n′
(1)
G″=K″(w)n″
(2)
式中:G′代表储能模量,G″代表损耗模量,n′和n″分别是其相关系数,w代表频率;K′是每个正弦剪切变形周期储存和恢复的能量;K′的增加显示出与弹性凝胶结构形成有关的样品的弹性;K″是在1 Hz条件下每个正弦剪切变形周期损耗的以热量形式散失的能量[16-17]。
1.3.2 结冷胶-茶多酚可食用膜的制备及性能测定
将制备好的不同比例结冷胶-茶多酚复合膜液倒入模具中, 60 ℃干燥18~24 h后结膜,再放置于(53±5)%(相对湿度)的干燥器中平衡至少48 h后,测定膜的相关性能。
1.3.2.1 厚度
在待测膜上随机取10个点,用游标卡尺测定(精确度0.001 mm),得其平均值即为膜的厚度。
1.3.2.2 机械性能
本实验测得可食用性膜的机械性能包括机械强度(tensile strength,TS)和断裂延伸率(elongation at break,EAB)。根据ASTM D882-02的方法[18],将样品裁剪成20 mm×90 mm大小,用物性仪测试各样品的TS和EAB。物性仪的参数设置为:距离60 mm,速度1 mm/s。
1.3.2.3 水蒸气透过率
膜样品的水蒸汽透过速率根据ASTM E96方法测定[19]。
1.3.2.4 阻氧性
根据油脂的过氧化值的大小,来评价待测膜的阻氧性。过氧化值的测定方法参照国标GB/T 5538—2005[22]。
1.3.2.5 抑菌性能
采用抑菌圈法检测复合膜抗菌性能[20]。将活化的微生物种子培养基涂布于固体平板培养基上,用打孔器将结冷胶-茶多酚复合膜制成直径为10 mm的小圆片,放置于平板中,37 ℃恒温培养24 h,用游标卡尺测量抑菌圈的直径大小。
1.3.2.6 扫描电镜
用TM3030扫描电镜观察膜样品的表面和横截面,放大倍数为2 000倍,电子束的加速电压1.0 kV。
2 结果与分析
2.1 结冷胶-茶多酚复合膜膜液的流变性能
在某一程度上,可食用膜溶液性质可以为成膜过程提供一定的参考,例如成膜溶液的假塑性、黏弹性能可以为脱气、干燥的过程提供依据[21]。
2.1.1 静态流变学性质
不同茶多酚浓度的结冷胶-茶多酚复合膜液的静态流变学性质如图1所示,所有样品随着剪切速率的增加,溶液的黏度不断减小,均出现了剪切变稀的现象[23]。随着茶多酚浓度的增加,复合膜液黏度有一定程度上升,但均不显著,例如在剪切速率为100 s-1、茶多酚质量浓度为0、1、2、3、4、5 g/L时,复合膜的黏度分别为1.651、1.749、1.833、1.875、1.878、1.922 Pa·S。这说明在结冷胶-茶多酚复合膜液中,结冷胶是决定复合体系流变学特性的关键因素,添加茶多酚可能增加了结冷胶分子的聚合[15],进而提高了溶液的黏度。
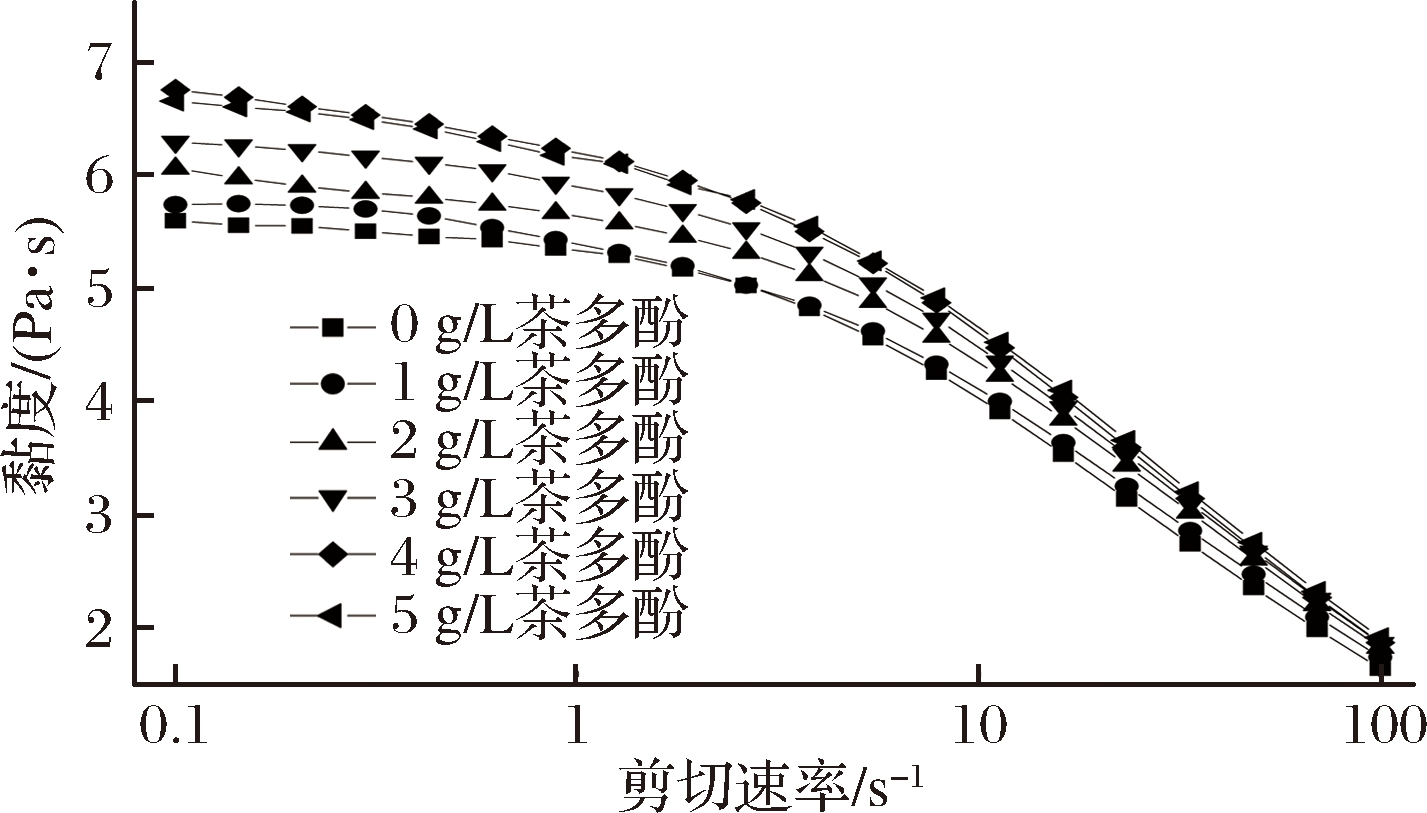
图1 结冷胶-茶多酚复合膜液静态流变曲线
Fig.1 Flow curves of gellan gum- tea polyphenols blending film-forming solutions
2.1.2 动态频率扫描
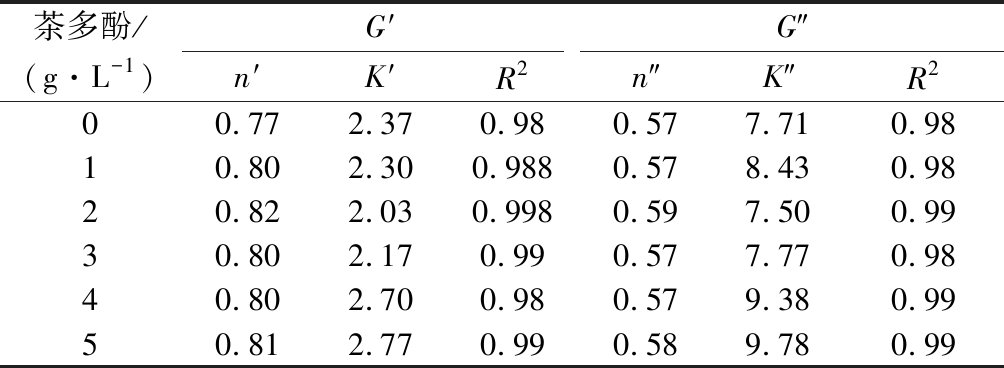
结冷胶-茶多酚复合膜液的储能模量G′和损耗模量G″随角频率的变化如图2所示,G′和G″随频率的增加逐渐增大,复合体系的G″均大于G′,说明所研究的复配体系都显示了高的黏弹性。随着茶多酚质量浓度的增加,复合体系的G′和G″增加,这可能是由于茶多酚使复合膜液结构内部的分子链间的缠节点增多,膜液内部的网络结构加强[24]。通过公式(1)、(2)对结冷胶-茶多酚复合膜液的线性黏弹区域的数据进行拟合,计算得到的参数如表1所示。由表1可知,n′和n″为正值,且K″>K′,说明结冷胶-茶多酚复合膜液呈现弱凝胶现象。茶多酚浓度对n′值影响不大,说明结冷胶-茶多酚复合膜液的动态流变学性能主要是由结冷胶的黏弹性决定的,在溶液中结冷胶形成了三维网状结构。随着茶多酚比例的增大,结冷胶-茶多酚复配体系的K′值增大,这也许归结于茶多酚的加入增加了结冷胶-茶多酚复合膜液连续相的黏弹性。随着茶多酚含量的增加,复配体系的弹性增加[17]。
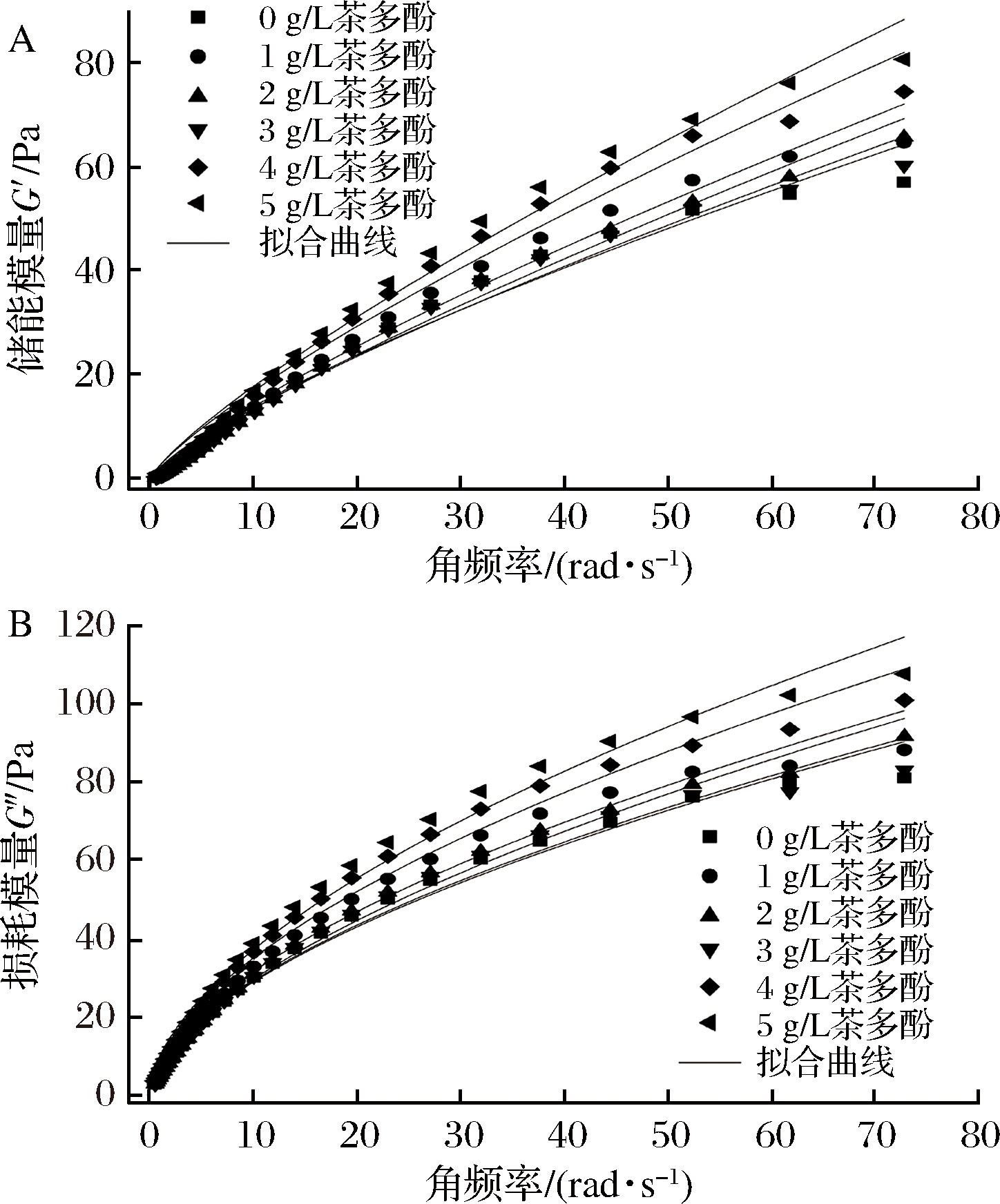
A-储能模量G′;B-损耗模量G″
图2 结冷胶-茶多酚复合膜液动态模量的变化
Fig.2 Dynamic modulus of gellan gum-tea polyphenols blending film-forming solutions
表1 结冷胶-茶多酚复合体系的公式(1)和公式(2)的参数
Table 1 The parameters as determined from Eqs (1) and Eqs (2) of gellan gum-tea polyphenols blending film-forming solutions
茶多酚/(g·L-1)G′G″n′K′R2n″K″R200.772.370.980.577.710.9810.802.300.9880.578.430.9820.822.030.9980.597.500.9930.802.170.990.577.770.9840.802.700.980.579.380.9950.812.770.990.589.780.99
结冷胶-茶多酚复合膜液的流变学结果说明,在复合体系中,结冷胶对复合膜液的流变性起主导作用,在所研究的范围内,茶多酚的加入不会影响复合体系从液态(成膜溶液)到固态(可食用膜)的变化,复合体系具有成膜性。
2.2 结冷胶-茶多酚复合膜的性能
2.2.1 机械性能
结冷胶-茶多酚复合膜的抗拉强度和断裂延伸率如图3所示。由图3可知,随着茶多酚比例增大,可食用膜的抗拉强度先增大后减小,在茶多酚质量浓度为4 g/L时,达到最大值,为14.08 MPa。抗拉强度增大原因可能是因为茶多酚是一种多羟基的化合物,与结冷胶大分子之间通过一系列氢键的相互作用构成致密的网络结构。当茶多酚的质量浓度为4 g/L以内时,断裂延伸率变化缓慢,而茶多酚质量浓度进一步增加时断裂延伸率下降很快,可能是因为茶多酚质量浓度升高,使得复合膜的不同分子间的迁移率下降,使得膜的脆性增加,较易断裂,即断裂延伸率下降[25]。
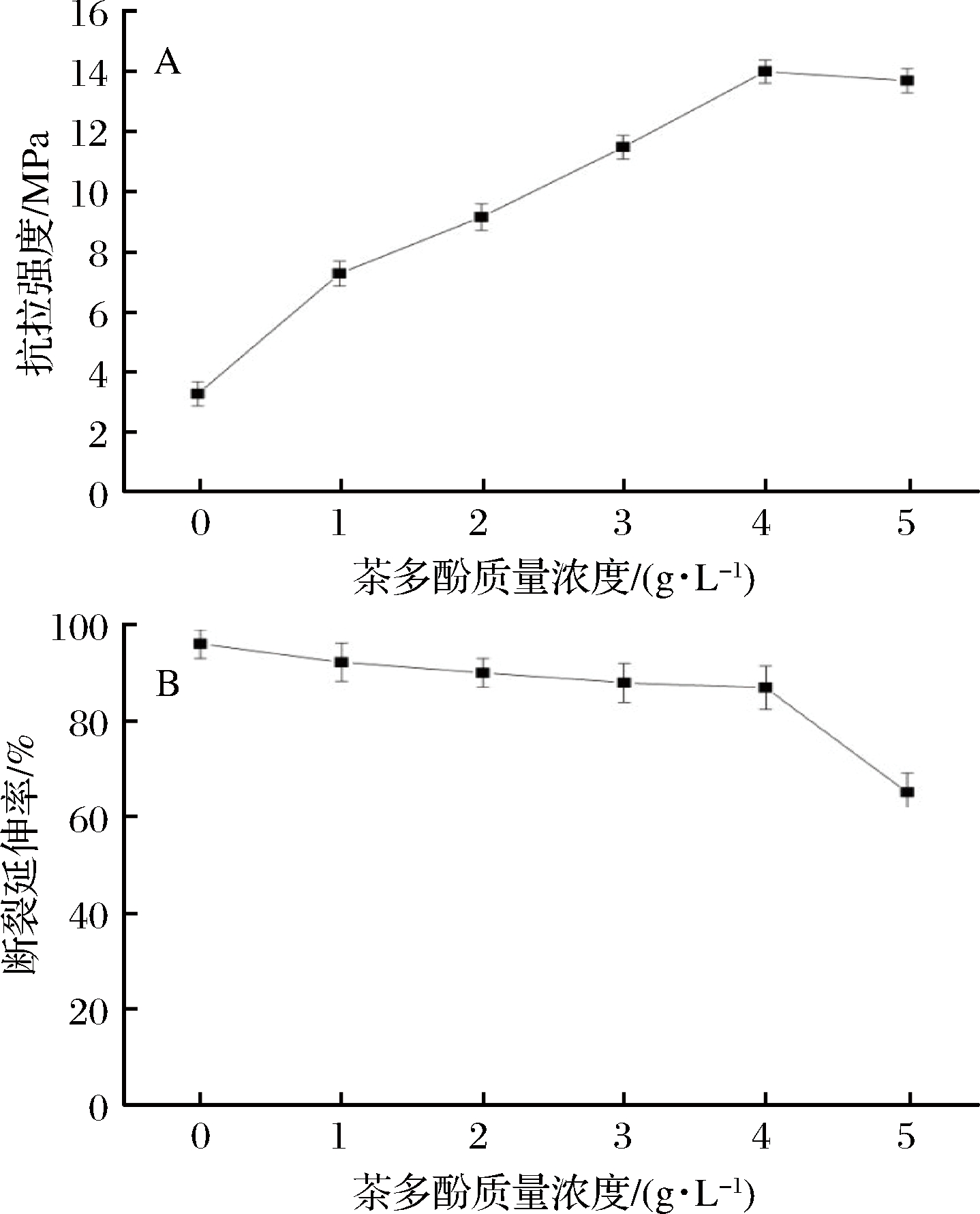
A-抗拉强度;B-断裂延伸率
图3 结冷胶-茶多酚复合膜的机械性能
Fig.3 Mechanical properties of the gellan gum- tea polyphenols blend film
2.2.2 水蒸气透过率
由图4可知,随着茶多酚比例的增大,可食用膜的水蒸气透过率先减小后增大。
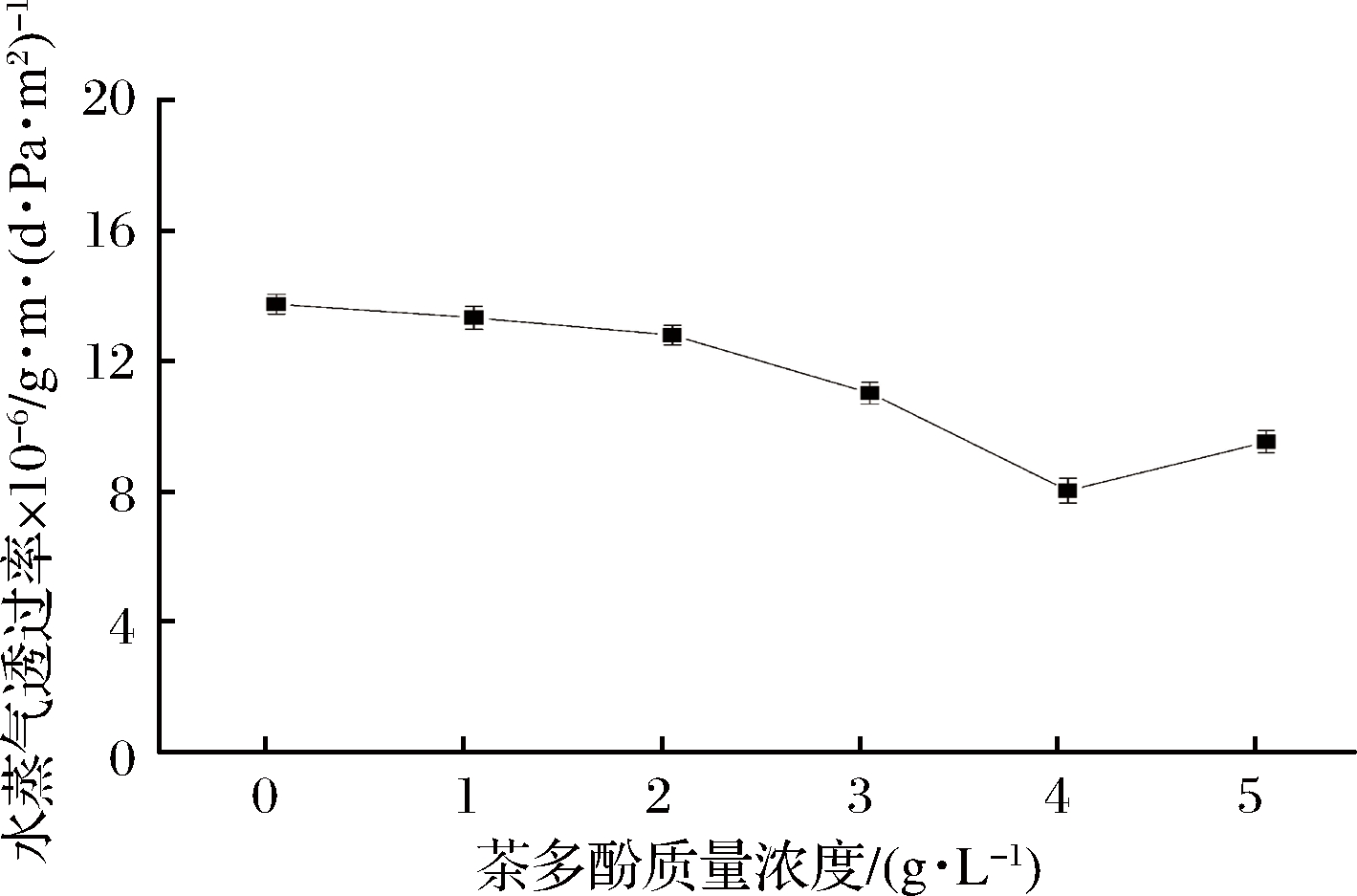
图4 结冷胶-茶多酚复合膜的水蒸气透过率
Fig.4 Watervapor permeability of the gellan gum- tea polyphenols blend film
相比于未添加茶多酚的对照组,结冷胶-茶多酚可食用膜的水蒸气透过率明显减小,当茶多酚的质量浓度为4 g/L时达到最小值8.01 (g·m)/(d·Pa·m2),可能的原因是茶多酚和其他分子形成氢键,通过各种相互作用使得大分子间的间隙减小,形成致密、稳固的结构,从而使得水蒸汽透过率减小[26],即膜的阻水性增强。
随着茶多酚比例进一步的增加,容易在膜表面形成结晶,膜的紧密程度下降,从而使得水蒸汽容易透过膜,水蒸汽透过率增大[27]。
2.2.3 阻氧性能
由图5可知,随着茶多酚含量的增加,油脂的过氧化值逐渐减小,即可食用膜的阻氧性逐渐增强。茶多酚中存在大量的酚羟基也可以阻止油脂氧化中的链传递,使得油脂氧化程度下降,即膜的阻氧性增强[28]。

图5 结冷胶-茶多酚复合膜的阻氧性
Fig.5 Oxygen barrier property of the gellan gum- tea polyphenols blend film
2.2.4 抑菌性能
结冷胶-茶多酚复合膜对枯草芽孢杆菌、产黄青霉、大肠杆菌和酿酒酵母的抑菌性能如表2所示。
表2 结冷胶-茶多酚可食用膜的抑菌性能
Table 2 Antimicrobial properties of the gellan gum- tea polyphenols blend film
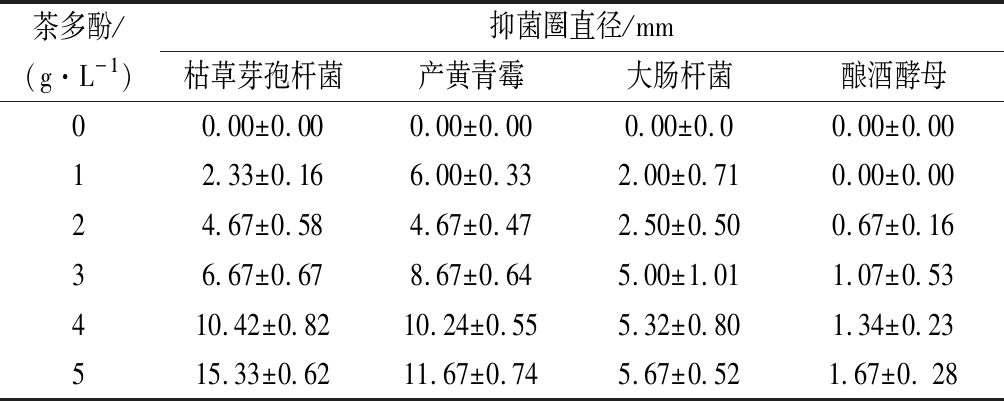
茶多酚/(g·L-1)抑菌圈直径/mm枯草芽孢杆菌产黄青霉大肠杆菌酿酒酵母00.00±0.000.00±0.000.00±0.00.00±0.0012.33±0.166.00±0.332.00±0.710.00±0.0024.67±0.584.67±0.472.50±0.500.67±0.1636.67±0.678.67±0.645.00±1.011.07±0.53410.42±0.8210.24±0.555.32±0.801.34±0.23515.33±0.6211.67±0.745.67±0.521.67±0. 28
未添加茶多酚的可食用膜对所测试的微生物没有抑制作用,其抑菌圈为零。复合膜中添加茶多酚对所研究的微生物均有比较高的抑菌性能。抑菌效果与茶多酚的含量和微生物的种类相关[29]。添加5 g/L茶多酚的复合膜抑菌性能最强,说明茶多酚质量浓度越高,抑菌性能越好。
另外,对于每种微生物,随着茶多酚在复合膜中的质量浓度降低,抑菌性能下降,例如当茶多酚质量浓度从5 g/L降到1 g/L时,枯草杆菌的抑菌圈直径从(15.33±0.62)mm 降到(2.33±0.16)mm。
综合表明,茶多酚对微生物的抑菌效果大小为枯草芽孢杆菌>产黄青霉>大肠杆菌>酿酒酵母。结果表明,茶多酚对革兰氏阳性菌的抑制效果最明显,对霉菌抑制效果次之,对酵母菌和革兰氏阴性菌抑制效果不明显。
2.2.5 扫描电镜
膜的扫描电镜图可用于揭示与成膜基体微观结构有关的一些信息,从而更好地解释可食用膜宏观性能变化的原因。结冷胶-茶多酚复合膜的扫描电镜图如图6所示,从图6-a和图6-c中可以看出,纯结冷胶膜和结冷胶-茶多酚复合膜的表面微观结构呈现均一体系,不存在任何的裂隙和小孔,说明两多糖间无相分离现象。比较添加2 g/L的茶多酚膜(图6-d)和纯结冷胶膜(图6-b)的横截面图发现茶多酚能很好地分布在膜基质中,具有一定的相互作用。

a-纯结冷胶膜的表面图; b-纯结冷胶膜的横截面图;c-结冷胶-茶多酚复合膜的表面图; d-结冷胶-茶多酚复合膜的横截面图
图6 膜样品的扫描电镜图
Fig.6 Scanning electron microscopy pictures of the film samples
3 结论
结冷胶-茶多酚复合膜液具有剪切变稀的现象,表观黏度随着茶多酚质量浓度的增加而增加。随着茶多酚含量的增加,储能模量G′和损耗模量G″增加。结冷胶-茶多酚复合膜液的流变学结果说明,在复合体系中,结冷胶对复合膜液的流变性起主导作用,在所研究的范围内,茶多酚的加入不会影响复合体系从液态(成膜溶液)到固态(可食用膜)的变化,复合体系具有成膜性[30-36]。
在结冷胶膜中加入茶多酚可提高复合膜拉伸强度和阻氧性,降低了复合膜的断裂伸长率,同时也提高了复合膜的阻水性能。与未加茶多酚的结冷胶膜相比,复合膜具有抑制枯草芽孢杆菌、大肠杆菌、产黄青霉和酿酒酵母的性能。
[1] HASSAN B, CHATHA S A S, HUSSAIN A I, et al. Recent advances on polysaccharides, lipids and protein based edible films and coatings: A review[J].International Journal of Biological Macromolecules, 2018, 109(4): 1 095-1 107.
[2] MARQUEZ G R, DIPIERRO P, MARINIELLO L, et al. Fresh-cut fruit and vegetable coatings by transglutaminase-crosslinked whey protein/pectin edible films [J]. LWT - Food Science and Technology, 2017, 75(1):124-130.
[3] GUERREIRO A C, GAGO C M L, FALEIRO M L, et al. The effect of edible coatings on the nutritional quality of ‘Bravo de Esmolfe’ fresh-cut apple through shelf-life [J]. LWT- Food Science and Technology, 2017, 75(1):210-219.
[4] MORRIS E R, NISHINARI K, RINAUDO M. Gelation of gellan:A review [J]. Food Hydrocolloids, 2012, 28(2): 373-411.
[5] ZIA K M, TABASUM S, KHAN M F, et al. Recent trends on gellan gum blends with natural and synthetic polymers: A review[J]. International Journal of Biological Macromolecules, 2018, 109(4):1 068-1 087.
[6] PRAJAPATI V D, JANI G K, ZALA B S, et al. An insight into the emerging exopolysaccharide gellan gum as a novel polymer [J]. Carbohydrate Polymers, 2013, 93(2): 670-678.
[7] YANG L, PAULSON A T. Effects of lipids on mechanical and moisture barrier properties of edible gellan film [J]. Food Research International, 2000, 33(7): 571-578.
[8] YANG L, PAULSON A T, NICHERSON M T. Mechanical and physical properties of calcium-treated gellan films [J]. Food Research International, 2010, 43(5): 1 439-1 443.
[9] DANALACHE F, CARVALHO C Y, ALVES V D, et al. Optimization of gellan gum edible coating for ready-to-eat mango (Mangifera indica L.) bars [J]. International Journal of Biological Macromolecules, 2016, 84(3):43-53.
[10] XU X, LI B, KENNEDY J F, et al. Characterization of konjac glucomannan-gellan gum blend films and their suitability for release of nisin incorporated therein[J]. Carbohydrate Polymers, 2007, 70(2): 192-197.
[11] LEE K Y, SHIM J, LEE H G. Mechanical properties of gellan and gelatin composite films[J]. Carbohydrate Polymers, 2004, 56(2): 251-254.
[12] PRANOTO Y, LEE C M, PARK H J. Characterizations of fish gelatin films added with gellan and kappa-carrageenan[J]. LWT-Food Science and Technology, 2007, 40(5): 766-774.
[13] ZHU G, SHENG L, LI J, et al. Preparation and characterisation of gellan/pullulan composite blend films[J]. International Journal of Food Science & Technology, 2013, 48(12): 2 683-2 687.
[14] ESPITIA P J P, DU W X, ![]() R, et al. Edible films from pectin: Physical-mechanical and antimicrobial properties - A review[J]. Food Hydrocolloids, 2014, 35(3):287-296.
R, et al. Edible films from pectin: Physical-mechanical and antimicrobial properties - A review[J]. Food Hydrocolloids, 2014, 35(3):287-296.
[15] SUN L, SUN J, CHEN L, et al. Preparation and characterization of chitosan film incorporated with thinned young apple polyphenols as an active packaging material[J]. Carbohydrate Polymers, 2017, 163:81-91.
[16] ZHANG L, LI S, DONG Y, et al. Tea polyphenols incorporated into alginate-based edible coating for quality maintenance of Chinese winter jujube under ambient temperature[J]. LWT - Food Science and Technology, 2016, 70(7): 155-161.
[17] 于林, 陈舜胜,王娟娟,等. 茶多酚改性胶原蛋白-壳聚糖复合膜对冷藏斜带石斑鱼的保鲜效果[J]. 食品科学, 2017, 38(3): 220-226.
[18] FENG M, YU L, ZHU P, et al. Development and preparation of active starch films carrying tea polyphenol[J]. Carbohydrate Polymers, 2018, 196(9):162-167.
[19] WU H, LEI Y, ZHU R. et al. Preparation and characterization of bioactive edible packaging films based on pomelo peel flours incorporating tea polyphenol [J]. Food Hydrocolloids, 2019,90(5):41-49.
[20] DOU L, LI B, ZHANG K, et al. Physical properties and antioxidant activity of gelatin-sodium alginate edible films with tea polyphenol[J]. International Journal of Biological Macromolecules, 2018, 118(10):1 377-1 383.
[21] LEI Y, WU H, JIAO C, et al. Investigation of the structural and physical properties, antioxidant and antimicrobial activity of pectin-konjac glucomannan composite edible films incorporated with tea polyphenol[J]. Food Hydrocolloids, 2019,94(9):128-135.
[22] GB/T 5538—2005, 动植物油脂过氧化值的测定[S]. 北京:中国标准出版社,2005.
[23] 朱桂兰, 叶银杉,葛洁. 低酰基结冷胶-果胶复配体系的性能[J]. 食品科学, 2017, 38(13):72-76.
[24] 朱桂兰, 陶思远,童群义. 结冷胶与黄原胶复配体系流变与凝胶特性[J]. 食品与发酵工业, 2013, 39(3):56-60.
[25] American Society for Testing and Materials (ASTM). Standard test method for tensile properties of thin plastic sheeting[S]. Philadelphia: American Society for Testing and Materials,2002.
[26] American Society for Testing and Materials (ASTM) E. Standard test methods for water vapor transmission of materials[S]. Philadelphia: American Society for Testing and Materials,1993.
[27] ATEF M, REZAEI M, BEHROOZ R. Characterization of physical, mechanical, and antibacterial properties of agar-cellulose bionanocomposite films incorporated with savory essential oil [J]. Food Hydrocolloids, 2015, 45(3):150-157.
[28] XIAO Q, TONG Q, ZHOU Y, et al. Rheological properties of pullulan-sodium alginate based solutions during film formation[J]. Carbohydrate Polymers, 2015, 130(11):49-56.
[29] 陈青, 马慧婷,陆海霞,等. 低酰基结冷胶/酪蛋白酸钠复合体系液-固转变流变学表征[J]. 农业机械学报, 2017, 48(8):327-332.
[30] UBONRAT S, BRUCER H. Physical properties and antioxidant activity of an active film from chitosan incorporated with green tea extract [J]. Food Hydrocolloids, 2010, 24(8): 770-775.
[31] 高丹丹, 徐学玲,江连洲,等. 普鲁兰多糖-明胶可食性膜的特性[J]. 食品科学, 2014, 35(1): 69-73.
[32] 朱明秀, 黄崇杏,蓝鸿雁,等. 茶多酚对壳聚糖/聚乙烯醇复合膜性能的影响[J]. 包装工程, 2018, 39(5): 110-114.
[33] WU J, CHEN S, GE S, et al. Preparation, properties and antioxidant activity of an active film from silver carp (Hypophthalmichthys molitrix) skin gelatin incorporated with green tea extract [J]. Food Hydrocolloids, 2013, 32(1): 42-51.
[34] 高艳阳, 赖仰洲,李昭昭,等. 基于茶多酚的壳聚糖基抗氧化复合膜的制备与性能研究[J]. 化工新型材料, 2016, 44(6): 178-180.
[35] HE L, ZOU L, YANG Q, et al. Antimicrobial activities of nisin, tea polyphenols, and chitosan and their combinations in chilled mutton [J]. Journal of Food Science, 2016, 81(6):M1 466-M1 471.
[36] LUO W, XIAO G, TIAN F, et al. Engineering robust metal-phenolic network membranes for uranium extraction from seawater[J]. Energy & Environmental Science, 2019,12(2): 607-614.