海菜属水鳖科,为水生植物,长年生长于水中。主要分布在中国沿海地区,云南滇西等地也生长较多,是一种天然野生水菜,其蛋白质含量丰富且富有多种维生素及微量元素,常常被作为民间美食素材。《中华本草》中曾记载海菜具有清热、止咳、利水、消肿之功效,是中国独有的珍稀濒危水生药用植物[1-2]。
海菜具有药食两用的价值,其中多元素含量对评价其营养价值及食用安全性具有重要意义。李原等用原子吸收及电感耦合等离子体原子发射光谱法(inductively coupled plasma atomic emission spectrometry, ICP-AES)分析测定了海菜花中10种矿质元素含量[3]。朱静等用高锰酸钾法、钼黄比色法分别测定了云南不同产地海菜花的不同部位Ca、P含量[4]。殷建忠等在海菜花营养成分分析评价中以ICP-AES及荧光法测定11种元素含量[5]。电感耦合等离子体质谱仪因其线性范围宽、检出限低、灵敏度高,能实现多元素同时测定,而被广泛应用在环境分析、地质矿样、半导体材料、食品安全等领域[6-8]。电感耦合等离子体质谱法用于植物样品中多元素的分析已有大量报道[9-12],而有关石墨消解海菜,ICP-MS测定其无机元素含量的方法尚未见报道。
植物样品中无机元素分析的前处理方法主要有干法灰化、湿法消解、微波消解,为使前处理操作简单快速及针对一些特定元素的测定,大试管回流消解法、风冷回流消解法、高温热水解法、溶剂萃取法被用在植物样品前处理中。不同的样品前处理方法各有其优点,或存在操作繁琐、试剂用量多、前处理周期长、检测元素种类受限制等不足[13-22]。本文经过海菜石墨消解条件的优化,建立了一种快速石墨消解海菜样品,ICP-MS分析海菜中13种无机元素的方法,旨在为植物样品中无机元素的快速分析提供一种简单、快速且实用的新方法。
1 材料与方法
1.1 材料与试剂
多元素混合标准溶液(10 μg/mL)、调谐液:Ce、Co、Li、Mg、Tl、Y,(1 μg/L)、内标溶液:Sc、Ge、In、Bi,(100 μg/mL),美国Agilent公司;单元素标准溶液:Na、Mg、K、Ca、Mn、Ni、Cu、Zn、As、Sr、Cd、Ba、Pb,(1 000 μg/mL), 中国计量科学研究院;HNO3(优级纯),德国Merck;H2O2(优级纯),苏州晶瑞;螺旋藻标准物质(GBW10025),地球物理地球化学勘查研究所;海菜,市售。
1.2 仪器与设备
Agilent7900型电感耦合等离子体质谱仪,美国Agilent公司;Digi24型石墨消解仪、Digi TUBES消解管50 mL,加拿大SCP公司;VB24up赶酸仪,北京莱伯泰科公司;ETHOS UP微波消解仪,意大利Milestone公司;ML204T/02型电子分析天平,梅特勒-托利多仪器(上海)有限公司;ELGA超纯水机,英国ELGA;B-400型均质仪,瑞士BUCHI。ICP-MS优化后的工作参数见表1。
表1 ICP-MS工作参数
Table 1 ICP-MS operating parameters

仪器条件工作参数射频功率RF1 550 W等离子气体流量15 L/min雾化气流量1.0 L/min辅助气体流量0.90 L/min雾化室温度2.0 ℃氧化物156/1400.279%双电荷70/1401.337%分辨率(W-10%)0.65~0.80 amu
1.3 实验方法
将供试品海菜用超纯水洗净、晾干,陶瓷刀切碎后用均质仪匀浆备用。称取0.5 g样品于50 mL带刻度Digi TUBES消解管中,加入65%浓HNO3 2.0 mL,加盖但不旋紧,放于石墨消解仪中在80 ℃下预消解10 min,使样品能够被硝酸完全浸润,之后取出,放冷,加入30% H2O2 1.0 mL,加盖但不旋紧,在120 ℃下消解20 min。冷却后用超纯水直接定容至25 mL待测,同时做试剂空白试验。
2 结果与分析
2.1 前处理条件的优化
2.1.1 消解体系的选择
元素测定中前处理方法体系的选择对于样品消解及元素测定有着重要的影响,试验选用HNO2作为主要的消解液,直接消解样品后,消解液呈黄色,且有絮状样品残余,至样品消解不完全。H2O2在样品消解中起辅助氧化作用,可以加速样品的消解,加入H2O2后样品消解液呈无色澄清状。所以,试验选用HNO3-H2O2体系对样品进行消解。
2.1.2 HNO3使用量的选择
在与1.3相同的实验方法下,分别加入1.0、1.5、2.0、2.5、3.0 mL HNO3溶液对样品进行消解,考察HNO3使用量对海菜中各个元素测定结果的影响。结果显示,随着HNO3用量的增加,样品消解液中残渣逐渐减少,且多个元素含量呈先增高至趋于平稳的变化趋势,在HNO3用量为2.0 mL条件下,样品消解完全,且元素含量测定达最大值,实验选用2.0 mLHNO3为最佳。
2.1.3 H2O2用量的选择
相同的试验条件下,考察H2O2用量对消解的影响,以加入H2O20.0、1.0、2.0、3.0 mL进行试验,发现不加H2O2时样品消解液为黄色浑浊状,且测定结果比加入H2O2偏低,之后随H2O2用量增加各元素测定值无明显变化,以试剂用量最少原则,试验选择加入H2O2用量为1.0 mL。
2.1.4 消解时间的影响
在石墨消解仪中消解样品10、20、30、40 min,结果发现Ni、Cd、Pb三个元素在消解20 min条件下测定值为最大值之后无明显变化,其他9个元素随消解时间的变化无明显差异。综合考虑样品消解充分性,选择20 min为最佳消解时间。
2.1.5 消解温度对测定结果的影响
在石墨消解仪预设的80、100、120、140 ℃的条件下消解样品,结果表明随着消解温度的升高,多个元素测定结果先增加后趋于平稳的变化趋势,试验最终选择消解温度为120 ℃。
2.2 ICP-MS的干扰及校正
ICP-MS的干扰主要有两大类,物理性干扰及质谱型干扰。物理干扰会造成信号灵敏度的损失,准确度降低,精密度差、测定结果漂移,物理性干扰主要与样品基体含盐量、黏性及共存离子有关,试验基于此类问题在标样、空白及样品配制及制备过程中使用相同浓度的HNO3溶液进行匹配,同时通过待测元素与内标元素质量数相近及电离势能匹配原则选择相应的内标元素,使用蠕动泵和T型混合三通在线添加内标,使信号抑制或增强的干扰得到有效校正。
质谱型干扰会造成待测元素测定结果不准确或结果的假阳性,其主要来自于同量异位数、分子离子及双电荷离子干扰,通过仪器条件的优化(表1)、依据各元素相互间干扰小,丰度高的原则选择最佳同位数,使用八级杆氦模式及四级杆质量过滤器消除相应的质谱型干扰。
2.3 工作曲线及检出限
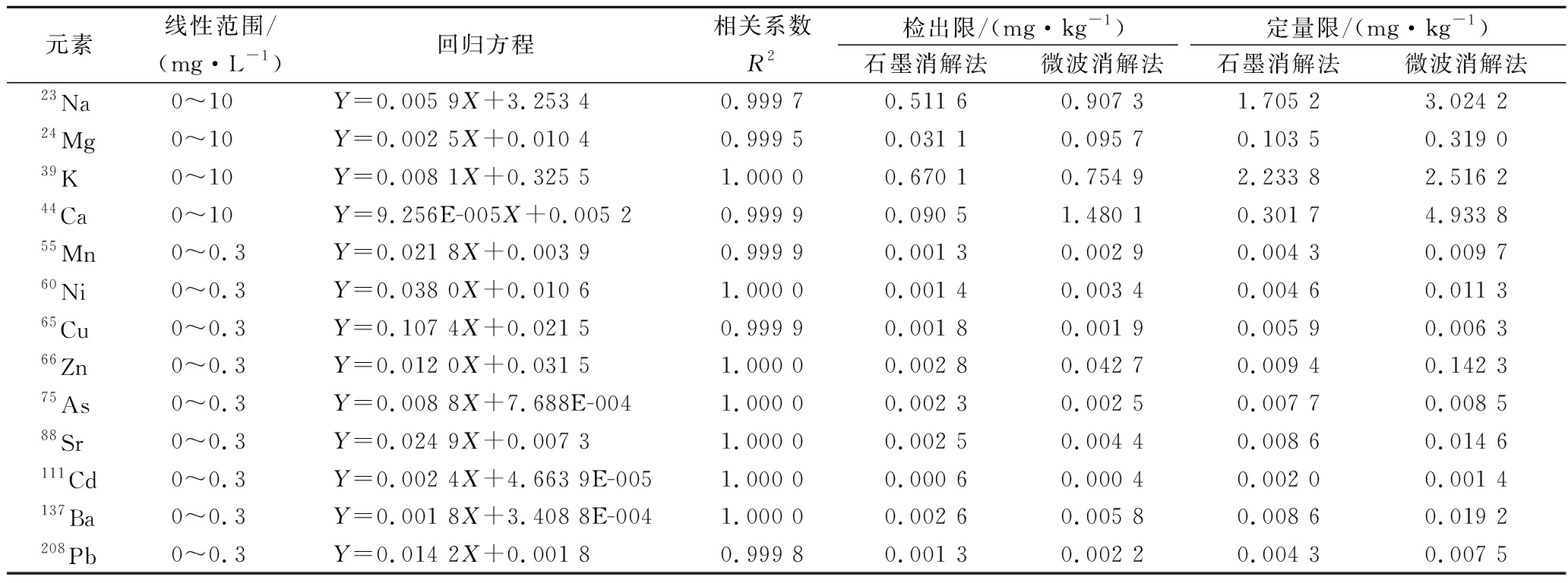
分别配制0.00、1.00、5.00、10.00、50.00、100.00、 300.00、500.00、1 000.00、2 500.00、5 000.00、10 000.00 μg/L多元素混合标准溶液,在表1仪器工作条件下在线加入1 000 μg/L的45Sc、72Ge、115In、209Bi内标溶液对各元素进行校正,建立标准曲线,各元素线性回归方程及相关系数见表2所示。同时对试剂空白溶液连续进行11次测定,计算相应元素的检出限,并与食品安全国家标准方法中微波消解法进行比较[23],结果表明,快速石墨消解法应用于海菜样品的前处理,各元素线性良好,相关系数均≥0.999 5,多个元素的检出限比微波消解法低,试剂用量较微波消解法少,且无需赶酸直接定容上机。
表2 标准工作曲线及方法检出限
Table 2 Standard curves and detection limits for the analyes
元素线性范围/(mg·L-1)回归方程 相关系数R2检出限/(mg·kg-1)定量限/(mg·kg-1)石墨消解法微波消解法石墨消解法微波消解法23Na0~10Y=0.005 9X+3.253 40.999 70.511 60.907 31.705 23.024 224Mg0~10Y=0.002 5X+0.010 40.999 50.031 10.095 70.103 50.319 039K0~10Y=0.008 1X+0.325 51.000 00.670 10.754 92.233 82.516 244Ca0~10Y=9.256E-005X+0.005 20.999 90.090 51.480 10.301 74.933 855Mn0~0.3Y=0.021 8X+0.003 90.999 90.001 30.002 90.004 30.009 760Ni0~0.3Y=0.038 0X+0.010 61.000 00.001 40.003 40.004 60.011 365Cu0~0.3Y=0.107 4X+0.021 50.999 90.001 80.001 90.005 90.006 366Zn0~0.3Y=0.012 0X+0.031 51.000 00.002 80.042 70.009 40.142 375As0~0.3Y=0.008 8X+7.688E-0041.000 00.002 30.002 50.007 70.008 588Sr0~0.3Y=0.024 9X+0.007 31.000 00.002 50.004 40.008 60.014 6111Cd0~0.3Y=0.002 4X+4.663 9E-0051.000 00.000 60.000 40.002 00.001 4137Ba0~0.3Y=0.001 8X+3.408 8E-0041.000 00.002 60.005 80.008 60.019 2208Pb0~0.3Y=0.014 2X+0.001 80.999 80.001 30.002 20.004 30.007 5
2.4 方法精密度及样品测定结果
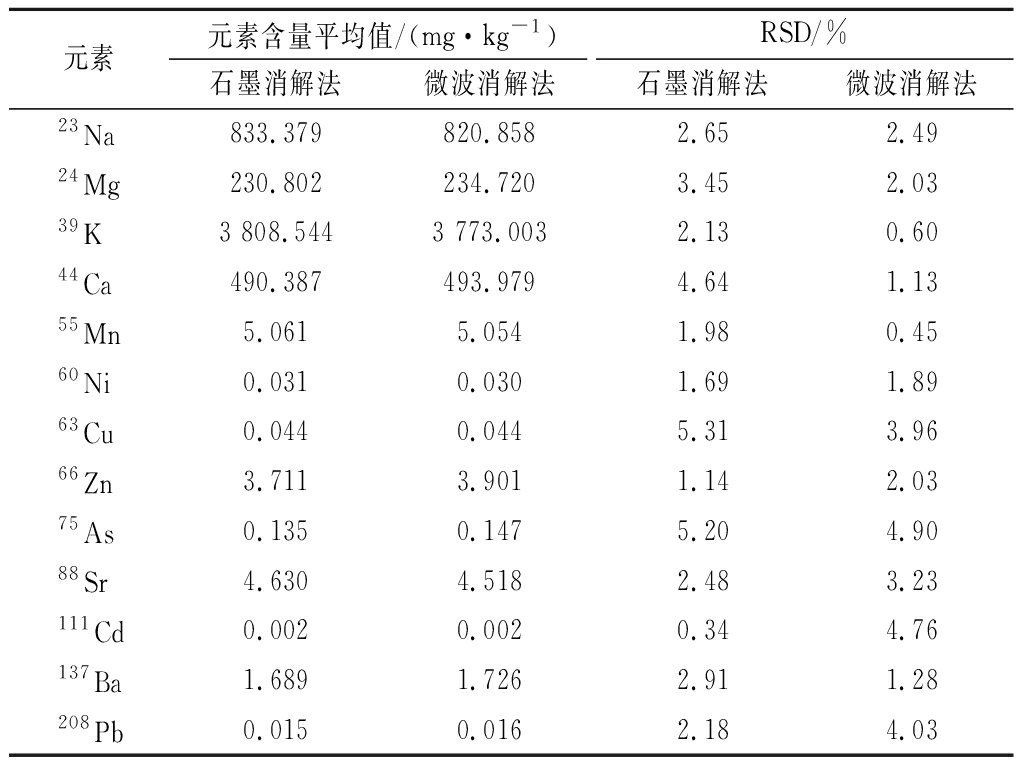
在相同的实验条件下,对海菜样品做6份平行试验,分别测定13种元素含量,计算海菜样品中各元素的含量及相对标准偏差(relative standard deviation,RSD)。并与微波消解法进行比较见表3。结果表明,快速石墨消解法用于海菜中多元素的测定其RSD在0.34%~5.31%,方法精密度良好。与微波消解法相比,二者无统计学差异(P>0.05)。
表3 快速石墨消解法测定结果及精密度(n=6)
Table 3 The determination results and precision by
rapid graphite digestion
元素元素含量平均值/(mg·kg-1)RSD/%石墨消解法微波消解法石墨消解法微波消解法23Na833.379820.8582.652.4924Mg230.802234.7203.452.0339K3 808.5443 773.0032.130.6044Ca490.387493.9794.641.1355Mn5.0615.0541.980.4560Ni0.0310.0301.691.8963Cu0.0440.0445.313.9666Zn3.7113.9011.142.0375As0.1350.1475.204.9088Sr4.6304.5182.483.23111Cd0.0020.0020.344.76137Ba1.6891.7262.911.28208Pb0.0150.0162.184.03
2.5 加标回收试验
取海菜样品0.5 g,进行13种元素的加标回收试验,以1.3方法处理样品,进一步验证方法的准确性。结果见表4,快速石墨消解法各元素加标回收率为87.6%~108.5%。
表4 13种元素加标回收率(n=6)
Table 4 Recovery rate of 13 elements

元素本底值加标量测定值回收率/%RSD/%23Na/(mg·L-1)18.79815.0034.851107.00.6124Mg/(mg·L-1)5.2265.0010.650108.52.0539K/(mg·L-1)85.893100.00184.89199.00.1244Ca/(mg·L-1)11.08410.0021.647105.60.9155Mn/(μg·L-1)114.140100.00214.421100.30.9860Ni/(μg·L-1)0.6971.001.712101.52.1263Cu/(μg·L-1)1.0921.002.01091.85.0666Zn/(μg·L-1)84.644100.00179.24094.60.9475As/(μg·L-1)3.2493.006.365103.93.2588Sr/(μg·L-1)104.421100.00206.678102.31.04111Cd/(μg·L-1)0.0420.050.08892.04.57137Ba/(μg·L-1)38.09950.0088.178100.21.41208Pb/(μg·L-1)0.3470.500.78587.62.81
2.6 标准物质验证试验
用1.3方法对国家标准物质螺旋藻生物成分分析标准物质(GBW10025)进行6份平行试验,结果见表5。该方法应用于螺旋藻生物成分分析标准物质中13种元素的测定值均在认定值范围内,且方法精密度良好。
2.7 方法应用扩展
采用1.3方法对植物样品甜菊叶、豆芽、韭菜、水芹菜进行预处理,在相同的试验条件下,4种样品能被完全消解,消解液呈浅黄色或无色且为澄清状,快速石墨消解法用于多种植物样品的预处理,具有一定的适用性。
表5 国家标准物质螺旋藻测定结果(n=6)
Table 5 Determination results for national
standard material

元素标准值测定值RSD/%23Na/(mg·kg-1)1.90±0.091.862.1124Mg/(g·kg-1)2.87±0.102.841.0739K/(g·kg-1)14.1±0.5014.161.7044Ca/(g·kg-1)1.58±0.151.703.4355Mn/(mg·kg-1)31.70±1.2030.610.0360Ni/(mg·kg-1)1.44±0.171.301.0363Cu/(mg·kg-1)7.70±0.67.140.3566Zn/(mg·kg-1)42.00±2.0040.664.2475As/(mg·kg-1)0.22±0.030.243.3788Sr/(mg·kg-1)36.00±2.0034.760.40111Cd/(ug·kg-1)0.37±0.030.395.2137Ba/(mg·kg-1)11.00±0.810.520.69208Pb/(mg·kg-1)2.80±0.202.830.48
3 结论
采用快速石墨消解ICP-MS法测定海菜中13种无机元素含量。该方法精密度良好,测定结果准确可靠,所得实验结果与国家标准方法中微波消解法相比,结果具有较好的一致性。与湿法消解、微波消解相比,该方法操作简单,试剂用量少,检出限低,样品从称样、消解到定容都在同一Digi TUBES消解管中实现,过程耗时短,且大大降低了前2种方法中由于赶酸、转移等后续步骤可能造成分析物污染和损失的风险。快速石墨消解-ICP-MS法测定海菜中13种微量元素,具有较好的实用性,该法还可用于植物样品中多元素检测样品的前处理及测定,具有一定的适用性。
[1] 蒋柱檀,李恒,刀志灵,等.云南传统食用植物海菜花(Otlelica acuminata)的民族植物学研究[J].内蒙古师范大学学报(自然科学汉文版),2010,39(2):163-168.
[2] 国家中医药管理局《中华本草》编委会.中华本草[M].上海:上海科学技术出版社,1999:7 104.
[3] 李原,杨君兴,崔桂华,等.海菜花营养成分初步分析[J].营养学报,2009,31(1):96-97.
[4] 朱静,杨亚维,郭爱伟,等.云南几大湖泊海菜花营养成分分析[J].安徽农业科学,2010,38(24):12 952-12 953.
[5] 殷建忠,周玲仙,王琦.云南产11种野生食用鲜花营养成分分析评价[J].食品研究与开发,2010,31(3):163-165.
[6] 曾涛,沈倩.电感耦合等离子体质谱法(ICP-MS)应用进展及展望[J].广东化工,2018,45(18):124-127.
[7] 宋敏,李蓓.电感耦合等离子体质谱法在食品中重金属检测中的应用[J].食品安全质量检测学报,2018,9(5):1 045-1 049.
[8] 张宏康,王中瑗,蔡斯斯.ICP-MS测定食品及相关产品中重金属等元素的研究进展[J].食品研究与开发,2016,37(17):195-200.
[9] 赵发,刘艳明,张喜琦,等.ICP-MS法蔬菜中七种元素同时测定[J].食品工业,2017,38(9):303-305.
[10] 冯新忠.电感耦合等离子体质谱法同时检测红枣中铅、砷、镉、汞、铜、锌和16种稀土元素[J].化学分析计量,2018,27(1):72-76.
[11] 陈国友.微波消解ICP-MS法同时测定蔬菜中14种元素[J].分析测试学报,2007(5):742-745.
[12] 李霞雪,刘爱平,陈亚,等.微波消解-电感耦合等离子体质谱法测定蔬菜中铬、镉、砷、铅、汞的含量[J].理化检验(化学分册),2019,55(1):39-45.
[13] 孙长霞,吴成亮,黄广远,等.预处理方法对可食性植物样品中微量元素测定结果的影响[J].食品工业科技,2009,30 (10):314-317;920.
[14] 刘亚轩,李晓静,白金峰,等.植物样品中无机元素分析的样品前处理方法和测定技术[J].岩矿测试,2013,32(5):681-693.
[15] 马生凤,温宏利,巩爱华,等.大试管回流消解-等离子体发射光谱/质谱法测定植物样品中多元素[J].岩矿测试,2007,26(3):183-187.
[16] 藏吉良,李志伟,赵伟,等.风冷回流消解-电感耦合等离子体质谱法同时测定植物样品中46个元素[J].岩矿测试,2012,31(2):247-252.
[17] 姚秀红,刘丽贞,杜俊逸,等.高温热水解-催化分光光度法测定植物样品中的痕量碘[J].地球与环境,2012,40(2):279-285.
[18] 周美丽,杨子秋,杨伟,等.3种前处理方法在电感耦合等离子体质谱测定螺旋藻中铅、镉含量的比较[J].食品与发酵工业,2018,44(12):256-260.
[19] 聂西度,符靓.盐酸浸提-电感耦合等离子体发射光谱法测定秋葵中Na、Mg、P、K、Ca含量[J].食品科学,2015,36(24):101-104.
[20] 聂西度,符靓,唐莉娟,等.电感耦合等离子体质谱法测定黑小麦中多种元素[J].食品科学,2015,36(12):125-128.
[21] 伍燕湘,周明慧,张洁琼,等.稀酸提取-ICP-MS法快速测定大米中锰、铜、锌、铅、镉、铷、锶含量的研究[J].中国粮油学报,2018,34(2):120-125.
[22] 郭红丽,张硕,王鹏娇,等.不同前处理法测定灵芝提取物中金属含量的对比研究[J].中国药学杂志,2016,51(2):96-100.
[23] GB 5009.268—2016, 食品安全国家标准食品中多元素的测定[S].北京:中国标准出版社,2017.