生物胺(Biogenic amines,BAs)是一类低分子量的含氮有机化合物,不具挥发性[1],热稳定性强,广泛存在于植物、动物和人体中。BAs根据其结构不同可分为3类:脂肪族(腐胺、尸胺、精胺、亚精胺)、芳香族(色胺、β-苯乙胺)和杂环族(组胺、酪胺)[2]。BAs作为一种有机碱,是细胞应对酸胁迫的产物,它是通过微生物(主要是细菌)产生的氨基酸脱羧酶作用于相应的氨基酸产生的[3],氨基酸脱羧酶使氨基酸脱去α-羧基产生相应的胺和CO2,如组氨酸脱羧生成组胺,酪氨酸脱羧生成酪胺,而腐胺则是由鸟氨酸(由谷氨酸和精氨酸转化而成)脱羧而成,并且可在亚精胺合成酶作用下进一步生成亚精胺[4]。不同的微生物可诱导不同BAs的产生,据报道,在大部分发酵食品中,革兰氏阴性菌、肠杆菌和假单胞菌是导致组胺、腐胺和尸胺积累的主要微生物[5],而在发酵肉制品中,由于在发酵过程中革兰氏阴性菌往往被抑制,因此革兰氏阳性菌,尤其是乳酸菌,是产生BAs的主要菌株[6]。
低浓度的生物胺具有生理活性,在人体中起着重要作用,它能够调节人体代谢,参与核酸和蛋白质的合成[7],但其含量积累到一定程度则会对人体有害,这是生物胺成为研究热点的主要原因之一。在BAs中,毒性最强的是组胺和酪胺,二者都具有细胞毒性作用,但作用方式显著不同。腐胺和尸胺是通过抑制组胺降解来间接增加组胺毒性,并且,据报道,腐胺的含量与胃癌的出现有密切的相关性[8],因此高效监测食品中的BAs以及制定限量标准成为当务之急。
目前,国内外用于检测食品中生物胺的常用方法主要有高效液相色谱法、气相色谱法、薄层色谱法、毛细管电泳法、生物传感器法等[9]。近几年,出现的新型检测方法有纳米纤维膜试纸技术[10]、竞争性荧光分子印迹聚合物(MIP)技术[11]、高光谱成像技术[12]等。高效液相色谱法具有柱效高、定量分析准确、灵敏度高等优点,因此依旧是最常用的生物胺分析检测技术。高效液相色谱检测生物胺面临的最大问题在于生物胺没有显著的紫外吸收峰,也不具备荧光特性,因此需要对生物胺进行衍生处理,衍生分为柱前衍生和柱后衍生2种,因柱后衍生设备昂贵、衍生产物不稳定、易分解,所以国内外目前广泛采用柱前衍生。丹磺酰氯和苯甲酰氯是最常用的生物胺柱前衍生剂[13],苯甲酰氯衍生温度低,时间短,但衍生产物不如丹磺酰氯衍生稳定。 NGELA等[14]采用中心复合设计优化了苯甲酰氯衍生生物胺的条件,研究表明,衍生剂体积和温度是影响苯甲酰氯衍生的最主要因素,在20 ℃,用量15 μL条件下衍生效果最好。LIU等[15]对丹磺酰氯和苯甲酰氯衍生产物的稳定性进行了对比分析,结果表明,苯甲酰氯的衍生物需要存放在4 ℃条件下,才能避免酪胺等衍生物的降解,而丹磺酰胺在4和25 ℃下保藏均能保持良好的稳定性。因此,丹磺酰氯更适合进行样品批处理。但不同的研究者在使用丹磺酰氯进行生物胺衍生时,采用的条件,即衍生温度、衍生时间、衍生剂体积等往往差异很大。
NGELA等[14]采用中心复合设计优化了苯甲酰氯衍生生物胺的条件,研究表明,衍生剂体积和温度是影响苯甲酰氯衍生的最主要因素,在20 ℃,用量15 μL条件下衍生效果最好。LIU等[15]对丹磺酰氯和苯甲酰氯衍生产物的稳定性进行了对比分析,结果表明,苯甲酰氯的衍生物需要存放在4 ℃条件下,才能避免酪胺等衍生物的降解,而丹磺酰胺在4和25 ℃下保藏均能保持良好的稳定性。因此,丹磺酰氯更适合进行样品批处理。但不同的研究者在使用丹磺酰氯进行生物胺衍生时,采用的条件,即衍生温度、衍生时间、衍生剂体积等往往差异很大。
虽然也有研究者优化生物胺的衍生条件,但并没有人探究过不同衍生因素之间的交互作用,而且在研究过程中往往以单个生物胺为考虑因素,而被检测样品中常含多种生物胺,所以实际意义可能并不大。因此本试验采用响应面法来优化丹磺酰氯的衍生条件,同时对衍生过程中3个关键因素:衍生温度、衍生时间和衍生剂用量之间的交互作用进行研究,以8种生物胺总面积为响应值,探讨衍生因素对多种生物胺衍生效果的综合影响,并在试验过程中对8种生物胺总面积作为响应值的合理性进行了验证,以期为生物胺衍生条件的优化提供科学、直观的理论依据。
1 材料与方法
1.1 材料与试剂
8种生物胺标准品(色谱纯):色胺、苯乙胺、腐胺、尸胺、组胺、酪胺、亚精胺、精胺,纯度均大于99%,购买于美国Sigma公司;丹磺酰氯、甲醇(色谱级)、乙腈(色谱级),购自重庆市钛新化工有限公司;HCl、NaOH、NaHCO3、NH3·H2O、丙酮、NaCl、三氯乙酸、正己烷均为分析级,购自上海源叶生物科技有限公司;娃哈哈纯净水、新鲜猪后腿肉、辅料(食盐,食品级NaCl、KCl、抗坏血酸钙,料酒、十三香、复合磷酸盐等),购自重庆市北碚区天生街道永辉超市;食品级Ⅱ-普通山楂核烟熏香味料,购买于济南华鲁食品有限公司。
1.2 仪器与设备
FA114A电子分析天平,上海海康公司;Lab Dancer漩涡混合器,德国IKA公司;HH-6富华数显恒温水浴锅,金坛市富华仪器有限公司;SB-5200DTD超声波清洗机,宁波SCIENTZ生物科技有限公司;L16M冷冻离心机,长沙湘智离心机仪器有限公司;LC-AD高效液相色谱仪,配有DGU-20A3自动过滤器、SPD-M20A PDA检测器、SIL-20A自动进样器、CTO-20A柱温箱,日本SHIMADZU公司;ChromplusTM C18(250 mm×4.6 mm×5 μm),美国SWELL公司。
1.3 试验方法
1.3.1 标准品及试剂的配制
标准品及试剂的配制参照陆永梅[16]和LI等[17]的方法,并稍作修改。
1.3.1.1 试剂的配制
1 mol/L HCl:量取8.6 mL盐酸于100 mL容量瓶中,用娃哈哈纯净水定容;0.1 mol/L HCl:用10 mL移液管吸取10 mL 1 mol/L HCl于100 mL容量瓶中,用娃哈哈纯净水定容;2 mol/L NaOH:称取8 g NaOH于烧杯中,用适量水溶解后转移至100 mL容量瓶中,加水定容;饱和NaHCO3:在100 mL水中加入NaHCO3,直至其不再溶解,所得上清液即为饱和NaHCO3溶液;10 mg/mL丹磺酰氯:准确称取0.5 g丹磺酰氯于50 mL烧杯中,加入适量丙酮溶解,将溶解液转移至50 mL容量瓶中,烧杯用丙酮清洗3次,并将清洗液转移至容量瓶中,最终用丙酮定容。
1.3.1.2 生物胺标准品的配制
生物胺混标使用液的配制:使用移液器分别吸取1 000 μL色胺、苯乙胺、腐胺、尸胺、酪胺、组胺、亚精胺、精胺的单标储备液(1 000 μg/mL)置于同一个10 mL容量瓶中,用0.1 mol/L HCl稀释至刻度,混匀,配制成100 μg/mL的含8种生物胺的混合使用液,存放在4 ℃冰箱保存。20 μg/mL生物胺使用液的配制:用移液枪移取2 mL 100 μg/mL的混标使用液,置于10 mL容量瓶中,用0.1 mol/L HCl稀释至刻度。
1.3.2 色谱条件
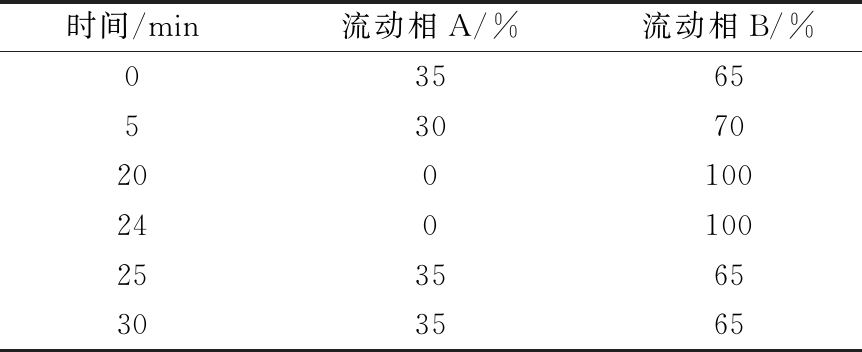
ChromplusTM C18(250 mm×4.6 mm×5 μm)色谱柱,柱温35 ℃,流速1 mL/min,检测波长254 nm,进样量20 μL;流动相A为娃哈哈纯净水,流动相B为色谱级乙腈,梯度洗脱程序如表1所示。有机相所占的比例在最初20 min一直在增加,随后保持最初比例直至洗脱结束,通过改变有机相的占比达到充分快速洗脱生物胺的目的。
表1 梯度洗脱程序
Table 1 Gradient elution program for biogenic amines analysis
时间/min流动相A/%流动相B/%0356553070200100240100253565303565
1.3.3 衍生程序
衍生操作参照![]() 等[18]的方法,并稍作修改。
等[18]的方法,并稍作修改。
吸取1 mL 20 μg/mL的生物胺混标溶液于10 mL离心管中,加入200 μL NaOH、300 μL饱和NaHCO3,使溶液呈碱性。涡旋振荡10 s后,加入适量10 mg/mL的丹磺酰氯,此时会出现分层现象,这表明衍生剂质量较好,并可用。将混合液涡旋20 s后放入水浴锅中,避光衍生。
衍生结束后,在混合液中加入100 μL NH3·H2O,混匀后,放入25 ℃水浴锅中进行终止反应。30 min后取出,用乙腈定容至5 mL,于4 ℃冷冻离心机中离心(3 000 r/min,10 min)。离心结束后,用2 mL注射器吸取上清液,过0.22 μm滤膜,然后注入1.5 mL进样小瓶中,待检测。
1.3.4 单因素试验设计
不同研究者采用丹磺酰氯衍生生物胺时,使用的衍生条件差异较大,最高的衍生温度可达65 ℃,时间为30 min[19],国内外以40 ℃,45 min[20-21]或45 ℃,60 min[15]作为衍生条件的较多,根据预试验,确定研究水平为衍生温度30、35、40、45、50 ℃;衍生时间25、30、35、40、45 min;衍生剂体积2、2.5、3、3.5、4 mL,以8种生物胺总面积为响应值。每组试验测定的指标均做3次平行。
1.3.5 衍生条件优化的响应面设计
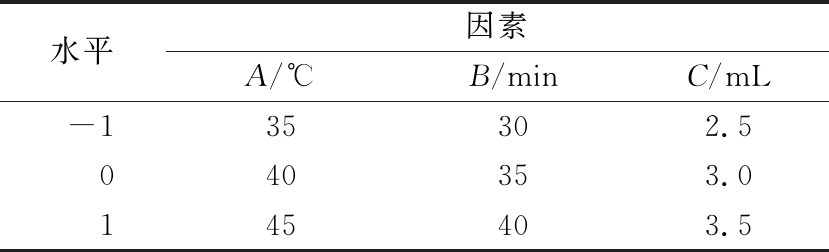
根据单因素试验结果,以衍生温度(A),衍生时间(B),衍生剂体积(C)为自变量,以生物胺总面积值(Y)为响应值,采用Design- Expert 8.06进行Box-Behnken试验设计,因素水平如表2所示。
表2 响应面试验因素水平表
Table 2 Factors and levels used in response surface design
水平因素A/℃B/minC/mL-135302.5040353.0145403.5
1.3.6 低盐腊肉样品中生物胺的检测
1.3.6.1 低盐腊肉的制备
低盐腊肉的制备参照柴子惠[22]的方法并稍作修改。选择肥瘦层次明显的新鲜猪后腿肉,去除淤血、筋膜,修整成瘦薄均匀、重约200 g的长条状肉块。将肉块浸泡在腌制液中,于10 ℃气温箱下密封腌制5 d,每隔24 h翻面一次,使肉块腌制均匀;腌制结束后,用适当温水洗去肉样表面杂质,采用液熏液液熏180 min;液熏结束后,于50 ℃烘箱中烘烤48 h,每隔12 h调整一下位置,使肉块受热均匀;将烘烤后的肉样取出,于自然条件下晾挂5 d,完成后熟即为成品,将样品储存在-18 ℃,待检测。
1.3.6.2 样品中生物胺的提取
样品生物胺的提取参照LIU等[15]的方法并稍作修改。取5 g(精确至0.01 g)绞碎的低盐腊肉,置于50 mL平底试管中,加入20 mL 5%的三氯乙酸溶液,均质处理1 min,获得匀浆,转移至100 mL具塞锥形瓶中,采用振荡提取方式(30 ℃,130 r/min)提取30 min后,转移至50 mL具塞离心管中离心(8 000×g,10 min,4 ℃),并将上清液转移至50 mL容量瓶中。残渣用提取试剂再提取1次,合并上清液,用提取试剂定容。
1.3.6.3 除脂
移取10 mL上述试样提取液于50 mL具塞试管中,加入0.5 g NaCl,待NaCl完全溶解后加入10 mL正己烷,涡旋振荡3 min,静置分层后弃去上层有机相,将下层试样溶液中加入10 mL正己烷,重复上述操作。
1.3.6.4 样品的衍生
样品的衍生采用上述响应面优化的衍生条件。具体衍生操作同标品。
1.3.7 数据处理
试验数据均采用IBM SPSS Statistics 17.0进行单因素方差分析,取置信度95%(P<0.05),采用Origin 2017绘图。
2 试验结果与讨论
2.1 单因素试验结果
2.1.1 衍生温度对衍生效果的影响
在衍生时间为35 min、衍生剂添加量为3 mL时,以8种生物胺总面积为响应值,由图1可知,当衍生温度小于35 ℃时,随着温度的升高,生物胺总面积呈下降趋势,当衍生温度介于35至40 ℃时,随着温度的升高,生物胺总面积值显著(P<0.05)升高,40 ℃时,达到最大;当继续升高衍生温度时,生物胺总面积则逐渐降低。这表明,适当升温会加快反应的进行,但温度过高则会影响丹磺酰胺的稳定。刘景等[23]在研究衍生温度对丹磺酰氯衍生组胺的影响时也发现适当升温会使衍生产物显著升高,但当温度超过60 ℃时,衍生产物则显著降低,但由于不同生物胺的热稳定性不同,因此最佳衍生温度对单胺来说并不固定。同时,有研究证实,高温导致丹磺酰胺的降解,在衍生物热稳定性方面,丹磺酰氯的衍生产物丹磺酰胺的耐高温能力比大四酰氯的衍生产物大四酰胺弱[24]。

图1 衍生温度对8种生物胺总面积的影响
Fig.1 Effect of derivatization temperature on the total area of 8 kinds of biogenic amine
试验过程中发现,在进行温度单因素试验时,8种生物胺中3种生物胺组胺、亚精胺、精胺的面积始终低于其他胺。为保证在生物胺总面积达到最大时,所有生物胺的面积尽可能均达到最大,由图2可知,这3种胺的总面积随温度的变化趋势与8种生物胺总面积的变化趋势几乎一致,而且也在40 ℃时达到最大值。这证实以生物胺总面积作为衍生温度的响应值是合理的。
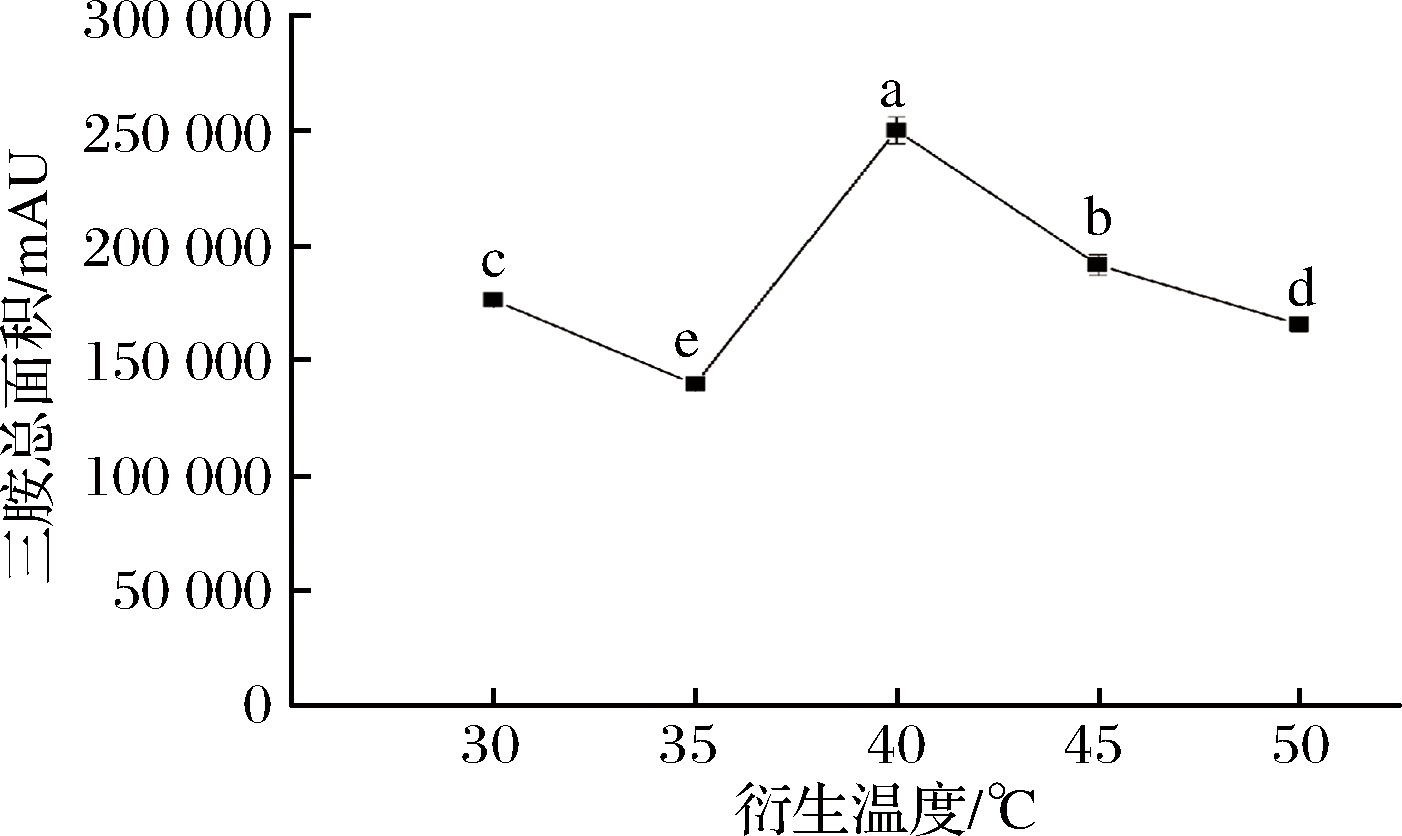
图2 衍生温度对3种生物胺总面积的影响
Fig.2 Effect of derivatization temperature on total area of 3 kinds of biogenic amines
2.1.2 衍生时间对衍生效果的影响
在衍生温度为40 ℃、衍生剂添加量为3 mL时,以8种生物胺总面积为响应值,由图3可知,当衍生时间在25~35 min时,随着衍生时间的延长,生物胺总面积显著增加,这表明在此段时间范围内,生物胺并未完全反应。当反应时间达到35 min时,生物胺总面积达到最大,随着时间的继续延长,生物胺总面积趋于稳定。这表明丹磺酰氯与生物胺反应存在饱和时间,此时二者反应已完全,继续延长反应时间无意义甚至出现负面效果。该结果与刘景[23]、吴迪[25]、董伟峰等[26]的类似。
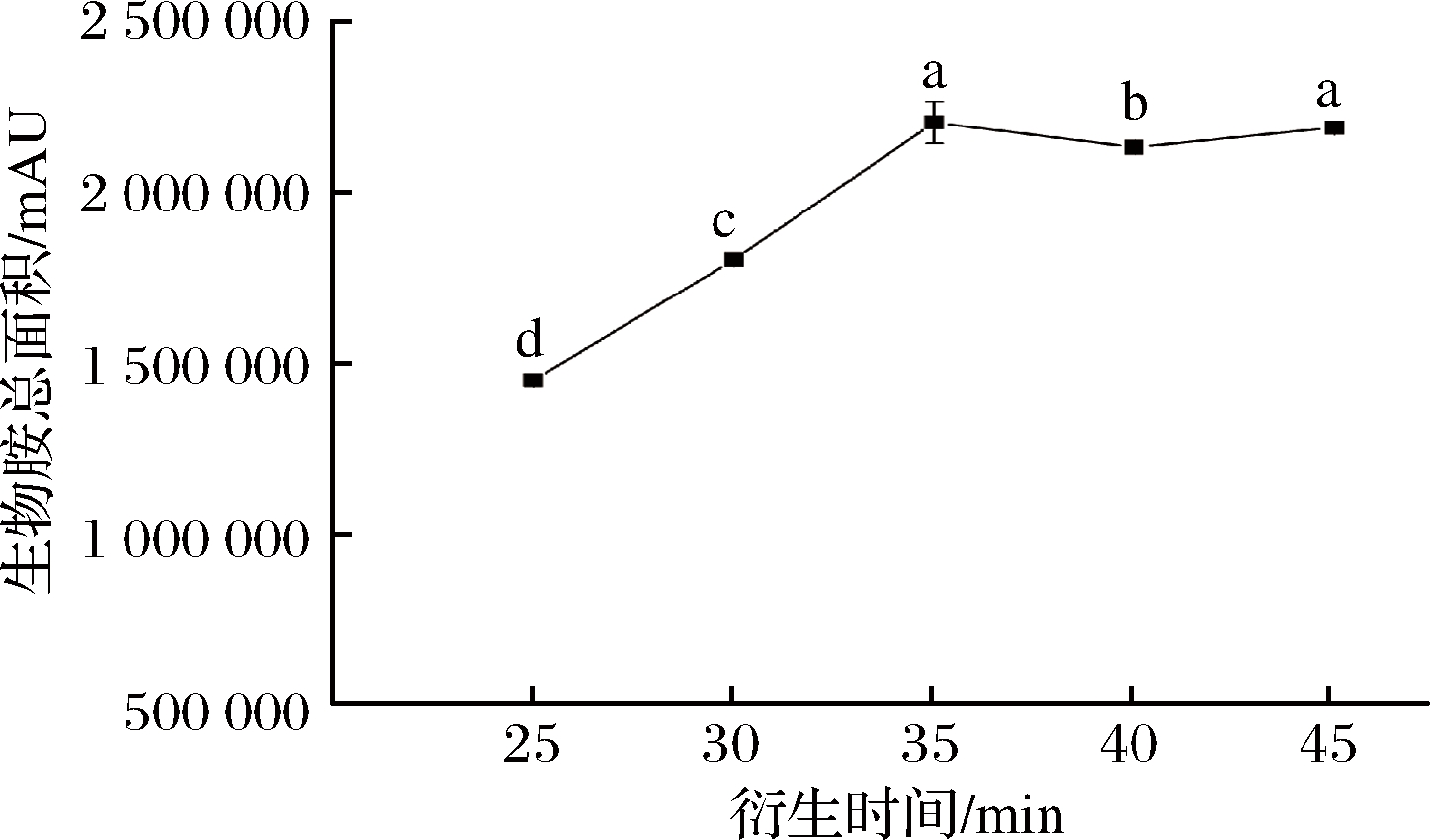
图3 衍生时间对8种生物胺总面积的影响
Fig.3 Effect of derivatization time on total area of 8 kinds of biogenic amine
在进行时间单因素试验时,8种生物胺中3种生物胺组胺、亚精胺、精胺的面积始终低于其他胺。因此本研究以这3种生物胺的总面积作为响应值,由图4可知,研究表明,3种生物胺总面积值随着衍生时间的延长呈现先增大后降低然后趋于稳定的趋势,在30 min时达到最大,35 min时有所降低,但二者之间并无显著差异。因此,选择生物胺总面积作为衍生时间的响应值是有效的。
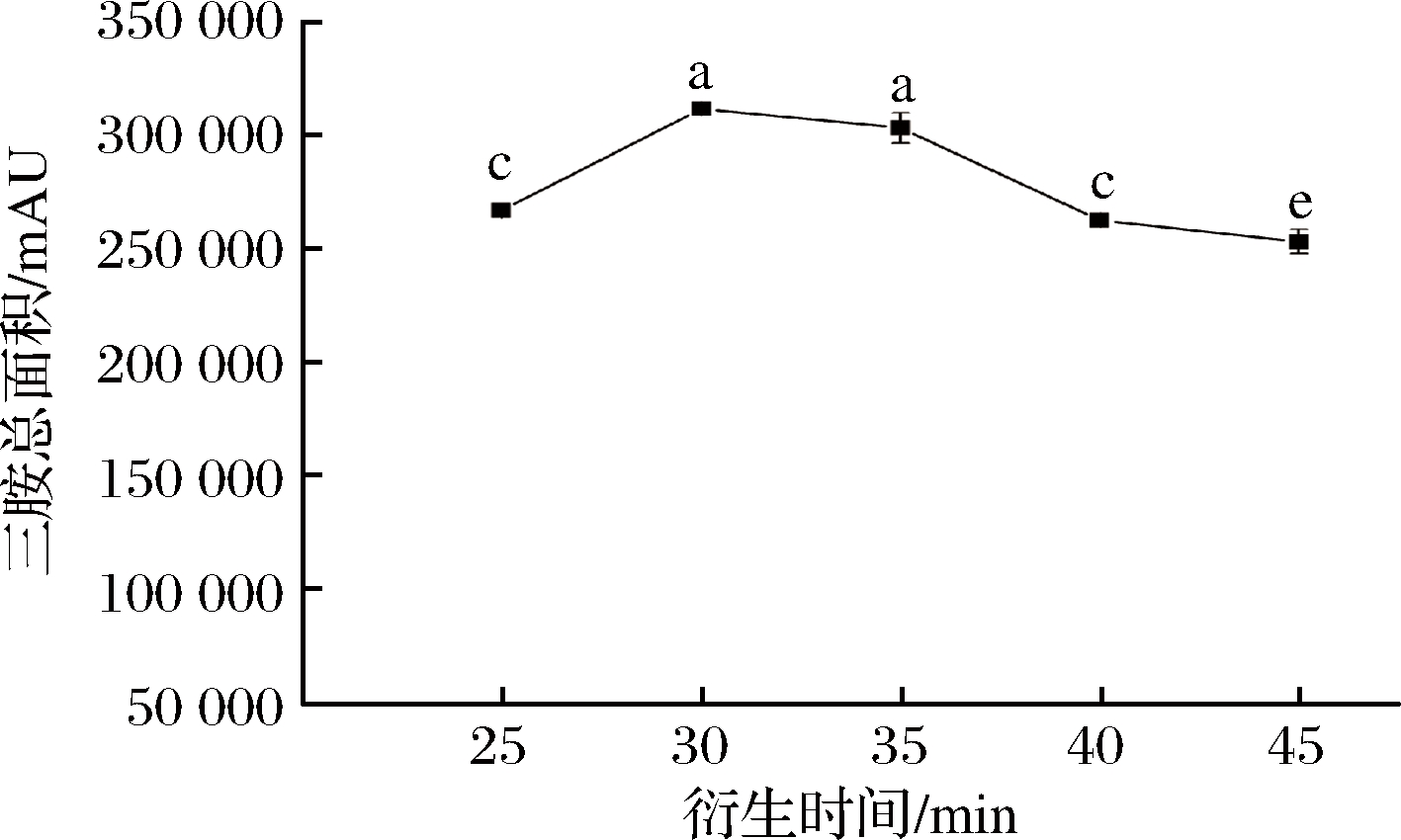
图4 衍生时间对3种生物胺总面积的影响
Fig.4 Effect of derivatization time on total area of 3 kinds of biogenic amine
2.1.3 衍生剂体积对衍生效果的影响
在衍生温度为40 ℃,衍生时间为35 min时,以8种生物胺总面积为响应值,由图5可知,当衍生剂用量小于3 mL时,随着衍生剂用量的增大,生物胺总面积值显著(P<0.05)增大,此时组胺、亚精胺、精胺的面积值仍小于其他5种生物胺。当衍生剂用量为3 mL时,生物胺总面积极显著(P<0.01)增大;当继续增大衍生剂的用量,生物胺总面积先降低后趋于稳定,此结果与吴迪等[25]类似。当衍生剂大于等于3 mL时,各生物胺的面积变化无明显规律,组胺、亚精胺、精胺不再是8种生物胺中响应值最小的3种生物胺,但通过试验表明,各生物胺的面积均在衍生剂体积为3 mL时达到最大,因此选择8种生物胺总面积值作为研究衍生剂体积对衍生效果的影响是可靠的。
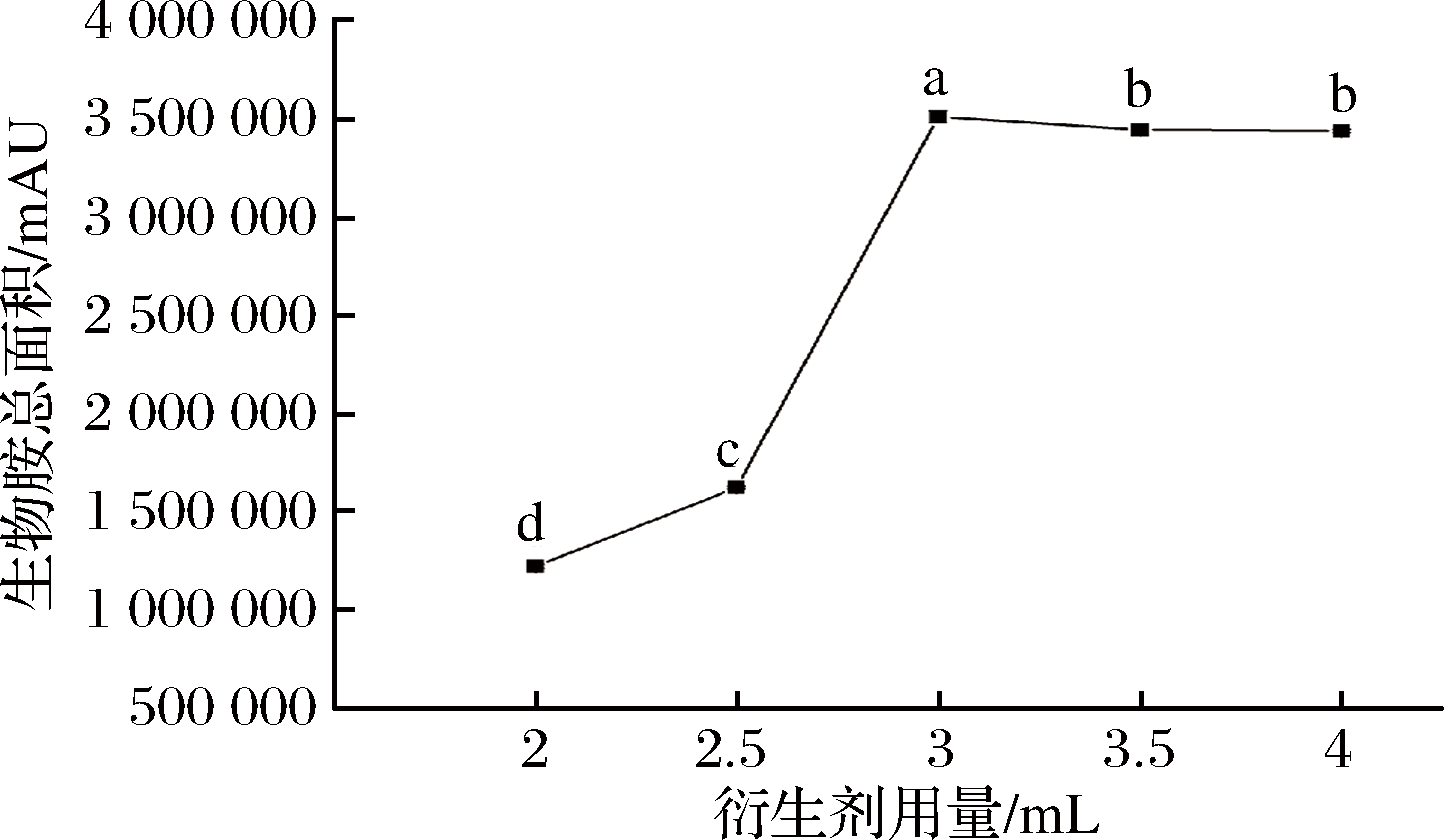
图5 衍生剂体积对生物胺总面积的影响
Fig.5 Effect of derivatizer volume on total area of 8 kinds of biogenic amine
通过上述单因素试验表明,在多种生物胺同时存在时,丹磺酰氯对不同胺的敏感程度可能不同,其对多胺(精胺、亚精胺)和组胺的反应能力要弱于其他胺。当反应时间并不充足,丹磺酰氯添加量不足时,这种现象尤为明显,而当反应时间最佳,反应温度适宜时适当增加丹磺酰氯的添加量可使这种差异性完全消失。
2.2 响应面结果分析
2.2.1 Box-Behnken试验结果
根据上述实验结果,分别选取衍生温度(A)、衍生时间(B)、衍生剂体积(C)中的高中低3水平进行Box-Brhnken响应面分析试验,其结果如表3所示。
2.2.2 多元回归模型的建立及显著性分析
对表3中的数据进行二次多元回归拟合,得到以生物胺总面积(Y)为响应值的回归方程(1)如下:
表3 响应面设计及试验结果
Table 3 Response surface design arrangement and experimental results
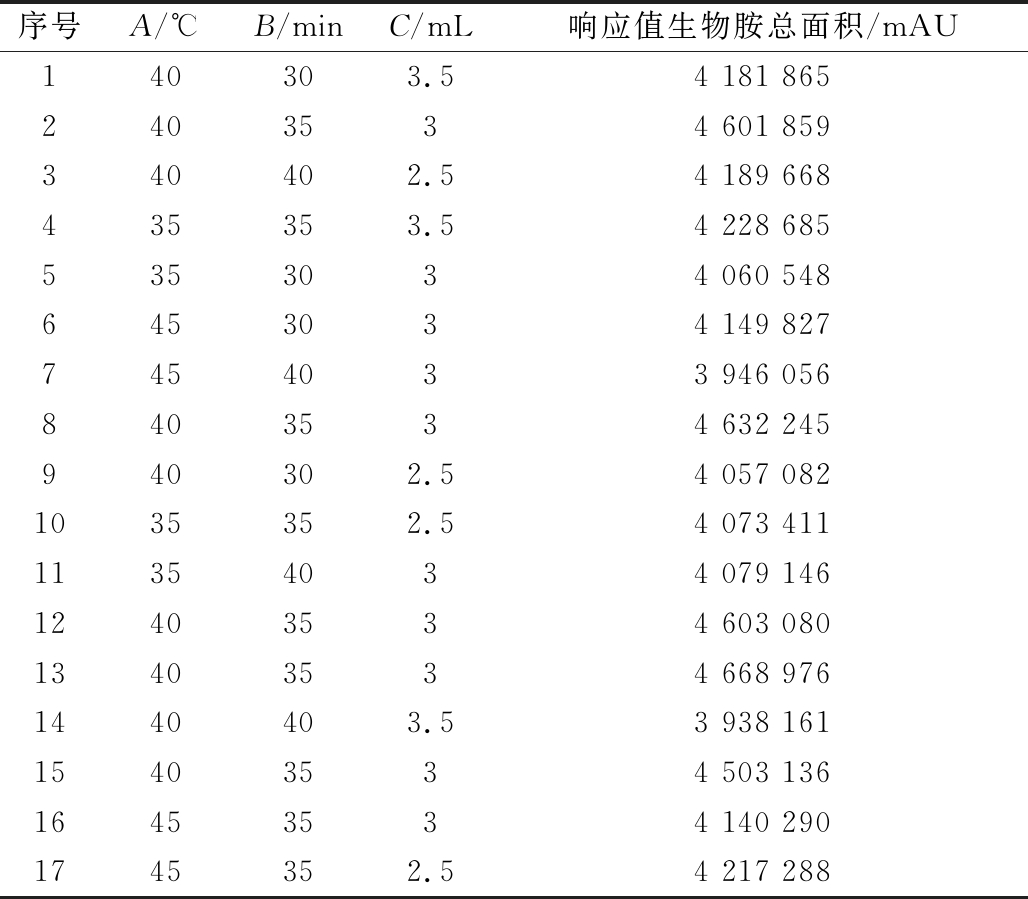
序号A/℃B/minC/mL响应值生物胺总面积/mAU140303.541818652403534601859340402.54189668435353.542286855353034060548645303414982774540339460568403534632245940302.540570821035352.540734111135403407914612403534603080134035346689761440403.5393816115403534503136164535341402901745352.54217288
Y=4 602 000+1 458.88A-37 036.37B-6 056.00C-55 592.25AB-58 068.00AC-94 072.50BC-234 900A2-308 100B2-202 100C2
(1)
对回归方程进行方差分析,结果见表4。
表4 生物胺总面积二次方模型回归方差分析
Table 4 Anlysis of variance (ANOVA)for regression equation

方差来源平方和自由度均方F值P值显著性模型9.668E+01191.074E+01133.65<0.0001**A1.703E+00711.703E+0075.333E-0030.9438B1.097E+01011.097E+0103.440.1061C2.934E+00812.934E+0080.0920.7706AB1.236E+01011.236E+0103.870.0898AC1.349E+01011.349E+0104.220.0789BC3.540E+01013.540E+01011.090.0126*A22.323E+01112.323E+01172.76<0.0001**B23.997E+01113.997E+011125.20<0.0001**C21.719E+01111.719E+01153.850.0002*残差2.235E+01073.192E+009失拟项7.171E+00932.390E+0090.630.6330纯误差1.518E+01043.794E+009总离差9.892E+01116决定系数R20.9774R2Adj0.9484信噪比14.938C.V(%)1.33
注:*-差异显著(P<0.05);**-差异极显著(P<0.01)。
由表4可知,方程的一次项A、B、C对Y的影响不显著;二次项A2、B2对Y的影响均为极显著(P<0.01),C2对Y的影响为显著(P<0.05);交互项中AB、AC对Y的影响均为不显著,而BC对Y的影响显著,且P值为0.012 6,这表明衍生时间和衍生剂用量在生物胺衍生过程中存在协同增效作用,而衍生温度与衍生时间、衍生温度和衍生剂用量之间则无此作用。由F值可知,3个因素对生物胺总面积影响的强弱顺序为B、C、A,即衍生时间、衍生剂用量、衍生温度;且衍生时间与衍生剂用量(BC)具有较强的交互作用。
本试验选择的回归模型为极显著(P<0.01),且决定系数R2和校正决定系数![]() 分别为0.977 4、0.948 4,这表明该方程的拟合效果较好。变异系数C.V代表实验的精确度,C.V越小,证明实验越可靠[26]。本试验C.V较低,为1.33%,说明该试验操作可信度高,真实可靠。
分别为0.977 4、0.948 4,这表明该方程的拟合效果较好。变异系数C.V代表实验的精确度,C.V越小,证明实验越可靠[26]。本试验C.V较低,为1.33%,说明该试验操作可信度高,真实可靠。
2.2.3 响应面因素交互作用分析
如表4所示,当以8种生物胺总面积为响应值时,衍生温度与衍生时间并无交互作用,这与刘景等[23]的研究结果相悖,可能是由于其研究是以组胺单胺为主,而本研究则考虑衍生因素对多种生物胺衍生效果的综合影响,并且有研究表明不同生物胺的热稳定性不同[28],当研究的生物胺种类和数量不同时,即使温度一致,最佳时间也会有显著差异[26,29],这也证实当考虑衍生因素对多种生物胺的综合影响时,衍生温度和衍生时间并无显著交互作用。
在响应面中,坡度、等高线形状反映了因素对响应值的影响强弱,坡度越陡表明因素对响应值的影响越大,等高线呈椭圆形则意味着两因素交互作用对响应值影响大[30]。响应面分析表明,BC,即衍生时间与衍生剂用量具有显著交互作用,响应面和等高线图如图6所示。由图6可知,生物胺总面积的最大值位于响应面的中心,并且衍生时间和衍生剂体积的交互作用等高线图呈明显的椭圆形,说明二者交互作用显著,对生物胺总面积有显著影响。当衍生剂体积用量3 mL和衍生时间35 min左右时,生物胺总面积值达到最大,表明此条件下衍生效果最好;当丹磺酰氯用量小于3 mL,衍生时间小于35 min时,生物胺总面积随着二者的增加而增加,表明在此范围内,衍生剂用量与衍生时间具有协同作用,延长衍生时间有利于丹磺酰氯与生物胺的充分反应;当衍生剂用量大于最佳添加量,衍生时间延长至超过最佳反应时间时,随着二者的增加,生物胺总面积值先降低后趋于稳定,这可能是由于反应时间的延长会降低衍生剂的效力,或是由于更复杂的原因,即反应时间的延长提高了衍生物对温度的敏感性,因此导致生物胺总面积的降低,但其具体机理尚不明确,有待进一步研究。
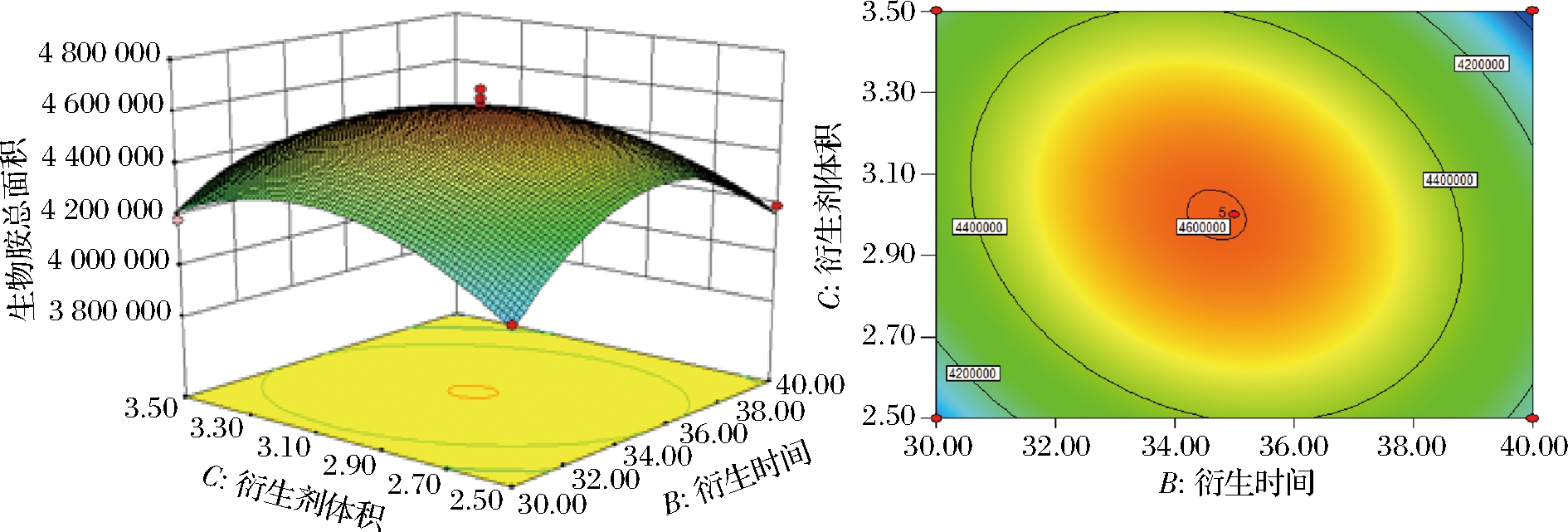
图6 BC交互作用的响应面和等高线图
Fig.6 Contour and response surface plots showing the interactive effects of BC
2.3.4 响应面生物胺衍生程序优化及验证试验
通过模型进行优化,得出生物胺衍生程序的最佳参数为衍生温度40.06 ℃、衍生时间34.70 min、衍生剂体积3 mL,由模型得到生物胺总面积的预测值为4 602 988。结合实际实验的可操作性,将最优衍生参数调整为衍生温度40 ℃、衍生时间35 min,衍生剂体积3 mL。使用上述参数进行验证试验,得到生物胺总面积为4 600 771,与预测值的吻合率达到100.05%,说明该模型能较好地预测生物胺的衍生效果,具有较高参考价值。
2.3.5 8种生物胺色谱图
按上述优化的衍生条件处理20 μg/mL的生物胺混标溶液,然后进行高效液相色谱检测,结果如图7所示。序号1-8,分别代表色胺、苯乙胺、腐胺、尸胺、组胺、酪胺、亚精胺、精胺。
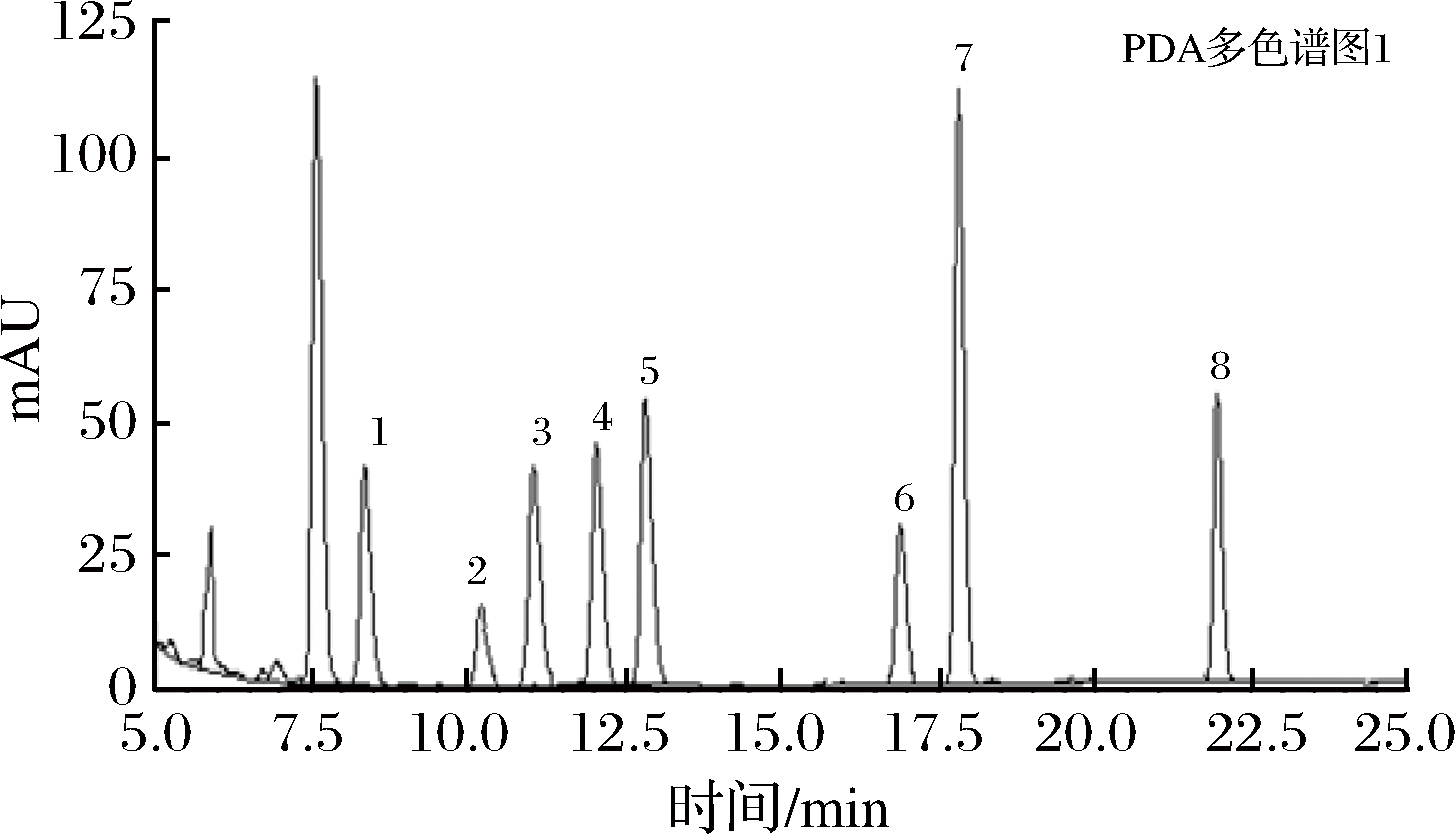
1-色胺;2-苯乙胺;3-腐胺;4-尸胺;5-组胺;6-酪胺;7-亚精胺;8-精胺
图7 八种生物胺标准品的色谱图
Fig.7 HPLC chromatogram of standard solutions of 8 kinds of biogenic amine
2.3.6 低盐腊肉中的生物胺
采用响应面法优化的衍生条件衍生低盐腊肉样品中的生物胺,结果如图8所示。在低盐腊肉成品中,8种生物胺均被检出,其中精胺和苯乙胺含量最高,分别为51.30、47.67 mg/kg,尸胺含量最低,为2.45 mg/kg。腐胺、组胺、酪胺、亚精胺含量差异则不显著(P<0.05),其含量分别为10.56、13.89、12.59、11.20 mg/kg。低盐腊肉中生物胺的种类和含量与原料肉的卫生条件和具体的加工工艺有关。采用此方法衍生腊肉中的生物胺数据较为稳定。
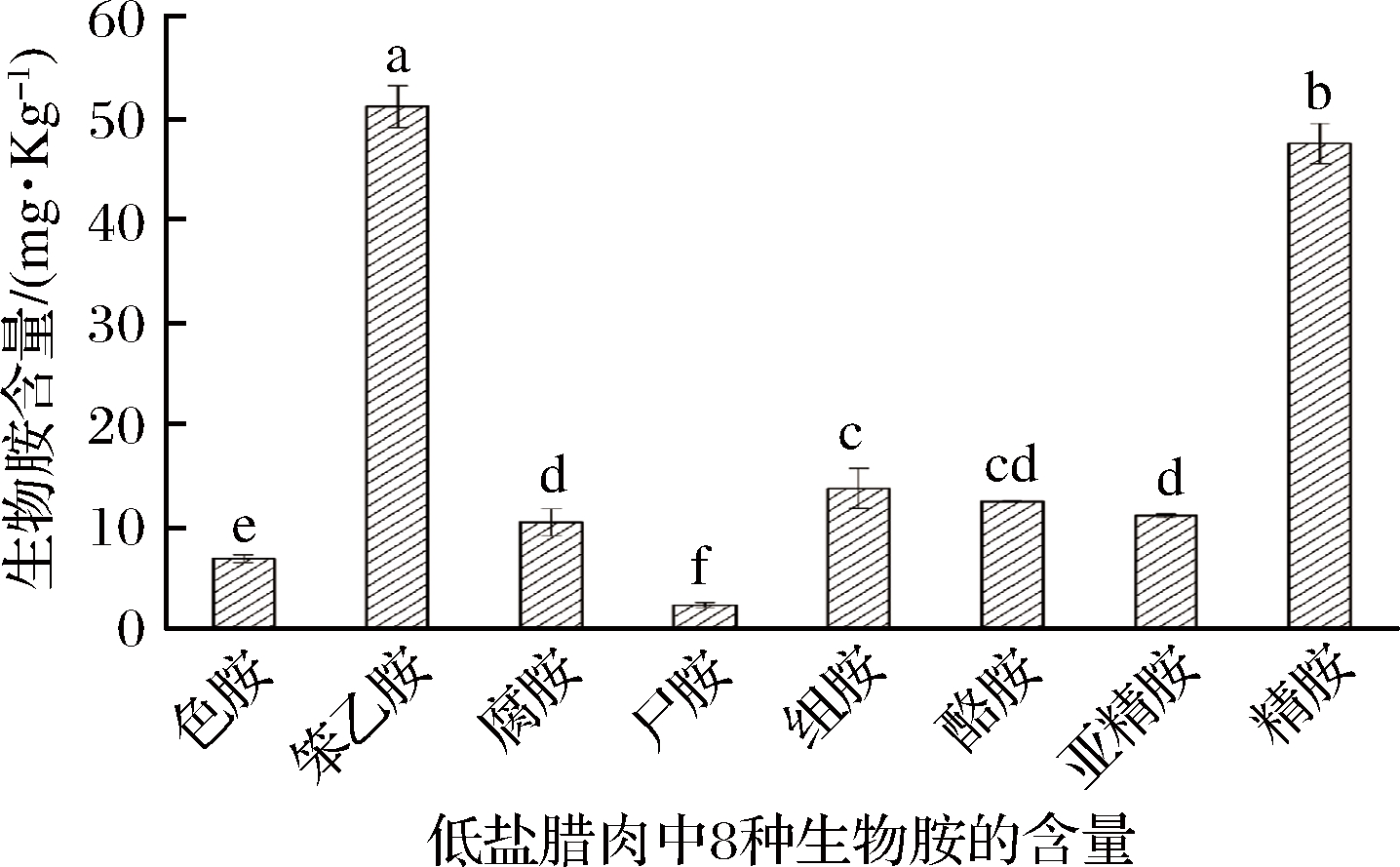
图8 低盐腊肉中的生物胺
Fig.8 BAs concentrations in low-salt bacon
3 结论
食品中生物胺产生需要具备3个条件:(1)可利用的氨基酸前体(2)氨基酸脱羧酶(3)产生氨基酸脱羧酶的微生物。因此,发酵食品(如奶酪、酒类、酱类和香肠、腊肉等发酵肉制品)是生物胺积累的合适底物,也是监测的主要对象。由于生物胺本身的特性,导致其检测前需要进行衍生处理。生物胺衍生使用最多的是丹磺酰氯,其衍生过程受到衍生温度、衍生时间、衍生剂用量等条件的制约,而不同学者在研究生物胺时,采用的衍生条件各异。本试验采用Box-Behnken设计,以生物胺总面积为响应值,优化了衍生过程中所用衍生温度、衍生时间、衍生剂用量的最佳值,方差检验表明所建模型回归效果极显著,拟合度良好,可用于最优衍生条件的预测。通过回归优化结合具体实验操作得出,使用10 mg/mL丹磺酰氯衍生20 μL/mL的生物胺混标工作液,在衍生温度为40 ℃、衍生时间35 min、衍生剂添加量3 mL时,衍生物产率最高。此衍生条件可用于有效检测样品中的多种生物胺。
[1] ALVAREZ M A,VICTORIA M M.The problem of biogenic amines in fermented foods and the use of potential biogenic amine-degrading microorganisms as a solution[J].Trends in Food Science &Technology,2014,39(2):146-155.
[2] MOHAMMED G I,BASHAMMAKH A S,ALSIBAAI A A,et al.A critical overview on the chemistry,clean-up and recent advances in analysis of biogenic amines in foodstuffs[J].Trends in Analytical Chemistry,2016,78(40):84-94.
[3] WUNDERLICHOVA L,BUNKOVA L,KOUTNY M,et al.Formation,degradation,and detoxification of putrescine by foodborne bacteria:a review[J].Compr.Rev.Food Sci.Food Saf.2014,13:1 012-1 033.
[4] HERNANDEZ-ORTE P,LAPENA A C,PENA-GALLEGO A,et al.Biogenic amine determination in wine fermented in oak barrels:factors affecting formation[J].Food Research International,2008,41(7):697-706.
[5] LANDETE J M,DE-LAS-RIVAS B,MARCOBAL A,et al.Updated molecular knowledge about histamine biosynthesis by bacteria[J].Crit Rev Food Sci Nutr,2008,48:697-714.
[6] MARCOBAL A,DE-LAS-RIVAS B,LANDETE J M,et al.Tyramine and phenylethylamine biosynthesis by food bacteria[J].Crit Rev Food Sci Nutr,2012,52:448-467.
[7] SMITH T A.Amines in food[J].Food Chemistry,1980,6:169-200.
[8] THERUVATHU J A,JARUGA P,NATH R G,et al.Polyamines stimulate the formation of mutagenic 1,N2-propanodeoxyguanosine adducts from acetaldehyde[J].Nucl Acid Res,2005,33:3 513-3 520.
[9] 盛雅萍.不产组胺和酪胺乳酸菌的筛选及其对发酵羊肉香肠品质的影响[D].呼和浩特:内蒙古农业大学,2017.
[10] YOUROVA N S,DANCHUK A,MOBAREZ S N.Functional electrospun nanofibers for multimodal sensitive detection of biogenic amines in food via a simple dipstick assay[J].Anal Bioanal Chem 2018,410:1 111-1 121.
[11] MATTSSON L,XU J J,PREININGER C,et al.Competitive fluorescent pseudo-immunoassay exploiting molecularly imprinted polymers for the detection of biogenic amines in fish matrix[J].Talanta,2018,181:190-196.
[12] YANG D,LU A X,REN D,et al.Rapid determination of biogenic amines in cooked beef using hyperspectral imaging with sparse representation algorithm[J].Infrared Physics &Technology,2017,86:23-34.
[13] MOHAMMMED G I,BASHAMMAKH A S,ALSIBAAI A A,et al.A critical overview on the chemistry,clean-up and recent advances in analysis of biogenic amines in foodstuffs[J].Trends in Analytical Chemistry,2016,78:84-94.
[14]  NGELA K,ARGOTTY S,JUAN J,et al.Central composite design to optimizate the derivatization procedure for analysis of biogenic amines by HPLC-UV[J].J Braz Chem Soc,2017,28(4):575-581.
NGELA K,ARGOTTY S,JUAN J,et al.Central composite design to optimizate the derivatization procedure for analysis of biogenic amines by HPLC-UV[J].J Braz Chem Soc,2017,28(4):575-581.
[15] LIU S J,XU J J,MA C L,et al.A comparative analysis of derivatization strategies for the determination of biogenic amines in sausage and cheese by HPLC[J].Food Chemistry,2018,266:275-283.
[16] 陆永梅.不产组胺和酪胺乳酸菌的筛选及其对发酵羊肉香肠品质的影响[D].南京:南京农业大学,2008.
[17] LI J,GUAN R F,WEI X M,et al.Detection of ten biogenic amines in Chinese commercial soybean paste by HPLC[J].International Journal of Food Properties,2018,21(1):1 344-1 350.
![]() A,et al.Biogenic amines content in traditional dry fermented sausage Petrovská klobása as possible indicator of good manufacturing practice[J].Food Control,2012,23:107-112.
A,et al.Biogenic amines content in traditional dry fermented sausage Petrovská klobása as possible indicator of good manufacturing practice[J].Food Control,2012,23:107-112.
[19] ZOTOU A,LOUKOU Z,SOUFLEROS E,et al.Determination of biogenic amines in wines and beers by high performance liquid chromatography with pre-column dansylation and ultraviolet detection[J].Chromat-ographia,2003,57(7-8):429-439.
[20] 王永丽.植物多酚及盐替代对干腌培根生物胺及亚硝胺调控机制研究[D].南京:南京农业大学,2015.
[21] 王新惠,张崟,王卫,等.四川腌腊肉制品食用安全性分析[J].食品工业科技,2014,35(24):49-56.
[22] 柴子惠,李洪军,李少博,等.低盐腊肉加工期间品质和菌相变化[J].肉类研究,2018,32(11):1-8.
[23] 刘景,苏米亚,徐致远,等.响应面法优化高效液相色谱-柱前衍生化检测发酵乳制品中的组胺[J].分析检测,2017,40(6):24-28.
[24] DE-MEY E,DRABIK-MARKIEWICZ G,DE-MAERE H,et al.Dabsyl derivatisation as an alternative for dansylation in the detection of biogenic amines in fermented meat products by reversed phase high performance liquid chromatography[J].Food Chemistry,2012,130:1 017-1 023.
[25] 吴迪,黄海琴,蔡成岗,等.生物胺丹磺酰氯衍生条件优化研究[J].食品与发酵科技,2018,54(1):45-49.
[26] 董伟峰,李宪臻,林维宣.丹磺酰氯作为生物胺柱前衍生试剂衍生化条件的研究[J].大连轻工业学院学 报,2005,24(4):115-118.
[27] DRAPER N R.Response surface methodology:Process and product optimization using designed experiments[J].Journal of Statistical Planning and Inference,1997,59(1):185-186.
[28] RUIZ-CAPILLAS C,HERRERO A M.Impact of Biogenic Amines on Food Quality and Safety[J].Foods,2019,8(62):1-16.
[29] 李志军,吴永宁,刘浩,等.葡萄酒中生物胺多组分的U -VD/FLD串联HPLC方法研究[J].卫生研究,2005,34(5):577-580.
[30] 顾仁勇,杨万根.响应面试验优化低盐湘西腊肉复配防腐剂的配方[J].食品科学,2015,36(22):46-49.