龙眼(Dimocarpus longan Lour)属无患子植物,主要在我国南方的广东、福建、广西、台湾等省(区)种植,其果实营养丰富,且药用价值较高,自古以来深受人们喜爱,更被视为珍贵补品[1]。但由于其收获季节性强、上市集中,果实皮薄多汁,易造成机械伤害;果实呼吸代谢高,蒸腾作用强,果实极易失水,造成萎蔫、褐变等特点,龙眼在采后损耗相当严重,将新鲜龙眼制成龙眼干(桂圆)是解决龙眼鲜果出路,保证龙眼产品常年供应的主要措施之一[2]。然而面对大量加工好的龙眼干,如何保证其贮藏稳定性、延长其货架期,成为学者们关注的重点。
迄今已有大量研究表明水分吸附等温线对预测食品货架期稳定性、贮藏期间湿度的变化、确定合适的包装和保质期具有的重要作用[3-6]。水分吸附等温线是指在一定的温度和相对湿度环境下,平衡含水率随水分活度变化的曲线[7]。通过不同温度下的吸附等温线数据进行拟合分析,可求得净等量吸附热、焓变和熵变等热力学特性参数,进而获得食品水分吸附过程中水的特性和能量需求信息,揭示食品水分吸附机理。目前,国内外学者们针对荔枝[8]、花椒[9]、杏仁[10]、豌豆种子[11]、核桃仁[12]、澳洲坚果[13]、玉米[14-15]、大米淀粉[16]、小麦粉[17]等食品的水分吸附等温线与热力学特性做了大量的研究,研究结果为食品储藏和包装提供了参考依据。而针对龙眼吸附等温线,学者们也进行了相关的探讨,陈羽白等[18]采用静态称重法,试验测定了“石硖”龙眼在不同温度和相对湿度条件下的解吸和吸湿平衡含水率,探讨了温度和相对湿度对“石硖”龙眼平衡含水率的影响,并对比分析了各平衡含水率模型对实验数据的拟合精度,确定了Halsey模型描述“石硖”龙眼平衡含水率的最适模型。JANJAI等[19]建立预测龙眼平衡含水率的多层神经网络模型,并利用反向传播算法对模型进行训练,结果发现经过训练后的模型具有较高的预测能力,效果优于GAB等传统模型预测方法,并在此基础上对龙眼净等量吸附热和熵变进行分析。由于平衡含水率与物料种类、物性特征、化学组分和环境条件等因素密切有关。“储良”龙眼是中国龙眼的主要种植品种之一,除部分鲜食外,大部分均为干制食品,但有关干制“储良”龙眼吸附等温线及热力学特性的研究目前未见相关报道。
为此,本文以干制“储良”龙眼作为实验物料,实验测定了干制“储良”龙眼在贮藏温度(20、30和40 ℃)和水分活度(0.113~0.946)条件下的吸附平衡含水率,并绘制其水分吸附等温线,在此基础上采用6种常用的农产品吸附模型进行拟合分析,获得描述干制“储良”龙眼吸附等温线的最适模型和在室温下储藏的安全含水率;同时,探讨干制“储良”龙眼的热力学特性,研究结果为“储良”龙眼加工、包装、贮藏和品质控制提供参考依据。
1 材料与方法
1.1 实验物料与试剂
实验用龙眼采购于广州市天河区长湴市场新鲜采摘的龙眼,品种为“储良”;龙眼前期进行剪枝、清洗和分级后,挑选个体饱满的作为本次实验物料,初始含水率为251.86%d.b.(干基含水率,下同)。用于吸附实验的样品先在50 ℃条件下干燥至含水率5%d.b.,并将其放置于5 ℃环境下密封保存待用。以密闭条件下饱和盐溶液在实验温度(20、30和40 ℃)时对应的相对湿度作为龙眼吸附实验环境的相对湿度(水分活度,小数),所选用的饱和盐:LiCl、MgCl2、Mg(NO3)2、KI、KNO3,皆为分析纯。
1.2 主要仪器设备
本实验所使用的仪器主要有:DZF-6050电热恒温真空干燥箱,上海一恒科技有限公司;PL-3K恒温恒湿装置,日本ESPEC;BS224S分析天平,赛多利斯科学仪器(北京)有限公司。
1.3 实验方法
1.3.1 吸附平衡含水率测定
采用静态称量法测定干制“储良”龙眼在不同温度和水分活度条件下的吸附平衡含水率。在前期处理好的的样品中选取果体表面无凹陷、无破裂、大小基本一致的干果为试样,各取5颗干果称重(且对每颗干果作记号),放入分别装有5种饱和盐溶液的密封玻璃干燥器皿中(水分活度0.113~0.946,如表1所示),并置于20、30、40 ℃的恒温恒湿箱中进行实验。对应温度和水分活度条件下分别做两组平行实验,每隔2 d称量一次,当连续3次质量平均值变化小于0.002 g时实验结束,并测定此时龙眼的含水率,该含水率即为对应该温度和水分活度下的吸附平衡含水率。初始含水率参照国标GB 5009.3—2016方法测定[20],3次测定取平均。而该温度下的吸附等温线,就是吸附平衡含水率和水分活度的关系曲线。
表1 不同条件下饱和盐溶液的水分活度
Table 1 Water activity of different saturated salt solutions under different conditions
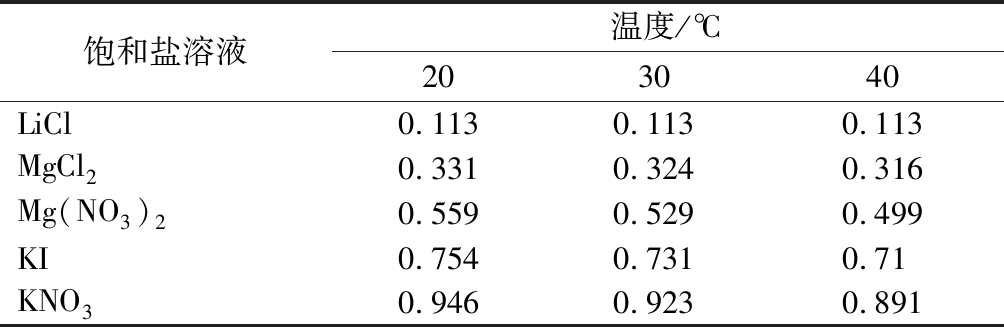
饱和盐溶液温度/℃203040LiCl0.1130.1130.113MgCl20.3310.3240.316Mg(NO3)20.5590.5290.499KI0.7540.7310.71KNO30.9460.9230.891
1.3.2 吸附等温线模型
参考国内外相关研究[21-24],选取应用较为广泛的6种农产品吸附平衡含水率模型对干制“储良”龙眼的吸附等温线进行拟合分析,如表2所示。
表2 吸附等温线模型
Table 2 Models for sorption isotherm

序号模型名称模型表达式1BETMe=m0caw(1-aw)[1+(c-1)aw]2HalseyMe=-alnaw()1/b3PelegMe=k1awn1+k2awn24SmithMe=a+bln(1-aw)5GABMe=m0ckaw(1-kaw)[1-kaw+ckaw]6OswinMe=aaw1-aw()b
注:Me-吸附平衡含水率,%d.b.;aw-水分活度;m0、c、k、a、b、k1、k2、n1、n2,均为模型常数。
模型拟合效果采用决定系数R2和均方根误差(root mean square error,RMSE)进行评价。R2越高,RMSE越低,说明模型拟合效果越好。如公式(1)所示
(1)
式中:RMSE,均方根误差;Mexp,i,平衡含水率的实验值,%;Mpre,i,平衡含水率的预测值,%;N,数据个数。
1.3.3 热力学特性参数确定
对于给定的含水率,净等量吸附热qst可通过克劳修斯-克拉贝龙(Clausius-Clayperon)方程计算[8, 25],如公式(2)所示:
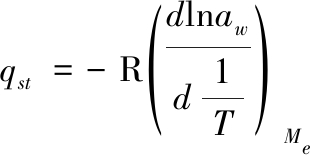
(2)
式中:qst,净等量吸附热,kJ/mol;T,绝对温度,K;aw,水分活度;R,通用气体常数,8.314 J/(mol·K);Me,平衡含水率,%d.b.。由公式(2)可知,通过lnaw与1/T作图可得到一条直线,由直线的斜率可确定净等量吸附热。而熵变(ΔS)可由吉布斯-亥姆霍兹方程计算,如公式(3)和公式(4)所示:
(3)
ΔG=-RTlnaw
(4)
将公式(4)代入公式(3)可得焓变ΔH与熵变ΔS之间的关系,如公式(5)所示;通过-lnaw与1/T做直线,并求直线的斜率和截距,可得到ΔH和ΔS。
(5)
式中:ΔH,焓变,kJ/mol;ΔS,熵变,kJ/(mol·K);ΔG,吉布斯自由能,kJ/mol。
1.3.4 焓-熵补偿理论
物料在不同条件下水分吸附基质以及吸附过程中涉及的物理、化学现象可通过焓-熵互补理论解释。该理论认为,对于特定的含水率,吸附的ΔH和ΔS之间成线性关系,如公式(6)所示[26-27]:
ΔH=Tβ(ΔS)+ΔGβ
(6)
式中:Tβ,等速温度,表示在吸附过程所有反应以相同的速率进行时的温度,K;ΔGβ,温度为Tβ时的自由能,kJ/mol。Tβ和ΔGβ分别为公式(6)ΔH与ΔS线性回归的斜率和截距。为证实补偿理论,KRUG等[28]推荐采用调和平均温度Thm与Tβ进行比较。调和平均温度定义如公式(7)所示:
(7)
式中:n,实验测定的等温线的数量;只有在Tβ≠Thm时,焓-熵补偿理论才适用。当Tβ>Thm时,吸附过程是焓驱动;而当Tβ<Thm时,则认为是熵驱动。
1.4 数据处理
对实验所得结果采用软件Excel和Matlab进行非线性回归和统计分析。
2 结果与分析
2.1 干制“储良”龙眼吸附等温线
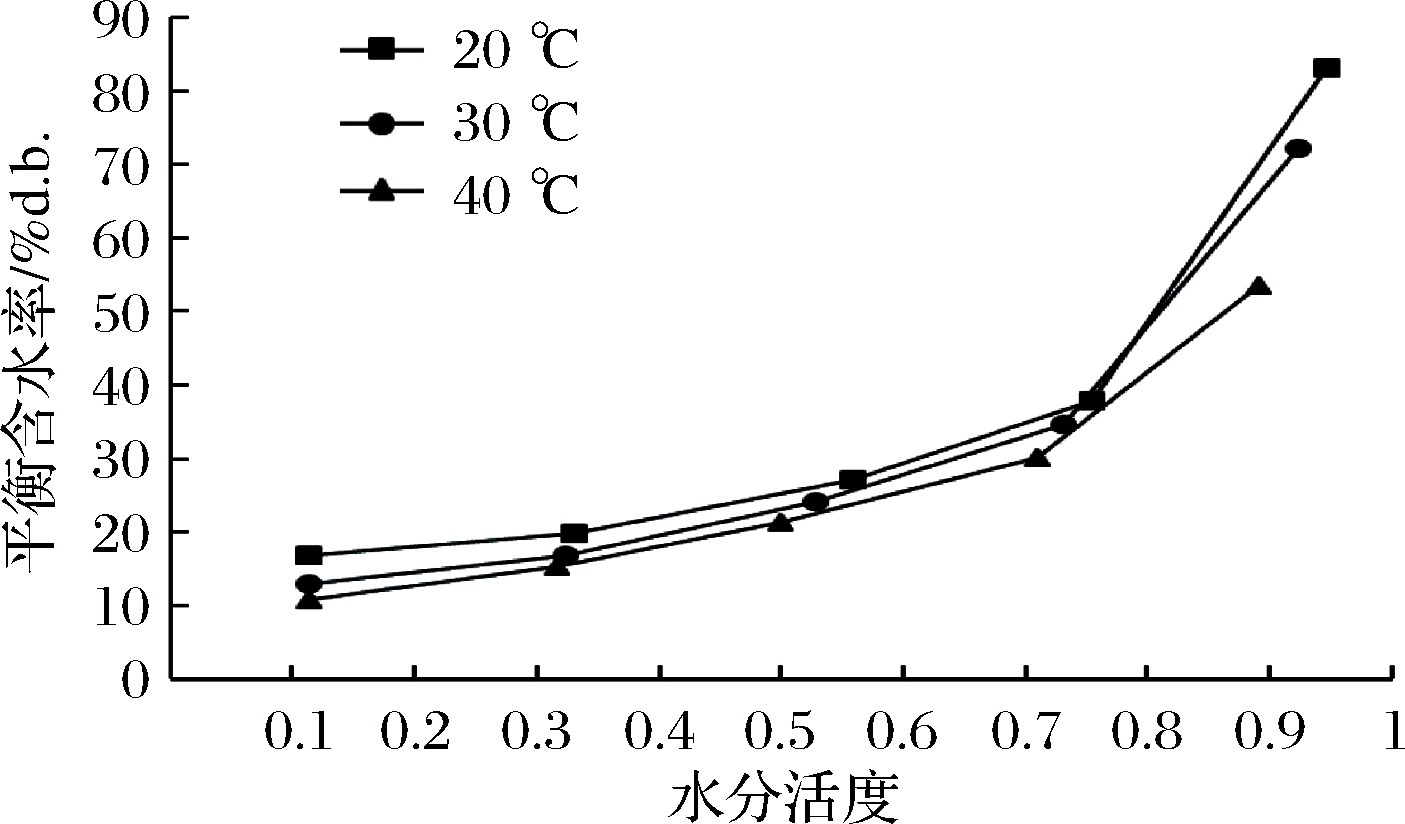
图1 干制“储良”龙眼吸附等温线
Fig.1 Sorption isotherm of dried "Chuliang" longan
由图1可知,干制“储良”龙眼在温度为20、30和40 ℃下的吸附等温线形状相似,按国际理论和应用化学联合会(international union of pure and applied chemistry, IUPAC)规定的分类方法,该吸附等温线属第Ⅲ种类型[29]。平衡含水率随水分活度的增加而增加。在水分活度为0.1~0.7时,平衡含水率增加较缓慢,当水分活度大于0.7时,则迅速增大。在水分活度相同的条件下,平衡含水率随温度的升高而降低,这可能是由于在较高的温度下,水分子变得活跃,很容易摆脱吸附的结合位点,从而使干制“储良”龙眼的吸附能力和平衡含水率下降,李辉等[8]在研究干制“乌叶”荔枝果肉吸附等温线时也发现相似的结果,即在较低和中等水分活度时,平衡含水率增加缓慢,在高水分活度时增加较快。
2.2 模型预测值与实验值比较
采用表2中6种常用的农产品吸附模型对20、30和40 ℃条件下干制“储良”龙眼的吸附等温线数据进行拟合分析,结果如表3所示。
表3 干制“储良”龙眼吸附等温线的拟合结果
Table 3 Fitting results of sorption isotherms of dried “Chuliang”longan
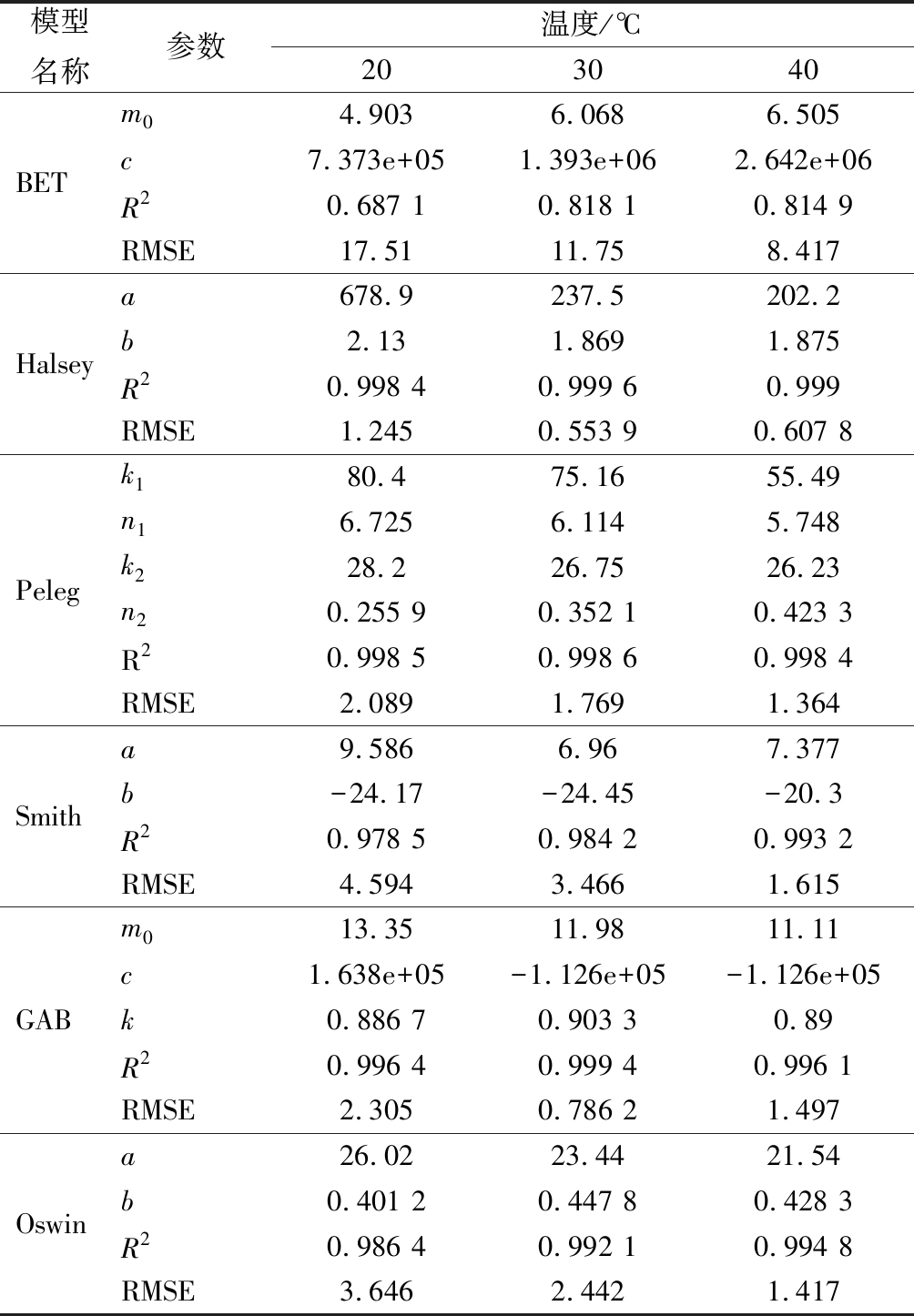
模型名称参数温度/℃203040BETm04.9036.0686.505c7.373e+051.393e+062.642e+06R20.687 10.818 10.814 9RMSE17.5111.758.417Halseya678.9237.5 202.2b2.131.8691.875R20.998 40.999 60.999 RMSE1.2450.553 90.607 8Pelegk180.475.1655.49n16.7256.1145.748k228.226.7526.23n20.255 90.352 10.423 3R20.998 50.998 60.998 4RMSE2.0891.7691.364Smitha9.5866.967.377b-24.17-24.45-20.3R20.978 50.984 20.993 2RMSE4.5943.4661.615GABm013.3511.9811.11c1.638e+05-1.126e+05-1.126e+05k0.886 7 0.903 30.89R20.996 40.999 40.996 1RMSE2.3050.786 21.497Oswina26.0223.4421.54b0.401 20.447 80.428 3R20.986 40.992 10.994 8RMSE3.6462.4421.417
由表3拟合结果可知,Halsey模型拟合综合效果最好,决定系数R2为0.998 4~0.999 6,RMSE为0.553 9~1.245 0,而GAB模型和Peleg模型拟合效果次之,BET模型拟合效果最差。由此确定Halsey模型是描述干制“储良”龙眼吸附等温线的最适模型。将Halsey模型中的参数a和b表示为温度的多项式函数AT2+BT+C,并进行非线性回归,得到a=2.031T2-145.7T+2780(R2=1),b=0.001 335T2-0.092 85T+3.453(R2=1),将a和b代入Halsey模型,得到干制“储良”龙眼在温度20~40 ℃吸附等温线方程如公式(8)所示:
Me=
(8)
为验证模型的准确性和可靠性,将干制“储良”龙眼吸附平衡含水率试验值与Halsey模型预测值进行比较,如图2所示。
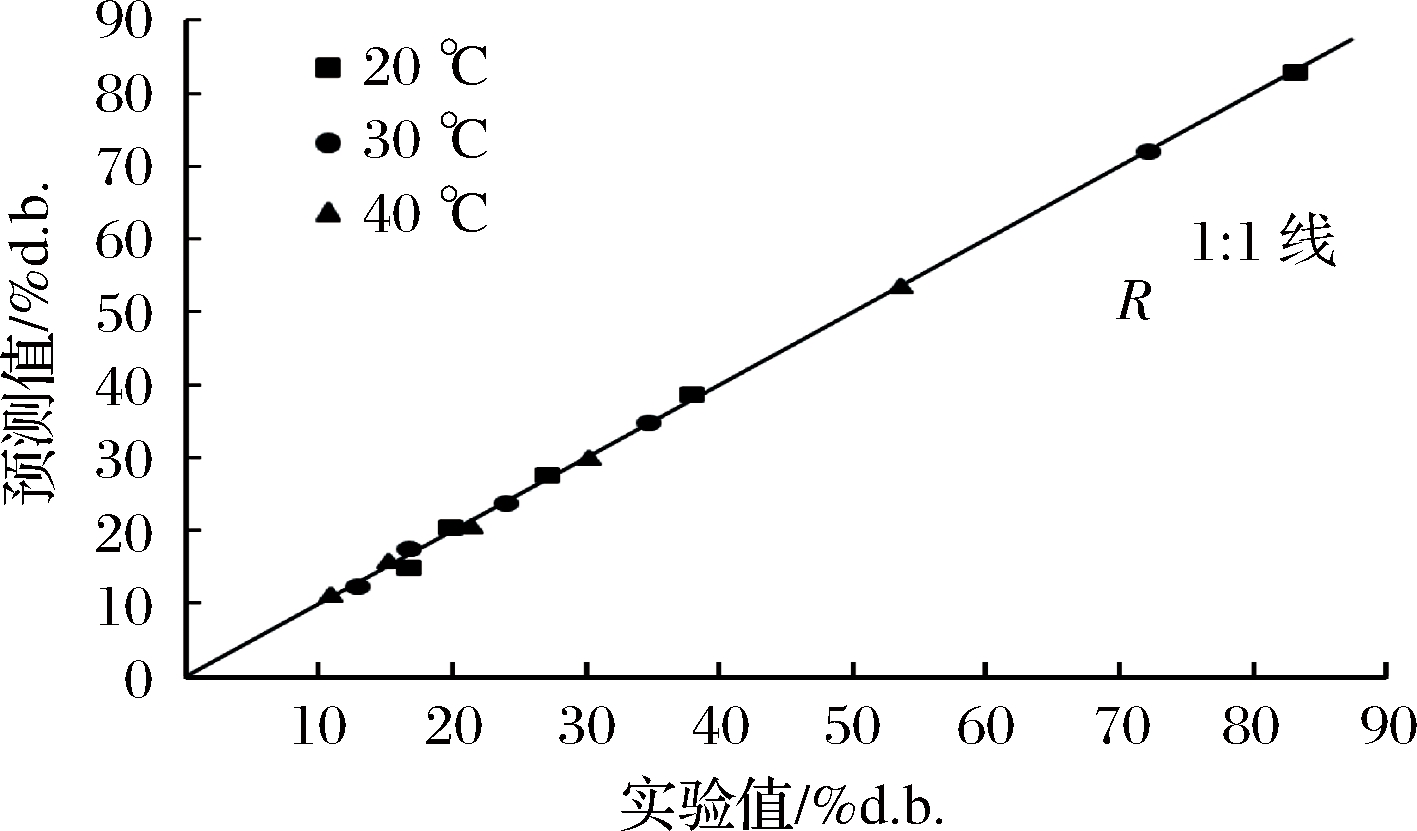
图2 试验值和模型预测值比较
Fig.2 Comparison between experimental and calculated equilibrium moisture content values
图2中实验值与模型预测值的数据点,基本都分布在1∶1线及其附近,这也表明Halsey模型的拟合效果较好(R2=0.998 7),在温度和水分活度分别为20~40 ℃和0.113~0.946范围内能准确地预测干制“储良”龙眼的吸附平衡含水率。
2.3 安全贮藏含水率
水分是微生物生命活动的必要条件之一,微生物在食品中的生长繁殖所需水取决于水分活度。而前人研究也表明,当水分活度低于0.70时,霉菌、酵母和细菌生长会受到强烈抑制;当水分活度低于0.65时,微生物的繁殖完全被抑制;而当水分活度低于0.60时,大部分微生物都将不能生存[7, 9, 30]。因此,当水分活度为0.60时,干制“储良”龙眼所对应的含水率为绝对安全含水率,而当水分活度为0.70时,则为相对安全含水率。于是,由上述所得的干制“储良”龙眼吸附等温线模型,通过计算可得到干制“储良”龙眼在室温25 ℃条件下的绝对安全含水率和相对安全含水率分别为29.89%d.b.和35.88%d.b.。
2.4 吸附热力学特性
根据Halsey模型可得到在温度为20~40 ℃和水分活度为0.113~0.946干制“储良”龙眼的吸附平衡含水率值,而由公式(2)可得到在任何给定的含水率时的净等量吸附热qst,绘制净等量吸附热qst与平衡含水率之间的关系曲线如图3所示。
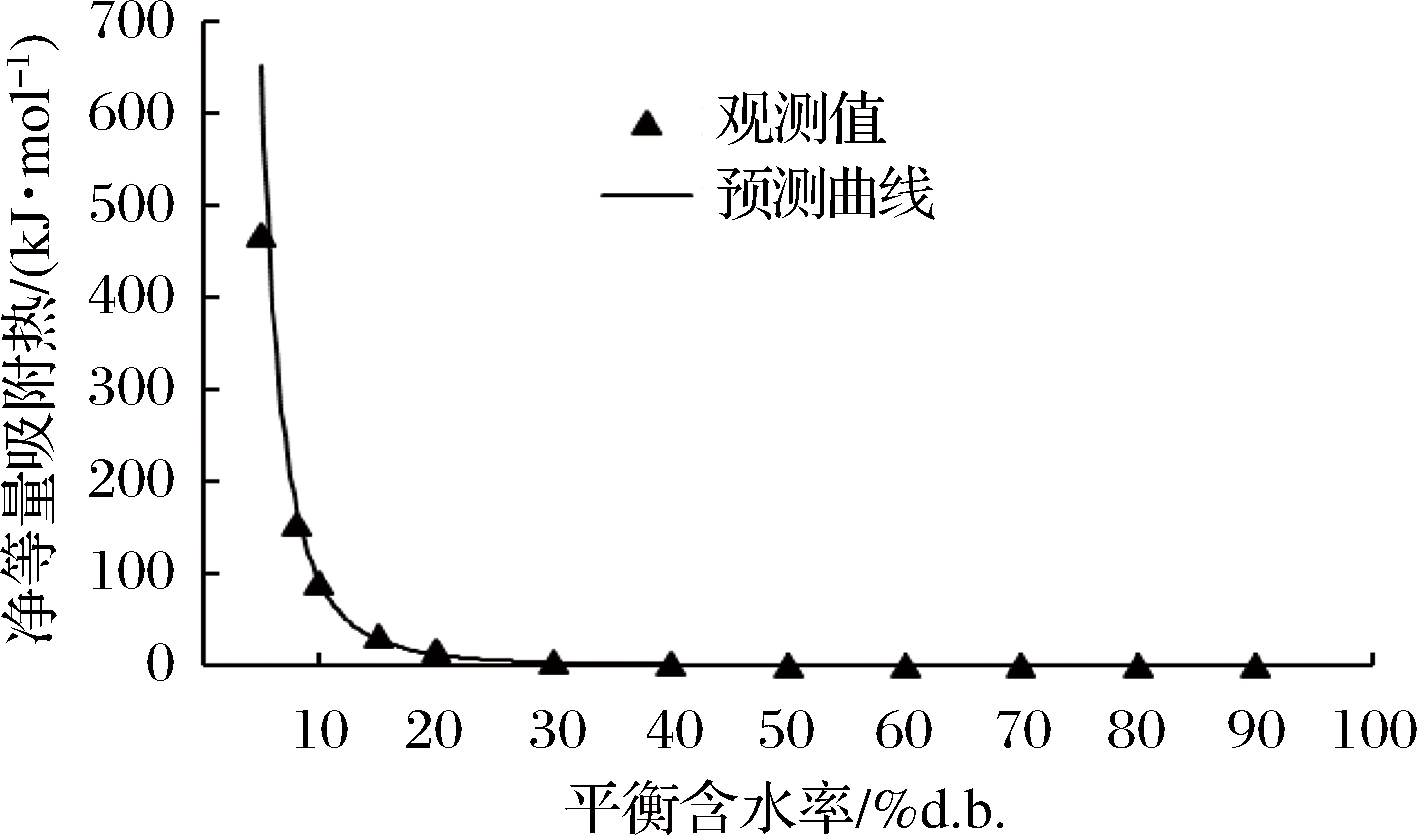
图3 干制“储良”龙眼净等量吸附热与平衡含水率的变化关系
Fig.3 Relationship of net isosteric heat with the equilibrium moisture content of dried "Chuliang" longan
由图3可知,净等量吸附热qst随平衡含水率的升高而降低,当平衡含水率Me大于30%d.b.时,qst趋近于0;而当Me小于10%d.b.时,qst迅速增大,表明干制“储良”龙眼中水与吸附表面的相互作用较强;这也表明,在低含水率范围,水分子主要被吸附在固体外表面的最强的结合位点,而随着含水率的升高,水分子与固体物料的结合位点逐渐减小,从而导致干制“储良”龙眼净等量吸附热下降[31]。
将净等量吸附热与平衡含水率之间的关系曲线进行非线性回归,如公式(9)所示:
(9)
由公式(9)表明,两者服从幂律关系;而从图3中也观察到,净等量吸附热曲线拟合效果较好,决定系数R2达到0.990 9,在干制“储良”龙眼贮藏过程中,用净等量吸附热方程来计算水分活度是非常有必要的。
由表4干制“储良”龙眼吸附热力学特性参数(ΔH、ΔS和ΔG)可知,焓变ΔH与净等量吸附热qst相等,其范围在0.2~467.69 kJ/mol;而熵变ΔS可由公式(3)和公式(4)计算求得,范围在0.15~1 421.11 J/(mol·K)。熵变ΔS随含水率的升高而减小,温度对其影响不显著,于是可由公式(5)直接求得熵变ΔS。而自由能ΔG同时受温度和含水率的影响,其值为0.14~53.76 kJ/mol。自由能ΔG表征水分吸附过程的自发性,自由能ΔG越高,物料的亲水性越好,吸附自发性也较高[7, 32]。
2.5 焓-熵补偿
由图4可知,通过对焓变ΔH和熵变ΔS进行线性回归得到Tβ和ΔGβ分别为329.16和0.7945(R2=1);而由公式(7)求出Thm为302.93 K。其中Tβ与Thm不同,这表明在本研究的含水率范围内,焓-熵互补理论适用于干制“储良”龙眼的吸附特性研究;同时,由于Tβ>Thm,由此可以推断出干制“储良”龙眼的水分吸附过程是焓驱动的。
表4 干制“储良”龙眼热力学特性参数
Table 4 Thermodynamic parameters of dried “Chuliang” longan
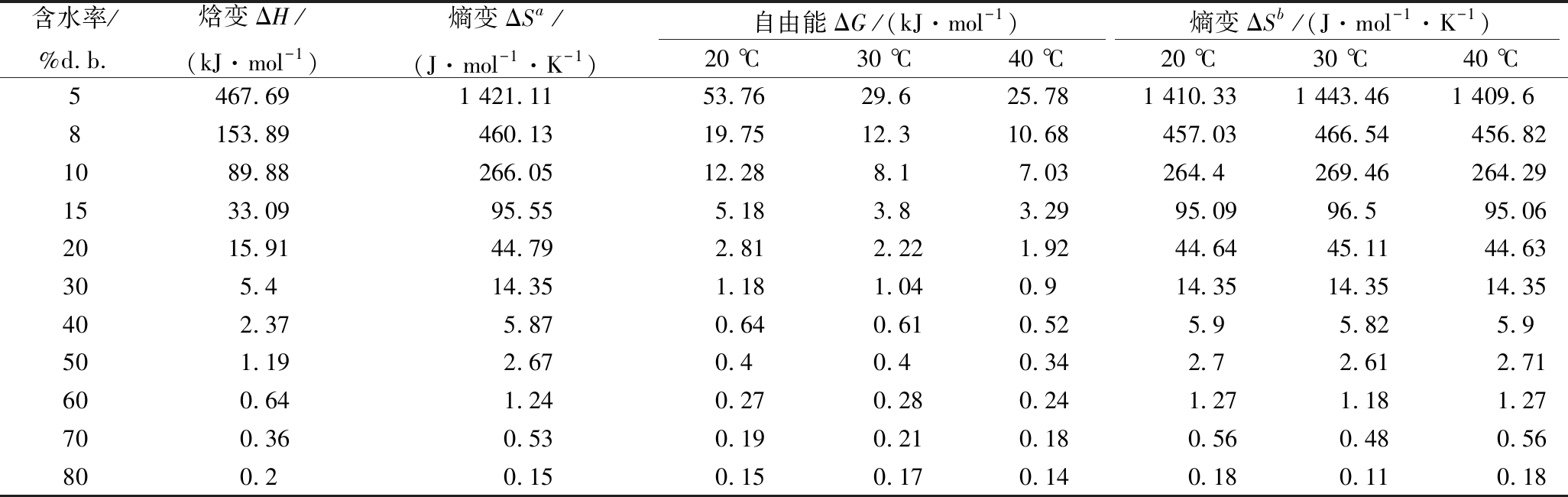
含水率/%d.b.焓变ΔH/(kJ·mol-1)熵变ΔSa/(J·mol-1·K-1)自由能ΔG/(kJ·mol-1)熵变ΔSb/(J·mol-1·K-1)20 ℃30 ℃40 ℃20 ℃30 ℃40 ℃5467.691 421.1153.7629.625.781 410.331 443.461 409.68153.89460.1319.7512.310.68457.03466.54456.821089.88266.0512.288.17.03264.4269.46264.291533.0995.555.183.83.2995.0996.595.062015.9144.792.812.221.9244.6445.1144.63305.414.351.181.040.914.3514.3514.35402.375.870.640.610.525.95.825.9501.192.670.40.40.342.72.612.71600.641.240.270.280.241.271.181.27700.360.530.190.210.180.560.480.56800.20.150.150.170.140.180.110.18
注:a,由式(5)算出的熵变ΔS;b,由式(3)算出的熵变ΔS。
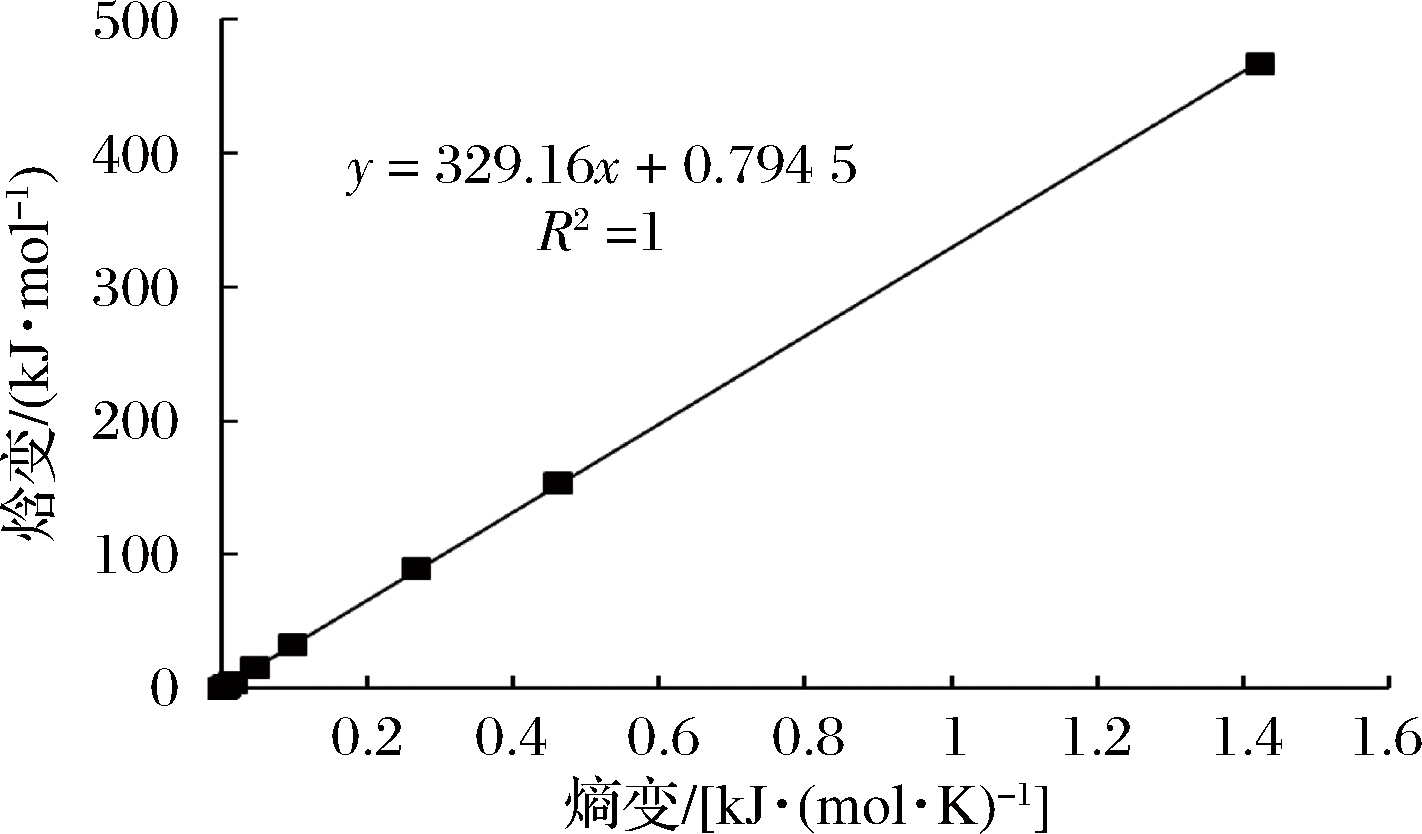
图4 焓变ΔH与熵变ΔS的关系
Fig.4 Relationship of enthalpy changes ΔH and entropy changes ΔS
3 结论
1)干制“储良”龙眼的水分吸附特性曲线呈Ⅲ型等温线,在水分活度相同的情况下,平衡含水率随温度的升高而减小。Halsey模型是描述龙眼在20~40 ℃范围内的吸附等温线的最适模型,其决定系数R2和均方根误差RMSE分别为0.998 4~0.999 6和0.553 9~1.245 0。根据上述模型得到“储良”龙眼在室温25 ℃条件下的相对安全含水率与绝对安全含水率分别为35.88%d.b.与29.89%d.b.。
2)干制“储良”龙眼的净等量吸附热随含水率的升高而降低,当平衡含水率Me大于30%d.b.时,其值趋近于0;而净等量吸附热与焓变相等,其值为0.2~467.69 kJ/mol;熵变随含水率的升高而减小,但温度对其影响不显著;自由能随含水率和温度的升高而降低。
3)干制“储良”龙眼水分吸附过程可用焓-熵补偿理论解释,且该过程是焓驱动的。研究结果为干制“储良”龙眼的加工、包装和贮藏稳定性研究提供参考依据。
[1] 黄美香,林河通,李辉,等. 龙眼果实加工技术研究进展[J]. 包装与食品机械, 2012, 30(2): 48-52.
[2] 林育钊,林毅雄,林河通,等. 龙眼果实品质劣变和贮藏保鲜技术研究进展[J]. 包装与食品机械, 2016, 34(6): 46-50.
[3] MART NEZ-LAS HERAS R, HEREDIA A, CASTELLO M L, et al. Moisture sorption isotherms and isosteric heat of sorption of dry persimmon leaves[J]. Food Bioscience, 2014, 7: 88-94.
NEZ-LAS HERAS R, HEREDIA A, CASTELLO M L, et al. Moisture sorption isotherms and isosteric heat of sorption of dry persimmon leaves[J]. Food Bioscience, 2014, 7: 88-94.
[4] BEJAR A K, MIHOUBI N B, KECHAOU N. Moisture sorption isotherms-Experimental and mathematical investigations of orange (Citrus sinensis) peel and leaves[J]. Food Chemistry, 2012, 132(4): 1 728-1 735.
[5] AGHA M K K, LEE W S, BUCKLIN R A, et al. Sorption isotherms for triticale seed[J]. Transactions of the ASABE, 2014, 57(3): 901-904.
[6] FREITAS M L F, POLACHINI T C, DE SOUZA A C, et al. Sorption isotherms and thermodynamic properties of grated Parmesan cheese[J]. International Journal of Food Science & Technology, 2016, 51(1): 250-259.
[7] 朱文学. 食品干燥原理与技术[M]. 北京: 科学出版社, 2009: 38-69.
[8] 李辉,林河通,林毅雄,等. 干制荔枝果肉吸附等温线及热力学性质[J]. 农业工程学报, 2014, 30(22): 309-315.
[9] 邱光应,彭桂兰,吴绍锋,等. 花椒吸附等温线及热力学性质[J]. 食品科学, 2015, 36(21): 1-5.
[10] TAITANO L Z, SINGH R P, LEE J H, et al. Thermodynamic analysis of moisture adsorption isotherms of raw and blanched almonds[J]. Journal of Food Process Engineering, 2012, 35(6): 840-850.
[11] 杨昭,李想,陶志超. 豌豆种子吸附等温线与热力学性质研究[J]. 农业机械学报, 2017, 48(10): 323-329.
![]() H, ARSLAN N. Moisture sorption isotherms and thermodynamic properties of walnut kernels[J]. Journal of Stored Products Research, 2007, 43(3): 252-264.
H, ARSLAN N. Moisture sorption isotherms and thermodynamic properties of walnut kernels[J]. Journal of Stored Products Research, 2007, 43(3): 252-264.
[13] 张绪坤,王高敏,姚斌,等. 单粒莲子热风干燥特性及其干燥动力学[J]. 现代食品科技, 2017, 33(4): 141-148.
[14] 李兴军,王双林,张元娣,等. 玉米吸湿特性及其等温线类型研究[J]. 中国粮油学报, 2012, 27(1): 80-86.
[15] SAMAPUNDO S, DEVLIEGHERE F, DE MEULENAER B, et al. Sorption isotherms and isosteric heats of sorption of whole yellow dent corn[J]. Journal of Food Engineering, 2007, 79(1): 168-175.
[16] 刘成梅,周国辉,万婕,等. 大米淀粉解吸等温线与吸附等温线的拟合模型研究[J]. 食品工业科技, 2014, 35(10): 198-201.
[17] 王明洁,吴小丽,袁建,等. 小麦粉水分的吸附与解吸特性[J]. 食品科学, 2012, 33(19): 45-51.
[18] 陈羽白,邵耀坚,刘道被,等. 龙眼平衡含水率及其模型的研究[J]. 华南农业大学学报, 1996, 17(4): 107-111.
[19] JANJAI S, INTAWEE P, TOHSING K, et al. Neural network modeling of sorption isotherms of longan (Dimocarpus longan Lour.)[J]. Computers and Electronics in Agriculture, 2009, 66(2): 209-214.
[20] 食品安全国家标准 食品中水分的测定[S]. 北京, 国家卫生和计划生育委员会, 2017.
[21] 赵亚,张平平,石启龙. 花生壳/仁的吸附等温线与热力学特性[J]. 食品科学, 2017, 38(7): 55-62.
[22] DALG Ç A C, PEKMEZ H, BELIBA LI K B. Effect of drying methods on the moisture sorption isotherms and thermodynamic properties of mint leaves[J]. Journal of Food Science and Technology, 2012, 49(4): 439-449.
Ç A C, PEKMEZ H, BELIBA LI K B. Effect of drying methods on the moisture sorption isotherms and thermodynamic properties of mint leaves[J]. Journal of Food Science and Technology, 2012, 49(4): 439-449.
[23] OSWIN C R. The kinetics of package life. III. The isotherm[J]. Journal of the Society of Chemical Industry, 1946, 65(12): 419-421.
[24] HALSEY G. Physical adsorption on non-uniform surfaces[J]. The Journal of Chemical Physics, 1948, 16(10): 931-937.
[25] XING C, LIU X, JIN Q, et al. Moisture sorption thermodynamics of camellia oleifera[J]. Food Biophysics, 2012, 7(2): 163-172.
[26] MCMINN W, AL-MUHTASEB A H, MAGEE T. Enthalpy-entropy compensation in sorption phenomena of starch materials[J]. Food Research International, 2005, 38(5): 505-510.
[27] BERISTAIN C I, GARCIA H S, AZUARA E. Enthalpy-entropy compensation in food vapor adsorption[J]. Journal of Food Engineering, 1996, 30(3-4): 405-415.
[28] KRUG R R, HUNTER W G, GRIEGER R A. Enthalpy-entropy compensation. 1. Some fundamental statistical problems associated with the analysis of van't Hoff and Arrhenius data[J]. The Journal of Physical Chemistry, 1976, 80(21): 2 335-2 341.
[29] SING W K S, EVERETT H D, HAUL W R A, et al. Reporting physisorption data for gas solid systems with special references to the determination of surface-area and porosity[J]. Pure Appl Chem, 1985, 57(4): 603-619.
[30] 张志健. 食品防腐保鲜技术[M]. 北京: 科学技术文献出版社, 2006: 40-41.
[31] TAITANO L Z, SINGH R P, LEE J H, et al. Thermodynamic analysis of moisture adsorption isotherms of raw and blanched almonds[J]. Journal of Food Process Engineering, 2012, 35(6): 840-850.
[32] 金兹布尔格 A. C. 食品干燥原理与技术基础[M]. 北京: 轻工业出版社, 1986.