橙汁是全球贸易量最大的柑桔果汁[1]。近年来,我国橙汁加工总量有明显增长[2],这得益于一种不同于传统加工方式的新型橙汁,即非浓缩还原(not from concentrate,NFC)橙汁的迅速发展。NFC橙汁是将成熟鲜果榨汁过滤得果汁,经巴氏杀菌后直接进行无菌灌装,在冷链条件下贮运销售,极大限度地保留了橙汁的营养和风味[3],深受广大消费者喜爱。NFC橙汁保留了原果中丰富的功能性成分,对促进人体健康具有重要意义。橙汁中的Vc、酚类化合物及类胡萝卜素等物质具有抗氧化[4-8]、抑菌[8-9]、抗肿瘤[10]等生理作用;其中,类胡萝卜素还是动物体内重要VA原[11-12]。但研究发现,在加工和贮藏过程中,橙汁中Vc、酚类化合物以及类胡萝卜素等营养物质会在环境因素的作用下氧化降解,导致橙汁品质降低,而O2则是使营养物质发生氧化降解的主要因素[13]。空气中的氧气浓度较高,可通过扩散作用溶解在果汁中,形成溶解氧(dissolved oxygen,DO)[14]。橙汁中的DO通常以分子或双自由基的三线态氧形式存在,三线态氧是能量较低的基态氧,但当光线和光催化剂存在时,三线态氧受到激发会转变为单线态氧[15-16],处于激发态的单线态氧极易与食品基质发生氧化反应。有研究发现,橙汁中DO浓度直接决定着Vc等营养物质的氧化降解速率[17],导致橙汁营养品质下降。因此,减少橙汁中的DO含量是提高NFC橙汁品质的有效途径之一。
关于O2含量对果汁品质影响的研究,前期主要集中在贮藏过程[18-19],近年来有学者开始转向加工过程,如苹果汁的加工过程[20];但关于橙汁的加工过程,特别是脱气工艺中O2含量的控制对橙汁品质的影响研究较少。鲜榨橙汁在过滤及管道流动过程中长时间曝气,管道空气中的O2不断地溶解到橙汁中,在精滤工序结束后,橙汁中的DO含量几近饱和。大量DO的存在很可能会在后续的加工和贮藏过程中造成橙汁营养流失和品质下降,因此,橙汁加工中的脱气环节尤为重要。本文以加工过程中的橙汁为实验对象,研究不同脱气温度下DO含量对橙汁品质的影响,以期为优化NFC橙汁加工工艺、提高橙汁品质提供理论参考。
1 材料与方法
1.1 原料与试剂
1.1.1 原料
北碚447锦橙,购买于重庆市北碚区歇马镇农户果园。
1.1.2 试剂
NaOH、酚酞、邻苯二甲酸氢钾、草酸、L-抗坏血酸、NaHCO3、2,6-二氯靛酚溶液、Folin-Ciocalteu试剂、Na2CO3、柠檬酸、一缩二乙醇、乙酸乙酯、甲基叔丁基醚(均为分析纯);甲醇、冰乙酸(色谱纯);橙皮苷、没食子酸、绿原酸、对羟基苯甲酸、咖啡酸、对香豆酸、阿魏酸、芸香柚皮苷、芦丁、香蜂草苷、橘皮素(标准品,纯度≥98%);重庆川东化工有限公司。
1.2 仪器与设备
S9溶氧仪,梅特勒托利多(上海)有限公司;KENWOOD榨汁机,德龙比荷卢股份公司;Color i5色差仪,瑞士Gretag Macbech公司;TU-1901紫外分光光度计,普析通用仪器有限责任公司;Ultimate 3000高效液相色谱,戴安(中国)有限公司;WAY-2S阿贝折光仪,上海精密科学仪器有限公司。
1.3 方法
1.3.1 橙汁样品处理
随机取出适量新鲜的锦橙果实,清水冲洗干净,自然晾干,用刀将果实切分成均匀的两部分,使用手动榨汁机进行压榨,双层纱布过滤制得鲜榨橙汁。实验组:模拟工厂脱气温度,用500 mL锥形瓶分别取400 mL鲜榨橙汁置于水浴锅中,将果汁温度分别保持在10、20和30℃。利用数显真空泵、水浴磁力搅拌器和密闭三口烧瓶组装成简易脱气装置,三口烧瓶分别接上溶氧仪探头、脱气阀和氮气阀。将鲜榨橙汁置于三口烧瓶内,瓶内真空度控制在10 kPa,通过控制脱气时间和溶氧仪实时测量,设定橙汁中的DO质量浓度,脱气结束后向烧瓶顶空充入适量高纯N2,不同温度下DO质量浓度设定如表1。将设置好DO含量的橙汁样品置于灭菌锅中,采用巴氏杀菌,于95℃下保持30 s杀菌。随后立即取出,于冷水浴中冷却至室温待测。空白对照组:取400 mL鲜榨橙汁于500 mL锥形瓶中,置于4℃冰箱中备用。
表1 脱气温度及DO含量设定表
Table 1 Degassing temperature and DO content setting

温度/℃溶解氧质量浓度设定/(mg·L-1)100.301.503.004.506.008.0011.00∗200.301.503.004.506.007.509.00∗300.301.503.004.506.007.50∗-
注:*表示橙汁样品在此温度条件下溶解氧接近饱和;“-”表示无法检出。
1.3.2 测定指标
1.3.2.1 可溶性固形物(TSS)的测定
采用阿贝折光仪测定,打开盖板用擦镜纸擦净棱镜,滴1~2滴蒸馏水于棱镜表面,合上盖板进行校正,校正结束后测定样品,结果以%表示。
1.3.2.2 色泽的测定
Color i5色差仪开机后选择光源C-02,设定测试参数L*、a*、b* 值,用黑白板进行校正,校正结束后每个样品平行测定5次,并计算ΔE值和BI值。ΔE和BI的计算公式(1)、(2)和(3)如下:
(1)
式中:ΔE,样品与空白对照间的色差;L*,亮度;a*,红绿值;b*,黄蓝值;L0、a0、b0,空白对照样品的测定值。
式中:BI,褐变指数;L*,亮度;a*,红绿值;b*,黄蓝值。
(2)
(3)
式中:BI,褐变指数。
1.3.2.3 抗坏血酸(Vc)的测定
根据国标第三法——2,6-二氯靛酚法[21]进行测定,结果以每100 g橙汁所含L-抗坏血酸毫克数表示(mg/100 g)。
1.3.2.4 总酚含量的测定
参照Folin-Ciocalteu法[22]加以修改进行测定。总酚标准曲线绘制:以没食子酸作为标准品,制得不同浓度的标准溶液并测定吸光值,得回归方程:Y=11.754X-0.105,方程中Y为质量浓度,X为吸光度,R2=0.996 8。
1.3.2.5 总黄酮含量的测定
根据行业标准NY/T 2010—2011[23]的方法进行测定。以橙皮苷为标准品,根据行业标准中的方法制作标准曲线,所得回归方程:Y=176.13X+0.039,方程中Y为质量浓度,X为吸光度,R2=0.998 9。
1.3.2.6 类黄酮特征单体(芦丁、橙皮苷和香蜂草苷)的测定
称取2份平行试样6 g于50 mL离心管中,加入8 mL乙酸乙酯,涡旋混匀5 min,于8 000 r/min条件下离心10 min,收集上清液,重复上述操作1次,合并上清液,氮吹浓缩至干, 50%甲醇溶液定容至2 mL,经0.22 μm微孔有机滤膜过滤后上机检测。将芦丁、橙皮苷和香蜂草苷标品配制成不同浓度梯度的混合溶液上机检测,制得3种类黄酮单体的标准曲线回归方程,见表2。
检测条件:色谱柱:AcclaimTM120 C18分析柱(4.6 mm×250 mm,5 μm);流动相:1%冰乙酸(A)和甲醇(B);梯度洗脱程序:0 min,75% A,25% B;30 min,55% A,45% B;50 min,0% A,100% B;60 min,75% A,25% B;75 min,75% A,25 %B;流速:1 mL/min;柱温:30 ℃;检测波长:283 nm。
1.3.2.7 酚酸特征单体(阿魏酸、对香豆酸和咖啡酸)的测定
称取2份平行试样6 g于50 mL离心管中,加入5 mL 8 mol/L的NaOH溶液,涡旋混匀反应1 h;8 mol/L的HCl调节pH至2.0,加入8 mL乙酸乙酯和甲基叔丁基醚(体积比1∶1)混合液,于10 000 r/min条件下离心10 min,收集上清液,重复上述操作1次,合并上清液,氮吹浓缩至干,50%甲醇溶液定容至2 mL,经0.22 μm微孔有机滤膜过滤后上机检测。将阿魏酸、对香豆酸和咖啡酸标品配制成不同浓度梯度的混合溶液上机检测,制得3种酚酸单体的标准曲线回归方程,见表2。
检测条件:色谱柱:AcclaimTM120 C18分析柱(4.6 mm×250 mm,5 μm);流动相:1%冰乙酸(A)和甲醇(B);梯度洗脱程序:0 min 80% A,20% B;22 min,70% A,30% B;52 min,0% A,100% B;60 min,80% A,20% B;66 min,80% A,20% B;流速:1 mL/min;柱温:30 ℃;检测波长:260 nm和320 nm。
表2 酚酸及类黄酮特征单体的标准曲线回归方程
Table 2 Standard curve regression equation for the characteristic monomer of phenolic acids and flavonoids

名称回归方程相关系数R2芦丁 y=3.202 6x+0.264 50.999 4黄酮橙皮苷 y=1.625 5x-0.212 80.999 4香蜂草苷y=1.818 7x-0.102 50.999 8咖啡酸 y=2.229 8x-0.025 20.999 9酚酸对香豆酸y=2.590 6x+0.441 10.999 5阿魏酸 y=2.807x+0.497 70.999 5
1.4 数据处理
本实验所有样品平行测定3次,测试结果以“平均值±标准差”表示。使用Origin 8.5进行相关图表的绘制,利用SPSS 11.5统计软件对数据进行两因素交互方差分析,采用Duncan法比较平均值之间的差异性,P <0.01表示差异极显著,P < 0.05表示差异显著,P > 0.05表示无显著性差异。
2 结果与分析
2.1 不同温度下DO对TSS含量的影响
可溶性固形物(TSS)的含量对橙汁的风味品质具有重要影响,图1是不同温度下DO质量浓度对TSS的影响情况。从图1可知,在3种不同的温度条件下,随着DO质量浓度的增加,TSS的含量呈小幅下降。温度和DO存在交互作用,通过两因素交互方差分析发现,这种交互作用对TSS含量具有显著性影响(P<0.05)。可能原因是TSS主要是指可溶性糖类,羟自由基可与糖类以109 mol/(L·s)的速率反应[24];羟自由基从葡萄糖中提取氢并形成葡萄糖基,再与三线态氧反应形成糖的过氧基,随后糖的过氧基被分解并产生低分子质量羰基化合物和超氧阴离子[25],从而使TSS含量降低。
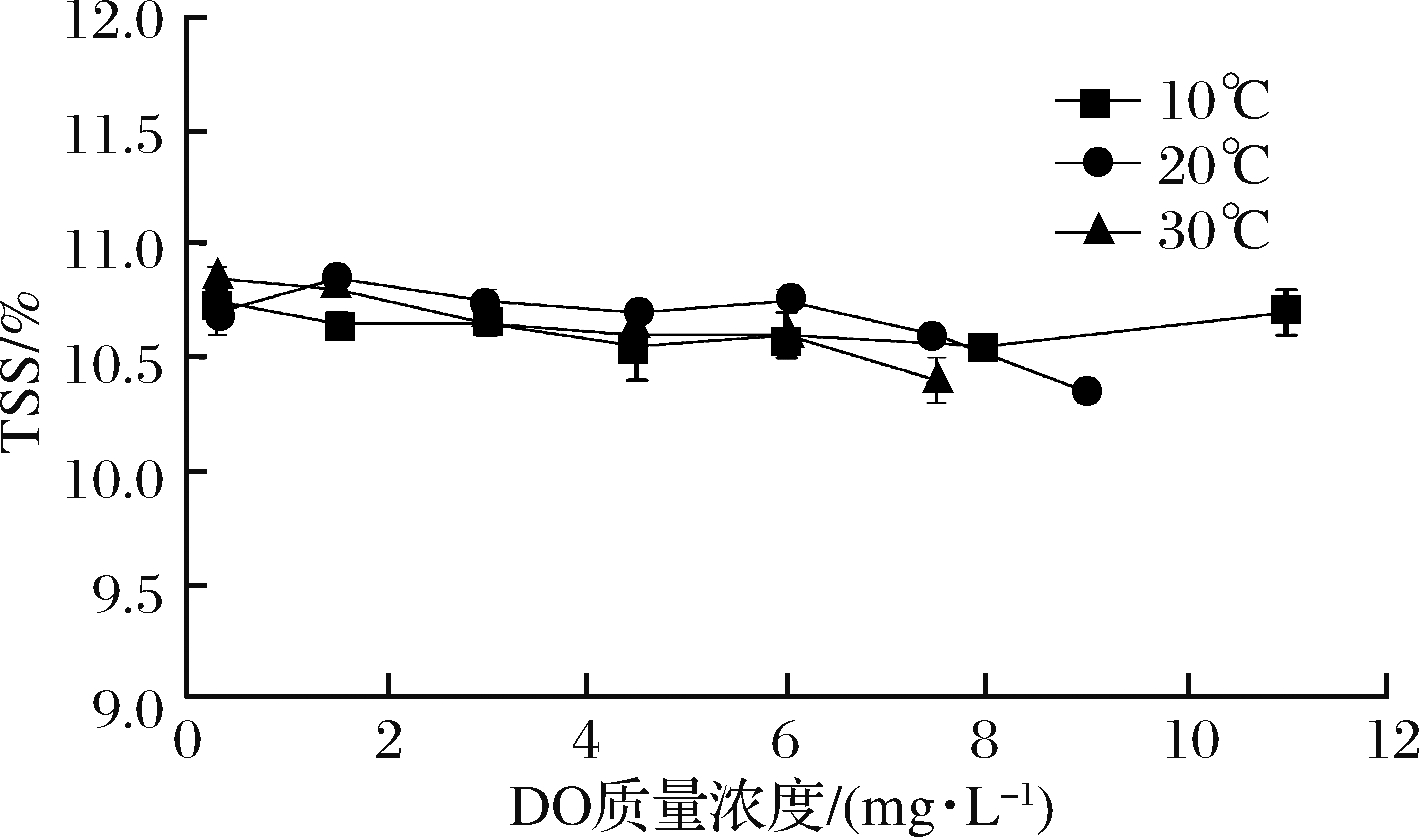
图1 不同温度下DO对TSS含量的影响
Fig.1 Effect of DO on TSS content at different temperatures
2.2 不同温度下DO对NFC橙汁色泽的影响
色泽是评价橙汁感官品质的重要指标之一,良好的橙汁色泽有助于激发消费者的购买欲。由表3可知,在3种不同温度条件下,除a*值外,其他指标均呈下降趋势,30℃加工条件下变化尤其明显;通过两因素交互方差分析发现,二者的交互作用对NFC橙汁各色泽指标影响差异极显著(P < 0.01)。在3种不同温度下,亮度L*均随DO质量浓度的升高而降低,即橙汁的亮度逐渐降低,说明褐变逐渐加重。表中a*值随样品中DO质量浓度的变化均为正值,说明橙汁样品都偏红色。b*值随DO质量浓度的升高呈显著下降趋势,指标b*主要受橙汁中类胡萝卜素的影响;温度和DO质量浓度越高,类胡萝卜素的异构化和氧化反应导致黄度降低,从而使得b*逐渐减小[26]。ΔE表示经处理的橙汁样品与空白对照之间的色差,随着DO质量浓度增加,ΔE逐渐增大,且在30℃条件下,当DO质量浓度≥6 mg/L时,橙汁样品与空白对照之间存在极显著差异(P < 0.01)。褐变指数(BI)越大,表示褐变越严重,而表中BI随DO质量浓度增加而显著下降,可能是由于BI值取决于L*、a*和b*值,橙汁中b*值主要受黄色色素影响,黄色色素氧化降解则b*值下降,BI值也随之下降。
表3 不同温度下DO对色泽的影响
Table 3 Effect of DO on color at different temperatures

温度/℃DO含量/(mg·L-1)L∗a∗b∗ΔEBI0.3051.79±0.011.41±0.0134.68±0.011.59±0.02102.44±0.091.5051.27±0.022.04±0.0134.36±0.011.89±0.01103.59±0.053.0051.68±0.011.93±0.0234.08±0.022.20±0.04100.91±0.07104.5051.71±0.062.09±0.0133.95±0.012.39±0.04100.48±0.146.0050.53±0.131.96±0.0333.89±0.012.25±0.03103.09±0.388.0050.25±0.011.33±0.0233.40±0.012.60±0.01101.25±0.0311.0049.77±0.040.98±0.0232.74±0.023.35±0.1199.10±0.240.3051.33±0.011.42±0.0134.67±0.021.39±0.02103.82±0.041.5051.25±0.021.40±0.0134.66±0.021.38±0.03104.01±0.073.0051.73±0.041.35±0.0234.80±0.041.45±0.02103.07±0.08204.5052.43±0.021.11±0.0233.61±0.012.33±0.0598.28±0.046.0050.71±0.011.22±0.0233.59±0.022.37±0.05100.51±0.097.5050.51±0.031.48±0.0333.03±0.022.95±0.1799.24±0.169.0050.42±0.011.77±0.0132.59±0.023.42±0.6897.48±0.030.3052.08±0.021.58±0.0435.66±0.031.36±0.01106.27±0.131.5051.69±0.041.45±0.0135.05±0.021.27±0.07104.48±0.233.0050.61±0.041.10±0.0333.34±0.052.59±0.0499.47±0.42304.5051.19±0.011.31±0.0233.87±0.082.09±0.08100.46±0.416.0049.95±0.020.60±0.0131.77±0.024.26±0.0193.59±0.147.5047.94±0.040.36±0.0128.10±0.028.37±0.0282.66±0.18
2.3 不同温度下DO对Vc含量的影响
Vc是橙汁中重要的营养成分之一,具有预防坏血病、抗肿瘤、抗氧化等生理功能[27],还具有保护橙汁中多酚等营养物质的作用[28];但其化学性质不稳定,对光、热和O2极其敏感。在有O2存在时,Vc进行有氧降解形成脱氢抗坏血酸,经一系列反应后最终生成还原酮,还原酮再参与美拉德反应生成黑褐色物质[18]。图2是不同温度下橙汁中DO质量浓度对Vc的影响趋势,由图可知,随着DO质量浓度的增加,3种温度条件下的Vc含量均显著下降,说明Vc受橙汁中的DO影响严重。
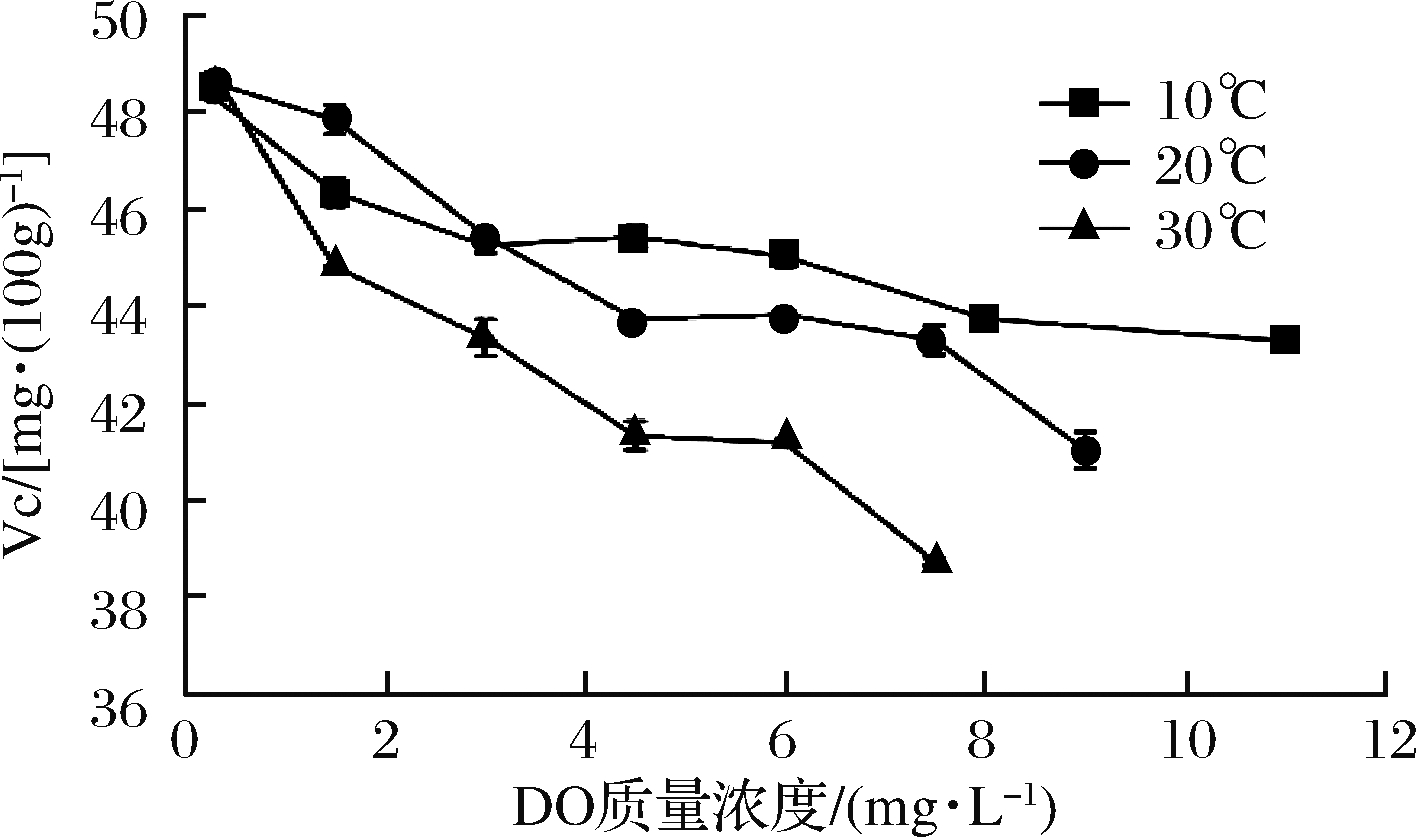
图2 不同温度下DO对Vc含量的影响
Fig.2 Effect of DO on Vc content at differenttemperatures
在10 ℃条件下,Vc含量减少约10%,20 ℃时Vc含量约减少16%,30 ℃时氧化反应相当迅速且Vc减少量达21%,这表明温度越高,对Vc的损害越大。通过两因素交互方差分析发现,温度和DO质量浓度的交互作用对Vc含量的影响差异极显著(P<0.01),即温度和DO质量浓度越高,Vc的降解量越大。这一结果与姚刚[20]对苹果清汁加工中Vc的变化研究结论一致。
2.4 不同温度下DO对总酚含量的影响
图3显示的是DO对总酚含量的影响情况,由图3可知,在3种不同温度条件下,随DO质量浓度的增加整体呈逐渐下降的趋势,总酚含量减少。这可能是由于橙汁中的多酚氧化酶在杀菌完成前未被灭活,易发生酶促氧化反应,即橙汁中的酚类化合物与DO在多酚氧化酶的催化下,迅速氧化生成醌类物质,醌类物质迅速聚合形成深褐色聚合物[29];DO质量浓度越高,反应越迅速,总酚减少量越大。10℃和20℃,总酚含量降幅较小,30℃总酚含量降幅较大,约为8%,其原因可能是多酚氧化酶的最适作用温度是30℃,在此温度条件下氧化速率加快,导致总酚含量减少量增多。通过方差分析可知,温度和DO的交互作用对总酚含量的影响差异极显著(P<0.01),即在一定范围内,随着温度升高和DO质量浓度的增加,总酚减少量越大,这与对Vc含量的影响具有一致性。

图3 不同温度下DO对总酚含量的影响
Fig.3 Effect of DO on total phenolic contentat different temperatures
2.5 不同温度下DO对总黄酮含量的影响
总黄酮是一类含有2个酚羟基的酚类化合物,其氧化反应与总酚相似,在多酚氧化酶被灭活前,主要发生酶促氧化反应。图4表示不同温度下DO对总黄酮的影响情况。
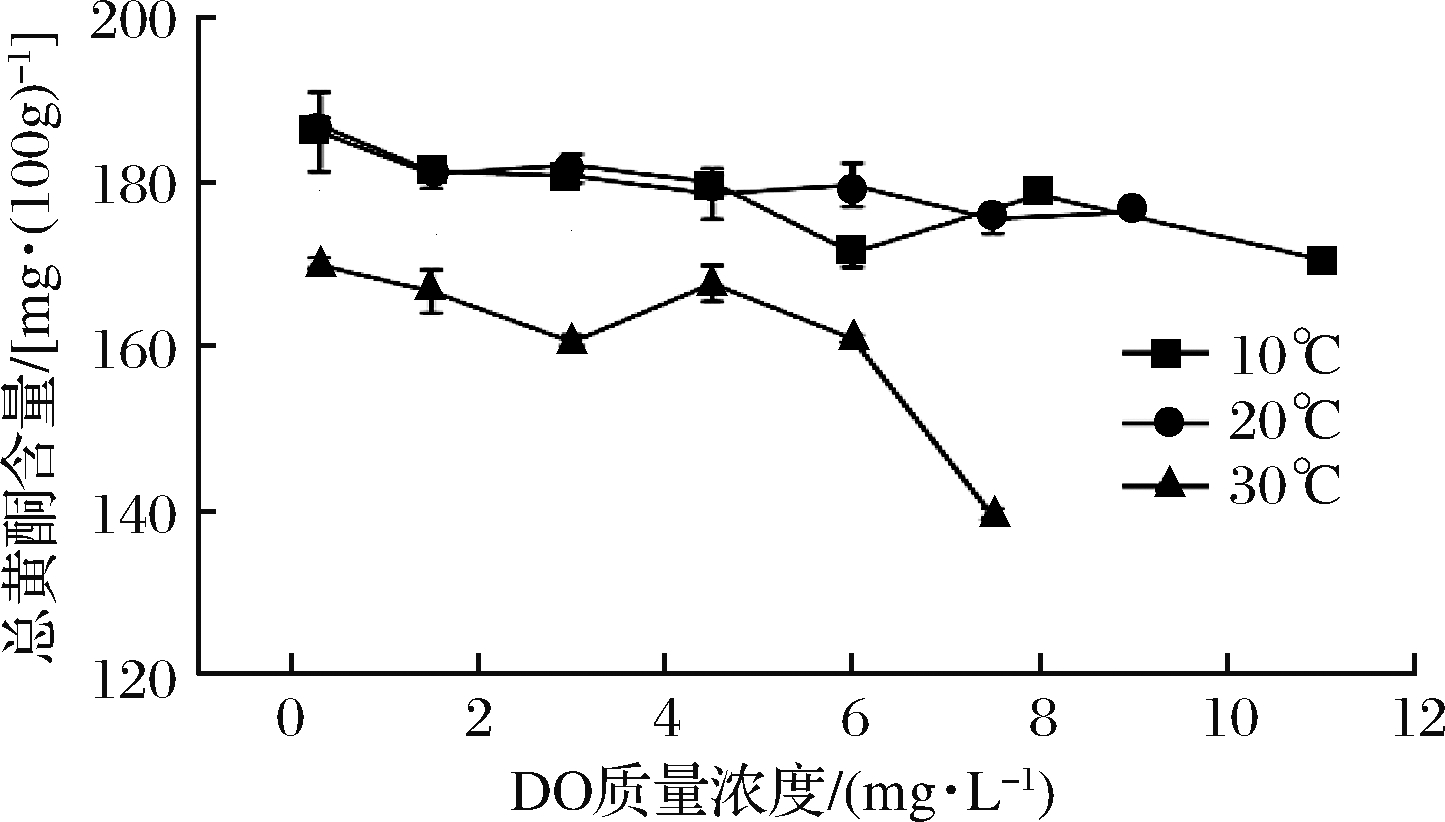
图4 不同温度下DO对总黄酮含量的影响
Fig.4 Effect of DO on total flavonoids contentat different temperatures
由图4可以看出,总黄酮的量随DO质量浓度的增加而呈下降趋势,但总体变化幅度不明显;通过方差分析发现,虽然温度和DO质量浓度的交互作用不显著,但温度对总黄酮含量的影响极显著(P<0.01);在10℃和20℃时,总黄酮含量的减少幅度较小,但在30℃时,总黄酮含量减少了12%。该结果与刘汉珍等[30]研究贮藏条件对滁菊中总黄酮含量的影响结果一致,即温度越高,总黄酮的含量越低。
2.6 不同温度下DO对三种类黄酮单体含量的影响
橙皮苷、芦丁和香蜂草苷是橙汁中含量较为丰富的3种类黄酮单体,它们具有广泛的生物活性,包括抑制微生物、抗氧化、抗癌和抗炎等[31]。本实验利用HPLC测定了橙汁样品中3种黄酮单体的含量,如图5所示。随着DO质量浓度和温度的变化,图5-a中的橙皮苷含量无明显变化趋势;经分析,DO质量浓度和温度对橙皮苷的含量均无显著性影响。经查阅文献[32],酚羟基的甲基化或糖基化会都降低柑橘酚类物质的自由基清除能力,而酚羟基数目越多,氧化反应越强烈,抗氧化活性越强。从橙皮苷的结构分析发现,其酚羟基数目仅为2,所以氧化反应活性较弱,含量无明显变化。由图5-b中可以发现,随着DO质量浓度和温度的增加,芦丁含量降幅明显,最大减少量达41%;通过分析发现,DO质量浓度和温度的交互作用对芦丁含量影响无显著性差异,但DO含量对芦丁质量浓度影响差异极显著(P<0.01)。可能原因是虽然芦丁的C3位具有糖基,但黄酮类化合物C环上的C3位的羟基似乎氧化活性不大,而且芦丁所含酚羟基数目较多,所以芦丁仍然具有较强的氧化反应活性[32]。该结果说明控制DO质量浓度对于保护橙汁中芦丁成分具有积极作用。由图5-c可观察到在DO和温度的交互作用下,香蜂草苷含量呈逐渐降低趋势,但DO和温度的交互作用对香蜂草苷含量无显著性影响。
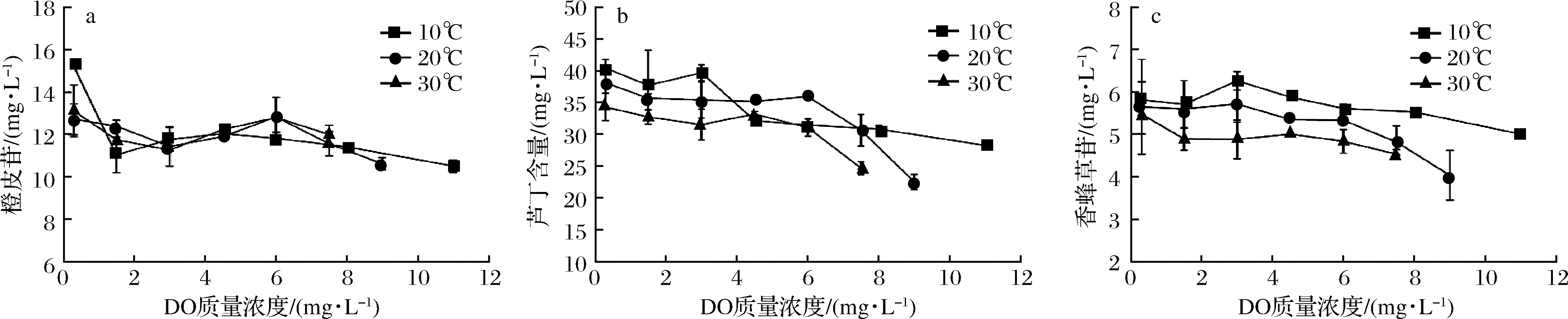
a-橙皮苷含量变化;b-芦丁含量变化;c-香蜂草苷含量变化
图5 不同温度下DO对类黄酮特征单体的影响
Fig.5 Effect of DO on characteristic monomers of flavonoids at different temperatures
2.7 不同温度下DO对3种酚酸单体含量的影响
酚酸是酚类化合物中的酸性酚,其氧化反应机理与总酚相似。图6是NFC橙汁中3种酚酸单体含量的变化情况。由图6-a、6-b和6-c可看出,在10℃和20℃条件下,随着DO质量浓度增加,3种酚酸单体含量均无明显变化;而在30℃条件下随DO质量浓度增加,3种酚酸单体呈不同幅度的下降趋势,阿魏酸、咖啡酸和对香豆酸的减少量分别为37%、23%和19%。这可能是在酶促氧化反应中,30℃是多酚氧化酶的最适反应温度,氧化速率加快的结果。通过两因素交互方差分析发现,温度和DO质量浓度的交互作用对阿魏酸、对香豆酸和咖啡酸含量的影响具有显著性差异(P<0.01)。3种酚酸特征单体的含量变化与张华等[32]对柑橘酚类物质单体的体外抗氧化活性研究结果具有一致性。

a-阿魏酸含量变化;b-对香豆酸含量变化;c-咖啡酸含量变化
图6 不同温度下DO对酚酸特征单体的影响
Fig.6 Effect of DO on characteristic monomers of phenolic acid at different temperatures
3 结论
本文通过真空脱气工艺控制橙汁中DO质量浓度,分析了不同脱气温度下DO质量浓度对NFC橙汁理化性质和部分生物活性物质的影响,发现“温度—溶解氧—活性物质氧化”与橙汁品质劣变高度关联。降低橙汁中的DO质量浓度,可减少氧化反应所需的活性氧底物,在较大程度上抑制Vc的氧化降解和酚类化合物的氧化反应。减少橙汁中的DO质量浓度和降低加工温度,对TSS影响差异显著;橙汁的色泽受DO质量浓度影响严重,尤其是在DO和温度的交互作用下,橙汁样品与对照样品相比差异显著,严重影响橙汁的感官品质。另外,DO质量浓度和温度的降低,减缓了酶促氧化和酚类化合物的自身氧化聚合反应,为酚类化合物单体的稳定存在提供了有利条件。所以,降低橙汁加工过程中的DO质量浓度和温度,有助于获得更高品质的NFC橙汁,进而提升橙汁产品的商业价值,为橙汁生产工艺优化提供科学依据。
[1] 庞泽兴,张放.2016年中国主要柑桔加工品进出口统计分析[J].中国果业信息,2017,34(9):25-34.
[2] 周常勇.我国柑桔产业发展面临的形势及对策[J].中国果业信息,2017,34(1):1-2.
[3] 杨雅利,沈海亮.中试条件下杀菌方式对NFC橙汁品质变化和贮藏温度的研究[J].农产品加工,2018,465(19):32-35.
[4] KSIRELKHATIMKA, ELAGIB R A A,HASSAN A B. Content of phenolic compounds and vitamin C and antioxidant activity in wasted parts of Sudanese citrus fruits[J]. Food Science & Nutrition,2018,6(5):1 214- 1 219.
[5] 从彦丽,彭梦雪,刘冬,等.柑橘在体外模拟胃肠消化过程中总多酚、总黄酮及总抗氧化活性的变化规律[J].食品科学,2016,37(17):96-103.
[6] BARBOSA P P M, RUVIARO A R,MACEDO G A. Comparison of different Brazilian citrus by-products as source of natural antioxidants[J]. Food Science and Biotechnology,2018,27(5):1 301-1 309.
[7] HU Yan, LI Yan, ZHANG Wenlin , et al. Physical stability and antioxidant activity of citrus flavonoids in arabic gum-stabilized microcapsules: Modulation of whey protein concentrate[J]. Food Hydrocolloids,2018,77:588-597.
[8] European Food Safety Authorxity(EFSA) S. Scientific opinion on dietary reference values for vitamin C[J]. European Food Safety Authority Journal.2013,11(11):3 418-3 485.
[9] 左龙亚. 柑橘亚属植物果皮多酚类物质提取及其抗氧化、抑菌活性检测[D].重庆:西南大学,2018.
[10] 吴梅青,刘捷频,陈丹.柑橘黄酮抗氧化和抗肿瘤作用研究进展[J].亚太传统医药,2017,13(1):83-85.
[11] VONLINTIG J. Metabolism of carotenoids and retinoids related to vision[J]. Journal of Biological Chemistry,2012,287(3):1 627-1 634.
[12] 田明,徐晓云,范鑫,等.柑橘中主要类胡萝卜素及其生物活性研究进展[J].华中农业大学学报,2015,34(5):138-144.
[13] AL FATA N, GEORGE S, DLALAH N, et al. Influence of partial pressure of oxygen on ascorbic acid degradation at canning temperature. Innovative Food Science and Emerging Technologies[J],2017,49:215-221.
[14] ANDERSSON K,LINGNERT H. Influence of oxygen concentration and light on the oxidative stability of cream powder[J]. LWT-Food Sci Tech,1998,31(2):169-176.
[15] QUAST D, KAREL M, Effects of oxygen diffusion on oxidation of some dry foods[J]. Food Science and Technology,1971,6(1):95-106.
[16] CHOE E, MIN D B. Chemistry and reactions of reactive oxygen species in foods[J]. Journal of Food Science,2005,70(9):R142-R159.
[17] DHUIQUE-MAYER C, TBATOU M, CARAIL M, et al. Thermal degradation of antioxidant micronutrients in citrus juice: Kinetics and newly formed compounds[J]. Journal of Agricultural and Food Chemistry,2007,55(10):4 209-4 216.
[18] VAN BREE I, BAETENS J M, SAMAPUNDO S, et al. Modelling the degradation kinetics of vitamin C in fruit juice in relation to the initial headspace oxygen concentration[J]. Food Chemistry,2012, 134(1):207-214.
[19] BACIGALUPI C, MAUREY A, BOUTYOY N, et al. Changes in nutritional value of a multi-vitamins fortified juice packed in glass and standard PET bottles[J]. Food Control, 2016,60:256-262.
[20] 姚刚.苹果清汁加工中VC的调控技术研究[D].北京:中国农业大学,2015.
[21] GB 5009.86—2016食品安全国家标准食品中抗坏血酸的测定[S].北京:中国标准出版社,2016.
[22] 苑博.果汁多酚的加工稳定性及与蛋白质作用对体外消化的影响[D].无锡:江南大学,2011.
[23] NY/T 2010—2011柑橘类水果及制品中总黄酮含量的测定[S].北京:中国农业出版社,2011.
[24] MOTOHASHI N, SAITO Y. Competitive measurement of rate constants for hydroxyl radical reactions using radiolytic hydroxylation of benzoate[J]. Chem Pharm Bull, 1993,41(10):1 842-1 845.
[25] BUCKNALL T,EDWARDS H E,KEMSLEY K G,et al.The formation of malondehyde in irradiated carbohyrates[J].Carbohydrates research,1978,62(1):49-59.
[26] SANT’ANNA V, GURAK P D, FERREIRA MARCZAK LD, et al.Tracking bioactive compounds with colour changes in foods-A review[J]. Dyes and Pigments,2013,98(3):601-608.
[27] 苏桂棋,黄和林,蒋娜,等.维生素C的作用及常见不良反应[J].世界最新医学信息文摘,2019,19(8):120-121;125.
[28] GUEVEDO R, PIAZ O,CAGUEO A, et al.Quantification of enzymatic browning kinetics in pear slices using non-homogenous L* color information from digital images[J].LWT-Food Science and Technology,2009,42(8):1 367-1 373.
[29] 刘伟伟,苹果酒中酚类物质氧化聚合反应的研究[D].无锡:江南大学,2006.
[30] 刘汉珍,俞浩,毛斌斌,等.不同贮藏温度对滁菊鲜品有机酸、黄酮类成分的影响[J].安徽科技学院学报,2014,28(5):34-37.
[31] LI Yongsheng, KANDHAR A D,MUKHERJEE A A, et al. Acute and sub-chronic oral toxicity studies of hesperidin isolated from orange peel extract in Sprague Dawley rats[J]. Regulatory Toxicology and Pharmacology,2019,105:77-85.
[32] 张华,周志钦,席万鹏.15种柑橘果实主要酚类物质的体外抗氧化活性比较[J].食品科学,2015,36(11):64-70.