纤维素是自然界中含量丰富的天然聚合物。在分子水平上,不同来源的纤维素都是相同的,即通过β-1,4糖苷键连接在一起的D-葡萄糖单元的无支链聚合物,但是纤维素在其晶体结构方面不一定相同[1]。纯纤维素晶型具有几种不同的排列结构,分别为纤维素Ⅰ、Ⅱ、Ⅲ和Ⅳ型。其中,只有纤维素Ⅰ型是天然存在的,其他(Ⅱ型,Ⅲ型和Ⅳ型)均可由Ⅰ型通过化学处理制备[2]。纳米纤维素(nano-crystal cellulose, NCC)是一种重量轻、密度低(约1.6 g/cm3)、强度性能优异的可生物降解纳米纤维[3],其表面具有丰富的羟基官能团[4],相较于微晶纤维素(microcrystalline cellulose,MCC),它具有更高的纯度、结晶度、亲水性、可及性、生物相容性和自组装特性[5],可以用来制备功能性材料[6]。因此NCC受到化工、食品、医药等领域的青睐。制备NCC的方法主要有化学法(酸水解法等)、物理法(球磨法等)、生物法(酶法等),以及三者两两结合法等。酸水解法是目前制备纳米纤维素最成熟、稳定的一种方法,其中硫酸水解法不仅能较好地分离纳米纤维素,而且能使纳米纤维素表面的羟基与硫酸根离子发生酯化反应,形成分散稳定的胶体体系[7-8]。虽然各类型纤维素的化学成分相似,但由于来源和提取方法的不同,它们在形貌、粒度、结晶度和某些性质上有所不同[9]。因此本文旨在探究以柚皮为原料制备的纳米纤维素的形态特征,为柚皮的深度开发提供新途径。
丰都红心柚风味独特,具有入口化渣、酸甜可口和果皮较厚等特点。其果皮中含有丰富的纤维素[10]、果胶[11]和以柚皮苷为主的黄酮类物质[12],其中果胶、黄酮类物质的提取及利用方面的研究报道较多,而在柚皮纤维素的提取与利用方面的研究报道并不多见[13-14]。为避免生产加工过程中因皮渣丢弃造成的环境污染、经济损失和资源浪费,提高柚子副产物的综合利用,本文在制备出柚皮MCC的基础上,采用硫酸水解法进行柚皮NCC的制备,以单因素试验和响应面分析法优化制备条件,并对制备出的NCC进行形态表征与结构分析,以期在开发柚皮纤维素新用途的同时,为处于研究热点的纳米纤维素提供新的植物来源。
1 材料与方法
1.1 材料与试剂
丰都红心柚,采购于重庆市丰都县三元镇。
NaOH,成都市科隆化学品有限公司;H2SO4、HCl、H2O2、无水乙醇,重庆川东化工有限公司;以上均试剂为分析纯。
1.2 仪器与设备
6202型高速粉碎机,北京燕山正德机械设备有限公司;HW.SY11-KP2型智能恒温水浴锅,北京市长风仪器仪表公司;电子天平,赛多利斯科学仪器(北京)有限公司;GZX-9240 MBE型数显鼓风干燥箱,上海博迅实业有限公司医疗设备厂;KQ5200E型超声波清洗器,昆山市超声仪器有限公司;DF-101S型集热式恒温加热磁力搅拌器,郑州长城科工贸有限公司;TGL-20M台式高速冷冻离心机,长沙高新技术产业开发区湘仪离心机仪器有限公司;LGJ-10型真空冷冻干燥机,北京松源华兴科技发展有限公司;Nicolet/is5010400型傅里叶变换红外光谱仪,重庆佳佰能仪器有限公司;X'Pert3 Powder10300型X射线衍射仪,荷兰帕纳特仪器有限公司;SU8020型场发射扫描电镜,日本日立公司。
1.3 实验方法
1.3.1 柚皮纤维素的提取及柚皮微晶纤维素的制备
参考曾小峰等[15-16]优化的超声波辅助化学法进行柚皮纤维素的提取与微晶纤维素的制备。
将粉碎后的柚皮粉以1∶20(g∶mL)的料液比与0.1 mol/L的HCl混合,85℃水浴2 h后抽滤,取滤渣用蒸馏水洗至中性后于60℃下烘干。将除去果胶的柚皮粉以1∶20的料液比与94 g/L的NaOH溶液混合,在超声功率200 W、温度84℃下超声77 min,抽滤并取滤渣,蒸馏水洗涤3次后,按1∶20的料液比加入体积分数为8%的H2O2溶液,使用NaOH调溶液pH至11左右,于30℃下反应30 min,蒸馏水洗涤滤渣至中性,用乙醇(体积分数为95%)洗脱色素等杂质,60℃烘干,得到柚皮纤维素。
将柚皮纤维素以1∶20的料液比置于体积分数为8 %的HCl中60℃下酸解80 min后过滤,蒸馏水将滤渣洗至中性,60℃烘干,即得柚皮微晶纤维素。
1.3.2 柚皮纳米纤维素的制备
将柚皮MCC与一定质量分数的H2SO4以1∶10(g∶mL)的比例混合,在一定温度下反应一定时间,升温过程不超过5 min,反应期间不断搅拌。到达反应时间后立即用10倍蒸馏水终止反应,即得NCC悬浮液。用等量蒸馏水在8 000 r/min,10 min的条件下离心洗涤4~5次,即得下层乳白色的NCC悬浮液。将其置于透析袋中透析至pH不再变化。对透析后的悬浮液进行超声分散20 min,通过冷冻干燥得到NCC固体粉末[17]。
1.3.3 纳米纤维素得率的测定
测量柚皮纳米纤维素胶体的总体积,移取20 mL悬浮液置于称量瓶中,60℃烘至恒重,将其放入干燥器中冷却30 min后称重[18],纳米纤维素得率计算如公式(1):
得率![]()
(1)
式中:m,原料的质量,g;m1,称量瓶与烘干后样品的总质量,g;m2,称量瓶的质量,g;V1,纳米纤维素胶体的总体积,mL;V2,移取的体积,mL。
1.3.4 NCC单因素试验设计
以柚皮纳米纤维素的得率作为评价指标,按照1.3.2中的制备工艺,依据表1列出的因素条件进行单因素试验分析。在进行单因素试验中,除选择的因素外,其余因素均选用水平3的条件进行试验。
表1 单因素水平设计表
Table 1 Levels design of single factor experiment
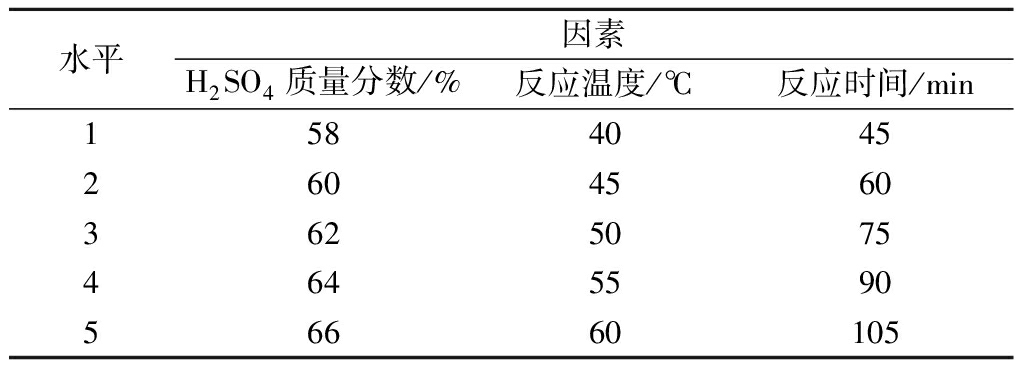
水平因素H2SO4质量分数/%反应温度/℃反应时间/min158404526045603625075464559056660105
1.3.5 响应面试验优化制备条件
基于单因素试验结果,选取对试验结果影响较大的H2SO4质量分数、反应温度、反应时间3个因素作为自变量,采用Box-Behnken设计3因素3水平响应面试验,因素与水平设计如表2。
表2 响应面试验因素水平表
Table 2 Factors and levels used in response surface experiments

水平因素H2SO4质量分数(A)/%反应温度(B)/℃反应时间(C)/min-160456006250751645590
1.3.6 场发射扫描电镜分析(SEM)
将超声分散后的纳米纤维素悬浮液滴在硅片上自然干燥后,将样品进行喷金处理后放在场发射扫描电子显微镜下,观察柚皮纳米纤维素的大小和形态。
1.3.7 傅立叶红外光谱分析(FT-IR)
以1∶200(g∶g)将样品与KBr混合压片,将压片的样品放在红外光谱仪上进行4 000~400 cm-1检测。
1.3.8 结晶度分析(XRD)
将样品粉末放入X射线衍射仪的衍射槽内进行扫描范围2θ=5~40°,步长0.02°,扫描速率2°/min的测试。采用经验公式-Segal公式(2)计算样品的相对结晶度(crystallinity index, CI)[19]:
(2)
式中:I002,002面(2θ=22.18°) 晶格衍射峰强度;Iam,纤维素无定形区衍射峰强度(2θ=18°)
2 结果与分析
2.1 单因素实验结果分析
2.1.1 H2SO4质量分数对NCC得率的影响
由图1可知,NCC得率随H2SO4质量分数含量的逐渐增加,呈现出先增大后减小的趋势,当质量分数为62%时,得率最高为57.40%。当质量分数为58%、60%时,得率不高的原因可能是H2SO4质量分数的降低不足以在特定的时间内水解无定形区,从而导致水解不充分;同时,由于纤维素在浓酸中存在溶胀反应[20],在酸含量较低的情况下,纤维素不能充分进行溶胀反应,导致产物粒径过大达不到纳米级尺寸,影响了得率。当H2SO4质量分数为62%时,酸浓度较适宜,纤维素水解反应充分,溶胀率高,产物粒径小,得率最高。随着酸含量的继续增大,试验发现反应制得的纤维素悬浮液不再呈现乳白色,而是趋近黄色,这可能是由于H2SO4含量过大,将纤维素的糖苷键水解成葡萄糖[21],进而呈现黄色半透明溶液,得率下降。当H2SO4质量分数达到70%时,纤维素呈现焦黑色,无法制备出纳米纤维素。
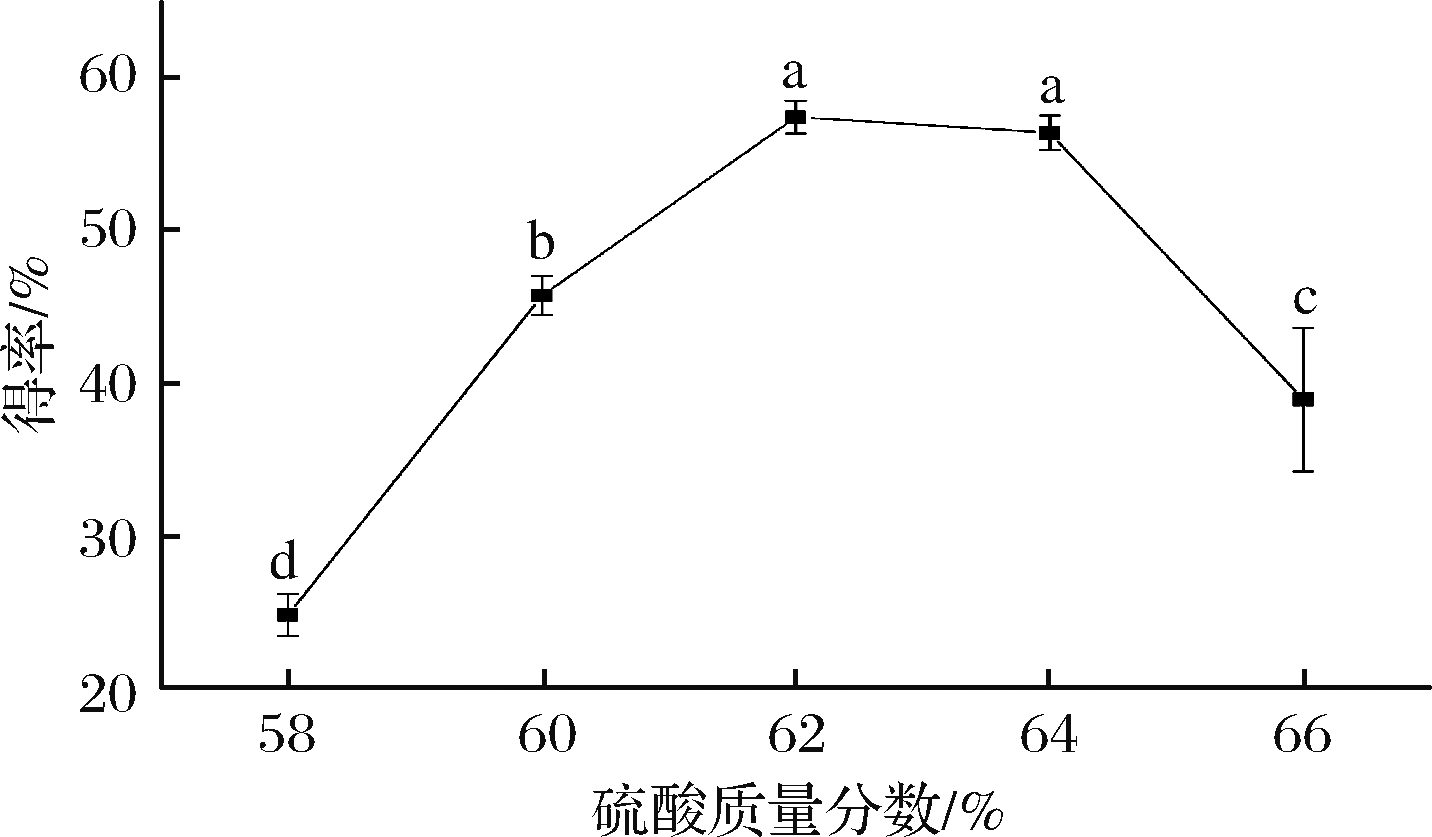
图1 硫酸质量分数对NCC得率的影响
Fig.1 Effects of sulfuric acid mass fraction onthe yield of nanocellulose from pomelo’s mesocarp注:不同小写字母表示显著性差异(P<0.05)。下同。
2.1.2 反应温度对NCC得率的影响
由图2可知,当温度为40℃时,NCC得率很低,仅有7.44%,说明温度过低,不足以使纤维素水解完全,水解产物粒径过大,导致得率很低。随着反应温度的逐渐升高,酸催化剂中的质子运动愈发活跃,其与纤维素中糖苷键的反应速率加快[22],酸解反应进行的更加充分,NCC得率逐渐提高。当温度达到50℃时,得率达到最高值60.49%,随后开始下降,可能是由于温度过高,纤维素分解速率过快,在相同的时间内,反应生成的纳米纤维素也被部分水解成了糖类物质,导致得率减少。

图2 反应温度对NCC得率的影响
Fig.2 Effects of reaction temperature on theyield of nanocellulose from pomelo’s mesocarp
2.1.3 反应时间对NCC得率的影响
由图3可知,随着反应时间的增加,得率呈现出先增大后迅速减小的趋势,当反应时间为75 min时,得率达到最大值64.39%,出现这种变化趋势的原因是时间过短,不足以使酸与糖苷键充分作用,酸解不完全,得率较低;随着时间的不断延长,酸继续与纤维素作用生成葡萄糖等糖类物质,水解过度,悬浮液开始变黄,产率下降。
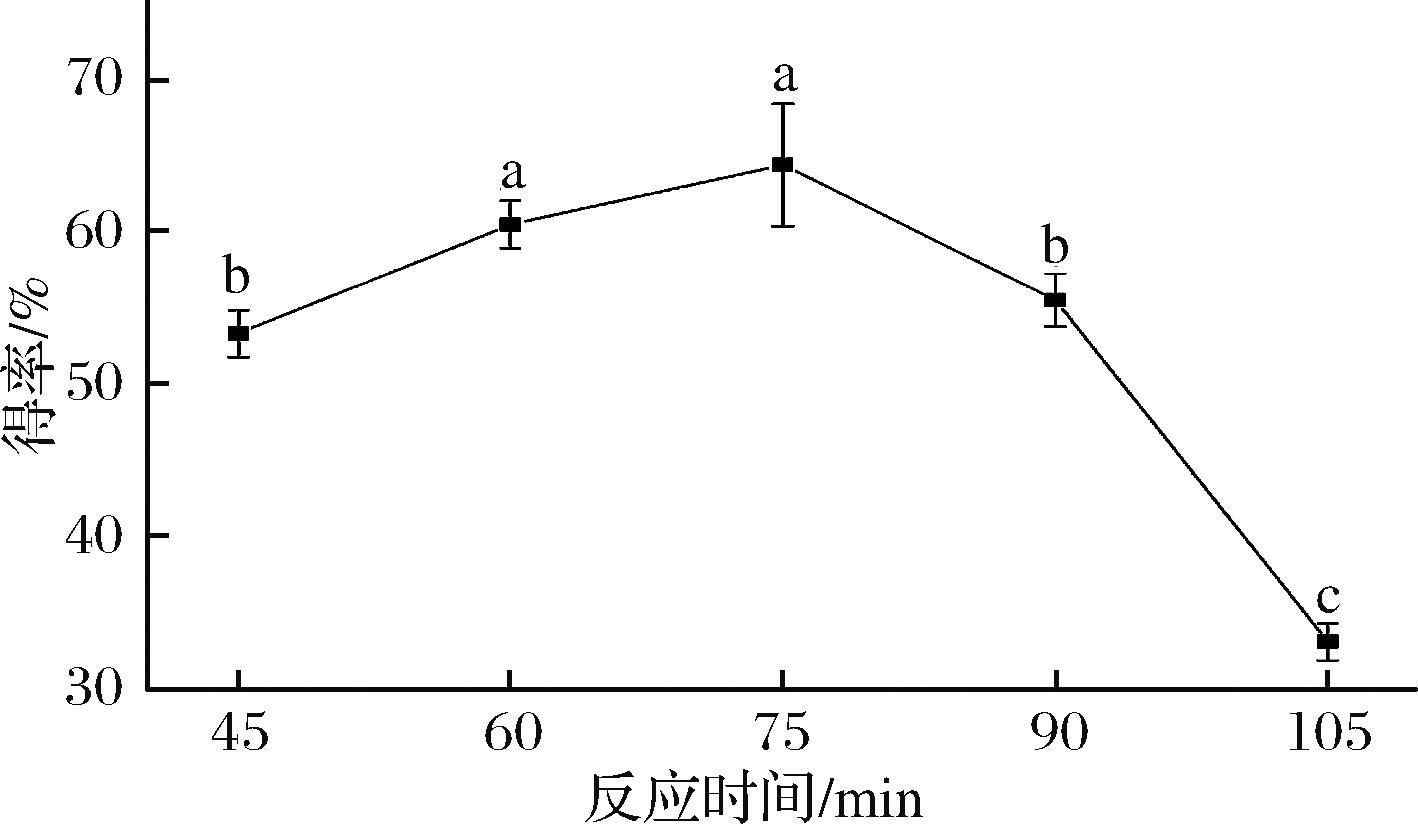
图3 反应时间对NCC得率的影响
Fig.3 Effects of reaction time on the yield ofnanocellulose from pomelo’s mesocarp
2.2 响应面结果分析
2.2.1 响应面设计方案与实验结果
以单因素试验结果为依据,选取H2SO4质量分数、反应温度和反应时间3个因素,以NCC得率为指标,采用Design-Expert8.0.6软件进行3因素3水平的响应面试验设计与分析。试验设计及结果如表3所示。
表3 响应面试验设计与结果
Table 3 Box-Behnken design with experimental results
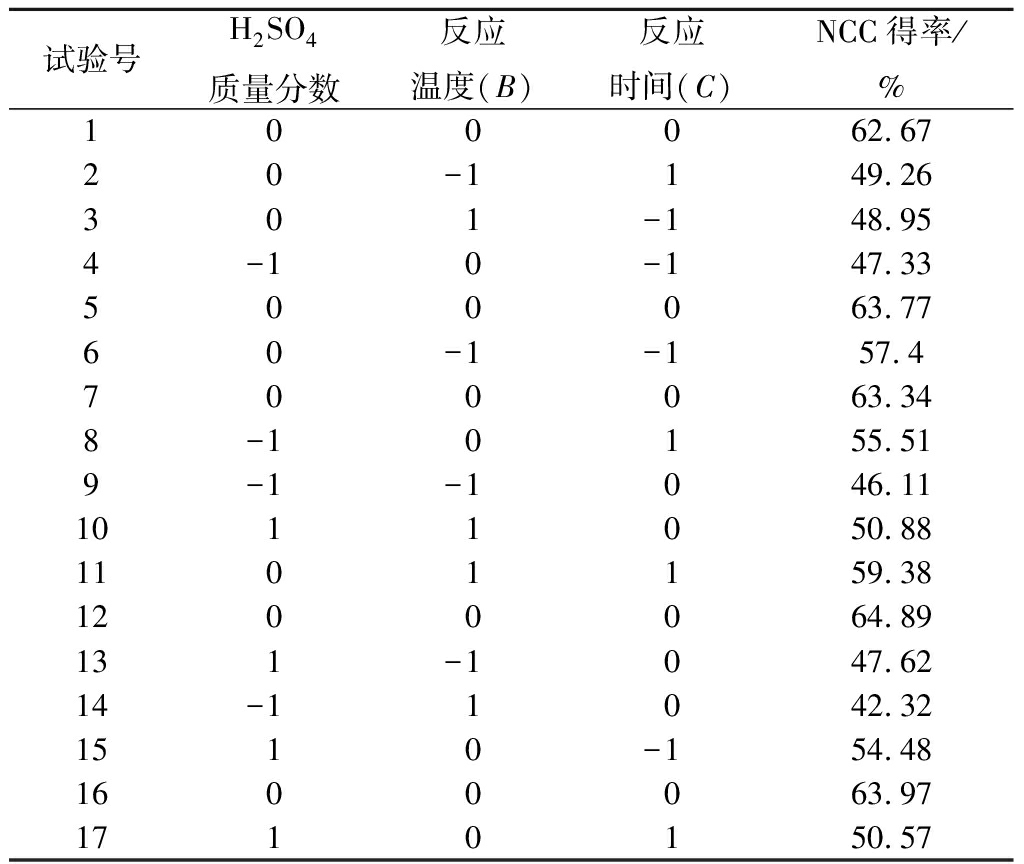
试验号H2SO4质量分数反应温度(B)反应时间(C)NCC得率/%100062.6720-1149.26301-148.954-10-147.33500063.7760-1-157.4700063.348-10155.519-1-1046.111011050.881101159.381200064.89131-1047.6214-11042.321510-154.481600063.971710150.57
2.2.2 模型的建立与显著性检验
通过对表3的数据进行回归分析,得到表4的结果,从表4可以看出本试验所建立的模型P<0.000 1,达到极显著水平,失拟项P=0.093 6>0.05,不显著,说明模型与实际试验拟合较好,回归方程的R2=0.986 7,校正系数![]() 说明模型与实际结果相近,该模型可靠适用。由表4的方差分析结果可知,因素A、AB(P < 0.05)对NCC得率的影响显著;交互项AC、BC,以及A2、B2、C2(P < 0.01)对NCC得率的影响极显著。由表中F值可以判断出各个因素对NCC得率的影响大小,按主次排序为:H2SO4质量分数(A)>反应时间(C)>反应温度(B)。通过对表3数据进行多元二次回归拟合,得到本模型的回归方程为Y=63.73+1.54A+0.14B+0.82C+1.76AB-3.02AC+4.64BC-9.39A2-7.61B2-2.37C2。
说明模型与实际结果相近,该模型可靠适用。由表4的方差分析结果可知,因素A、AB(P < 0.05)对NCC得率的影响显著;交互项AC、BC,以及A2、B2、C2(P < 0.01)对NCC得率的影响极显著。由表中F值可以判断出各个因素对NCC得率的影响大小,按主次排序为:H2SO4质量分数(A)>反应时间(C)>反应温度(B)。通过对表3数据进行多元二次回归拟合,得到本模型的回归方程为Y=63.73+1.54A+0.14B+0.82C+1.76AB-3.02AC+4.64BC-9.39A2-7.61B2-2.37C2。
表4 回归模型方差分析表
Table 4 Analysis of variances for the developed regression equation

方差来源平方和自由度均方F值P值显著性模型854.28994.9257.79< 0.000 1∗∗H2SO4质量分数(A)18.85118.8511.480.0116∗反应温度(B)0.1610.160.0990.762 3反应时间(C)5.3815.383.270.113 3AB12.43112.437.560.028 5∗AC36.54136.5422.250.002 2∗∗BC86.21186.2152.490.000 2∗∗A2370.881370.88225.79< 0.000 1∗∗ B2243.861243.86148.46< 0.000 1∗∗C223.66123.6614.40.006 8∗∗残差11.5071.64失拟项8.8232.944.390.093 6不显著纯误差2.6840.67总和865.7816
注:*,P < 0.05,差异显著;**,P < 0.01,差异极显著。
2.2.3 响应面分析与寻优
根据回归方程,得到各因素交互作用对NCC得率影响的响应面图和等高线图(图4)。由图4-a中等高线图可以看出,等高线呈微椭圆形,说明A(H2SO4质量分数)、B(反应温度)两因素存在交互作用且对得率的影响较显著(P < 0.05);由3D曲面图可看出,当反应时间不变时,随着H2SO4含量(质量分数)的增大和反应温度的升高,纳米纤维素得率均呈现先升高后下降的变化趋势,曲面在H2SO4含量的-0.50~0.50水平和反应温度的-0.50~0.00水平出现极值,即为最大值。由图4-b中曲面图可以看出,当固定反应温度时,NCC得率随着H2SO4含量的增大呈现先升高后下降的趋势,而随着反应时间的延长,NCC得率呈现先逐渐上升而后略微下降的趋势,图中可明显看出H2SO4含量变化曲面较反应时间更陡,说明H2SO4含量对NCC得率的影响比反应时间对其的影响更为显著;等高线图中发现等高线呈现椭圆形,说明A(H2SO4质量分数)、C(反应时间)两因素的交互作用对得率影响显著(P<0.01),这与方差分析的结果一致。图4-c中曲线图呈现出当H2SO4含量一定时,NCC得率受反应温度的影响较反应时间更显著,在反应温度的-0.50~0.50水平和反应时间的-1.00~0.00水平,曲面出现最高点,即为得率最高的反应时间、温度条件;等高线图显示B(反应温度)、C(反应时间)两因素交互作用明显且对得率结果影响显著(P<0.01)。

图4 各因素交互作用对纳米纤维素得率影响的响应面图和等高线图
Fig.4 Response surface and contour plots showing theeffect of various factors on nanocellulose yield
2.2.4 验证试验
通过响应面回归方程计算与分析预测出的最优制备条件为:H2SO4质量分数62.11%,反应温度50.42℃,反应时间78.31 min,此条件下计算出的最高NCC得率为63.86%。考虑到实际操作情况,将条件调整为H2SO4质量分数62%,反应温度50℃,反应时间78 min。为验证该模型的可靠性,采用最优条件进行验证试验,得NCC得率为63.27%,与理论值接近,说明分析结果可靠,可以较好地预测实际值。
2.3 SEM分析结果
图5为2种不同放大倍数下的柚皮纳米纤维素场发射扫描电镜图。由图5可以看出柚皮NCC呈类球状,粒径在100~200 nm,大小一致且分布均匀,部分粒子之间存在团聚的现象,这是由于NCC表面具有大量的羟基,经水解处理后,纤维素尺寸变小,比表面积增大,其表面的羟基更易相互结合形成氢键[23],从而产生团聚的现象。与之前研究制备出的MCC[15]相比,硫酸水解反应使MCC原本不规则且表面粗糙的结构减小为纳米级且大小均匀的类球状结构,比表面积进一步增大,使MCC的物化性能进一步提高。

a-柚皮纳米纤维素1万倍电镜放大图;b-柚皮纳米纤维素10万倍电镜放大图
图5 柚皮纳米纤维素的场发射扫描电镜图
Fig.5 SEM of NCC from pomelo’s mesocarp
2.4 红外光谱分析结果
红心柚皮微晶纤维素与纳米纤维素的红外光谱图如图6所示,红心柚皮微晶纤维素与纳米纤维素均在3 400 cm-1附近出现强的吸收峰,是由于纤维素分子表面的—OH基团伸缩振动产生,这是所有纤维素具有的特征峰[24]。NCC在该处的峰强度明显大于MCC,说明酸水解处理过程中氢键断裂使纤维素分子中的—OH基团增强[25]。2 370 cm-1附近出现的吸收峰是由于空气中CO2的不对称伸缩产生的。MCC与NCC在1 650 cm-1附近出现的吸收峰是由纤维素分子表面的羰基(C![]() O键)拉伸振动引起的[26]。MCC在1 473.62 cm-1处出现的吸收峰由-CH2弯曲振动产生,NCC在1 388.75 cm-1处出现的吸收峰是由—CH键弯曲振动产生。MCC与NCC在1 105~1 010 cm-1附近出现的吸收峰是由于—OH键的变角振动引起的;在893 cm-1附近的吸收峰对应于纤维素脱水葡萄糖单元间β-糖苷键中—OH振动的特征峰[27]。由图6可看出MCC与NCC的吸收峰没有发生明显的变化,没有新的官能团产生,说明在制备NCC的过程中并没有改变纤维素结构,两者仍然具有相同的结构。
O键)拉伸振动引起的[26]。MCC在1 473.62 cm-1处出现的吸收峰由-CH2弯曲振动产生,NCC在1 388.75 cm-1处出现的吸收峰是由—CH键弯曲振动产生。MCC与NCC在1 105~1 010 cm-1附近出现的吸收峰是由于—OH键的变角振动引起的;在893 cm-1附近的吸收峰对应于纤维素脱水葡萄糖单元间β-糖苷键中—OH振动的特征峰[27]。由图6可看出MCC与NCC的吸收峰没有发生明显的变化,没有新的官能团产生,说明在制备NCC的过程中并没有改变纤维素结构,两者仍然具有相同的结构。
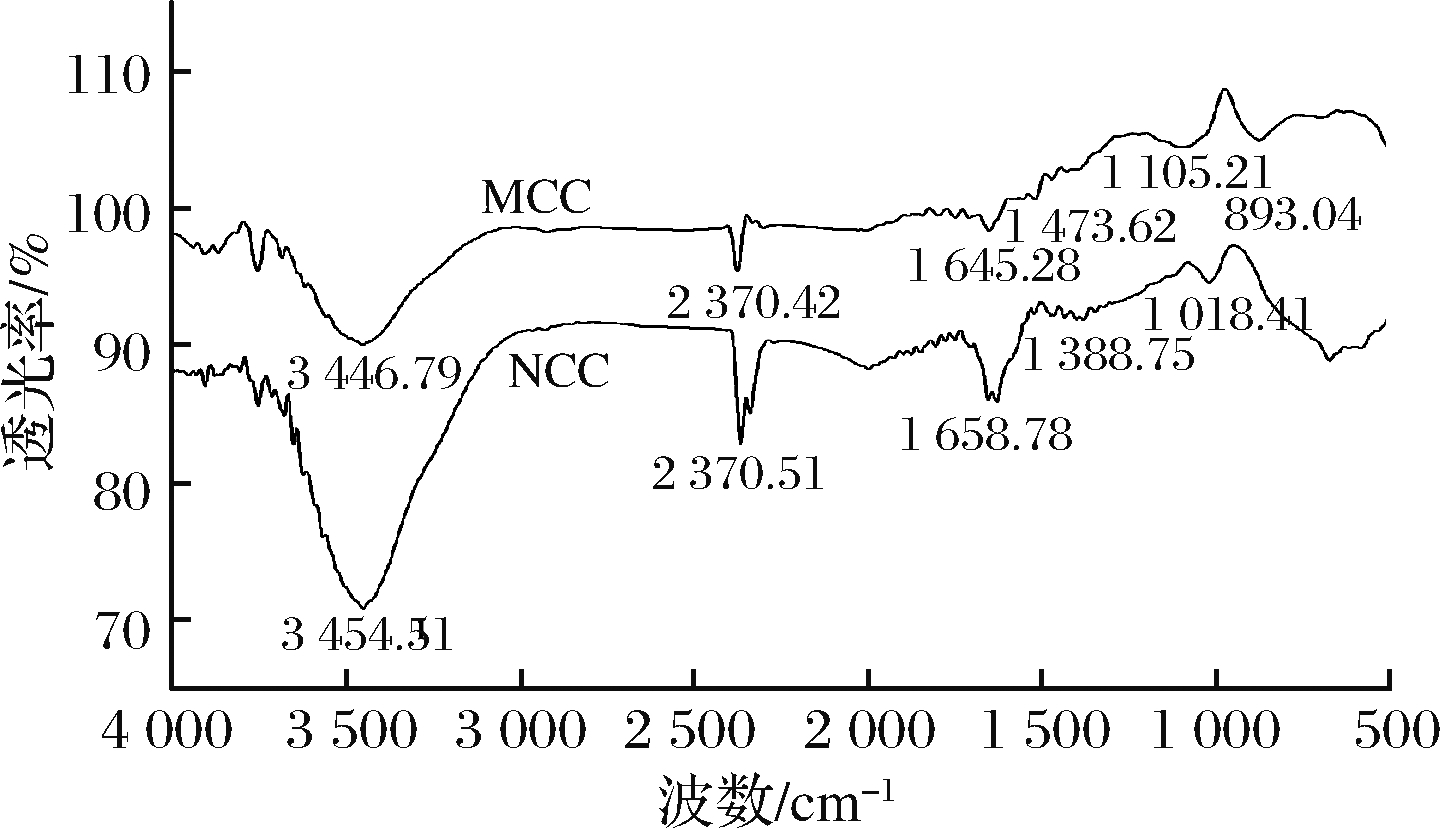
图6 红心柚皮微晶纤维素与纳米纤维素的红外光谱图
Fig.6 FTIR spectra of MCC and NCC from pomelo’smesocarp
2.5 X射线衍射分析
图7为红心柚皮微晶纤维素(MCC)与纳米纤维素(NCC)的XRD图,由图7可以看出,MCC与NCC的衍射峰位置基本一致,均在衍射角2θ为15.08°、22.18°、34.62°处出现衍射峰,说明样品晶型没有发生改变,同时根据衍射峰存在的位置表明样品的结晶类型属于典型的纤维素Ⅰ型[28],说明酸解反应没有改变纤维素的结构,这与FTIR的结果一致。由Segal公式计算得出MCC与NCC的结晶度分别为44.72%和53.75%,NCC的结晶度增大,说明酸水解过程主要发生在MCC的无定形区,而结构致密的结晶区没有受到较大程度的破坏,所以结晶区域的相对百分比增加,结晶度上升。
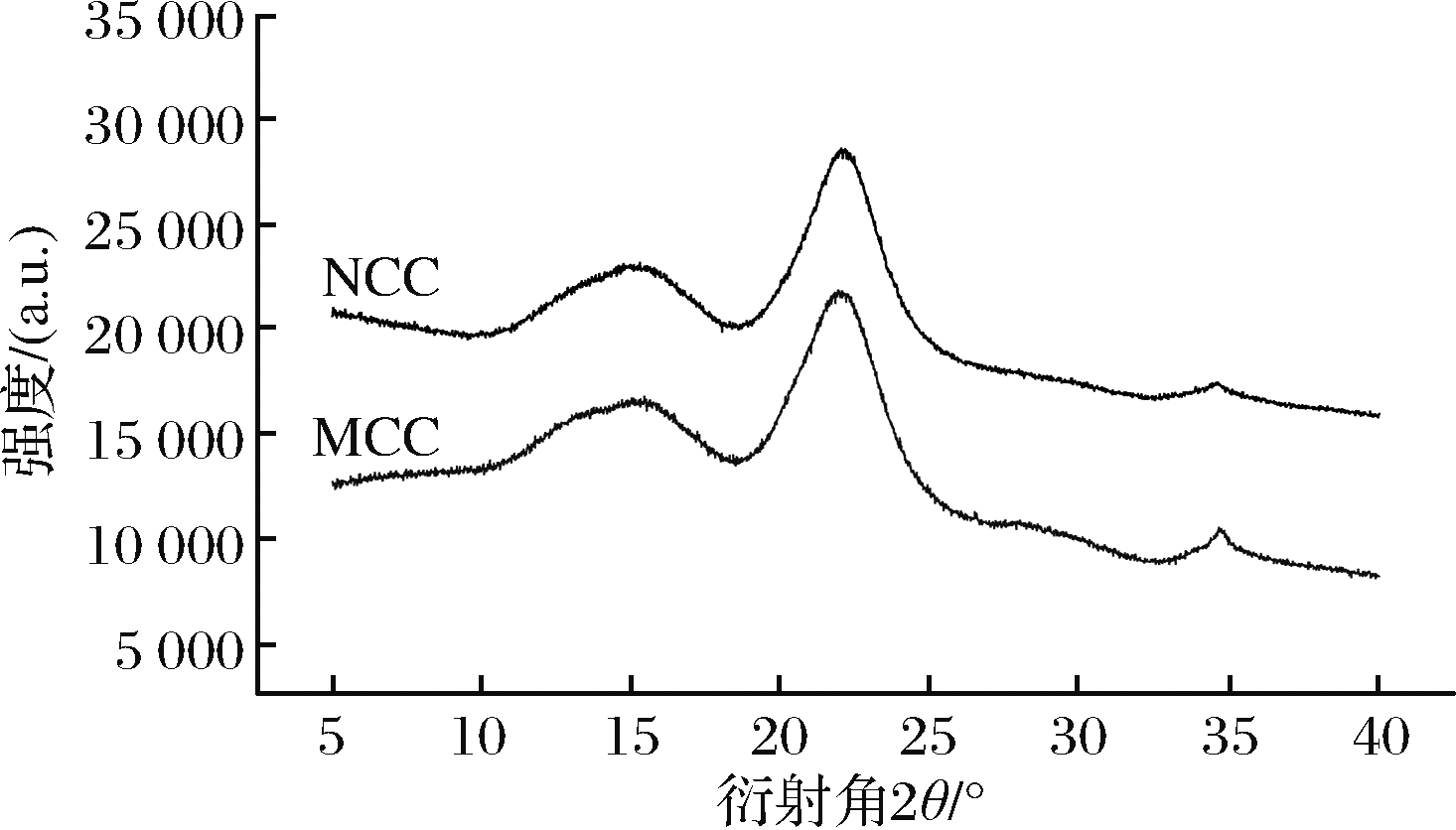
图7 红心柚皮微晶纤维素与纳米纤维素的XRD图
Fig.7 XRD analysis of MCC and NCC in mesocarpof pomelo
3 结论
通过单因素试验和响应面试验分析,在料液比1∶10的条件下,筛选出制备柚皮纳米纤维素的最优条件:H2SO4质量分数62%,反应温度50℃,反应时间78 min,此条件下预测出的得率为63.86%,通过验证试验得到此条件下实际得率为63.27%,与预测值接近,说明建立的回归模型良好可靠。由于单因素实验中,反应时间为60 min与75 min时的得率无显著性差异,考虑到实际生产的成本问题,可将反应时间缩短至60 min,以作为工业化生产的最适条件。由扫描电镜结果得出,由MCC制备出的NCC粒径减小至纳米级(100~200 nm),呈类球状,大小分布均匀。红外光谱和X射线衍射结果表明,制备出的NCC结构没有发生改变,仍保持纤维素I型结构,结晶度53.75%,相较于MCC有明显提高。综上所述,在没有破坏纤维素结构的基础上,制备出的NCC比原料MCC具有更规则的结构、更大的比表面积和更高的结晶度,使柚皮纤维素具有更高的应用价值。同时NCC作为一种可生物降解的环保型材料,在食品包装、增强复合材料、构建药物载运体系等方面有巨大的潜力。较高的得率和稳定的晶型说明柚皮可以作为制备纳米纤维素的良好来源,这不仅提高了柚皮的综合利用,拓宽了柚皮纤维素的用途,也为纳米纤维素的生产提供了新的来源。
[1] BRETT C, WALDRON K. Physiology and Biochemistry of plant cell walls[J]. Topics in Plant Physiology,1990,24(1):98.
[2] PARK Y B, KAFLE K, LEE C M, et al. Does cellulose II exist in native alga cell walls? Cellulose structure of Derbesia cell walls studied with SFG, IR and XRD[J]. Cellulose,2015,22(6):3 531-3 540.
[3] PHANTHONG P, REUBROYCHAROEN P,HAO X, et al. Nanocellulose: Extraction and application[J]. Carbon Resources Conversion,2018,1(1):32-43.
[4] HABIBI Y. Key advances in the chemical modification of nanocelluloses[J]. Chemical Society Reviews,2014,43(5):1 519-1 542.
[5] 禚晓.纳米纤维素纸基生物传感器设计[D].泰安:山东农业大学,2018.
[6] BOUJEMAOUI A, MONGKHONTREERAT S, MALMSTRÖM E, et al. Preparation and characterization of functionalized cellulose nanocrystals[J]. Carbohydrate Polymers,2015,115:457-464.
[7] DAS K, RAY D, BANDYOPADHYAY N R, et al. A study of the mechanical, thermal and morphological properties of microcrystalline cellulose particles prepared from cotton slivers using different acid concentrations[J]. Cellulose,2009,16(5):783-793.
[8] LU P, HSIEH Y L. Preparation and properties of cellulose nanocrystals: Rods, spheres, and network[J]. Carbohydrate Polymers,2010, 82(2):329-336.
[9] ELAZZOUZI-HAFRAOUI S, NISHIYAMA Y, PUTAUX J L, et al. The shape and size distribution of crystalline nanoparticles prepared by acid hydrolysis of native cellulose[J]. Biomacromolecules,2007,9(1):57-65.
[10] HIASA S H, IWAMOTO S, ENDO T, et al. Isolation of cellulose nanofibrils from mandarin (Citrus unshiu) peel waste[J]. Industrial Crops and Products,2014,62:280-285.
[11] SHARMA K, MAHATO N, CHO M H, et al. Converting citrus wastes into value-added products: Economic and environmently friendly approaches[J]. Nutrition,2017,34:29-46.
[12] KHAN M K, DANGLES O. A comprehensive review on flavanones, the major citrus polyphenols[J]. Journal of Food Composition and Analysis,2014,33(1):85-104.
[13] BICU I, MUSTATA F. Optimization of isolation of cellulose from orange peel using sodium hydroxide and chelating agents[J]. Carbohydrate Polymers,2013,98(1):341-348.
[14] BICU I, MUSTATA F. Cellulose extraction from orange peel using sulfite digestion reagents[J]. Bioresource Technology,2011,102(21):10 013-10 019.
[15] 曾小峰,彭雪娇,谈安群,等.柚皮微晶纤维素的制备及其结构特性研究[J].食品与发酵工业,2016,42(9):98-103.
[16] 曾小峰,白小鸣,盖智星,等.响应面试验优化超声辅助提取柚皮纤维素工艺[J].食品科学,2015,36(14):34-38.
[17] NAZ S, AHMAD N, AKHTAR J, et al. Management of citrus waste by switching in the production of nanocellulose[J]. IET Nanobiotechnology,2016,10(6):395-399.
[18] 唐丽荣,欧文,林雯怡,等.酸水解制备纳米纤维素工艺条件的响应面优化[J].林产化学与工业,2011,31(6):61-65.
[19] 陈珊珊,陶宏江,王亚静,等.葵花籽壳纳米纤维素制备工艺优化及其表征[J].农业工程学报,2015,31(15):302-308.
[20] 赵群.纳米微晶纤维素的制备、改性及其增强复合材料性能的研究[D].上海:东华大学,2014.
[21] 杜海顺,刘超,张苗苗,等.纳米纤维素的制备及产业化[J].化学进展,2018,30(4):448-462.
[22] JIANG F, HSIEH Y L. Cellulose nanocrystal isolation from tomato peels and assembled nanofibers[J]. Carbohydrate Polymers,2015,122:60-68.
[23] 张恒,高洪坤,王哲,等.纳米微晶纤维素的制备与表征[J].首都师范大学学报(自然科学版),2018,39(4):31-35.
[24] 刘羽,邵国强,许炯.竹纤维与其它天然纤维素纤维的红外光谱分析与比较[J].竹子研究汇刊,2010,29(3):42-46.
[25] LIU Xiuyu, JIANG Yan, SONG Xueping, et al. A bio-mechanical process for cellulose nanofiber production - Towards a greener and energy conservation solution[J]. Carbohydrate Polymers,2019,208:191-199.
![]() M, PIECZYMEK P M, et al. Tailored nanocellulose structure depending on the origin. Example of apple parenchyma and carrot root celluloses[J]. Carbohydrate Polymers,2019,210:186-195.
M, PIECZYMEK P M, et al. Tailored nanocellulose structure depending on the origin. Example of apple parenchyma and carrot root celluloses[J]. Carbohydrate Polymers,2019,210:186-195.
[27] SIR I,PLACKETT D. Microfibrillated cellulose and new nanocomposite materials: A review[J]. Cellulose,2010,17(3):459-494.
I,PLACKETT D. Microfibrillated cellulose and new nanocomposite materials: A review[J]. Cellulose,2010,17(3):459-494.
[28] ELAZZOUZI-HAFRAOUI S, NISHIYAMA Y, PUTAUX J L, et al. The Shape and size distribution of crystalline nanoparticles prepared by acid hydrolysis of native cellulose[J]. Biomacromolecules,2008,9(1):57-65.