麦芽糖醇是一种新型的功能性甜味剂,具有低热量、非龋齿性、难消化性以及促进钙的吸收等多种生理特性,被广泛应用于食品(尤其是无糖食品)和化工产业[1-4]。
麦芽糖醇的生产,是以淀粉为原料,经过酶水解获得超高麦芽糖浆后,再经加氢还原制成[5-6]。未经过提纯的麦芽糖醇产品,因含有麦芽三糖醇及其他低聚糖醇,使得溶液的黏度增大,从而抑制结晶,给结晶麦芽糖醇的生产增加了难度[7]。现阶段的工业化生产中,结晶麦芽糖醇主要通过色谱与结晶相结合的方式制备[8]。但因杂醇难以去除,导致产品纯度低、结晶收率低,生产成本居高不下,企业难以获得良好的经济效益。
三组分色谱分离技术[9],其分离模式是在一个均相混和液中,无论它含有多少种成分,都可以根据其在色谱树脂中出峰的快慢,分为快组分C、中间组分B和慢组分A,分离的目标组分是中间组分B。三组分分离模式多种多样,但目前效果最好的是集中进料模式。这种模式的特点是一个大周期的原料,一次性从中间组分区域进完,然后分多次分离出快组分C和慢组分A,暂时不出中间组分B,待中间组分B充分纯化后,一次性出完。三组分分离工艺优点为:产品纯度较高;能够有效去除杂醇,提升结晶收率;经过色谱分离后,各组分都能够得到很好利用。三组分分离工艺缺点为:色谱水耗较高;色谱处理量较小;由于色谱单独从一个固定柱进料,所以对于原料的要求较高。为了减少色谱树脂的反洗周期,色谱来料以及色谱进水的电导要求控制在10 μs/cm以下;同时必须定期跟踪原料的蛋白含量,以免影响色谱的分离效果。
目前,随着三组分分离技术越来越受关注,这种高效三组分色谱分离模式具有广阔的市场前景。本研究开发利用此技术,突破了这一瓶颈,使得麦芽糖醇的生产成本从根本上降低,产品的纯度与收率得到极大提升。研究中以色谱中试数据为例,对三组分的分离工艺进行探究和论证。
1 材料与方法
1.1 实验材料
麦芽糖醇(成分包括山梨糖醇、麦芽糖醇、麦芽三糖醇、杂醇等):浙江华康药业股份有限公司;色谱分离专用99Ca310型树脂:美国陶氏化学公司。
1.2 仪器与设备
检测仪器:PHB-3pH计,上海三信仪表厂;HZS-HA水浴恒温振荡器,上海亚荣生化仪器厂;WAY-ZT阿贝折光仪,上海精科仪器厂;DT-500电子天平,常熟市金羊天平仪厂;JOAN 200 μL移液枪,杭州天裕化工仪器有限公司;SHZ-D(Ⅲ)真空抽滤泵,英峪予华仪器厂;0.45 μm微滤膜,上海密粒膜;UPHW-1V-90T纯化水机,优普纯水机;Waters e2695高效液相色谱仪,沃特斯仪器。
实验设备:上海兆光色谱分离技术有限公司中试色谱装置;树脂总装填量为3.5 m3;PLC控制系统;SSMB三子步顺序操作模式。
1.3 实验方法
1.3.1 中式色谱分离设备的操作方法
首先用隔膜泵装填实验所用的树脂,待树脂装填完毕,对每个色谱柱进行补压排空。然后用热水对系统进行升温,温度到达以后,输入初步的参数,将系统设置为自控,调整泵频。设备运行完一个大周期以后,温度压力都达到平衡,再把料罐中的水换成原料,正式进料开始运行。一般4 h后,开始取样分析提取液、残液的浓度及组成,计算提取物收率,并根据化验数据进行分离参数调节。
1.3.2 麦芽糖醇中各个组分含量的检测方法
利用高效液相色谱仪面积归一法:首先利用标准样品确定各糖醇的归属,然后用各糖醇的峰面积比上所有色谱峰的总面积,计算各成份的相对含量。
Sugar Park-1色谱柱液相条件为:柱温85 ℃,示差检测器,检测器温度40 ℃,进样量10 μL,流动相流速0.6 mL/min,流动相为超纯水,色谱柱为Sugar Park-1(7.8 mm×300 mm)。
1.3.3 结晶麦芽糖醇的传统生产工艺
在传统的生产工艺中,主要采用两相色谱分离与结晶方式相结合来制备[10]高纯度的结晶麦芽糖醇,即选用合适的糖化酶,通过控制葡萄糖的生成,制备含量高于90%的高纯度麦芽糖;经过氢化还原后制备纯度为85%左右的麦芽糖醇;再采用两组分色谱分离将麦芽糖醇纯度从85%提升至91%,最后经过结晶制备高纯度的结晶麦芽糖醇[11]。色谱与结晶结合法制备结晶麦芽糖醇的传统工业流程[12]如下:
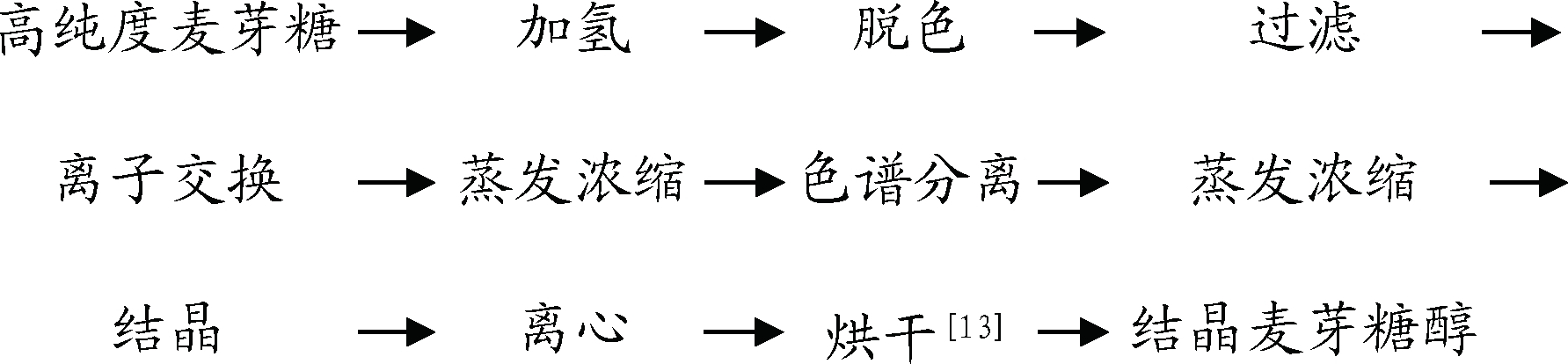
以上生产工艺主要是通过逐步提高麦芽糖醇的纯度,从而达到结晶目的。具体实验方法如下:
(1)超高麦芽糖浆的制取。选取生产上的糖化液(控制DE值≤10%),液化均匀,清亮透明,无碘试反应,倒入糖化罐中,调pH值到3左右加热进行灭酶,然后向液化液中加入适量煮沸的蒸馏水,使之浓度稀释至20%左右,迅速降温到60 ℃,调节pH值至5.2~5.4,加入β-淀粉酶、普鲁兰酶、麦芽三糖酶,加酶量按干基添加,分别为:0.50、0.39和0.58 g/kg,加完搅拌均匀,60 ℃保温糖化48 h后,补加真菌酶(0.16 g/kg)糖化60 h,出料,液相法检测麦芽糖含量在90%以上。
(2)麦芽糖氢化生成麦芽糖醇。将制得的麦芽糖浆浓缩至50%,调pH值至7.5~8.0,按干物质的10%加入镍催化剂,在氢气压力为9~10 MPa,温度125~135 ℃,搅拌转速300 r/min条件下反应2 h。氢化后保证麦芽糖醇的纯度在85%以上。
(3)脱色。按照滤液干物的0.5%~1.0%加入粉末活性炭,加前先将活性炭与等量滤液混合,这样易于活性炭的混合。脱色操作条件:pH 4.5~5.0,温度80 ℃,在20~25 r/min转速下搅拌30 min。
(4)过滤。以硅藻土为助滤剂(用量为0.5 kg/m2),板框式压滤机压滤。少量糖化液调匀硅藻土后,泵入压滤机,压力要求在0.1 MPa以下,使硅藻土均匀地沉积在滤面上,初始滤液不清,将其回流到脱色罐,直至滤液澄清为止,关闭回流管,将滤液送至储罐,过滤压力控制在0.2~0.3 MPa。
(5)离子交换。通过离子交换除去滤液中的金属离子、色素以及可溶性的含氮等杂质。交换时控制流速为700 kg/h,温度40 ℃左右。
(6)蒸发浓缩。真空度为-0.092 MPa,出料浓度58%~60%。
(7)色谱分离。在两组分色谱分离过程中,山梨醇始终富集在麦芽糖醇周围,随着生产的不断发展,色谱分离后的主产品中,山梨醇的含量逐步升高,麦芽糖醇的含量逐渐降低,从而对产品的纯度与结晶收率产生很大影响。为了消除山梨醇对结晶麦芽糖醇生产工艺的影响,在两组分色谱分离技术的基础上,开发出了三组分色谱分离技术,以最大程度去除山梨醇。
1.3.4 三组分色谱分离技术
三组分色谱分离与结晶相结合的工艺生产麦芽糖醇,即通过三组分色谱分离,将麦芽糖醇纯度从85%左右提升至95%以上,然后再结晶制备高纯度的结晶麦芽糖醇。该工艺不仅体现了当今清洁生产[14]的新理念,还为客户开发多元化产品[15]奠定了基础。三组分色谱分离制备结晶麦芽糖醇的工艺流程如下[16]:
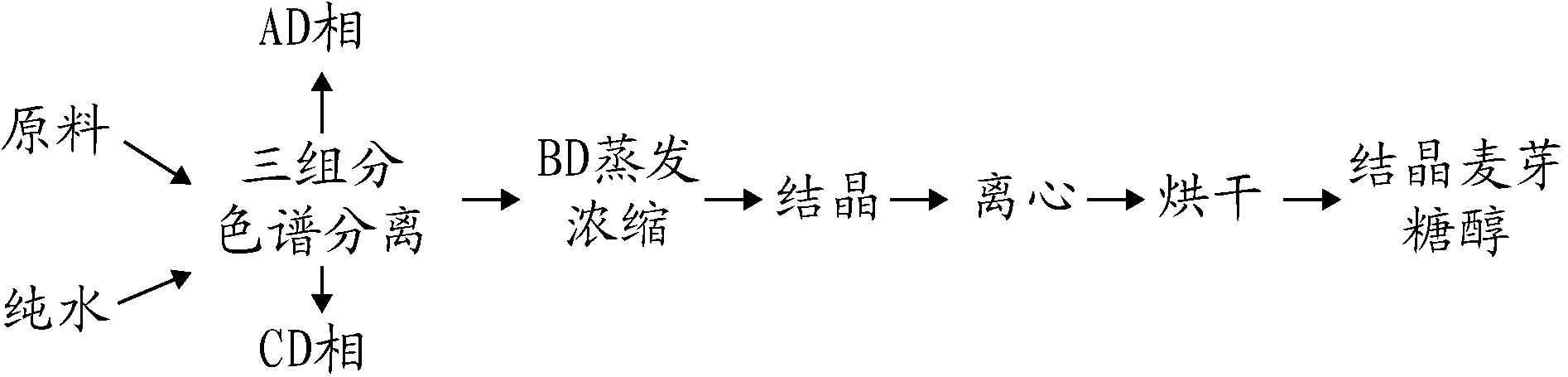
2 结果与分析
2.1 两组分色谱分离效果
两组分色谱分离过程中,受色谱进料组成不稳定的影响,色谱出料的各个组分始终处于波动状态,表1与表2中各个组分的波动不是由测量产生,而是由进料组成的波动所产生。所以从数据表面看,每组样品的各个组成的偏差不是由测量仪器所产生的测量误差。于是,选择用求多个样品平均值的方式来反映色谱的分离效果。在实际的工业化生产中,对于产品的纯度与收率的核算,也是通过这种方式来进行。
表1 色谱分离中慢组分(AD液)指标 单位:%
Table 1 The chromatogram AD liquid index
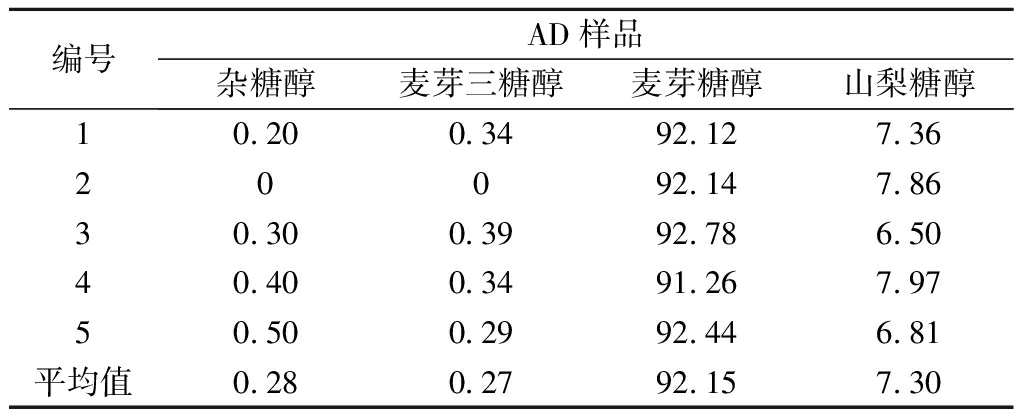
编号AD样品杂糖醇麦芽三糖醇麦芽糖醇山梨糖醇10.200.3492.127.3620092.147.8630.300.3992.786.5040.400.3491.267.9750.500.2992.446.81平均值0.280.2792.157.30
注:两组分色谱分离过程中,A代表慢组分,B代表快组分,D代表洗脱剂纯水。由于2种组分都是用水作为洗脱剂进行解析,所以用AD代表慢组分的出料产品,用BD代表快组分的出料产品。下同。
表2 色谱分离中快组分(BD液)指标 单位:%
Table 2 The chromatogram BD liquid index
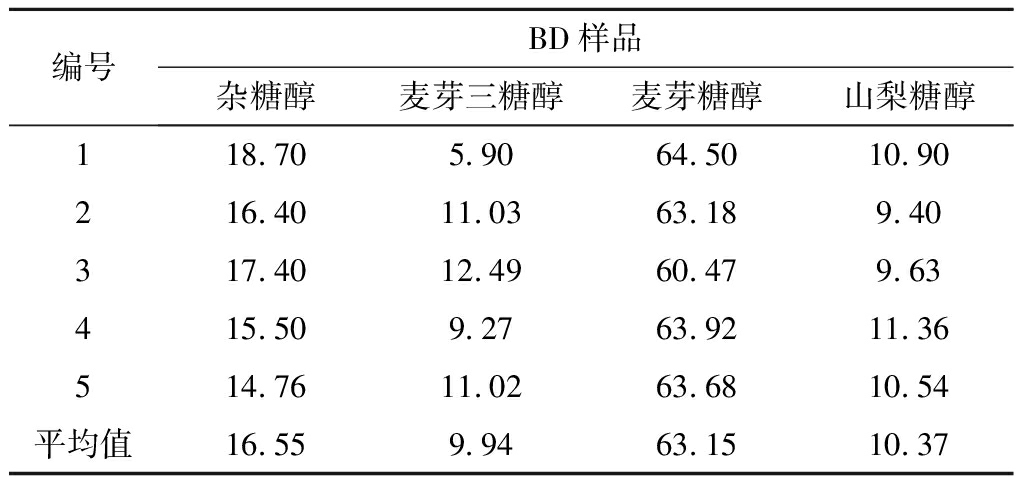
编号BD样品杂糖醇麦芽三糖醇麦芽糖醇山梨糖醇118.705.9064.5010.90216.4011.0363.189.40317.4012.4960.479.63415.509.2763.9211.36514.7611.0263.6810.54平均值16.559.9463.1510.37
由表1和表2可知,AD指标为:杂糖醇0.20%~0.30%、麦芽三糖醇0.20%~0.30%、麦芽糖醇91%~93%和山梨糖醇9.5%~10.5%;BD指标为:杂糖醇15%~17%、麦芽三糖醇9%~12%、麦芽糖醇63%~65%和山梨糖醇9%~11%;AD麦芽糖醇纯度为92.1%,麦芽糖醇收率为92%。
由表2可知,在色谱分离过程中,山梨醇始终与麦芽糖醇富集,所以很难得到高纯度的麦芽糖醇。在两组分色谱分离工艺中,原料中山梨醇含量的高低,是决定产品中麦芽糖醇含量高低的关键因素。原料中山梨醇含量高,则产品中麦芽糖醇含量低;反之,原料中山梨醇含量低,则产品中麦芽糖醇含量高。
2.2 三组分中试色谱分离
在三组分的色谱分离过程中,受色谱进料组成不稳定的影响,色谱出料的各个组分始终处于波动状态,表明表3~表5中各个组分的波动不是由测量所产生的,而是由进料组成的波动所产生的。所以从数据表面看,每组样品的各个组成的偏差不是由测量仪器所产生的测量误差。因此选择用求多个样品平均值的方式,来反映色谱的分离效果。在实际的工业化生产中,对于产品的纯度与收率的核算,也是通过这种方式来进行的。
由表3、表4和表5可知,AD液指标为:杂糖醇8%~10%、麦芽三糖醇0.5%~0.9%、麦芽糖醇53%~55%和山梨糖醇35%~37%;BD液指标为:杂糖醇1.5%~2.5%、麦芽三糖醇0.2%~0.4%、麦芽糖醇95%~96%和山梨糖醇1.5%~2.5%;CD液指标为:杂糖醇55%~57%、麦芽三糖醇9%~11%、麦芽糖醇7%~10%和山梨糖醇25%~28%;麦芽糖醇纯度为95.63%,收率为95%,杂糖醇收率65%以上。
表3 色谱出料慢组分(AD液)指标 单位:%
Table 3 The chromatogram Ad liquid index
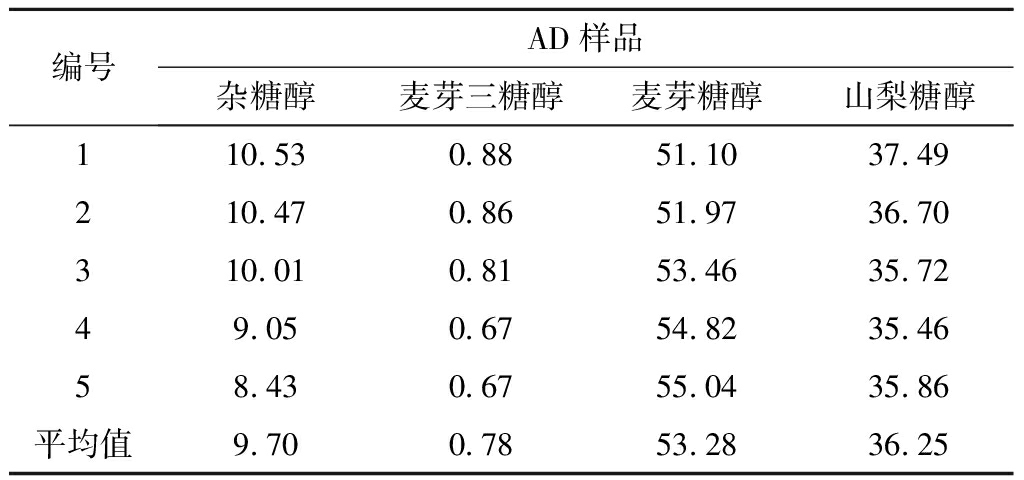
编号AD样品杂糖醇麦芽三糖醇麦芽糖醇山梨糖醇110.530.8851.1037.49210.470.8651.9736.70310.010.8153.4635.7249.050.6754.8235.4658.430.6755.0435.86平均值9.700.7853.2836.25
注:在三组分色谱分离过程中,A代表慢组分,B代表中间组分,C代表快组分,D代表洗脱剂纯水。由于3种组分都是用水作为洗脱剂进行解析,所以AD代表慢组分的出料产品,BD代表中间组分的出料产品,CD代表快组分的出料产品。下同。
表4 色谱分离中中间组分(BD液)指标 单位:%
Table 4 The chromatogram BD liquid index
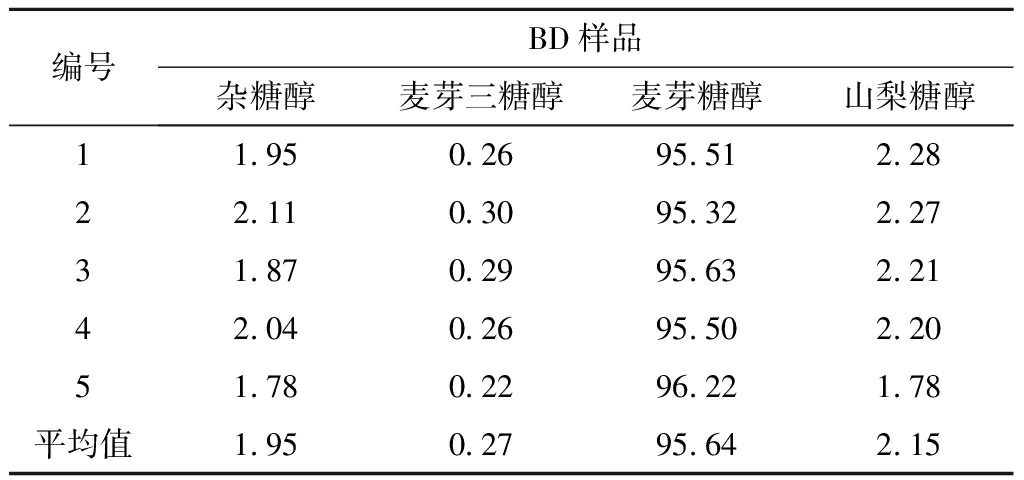
编号BD样品杂糖醇麦芽三糖醇麦芽糖醇山梨糖醇11.950.2695.512.2822.110.3095.322.2731.870.2995.632.2142.040.2695.502.2051.780.2296.221.78平均值1.950.2795.642.15
表5 色谱分离中快组分(CD液)指标 单位:%
Table 5 The chromatogram CD liquid index
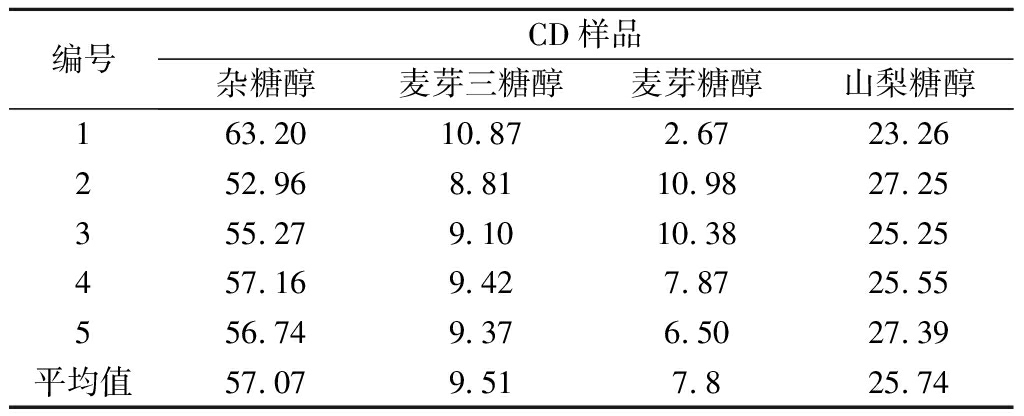
编号CD样品杂糖醇麦芽三糖醇麦芽糖醇山梨糖醇163.2010.872.6723.26252.968.8110.9827.25355.279.1010.3825.25457.169.427.8725.55556.749.376.5027.39平均值57.079.517.825.74
2.3 两种生产工艺指标及经济效益比对
表6反映的是在同种物料的条件下,经过两组分与三组分2种不同的工艺后,色谱出料产品的各项指标的对比表。通过两组分的分离工艺,主产品麦芽糖醇的纯度在92%左右,山梨醇纯度在7.42%,也就是说山梨醇始终是在主产品这边富集,采用两组分的分离工艺,山梨醇很难去除。而采用三组分的分离工艺,主产品的纯度能达到95%以上,山梨醇纯度能降到2.15%,所以说采用三组分的工艺,能降低山梨醇含量。由于麦芽糖醇纯度提高,山梨醇含量降低,所以说采用三组分分离工艺色谱收率以及后道工序的结晶收率大大提高。
表6 同种物料情况下两种生产工艺出料指标对比 单位:%
Table 6 In the case of the same kind of material,the two production processes output index comparison
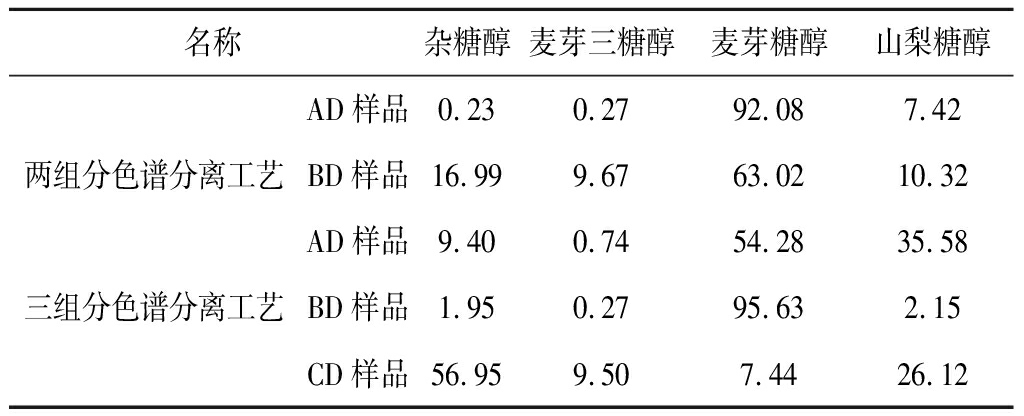
名称杂糖醇麦芽三糖醇麦芽糖醇山梨糖醇AD样品0.230.2792.087.42两组分色谱分离工艺BD样品16.999.6763.0210.32AD样品9.400.7454.2835.58三组分色谱分离工艺BD样品1.950.2795.632.15CD样品56.959.507.4426.12
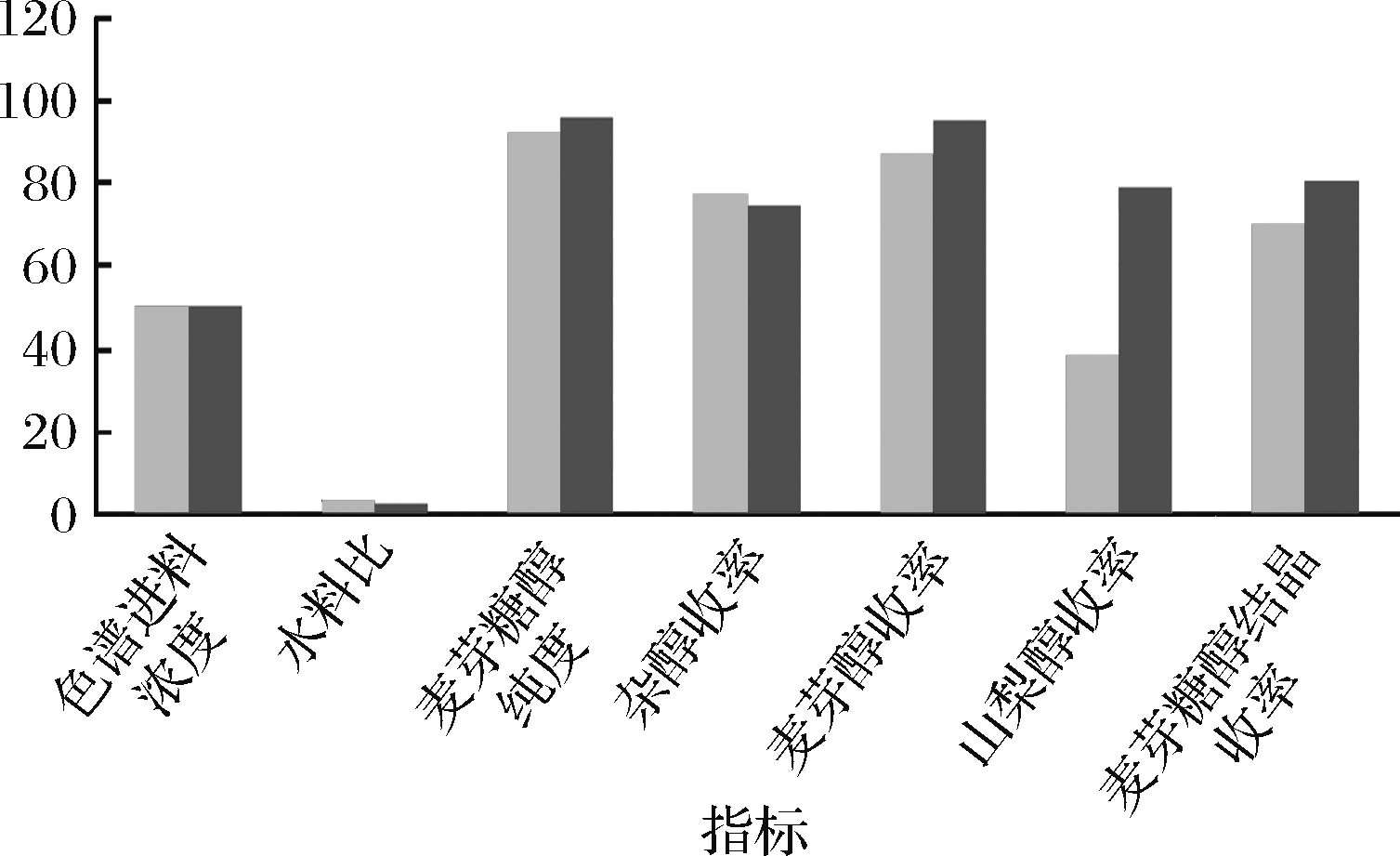
图1 同种物料情况下两种生产模式的工艺指标对比
Fig.1 In the case of the same kind of material, the comparisontable of the process indexes of the two production modes
图1是在同种物料的情况下,2种生产模式的工艺指标对比表,结果表明,在2种不同的工艺下,色谱所采用的进料浓度都是50%;两组分分离工艺的水料比为2.7,三组分分离工艺的水料比为2.2;水料比2.7指的是色谱进料为1 t时需要用2.7 t的水进行洗脱,为质量比;水料比2.2指的是色谱进料为1 t时需要用2.2 t的水进行洗脱,为质量比;麦芽糖醇的纯度是采用高压液相色谱仪所测定出来的,它反映的是麦芽糖醇的干基占样品总干基的质量百分比;杂醇、麦芽糖醇、山梨醇的收率指的是产品中各个组分的干基重与色谱进料中相对应的各个组分干基重的比值;麦芽糖醇的结晶收率指的是麦芽糖醇结晶后结晶产品的干基重量与结晶前麦芽糖醇投入料的干基重量的比值。
表7是年产1万t结晶麦芽糖醇经济效益分析表,结果表明,对于两组分的分离工艺来讲,生产1 t结晶麦芽糖醇需要消耗1.8 t原料,消耗12 t纯水,消耗蒸汽4.2 t,消耗电52度,折合成价格,生产1 t结晶麦芽糖醇成本约为11 609.2元;对于三组分的分离工艺来讲,生产1 t结晶麦芽糖醇需要消耗1.45 t原料,消耗7.86 t纯水,消耗蒸汽2.75 t,消耗电47.5度,折合成价格,生产1 t结晶麦芽糖醇成本约为9 239.264元。
表7 以年产1万t结晶麦芽糖醇为例进行经济效益分析
Table 7 Taking an annual output of 10 000 tons of crystalline maltose as an example to analyze economic benefits
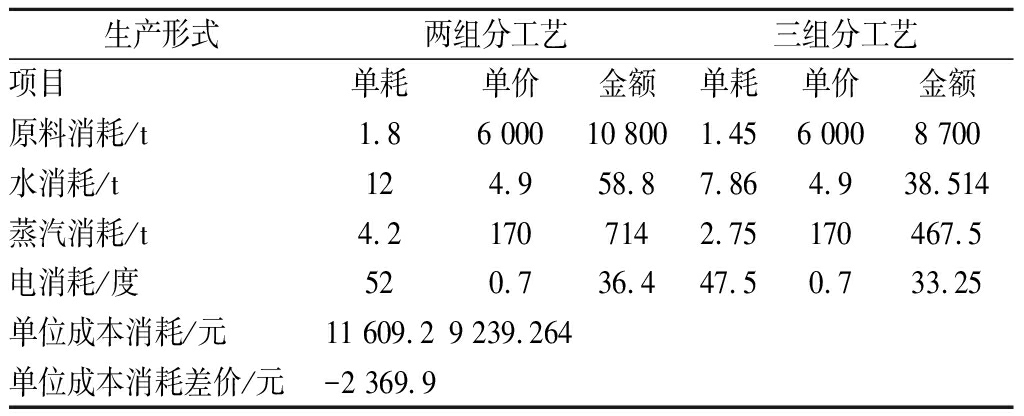
生产形式两组分工艺三组分工艺项目单耗单价金额单耗单价金额原料消耗/t1.86 00010 8001.456 0008 700水消耗/t124.958.87.864.938.514蒸汽消耗/t4.21707142.75170467.5电消耗/度520.736.447.50.733.25单位成本消耗/元11 609.29 239.264单位成本消耗差价/元-2 369.9
从生产成本上来讲,三组分分离工艺比两组分分离工艺节省成本为11 609.2-9 239.264=2 369.9元;以年产1万t结晶麦芽糖醇为例,利用三组分色谱分离技术,每年可以降低的成本为10 000×2 369.9=2 369.9万元,得出结论为在物料相同的条件下,采用三组分分离技术,每年可以多收入2 369.9万元。
3 结论
在色谱进料量相同的条件下,洗脱水的用量是决定产品纯度以及收率高低的关键因素。用水量高则产品的纯度与收率高,用水量低则产品的纯度与收率低。然而,在实际生产过程中,为了获得高附加值或者是高纯度的产品,我们会不惜加大用水量。这无疑会增加色谱的运行成本,色谱三组分技术的应用,不但解决了色谱的水耗问题,而且实现了产品利润的最大化。
杂醇与山梨醇积累,是影响结晶麦芽糖醇结晶收率高低的决定因素。采用色谱三组分分离技术,不但解决了杂醇积累问题,而且可以使结晶收率提升10%,最终完成糖醇加工产业链的深化发展与企业的转型升级[17-20]。
麦芽糖醇中试三组分色谱分离实验的成功,证明该工业化色谱分离技术是可行的,它的成功研发为现代化的企业的发展开辟了一条崭新的工艺路线。
[1] 甜味剂在食品工业中得到广泛应用[J]. 广西糖业, 2017(2):52.
[2] 关于甜味剂的科学解读[J]. 轻工标准与质量, 2016(3):76-76.
[3] 李露露.糖醇在核桃乳中的应用研究[D].无锡:江南大学, 2017.
[4] 赵光辉,修秀红,李玉珍.麦芽糖及麦芽糖醇的生产与应用[C]. 中国国际食品添加剂和配料展览会学术论文集,上海:《中国食品添加剂》杂志社,2011:149-152.
[5] 叶红玲.全酶法制备超高麦芽糖浆工艺的研究[D].合肥:安徽农业大学,2010.
[6] 孙永泰.碎米制备麦芽糖醇工艺[J].粮食加工,2016,41(2):22-23.
[7] 姜维.麦芽糖色谱法分离提纯及结晶的研究[D].广州:华南理工大学,2011.
[8] 贺东海,修秀红,方春雷.麦芽糖醇的功能特性、应用及生产[J].齐鲁工业大学学报(自然科学版),2012,26(1):31-34.
[9] 杨永辉,刘冰,陈雪波.模拟移动床色谱分离技术综述[J].化学通报,2015,78(2):132-139.
[10] 李培.一种麦芽糖醇的制备方法:中国, CN106755212A[P]. 2017-05-31.
[11] 侯静美.麦芽糖醇结晶过程及产品结块机理的研究[D].天津:天津大学, 2012.
[12] 王宜军.麦芽糖醇生产工艺自动控制系统的设计[J].科技与企业,2012(6):249-251.
[13] 黄华国,刘景圣,郑明珠,等.麦芽糖粉末喷雾干燥的研究进展[J].浙江农业科学,2011(4):845-847.
[14] 杨铮. 浅析工业控制系统信息安全现状及未来趋势[C].第三十二届中国(天津)2018’IT、网络、信息技术、电子、仪器仪表创新学术会议论文集,2018:206-209.
[15] 王家军.麦芽糖醇生产工艺自动控制系统的设计[D].青岛:山东轻工业学院,2012.
[16] 杨玉芬,陈啟虎,张永晖,等.化工新型分离技术的研究进展[J].当代化工研究,2010,6(7):9-13.
[17] 孟祥平,张普查.浅谈功能性甜味剂麦芽糖醇的特性及在食品工业中的应用[J].中国食物与营养,2013,19(8):32-34.
[18] 高辉,邹磊.高纯度结晶麦芽糖醇制备工艺的研究[J].中国调味品,2011,36(6):97-99.
[19] 罗建勇,徐丽霞,扶雄,等.结晶麦芽糖性质及其制备工艺[J].粮食与油脂,2011(6):47-49.
[20] 王成福,赵光辉,孙鲁,等.功能糖醇的生产与应用[C].第十六届中国国际食品添加剂和配料展览会学术论文集,上海:《中国食品添加剂》杂志社,2012:192-197.