大菱鲆(Scophthatmus maximus),其英文名为turbot,在中国被音译为“多宝鱼”,俗称欧洲比目鱼。是我国北方沿海重要的养殖经济鱼种之一[1]。2017年我国鲆鱼类养殖总产量达到10.62万t[2]。
蛋白质氧化是指蛋白质分子在ROS(reactive oxygen species)(如![]() 以及H2O2等)的直接作用下,或通过次生氧化产物(包括氢过氧化物、活性醛类等)的间接作用,引起蛋白质结构与功能性质发生改变[3]。蛋白质氧化会导致氨基酸残基形成羰基化合物、蛋白降解及聚合,从而影响到肉类组织的品质。FUENTES等[4]研究发现干腌肉的硬度和蛋白质氧化程度之间存在显著的相关性,还发现肉质的改变是由蛋白的交联引起的。陈霞霞等[5]研究发现羟自由基氧化体系促进银鲳各项理化指标发生了明显的改变。HUFF-LONERGAN等[6]研究发现动物宰后成熟过程中的蛋白质氧化对肉品持水力的改变具有重要的作用。
以及H2O2等)的直接作用下,或通过次生氧化产物(包括氢过氧化物、活性醛类等)的间接作用,引起蛋白质结构与功能性质发生改变[3]。蛋白质氧化会导致氨基酸残基形成羰基化合物、蛋白降解及聚合,从而影响到肉类组织的品质。FUENTES等[4]研究发现干腌肉的硬度和蛋白质氧化程度之间存在显著的相关性,还发现肉质的改变是由蛋白的交联引起的。陈霞霞等[5]研究发现羟自由基氧化体系促进银鲳各项理化指标发生了明显的改变。HUFF-LONERGAN等[6]研究发现动物宰后成熟过程中的蛋白质氧化对肉品持水力的改变具有重要的作用。
目前国内外对肉类蛋白质氧化的研究多集中在畜禽肉上[7-8],而在蛋白质氧化对鱼类等水产品品质影响方面的研究就少。本文以大菱鲆为研究对象,通过测定感官评分、持水性、质构、肌原纤维蛋白羰基含量、总巯基含量、二硫键含量和表面疏水性等指标,并进行相关性分析,探明贮藏过程中蛋白质氧化对大菱鲆鱼肉品质变化的影响机理,以期为鱼肉品质变化机制研究及鱼类保鲜加工提供依据和参考。
1 材料与方法
1.1 材料与仪器
鲜活大菱鲆,2018年5月购于青岛市胶南大场养殖基地,体质量为(1±0.2)kg/条,体表富有光泽、黏液透明、眼球饱满,有水充氧保活运回实验室。
盐酸胍、Na2HPO4、NaH2PO4、乙二胺四乙酸(EDTA)、1-苯奈氨-8-磺酸(ANS)、三羟甲基氨基甲烷(Tris)、NaCl均为分析纯,购于国药集团化学试剂有限公司。
UV1102Ⅱ紫外分光光度计,上海天美科学仪器有限公司;BSA2202S电子天平,北京赛多利科学仪器有限公司;Neofuge 15R高速冷冻离心机,上海力申科学仪器有限公司;TA-XT plus型质构分析仪,英国Stable MicroSystem公司。
1.2 实验方法
1.2.1 样品处理方法
取鲜活大菱鲆放血宰杀后,用刀沿大菱鲆背部和腹部脊柱方向从头到尾划开,将鱼骨两侧鱼片取下,在尾部鱼肉和鱼皮分界处用刀割开,将鱼皮慢慢剥离,取鱼片(85±10) g,用去离子水清洗后沥干,放入聚氯乙烯袋中后密封。所有鱼片随机分为2组,分别进行冷藏(4 ℃)和冰藏(0 ℃),每隔2 d随机选取3袋样品进行检测,根据感官评分结果来确定实验周期。
1.2.2 感官评价
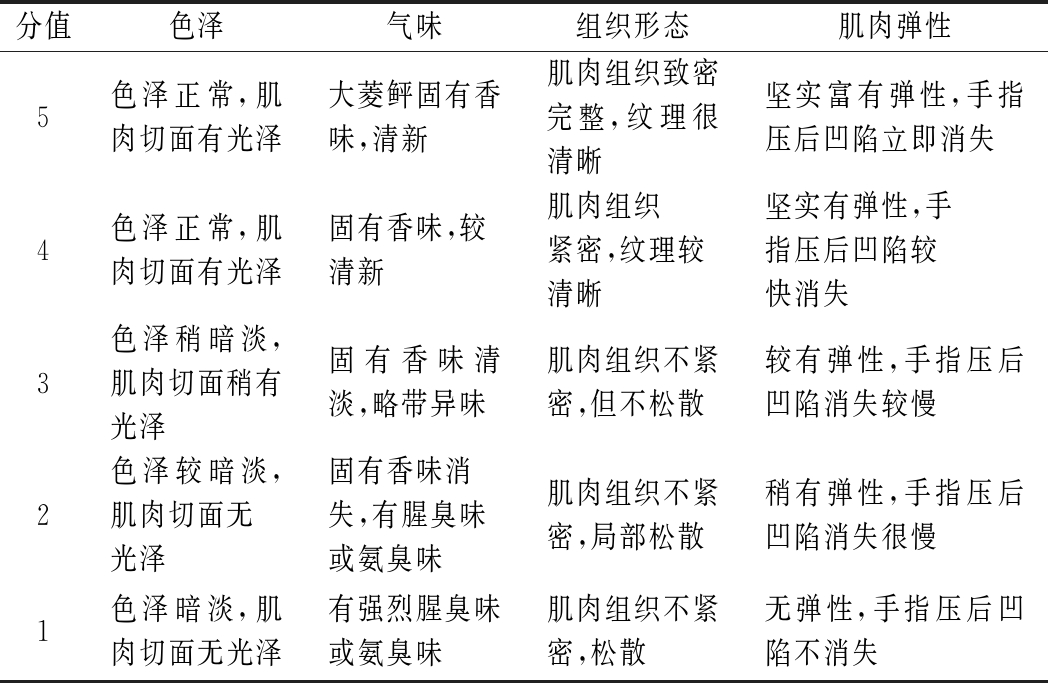
参考王尊等[9]的方法略有改进。10人组成感官评定小组,根据大菱鲆鱼片的色泽、气味、组织形态和肌肉弹性打分评定,最高分和最低分分别为5分和1分,综合得分2分以下的则代表为感官不可接受。
表1 大菱鲆鱼片感官评定评分标准
Table 1 Sensory score standards for turbot fillets
分值色泽气味组织形态肌肉弹性5色泽正常,肌肉切面有光泽大菱鲆固有香味,清新肌肉组织致密完整,纹理很清晰坚实富有弹性,手指压后凹陷立即消失4色泽正常,肌肉切面有光泽固有香味,较清新肌肉组织紧密,纹理较清晰坚实有弹性,手指压后凹陷较快消失3色泽稍暗淡,肌肉切面稍有光泽固有香味清淡,略带异味肌肉组织不紧密,但不松散较有弹性,手指压后凹陷消失较慢2色泽较暗淡,肌肉切面无光泽固有香味消失,有腥臭味或氨臭味肌肉组织不紧密,局部松散稍有弹性,手指压后凹陷消失很慢1色泽暗淡,肌肉切面无光泽有强烈腥臭味或氨臭味肌肉组织不紧密,松散无弹性,手指压后凹陷不消失
1.2.3 质构的测定
参照林婉玲等[10]的方法,将样品切成2 cm×2 cm×1 cm规格,使用质构分析仪进行测定,每组样品做6个平行。
1.2.4 持水性的测定
1.2.4.1 蒸煮损失率的测定
参考张远等[11]的方法略作修改,将样品切成2 cm×2 cm×1 cm规格,称取质量(M1)后装入蒸煮袋,85 ℃水浴15 min,样品的质量(M2)于蒸煮后冷却到室温后再进行称重。按照公式(1)进行蒸煮损失率的计算:
蒸煮损失率![]()
(1)
1.2.4.2 滴水损失率的测定
参考张远等[11]的方法略作修改,将样品切成2 cm×2 cm×1 cm的规格,称取质量(M1),随后用细铁丝将样品的一端钩住,放置到充空气的密封袋内,保持样品垂直向下,不得接触袋子的内壁,密封后,4 ℃静置24 h,取出样品再次称重(M2)。滴水损失率的计算如公式(2):
滴水损失率![]()
(2)
1.2.5 肌原纤维蛋白的提取与几个相关指标测定
1.2.5.1 肌原纤维蛋白的提取
参考CHIN等[12]和PARK等[13]的方法略作改进,取绞碎鱼肉3 g,加入15 mL10 mmol/L Tris-HCl(pH 7.2),8 000 r/min冰浴均质90 s,4 ℃下10 000 r/min离心15 min,取沉淀,加入5倍10 mmol/L Tris-HCl缓冲液(含0.6 mol/L NaCl,pH 7.2),4 ℃下10 000 r/min离心15 min,上清液即为所需肌原纤维蛋白样品,用于下述指标测定分析。
1.2.5.2 羰基含量的测定
参照李学鹏等[14]的方法进行测定。
1.2.5.3 总巯基含量测定
参照赵兵等[15]的方法进行测定。
1.2.5.4 二硫键含量的测定
参考THANNHAUSER等[16]的方法,调整蛋白质浓度为5 g/L,取0.2 mL蛋白液与5 mL新鲜配制的NTSB溶液混合,室温下避光反应30 min,然后在412 nm下测定吸光度值(A),二硫键含量的计算公式如公式(3):
二硫键含量/(nmol·mg-1蛋白质![]()
(3)
式中:A为波长412 nm处的吸光度;n为稀释倍数;ε为摩尔吸光系数13 600/(L·mol·cm)。
1.2.5.5 表面疏水性的测定
参考CHEIH等[17]的方法。向1 L 4 g/L肌原纤维蛋白溶液中加入1 g/L 200 μL溴酚蓝钠(BPB)。空白组用20 mol/L磷酸盐缓冲液(pH 6.0)替代。室温振荡10 min,5 000 r/min离心15 min。取上清液,将其10倍稀释,于 595 nm处测吸光度。疏水性用BPB结合量表示如公式(4):
BPB结合量![]()
(4)
式中:A空白,空白组595 nm处吸光之;A样品,冷藏组或冰藏组样品595nm处的吸光度。
1.3 数据分析
采用SPSS 18.0和Origin 8.5软件对数据统计分析和作图,数据分析采用方差分析(One-way ANOVA)进行显著性分析,P>0.05表示差异性不显著,P<0.05表示差异性显著,P<0.01表示差异性极显著。
2 结果与分析
2.1 冷藏和冰藏条件下大菱鲆鱼片感官评分的变化
大菱鲆宰杀后,由于内源水解酶和外源微生物的作用,导致肌肉组织发生腐败变质。在这个过程中,鱼肉的色泽、气味和组织结构都会发生显著性变化。感官评价是通过人的感觉来鉴别鱼肉品质变化的一种最直观的评价方法[18]。由图1可以看出,随着贮藏时间的延长,冷藏和冰藏条件下大菱鲆鱼片感官评分呈持续下降趋势。贮藏前4 d,2组样品的感官评分差异不显著(P<0.05),从贮藏第6天开始出现明显差异,冷藏组样品的感官评分下降速度明显快于冰藏组,相同贮藏时间内冷藏鱼片的感官评分低于冰藏鱼片。冷藏组和冰藏组样品分别在第8天和第12天时感官不可接受,此时,大菱鲆鱼片表面光泽暗淡、腥臭味较为强烈、肌肉组织松散且无弹性。崔正翠等[19]通过感官评价发现大菱鲆在0 ℃和3 ℃贮藏时其较好品质时间分别433 h和197 h,与本实验的结果相近。因此4 ℃冷藏鱼片和0 ℃冰藏鱼片的实验周期分别设定为10 d和14 d。
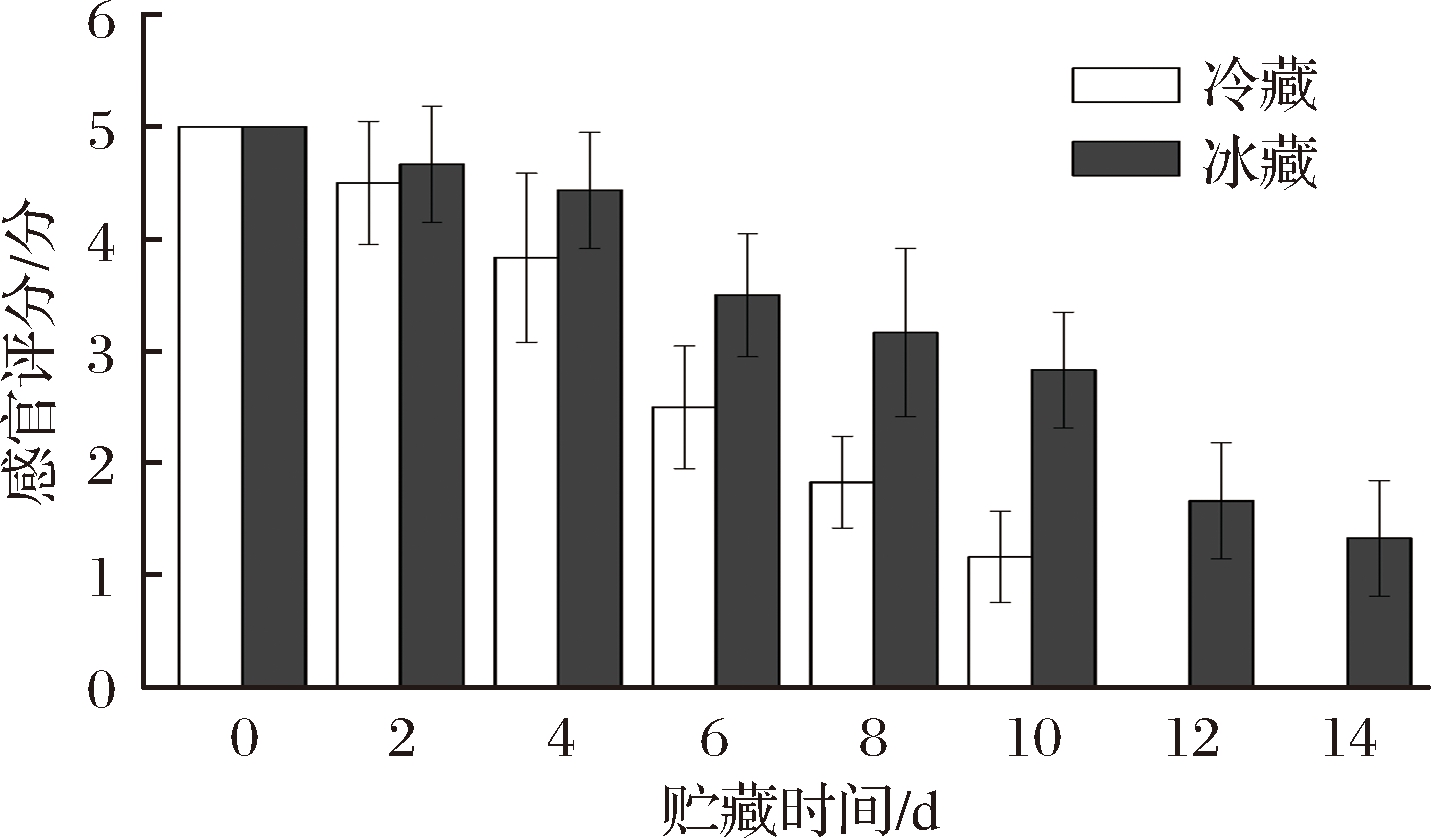
图1 冷藏和冰藏条件下大菱鲆鱼片感官评分的变化
Fig.1 Change in sensory evaluation score of turbot fillets during under refrigerated and ice storage
2.2 冷藏和冰藏条件下大菱鲆鱼片持水性的变化
持水性(water binding capacity or water holding capacity,WHC)是指肌肉组织在贮藏和加工等过程中保持其水分的能力[11]。由图2可以看出,冰藏和冷藏条件下大菱鲆鱼片的蒸煮损失率和滴水损失率均随贮藏时间的延长而逐渐上升,表明2组样品的持水性均呈下降的趋势。主要因为动物死后,肌糖原酵解产生乳酸,pH值下降,肌肉蛋白束缚水分的能力减弱,同时肌肉收缩,导致水分从肌肉中挤出[20]。也有研究表明鱼肉蛋白在贮藏过程中会发生变性及降解,其空间网络结构被破坏,导致肌肉的保水能力下降[21],而低温能够在一定程度上抑制蛋白质变性,从而降低鱼肉水分的损失。邓星星等[22]研究发现白乌鳢肌肉的蒸煮损失率随贮藏时间的延长而升高,并且低温有利于维持肌肉的持水力。王晓君等[23]也发现相同贮藏时间内,0 ℃贮藏下大口鲇鱼肉的持水性要优于4 ℃。
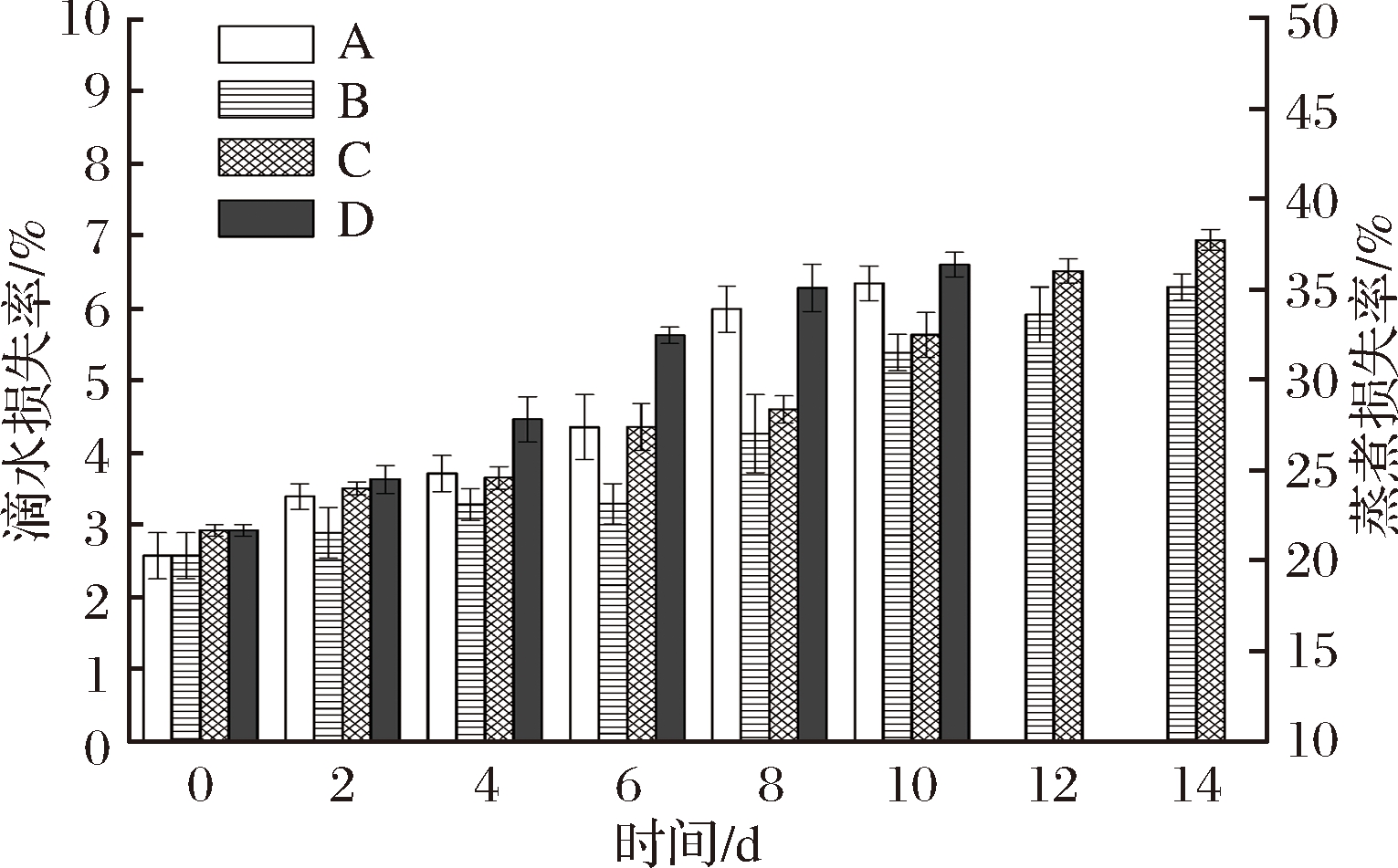
A-冷藏组滴水损失率;B-冰藏组滴水损失率;C-冰藏组蒸煮损失率;D-冷藏组蒸煮损失率
图2 冷藏和冰藏条件下大菱鲆鱼片蒸煮损失率和滴水损失率的变化
Fig.2 Change in cooking loss rate and drip loss rate of turbot fillets during under refrigerated and ice storage
2.3 冷藏和冰藏条件下大菱鲆鱼片质构特性的变化
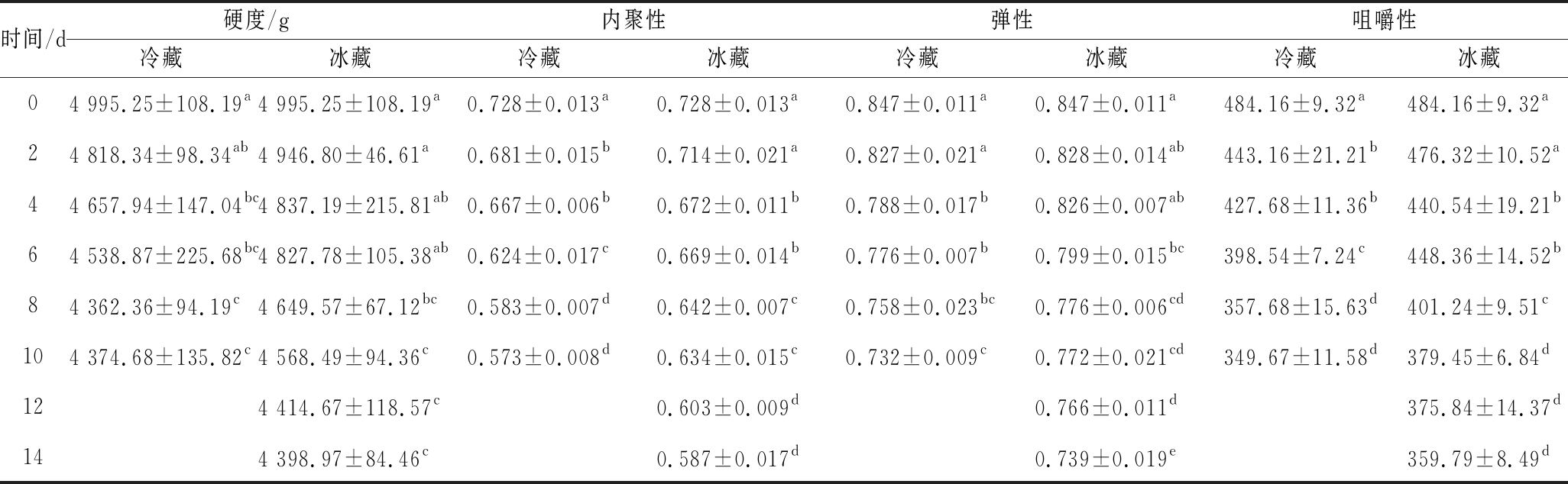
冰藏和冷藏条件下大菱鲆鱼片质构特性的变化如表2所示。随着贮藏时间的延长,2组样品的硬度、弹性和内聚性均呈显著下降趋势(P<0.05)。新鲜大菱鲆鱼片的硬度、内聚性和弹性分别为4 995.25 g、0.728和0.847,冷藏组在贮藏到第10天时分别降至4 374.68 g、0.573和0.732,而冰藏组在贮藏第14天时分别降至4 414.67 g、0.766和0.603。咀嚼性是一项综合评价指标,是肌肉的硬度、内聚性、弹性等共同作用的结果[24]。由表2可知,2组样品的咀嚼性均随储藏时间的延长而逐渐下降,其中冷藏组样品的咀嚼性下降更快,贮藏10天后,鱼肉咀嚼性从初始的484.16下降至349.67,降低了27.78%,而冰藏组在贮藏第10 d时,鱼肉咀嚼性为379.45,降低了21.63%,贮藏14 d后,下降至359.79,较初始值降低了25.69%,表明0 ℃冰藏更利于大菱鲆鱼肉质构品质的保持。这与王晓君等[23]研究0 ℃和4 ℃贮藏下大口鲇质构品质变化结果相似。
2.4 冷藏和冰藏条件下大菱鲆鱼片羰基含量的变化
羰基(醛基和酮基等)是蛋白质氧化过程中产生的重要成分,被广泛应用于评估蛋白质的氧化程度[25]。由图3可以看出,随着贮藏时间的延长,两组样品的羰基含量均呈增加的趋势,表明在冷藏和冰藏过程中大菱鲆鱼片蛋白质均发生了不同程度的氧化,并且随贮藏时间越长,蛋白质氧化程度越严重。大菱鲆鱼片羰基的初始含量为1.32 nmol/mg蛋白质,试验开始2天羰基含量增加较缓慢,2 d后开始显著上升,并且冷藏组羰基含量上升速度明显快于冰藏组。表明冰藏能延缓鱼肉蛋白质氧化,因为贮藏温度越低,肌肉中的各类化学反应速度越慢,在一定程度上延缓了肌原纤维蛋白的氧化变性,同时低温抑制微生物的生长和酶的活性,从而抑制蛋白质降解以及肽键断裂,羰基含量上升速度减慢。LU等[26]研究发现贮藏过程中鱼肉羰基含量逐渐增加,并且微冻组鱼肉羰基含量的上升速度低于冷藏组。PASSI等[27]也发现在冰藏过程中鱼肉羰基含量明显升高。大菱鲆鱼片羰基的整体变化趋势与感官评价的趋势相近,蛋白质氧化裂解会生成醛、酮类等挥发性物质,鱼体气味发生改变,进而影响感官评分。FENG等[28]研究发现,辐照处理牛肉中醛类和酮类挥发性物质的生成与蛋白质氧化显著相关。徐永霞等[29]研究发现,冷藏过程中大菱鲆中醛类和酮类物质发生明显改变。
表2 冷藏和冰藏条件下大菱鲆鱼片质构特性的变化
Table 2 Change in texture characteristics of turbot fillets during under refrigerated and ice storage
时间/d硬度/g内聚性弹性咀嚼性冷藏冰藏冷藏冰藏冷藏冰藏冷藏冰藏04 995.25±108.19a4 995.25±108.19a0.728±0.013a0.728±0.013a0.847±0.011a0.847±0.011a484.16±9.32a484.16±9.32a24 818.34±98.34ab4 946.80±46.61a0.681±0.015b0.714±0.021a0.827±0.021a0.828±0.014ab443.16±21.21b476.32±10.52a44 657.94±147.04bc4 837.19±215.81ab0.667±0.006b0.672±0.011b0.788±0.017b0.826±0.007ab427.68±11.36b440.54±19.21b64 538.87±225.68bc4 827.78±105.38ab0.624±0.017c0.669±0.014b0.776±0.007b0.799±0.015bc398.54±7.24c448.36±14.52b84 362.36±94.19c4 649.57±67.12bc0.583±0.007d0.642±0.007c0.758±0.023bc0.776±0.006cd357.68±15.63d401.24±9.51c104 374.68±135.82c4 568.49±94.36c0.573±0.008d0.634±0.015c0.732±0.009c0.772±0.021cd349.67±11.58d379.45±6.84d124 414.67±118.57c0.603±0.009d0.766±0.011d375.84±14.37d144 398.97±84.46c0.587±0.017d0.739±0.019e359.79±8.49d
注:同列数据上标不同英文字母表示有显著性差异(P <0.05)。
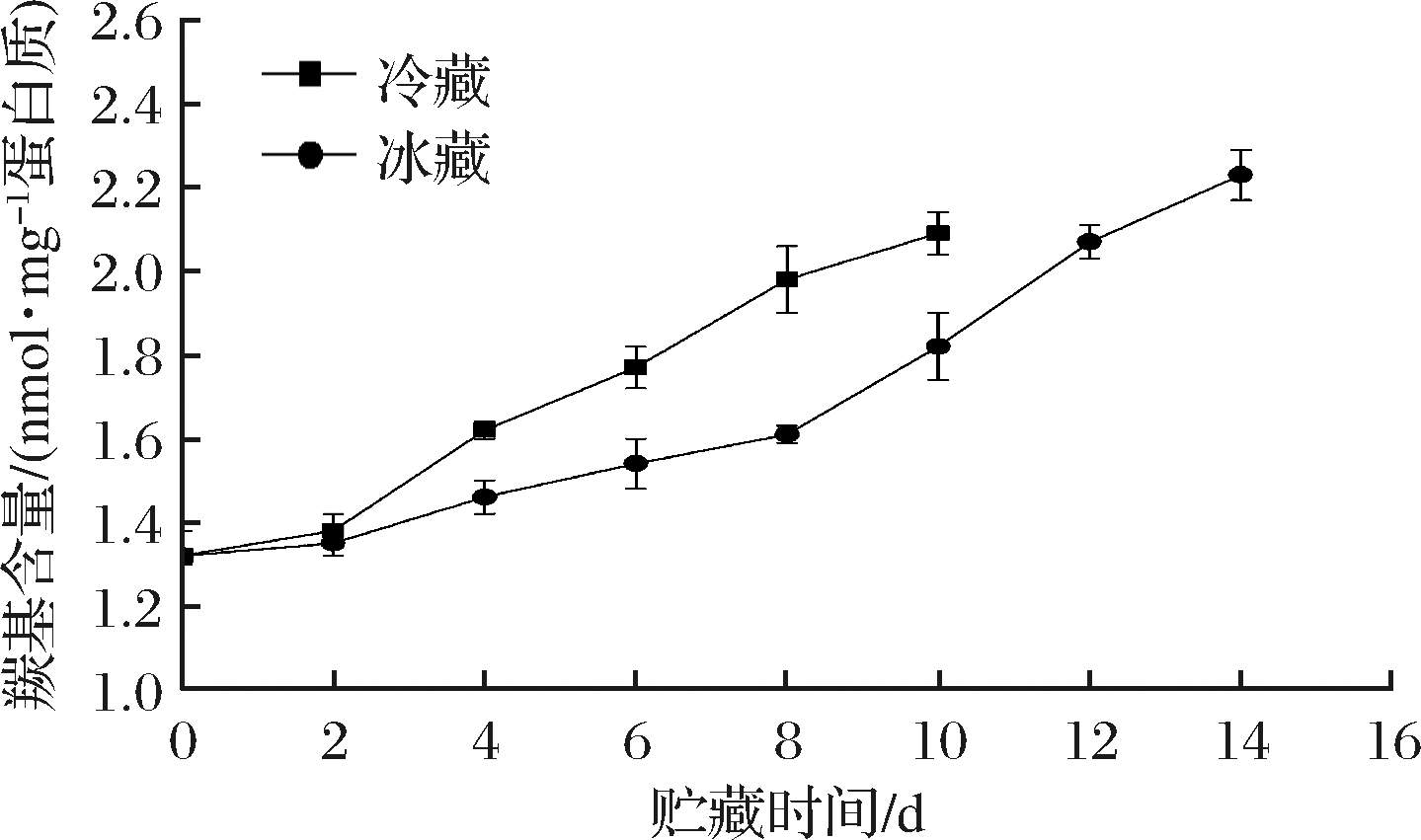
图3 冷藏和冰藏条件下大菱鲆鱼片羰基含量的变化
Fig.3 Change in carbonyl content of turbot fillets during under refrigerated and ice storage
2.5 冷藏和冰藏条件下大菱鲆鱼片总巯基和二硫键含量的变化
2个巯基脱氢可形成双硫键,引起蛋白质分子间交联、聚合,进而导致肌原纤维蛋白空间结构发生变化[30]。由图4曲线图可以看出,随着贮藏时间的延长,冷藏和冰藏条件下大菱鲆鱼片肌原纤维蛋白的总巯基含量呈现显著下降趋势(P<0.05)。冷藏组样品和冰藏组样品的巯基含量总体分别下降了33.13%和29.4%。由图4柱形图可以看出,2组样品肌原纤维蛋白的二硫键含量随着贮藏时间的延长而显著上升(P<0.05)。研究表明,在低温贮藏过程中,肌原纤维蛋白会发生构象变化,埋藏在分子内部的疏基暴露出来,进而氧化生成二硫键,从而导致总巯基含量减少、二硫键含量上升[31]。由图4还可以看出,冷藏大菱鲆鱼片巯基含量的下降速率以及二硫键的升高速率明显快于冰藏组。因此,冰藏处理比冷藏处理更好地保护蛋白质免受氧化变性。研究表明蛋白质氧化生成二硫键等蛋白交联化合物,会强化肌原纤维蛋白的结构,对肉的硬度和嫩度都具有重要的影响[32-33]。
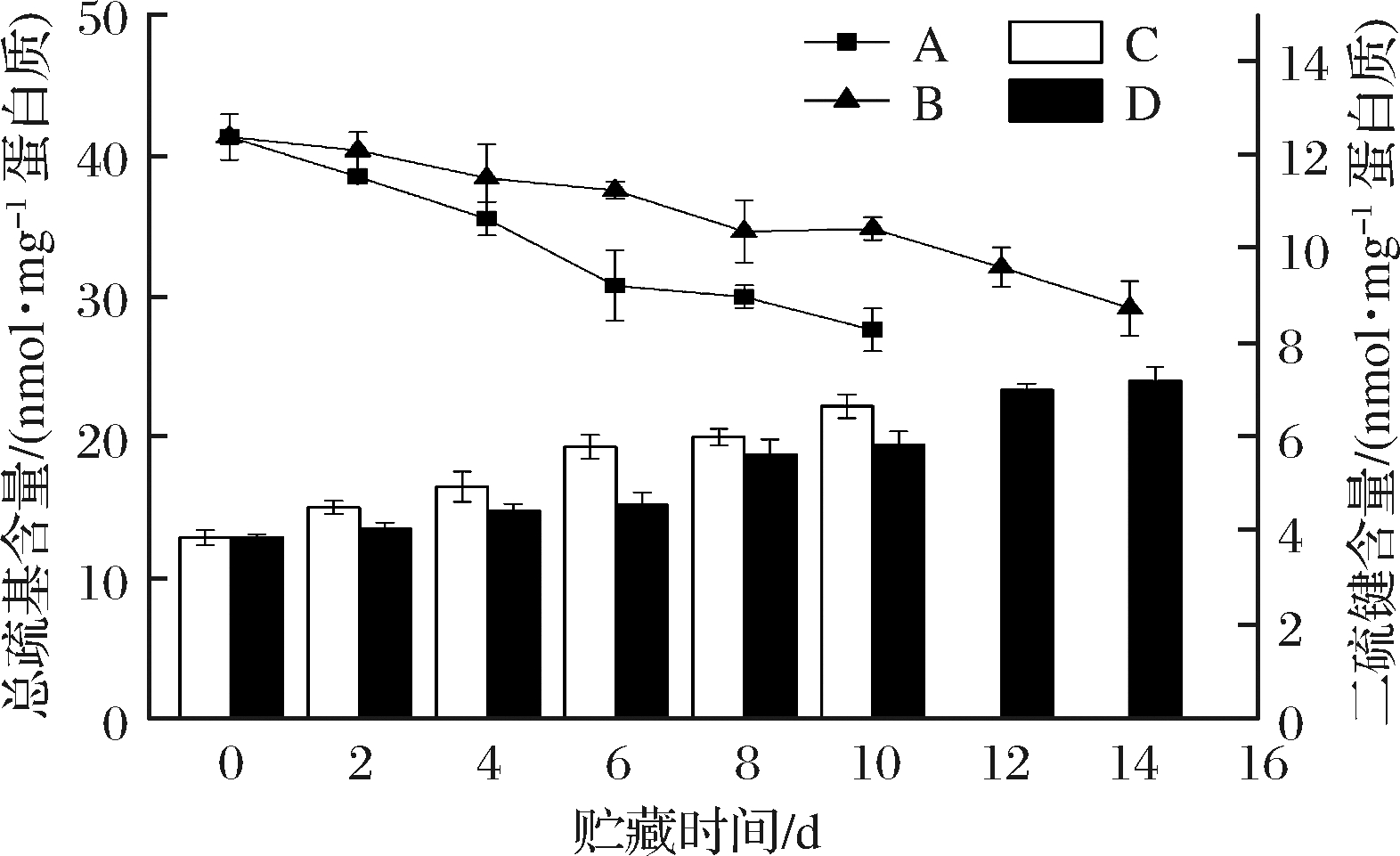
A-冷藏组巯基含量;B-冰藏组巯基含量;C-冰藏组二硫键含量;D-冷藏组二硫键含量
图4 冷藏和冰藏条件下大菱鲆鱼片总巯基含量和二硫键含量的变化
Fig.4 Change in total sulfhydryl content and disulfide content of turbot fillets during under refrigerated and ice storage
2.6 冷藏和冰藏条件下大菱鲆鱼片表面疏水性的变化
蛋白质的表面疏水性反映的是蛋白质分子表面疏水性氨基酸的相对含量,可以用来反映蛋白质分子构象变化情况。由图5可知,随着贮藏时间的延长,冰藏和冷藏条件下大菱鲆鱼片肌原纤维蛋白的表面疏水性均呈上升趋势。这可能是因为贮藏过程中鱼肉肌原纤维蛋白发生氧化变性,蛋白分子逐渐伸展,空间构象改变,亲水基团和疏水基团的相对位置发生改变,疏水性脂肪族和芳香族氨基酸残基暴露出来,从而导致蛋白质疏水性增加[34]。由图5还可以看出,冷藏组前6 d及冰藏组前8 d肌原纤维蛋白的表面疏水性快速升高,之后缓慢上升,这可能是因为肌原纤维蛋白表面疏水基团在疏水相互作用下发生了蛋白质聚集[35]。

图5 冷藏和冰藏条件下大菱鲆鱼片表面疏水性的变化
Fig.5 Change in surface hydrophobicity of turbot fillets during under refrigerated and ice storage
此外,在相同的贮藏时间内,冰藏组样品肌原纤维蛋白的表面疏水性低于冷藏组,表明冰藏更有利于保持肌原纤维蛋白的空间结构。大菱鲆鱼片表面疏水整体变化趋势与蒸煮损失率和滴水损失率的趋势相近,TRAORE等[36]研究发现猪肉蛋白质氧化与滴水损失存在相关性,表明蛋白质氧化能够引起肉持水性的下降。
2.7 相关性分析
冷藏和冰藏过程中大菱鲆鱼片蛋白质氧化和品质指标间的相关性如表3和表4所示,由表中可以看出,4 ℃冷藏条件下,除二硫键含量外,大菱鲆鱼肉蛋白质氧化指标与感官评分之间显著线性相关(P<0.05)。鱼肉蛋白质氧化指标均与滴水损失率、硬度和咀嚼性显著相关(P<0.05),与蒸煮损失率极显著相关(P<0.01)。0 ℃冰藏条件下,大菱鲆鱼肉蛋白质氧化指标均与感官评分和持水性指标(滴水损失率和蒸煮损失率)之间显著性相关(P<0.05)。对于质构而言,大菱鲆鱼肉蛋白质氧化指标均与硬度极显著相关(P<0.01),与弹性和咀嚼性显著相关(P<0.05)。另外,除总巯基含量外,鱼肉内聚性与其他蛋白质氧化指标显著相关(P<0.05)。总体来说在冷藏和冰藏条件下,大菱鲆鱼片蛋白质氧化与感官评分、持水性以及质构特性之间存在良好的线性相关性。
表3 冷藏条件下大菱鲆鱼片蛋白质氧化与品质指标的相关性分析
Table 3 Correlation between protein oxidation and quality indicators of turbot fillets under refrigerated storage

感官评分滴水损失率蒸煮损失率硬度内聚性弹性咀嚼性羰基含量总巯基含量二硫键含量表面疏水性感官评分1-0.910**-0.893**0.827*0.861**0.929**0.846*-0.870**0.835*-0.786-0.865**滴水损失率10.882**-0.967**-0.827*-0.881**-0.829*0.897**-0.885**0.830*0.941**蒸煮损失率1-0.929**-0.785-0.826*-0.881**0.887**-0.893**0.874**0.933**硬度10.882**0.816*0.892**-0.813*0.814*-0.930**-0.879**内聚性10.7520.818*-0.7670.762-0.821*-0.860**弹性10.957**-0.836*0.874**-0.866**-0.788咀嚼性1-0.869**0.813*-0.879**-0.817*羰基含量1-0.913**0.864**0.961**总巯基含量1-0.966**-0.832*二硫键含量10.889**表面疏水性1
注:*表示显著相关(P<0.05);**表示极显著相关(P<0.01)。下同。
3 结论
随着贮藏时间的延长,冷藏和冰藏条件下大菱鲆鱼肉均发生了蛋白质氧化,同时鱼肉品质逐渐劣化,并且贮藏温度越低,大菱鲆肌肉蛋白质氧化程度越低,鱼肉品质保持得越好,相关性分析表明在冷藏和冰藏条件下大菱鲆鱼肉各项品质指标与蛋白质氧化指标均存在良好的线性相关性。显示贮藏过程中大菱鲆鱼肉品质变化与蛋白质氧化密切相关,但蛋白质氧化对鱼肉品质变化的作用机理以及实际加工过程中蛋白质氧化控制利用技术还需要进一步深入研究。
表4 冰藏条件下大菱鲆鱼片蛋白质氧化与品质指标的相关性分析
Table 4 Correlation between protein oxidation and quality indicators of turbot fillets under ice storage
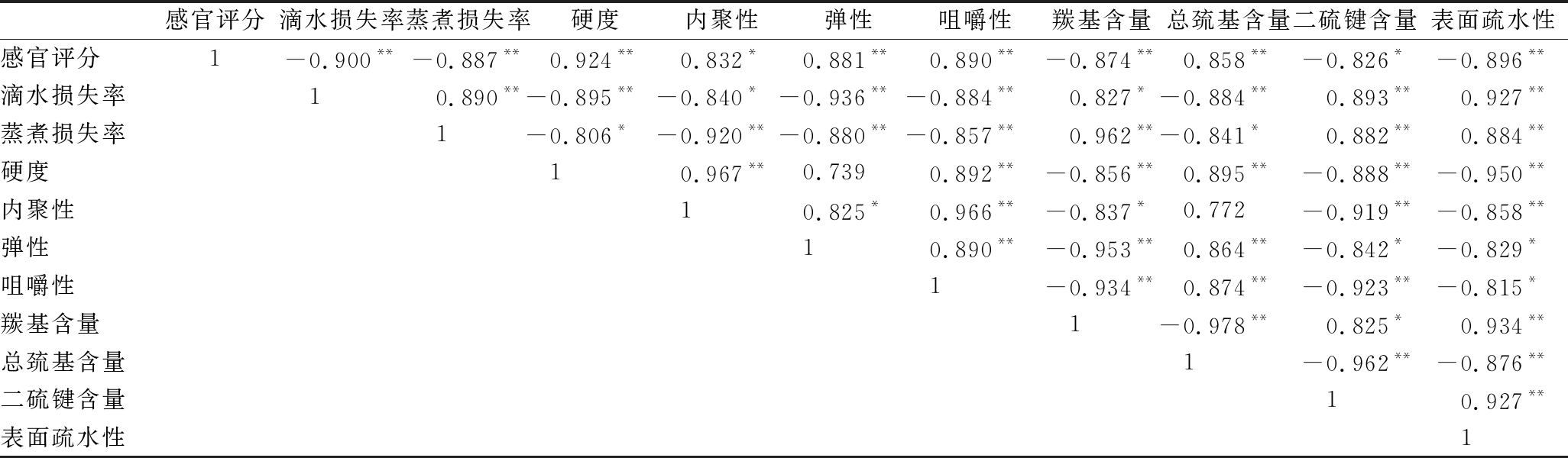
感官评分滴水损失率蒸煮损失率硬度内聚性弹性咀嚼性羰基含量总巯基含量二硫键含量表面疏水性感官评分1-0.900**-0.887**0.924**0.832*0.881**0.890**-0.874**0.858**-0.826*-0.896**滴水损失率10.890**-0.895**-0.840*-0.936**-0.884**0.827*-0.884**0.893**0.927**蒸煮损失率1-0.806*-0.920**-0.880**-0.857**0.962**-0.841*0.882**0.884**硬度10.967**0.7390.892**-0.856**0.895**-0.888**-0.950**内聚性10.825*0.966**-0.837*0.772-0.919**-0.858**弹性10.890**-0.953**0.864**-0.842*-0.829*咀嚼性1-0.934**0.874**-0.923**-0.815*羰基含量1-0.978**0.825*0.934**总巯基含量1-0.962**-0.876**二硫键含量10.927**表面疏水性1
[1] 雷霁霖,梁萌青,刘新富,等. 大菱鲆营养成分与食用价值研究概述[J]. 海洋水产研究, 2008, 29(4): 112-115.
[2] 徐乐俊,吕永辉,高宏泉,等. 中国渔业统计年鉴[M]. 北京:中国农业出版社, 2018: 26.
[3] ESTEVEZ M. Protein carbonyls in meat systems: A review[J]. Meat Science, 2011, 89(3): 259-279.
[4] FUENES V, VENTANAS J, MORCUENDE D, et al. Lipid and protein oxidation and sensory properties of vacuum-packaged dry-cured ham subjected to high hydrostatic pressure[J]. Meat Science, 2010, 85(3): 506-514.
[5] 陈霞霞,杨文鸽,吕梁玉,等. 羟自由基氧化体系对银鲳肌原纤维蛋白生化特性及其构象单元的影响[J]. 食品科学, 2016, 37(23): 135-141.
[6] HUFF-LONERGAN E, LONERGAN S M. Mechanisms of water-holding capacity of meat: The role of postmortem biochemical and structural changes[J]. Meat Science, 2005, 71(1): 194-204.
[7] DELLES R M, XIONG Y L. The effect of protein oxidation on hydration and water-binding in pork packaged in an oxygen-enriched atmosphere[J]. Meat Science, 2014, 97(2): 181-188.
[8] ROWE L J, MADDOCK K R, LONERGAN S M, et al. Influence of early postmortem protein oxidation on beef quality[J]. Journal of Animal Science, 2004, 82(3): 785-796.
[9] 王尊,谢晶,钱韻芳. 带鱼冷藏过程中品质变化与水分迁移的相关性[J]. 食品科学, 2017,38(13): 263-268.
[10] 林婉玲,杨贤庆,李来好,等. 脆肉鲩质构与感官评价的相关性研究[J]. 现代食品科技, 2013,29(1): 1-7.
[11] 张远,赵改名,黄现青,等. 性别对猪肉品质特性的影响[J]. 食品科学, 2014, 35(7): 48-52.
[12] CHIN K B, GO M Y, XIONG Y L. Konjac flour improved textural and water retention properties of transglutaminase-mediated, heat-induced porcine myofibrillar protein gel: Effect of salt level and transglutaminase incubation[J]. Meat Science, 2009, 81(3): 565-572.
[13] PARK D, XIONG Y L, ALDERTON A L. Concentration effects of hydroxyl radical oxidizing systems on biochemical properties of porcine muscle myofibrillar protein[J]. Food Chemistry, 2007, 101(3): 1 239-1 246.
[14] 李学鹏,王祺,周凯,等. 丙烯醛氧化对大黄鱼肌肉组织和肌原纤维蛋白结构性质的影响[J]. 现代食品科技, 2014,30(10): 1-7.
[15] 赵冰,李素,张顺亮,等. 蛋白质氧化对肌原纤维蛋白凝胶构效关系的影响[J]. 食品科学, 2018, 39(3): 55-61.
[16] THANNHAUSER T W, THEODORE W. Analysis for disulfide bonds in peptides and proteins[J]. Methods in Enzymology, 1987, 143(1): 115-119.
[17] CHELH I, GATELLIER P, SANTELHOUTELLIER V. Technical note: A simplified procedure for myofibril hydrophobicity determination[J]. Meat Science, 2006, 74(4): 681-683.
[18] KIM Y M, PAIK H D, LEE D S. Shelf-life characteristics of fresh oysters and ground beef as affected by bacteriocin-coated plastic packaging film[J]. Journal of the Science of Food and Agriculture, 2002, 82(9): 998-1 002.
[19] 崔正翠,许钟,杨宪时,等. 大菱鲆冷藏过程中的鲜度变化与货架期[J]. 食品科学, 2011, 32(2): 285-289.
[20] 王文娟,汪水平,李代金,等. 不同贮藏温度齐口裂腹鱼肌肉品质的变化及货架期预测[J]. 食品科学, 2014, 35(14): 229-233.
[21] DASLVA C C, M RSICO E T, RIBEIRO R O R, et al. Studies of the effect of sodium tripolyphosphate on frozen shrimp by physicochemical analytical methods and low field nuclear magnetic resonance(LF 1H NMR)[J]. LWT-Food Science and Technology, 2013, 50(2): 401-407.
RSICO E T, RIBEIRO R O R, et al. Studies of the effect of sodium tripolyphosphate on frozen shrimp by physicochemical analytical methods and low field nuclear magnetic resonance(LF 1H NMR)[J]. LWT-Food Science and Technology, 2013, 50(2): 401-407.
[22] 邓星星,雷骆,杨合霖,等. 不同贮藏温度及时间对白乌鳢肌肉品质及营养成分的影响[J]. 食品与发酵工业,2019,45(14):170-176.
[23] 王晓君,沈秋霞,卢朝婷,等. 不同贮藏温度下南方大口鲇品质的变化[J]. 食品与发酵工业, 2018, 44(11): 249-254.
[24] 徐永霞,张朝敏,赵佳美,等. 微冻和冷藏对牙鲆贮藏品质的影响[J]. 食品工业科技, 2016, 37(4): 337-341.
[25] CHAMBA M V M, HUA Y, KATIYO W. Oxidation and structural modification of full-fat and defatted flour based soy protein isolates induced by natural and synthetic extraction chemicals[J]. Food Biophysics, 2014, 9(3): 193-202.
[26] LU H, WANG H, LUO Y. Changes in protein oxidation, water holding capacity, and texture of bighead carp(Aristichthys Nobilis) fillets under chilled and partial frozen storage[J]. Journal of Aquatic Food Product Technology, 2016, 26(5): 565-577.
[27] PASSI S, CATAUDELLA S, TIANO L, et al. Dynamics of lipid oxidation and antioxidant depletion in Mediterranean fish stored at different temperatures[J]. Biofactors, 2010, 25(1-4): 241-254.
[28] FENG X, AHN D U. Volatile profile, lipid oxidation and protein oxidation of irradiated ready-to-eat cured turkey meat products[J]. Radiation Physics and Chemistry, 2016, 127: 27-33.
[29] 徐永霞,刘滢,姜程程,等. 电子鼻结合气质联用法分析大菱鲆冷藏过程中挥发性成分变化[J]. 食品与发酵工业, 2014, 40(1): 193-197.
[30] 吴伟. 蛋白质氧化对大豆蛋白结构和凝胶性质的影响[D]. 无锡:江南大学, 2010.
[31] BALANGE A K, BENJAKUL S. Cross-linking activity of oxidised tannic acid towards mackerel muscle proteins as affected by protein types and setting temperatures[J]. Food Chemistry, 2010, 120(1): 268-277.
[32] SOLADOYE O P, JUAREZ M L, AALHUS J L, et al. Protein oxidation in processed meat: Mechanisms and potential implications on human health[J]. Comprehensive Reviews in Food Science and Food Safety, 2015, 14(2): 106-122.
[33] LUND M N, HEINONEN M, BARON C P, et al. Protein oxidation in muscle foods: A review[J]. Molecular Nutrition and Food Research, 2011, 55(1): 83-95.
[34] BADII F, HOWELL N K. A comparison of biochemical changes in cod (Gadus morhua) and haddock (Melanogrammus aeglefinus) fillets during frozen storage[J]. Journal of the Science of Food and Agriculture, 2002, 82(1): 87-97.
[35] LEELAPONGWATTANA K, BENJAKUL S, VISESSANGUAN W, et al. Physicochemical and biochemical changes during frozen storage of minced flesh of lizardfish (Saurida micropectoralis)[J]. Food Chemistry, 2005, 90(1-2): 141-150.
[36] TRAORE S, AUBRY L, GATELLIER P, et al. Effect of heat treatment on protein oxidation in pig meat[J]. Meat Science, 2012, 91(1): 14-21.