食品风味物质从食品向聚合物包装材料中的传质分为吸附和扩散2个步骤,主要通过分配系数和扩散系数来表征[1-4]。风味物质在食品相和聚合物相间的分配系数,表达了风味物质在两相间的分配关系,主要依赖于风味物质的极性和两相介质的极性[5-6]。风味物质在聚合物中的扩散系数,表达了风味物质在聚合物中的扩散速率,主要依赖于储存温度、风味物质特性、聚合物材料特性等因素[7-10]。其中,温度是影响风味物质吸附扩散过程的重要环境变量[11]。蒸馏、热灌装、杀菌、微波加热和袋蒸煮加工等通过提高温度的食品加工技术,会对食品的风味物质在聚合物包装中的传质产生影响,从而改变食品的品质[12-13]。随着先进分析仪器的发展,顶空固相微萃取、气相色谱质谱联用法(chromatography-mass spe-ctrometer,GC-MS)、液相色谱-质谱/质谱联用法、电子鼻测定法等仪器测定法已广泛用于分析风味物质在聚合物中的吸附扩散行为[14-19]。
本文主要利用顶空固相微萃取和气相色谱质谱联用法,使用双面薄膜浸泡法吸附实验,研究了不同储存温度对D-柠檬烯、月桂烯、己酸乙酯、2-壬酮、芳樟醇5种风味物质在聚乙烯薄膜中分配系数和扩散系数的影响。
1 材料与方法
1.1 实验材料
1.1.1 实验材料与试剂
低密度聚乙烯(low density polyethylene,LDPE)包装薄膜,厚47.76 μm,密度0.912 g/cm3,由台州市某塑料有限公司提供;D-柠檬烯(D-LE,分析纯)、2-壬酮(2-NO,分析纯)和芳樟醇(LO,分析纯),Macklin公司;己酸乙酯(EH,分析纯)、月桂烯(ME,分析纯),分别采购自TCI和阿拉丁公司;无水乙醇(化学纯)、正己烷(分析纯),天津元立化工公司。
1.1.2 实验仪器
固相萃取头(50/30 μm DVB/CAR/PDMS),美国Supelco公司;气质联用色谱仪(GC-MS-QP 2010),日本岛津仪器公司;恒温磁力搅拌器(IKA ETS-D5),德国IKA公司;数控超声波水浴箱(KH-600 DB),昆山禾创超声仪器有限公司;恒温恒湿试验机(ETH-408-40-CP-AR),苏州巨孚仪器公司。
1.2 实验方法
1.2.1 食品模拟液稳定性测定
将D-柠檬烯、月桂烯、己酸乙酯、2-壬酮、芳樟醇5种风味物质分别以质量浓度500 mg/L一起配制于体积分数为10 %的乙醇水溶液[11]中,均匀混合后制成食品模拟液备用。在15 mL的顶空瓶中,加入5 mL配制好的食品模拟液,50 ℃温度下平衡处理30 min,转速220 r/min;而后插入固相萃取头,50 ℃温度下吸附萃取30 min,转速220 r/min,之后进行第1次GC-MS测定。将20 mL食品模拟液样品密封在20 mL样品瓶中,放置于4、23、40、64 ℃四种储存温度下15 d后取出,进行第2次GC-MS检测。用第2次检测的峰面积除以第1次检测的峰面积,得到各风味物质在食品模拟液中的保留率。每次检测值均为测量5次求平均值。
1.2.2 吸附实验设计
吸附实验采用双面薄膜浸泡法,首先对LDPE薄膜进行酒精快速擦拭处理备用。而后,将尺寸为5 cm×3 cm的LDPE薄膜片材放置于装有20 mL配制好的食品模拟液的样品瓶中,使用聚四氟乙烯垫片的瓶盖旋紧后,再用密封膜缠绕[20]。不同温度下储存一定时间后取出吸附薄膜,用试纸擦拭至干。将吸附薄膜剪碎后,置于装有20 mL正己烷的样品瓶中密封,而后放置于超声波水浴箱中以60 Hz频率常温超声萃取1 h。最后将萃取完成的待测液静置24 h后,取1 μL的待测液进行GC-MS测定。
1.2.3 GC-MS实验条件
测定萃取液中的吸附量时,采用DB-5石英毛细管柱(30 m×0.25 mm×0.25 μm)和氢火焰离子化检测器。测定食品模拟液中风味物质的稳定性时,因为气体进样中含极性水分子,故选择BR-SWax(30 m×0.32 mm×0.50 μm)色谱柱进行检测,其他条件相同。进样口温度为250 ℃,分流进样,分流比为20∶1,离子源温度为200 ℃。柱温采用程序升温的方式,初始温度为40 ℃,保持3 min,以4 ℃/min的速率升温至150 ℃,保持1 min,再以8 ℃/min升温至250 ℃,保持6 min[11,19]。
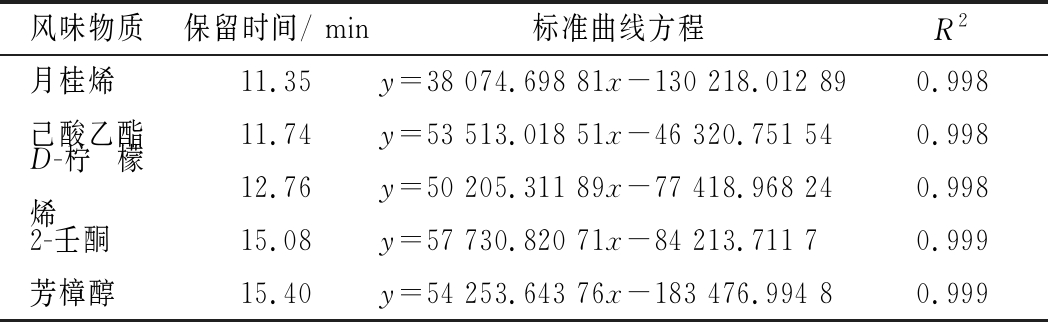
采用外标法进行GC-MS定量分析,将5种风味物质标样以质量浓度5、10、50、100、200 μL/L配置于正己烷溶液中,用进样器取样后分别进样,经过GC-MS仪器分析,得到各风味物质的峰面积,通过线性拟合后获得风味物质的标准曲线方程,见表1。将测定液中各风味物质的峰面积代入标准曲线方程中,通过计算可得到测定液中风味物质的实际浓度。
表1 五种风味物质的标准曲线方程
Table 1 Standard curve equations of five flavors
风味物质保留时间/ min标准曲线方程R2月桂烯11.35y=38 074.698 81x-130 218.012 890.998己酸乙酯11.74y=53 513.018 51x-46 320.751 540.998D-柠檬烯12.76y=50 205.311 89x-77 418.968 240.9982-壬酮15.08y=57 730.820 71x-84 213.711 70.999芳樟醇15.40y=54 253.643 76x-183 476.994 80.999
1.3 数据处理
1.3.1 吸附量计算
t时刻单位质量包装薄膜吸附风味物质的量Mi,t由公式(1)计算获得:
(1)
式中:mi,t,t时刻包装薄膜吸附风味物质i的量,mg;Ci,t,t时刻GC-MS检测出的萃取液中风味物质i的浓度,mL/mL;VE,萃取液的体积,mL;mP,LDPE薄膜萃取面积的质量,g。
1.3.2 分配系数计算
分配系数KP,F是平衡时风味物质在薄膜中的浓度与在食品模拟液中的浓度之比[21],其计算如公式(2):
(2)
式中:CP,e,平衡时薄膜中风味物质的质量浓度,mg/g;CF,e,平衡时食品模拟液中风味物质的质量浓度,mg/g;CF,0,食品模拟液中风味物质的初始质量浓度,mL/L;VS,吸附实验食品模拟液的体积,L。
1.3.3 扩散系数计算
Fick第二定律可用于描述风味物质在LDPE薄膜中的吸附扩散过程,经过长时间吸附后风味物质被包装薄膜吸附量的数学模型[1]如公式(3):
(3)
式中:Mi,e,平衡时薄膜吸附风味物质i的吸附量,mg/g;L,薄膜厚度,cm;D,风味物质在薄膜中的扩散系数,cm2/s。扩散系数D可用最小二乘法基于数学模型公式(3)拟合实验数据获得。
2 结果与分析
2.1 不同温度下风味物质在食品模拟液中的稳定性
将D-柠檬烯、月桂烯、己酸乙酯、2-壬酮、芳樟醇5种风味物质分别以质量浓度为500 mg/L一起配制于体积分数为10 %的乙醇水溶液中,均匀混合后放置于4、23、40、64 ℃四种储存温度下15 d后,测定分析不同温度下风味物质在食品模拟液中的稳定性。在预实验中,选择蒸馏水、体积分数为3%的乙酸溶液、体积分数为10 %乙醇溶液和植物油作为食品模拟液[20],发现5种风味物质在10%乙醇溶液中被LDPE薄膜吸附量均最大,其次是3 %乙酸溶液,再者是蒸馏水,植物油中风味物质被薄膜吸附量最小,因此选用10 %乙醇溶液作为食品模拟液来研究LDPE薄膜的吸附特性。因为10 %乙醇水溶液是水性模拟液,不能直接进样GC-MS,故采用固相微萃取的方法进行取样测定。经过GC-MS测定计算得到各风味物质在食品模拟液中的保留率(图1)。
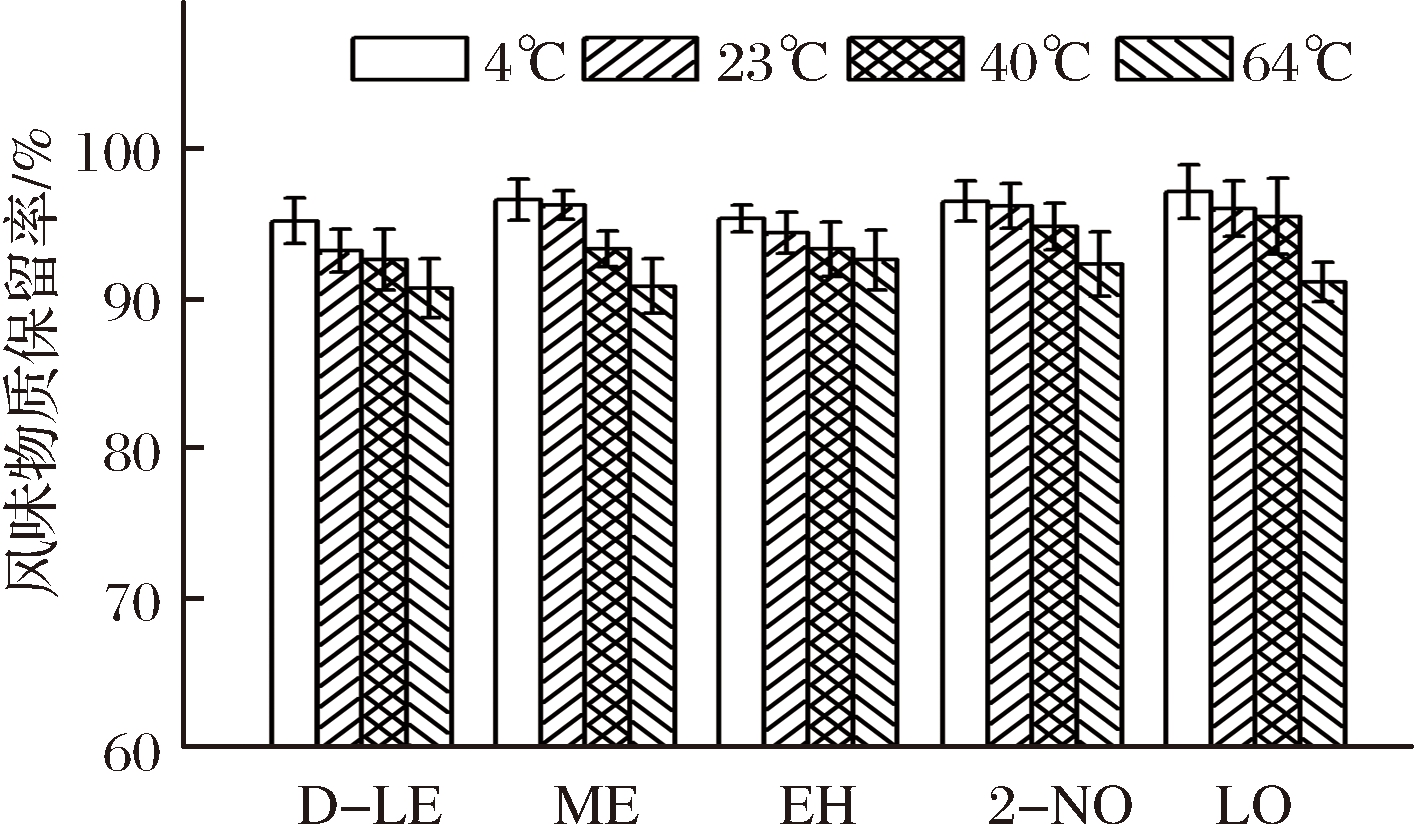
图1 五种风味物质在食品模拟液中的保留率
Fig.1 Retention rate of five flavor substances in food simulator
图1中,5种风味物质在10 %乙醇水溶液中均具有较好的稳定性,储存一定时间后,风味物质的浓度均有所减小,但是保留率都高于90 %。随着储存温度的升高,风味物质在食品模拟液中的保留率均降低,其中芳樟醇在4 ℃下保留率最高,达97.20%,D-柠檬烯在64 ℃下保留率最低,只有90.72 %。较高的储存温度,加速了风味物质在食品模拟液中的扩散,风味物质有向外部逸出扩散的可能。图1中的保留率也进一步说明,10 %乙醇水溶液适合做吸附实验的食品模拟液。
2.2 不同温度下风味物质在包装薄膜/食品模拟液中的分配系数
本文研究分析D-柠檬烯、月桂烯、己酸乙酯、2-壬酮、芳樟醇5种风味物质在LDPE薄膜中吸附扩散情况,主要选择4、23、40、64 ℃四种不同包装储存温度。这是因为4 ℃为食品冷藏温度,23 ℃为常温包装温度,40 ℃为夏天高温存储温度,64 ℃为液体食品巴氏杀菌的温度,实验模拟了液体食品在生产和存储过程中可能出现的4个温度。采用平衡时间15 d,测得风味物质在不同储存温度下风味物质在LDPE薄膜中的吸附平衡量如表2所示。
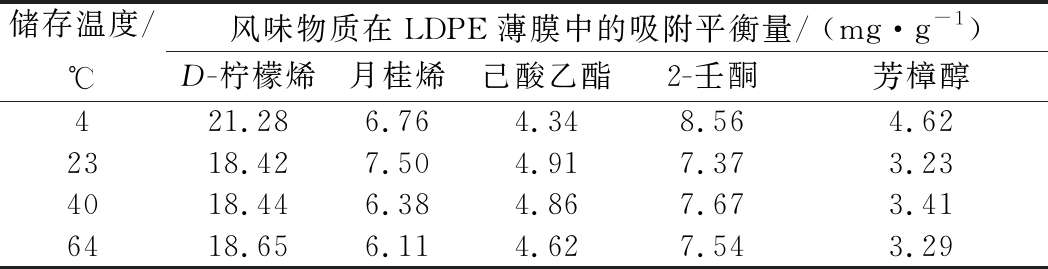
表2 不同储存温度下风味物质在LDPE薄膜中的吸附平衡量
Table 2 Adsorption equilibrium amounts of flavor substances in LDPE films at different temperatures
储存温度/℃风味物质在LDPE薄膜中的吸附平衡量/ (mg·g-1)D-柠檬烯月桂烯己酸乙酯2-壬酮芳樟醇421.286.764.348.564.622318.427.504.917.373.234018.446.384.867.673.416418.656.114.627.543.29
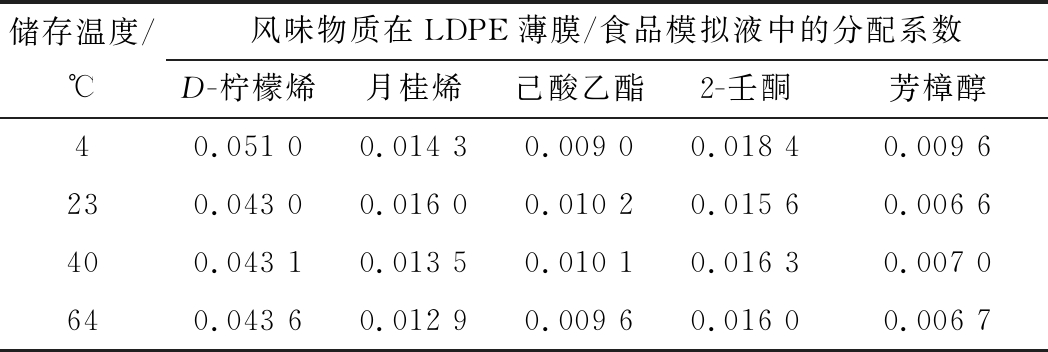
由表2可以看出,除了4 ℃外,23、40和64 ℃下LDPE薄膜对食品风味物质的吸附平衡量较为接近,4 ℃时的吸附平衡量略高。这与4℃储存温度下风味物质在食品模拟液中具有较好的保留率有关。将表2中吸附平衡量代入公式(2)中,可以计算出不同储存温度下风味物质在包装薄膜/食品模拟液中的分配系数KP,F。由表3可以看出,同一温度下,5种风味物质在包装薄膜/食品模拟液中的分配系数较为接近,说明温度对风味物质在两相间的分配影响不大,这与HAMBLETON等的研究结果一致[22]。但是,由于分配系数与温度的相关性没能到达足够小,所以在吸附扩散模型中还需要考虑分配系数的影响。不同温度下,D-柠檬烯的分配系数均最大,月桂烯、己酸乙酯、2-壬酮居中,芳樟醇除了4 ℃外均最小。风味物质在包装薄膜/食品模拟液中的分配关系,与风味物质、包装薄膜和食品模拟液的极性有关。LDPE薄膜是非极性聚合物材料,乙醇水溶液是极性食品模拟液。风味物质中,D-柠檬烯为弱极性,月桂烯、己酸乙酯、2-壬酮为中极性,芳樟醇为极性物质。根据相似相溶原理,D-柠檬烯更容易被LDPE吸附,而芳樟醇更容易在乙醇水溶液中存在。
表3 不同温度下5种风味物质在LDPE薄膜/10 %乙醇溶液中的分配系数
Table 3 Partition coefficients of five flavors in LDPE/10 %ethanol solution at different temperatures
储存温度/℃风味物质在LDPE薄膜/食品模拟液中的分配系数D-柠檬烯月桂烯己酸乙酯2-壬酮芳樟醇40.051 00.014 30.009 00.018 40.009 6230.043 00.016 00.010 20.015 60.006 6400.043 10.013 50.010 10.016 30.007 0640.043 60.012 90.009 60.016 00.006 7
2.3 不同温度下风味物质在包装薄膜中的扩散系数
为了分析不同包装存储温度下风味物质在LDPE薄膜中的扩散性能,选择多个吸附时间点进行吸附量测定(如图2所示),并基于Fick第二定律数学模型(3)利用Matlab软件,对5种风味物质在LDPE薄膜中的吸附量进行最小二乘法拟合从而获得扩散系数值,结果如表4所示。由图2和表4可以看出,5种风味物质在LDPE薄膜中的吸附量拟合公式(3)的R2值均大于0.9,说明不同包装存储温度下风味物质在LDPE薄膜中的扩散符合Fick第二定律扩散。
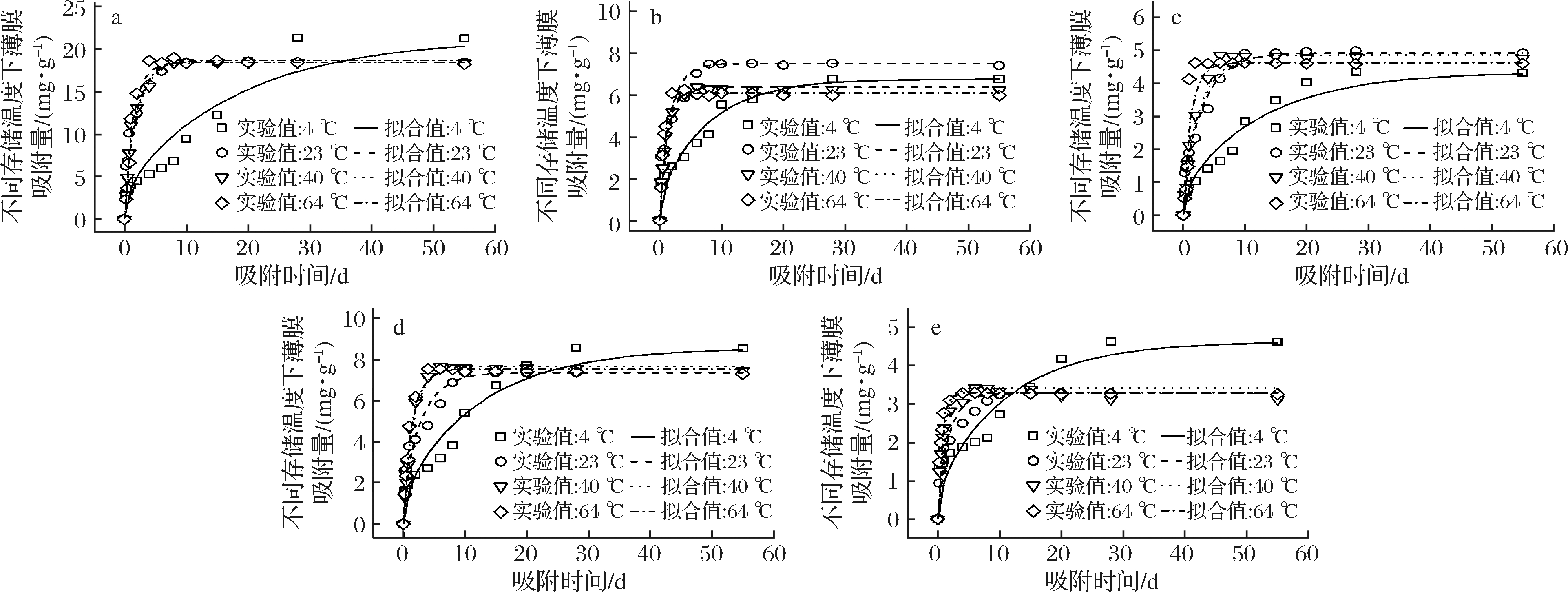
a-D-柠檬烯;b-月桂烯;c-己酸乙酯;d-2-壬酮;e-芳樟醇
图2 不同存储温度下5种风味物质在LDPE薄膜中吸附扩散的情况
Fig.2 Adsorption and diffusion of five flavor substances in LDPE films at different temperatures
表4 不同存储温度下5种风味物质在LDPE薄膜中的扩散系数
Table 4 Diffusion coefficients of five flavor substances in LDPE films at different temperatures

风味物质4 ℃23 ℃40 ℃64 ℃D/(cm2·s-1)R2D/(cm2·s-1)R2D/(cm2·s-1)R2D/(cm2·s-1)R2D-柠檬烯5.64×10-120.926.69×10-110.984.95×10-110.985.13×10-110.97月桂烯1.32×10-110.955.72×10-110.967.61×10-111.001.16×10-100.98己酸乙酯8.07×10-120.963.08×10-110.983.58×10-110.987.54×10-110.872-壬酮8.22×10-120.953.50×10-110.985.67×10-110.986.51×10-110.98芳樟醇9.07×10-120.905.41×10-110.971.02×10-100.971.58×10-101.00
由图2可以看出,在23、40、64 ℃不同温度下,风味物质在LDPE薄膜中的扩散规律基本类似:开始时扩散速率较快,然后逐渐变得缓慢,最后达到平衡,吸附平衡量也趋向一致。在4 ℃的条件下,风味物质扩散速率较为缓慢,吸附平衡时间较长,总吸附量高于其他温度;64 ℃的巴氏杀菌温度下,各风味物质浓度在达到平衡后的吸附量都有下降的趋势,其中D-柠檬烯吸附变化量较大,下降率达3.89 %。这是因为长时间高温吸附,食品模拟液中的风味物质有向外逸出的可能性。
由表4可以看出,除了D-柠檬烯外,包装存储温度越高,风味物质在LDPE薄膜中扩散系数越大。高温促进了风味物质在包装材料的扩散,更快到达平衡;低温减缓了风味物质在包装材料的扩散,更慢地达到平衡。这是因为在较高温度下风味分子获得更多能量,其扩散行为更为活跃;聚合物链蠕动性增强,自由体积增大,风味分子有了更多的自由扩散空间等。D-柠檬烯在高温下,扩散系数有所较小,可能是因为吸附量较大的D-柠檬烯进入LDPE薄膜后,占据了更多的薄膜自由“空穴”,同类分子的扩散竞争从而影响其扩散速率。为了更好地分析扩散系数的规律,对扩散系数对数值与T-1线性拟合,可得到它们的关系曲线(见图3)。如图3所示,除D-柠檬烯外,风味物质在LDPE中的扩散系数的线性拟合较好(R2>0.9),这表明风味物质的扩散系数与温度关系基本符合Arrhennius方程关系。
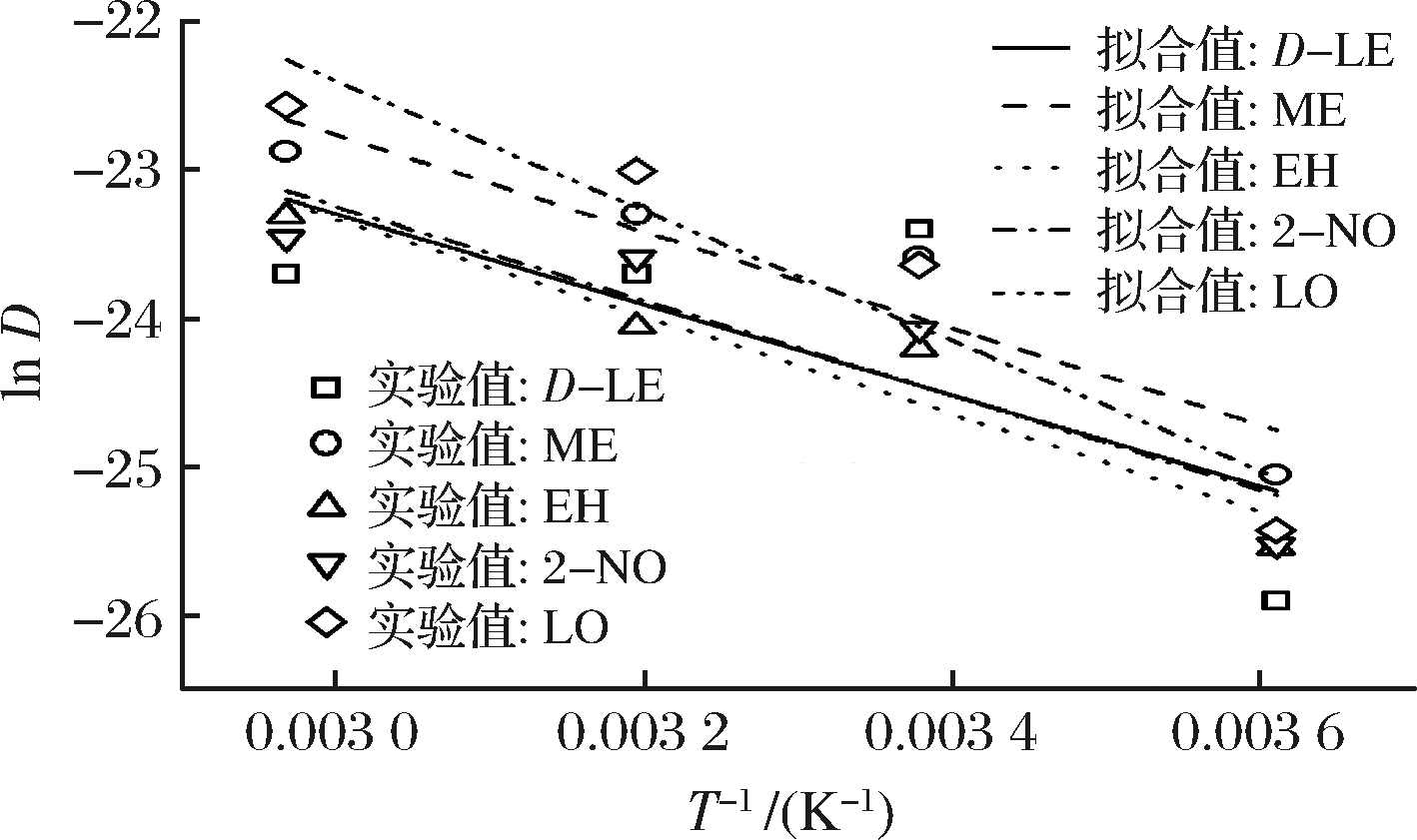
图3 扩散系数对数值lnD与T-1线性拟合图
Fig.3 Linear fitting diagram of lnD with T-1
3 结论
本文利用双面薄膜浸泡法进行吸附实验,研究了不同储存温度下D-柠檬烯、月桂烯、己酸乙酯、2-壬酮、芳樟醇5种风味物质在LDPE薄膜中吸附扩散的过程以及重要参数(分配系数和扩散系数)的分析。结果表明:
(1)五种风味物质在体积分数为10 %的乙醇水溶液中具有较高的保留率,均达到90 %以上。
(2)在不同温度下,同一风味物质在包装薄膜/食品模拟液中的分配系数较为接近;在同一温度下,D-柠檬烯的分配系数均最大,月桂烯、己酸乙酯、2-壬酮居中,芳樟醇除了4 ℃外均最小。
(3)除了D-柠檬烯外,包装存储温度越高,风味物质在LDPE薄膜中扩散系数越大;通过对扩散系数对数值与T-1的线性拟合,表明风味物质的扩散系数与温度关系基本符合Arrhennius方程关系。
(4)因为温度对扩散系数的较大影响,蒸馏、热灌装、杀菌、微波加热和袋蒸煮加工等食品加工技术,会导致风味物质在聚合物包装材料的吸附扩散,从而使得食品的品质下降。
[1] SAFA L,ZAKI O,LEPRINCE Y, et al.Evaluation of model compounds-polypropylene film interactions by fourier transformed infrared spectroscopy (FTIR) method[J].Packaging Technology and Science,2008,21(3):149-157.
[2] DENKTAS C.Influence of apple flavor absorption on physical and mechanical properties of poly(ethylene terephthalate) films[J].Journal of Applied Polymer Science,2006,99(4):1 802-1 807.
[3] POGORZELSKA Z,MIELNICZUK Z.Determination of ε-Caprolactam migration from polyamide plastics: A new approach[J]. Packaging Technology and Science,2001,14(1):31-35.
[4] SUPPAKUL P,SONNEVELD K,BIGGER S W, et al.Diffusion of linalool and methylchavicol from polyethylene-based antimicrobial packaging films[J].Food Science and Technology,2011,44(9):1 888-1 893.
[5] CANER C.Sorption phenomena in packaged foods: factors affecting sorption processes in package-product systems[J]. Packaging Technology and Science,2011,24(5):259-270.
[6] DOMBRE C,RIGOU P, CHALIER P. The use of active PET to package rose wine: Changes of aromatic profile by chemical evolution and by transfers[J]. Food Research International,2015,74(4):63-71.
[7] CROOK L R,BOYLSTON T D, GLATZ B A.Effect of gas environment and sorbate addition on flavor characteristics of irradiated apple cider during storage[J].Journal of Agricultural Science and Technology,2004,52(23):6 997-7 004.
[8] PEYCHES-BACH A,MOUTOUNET M,PEYRON S, et al. Factors determining the transport coefficients of aroma compounds through polyethylene films[J].Journal of Food Engineering,2009,95(1):45-53.
[9] KASSOUF A,RAKWE M E,CHEBIB H, et al. Independent components analysis coupled with 3D-front-face fluorescence spectroscopy to study the interaction between plastic food packaging and olive oil[J].Analytica Chimica Acta,2014,839(8):14-25.
[10] SALAZAR R,DOMENEK S,DUCRUET V. Interactions of flavoured oil in-water emulsions with polylactide[J]. Food Chemistry,2014,148(4):138-146.
[11] 卢立新,孙一超,唐亚丽,等.风味物质初始质量分数与储存温度对LDPE吸附性能的影响[J].食品与生物技术学报,2016,35(6):635-639.
[12] JUNIOR L M,CRISTIANINI M,PADULA M,et al.Effect of high-pressure processing on characteristics of flexible packaging for foods and beverages[J].Food Research International,2019,119(1):920-930.
[13] FERTIKH N,TOUBAL A,LARBI L,et al.Sorption and diffusion of flavours contained in rose-water in plastic packaging[J]. International Journal of Engineering and Technology Sciences,2013,1(3):149-162.
[14] CHANDRA P,KOROS W J.Sorption and transport of methanol in poly(ethylene terephthalate)[J].Polymer,2009,50(1):236-244.
[15] AURAS R,HARTE B,SELKE S.Sorption of ethyl acetate and d-limonene in poly(lactide) polymers[J].Journal of the Science of Food and Agriculture,2006,86:648-656.
[16] CHANDRA P,KOROS W J.Sorption of lower alcohols in poly(ethylene terephthalate)[J].Polymer,2009,50(17):4 241-4 249.
[17] LIMAM M,TIGHZERT L,FRICOTEAUX F,et al.Sorption of organic solvents by packaging materials: Polyethylene terephthalate and TOPAS[J].Polymer Testing,2005,24(3):395-402.
[18] CAVA D,CATALA R,GAVARA R, et al. Testing limonene diffusion through food contact polyethylene by FT-IR spectroscopy: Film thickness, permeant concentration and outer medium effects[J].Polymer Testing,2005,24(4):483-489.
[19] 王蓓,许时婴. SPME-GC-MS对不同牛奶香精和稀奶油中的挥发性风味物质比较[J].食品与发酵工业,2008,34(7):115-121.
[20] 孙一超,卢立新.食品中不同种类风味物质对LDPE吸附现象的影响研究[J].包工程,2013,34(1):34-37.
[21] TEHRANY E A,FOURRNIER F,DESOBRY S.Simple method to calculate partition coefficient of migrant in food simulant/polymer system[J].Journal of Food Engineering,2006,77(1):135-139.
[22] HAMBLETON A,VOILLEY A,DEBEAUFORT F. Transport parameters for aroma compounds through i-carrageenan and sodium alginate-based edible films[J].Food Hydrocolloids,2011,25(5):1 128-1 133.