在酿造酒行业中,氨基酸不仅能赋予酿造酒鲜、甜、苦、涩等多种味觉特征,同时还为发酵过程中酵母等微生物的生长代谢提供氮源,促进发酵作用[1-3],因此氨基酸含量水平是食品发酵工业中一个重要的指标[4]。氨基酸水平通常以氨基酸态氮进行表征,以衡量原料蛋白质的水解程度、发酵液的氮源水平及产品质量等。
在食品发酵领域,氨基酸态氮的常用测定方法是甲醛滴定法和茚三酮比色法。甲醛滴定法常用于黄酒、酱油等产品中氨基酸态氮的测定[5-6],该方法通过甲醛结合氨基,使氨基酸显酸性,进而通过标准NaOH溶液对其进行定量。甲醛滴定法虽然操作简单,但甲醛为一类致癌物[7],且该方法检测限较高[8],常用于对氨基酸含量较高的产品进行检测。茚三酮比色法是啤酒等产品中氨基酸态氮的测定方法[9-10],也常用于测定茶叶等食品中游离氨基酸总量[11],是一种操作方便、重现性和准确度都比较高的分析方法。此外,氨基酸的分析也可通过基于色谱技术的氨基酸分析仪,利用衍生物质与氨基酸的结合来实现氨基酸分析,该方法能准确定量样品中近20种常见的游离氨基酸,但是成本较高,操作较为繁琐[12]。已有研究比较了甲醛滴定法与茚三酮比色法对特定产品中氨基酸态氮的测定[8, 13],结果表明,这2种方法均具有较高的准确度和精密度,但测定结果有一些差异。此外,茚三酮比色法虽然不能检测脯氨酸等氨基酸,但相对于甲醛滴定法,其检测限更低,测定浓度范围更广[8]。总体而言,2种方法各有优缺点,对于不同的测定目的,应选择合适的测定方法。
目前黄酒中氨基酸态氮的测定在国际上采用的是甲醛滴定法[5]。但是,近年来清爽型黄酒以及米酒逐渐受到市场的欢迎,而这些产品中氨基酸含量相对较低,利用甲醛滴定法测定某些清爽型黄酒,测定结果误差可能相对较大。特别是一些米酒产品,利用酒药(小曲或米曲)而不是麦曲作为糖化发酵剂进行酿造,氨基酸含量相对更低,甲醛滴定法是否可以准确地测定其中的氨基酸态氮含量,成为目前出现的问题。
本研究通过对黄酒和米酒中氨基酸态氮不同测定方法的比较,重点探讨了茚三酮比色法在米酒和黄酒等中国传统酿造酒中的适用性,为米酒行业中氨基酸态氮分析指标的建立提供依据。
1 材料与方法
1.1 材料与试剂
1.1.1 样品
本研究所用黄酒和米酒样品均为市售商品或由生产厂家提供的产品,包括9个黄酒样品和8个米酒样品,共17个。产地来源以浙江、江苏、上海和湖北为主,产品类型涉及干、半干、半甜和甜型等各种类型,酒精度范围为5%~18%vol。
1.1.2 实验试剂
甲醛水溶液、乙醇、酚酞、NaOH、邻苯二甲酸氢钾、Na2HPO4、KH2PO4、水合茚三酮、果糖、碘酸钾、甘氨酸四氢呋喃、三乙胺、盐酸、结晶乙酸钠、三氯乙酸:分析纯,上海国药集团;甲醇、乙腈:色谱纯,美国TEDIA公司;17种氨基酸标准品,Sigma公司。
1.2 仪器与设备
FE20型pH计,瑞士Mettler Toledo;CYTATION3型酶标仪,BioTek公司;Centrifuge 5810R型高速离心机,德国Eppendorf公司;Agilent1100型高效液相色谱仪系统,美国安捷伦公司。
1.3 实验方法
1.3.1 酒样处理
取酒样40 mL于50 mL离心管中,4 ℃下8 000 r/min离心5 min后,取上清作为实验试样,存放于4 ℃冰箱备用。
样品酸度调节:先以0.5 mol/L的NaOH溶液对样品进行中和处理,调节样品pH至8.20,然后添加适量乳酸调节处理后的样品,达到所需的总酸含量(以乳酸计)。
样品乙醇浓度调节:利用旋转蒸发仪在40 ℃、100 hPa压力下对酒样进行减压蒸馏处理0.5~1 h去除乙醇,然后加入适量无水乙醇调节处理后样品中的乙醇含量至所需要的水平。
1.3.2 测定分析方法
甲醛滴定法参照黄酒国标GB/T 13662—2018[5]。
茚三酮比色法参照啤酒工业手册[9]并略加改进。将酒样稀释100倍后取稀释酒样2.00 mL,置于10 mL离心管中,加显色剂1.00 mL,摇匀,在恒沸水浴中准确加热16 min后,于20 ℃水浴中冷却20 min,加5 mL KIO3稀释溶液,摇匀,用酶标仪于570 nm波长处测定其吸光度(OD值)。标准曲线制作:用不同浓度的甘氨酸标准溶液(浓度范围为1.60~53.57 mg/L)进行上述操作测定吸光度后绘制标准曲线。
氨基酸分析仪采用OPA柱前衍生反相高效液相色谱-紫外检测法[14]。样品处理:样品经三氯乙酸沉淀后静置0.5 h,取上清过0.22 μm有机微孔滤膜,滤液进样。色谱条件:色谱柱为Agilent Hypersil ODS柱,流动相A为27.6 mmol/L醋酸钠-三乙胺-四氢呋喃(体积比为500∶0.11∶2.5),流动相B为80.9 mmol/L醋酸钠-甲醇-乙腈(体积比为1∶2∶2),采用梯度洗脱,洗脱程序为:0 min,8%B;17 min,50%B;20.1 min,100%B;24.0 min,0%B;流动相流速为1.0 mL/min;柱温为40 ℃;紫外检测器(VWD)检测波长为338 nm,其中脯氨酸在262 nm波长下检测。
氨基酸态氮计算。根据氨基酸分析仪测得的各氨基酸含量及其所含的氨基酸态氮、α-氨基酸态氮分别进行换算得到总氨基酸态氮和α-氨基酸态氮含量。
2 结果与分析
2.1 黄酒和米酒特性对茚三酮比色法测定氨基酸态氮的影响
茚三酮比色法是啤酒行业中氨基酸态氮测定的标准方法[9-10]。与啤酒相比,黄酒和米酒在一些特性上存在着较大差异,如黄酒色泽较深,乙醇和总酸含量远高于啤酒等,因此,首先对黄酒和米酒的这些特性是否会影响茚三酮比色法的测定结果进行了探究。
2.1.1 色泽对茚三酮比色法测定的影响
茚三酮比色法较为灵敏,在测定啤酒样品时需要进行100倍左右的稀释[15]。黄酒酒液由于颜色较深,可能会对茚三酮比色法的结果产生干扰[16]。因此,参考啤酒样品的处理方法,首先对黄酒和米酒样品进行100倍稀释处理,对稀释前后的所有样品在400~700 nm之间进行全波长扫描,主要对各样品570 nm波长处测定的OD值进行分析,考察黄酒和米酒色泽是否对茚三酮比色法的测定有影响。结果如图1所示,黄酒样品在570 nm处的OD值平均在0.20左右,高的可达0.35,而米酒样品的OD值相对较低。由于比色法需要对样品进行稀释处理,在稀释100倍后,黄酒和米酒样品的OD值均降低至0.037~0.041,与纯水的吸光度接近,因此可以认为黄酒和米酒的色泽在茚三酮比色法的测定中不会对测定结果产生明显影响。
2.1.2 总酸对茚三酮比色法测定的影响
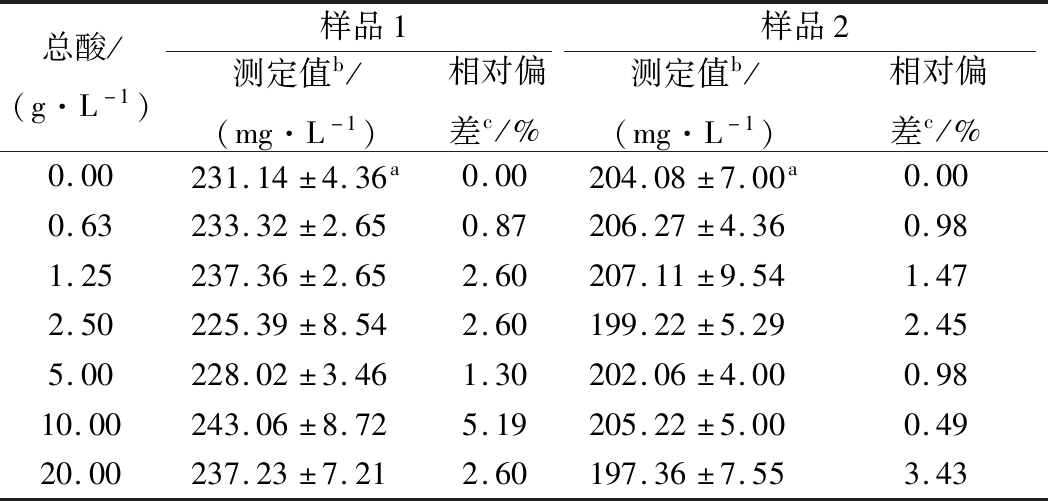
黄酒或米酒中总酸(以乳酸计)一般在10 g/L以下,随机选取黄酒和米酒样品各1个,调节样品中的总酸含量为0 ~20 g/L,利用茚三酮比色法测定不同酸度下样品的氨基酸态氮。结果如表1所示,不同酸度对2个样品中比色法测定值的相对偏差基本小于3.00%,最高为5.19%,因此可以认为黄酒或米酒的酸度不会对茚三酮比色法的测定结果产生明显影响。
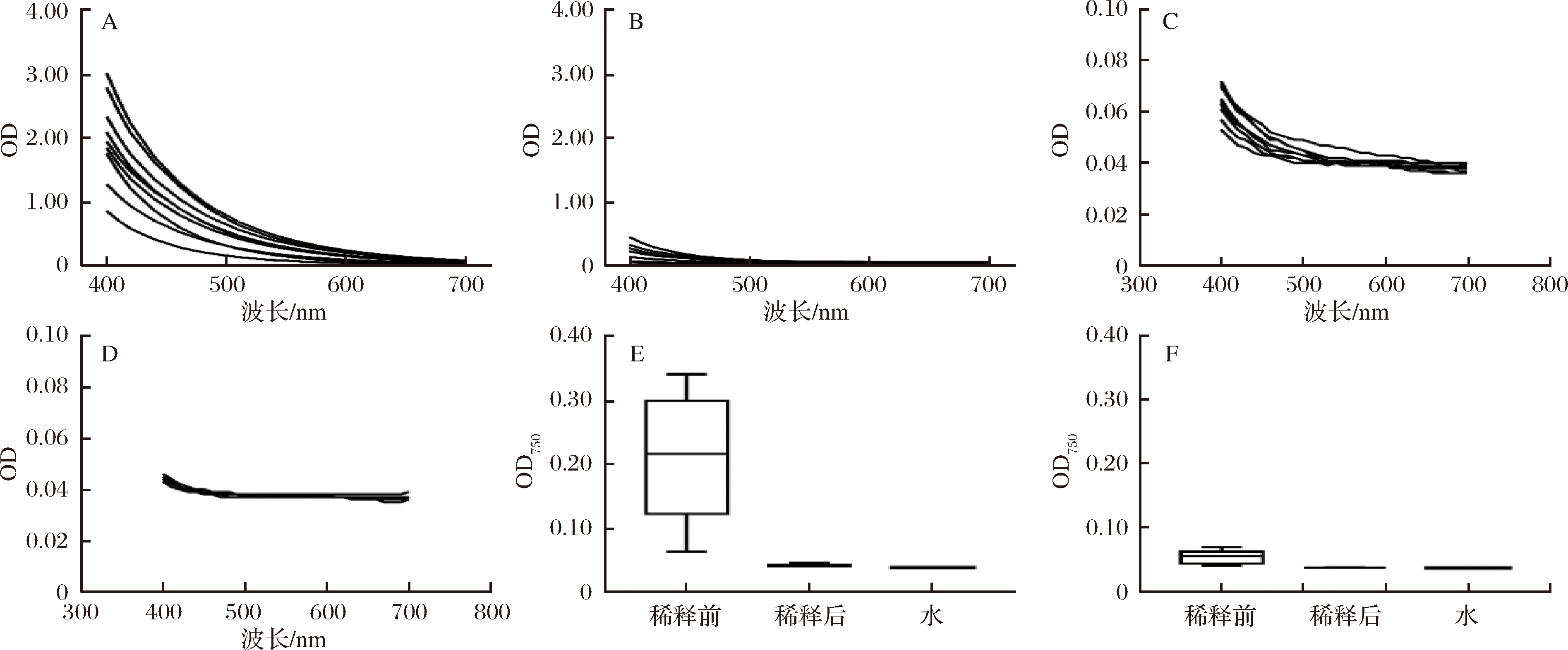
A-黄酒稀释前的OD值;B-米酒稀释前的OD值;C-黄酒稀释后的OD值;D-米酒稀释后的OD值;E-570 nm处黄酒OD值;F-570 nm处米酒OD值
图1 稀释前后黄酒和米酒OD值的变化
Fig.1 Changes in OD values of Huangjiu and Mijiu before and after dilution
表1 总酸对氨基酸态氮测定结果的影响
Table 1 Effect of total acid content on the determination of amino acid nitrogen
总酸/(g·L-1)样品1样品2测定值b/(mg·L-1)相对偏差c/%测定值b/(mg·L-1)相对偏差c/%0.00231.14±4.36a0.00204.08±7.00a0.000.63233.32±2.650.87206.27±4.360.981.25237.36±2.652.60207.11±9.541.472.50225.39±8.542.60199.22±5.292.455.00228.02±3.461.30202.06±4.000.9810.00243.06±8.725.19205.22±5.000.4920.00237.23±7.212.60197.36±7.553.43
注:a为对照值,b、c分别为不同酸度下样品3次测定值的平均值及其与对照值的相对偏差。
2.1.3 酒精含量对茚三酮比色法测定的影响
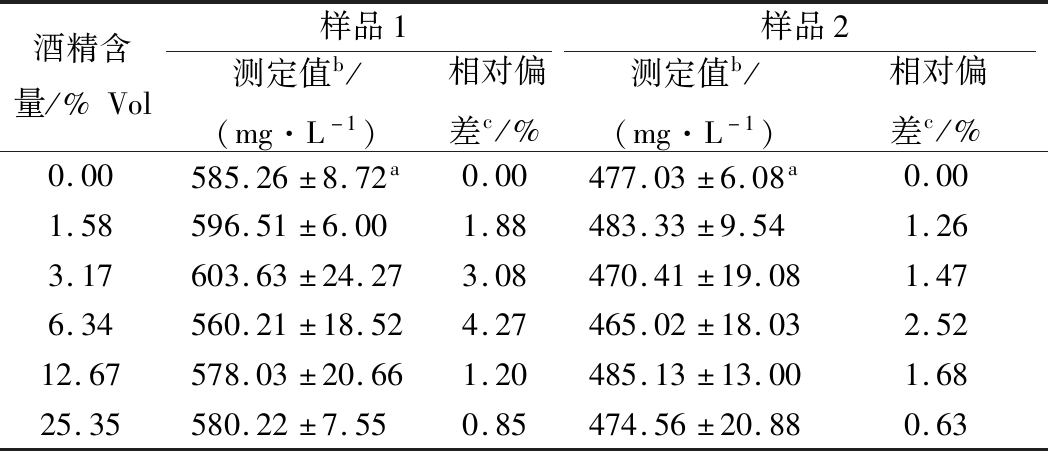
相对于啤酒,黄酒和米酒的酒精度要高出很多,黄酒中酒精度一般为8%~18%vol。随机选取黄酒和米酒样品各1个,调节样品中的酒精度为0~25.35%vol,利用茚三酮比色法测定不同乙醇含量酒样的氨基酸态氮。结果如表2所示,不同乙醇含量对2个样品中比色法测定值的相对偏差均较小,最大为4.27%,因此可以认为黄酒或米酒的酒精含量不会对茚三酮比色法的测定结果产生明显影响。
2.2 茚三酮比色法和甲醛滴定法精密度和准确性比较
由于黄酒或米酒的色泽、总酸及酒精含量等特性不会对茚三酮比色法的测定结果产生明显影响,进一步对该方法测定黄酒和米酒氨基酸态氮的精密度和准确性进行检验,并与甲醛滴定法进行比较,结果如表3和表4所示。
表2 酒精含量对比色法测定结果的影响
Table 2 Effect of alcohol content on the determination of amino acid nitrogen
酒精含量/%Vol样品1样品2测定值b/(mg·L-1)相对偏差c/%测定值b/(mg·L-1)相对偏差c/%0.00585.26±8.72a0.00477.03±6.08a0.001.58596.51±6.001.88483.33±9.541.263.17603.63±24.273.08470.41±19.081.476.34560.21±18.524.27465.02±18.032.5212.67578.03±20.661.20485.13±13.001.6825.35580.22±7.550.85474.56±20.880.63
注:a为对照值,b、c分别为不同酒精含量下样品3次测定值的平均值及其与对照值的相对偏差。
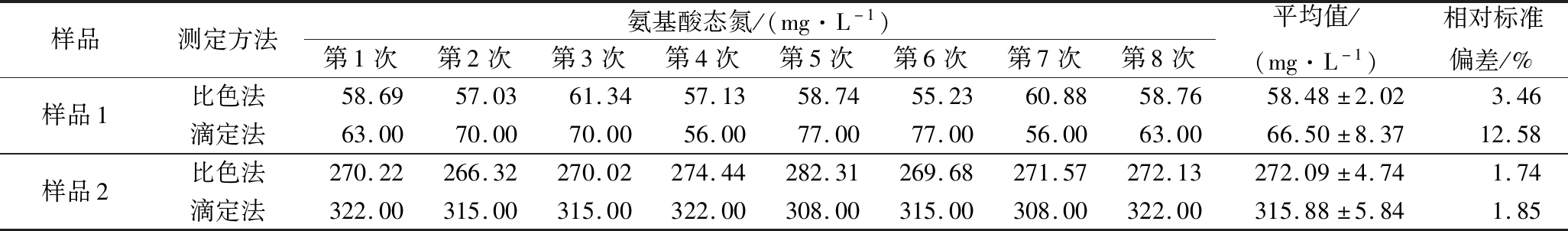
对于氨基酸态氮含量相对较高的样品(如样品2),2种测定方法的精密度和准确性均较好,RSD值(相对标准偏差)均小于2.00%,加标回收率也接近100%。但对于氨基酸态氮含量相对较低的样品(如样品1),滴定法的精密度较差,RSD值为12.58%,且由于测定的重复性较差,因此加标回收率的变化也较大,而比色法仍表现出较好的精密度和准确性。该结果与这2种方法在鲜味提取物[17]和胶原水解物[8]中氨基酸态氮的测定结果相类似。由于滴定法所固有的误差,当样品氨基酸态氮含量较低(滴定值较小)时,其相对误差较大,因而精密度和准确性相对较低。因此在测定含量相对较低的样品(如米酒样品)时,比色法的重复性和准确性更高。
表3 茚三酮比色法和甲醛滴定法的精密度检验
Table 3 Precision test of ninhydrin colorimetry and formaldehyde titration
样品测定方法氨基酸态氮/(mg·L-1)第1次第2次第3次第4次第5次第6次第7次第8次平均值/(mg·L-1)相对标准偏差/%样品1比色法58.6957.0361.3457.1358.7455.2360.8858.7658.48±2.023.46滴定法63.0070.0070.0056.0077.0077.0056.0063.0066.50±8.3712.58样品2比色法270.22266.32270.02274.44282.31269.68271.57272.13272.09±4.741.74滴定法322.00315.00315.00322.00308.00315.00308.00322.00315.88±5.841.85
表4 茚三酮比色法和甲醛滴定法的准确性检验
Table 4 Accuracy test of ninhydrin colorimetry and formaldehyde titration
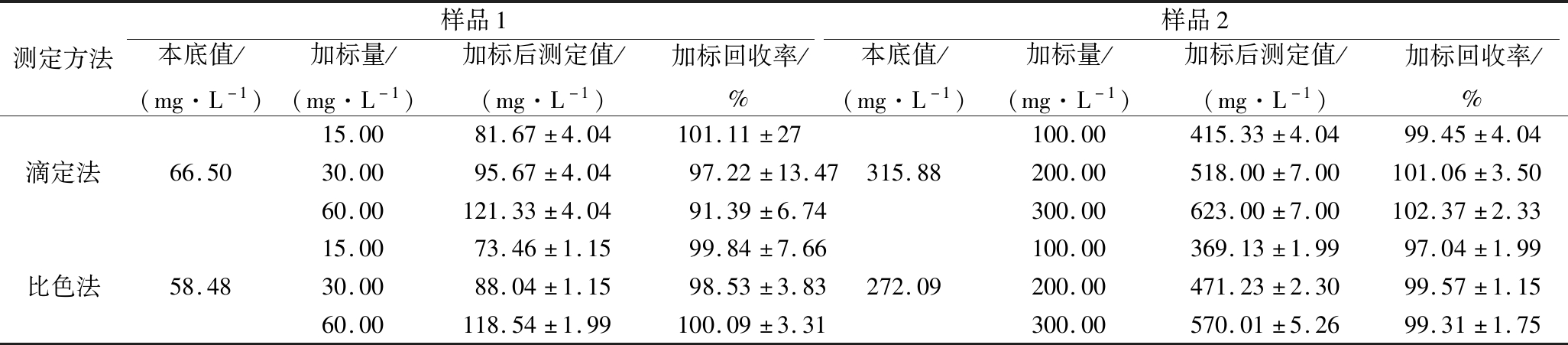
测定方法样品1样品2本底值/(mg·L-1)加标量/(mg·L-1)加标后测定值/(mg·L-1)加标回收率/%本底值/(mg·L-1)加标量/(mg·L-1)加标后测定值/(mg·L-1)加标回收率/%15.0081.67±4.04101.11±27100.00415.33±4.0499.45±4.04滴定法66.5030.0095.67±4.0497.22±13.47315.88200.00518.00±7.00101.06±3.5060.00121.33±4.0491.39±6.74300.00623.00±7.00102.37±2.3315.0073.46±1.1599.84±7.66100.00369.13±1.9997.04±1.99比色法58.4830.0088.04±1.1598.53±3.83272.09200.00471.23±2.3099.57±1.1560.00118.54±1.99100.09±3.31300.00570.01±5.2699.31±1.75
2.3 茚三酮比色法和甲醛滴定法测定黄酒和米酒中氨基酸态氮的结果比较
在明确了茚三酮比色法测定黄酒和米酒中氨基酸态氮的可行性后,对来自不同产地、不同类型的9个黄酒样品和8个米酒样品分别利用茚三酮比色法和甲醛滴定法进行氨基酸态氮的测定,并与利用氨基酸分析仪测定各酒样中17种氨基酸的定量结果进行比较分析。氨基酸分析仪测定的黄酒和米酒氨基酸含量结果如表5所示。
表5 黄酒和米酒中氨基酸分析仪测定的脯氨酸及总氨基酸含量
Table 5 Content of proline and total amino acid in Huangjiu and Mijiu
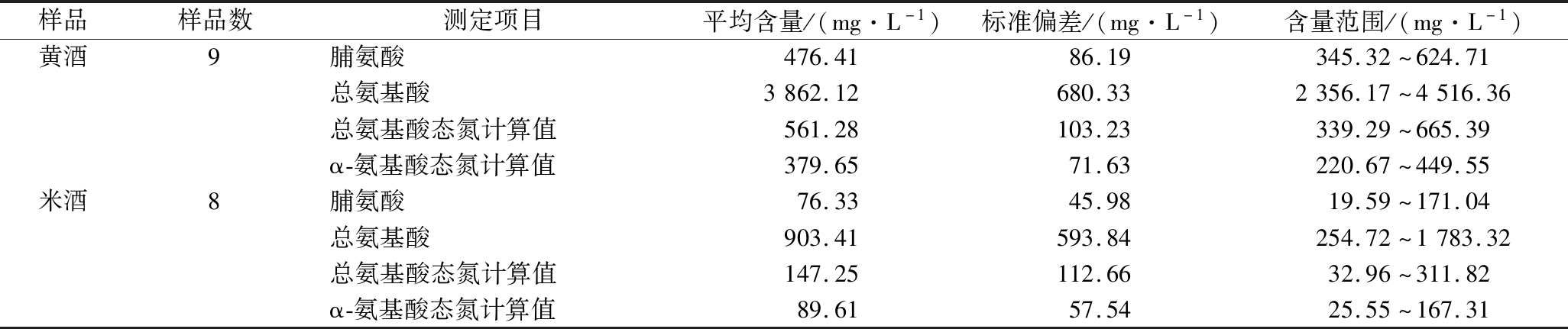
样品样品数测定项目平均含量/(mg·L-1)标准偏差/(mg·L-1)含量范围/(mg·L-1)黄酒9脯氨酸476.4186.19345.32~624.71总氨基酸3862.12680.332356.17~4516.36总氨基酸态氮计算值561.28103.23339.29~665.39α-氨基酸态氮计算值379.6571.63220.67~449.55米酒8脯氨酸76.3345.9819.59~171.04总氨基酸903.41593.84254.72~1783.32总氨基酸态氮计算值147.25112.6632.96~311.82α-氨基酸态氮计算值89.6157.5425.55~167.31
首先对茚三酮比色法和甲醛滴定法的测定结果进行比较,结果如图2-A所示,两者对米酒和黄酒的测定结果具有很好的线性相关性(R2=0.983 1),但滴定法的测定结果明显高于比色法(斜率为1.371 8)。在表5中也比较了米酒和黄酒中根据氨基酸分析仪测定结果计算得到的总氨基酸态氮和α-氨基酸态氮含量,可以发现,相同样品总氨基酸态氮含量比α-氨基酸态氮含量平均要高50%左右。一般认为,甲醛滴定法的测定结果为总的氨基酸态氮含量,而茚三酮比色法的测定结果主要为α-氨基酸态氮含量(不含α-亚氨基酸,如脯氨酸和羟脯氨酸)[13,18],因为在570 nm处一些非α-氨基酸,如脯氨酸等与茚三酮的反应产物无明显吸收,无法被定量[19],因此甲醛滴定法的测定值通常会高于茚三酮比色法[8]。黄酒和米酒中含有较高含量的脯氨酸(表5),约占总氨基酸含量的10%,进一步比较了比色法测定值加上脯氨酸态氮后与滴定法测定值的差异,结果如图2-B,两者的线性相关性仍然很好(R2=0.987 3),但斜率下降至1.204 0,即两者的差异缩小,表明脯氨酸的确是引起滴定法的测定结果高于比色法的一个重要原因。同时,由于黄酒和米酒中其他含氨基化合物,包括氨和胺类等化合物也都可能与甲醛进行反应进而被测定,使得甲醛滴定法测定氨基酸态氮的结果偏高[20]。因此,虽然茚三酮比色法和甲醛滴定法的测定结果具有较好的相关性,但由于2种测定方法存在的差异,针对不同的目的和对象,应该选择适当的测定方法。

A-比色法与滴定法测定值的直接比较;B-比色法测定值中加入脯氨酸计算值与滴定法的比较
图2 比色法和滴定法的线性关系
Fig.2 Linear relationship between ninhydrin colorimetry and formaldehyde titration
由于米酒的氨基酸态氮含量远低于黄酒(表5),进一步根据氨基酸分析仪测定结果,计算各酒样中总氨基酸态氮和α-氨基酸态氮的含量,分别对黄酒和米酒茚三酮比色法和甲醛滴定法的测定结果进行比较分析,结果如图3所示。结果表明,滴定法的测定结果更接近于总氨基酸态氮的计算含量(图3-A、B),其斜率相比比色法更接近于1;而比色法的测定结果则更接近于α-氨基酸态氮的计算含量(图3-C、D),这与之前的分析结果一致,即甲醛滴定法的测定结果为总的氨基酸态氮含量,茚三酮比色法的测定结果主要为α-氨基酸态氮含量[18]。从线性关系来看,无论是总氨基酸态氮还是α-氨基酸态氮,与比色法相比,滴定法的测定值与氨基酸分析仪的计算值线性关系相对较差(R2相对更小),特别是对于氨基酸含量相对更低的米酒,比色法的测定值偏差较小,与氨基酸分析仪计算值的线性关系相对更好(图3-C、D),说明比色法与氨基酸分析仪的测定结果一致性更高。比色法虽然不能测定脯氨酸等氨基酸,但可以测定几乎所有α-氨基酸态氮及少量其他氨态氮[21];而氨基酸分析仪通常只能定量样品中接近20种游离氨基酸,并非所有氨基酸。两者测定的对象不完全相同,但绝大部分是一致的。与这2种方法相比,滴定法的测定对象则更为复杂。因此这可能是比色法与氨基酸分析仪测定结果有更好相关性的主要原因。
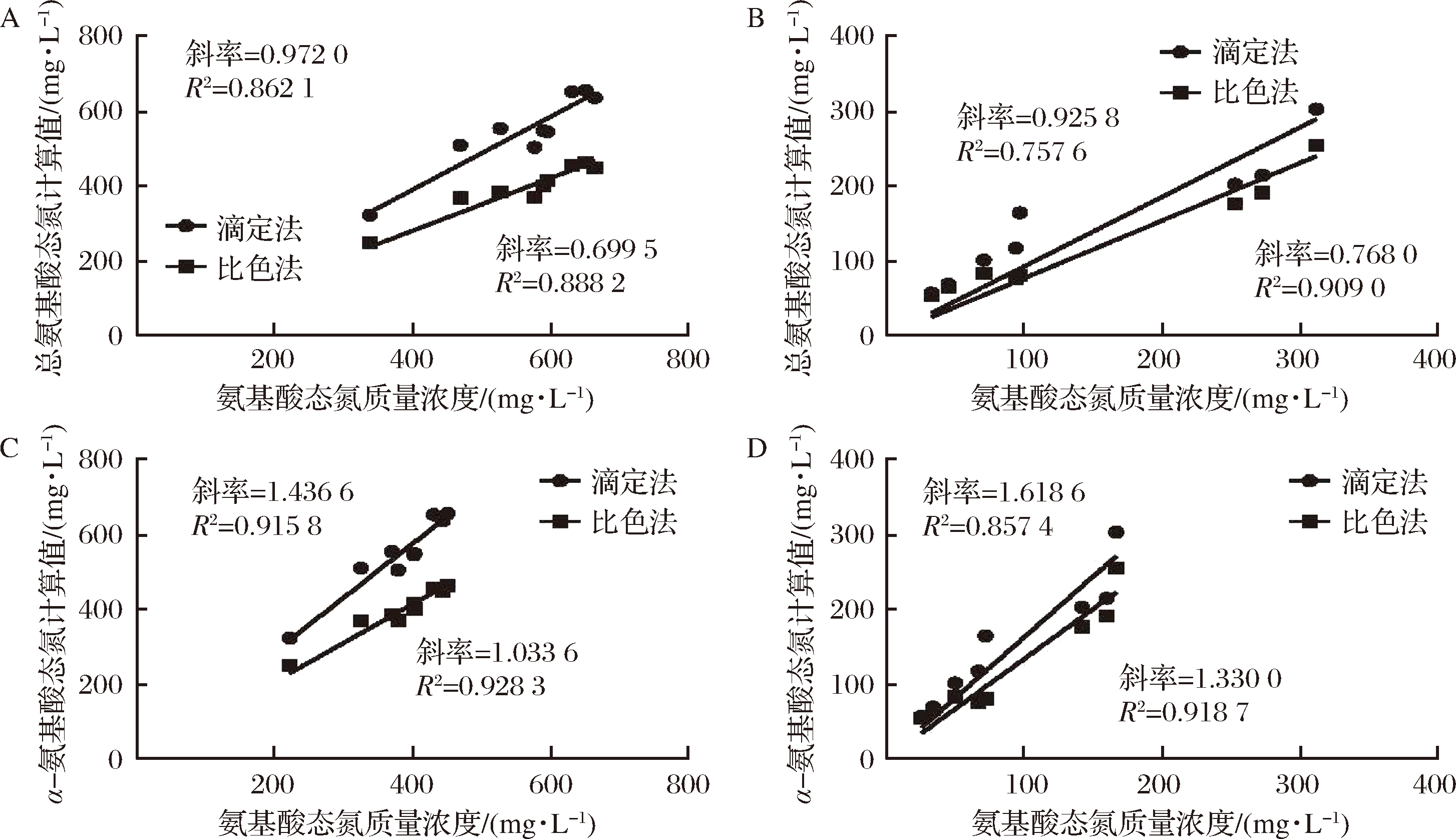
A-黄酒总氨基酸态氮结果比较;B-米酒总氨基酸态氮结果比较;C-黄酒α-氨基酸态氮结果比较;D-米酒α-氨基酸态氮结果比较
图3 比色法、滴定法测定结果分别与氨基酸分析仪计算结果的线性关系
Fig.3 Linear relationship between colorimetric method as well as titration method and amino acid analyzer
氨基酸态氮是黄酒的产品质量指标之一,同时氨基酸也赋予了酿造酒鲜、甜、苦、咸等多种味感,使酒体具有更加丰富的味觉层次,脯氨酸也是黄酒和米酒中重要的甜味贡献物[19]。实际上,由于氨基酸态氮各种方法测定的原理和对象不同,测定结果存在一定的差异。因此,根据不同的目的和要求,应该采用不同的测定方法。滴定法的测定结果更能反映产品总体的氨基酸水平。而在酿造过程中,酵母主要通过对游离氨基酸的利用进行生长代谢,而脯氨酸和羟脯氨酸几乎不被酵母利用[22],因此比色法的测定结果更能表征影响发酵过程的α-氨基氮含量。此外,如果比色法采用酶标仪进行测定,可同时对数十个微量样品进行分析,对大量样品的快速测定具有优势。
3 结论
本研究主要考察了茚三酮比色法在黄酒和米酒氨基酸态氮测定中的适用性。研究结果表明,黄酒和米酒的色泽、总酸和酒精度等特性对茚三酮比色法的测定结果无显著影响。茚三酮比色法与甲醛滴定法测定结果之间具有较好的线性关系,但甲醛滴定法测定值相对偏高。黄酒和米酒中脯氨酸及其他含氨基化合物,包括氨和胺类等化合物可能是造成两者测定结果差异的主要原因。
虽然甲醛滴定法目前是黄酒行业通用的氨基酸态氮测定方法,但对米酒等氨基酸态氮含量较低的样品测定时,茚三酮比色法则具有较高的精密度和准确性。对照氨基酸分析仪分析结果,甲醛滴定法更适于表征产品的总体氨基酸含量,而茚三酮比色法则能更准确反映发酵过程中的α-氨基酸含量。此外,茚三酮比色法作为一种在测定低氨基酸态氮时具有同样高可靠性的方法,还可在较短时间内对大批量样品进行快速测定,具有安全、低成本、易操作等优点,适合在酿造行业生产及科研中推广。该方法不仅是对黄酒的氨基酸态氮测定方法的补充,还可为米酒行业氨基酸态氮分析指标的建立提供依据。
[1] YANG Y, XIA Y, WANG G, et al.Effects of boiling, ultra-high temperature and high hydrostatic pressure on free amino acids, flavor characteristics and sensory profiles in Chinese rice wine[J]. Food Chemistry, 2019, 275: 407-416.
[2] YU H Y, ZHAO J, LI F H, et al.Characterization of Chinese rice wine taste attributes using liquid chromatographic analysis, sensory evaluation, and an electronic tongue[J]. Journal of Chromatography B-Analytical Technologies in the Biomedical and Life Sciences, 2015, 997: 129-135.
[3] 尹花,贺扬,董建军,等.麦汁关键氨基酸对Lager酵母发酵性能的影响[J].食品与生物技术学报, 2018, 37(9): 987-993.
[4] 潘慧青,曹钰,石慧媛,等.黄酒酿造后酵工艺对氨基酸态氮生成的影响[J].食品与生物技术学报, 2016, 35(2): 144-150.
[5] GB/T 13662—2018,黄酒[S].北京:中国国家标准化管理委员会, 2018: 28.
[6] GB 5009.124—2016,食品安全国家标准,食品中氨基酸的测定[S].北京:国家食品药品监督管理总局,2016: 12.
[7] SQUIRE R A,CAMERON L L.An analysis of potential carcinogenic risk from formaldehyde[J].Regulatory Toxicology and Pharmacology, 1984, 4(2):107-129.
[8] 崔敏,傅婕,迟原龙,等.茚三酮比色法和甲醛滴定法测定水解胶原的比较[J].中国皮革,2011,40(7):1-4.
[9] 管敦仪.啤酒工业手册(中册)[M].北京:中国轻工业出版社,1982:191-193.
[10] ABERNATHY D G, SPEDDING G, STARCHER B. Analysis of protein and total usable nitrogen in beer and wine using a microwell ninhydrin assay[J]. Journal of the Institute of Brewing, 2009, 115(2): 122-127.
[11] 涂云飞.茚三酮法测定茶叶游离氨基酸总量研究[J].现代农业科技,2018(14):235;238.
[12] HE X, WU Z, YE Y, et al. Research progress on detection of amino acids by high performance liquid chromatography[J]. Journal of Instrumental Analysis, 2016, 35(7): 922-928.
[13] 迟原龙,文振华,崔敏,等.胶原水解度的测定[J].中国皮革,2010, 39(19):13-16.
[14] HERBERT P, BARROS P, RATOLA N, et al. HPLC determination of amino acids in musts and port wine using OPA/FMOC derivatives[J]. Journal of Food Science, 2000, 65(7):1 130-1 133.
[15] 张永国,秦锐兰.麦汁中α-氨基氮含量的测定方法[J].啤酒科技,2008(3):35-37.
[16] 惠明,邱聪,张会娟,等.老户周黄酒色泽与易褐变营养物含量的相关性研究[J].河南工业大学学报(自然科学版),2018,39(2):15-19.
[17] 岳元媛,田艳.鲜味提取物中氨基酸态氮测定方法的比较研究[J].中国井矿盐,2015,46(1):39-43.
[18] MENDEL F. Applications of the ninhydrin reaction for analysis of amino acids, peptides, and proteins to agricultural and biomedical sciences[J]. Journal of Agricultural & Food Chemistry,2004,52(3):385-406.
[19] 李绍军,龚月桦,王俊儒,等.关于茚三酮法测定脯氨酸含量中脯氨酸与茚三酮反应之探讨[J]. 植物生理学通讯,2005(3):365-368.
[20] TUR’YAN. Theoretical bases of the ammonium ion determination by formol titration[J]. Reviews in Analytical Chemistry, 2010, 29(1):25-37.
[21] LIE S. The EBC-Ninhydrin method for determination of free alpha amino nitrogen[J]. Journal of the Institute of Brewing,1973(79):37-41.
[22] 顾国贤.酿造酒工艺学[M].北京:中国轻工业出版社.2009:456-457.