β-葡萄糖苷酶(β-D-Glucosidase,EC3.2.1.21)即纤维二糖酶(cellobias,CB)[1],可催化水解烃基或芳香基与糖基原子团间的糖苷键,生成葡萄糖并释放相应的配基[2]。高活性的β-葡萄糖苷酶可有效降解纤维二糖,从而提高纤维素酶系的作用效率[3]。此外,β-葡萄糖苷酶在食品、纺织、饲料、造纸和医药等领域都有广泛应用[4-5]。
β-葡萄糖苷酶存在于多种生物体中[6]。植物源β-葡萄糖苷酶活性低且不稳定,目前国内外研究所用的β-葡萄糖苷酶主要来源于微生物[7]。2016年,YAO等[8]利用基因工程手段对草酸青霉进行改造,得到了优良的产β-葡萄糖苷酶突变菌株;2017年,李永博等[9]从浓香型大曲中分离出1株β-葡萄糖苷酶活力达到55.7 U/mL的枯草芽孢杆菌;2018年,王凤梅等[10]从340株葡萄酒相关酵母菌株中筛选得到66株产β-葡萄糖苷酶的酵母菌株并研究了部分菌株的理化性质。多项研究表明,从自然界分离所得菌株的β-葡萄糖苷酶活力普遍偏低[11],运用各种诱变手段对野生菌种进行改造,是获得高产酶活力菌株的有效方法之一[12]。
诱变育种具有高效便捷的优点,常用的诱变方法有物理诱变、化学诱变、常压室温等离子体(atmospheric and room temperature plasma,ARTP)诱变等[13]。用单一的诱变方式得到目的突变株的可能性较低,复合诱变是一种能够大大提高菌株正向突变概率的方法[14]。本研究从腐木样品中分离得到1株产β-葡萄糖苷酶的青霉菌株;先后用ARTP诱变和硫酸二乙酯(diethyl sulfate,DES)诱变方法对该菌株进行诱变,结合七叶苷平板法[15]初筛和摇瓶发酵复筛,最终获得酶活力显著提升且遗传稳定的突变株;最后通过响应面法[16-18]对所得突变菌株的产酶发酵条件进行优化,进一步提高其酶活力。本实验旨在为产β-葡萄糖苷酶菌株的开发和应用提供高效菌种。
1 材料与方法
1.1 材料与仪器
1.1.1 样品
2018年1月份,在河南南阳独山森林公园随机挑选10个地点,每个地点相距约500 m,采集腐木样品,装入已灭过菌的牛皮纸袋内,封袋,并在每个袋上记录下取样地点和时间,置于4 ℃保存,备用。
1.1.2 仪器与设备
ZWYR-D2403恒温培养振荡器,上海智城分析仪器制造有限公司;ARTP诱变育种仪,无锡源清天木生物科技有限公司;JW-2019H台式高速离心机,安徽嘉文仪器装备有限公司;V-1200分光光度计,翰艺仪器(上海)有限公司。
1.1.3 培养基
马铃薯葡萄糖琼脂培养基(potato dextrose agar,PDA)培养基:200 g土豆去皮切块,加纯水煮沸30 min后用4层纱布过滤,将滤液用ddH2O定容至1 L,分别加入20 g葡萄糖和15 g琼脂粉,完全溶解后分装入三角瓶中,待灭菌。
七叶苷培养基:蛋白胨10 g,酵母粉3 g,NaCl 5 g,七叶苷0.1 g,柠檬酸铁铵0.2 g,加dd H2O 1 L,溶解后加入15 g琼脂粉,混匀分装入三角瓶中,待灭菌。
基础发酵培养基(每100 mL):3 g麸皮,0.4 g (NH4)2SO4,0.6 g KH2PO4,0.1 g MgSO4·7H2O,0.05 g CaCl2,0.01 g FeSO4。
所有培养基均在0.1 MP,121 ℃条件下灭菌20 min。
1.2 实验方法
1.2.1 菌株筛选
分别称取采集于10个不同地点的腐木样品5 g,在无菌研钵中充分研碎,过40目筛,除去杂质和未研碎的大颗粒物。将所有腐木粉置入100 mL无菌离心管内,在振荡器上连续振荡10 min,将样品混匀。从上述混合样品中称取1 g腐木粉,加20 mL ddH2O,转入100 mL无菌锥形瓶中,28 ℃,150 r/min振荡30 min,取出静置20 min,取上清液以10倍的浓度梯度差进行稀释,分别将10-3、10-4和10-5倍稀释液涂布于PDA平板(含50 μg/mL的氨苄青霉素)上,倒置,28 ℃恒温培养。每天观察,及时分离新长出的菌落,并多次纯化至纯培养。用七叶苷培养基定性检测纯化菌株是否产β-葡萄糖苷酶,根据变色圈的大小和颜色,挑选相关产酶菌株进行摇瓶发酵培养,定量测定发酵液中β-葡萄糖苷酶活力。
1.2.2 酶活测定
取1 mL发酵液,8 000 r/min离心10 min,吸取上清液稀释10倍后得到粗酶液。参考刘德海[19]的方法制作标准曲线,得到回归方程:Y=0.161 3x-0.005 2,相关系数R2=0.999 8,再检测酶活。
1.2.3 菌株鉴定
1.2.3.1 菌株形态观察
将复筛所得菌株接种在PDA平板上,28 ℃恒温培养2~5 d,观察菌落的生长速度、菌落形态和颜色等。插片法观察菌丝形态,孢子大小和形态等。
1.2.3.2 菌株分子生物学鉴定
采用CTAB法[20]提菌株基因组,在生工生物公司合成引物ITS序列通用引物ITS1:5’-TCCGTAGGTGAACCT-3’和ITS4:5’-TCCTCCGCTTATTGATATGC-3’;持家基因BenA引物Bt2a:5’-GGTAACCAAATCGGTGCTGCTTTC-3’和Bt2b:5’-ACCCTCAGTGTAGTGACCCTTGGC-3’[21],总反应体系为25 μL:上下游引物各1 μL,rTaq 0.15 μL,10×buffer 2.5 μL,dNTP 2 μL,dd H2O 17 μL,g DNA 1 μL。PCR反应程序为:94 ℃ 4 min;94 ℃ 45 s,55 ℃ 30 s,72 ℃ 1 min,循环33次;72 ℃ 5 min。PCR产物经1%琼脂糖凝胶检查,根据其结果,挑选相关PCR产物送上海生物工程公司测序,将测序成功的序列在NCBI数据库中进行Blast比对,用MEGA 6.0构建系统发育树。
1.2.4 复合诱变
1.2.4.1 孢子悬液的制备
用15%的无菌甘油冲洗培养7 d的固体平板,收集菌悬液于小三角瓶中,在28 ℃摇床中振荡培养1 h,用8层无菌纱布过滤,得到单孢子悬浮液,用15%的无菌甘油将其定容至108个/mL,备用。
1.2.4.2 ARTP诱变
参考ZOU等[22]的方法,把加有10 μL孢子悬液的圆形铁片放在操作室的凹槽中,设置电源功率110 W,气流量10 SLM,处理距离为2 mm,分别处理0、30、60、90、120、150,180、210、240、270、300 s。将处理完的小铁片分别放入装有1 mL无菌水的EP管中,振荡混匀后进行梯度稀释,取100 μL 10-3倍稀释液涂布于PDA平板上,28 ℃恒温培养2 d,进行单菌落计数,计算致死率,实验重复3次。
选取致死率为80%的照射时间对菌株进行诱变,挑取形态发生较大变化的单菌落于七叶苷平板上,培养2~3 d后观察产酶变色圈的大小,根据其结果,选取变色圈较大的菌株进行活化,通过发酵培养,测定发酵液中β-葡萄糖苷酶活力,挑选酶活力提高最大的突变菌株,10 ℃斜面保存,备用。
1.2.4.3 DES化学诱变
以ARTP诱变筛选到的高酶活突变菌株,制备孢子悬液,方法同1.2.4.1。参考文献[23],具体方法如下:每0.1 mL孢子悬液加9.9 mL磷酸缓冲液(pH 7.0),分别加入0、20、40、60、80、100 μL DES原液,使DES的体积分数为0、0.2%、0.4%、0.6%、0.8%和1.0%,28 ℃摇床振荡培养20 min,加入1 mL Na2S2O3溶液终止反应,混匀后进行10倍浓度差的梯度稀释,将100 μL 10-3倍稀释液涂布于PDA平板上,28 ℃恒温培养2 d,计算单菌落和致死率,实验重复3次。参照ARTP诱变筛选高产菌方法进行酶活力提高的突变株筛选。
1.2.4.4 遗传稳定性研究
将筛选得到的高产酶菌株,依次连续传代培养6次,测定每个时代各菌株发酵液酶活力,判断突变菌株的遗传稳定性。挑选经过6次传代,酶活力变化幅度不明显的菌株,于10 ℃斜面保存,备用。
1.2.5 发酵条件优化
Plackett-Burman预实验表明,碳源添加量、氮源添加量和装液量3个因素的P值都小于0.05,这3个因素是影响发酵条件和酶活力的显著因素性,因此,选择这3个因素进行响应面分析。
用Design Expert 8.0软件设计试验,选择三因素三水平实验,响应值为酶活力,每个实验重复3次,取平均值。实验设计见表1。
表1 响应面分析试验因素及水平
Table 1 Code and level of independent variables used for response surface methodology

水平碳源添加量/(g·L-1)氮源添加量/(g·L-1)装液量/mL-135450045765+1551080
2 结果与分析
2.1 产β-葡萄糖苷酶菌株筛选
2.1.1 七叶苷平板初筛
将分离纯化的菌株接种在七叶苷平板上,观察菌落生长情况和培养基颜色变化,从26种菌株中挑选出9种产酶变色圈较大的菌株,编号为L1~L9,如图1所示。
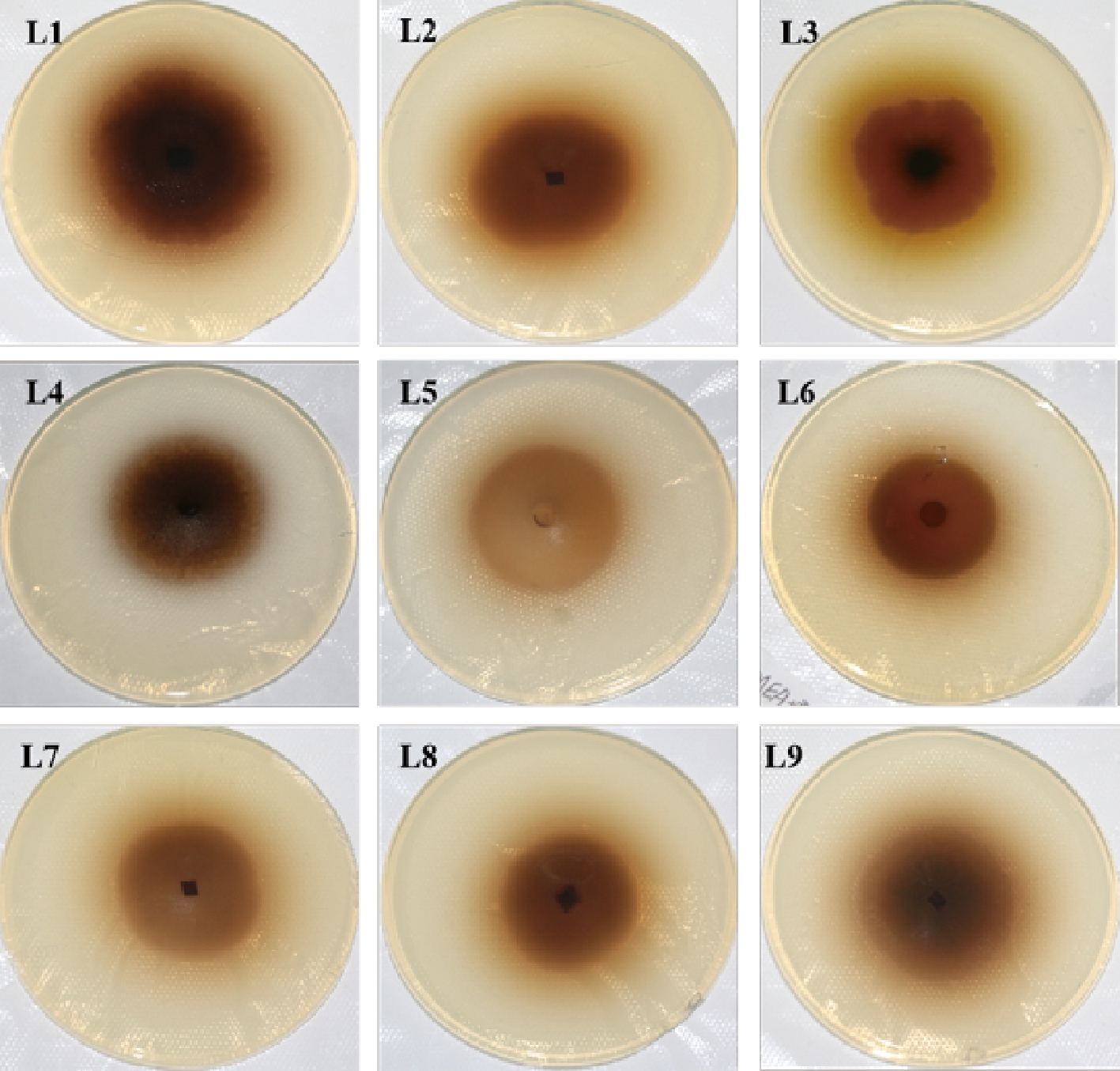
图1 七叶苷平板初筛产β-葡萄糖苷酶菌株
Fig.1 Preliminary screening of strains producing β-glucosidase on esculin agar plates 注:图中L1~L9为菌株编号。
L1菌株的产酶变色圈明显大于其它菌株,且颜色深于其它菌株,推测L1菌株可能有较高的β-葡萄糖苷酶活性,因此初步确定以L1作为后续研究菌株。
2.1.2 摇瓶发酵复筛
为定量测定L1~L9这9个菌株的β-葡萄糖苷酶活力,用基础产酶发酵培养基,分别对这9个菌株进行摇瓶发酵培养,5 d后测定各发酵液酶活力,实验重复3次,取酶活平均值,结果见图2。
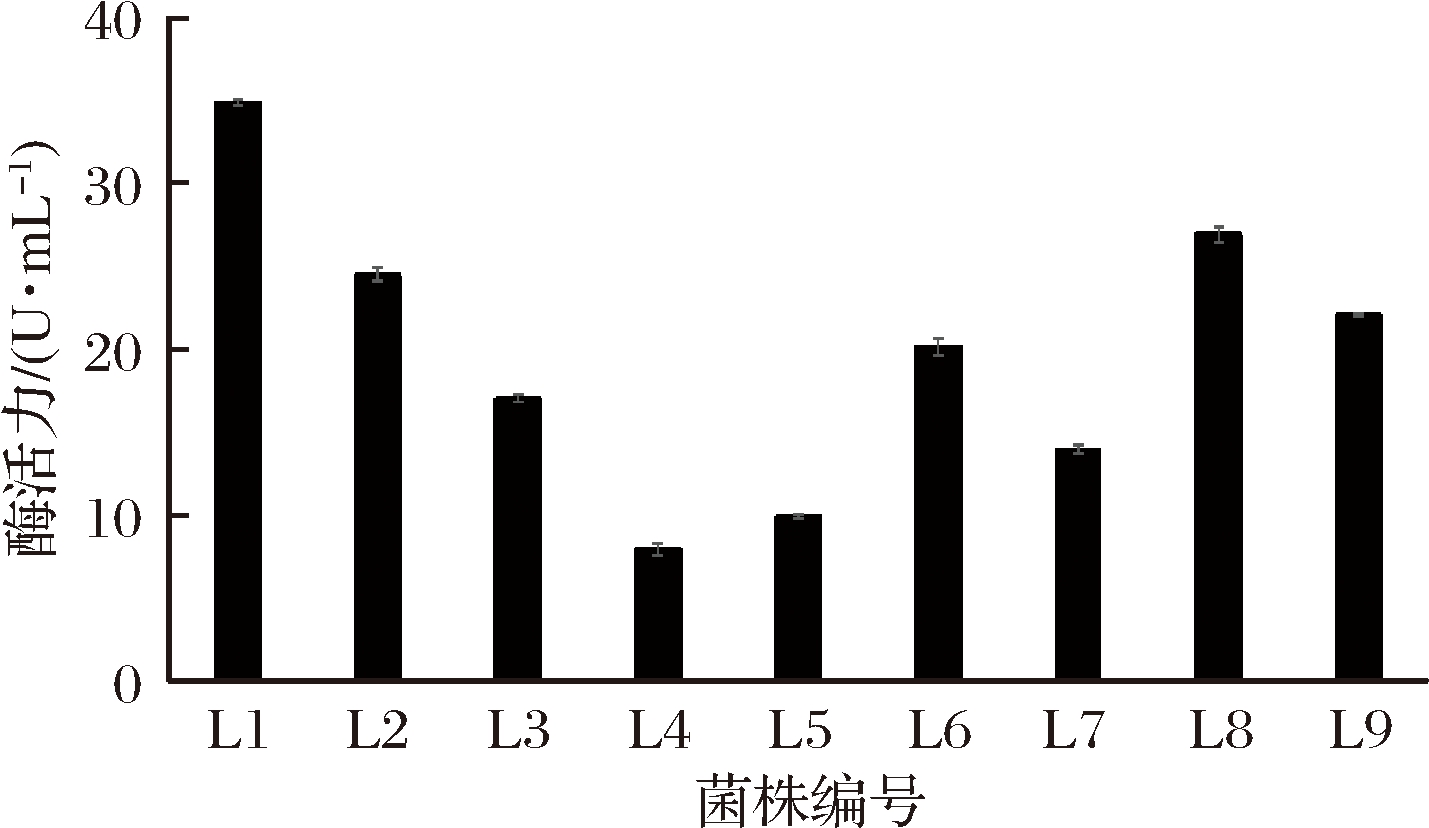
图2 L1~L9菌株发酵液的β-葡萄糖苷酶活统计
Fig.2 The activity of β-glucosidase in fermentation broth of strain L1~L9
定量实验结果表明,L1菌株经基础产酶培养基发酵时,其酶活力平均值达34.85 U/mL,L2~L9菌株的酶活力平均值依次为24.49、16.98、7.92、10.00、20.17、14.00、26.91和22.03 U/mL,L1菌株酶活力最高,结合2.1.1定性实验结果,选择L1作为后续诱变及发酵产酶菌株。
2.2 菌种鉴定
2.2.1 形态学观察
将菌株L1接种于PDA平板上,28 ℃恒温培养5 d,可以看到该菌株菌落的中间呈灰绿色粉末状,且表面有渗出液,菌落边缘呈白色气生菌丝,菌落背面为米白色,如图3-a、3-b所示。用插片法观察L1在PDA平板上培养3 d后的菌丝显微形态,如图3-c所示,该菌株形成无隔菌丝,分生孢子头顶端膨大成典型的扫帚状,分生孢子呈球形,直径约2.5 μm,是典型的青霉菌属形态特征,推测该菌株可能是青霉属的一个种。
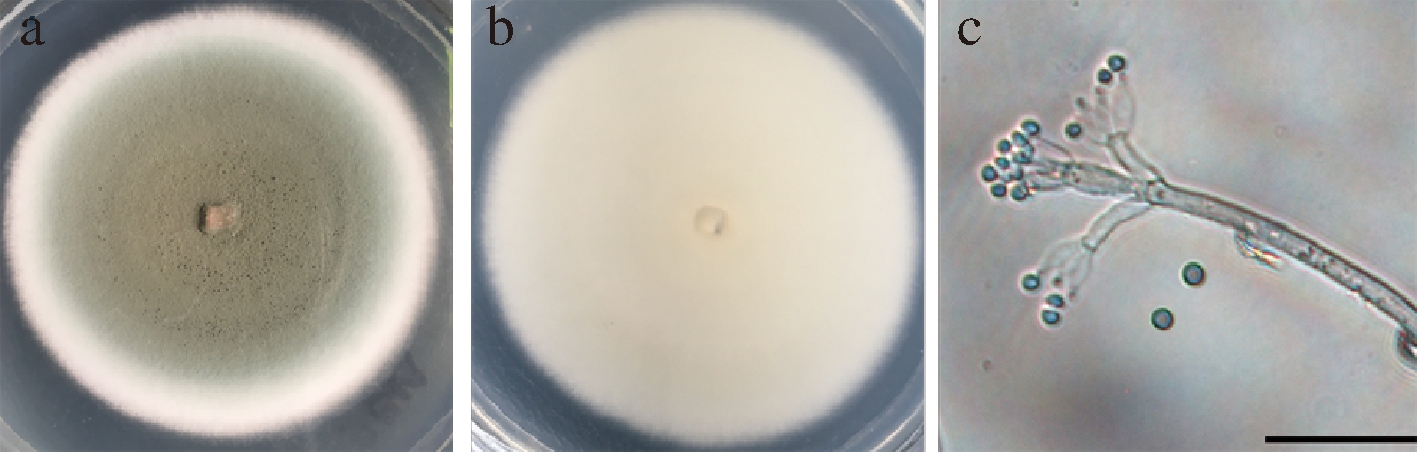
图3 菌株L1在PDA平板上的菌落形态及显微形态(C图中比例尺为20 μm)
Fig.3 Colony morphology and micromorphology of strain L1 on PDA plate
2.2.2 分子鉴定
为了鉴定该菌株,以其基因组DNA为模板,分别以ITS1/ITS4和Bt2a/Bt2b为引物,扩增L1菌株的ITS序列和持家基因BenA。获得了长度为545 bp的ITS序列和414 bp的BenA序列,将序列分别在NCBI数据库中进行Blast比对,结果显示,L1菌株的ITS序列与已报道的赭绿青霉(Penicillium ochrochloron)的序列相似性达99.45%,持家基因BenA与P.ochrochloron的序列相似性达94.21%,结合菌株形态特征以及分子鉴定的结果,认为L1菌株属于青霉属的P. ochrochloron。根据序列的相似性比对结果,挑选相关菌株的BenA和ITS序列,将2个序列进行组合,用MEGA 6.0软件构建系统发育树如图4所示,光滑青霉菌(P. glabrum)为外群。
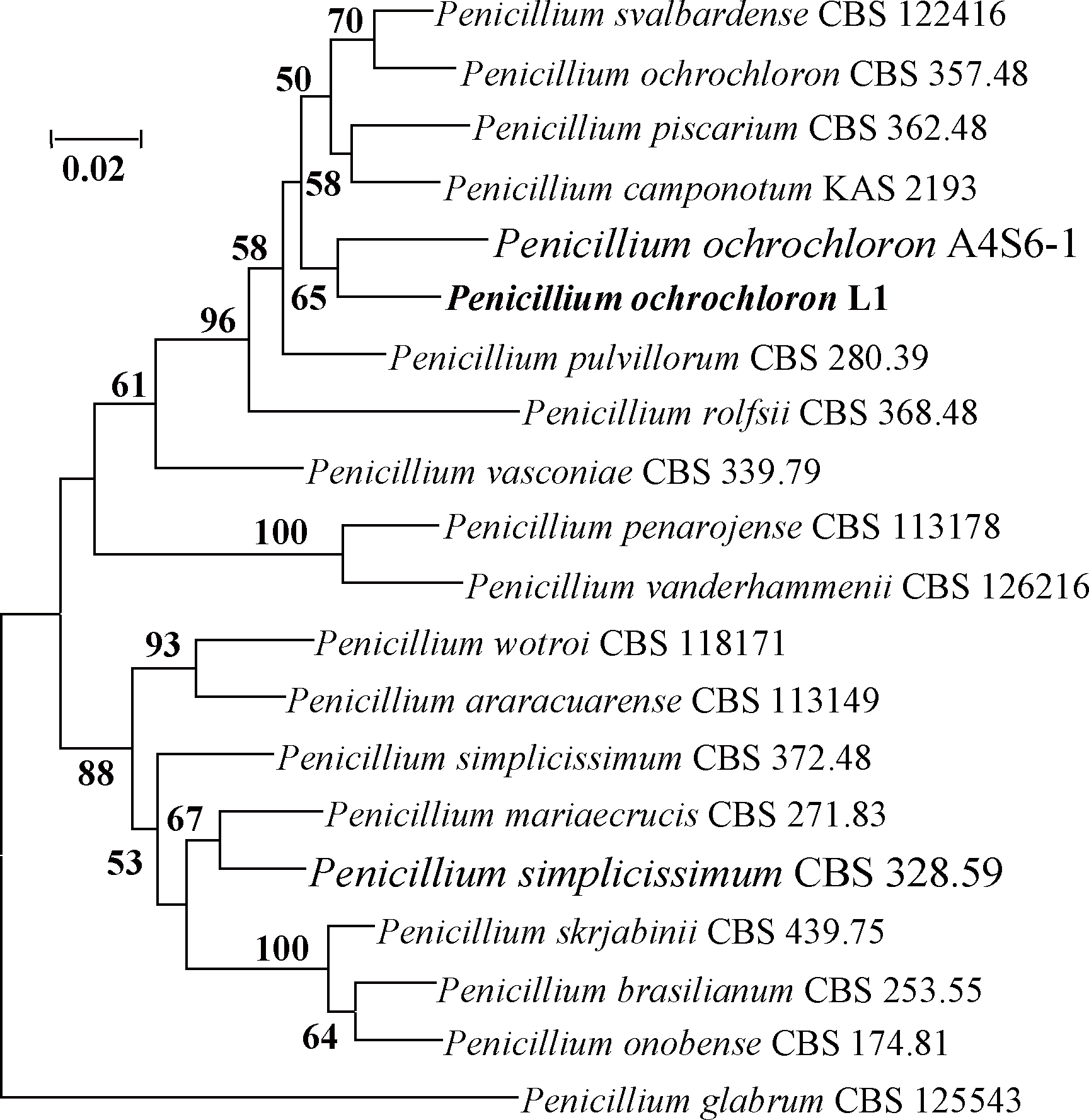
图4 最大似然法构建菌株L1基于BenA和ITS序列的系统发育树
Fig.4 Phylogenetic tree obtained Maximum-Likelihood analysis based on a combined data set of BenA and ITS sequences of strain L1
2.3 诱变结果
2.3.1 ARTP诱变
2.3.1.1 致死率曲线
ARTP诱变中的等离子体富含多种化学活性粒子,能引起细胞膜通透性和蛋白质物质发生改变,同时会造成菌株DNA的损伤,导致照射时间越长,菌株的存活率就越低。为确定最佳诱变时间,将L1菌株的孢子悬浮液置于ARTP诱变仪中,分别照射0、30、60、90、120、150,180、210、240、270和300 s,将照射后的悬浮液进行稀释,根据预实验中关于不同浓度孢子悬液与单菌落数的关系(结果未显示),选择10-3倍稀释液涂布于PDA平板上,28 ℃恒温倒置培养2 d,实验重复3次,统计各个平板上单菌落数,取平均值,制作诱变时间-致死率曲线,结果见图5。
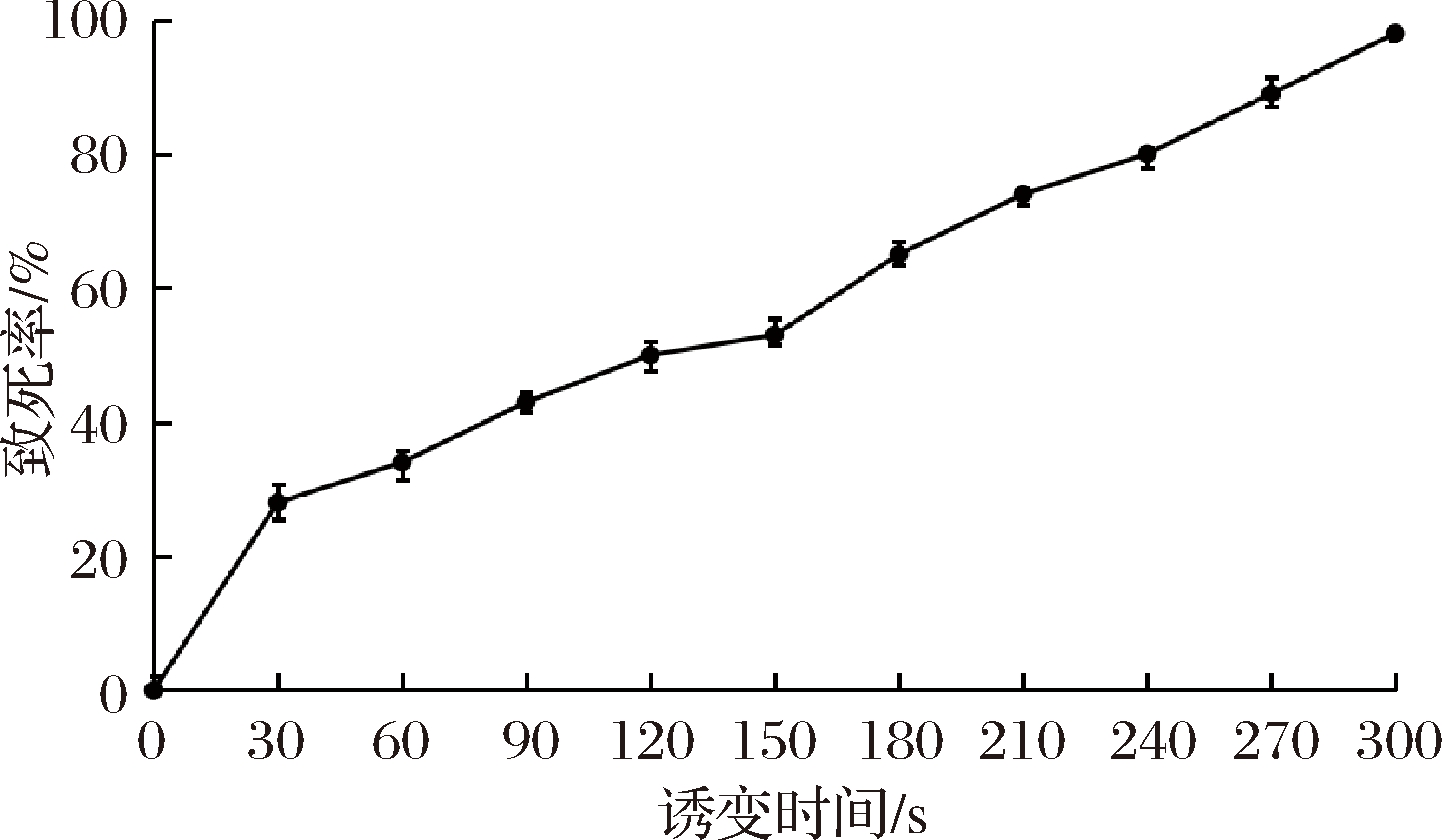
图5 ARTP诱变不同时间的致死率曲线
Fig.5 Curve of the mutagenized death rate of different ARTP mutation time
不同处理时间所对应的单菌落数分别为225、162、149、128、112、106、79、58、45、25、5,对应致死率分别为:0、28%、34%、43%、50%、53%、65%、74%、80%、89%和98%。由此可见,不同的诱变时间导致菌株致死率变化较大,对于ARTP和DES诱变来说,通常选择致死率为75%~85%所对应的诱变条件为最佳参数,结合本实验的测定结果,ARTP诱变时间为240 s,致死率为80%。因此,选择对L1菌株的ARTP最佳诱变时间为240 s。
2.3.1.2 ARTP诱变突变株酶活力测定
以L1为出发菌株,以240 s作为ARTP诱变的最佳时间进行诱变,挑选与出发菌株L1有较大形态差异的40~50个突变菌,定性检测这些菌株在七叶苷平板上的产酶变色圈,筛选出8~10株产酶变色圈较大的突变株,将其活化后通过摇瓶发酵,测定酶活力,重复ARTP诱变20次。结果共筛选出180株在七叶苷平板上产酶变色圈较大突变菌株,进一步进行发酵产酶酶活力测定,结果显示,其中有15株突变菌株的酶活力提高明显,与出发菌株L1相比,提高比例高于40%,15株突变菌株的编号依次为:A-1~A-15,结果如图6所示。其中,突变菌株A-2的发酵液酶活力为57.84 U/mL,比出发菌株L1的酶活提高了52%,高于所有突变株酶活力,故挑选该菌株作为后续DES诱变处理的出发菌株。

图6 ARTP诱变部分突变株与L1菌株的β-葡萄糖苷酶活比较
Fig.6 Comparison of the partially ARTP mutation strains and the strain L1 on β-glucosidase activity
2.3.2 DES诱变
2.3.2.1 致死率曲线
DES是一种高效化学诱变剂,预实验结果发现,1%的DES浓度对突变菌株A-2的致死率已接近100%。为确定最佳的诱变剂量,设置0、0.2%、0.4%、0.6%、0.8%和1.0% DES体积分数梯度,对应平板单菌落个数分别为272、202、143、94、54和7,其致死率分别为0、25%、47%、65%、80%和97%,制作DES浓度-致死率曲线,如图7所示。考虑到诱变致死率为75%~85%之间时正突变比例较高[24],结合本实验结果,选择0.8% DES体积分数作为最佳诱变剂量。
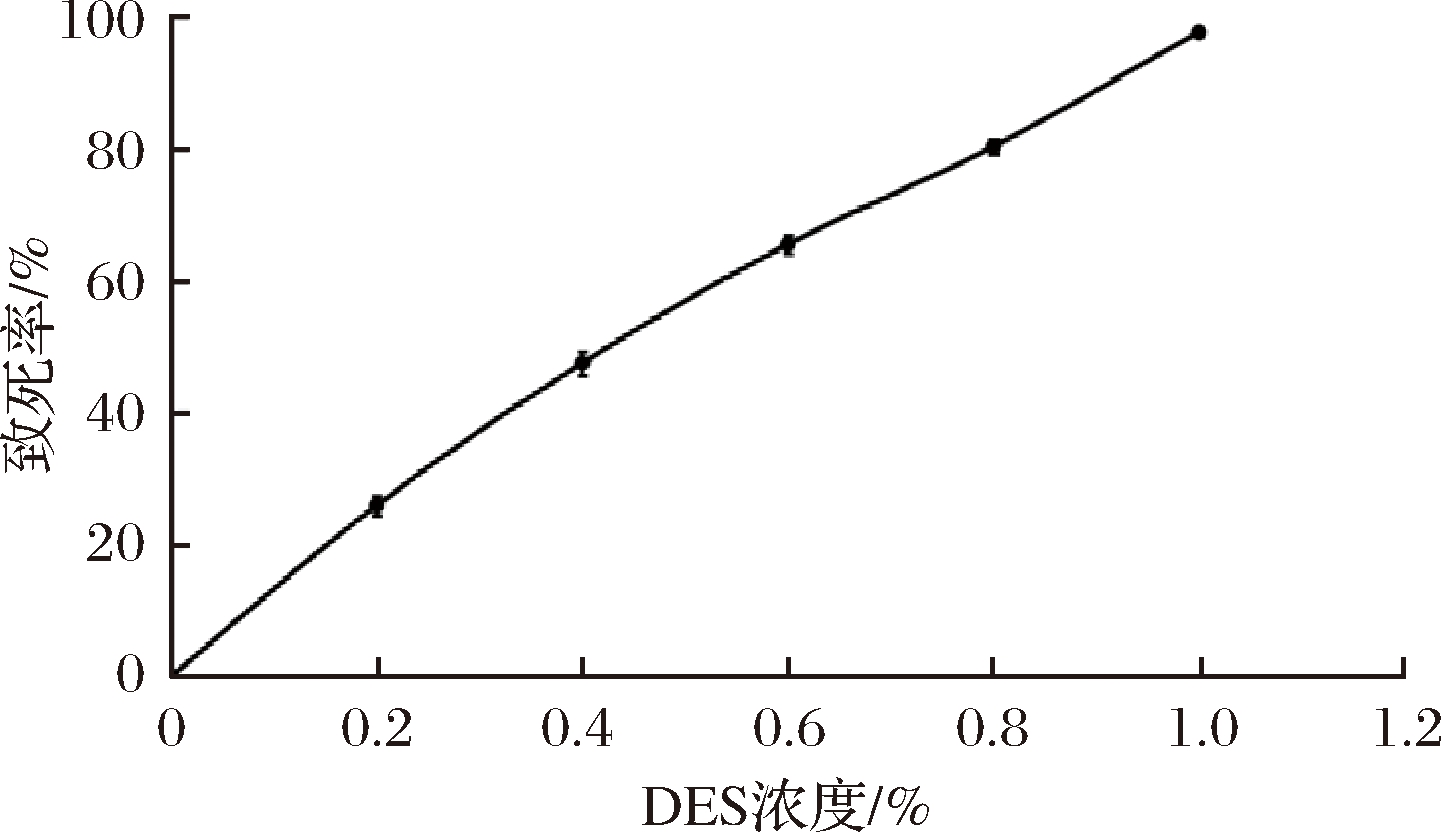
图7 DES诱变致死率曲线
Fig.7 Lethality of DES concentration to strain A-2
2.3.2.2 DES诱变突变株酶活力测定
以ARTP诱变筛选到的突变菌株A-2为出发菌株,进行DES化学诱变,高产酶突变菌株的初筛方法同ARTP诱变,共挑选出100株在七叶苷平板上产酶变色圈较大的突变菌,经摇瓶发酵培养后,计算各突变菌株酶活,并与出菌株A-2的酶活进行比较,最终挑选出10株酶活提高30%以上的突变株,突变菌株编号依次为D-1~D-10,结果见图8所示,其中,D-6菌株酶活力为94.74 U/mL,高于其他各突变菌株,且比出发菌株A-2的酶活力提高了75.1%,比初始菌株L1提高了148.2%。
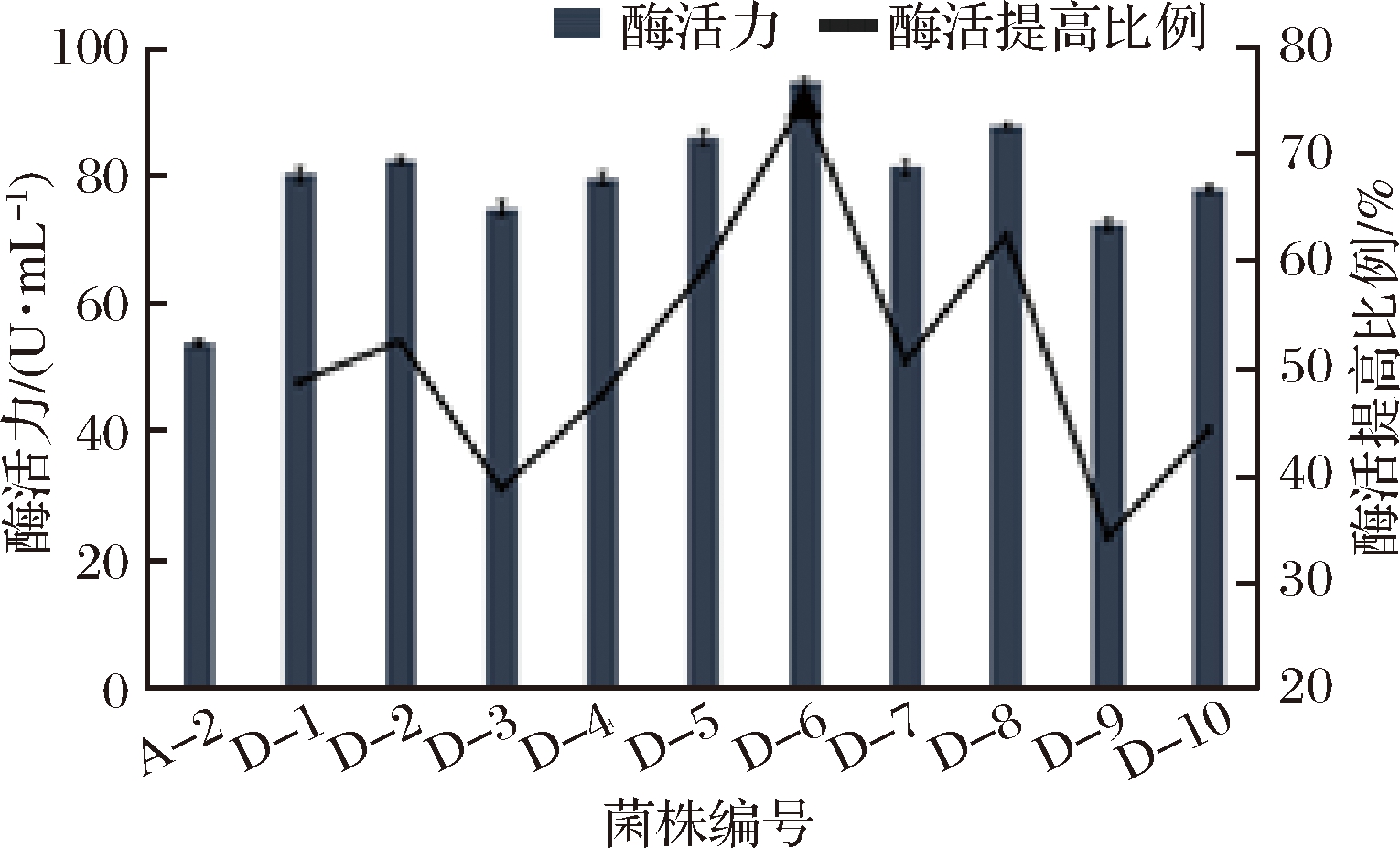
图8 DES诱变部分突变株与A-2菌株的β-葡萄糖苷酶活比较
Fig.8 Comparison of the partially DES mutation strains and the strain A-2 on β-glucosidase activity
2.3.3 遗传稳定性检验
为检测产酶活力明显提高的突变株D-6的遗产稳定性,将突变株D-6依次传代培养6次,对每一代进行摇瓶发酵,实验重复3次,测定各代菌株的β-葡萄糖苷酶活力,以酶活力平均值-传代次数作图,结果见图9,各代菌株的酶活力分别为:94.94、91.79、93.54、92.89、92.07和90.90 U/mL,不同世代酶活力差异不显著,表明突变株D-6的遗传稳定性良好,可作为后续发酵实验菌株。
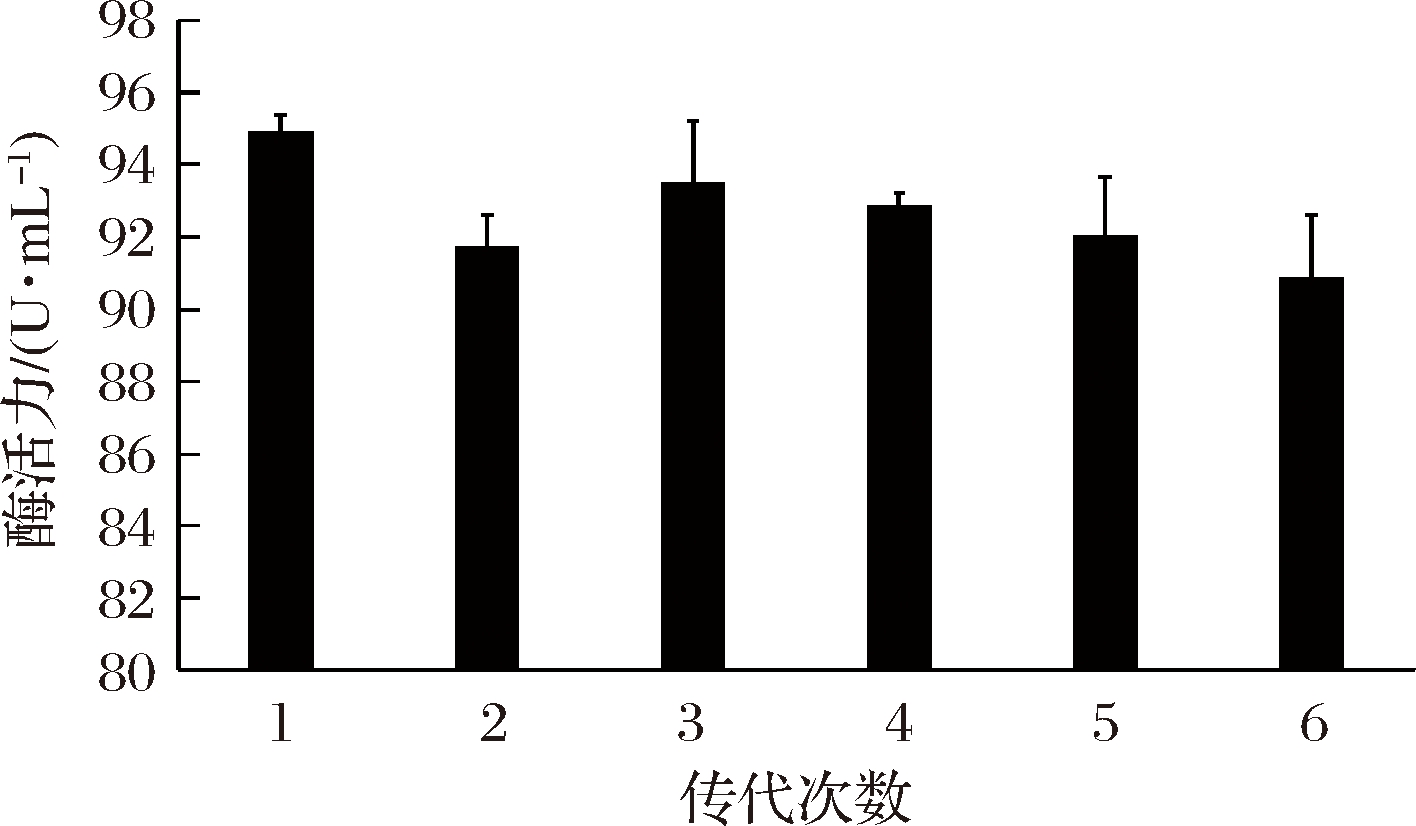
图9 突变菌株D-6的发酵液酶活稳定性检测
Fig.9 Detection of enzyme activity stability in fermentation broth of mutant strain D-6
2.4 响应面实验
2.4.1 Box-Behnken响应面分拆
Box-Behnken响应面实验结果见表2,酶活力Y与显著因子之间的回归方程为:
模型中二次项系数均为负数,表明该模型抛物面开口向下,有极大值点。该模型的R2值为0.983 4,校正系数R2 Adj值为0.962 1,表明回归模型可以说明98.34%响应值的变化,说明该模型拟合程度高,能较好地预测发酵条件与菌株产酶活性的关系,精密度大于4.0,视为合理且拟合程度良好。回归方程一次项系数绝对值的大小决定了各因素对响应值影响的主次顺序,本实验中各因素对响应值影响排序为:装液量(X5)>碳源添加量(X1)>氮源添加量(X2)。
表2 Box-Behnken试验结果
Table 2 Box-Behnken test design combination and results
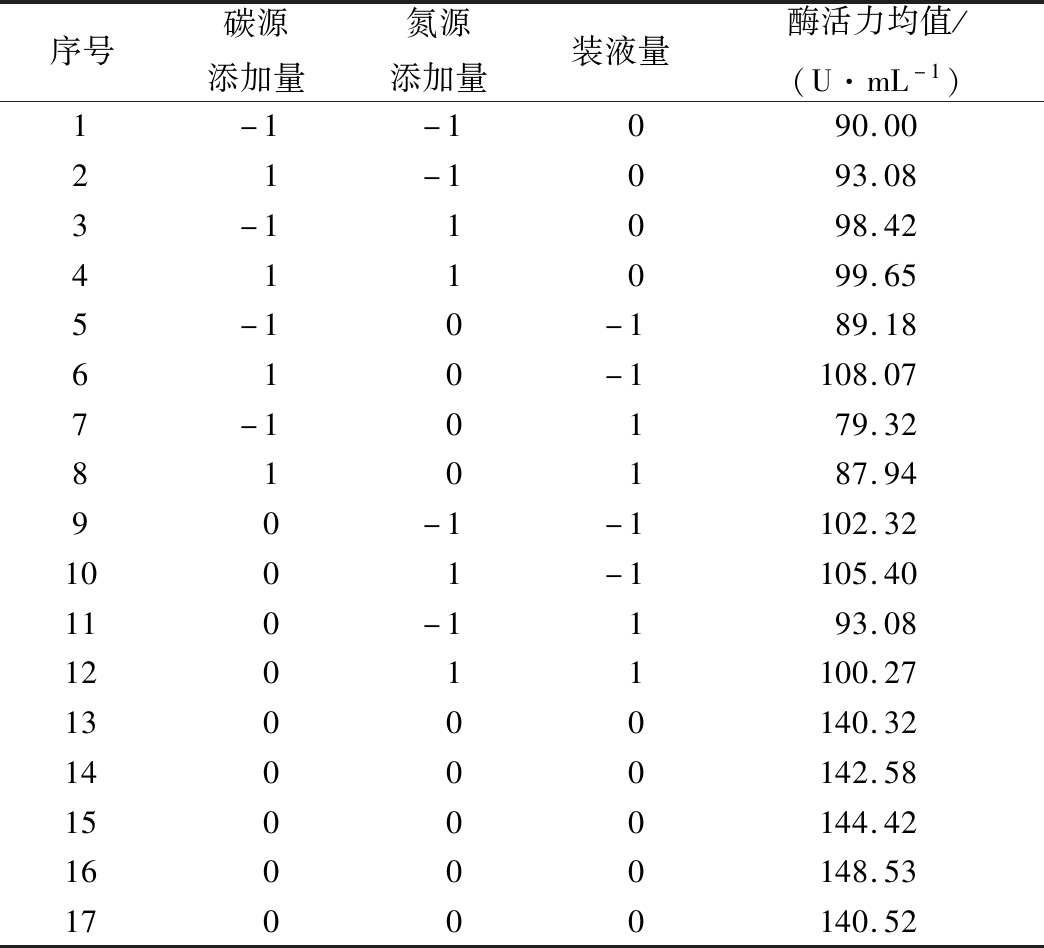
序号碳源添加量氮源添加量装液量酶活力均值/(U·mL-1)1-1-1090.0021-1093.083-11098.42411099.655-10-189.18610-1108.077-10179.32810187.9490-1-1102.321001-1105.40110-1193.0812011100.2713000140.3214000142.5815000144.4216000148.5317000140.52
方差分析表明,模型P值小于0.000 1,说明该模型极显著;失拟项P值为0.162 8,大于0.05,说明此模型建立有效。综合以上回归模型分析和预测发酵条件对菌株产酶活性影响的结果,回归模型系数显著性结果显示,X5-装液量的一次项、X1-碳源添加量的一二次项对菌株产酶活性回归模型影响显著(P<0.05),X2-氮源添加量一次项对菌株产酶活性回归模型影响不显著(P>0.05)。3个因素的二次项对该模型的影响均不显著(P>0.05),3因素的交互项影响均不显著(P>0.05)。
2.4.2 响应面试验最佳条件与模型验证
对碳源添加量(X1)、氮源添加量(X2)、装液量(X5)进行交互分析,发现3个因素均存在极值点,且响应面覆盖了最大值所在的区域。利用Design-Expert 8.0.6软件进行参数优化,得到的最佳产酶条件是:KH2PO4 6 g/L、MgSO4·7H2O 1 g/L、CaCl2 0.5 g/L、FeSO4 0.1 g/L,初始pH 5.2,接种量5%(孢子浓度108个/mL),碳源添加量(X1) 玉米秸秆45.74 g/L、氮源添加量(X2) (NH4)2SO4 7.23 g/L、装液量(X5) 63.21 mL/250 mL,发酵温度28 ℃,摇床转速160 r/min,发酵时间132 h,D-6菌株的β-葡萄糖苷酶活力为143.88 U/mL。验证性实验表明,D-6菌株的酶活力均值为142.92 U/mL,与预测值的误差很小,且与基础培养基发酵后的酶活92.69 U/mL相比,酶活提高了54.2%。综上所述,响应面法优化产酶条件准确可靠,具有一定的实用价值。
3 结论
从腐木样品中分离出来1株可以产β-葡萄糖苷酶的青霉菌株L1,经过ARTP-DES复合诱变获得1株具有较好遗传稳定性的突变菌株D-6,其发酵液酶活力比初始菌株L1提高了148.2%。通过响应面法进行发酵条件优化,结合软件分析和实验所得结果,得到D-6突变株产β-葡萄糖苷酶的最佳条件,且在此条件下,测得菌株酶活力可达142.92 U/mL,比基础培养基发酵时酶活提高了54.2%;与出发菌株L1相比,酶活力提升了274.4%。在本实验范围内建立的二次回归模型准确有效,可用来预测发酵产酶条件曲工艺参数,对实验有较好拟合性,具有一定的实用价值。
[1] 苏敏,朴春红,梁德春,等.产β-葡萄糖苷酶酵母菌的分离鉴定及其在人参皂苷Rg3转化中的应用[J].食品科学,2018,39(14):172-178.
[2] 苏龙,梁广波,龙文英,等.产β-葡萄糖苷酶罗尔夫青霉发酵条件的优化[J].贵州农业科学,2017,45(2):105-111.
[3] SU Linhui,ZHAO Shuai,JIANG Suixin.et al.Cellulase with high β-glucosidase activity by Penicillium oxalicum under solid state fermentation and its use in hydrolysis of cassava residue[J].World J Microbiol Biotechnol,2017,33: 37.
[4] JUTURU V,WU J C.Microbial cellulases:Engineering,production and applications[J].Renewable and Sustainable Energy Reviews,2014,33:188-203.
[5] 刘欢,李皓,陈长武,何文兵.β-葡萄糖苷酶对‘双优’干红葡萄酒理化性质和香气物质的影响[J].食品与发酵工业,2018,44(11):138-146.
[6] RUCHI A,VERMA A K,SATLEWAL A.Application of nanoparticle-immobilized thermostable β-glucosidase for improving the sugarcane juice properties[J].Innovative Food Science and Emerging Technologies,2016,33:472-482.
[7] 姚瑶,霍元鹏,周伟,等.高产β-葡萄糖苷酶菌株的筛选及产酶条件优化[J].江西农业学报,2018,30(3):97-101.
[8] YAO Guangshan,WU Ruimei,KAN Qinbiao,et al.Production of a high-efficiency cellulase complex via β-glucosidase engineering in Penicillium oxalicum[J].Biotechnol Biofuels,2016,9:78.
[9] 李永博,李星,唐敏,等.浓香型大曲中产β-葡萄糖苷酶微生物的筛选鉴定及其产酶条件优化[J].食品科技,2017,42(12):17-22.
[10] 王凤梅,张邦建,岳泰新.葡萄酒相关酵母β-葡萄糖苷酶活性及影响因素研究[J].中国酿造,2018,37(7):83-87.
[11] ÇELIK A,DINÇER A,AYDEMIR T.Characterization of β-glucosidase immobilized on chitosan-multiwalled carbon nanotubes (MWCNTS) and their application on tea extracts for aroma enhancement[J].International Journal of Biological Macromolecules, 2016,89:406-414.
[12] 李豪,白光剑,吴静,等.紫外-常压室温等离子体复合诱变高产纤维素酶真菌[J].食品与发酵工业,2019,45(15):81-86.
[13] LI Xiangyu,LIU Ruijie,LI Jing,et al.Enhanced arachidonic acid production from Mortierella alpina combining atmospheric and room temperature plasma (ARTP) and diethyl sulfate treatments[J].Bioresource Technology,2015,177:134-140.
[14] 蒋汶,张庆庆,汤文晶,等.紫外-等离子体复合诱变红曲霉产胞外多糖[J].食品与发酵工业,2016,42(1):64-69.
[15] 宋欣,曲音波,袁晓华.一种将七叶苷用于高产β-葡萄糖苷酶产生菌的平板筛选的方法:CN,101177699A[P].2008-05-14.
[16] SINGH R S,CHAUHAN K.,JINDAL A.Response surface optimization of solid state fermentation for inulinase production from Penicillium oxalicum using corn bran[J].J Food Sci Technol,2018,55:2 533.
[17] BATRA J,BERI D,MISHRA S.Response surface methodology based optimization of β-Glucosidase production from Pichia pastoris[J].Appl Biochem Biotechnol,2014,172:380.
[18] PARK A R,PARK J H,AHN H J,et al.Enhancement of β-Glucosidase activity from a brown rot fungus Fomitopsis pinicola KCTC 6208 by medium optimization[J].Mycobiology,2015,43(1):57-62.
[19] 刘德海,郝益民,岳丹丹,等.一株产β-葡萄糖苷酶菌株的筛选及酶学性质研究[J].中国酿造,2013,32(6):47-51;60.
[20] 钟志敏,赖小平,黄松,等.石斛内生炭角菌DNA提取方法优化及分子鉴定[J].菌物学报,2018,37(1):73-78.
[21] 李慧芳,赵利娜,郑香峰,等.1株产桔青霉素扩展青霉的鉴定及其产毒条件优化[J].食品科学,2018,39(24):162-167.
[22] ZOU Zongsheng,ZHAO Yunying,ZHANG Tingzhou,et al.Efficient Isolation and Characterization of a Cellulase Hyperproducing Mutant Strain of Trichoderma reesei[J].Journal of Microbiology and Biotechnology,2018,28(9):1 473-1 481.
[23] 李聪,扶教龙,施磊,等.ε-聚赖氨酸生产菌的硫酸二乙酯诱变及其发酵培养基优化[J].中国调味品,2018,43(3):34-40.
[24] 熊建春.甘蔗威士忌酯香酵母菌的选育及发酵工艺研究[D].广州:华南理工大学,2010.