Pickering乳液是以纳米固体颗粒为稳定剂的乳液体系,相比于传统液体表面活性剂乳液,Pickering乳液具有稳定性好、乳化剂用量少、制备方便以及环境友好等优势,成为近几年食品乳液领域研究的热点[1-3]。
柠檬醛是一类从植物中提取的天然芳香成分,挥发性强,对光、热和氧气敏感,稳定性较差,这使其应用受到极大的限制[4-5]。将柠檬醛制备成稳定水包油型乳液,可提供柠檬醛的水溶形式,增加其贮存稳定性及应用性能[6-8]。目前关于柠檬醛乳液的报道大多是利用传统液体表面活性剂法[9-11],而利用β-环糊精制备柠檬醛的Pickering乳液还未见报道。
β-环糊精是由7个葡萄糖组成的环状低聚糖,其圆锥形分子内腔具有内疏水、外亲水的结构特性,表现出良好的乳化性能[12]。在水-油体系中,β-环糊精可以通过内腔包埋油相分子、外表面吸附水相,以包合物颗粒形式在油水界面形成界面膜,从而形成稳定的水包油型Pickering乳液体系[13-15]。本文即通过β-环糊精包埋柠檬醛形成纳米级包合物颗粒,来制备水-柠檬醛Pickering乳化体系,研究影响乳液结构及稳定性的因素,以期得到一种新型绿色的柠檬醛乳液制备方法[16]。
1 材料与方法
1.1 材料与仪器
β-环糊精,国药集团;柠檬醛,吉安国光香料厂;黄原胶,酷尔生物工程有限公司;其他试剂均为分析纯,国药集团有限公司。
XHF-D高速分散器,宁波新芝生物科技股份有限公司;Zetasizer NANO-ZS90激光粒度仪,英国Malvern公司;ARES-G2流变仪,TA公司;Phenix PH50- 3A43L-A型光学显微镜,凤凰光学股份有限公司;雷磁PHS-3E型pH计,上海仪电科学仪器股份有限公司;电子分析天平,赛多利斯科学仪器(北京)有限公司。
1.2 方法
1.2.1 β-环糊精稳定柠檬醛Pickering乳液的制备
准确称取一定量的β-环糊精,加入30 mL水后置 60 ℃水浴中加热溶解,再加入一定体积比例的柠檬醛,在10 000 r/min条件下高速均质乳化,每次乳化20 s,间歇10 s,共重复乳化6次,制得β-环糊精稳定的柠檬醛Pickering乳液。
1.2.1.1 油水比对β-环糊精-柠檬醛乳液制备的影响
固定3%的β-环糊精加量,选取油水体积比分别为3∶7、4∶6、5∶5、6∶4、7∶3和8∶2,采用上述Pickering乳液制备方法,研究不同油水体积比对所得乳液体积和粒径的影响。
1.2.1.2 β-环糊精加量对β-环糊精-柠檬醛乳液制备的影响
选取油水体积比为6∶4,β-环糊精加量分别为10、20、30 g/L,按1.2.1制作乳液,研究β-环糊精加量对所得乳液体积和粒径的影响。
1.2.2 β-环糊精-柠檬醛乳液微观结构的观察
取适量β-环糊精-柠檬醛乳液,均匀涂布或适度稀释后涂布在载玻片上,光学显微镜放大100倍观察,并用附带相机对选取的界面进行拍摄。
1.2.3 β-环糊精-柠檬醛乳液平均粒度和Zeta电位的测定
取0.5 mL乳状液,加入9.5 mL蒸溜水摇匀(稀释10倍),立即利用激光粒度仪分别对乳液粒度和Zeta电位进行测定,平行进行3次,取平均值。
1.2.4 黄原胶对β-环糊精-柠檬醛乳液稳定性的影响
选取油水体积比为6∶4、β-环糊精加量为3%,高速均质后添加水相质量浓度0.5%的黄原胶(预先配制成2%的溶液),再5 000 r/min均质20 s,研究体系添加黄原胶对乳液稳定性(粒径及Zeta电位)的影响,同时利用流变仪测定黄原胶添加前后乳液体系粘度的变化。
1.2.5 酸碱度对β-环糊精-柠檬醛乳液稳定性的影响
选取油水体积比为6∶4、β-环糊精加量为30 g/L,用HCl或NaHCO3调节水相的酸碱度分别为pH 3.0、6.5和9,按1.2.1制作乳液,研究酸碱度对乳液稳定性(粒径及Zeta电位)的影响。
1.2.6 加热或冷冻处理对β-环糊精-柠檬醛乳液的影响
加热处理:制备油水体积比为6∶4的β-环糊精-柠檬醛乳液(加或不加黄原胶),在80 ℃水浴条件下加热处理15 min,取出室温冷却,观察乳液稳定性,读取乳化比。
冷冻处理:制备油水体积比为6∶4的β-环糊精-柠檬醛乳液(加或不加黄原胶),放入冰箱-18 ℃存放过夜,第2天放室温自然解冻,观察乳液稳定性,读取乳化比。
1.2.7 乳液的贮存稳定性测定[17]
新制备的乳液在室温、密封条件下存放60 d,量取料液总体积和乳相体积,通过计算乳相体积占总体积的百分比得到乳液的乳化系数,为乳液贮存稳定性指标。
(1)
式中:ESI,为乳化系数, %;V1,贮存后乳相体积,mL;V2,贮存后总料液体积,mL。
1.2.8 乳液黏度的测定
采用ARES-G2流变仪对乳液进行黏度测定。测定条件:选用直径为40nm夹具,设置间隙0.5mm,温度25℃,剪切速率变化范围为:0.01~100 r/s。将乳液均匀涂在圆盘器具上,在乳液的缝隙处均匀涂布一层甲基硅油,测定时记录数据,并用Excel绘图。
2 结果与分析
2.1 β-环糊精稳定柠檬醛Pickering乳液的制备
选取β-环糊精添加量为30 g/L、油水比6∶4,利用高速剪切法对含有β-环糊精的柠檬醛-水体系进行处理,制备得到环糊精稳定柠檬醛Pickering乳液。外观看乳液呈乳白色半流体,质地细腻、均一,具有浓郁的柠檬醛芬芳气味。
将乳液加水搅拌稀释,发现能够均匀分散,说明该乳液属于水包油型[18]。光学显微镜下放大100倍观察,发现乳液微观结构是由球形油滴均匀堆积于水相中而成,大小分布略不均匀,尺寸在数百纳米,如图1所示。
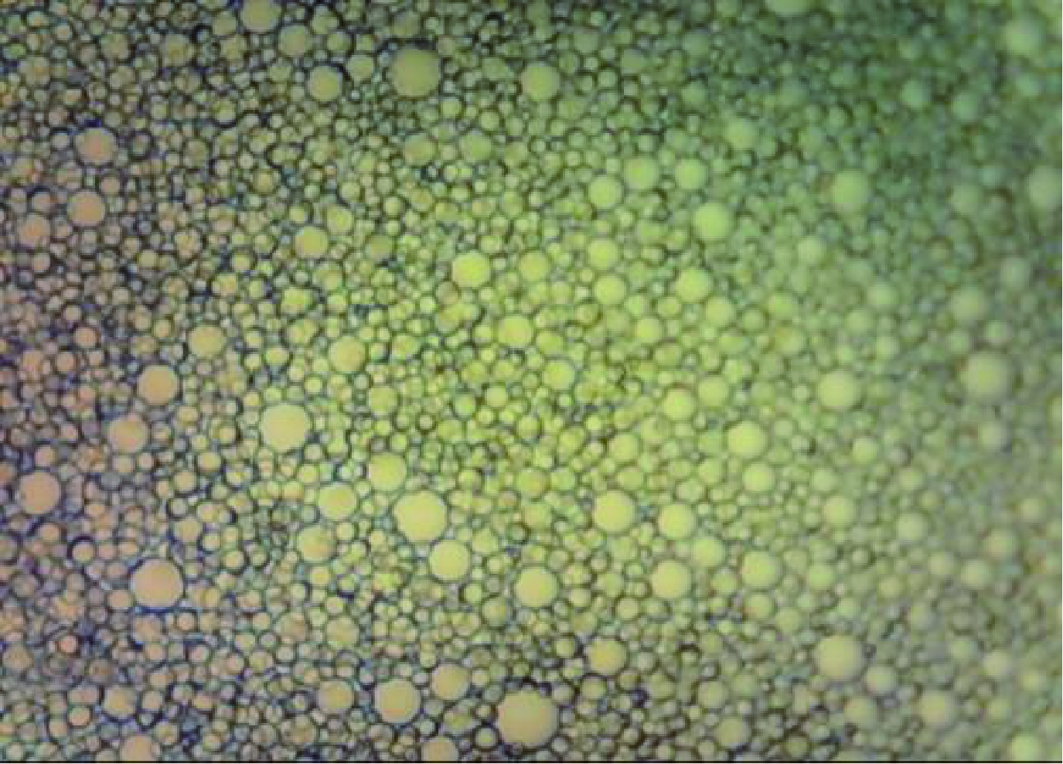
图1 β-环糊精稳定柠檬醛乳液的光学显微结构
Fig.1 Microstructure of citral Pickering emulsion stabilized
by β-cyclodextrin
2.1.1 油水体积比对β-环糊精-柠檬醛乳液制备的影响
选取油水体积比分别为3∶7、4∶6、5∶5、6∶4、7∶3和8∶2,选取β-环糊精添加量30 g/L,乳化制备Pickering乳液,研究不同油水比例对形成乳液体积大小及乳液粒径的影响,结果如图2所示。制备乳液时所用油水体积比对Pickering乳液的形成有很大影响。当柠檬醛和水体积比为6∶4时形成全乳体系,油水体积比低于6∶4时柠檬醛可以全部被乳化,但在乳液相下部会出现水相层,且水相体积随油水比增加而减少。当柠檬醛和水体积比提高至为7∶3时,无水相出现,但会有少量柠檬醛未能乳化;进一步油水体积比提至为8∶2时乳化效果变差,有较多柠檬醛及水不能乳化,形成上层油相、中间乳液相、下层水相的三相体系。这一结果说明控制柠檬醛与水体积比在6∶4~7∶3,可制备柠檬醛含量达70%的乳液;在油水比偏低时体系有较多水相析出,也说明乳液容纳水的能力不强。从乳液微观结构可以看出,β-环糊精稳定的Pickering乳液属于油滴堆积型体系,β-环糊精包合物颗粒形成的界面膜结合外相水的能力有限,因此该体系呈不透明半流体乳液状。
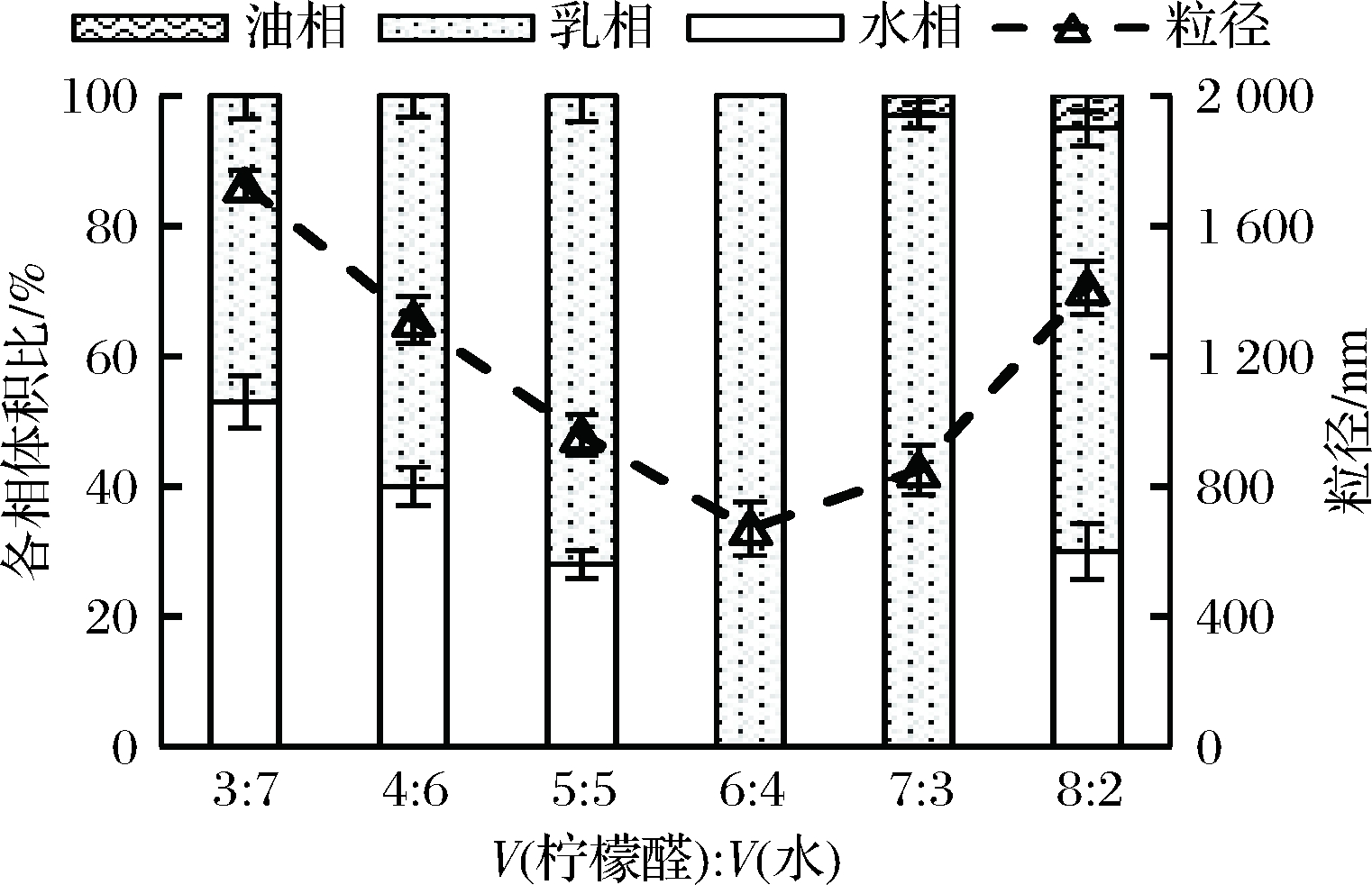
图2 不同油水体积比对乳液形成体积及粒径大小
的影响
Fig.2 Effect of various ratio of oil to water on both
the emulsion volume and particle size
对乳液粒径测定结果显示,随着油水比的改变,乳液的平均粒径也随之改变。当β-环糊精添加量为30 g/L、油水体积比为6∶4时乳液粒径达到最小值670 nm。粒径是判断乳液稳定性的一个重要参数,通常粒径越小稳定性越高[19-20]。
2.1.2 β-环糊精加量对β-环糊精-柠檬醛乳液制备的影响
选取油水体积比为6∶4、β-环糊精加量分别为10、20、30、40 g/L,通过高速乳化制备乳液,观察体系各相体积比,并对乳液粒径大小进行测定。结果如图3所示。在油水体积比6∶4时,除β-环糊精加量为10 g/L时的乳化系数为83%外,β-环糊精加量为20~40 g/L均可使体系全部形成乳液,但乳液的粒径大小有很大差别。随着β-环糊精添加量从10 g/L增加到40 g/L,乳液粒径显著降低(从1 847 nm降至584 nm),说明增加环糊精用量,在乳液细小油滴形成时能够保证有足够多的包合物颗粒吸附于油-水界面以强化界面膜的致密度[21-22],从而达到降低乳液平均粒径、稳定乳液的目的。当β-环糊精加量超过30 g/L时,其用于形成并强化界面膜的浓度接近饱和,乳液粒径也因此变化趋缓。
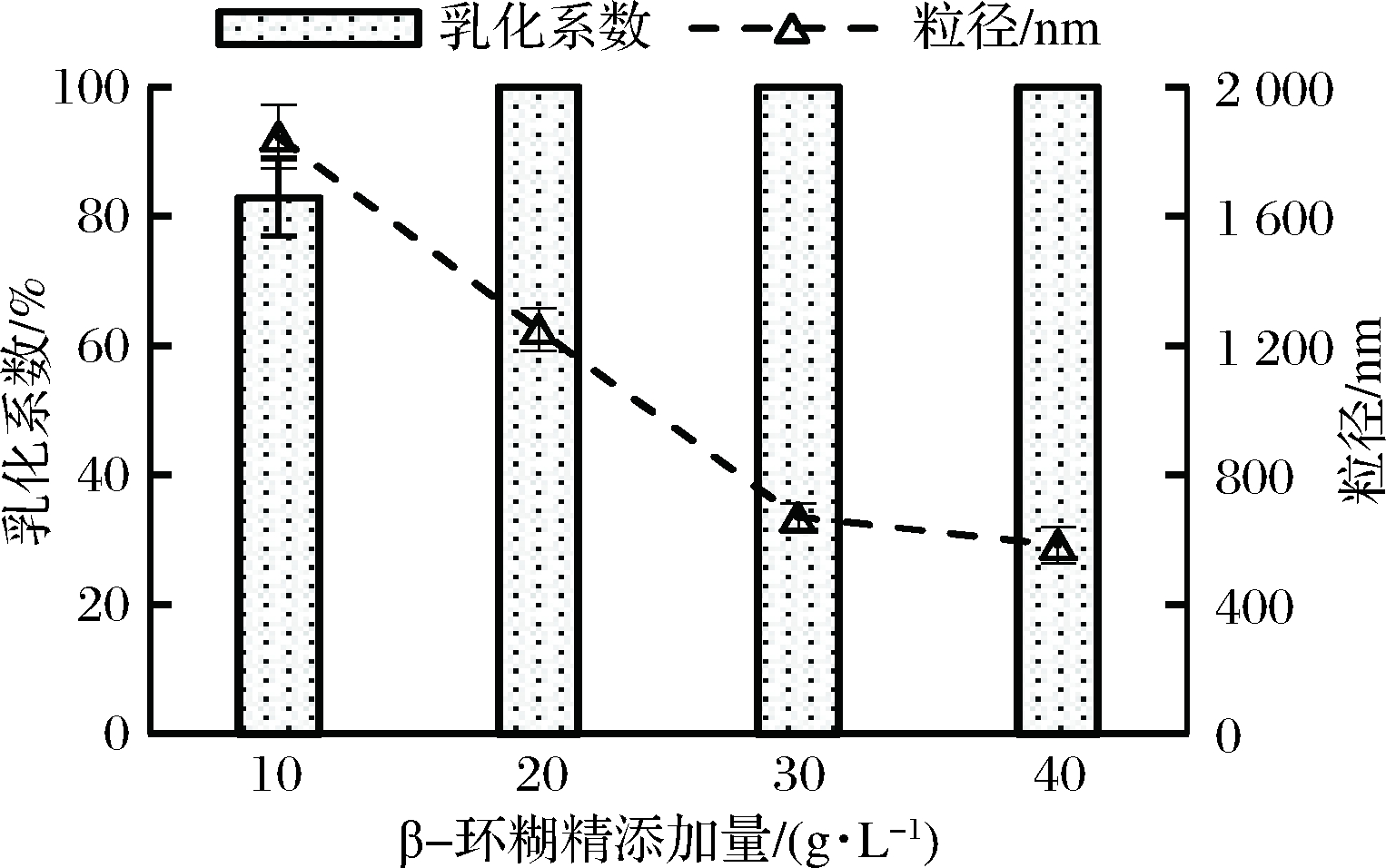
图3 不同β-环糊精加量对乳液体积及粒径
的影响(油水体积比6∶4)
Fig.3 Effects of additive amount of β-CD on both the
emulsion volume and particle size
考虑到原则上应减少β-环糊精用量以及增加乳化油含量,后续实验中乳液的制备选择使用油水体积比(6∶4)、β-环糊精添加量为30 g/L的条件进行。
2.2 体系添加黄原胶对β-环糊精-柠檬醛乳液稳定性的影响
黄原胶是一种具有优良乳化性能的微生物多糖,通常认为其对乳液具有稳定作用。因此,本实验尝试添加黄原胶,研究其对柠檬醛Pickering乳液的增稳作用。
选取油水体积比为6∶4、β-环糊精加量为30 g/L以及黄原胶添加量为5 g/L,按1.2.1方法制备乳液,通过测定胶粒直径以及Zeta-电位来评价乳液分散体系的稳定性。Zeta-电位是连续相与附着在分散胶体上的流体稳定层之间的电势差,是对颗粒之间相互排斥或吸引力强度的度量。胶体粒子越小,Zeta电位的绝对值越高,体系越就越稳定[23-24]。通常认为,乳状液Zeta-电位绝对值高于30 mV时乳状液比较稳定。
实验中发现,在对体系进行高速均质前将黄原胶加入水相,会对乳液形成产生干扰,致使体系有较多柠檬醛不能乳化,乳液相不均一。如果先高速均质制备乳液,再将溶解的黄原胶溶液加入,之后轻度均质混匀,则发现可形成具有一定黏度的均一乳液。本实验先通过β-环糊精加量30 g/L、油水体积比(6∶4)制备乳液,然后将适量质量分数为2%的黄原胶溶液添加到乳液体系,使乳液水相黄原胶含量为0.5%,机械搅打均匀,最后形成的乳液体系油水体积比为5.5∶4.5,β-环糊精含量为27 g/L。对添加黄原胶的体系进行粒径和Zeta电位测定,同时进行流变黏度测定,具体结果见图4和图5。
由图4可知,添加黄原胶后乳液粒径从760 nm增加到845nm,Zeta电位绝对值从32.4mv提高到38.6mv,这2个结果表明,添加黄原胶对乳液稳定性产生不同的影响。但黄原胶作为一种高黏度的亲水多糖,其还可通过增加乳液外水相黏度来提高乳液的稳定性。由图5可知,环糊精柠檬醛乳液为剪切变稀流体,体系添加5 g/L黄原胶后其黏度从61.1Pa·s增加到89.0 Pa·s,乳液黏度增加显著。外水相黏度的增加,可以起到空间阻碍作用,有效降低乳液液滴的活动性,减少碰撞合并的几率;同时亲水性多糖分子增加乳液胶粒表面水化膜的厚度,在一定程度上也会提高胶粒的稳定性。
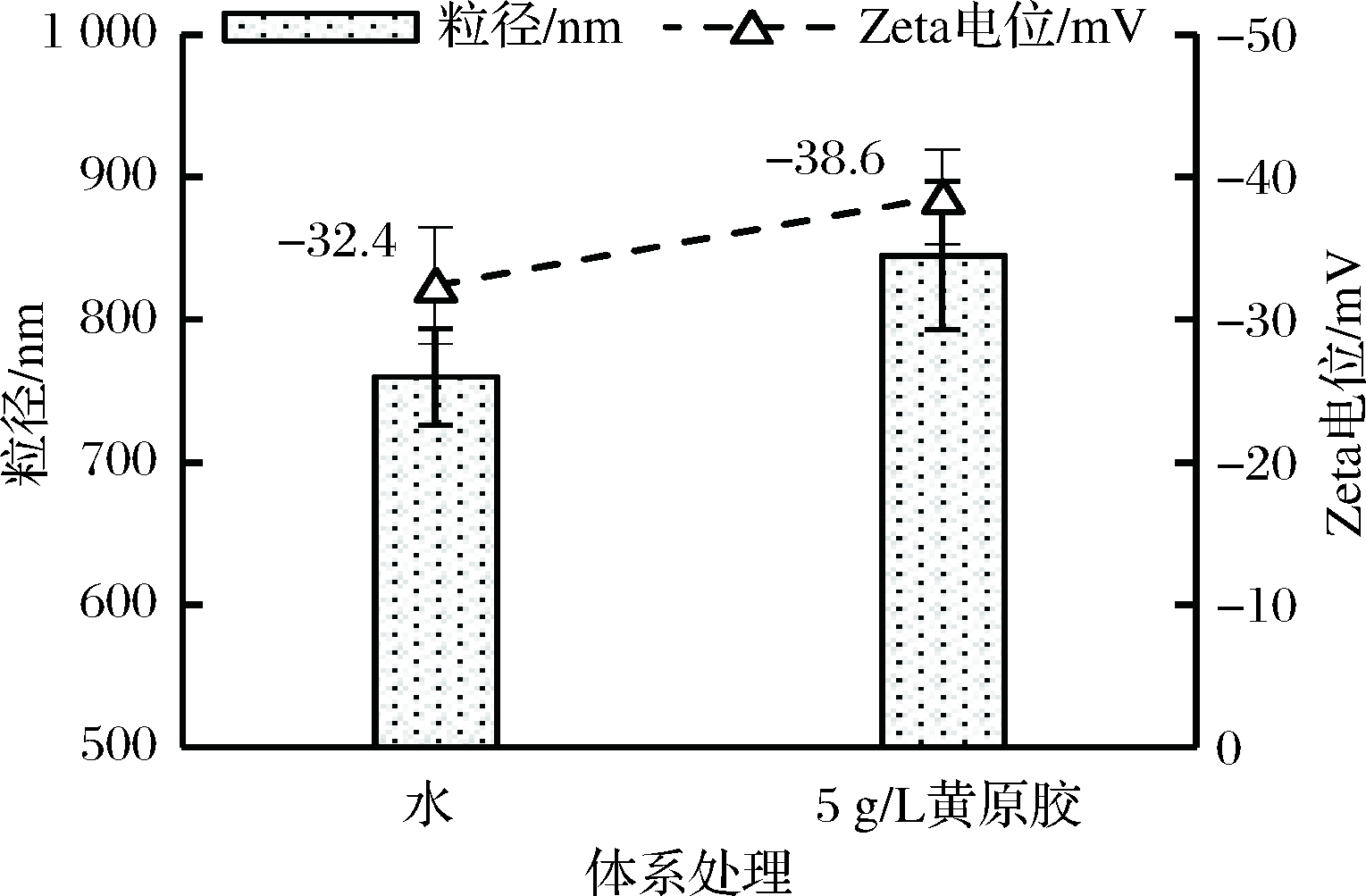
图4 体系添加黄原胶对乳液平均粒径和
平均Zeta-电位的影响
Fig.4 Effects of additional xanthan gum on both
the particle size and Zeta-potential of emulsion
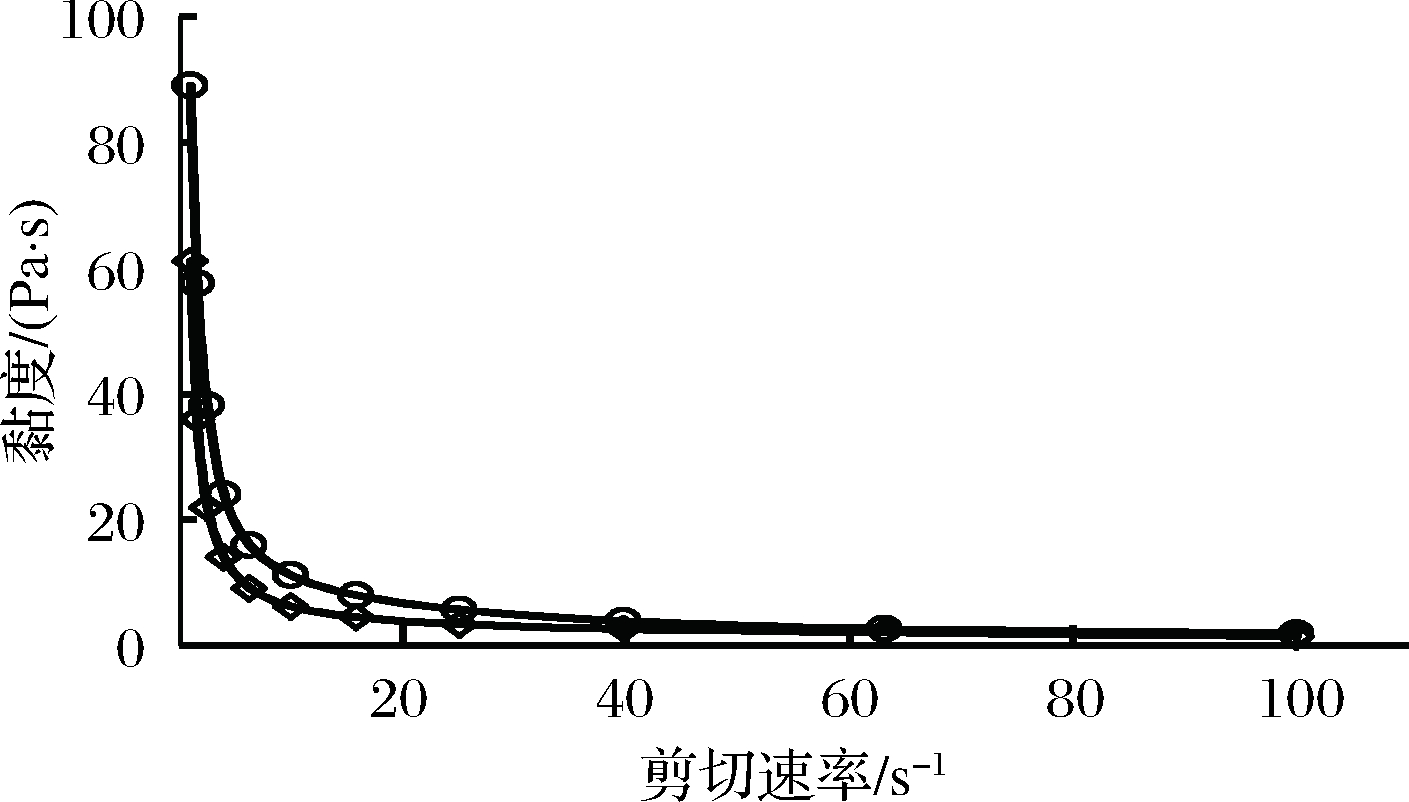
图5 黄原胶添加量5 g/L对乳液黏度的影响
Fig.5 Effects of additional 5 g/L xanthan gum on
the viscosity of emulsion
上述实验只是从不同角度对黄原胶对乳液的理化指标影响进行检测,黄原胶对乳液稳定性的影响最终结果还要通过贮存稳定性和耐热耐冻稳定性进行一步进行验证。
2.3 酸碱度对β-环糊精-柠檬醛乳液稳定性的影响
体系pH值会影响液滴带有电荷的类型和数量,进而影响液滴Zeta-电位,最终影响乳液的稳定性[25-26]。由图6可以看出,pH 3.0、6.5和9.0时的平均粒径分别为685、760和721 nm,而Zeta-电位绝对值分别为37.4、28.2和31.5 mV,即随着乳液体系pH值偏离中性条件时乳液胶粒的平均粒径明显变小,Zeta-电位绝对值随着pH值的偏向酸性或碱性而逐渐增大。这一结果说明,偏离中性pH环境会使油滴的环糊精界面膜带有更多的电荷,油滴间静电斥力增大,从而更有利于乳液的稳定。
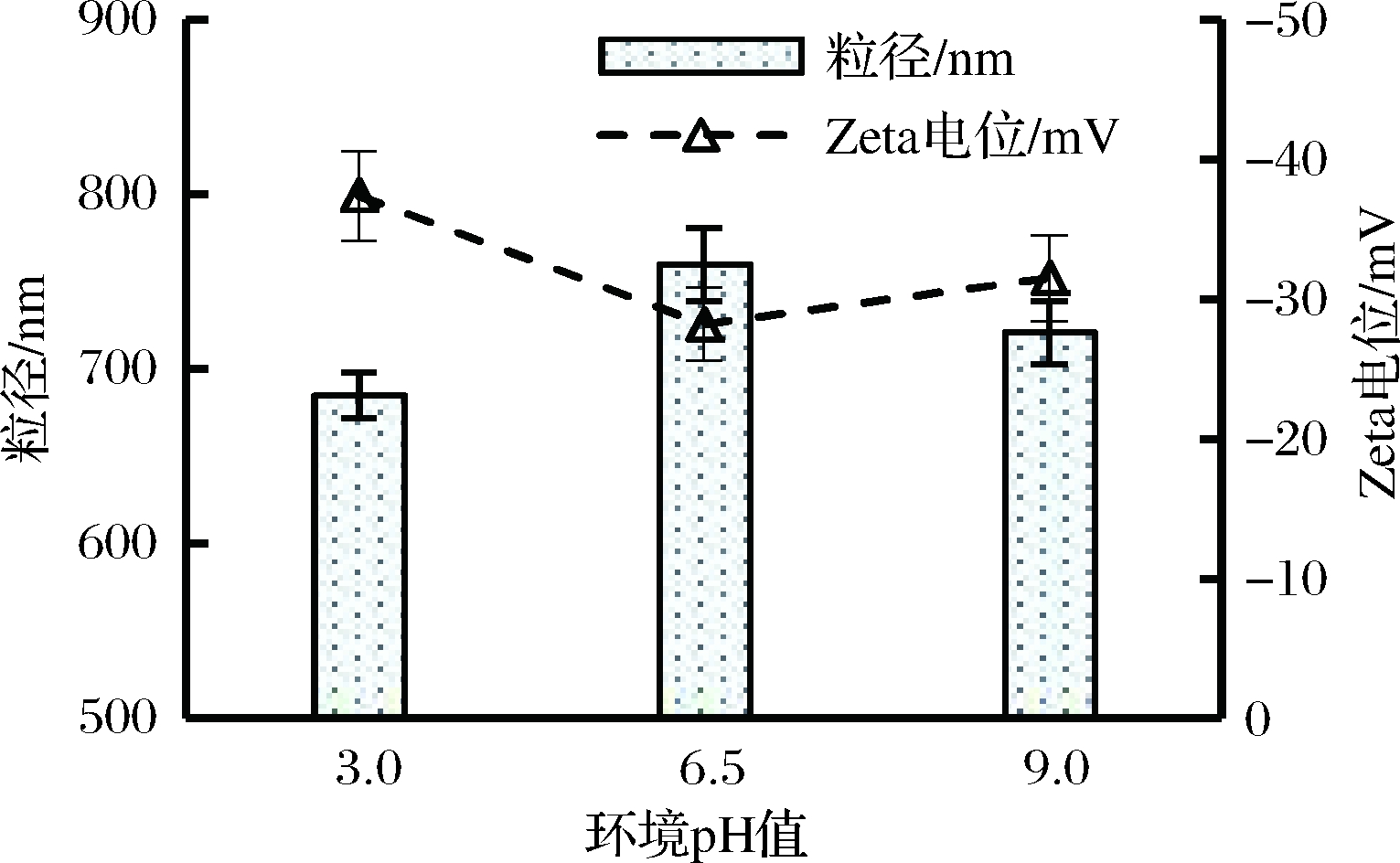
图6 不同pH条件下乳液的平均粒径和平均
Zeta-电位
Fig.6 Effects of various pH values on both the particle
size and Zeta-potential of emulsion
2.4 加热冷冻处理对β-环糊精-柠檬醛乳液稳定性的影响
将β-环糊精-柠檬醛乳液在80 ℃条件下加热处理15min,然后放置室温自然冷却,或将乳液进行-18℃冷冻过夜处理,然后室温自然解冻,分别测定乳液的各相体积,结果如图7所示。

图7 加热冷却处理对乳液稳定性的影响
Fig.7 Effects of heat or freezing treatment on the
stability of emulsion
加热处理的乳液,无论添加黄原胶与否,均未观察到乳液的分层现象,说明β-环糊精-柠檬醛乳液具有较好的耐热稳定性。但经过冷冻过夜处理的乳液,则发现有柠檬醛油相及水相的析出。油水体积比为6∶4的乳液经冷冻后有40%(体积分数)的柠檬醛相和10%(体积分数)的水相析出,体系添加黄原胶的乳液有大约23%(体积分数)的柠檬醛相析出,无水析出,这说明外水相添加黄原胶在一定程度上增加乳液耐冷冻的能力。
2.5 β-环糊精-柠檬醛乳液的贮存稳定性
乳状液稳定性用乳化系数来进行评判[27]。取油水体积比6∶4、β-环糊精添加量30 g/L、添加或不添加5 g/L的黄原胶制备乳液,室温贮存60 d,计算乳液的乳化系数。结果如表1所示。经过60 d贮藏,所测试的2种柠檬醛乳液均能保持稳定,乳化系数为100%,未发生分层现象,说明乳液具有较好的贮存稳定性。
表1 β-环糊精稳定柠檬醛乳液的贮存稳定性
Table 1 The stability of β-CD-citral Pickering emulsion
样品组未加黄原胶添加5 g/L黄原胶乳化系数(ESI)/%100100
注:乳液制备条件:油水体积比6∶4、β-环糊精添加量30 g/L。
如前所述,在以β-环糊精乳化稳定的柠檬醛Pickering乳液中,界面膜是由β-环糊精包合物纳米颗粒通过紧密排列而成,相比于传统液体膜,这种固态界面膜具有理想的韧性和强度,从而赋予Pickering乳液较高的稳定性[28-29]。
3 结论
(1)通过β-环糊精与柠檬醛形成颗粒包合物用以制备柠檬醛的Pickering乳液,乳液为水包油型,其中油滴呈标准的球形,直径在数百纳米范围;当柠檬醛与水的体积比为6∶4、β-环糊精用量为30 g/L时可形成稳定的全乳液体系,乳液室温贮存60d,未发生分层现象,说明乳液具有很好的贮存稳定性。
(2)乳液制备时,高速均质处理前添加黄原胶不利于乳液的形成,高速均质后再添加黄原胶,会使乳液粒径略有增大、电位绝对值显著增加,有利于乳液的稳定;调整体系pH值偏酸或偏碱性条件时,则可使乳液粒径减小、电位绝对值增大,从而增加乳状液的稳定性。
(3)β-环糊精稳定的柠檬醛Pickering乳液耐热稳定性较高、耐冻能力较低。80℃条件加热15min时乳体系仍能保持稳定,但经过-18℃冷冻过夜处理可使乳液发生分层,乳体系形成后期加入5 g/L的黄原胶则有利于乳液耐冻性的增强。
[1] XIAO J, LI Q, HUANG Q R. Recent advances on food-grade particles stabilized Pickering emulsions: Fabrication, characterization and research trends[J]. Trends in Food Science and Technology, 2016, 55:48-60.
[2] 李海明,杨盛,韦何雯,等.食品级Pickering乳液的研究进展[J]. 食品科学, 2015, 36(19): 265-270.
[3] CHRISTINA L,STEPHAN D. Pickering emulsions in foods - opportunities and limitations[J]. Critical Reviews in Food Science Nutrition, 2018, 58(12):1 971-1 985.
[4] 李丹凤,徐婷,胡静,等.香料化合物柠檬醛稳定性研究进展[J].食品工业, 2016, 37(9): 215-219.
[5] MASWAL M, DAR A A. Formulation challenges in encapsulation and delivery of citral for improved food quality[J]. Food Hydrocolloids, 2014, 37:182-195.
[6] ZAHI MR, LIANG H, YUAN Q. Improving the antimicrobial activity of D-limonene using a novel organogel-based nanoemulsion[J]. Food Control, 2015, 50:554-559.
[7] WAGONER T B, FOEGEDING E A. Whey protein-pectin soluble complexes for beverage applications[J]. Food Hydrocolloids, 2017, 63: 130-138.
[8] PIORKOWSKI D T, MCCLEMENTS D J. Beverage emulsions: Recent developments in formulation, production, and applications[J]. Food Hydrocolloids, 2014, 42:5-41.
[9] TIAN H X, LI D F, XU T, et al. Citral stabilization and characterization of nanoemulsions stabilized by a mixture of gelatin and Tween 20 in an acidic system[J]. Joutnal of the Science of Food and Agriculture, 2017, 97(9): 2 991-2 998
[10] YANG X Q, TIANH X, HO C T, et al. Inhibition of citral degradation by oil-in-water nanoemulsions combined with antioxidants[J].Journal of Agricultural and Food Chemistry, 2011, 59(11): 6 113-6 119.
[11] YANG Y, CUI S, GONG J, et al. Stability of citral in oil-in-water emulsions protected by a soy protein-polysaccharide Maillard reaction product[J]. Food Research International, 2015, 69: 357-363.
[12] MOTOKI I, KANAME H, HIROYUKI T, et al. Emulsifying ability of β-cyclodextrins for common oils[J]. Journal of Dispersion Science and Technology, 2010, 31:1 648-1 651.
[13] XI Y K, LUO Z G, LU X X, et al. Modulation of cyclodextrins particles amphiphilic properties to stabilize Pickering emulsion[J]. Journal of Agriculture and Food Chemistry, 2018, 66(1): 228-237.
[14] MATHAPA B G, PAUNOV V N. Self-assembly of cyclodextrin-oil inclusion complexes at the oil-water interface: A route to surfactant-free emulsions[J]. Journal of Materials Chemistry A, 2013, 1(36):10 836-10 846.
[15] 袁继凤,徐化能,王周平. 基于β-环糊精稳定的Pickering乳液微观结构与流变性质研究[J]. 食品与生物技术学报, 2014, 33(4): 374-380.
[16] CHAUDHARI A, PAN Y, NITI N. Beverage emulsions: Comparison among nanoparticle stabilized emulsion with starch and surfactant stabilized emulsions[J]. Food Research International, 2015, 69:156-163.
[17] LI P H, LU W C. Effect of storage condition on the physical stability of D-limonene nanoemulsion[J]. Food Hydrocoll, 2016, 53:218-224.
[18] YANG Y, ZHAO C Y, TIAN G F, et al. Effects of preheating and storage temperatures on aroma profile and physical properties of citrus-oil emulsions[J]. Journal of Agricultural and Food Chemistry, 2017, 65(35): 7 781-7 789.
[19] HU J W, YEN M W, WANG A J, et al. Effect of oil structure on cyclodextrin-based Pickering emulsions for bupivacaine topical application[J]. Colloids and Surfaces B: Biointerfaces, 2018, 161:51-58.
[20] ARAB D, KANTZAS A, BRYANT S L. Nanoparticle stabilized oil in water emulsions: A critical review[J]. Journal of Petroleum Science and Engineering, 2018, 163:217-242.
[21] RAO J J, MCCLEMENTS D J. Formation of flavor oil microemulsions, nanoemulsions and emulsions: Influence of composition and preparation method[J]. Journal of Agricultural and Food Chemistry, 2011, 59(9): 5 026-5 035.
[22] KATEPALLI H, VIJAY T J, TRIPATHI A, et al. Microstructure and rheology of particle stabilized emulsions: Effects of particle shape and inter-particle interactions[J]. Journal of Colloid and Interface Science, 2017, 485:11-17.
[23] HONARY S, ZAHIR F. Effect of zeta potential on the properties of nano-drug delivery systems-A review (part 2)[J]. Tropical Journal of Pharmaceutical Research, 2013, 12(2): 265-273.
[24] RAVINDRAN S, WILLIAMS M A K, WARD R L, et al. Understanding how the properties of whey protein stabilized emulsions depend on pH, ionic strength and calcium concentration, by mapping environmental conditions to zeta potentia[J]. Food Hydrocolloids, 2018, 79: 572-578.
[25] SAV A R, MEER T A, FULE R A, et al. Investigational studies on highly purified fenugreek gum as emulsifying agent[J]. Journal of Dispersion Science and Technology, 2013, 34(5): 657-662.
[26] SONG X Y, PEI Y Q, QIAO M W. Preparation and characterizations of Pickering emulsions stabilized by hydrophobic starch particles[J]. Food Hydrocolloids, 2015, 45: 256-263.
[27] DERAKHSHANDEH M, PILAPIL B K, WORKMAN B. Analysis of network formation and long-term stability in silica nanoparticle stabilized emulsions[J]. Soft Matter, 2018, 14(21): 4 268-4 277.
[28] CATHERINE P W, LOTTE L, LANG C. Structure of concentrated oil-in-water Pickering emulsions[J]. Soft Matter, 2012, 8(30): 7 784-7 789.
[29] 朱雨晴,刘伟,陈兴,等. 食品级皮克林乳液的稳定机制及稳定性研究进展[J]. 食品工业科技, 2018, 39(7): 315-322.