食品包装能够避免食品直接暴露在空气中,对于微生物、氧气以及二氧化碳具有一定的阻隔作用,在一定程度上能够有效延缓食品腐败变质,延长食品的货架期。传统包装材料对于食品保鲜具有良好的作用效果。然而,随着环境污染问题的日益严重,以塑料为主体的传统包装材料由于缺乏生物降解性对社会环境所造成的污染逐渐加重。为了节约化石燃料资源并减少对环境的污染,开发制备环境友好型可降解的食品包装材料替代传统包装材料成为当下的研究热点。大豆分离蛋白来源广泛,具有良好的成膜性及生物可降解性,常作为制备包装膜的材料。但是,相比于传统的包装材料,蛋白膜机械强度较低且易导致细菌滋生,从而引起食品腐败变质现象,导致食品的安全性降低,大大缩短了食品贮藏货架期,对企业经济效益产生巨大影响。因此,可通过改性大豆分离蛋白或向其中添加对人体无毒无害且具有高效抗菌性的天然物质制备复合可食膜以达到延长食品保质期的目的。多酚、精油等功能因子具有抗癌、抗菌、抗氧化等多重功效,通过构建稳定包埋体系,可实现功能因子的缓控释放并增强其稳定性,避免失活失效。
目前国内外有关可食膜的研究主要集中在源自食品成分的可生物降解材料如蛋白质可食膜、多糖类可食膜、脂质可食膜等[1]。深入研究可食包装膜有利于分析食品组分的构效关系,研发新型多功能、环境友好型包装材料,进而解决目前食品保鲜、贮存中出现的问题。本文重点阐述以大豆分离蛋白为基础物质,通过对其进行改性处理以及与多糖复合等方式,改善单一蛋白质膜的缺陷,并通过蛋白膜负载功能因子,赋予膜新的性能。本文展望了大豆分离蛋白基可食膜的相关研究以及发展趋势,为后续研发性能优良、集多功效于一体的生物可降解环境友好型包装材料提供理论依据。
1 大豆分离蛋白膜简介
大豆蛋白是由球蛋白和白蛋白构成的混合物,其中主要为β-伴大豆球蛋白(7S)和大豆球蛋白(11S)。7S球蛋白由α亚基(67 kDa)、α'亚基(71 kDa)和β亚基(50 kDa)组成;11S球蛋白包含5个不同的亚基,每个亚基由酸性亚基A(35 kDa)和碱性亚基B(20 kDa)组成,二者通过二硫键进行连接[2]。大豆分离蛋白(SPI)是由大豆蛋白精制、纯化而成,其蛋白质含量高达90%。SPI材料易得,具有良好的乳化性和成膜性,制备的包装膜价格较低,可食、可降解,有一定的抗氧化能力,但水蒸气透过率高,机械强度较差,并且膜的机械性能会随环境温度和湿度的改变而发生变化[3],这极大地限制了SPI膜的应用与推广。
SPI的微观结构决定了SPI膜的功能性质。由于SPI的疏水中心含有大量的疏水性氨基酸残基,能促进蛋白质与疏水物质相结合,所以SPI在水溶液中可以形成疏水性中心在内、亲水性外层在外的球状结构[4],这直接造成了SPI膜的水敏感性;成膜过程中,分子间二硫键与氢键、疏水相互作用与静电力的结合是导致SPI膜机械强度低的主要原因[5]。
为了提升SPI的功能性质,可对其进行改性处理。大量研究表明,改性后的SPI具有更好的乳化性、热稳定性和阻氧性。而将SPI与多糖、脂质或其他蛋白质结合,则往往表现出更利于其实际应用的功能协同作用[6]。壳聚糖(CS)常被用作乳液稳定剂和天然抗菌剂,与SPI通过静电作用结合后使SPI膜表现出优良的抗氧化性、阻水性和阻油性[7];脂肪酸(SA)与SPI共轭制备的SPI-SA膜有效增强了SPI膜的阻水性、机械性能、热稳定性以及疏水性脂肪酸和亲水性蛋白之间的界面相容性[8];小麦面筋蛋白(WP)和SPI共组装形成的复合物具有更稳定的展开结构,弥补了单一蛋白所含氨基酸种类不能满足人体需求的缺陷[9]。
目前,新型包装材料的研发备受关注,而性能优越的SPI基可降解复合可食膜或已成为食品保鲜领域取代聚乙烯塑料包装的不二选择。
2 大豆分离蛋白膜制备方法
制备大豆分离蛋白膜常用的方法主要有湿法和干法。湿法也称为溶液流延法或溶液浇筑法;干法主要指通过熔融加工技术如挤出、热压、注塑、吹塑等方法制备蛋白薄膜。
2.1 湿法
湿法是指利用蛋白质在溶剂中的分散或增溶作用,将蛋白悬浮液与预先分散在水中的聚合物溶液或纳米颗粒分散液混合,通过均质化处理,使蛋白质在溶剂中充分溶解并分散在平坦的表面上,经过流延和干燥,在一定的控制条件下除去溶剂形成膜的方法。由于其简便性及可重复性,湿法制备薄膜在实验室条件下得到广泛使用。
湿法制备的薄膜中,分子之间的稳定连接主要依靠氢键、静电作用、疏水作用等非共价相互作用。蛋白质分子质量显著影响分子之间的连接稳定性。通过蒸煮和碱处理降低蛋白质分子质量,赋予蛋白热塑性已被广泛应用于蛋白质基薄膜的生产[10]。可食膜的成膜本质是膜液中的物质通过非共价相互作用连接形成稳定且干燥的三维凝胶结构[11]。ECHEVERRíA等[12]采用流延成膜方法制备SPI-蒙脱石共混膜,结果表明,通过在浇铸步骤中保持足够的流动性可去除分散体中的气泡,保证纳米复合膜的表面均一性。除表面结构特性外,流延法制备的SPI膜具有较高水接触角值,其原因是较长的干燥时间促使蛋白质链发生重排以及疏水基团从非极性残基向表面暴露[13],导致薄膜表现出较高的疏水性和耐水性。湿法制备薄膜过程中,蛋白质分子的微观结构发生了显著变化,往往表现为α螺旋结构增加以及无规卷曲结构向β-折叠结构转变。
典型的薄膜流延生产技术需较长的干燥时间,导致流延法制备薄膜技术的应用存在一定的局限性。JENSEN等[14]利用热表面流延成膜方法,将纤维素-SPI共混膜液浇筑在85℃玻璃台上。实验结果表明采用加热流延制备的SPI膜与常规的环境干燥方法制备的SPI膜具有相似的机械性能。与常规环境干燥流延法所需的干燥时间相比,使用热表面流延法可将干燥时间由10 h减少至25 min。除上述问题外,流延法制备薄膜还存在生产效率低、耗能高且可能造成环境污染等诸多问题,限制了该法在工业生产中的应用。ORTIZ等[15]为大规模生产薄膜提供了新思路,即采用带式流延成膜方法,将由蛋白质、溶剂和增塑剂组成的胶体分散液倾倒在适当的干燥载体上,通过刮刀装置将成膜悬浮液铺展在支撑物上,以保证悬浮液的厚度均一。随后,将悬浮液在对流烤箱中干燥6~12 h,即可实现工业化生产。
2.2 干法
干法是利用成膜原料的热塑性特性,通过熔融加工技术,给予高于成膜材料熔点的温度,使原料呈现流动状态,而后给予高压获得薄膜的加工技术。与湿法相比,干法无溶剂加入、生产时间较短、对加工条件要求低,更适用于规模化生产。
与流延成膜不同的是,成膜过程中,二硫键对薄膜的稳定性起决定作用[16],二硫键越多,蛋白质的抗外界干扰能力越强,所制备的薄膜稳定性也越高。干法制备的薄膜中,分子之间的稳定连接主要依靠氢键、二硫键等分子相互作用(图1)。蛋白质的聚集程度以及网状结构交联度决定膜的最终性能。干法制备大豆蛋白可食膜过程中,温度显著影响膜的性能,高温使得11S亚基中部分疏水基团和二硫键暴露,随着加热时间的增加,这些基团通过硫氢基氧化(形成新的二硫键)、硫醇-二硫键交换反应(将分子内二硫键重组为分子间二硫键)[17]形成更紧密的聚合网状结构,增大了蛋白质的聚集程度,提升了膜的综合性能。
制备薄膜的过程中往往添加适量增塑剂,如甘油、山梨糖醇等。增塑剂能进入SPI的三级结构内部(如图1),使自由体积和蛋白质链的迁移速率增大,从而提升SPI膜的柔韧性[18],降低蛋白膜的脆性。研究表明,干法加工中较高的加工温度会导致蛋白发生较大程度的变性,从而促进蛋白质与增塑剂之间的相互作用,发生物理交联,形成稳定的三维网状结构。与湿法相比,干法在缩小分子内部孔径的同时还减少了孔径数量,使薄膜具有较低的水蒸气透过率、较高的拉伸强度以及断裂伸长率,并显著降低了薄膜中的水分含量。此外,由于高温与高压的共同作用,压缩膜的透明度更高并且表面更加平整光滑[9,13]。
除单一蛋白质膜外,CIANNAMEA[19]在向大豆蛋白膜中添加红葡萄提取物(一种天然多酚)通过流延成膜法以及热压成膜法制备薄膜的过程中发现,热压法制备的薄膜具有较高的水蒸气透过率以及抗氧化活性,其原因可能是随着时间的推移,多酚在热压法制备的薄膜基质中释放速率更高。
干法加工制备的薄膜虽具有更好的性能,但由于蛋白质的玻璃化转变温度通常非常接近其热降解温度,且纯大豆蛋白显示出较差的熔体流动性,因此尚未广泛用于蛋白质类薄膜的制备。
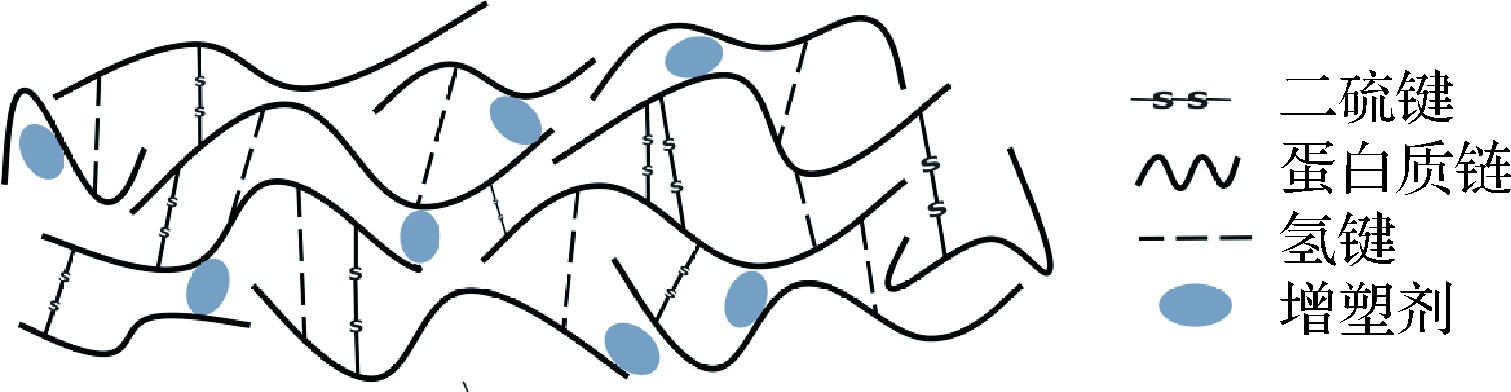
图1 蛋白可食膜中蛋白分子链间的相互作用
Fig.1 Interaction between protein molecular chains
in protein edible films
3 大豆分离蛋白可食膜的改性技术
3.1 单独大豆分离蛋白改性
常用的大豆分离蛋白膜改性方法主要有物理改性、化学改性、酶改性3种方法。
3.1.1 物理改性
物理改性是指通过高温、高压、超声波等物理手段改变蛋白质的高级结构从而对蛋白质的功能性质产生一定的影响。大多数蛋白质在高温下会发生变性作用,这是由于热破坏了蛋白质分子中的氢键和非极性疏水基团,使得氨基酸基团暴露于溶剂中并产生更开放的结构所导致。加热增强了蛋白质与蛋白质间的相互作用,使分子堆积更紧密,并降低了聚合物链的流动性[20]。STUCHELL等[21]研究表明,经过85℃热处理的SPI膜较未加热的SPI膜有较高的拉伸强度、较大的断裂伸长率以及较低的水蒸气透过率,且膜更光滑透明、均匀性更高。除热处理外,物理射线也常常被用于蛋白的改性。经过射线辐照,蛋白质中的氨基酸发生氧化反应,分子内部发生共价交联作用,使蛋白质聚集从而形成新的致密网状结构。LEE[22]利用γ射线处理过的SPI溶液制备的SPI膜与普通蛋白膜相比,拉伸强度提高了约2倍,水蒸气透过率降低了13%。
3.1.2 化学改性
化学改性是指通过共价交联等反应破坏蛋白质的二、三级或四级结构,使氨基酸侧链暴露,通过化学键产生新的相互作用,改变蛋白质的完整结构。KANG等[3]以三羟甲基丙烷-三[3-(2-甲基吖丙啶基)丙酸酯](TMPTAP)与咖啡酸(CA)为交联体系制备SPI膜,其结果表明,TMPTAP/ CA的引入使得分子之间通过共价交联而形成稳定网络结构。TMPTAP促进了SPI链的空间延伸并且使其发生开环反应,CA则充当潜在的交联剂,与肽链的—NH2/—SH基团发生反应,从而压缩SPI网络结构,进而形成更有序的3D网络,使其具有良好的机械性能和疏水性。同时,OU等[23]研究表明通过阿魏酸共价交联修饰SPI,可使SPI薄膜的拉伸强度提高约10%(最终值为1.6 MPa),这是由于阿魏酸发挥了增塑剂的作用。NIE等[24]发现加入酚类化合物制备的蛋白膜具有较高的柔韧性和较低的水蒸气透过率,原因可能是由于蛋白质与多酚之间的相互作用会封闭部分亲水基团。同时,由于多酚具有抗氧化作用,在其结合到氨基酸侧链后,可以赋予可食膜一定的抗氧化性。研究表明酚类化合物可以稳定蛋白质的二级结构,提高其热稳定性,并显著降低其生物降解速率,同时提高其抗氧化能力。因此,多酚修饰蛋白制备的可食膜可以更好地应用在食品包装体系,并减少由于氧化褐变而导致的食品腐败变质现象的发生,延长食品的保质期。
3.1.3 酶改性
常见的酶改性方法是TG酶改性,TG酶能够催化谷氨酰胺残基的γ-羧酰胺基团与蛋白质的一级ε-胺基形成异肽键,使蛋白质分子内部以及不同蛋白质分子之间形成交联,对蛋白质的溶解度、乳化能力、起泡特性和凝胶化功能具有显著影响。经TG酶改性的SPI与纯化的果胶共混制备的薄膜具有高度耐水性以及适度的水蒸气透过率[25]。TANG等[26]也得出了相同的结果,并且发现经过TG酶改性的薄膜表现出更大的拉伸强度,其原因可能是由于酶使薄膜内部产生了更致密的结构。
3.2 大豆分离蛋白与多糖复合制备可食膜
研究表明,由多糖制备的薄膜具有良好的阻油性和透明性,但其气体阻隔性较差;而以蛋白质为原料制成的薄膜具有良好的气体阻隔性,但缺乏一定的机械性能。因此,越来越多的科研工作者通过将多糖与蛋白质混合,构建蛋白质-多糖复合体系制备共混膜,利用分子间的相互作用形成致密网络结构,使膜在具有气体阻隔性的同时具备良好的阻油性、机械性能(表1)。
在蛋白质中加入多糖,主要是为了增强分散系统的稳定性。多糖存在下的稳定作用归因于在界面处蛋白质与多糖形成的蛋白质-多糖聚集体。高度亲水性多糖由于不会在界面处自行吸附而表现出与蛋白质的协同行为,从而促进了膜表面压力的显著增加[27]。ZHENG等[28]证明加入二醛羧甲基纤维素(DCMC)后,利用SPI与DCMC之间的相互作用,有效增强SPI薄膜拉伸强度的同时提高其耐水性和热稳定性。多糖和蛋白质共混薄膜被广泛应用于食品表面的保护,通过降低食品与周围环境之间的水蒸气和气体的转移速率,可达到保鲜的目的。ZHANG等[29]研究发现SPI-壳聚糖涂层具有对水蒸气的良好阻隔性能,可显著降低杏子的重量减轻速率。与多糖复合的SPI膜不仅在机械性能方面有所提高,更被赋予了新的功能。由于部分多糖具有一定的抗菌、抗微生物特性,将SPI与多糖共混,可实现制备机械性能优良的环境友好型可食抑菌膜,为今后可食膜的研究发展提供了新的思路。
3.3 复合型改性技术制备大豆分离蛋白基可食膜
蛋白经过改性修饰后,其乳化性、成膜性等得到极大改善,具有较强的结构与功能特性,可以弥补蛋白膜功能缺陷性问题。因此,基于蛋白质-多糖复合膜的研究,考虑将改性蛋白与多糖混合以显著提高包装膜的功能性质。超声波能够破坏蛋白质的分子间相互作用,从而促进大量沉淀物向胶体悬浮液的转化。通过超声作用预处理制备的SPI-柑橘果胶(CP)复合物更加均一且其表面疏水性显著增加。复合物的这些物理化学和结构性质的变化有助于高强度超声场下悬浮液粘度和复合物尺寸的降低,从而改善乳化稳定性,获得更理想的乳化性质[30]。YUAN等[31]研究表明加热的SPI-壳聚糖(CS)复合物比未加热的SPI-CS混合物显示出更高的酸性溶解度,推测最可能的原因是,当热处理SPI-CS混合物时,CS起到分子伴侣的作用。在加热过程中,蛋白质上更多电负性基团暴露并与CS的氨基相互作用。受热的SPI-CS复合物可能形成由非共价力(例如静电相互作用)驱动的可溶聚集体。在水溶液中大豆球蛋白和CS之间的络合也观察到了相似的结果。除物理手段外,TG酶可在催化SPI内部形成网状交联结构的同时降低CS基质分子间的链迁移率,进而提高其拉伸强度。此外,致密的网状结构显著降低了氧气、二氧化碳和水蒸气的渗透性。同时,在存在酶的情况下,由于酶催化引起的大豆蛋白内部分子交联显著减少了薄膜内部的自由体积。获得的果胶-大豆蛋白薄膜对氧气和二氧化碳的渗透性甚至比聚乙烯薄膜低,这显示出了改性后的大豆蛋白在气体阻隔性上的强烈优势[25]。改性蛋白质与多糖共混制备的包装膜的多种功能赋予了新型生物塑料极高的潜在实际应用价值,研究具有抗菌、抗氧化、优良机械性能、低气体渗透性等优点集一体的可食膜成为新的可探索的一个发展领域。
表1 SPI与不同多糖复合成膜的方法及性能特点
Table 1 Method and performance characteristics of
composite film formed by SPI and different polysaccharides

蛋白质多糖成膜方法性能特点SPI二醛羧甲基纤维素浇筑成膜拉伸强度增大,耐水性、热稳定性提高[28]琼脂浇筑成膜拉伸强度增大、断裂伸长率增大[32]马铃薯淀粉流延成膜水蒸气透过率降低,拉伸强度增大[33]壳聚糖流延成膜粗糙度增加、疏水性增强[34]羧甲基魔芋葡甘露聚糖浇筑成膜机械性能增强,热稳定性和水蒸气阻隔性能提高[35]
4 大豆分离蛋白基可食膜的理化性质
4.1 膜厚度
膜厚度在膜的阻隔性能中起重要作用,且膜厚度与膜透明度密切相关,是膜制品的重要参数。膜的厚度取决于成膜乳液基质中非溶剂的总量,特别是固体含量。由于较多的固体物质引入到膜基质中,且引入物一般会破坏膜基质的有组织结构,并与之发生反应产生新的交联形式,因此,复合膜的厚度一般均大于单一蛋白膜[36]。但向蛋白膜中加入小分子时,由于大豆分离蛋白微观上为球状结构,分子间产生较多空隙与通道,加入的固体小分子填补了其孔隙与通路,其厚度变化可能不是十分明显。
4.2 透明度
包装薄膜的透明度对食品的外观有很大影响。不同的薄膜厚度、不同的表面和内部结构的综合作用影响其光散射特性[37]。掺入酚类化合物的蛋白膜较普通膜呈现出更暗的颜色,主要是因为在添加酚类物质之后,光可能会被添加物的液滴或新形成的交联结构散射和折射,从而产生较暗的视觉感受[36]。SPI膜的透明度与其抗紫外线能力息息相关,控制薄膜透明度可有效控制产品的紫外线暴露量,延缓食品的氧化变质。在SPI与壳聚糖的复合体系中,复合膜表现出良好透明度的同时也起到一定抑制紫外线的作用,对于延长脂质氧化具有一定功效[38]。
4.3 机械性能
机械性能决定材料在特定条件下对于外力的抵抗能力。食品膜的机械性能常用拉伸强度(tensile strength, TS)和断裂拉伸率(elongation at break, E)来度量。单一大豆分离蛋白膜脆性强、不具备热塑性、机械性能较差,且机械性能随环境温度的降低和湿度的增大而减弱,这些因素限制了其在食品包装领域的广泛应用。SPI中含有羟基、羧基等基团,因此可通过多种方式改善单一SPI膜的机械性能。向SPI薄膜中添加茶多酚,利用茶多酚中的活性羟基使蛋白质内部形成更多氢键,可在一定程度上提高膜的致密性以增强机械性能和黏弹性[39]。SPI也可与多糖通过形成氢键实现非共价自组装提升共混膜的机械性能。将一定浓度的SPI与黄麻纤维结合,其成品膜表现出较高的拉伸强度,这是由于SPI通过基质聚合物将黄麻纤维紧密螯合其中所致[40]。同时,部分研究者通过向膜中加入精油使产品膜具备一定的抑菌性能,但精油的疏水性使得蛋白质分子间作用力减弱导致机械性能降低,如制备的肉桂醛-SPI膜的TS和E值显著低于纯SPI膜[41]。
4.4 阻水性能
水蒸气透过率(water vapor permeability, WVP)是常用来表征膜阻水性能的重要指标,指在恒定湿度下,单位时间内在单位膜面积上透过的水蒸气量。WVP值越低,包装膜的阻水有效期越长,包装产品所处的环境越稳定,产品货架期越长。SPI由于其自身的高度亲水性,使得单一SPI膜具有较大的WVP。人们向SPI基质中添加适当比例精油构建的SPI-植物精油体系,基于精油的疏水性,可截留大部分水蒸气、显著降低WVP。此外,膜内部结构的致密程度也会影响WVP值,这可能是由于不规则的紧密区域使水蒸气的渗入路径复杂化。但当精油添加过量时,过量的精油导致膜微观结构中结晶区被破坏,WVP增大,阻水性能下降,且干燥过程中精油的挥发也不可避免地产生微孔,进一步损坏膜结构,缩短水蒸气的渗入路程[42]。
4.5 抗氧化性
包装材料的抗氧化能力是影响其保鲜效果的关键,食品贮藏期间导致食品腐败变质的相关生化反应,如脂质氧化、酶促褐变以及食品的组织结构变化均与体系内氧气含量及周围环境变化有关。生物膜的抗氧化性常用DPPH自由基清除率表示,清除率越高,其抗氧化活性越强。纯SPI膜自身存在的弱抗氧化能力可能是由于小肽和羧基末端芳香酪氨酸残基的存在[43]。添加物的组成、化学性质及其与膜聚合物基体间的相互作用以及膜结构等会影响膜的抗氧化性能。多酚类物质可增强SPI膜的抗氧化性,主要基于多酚自身的自由基清除能力。植物精油的不饱和双键、酚类以及黄酮类物质,可直接消灭单线态氧,达到清除自由基的效果。
5 大豆分离蛋白基可食膜的应用
5.1 SPI基可食膜稳定食品活性成分
近年来,SPI膜的基础物理性能正在逐步得到改善以适应生产和消费需求,同时,开发新型具有生物活性的SPI膜成为当下研究热点。食品功能因子作为极具生物活性的代表,可被广泛应用于SPI膜中,赋予膜新功能的同时,通过构建的SPI-功能因子包埋体系可增强其稳定性,保证在食品体系中的生物活性。总体来看,影响活性物质在SPI膜中稳定性的因素主要有两个方面,一是自身的相对扩散速率,二是其在混合体系中的分配系数[44]。精油和多酚等活性物质可与SPI复合,构建功能性可食膜精油作为一种从植物中提取的天然高效抑菌活性物质,已被应用于SPI膜中实现其缓控释放,达到长期抑菌目的。SPI可通过氢键等作用力与其结合并形成致密的网络结构,增强膜阻水性能的同时也延长了精油挥发的通道。研究表明,将百里香酚、肉桂和麝香草醛精油加入SPI膜体系中,均不同程度地提升了其稳定性,其中百里香酚得益于其支链烷基的阻碍作用,肉桂则由于共轭不饱和体系的扩增实现其稳定性的提高[44]。在SPI膜中添加多酚,其活性羟基促使蛋白形成更多氢键,增强了自身结构体系稳定性[39],且多酚被包埋在蛋白结构内部也不易与空气直接接触而发生氧化。整体来看,SPI膜对于食品功能因子的稳定性具有普遍提升的作用,且其良好的生物相容性可使功能因子最大程度地发挥其生物活性,是用于包埋稳定功能因子的优良绿色载体。
5.2 SPI复合膜在食品体系中的保鲜应用
由于具有良好的机型性能、阻水阻气性和生物降解性等,SPI基可食膜在食品体系有着广泛的应用(图2)。食品的氧化往往改变食物的组成及口味,是引起食物变质、造成浪费现象的主要原因。含脂量高的食品直接暴露在空气中极易发生氧化变质,不仅影响食品的外观、风味、口感,还可能存在一定的食品安全隐患。SPI基复合膜由于其良好的氧气阻隔性能而在食品抗氧化包装方面受到广泛应用。ECHEVERRíA [45]将SPI-蒙脱土(MMT)-丁香精油(CEO)活性纳米复合薄膜包裹于蓝鳍金枪鱼片上发现,金枪鱼肌肉中的硫代巴比妥酸(TBA)含量在前四天基本维持恒定,证明SPI基复合薄膜可以防止或减缓金枪鱼片中脂质的自氧化;CHO等[46]制备的SPI-玉米醇溶蛋白(SPI/CZ)复合可食膜能延缓橄榄油的氧化酸败,封藏120 d后,橄榄油的过氧化值(POV)仅为对照组的1/3;覆盖有阿魏酸-SPI膜的新鲜猪油在试验期间同样出现过氧化值显著降低的现象[23]。果蔬的褐变主要是由于不稳定的酚类物质在酶的催化作用下与氧气接触发生氧化作用、生成不愉快的黑色素,进而影响果蔬的风味、色泽。ALVES[47]将阿魏酸-SPI膜应用于鲜切苹果之上能够有效抑制苹果褐变指数的上升,保证苹果颜色较长时间内不发生变化;GHIDELLI[48]在实验中发现,经1%半胱氨酸(Cys)修饰的SPI涂层可使鲜切茄子保持新鲜状态8~9 d而不发生酶促褐变,从而延长了茄子的货架期。
新鲜蔬菜和水果在采摘后仍然进行呼吸作用,消耗自身营养物质(如蛋白质、碳水化合物)并产生二氧化碳、酒精等物质,使食物品质持续降低;储藏期间水分的不断流失导致果蔬质量减轻,枝叶萎蔫,颜色、口感被破坏。大量研究表明,SPI基复合膜能够改善单纯SPI膜亲水性强、水蒸气透过率高的缺点,因此在果蔬保鲜体系中得到了广泛的应用。ZHANG[29]证明SPI-壳聚糖复合涂层可以减少杏中的水分流失,抑制决定杏子质地的果胶分子的降解,保证其口感在储藏期间不发生明显变化。GHIDELLI等[48]发现,1%Cys-SPI涂层可以减缓鲜切茄子的重量损失速率,使鲜切茄子能较长时间的保持硬挺。阿魏酸-SPI复合膜与抗坏血酸钠相比对水蒸气有更好的阻隔性能,可以有效控制鲜切苹果的重量减轻,同时保持其硬度[47]。
微生物大量繁殖是食物腐败变质的主要因素,但SPI膜抑菌活性极弱且对水敏感,吸水后又为微生物的繁殖提供了有利条件,故常向SPI膜中添加天然抗菌剂以制备具有抗菌性的可食膜。ECHEVERR A[45]发现,添加百里香精油的SPI纳米复合薄膜使金枪鱼中的假单胞菌数目明显减少,同时乳酸菌和大肠杆菌的数量几乎保持在检出极限以下,使蓝鳍金枪鱼的保质期延长了一周左右;
A[45]发现,添加百里香精油的SPI纳米复合薄膜使金枪鱼中的假单胞菌数目明显减少,同时乳酸菌和大肠杆菌的数量几乎保持在检出极限以下,使蓝鳍金枪鱼的保质期延长了一周左右;![]() 制备的大豆蛋白-牛至-百里香精油可食膜表现出对大肠杆菌、金黄色葡萄球菌的显著抑制作用,并能显著降低鲜牛肉饼中大肠杆菌和假单胞杆菌的数量。
制备的大豆蛋白-牛至-百里香精油可食膜表现出对大肠杆菌、金黄色葡萄球菌的显著抑制作用,并能显著降低鲜牛肉饼中大肠杆菌和假单胞杆菌的数量。
综上可知,SPI基复合膜良好的阻氧性能够有效减缓食物的氧化和酸败,利于食物的长期贮存;SPI基复合膜良好的阻水阻气性能够有效抑制果蔬的呼吸作用,减缓水分的流失,保证果蔬良好的品质。同时,具有抗菌性能的SPI基复合膜能避免微生物的污染,延长产品的货架期。
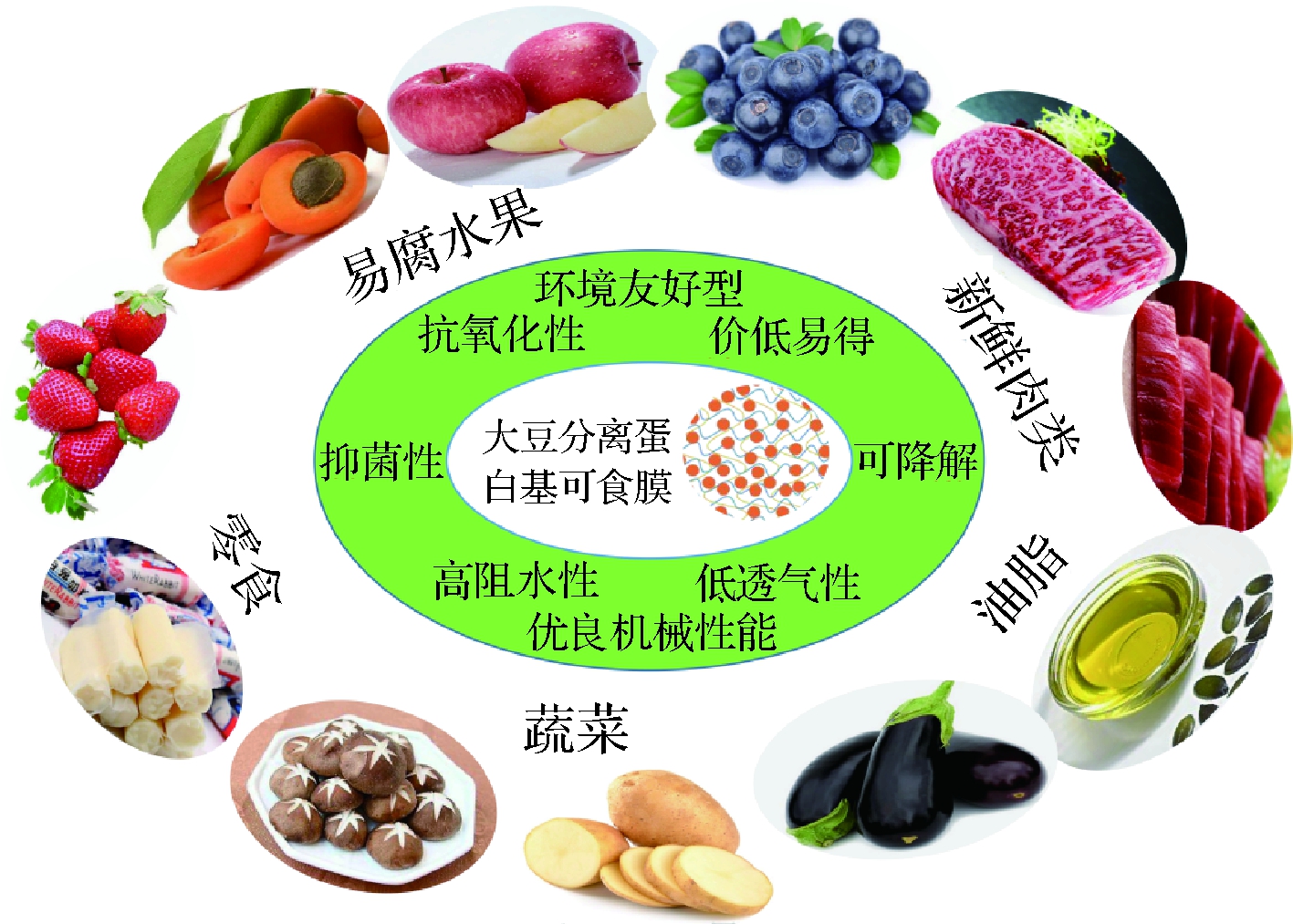
图2 大豆分离蛋白复合膜在食品体系中的应用
Fig.2 Application of soy protein isolate composite film in
food system
6 总结与展望
大豆分离蛋白由于其价低、可食、安全无害、可降解的特点成为近年来包装材料的研究热点。鉴于单一SPI膜的功能缺陷,人们通过改性蛋白以及向SPI中添加多糖制备SPI-多糖共混体系,以提高SPI膜的机械性能、改善单一SPI膜水蒸气透过率高、抗氧化能力差等缺点。但是,对于SPI膜的研究和应用还存在着诸多问题,如干法加工过程中提供的高温条件,使得蛋白质易发生降解,限制了干法技术在蛋白质类薄膜制备中的广泛应用。同时,人们将具有抗菌、抗氧化作用的功能因子加入体系之中,构建包埋活性功能因子的复合控释体系,赋予包装膜更多功能特性,从而拓宽SPI复合膜的应用范围,如可用于医药工程的药物递送等等。但功能因子如精油对温度敏感且具有不稳定易降解易挥发的特性,在制备过程中如何确定其有效作用量并最大限度保证其生物活性是值得深入探究的一个问题。
寻找新型制备方法,改善高温对蛋白质结构功能的影响;研究蛋白改性、蛋白与多糖共混作用机理,探究改性蛋白与多糖共混制备更优膜的基材配方;向蛋白膜中添加天然活性成分,探究活性成分与蛋白分子间的作用机理、缓释规律,可为新型的环境友好型、多功能食品包装材料的研究与制备提供参考。在未来,环境友好型、多功能SPI基复合膜有望代替石油基塑料成为新一代包装界的宠儿。
[1] 张赟彬, 江娟. 可食膜的研究进展[J]. 中国食品添加剂, 2011 (1): 191-198.
[2] NISHINARI K, FANG Y, GUO S, et al. Soy proteins: A review on composition, aggregation and emulsification[J]. Food Hydrocolloids, 2014, 39: 301-318.
[3] KANG H, WANG Z, ZHANG W, et al. Physico-chemical properties improvement of soy protein isolate films through caffeic acid incorporation and tri-functional aziridine hybridization[J]. Food Hydrocolloids, 2016, 61: 923-932.
[4] LI D, LI X, WU G, et al. The characterization and stability of the soy protein isolate/1-Octacosanol nanocomplex[J]. Food Chemistry, 2019, 297: 124766.
[5] SOTHORNVIT R, KROCHTA J M. Plasticizer effect on mechanical properties of β-lactoglobulin films[J]. Journal of Food Engineering, 2001, 50(3): 149-155.
[6] KOSHY R R, MARY S K, THOMAS S, et al. Environment friendly green composites based on soy protein isolate-A review[J]. Food Hydrocolloids, 2015, 50: 174-192.
[7] YUAN Y, KONG Z Y, SUN Y E, et al. Complex coacervation of soy protein with chitosan: Constructing antioxidant microcapsule for algal oil delivery[J]. LWT, 2017, 75: 171-179.
[8] YE Q, HAN Y, ZHANG J, et al. Bio-based films with improved water resistance derived from soy protein isolate and stearic acid via bioconjugation[J]. Journal of Cleaner Production, 2019, 214: 125-131.
[9] HE J, WANG R, FENG W, et al. Design of novel edible hydrocolloids by structural interplays between wheat gluten proteins and soy protein isolates[J]. Food Hydrocolloids, 2020, 100: 105395.
[10] YANG Y, REDDY N. Biothermoplastics from soyproteins by steaming[J]. Industrial Crops and Products, 2012, 36(1): 116-121.
[11] GARRIDO T, ETXABIDE A, PE ALBA M, et al. Preparation and characterization of soy protein thin films: Processing-properties correlation[J]. Materials Letters, 2013, 105: 110-112.
ALBA M, et al. Preparation and characterization of soy protein thin films: Processing-properties correlation[J]. Materials Letters, 2013, 105: 110-112.
[12] ECHEVERRíA I, EISENBERG P, MAURI A N. Nanocomposites films based on soy proteins and montmorillonite processed by casting[J]. Journal of Membrane Science, 2014, 449: 15-26.
[13] GARRIDO T, LECETA I, CABEZUDO S, et al. Tailoring soy protein film properties by selecting casting or compression as processing methods[J]. European Polymer Journal, 2016, 85: 499-507.
[14] JENSEN A, LIM L T, BARBUT S, et al. Development and characterization of soy protein films incorporated with cellulose fibers using a hot surface casting technique[J]. LWT-Food Science and Technology, 2015, 60(1): 162-170.
[15] ORTIZ C M, DE MORAES J O, VICENTE A R, et al. Scale-up of the production of soy (Glycine max L.) protein films using tape casting: Formulation of film-forming suspension and drying conditions[J]. Food Hydrocolloids, 2017, 66: 110-117.
[16] CIANNAMEA E M, STEFANI P M, RUSECKAITE R A. Physical and mechanical properties of compression molded and solution casting soybean protein concentrate based films[J]. Food Hydrocolloids, 2014, 38: 193-204.
[17] LODHA P, NETRAVALI A N. Thermal and mechanical properties of environment-friendly ‘green’plastics from stearic acid modified-soy protein isolate[J]. Industrial Crops and Products, 2005, 21(1): 49-64.
[18] VIEIRA M G A, DA SILVA M A, DOS SANTOS L O, et al. Natural-based plasticizers and biopolymer films: A review[J]. European Polymer Journal, 2011, 47(3): 254-263.
[19] CIANNAMEA E M, STEFANI P M, RUSECKAITE R A. Properties and antioxidant activity of soy protein concentrate films incorporated with red grape extract processed by casting and compression molding[J]. LWT, 2016, 74: 353-362.
[20] WIHODO M, MORARU C I. Physical and chemical methods used to enhance the structure and mechanical properties of protein films: A review[J]. Journal of Food Engineering, 2013, 114(3): 292-302.
[21] STUCHELL Y M, KROCHTA J M. Enzymatic treatments and thermal effects on edible soy protein films[J]. Journal of Food Science, 1994, 59(6): 1 332-1 337.
[22] LEE M, LEE S, SONG K B. Effect of γ-irradiation on the physicochemical properties of soy protein isolate films[J]. Radiation Physics and Chemistry, 2005, 72(1): 35-40.
[23] OU S, WANG Y, TANG S, et al. Role of ferulic acid in preparing edible films from soy protein isolate[J]. Journal of Food Engineering, 2005, 70(2): 205-210.
[24] NIE X, GONG Y, WANG N, et al. Preparation and characterization of edible myofibrillar protein-based film incorporated with grape seed procyanidins and green tea polyphenol[J]. LWT-Food Science and Technology, 2015, 64(2): 1 042-1 046.
[25] DI PIERRO P, MARINIELLO L, GIOSAFATTO C V L, et al. Solubility and permeability properties of edible pectin-soy flour films obtained in the absence or presence of transglutaminase[J]. Food Biotechnology, 2005,19(1):37-49.
[26] TANG C H, JIANG Y, WEN Q B, et al. Effect of transglutaminase treatment on the properties of cast films of soy protein isolates[J]. Journal of Biotechnology, 2005, 120(3): 296-307.
[27] PIAZZA L, DüRR-AUSTER N, GIGLI J, et al. Interfacial rheology of soy proteins-High methoxyl pectin films[J]. Food Hydrocolloids, 2009, 23(8): 2 125-2 131.
[28] ZHENG T, YU X, PILLA S. Mechanical and moisture sensitivity of fully bio-based dialdehyde carboxymethyl cellulose cross-linked soy protein isolate films[J]. Carbohydrate Polymers, 2017, 157: 1 333-1 340.
[29] ZHANG L, CHEN F, LAI S, et al. Impact of soybean protein isolate-chitosan edible coating on the softening of apricot fruit during storage[J]. LWT, 2018, 96: 604-611.
[30] MA X, YAN T, HOU F, et al. Formation of soy protein isolate (SPI)-citrus pectin (CP) electrostatic complexes under a high-intensity ultrasonic field: Linking the enhanced emulsifying properties to physicochemical and structural properties[J]. Ultrasonics Sonochemistry, 2019, 59: 104 748.
[31] YUAN Y, WAN Z L, YIN S W, et al. Characterization of complexes of soy protein and chitosan heated at low pH[J]. LWT-Food Science and Technology, 2013, 50(2): 657-664.
[32] TIAN H, XU G, YANG B, et al. Microstructure and mechanical properties of soy protein/agar blend films: Effect of composition and processing methods[J]. Journal of Food Engineering, 2011, 107(1): 21-26.
[33] GALUS S, LENART A, VOILLEY A, et al. Effect of oxidized potato starch on the physicochemical properties of soy protein isolate-based edible films[J]. Food Technology and Biotechnology, 2013, 51(3): 403-409.
[34] SILVA S S, GOODFELLOW B J, BENESCH J, et al. Morphology and miscibility of chitosan/soy protein blended membranes[J]. Carbohydrate Polymers, 2007, 70(1): 25-31.
[35] WANG L, XIAO M, DAI S, et al. Interactions between carboxymethyl konjac glucomannan and soy protein isolate in blended films[J]. Carbohydrate Polymers, 2014, 101: 136-145.
[36] ADILAH Z A M, JAMILAH B, HANANI Z A N. Functional and antioxidant properties of protein-based films incorporated with mango kernel extract for active packaging[J]. Food Hydrocolloids, 2018, 74: 207-218.
[37] XUE F, GU Y, WANG Y, et al. Encapsulation of essential oil in emulsion based edible films prepared by soy protein isolate-gum acacia conjugates[J]. Food Hydrocolloids, 2019, 96: 178-189.
[38] 左贯杰, 陈复生, 张丽芬, 等. 复合型可食用膜的研究进展[J]. 食品工业, 2016 (11): 190-194.
[39] 田梅, 覃思, 余冰, 等. 速溶绿茶及其提取物对大豆分离蛋白界面性能的影响研究[J]. 食品工业科技, 2007, 28(2): 140-145.
[40] REDDY N, YANG Y. Completely biodegradable soyprotein-jute biocomposites developed using water without any chemicals as plasticizer[J]. Industrial Crops and Products, 2011, 33(1): 35-41.
[41] WU J, SUN Q, HANG H, et al. Enhanced physico-mechanical, barrier and antifungal properties of soy protein isolate film by incorporating both plant-sourced cinnamaldehyde and facile synthesized zinc oxide nanosheets[J]. Colloids and Surfaces B: Biointerfaces, 2019, 180: 31-38.
[42] 张慧芸, 郭新宇, 康怀彬, 等. 添加适量丁香精油提高大豆分离蛋白膜性能[J]. 农业工程学报, 2014, 30(4): 247-254.
[43] WANG Y, WANG X. Binding, stability, and antioxidant activity of quercetin with soy protein isolate particles[J]. Food Chemistry, 2015, 188: 24-29.
[44] HU C Y, CHEN M, WANG Z W. Release of thymol, cinnamaldehyde and vanillin from soy protein isolate films into olive oil[J]. Packaging Technology and Science, 2012, 25(2): 97-106.
[45] ECHEVERR A I, L
A I, L PEZ-CABALLERO M E, G
PEZ-CABALLERO M E, G MEZ-GUILL
MEZ-GUILL N M C, et al. Active nanocomposite films based on soy proteins-montmorillonite-clove essential oil for the preservation of refrigerated bluefin tuna (Thunnus thynnus) fillets[J]. International Journal of Food Microbiology, 2018, 266: 142-149.
N M C, et al. Active nanocomposite films based on soy proteins-montmorillonite-clove essential oil for the preservation of refrigerated bluefin tuna (Thunnus thynnus) fillets[J]. International Journal of Food Microbiology, 2018, 266: 142-149.
[46] CHO S Y, LEE S Y, RHEE C. Edible oxygen barrier bilayer film pouches from corn zein and soy protein isolate for olive oil packaging[J]. LWT-Food Science and Technology, 2010, 43(8): 1 234-1 239.
[47] ALVES M M, GONCALVES M P, ROCHA C M R. Effect of ferulic acid on the performance of soy protein isolate-based edible coatings applied to fresh-cut apples[J]. LWT, 2017, 80: 409-415.
[48] GHIDELLI C, MATEOS M, ROJAS-ARGUDO C, et al. Extending the shelf life of fresh-cut eggplant with a soy protein-cysteine based edible coating and modified atmosphere packaging[J]. Postharvest Biology and Technology, 2014, 95: 81-87.
![]() Z K, YEMIS G P, COSKUN B K, et al. Antimicrobial activity of soy edible films incorporated with thyme and oregano essential oils on fresh ground beef patties[J]. Meat Science, 2010, 86(2): 283-288.
Z K, YEMIS G P, COSKUN B K, et al. Antimicrobial activity of soy edible films incorporated with thyme and oregano essential oils on fresh ground beef patties[J]. Meat Science, 2010, 86(2): 283-288.