何金凤1,吕新广1*,林勤保1*,李忠2,许彩芸2,谢德明3
1(暨南大学 包装工程研究所,广东普通高校产品包装与物流重点实验室,广东 珠海,519070) 2(拱北海关技术中心,广东 珠海,519015) 3(暨南大学 生命科学技术学院,广东 广州,510623)
摘 要 使用气相色谱-质谱联用仪(gas chromatography-mass spectrometry,GC-MS)建立了聚乳酸(polyactic acid, PLA)发泡餐盒中2种爽滑剂(硬脂酰胺和芥酸酰胺)的检测方法,并研究这2种爽滑剂向3种食品模拟物的迁移,PLA发泡餐盒在40 ℃和70 ℃下与异辛烷、无水乙醇和95%体积分数乙醇的双面接触;使用毒理学关注阈值法(threshold of toxicological concern, TTC)对餐盒中2种爽滑剂进行风险评估。结果表明,2种爽滑剂向95%体积分数的乙醇和无水乙醇的迁移量几乎相同,均高于在异辛烷中的迁移量;与芥酸酰胺相比,硬脂酰胺向食品模拟物中迁移的更快,有更高的迁移率,但由于芥酸酰胺在餐盒中的初始含量远大于硬脂酰胺,所以芥酸酰胺的迁移量要大于硬脂酰胺;从PLA发泡餐盒中迁移到食品模拟物中的硬脂酰胺和芥酸酰胺,其估计日摄入量(estimated daily intake,EDI)分别为0.34 mg/(人·d),0.73 mg/(人·d),均超过安全阈值0.09 mg/(人·d),说明该PLA发泡餐盒作为食品接触材料使用时要严格控制爽滑剂的用量,确保食品安全。
关键词 气相色谱-质谱联用(GC-MS);聚乳酸;发泡餐盒;硬脂酰胺;芥酸酰胺;迁移;毒理学关注阈值(threshold of toxicological concern,TTC)
第一作者:硕士研究生(吕新广教授和林勤保研究员共为通讯作者,E-mail:573760311@qq.com,7899966@qq.com)。
基金项目:国家质检总局科技计划项目(2017IK133)
收稿日期:2018-11-05,改回日期:2018-12-07
DOI:10.13995/j.cnki.11-1802/ts.019242
由于石油资源丰富,石化塑料大量用作包装材料,而聚乙烯(polyethylene, PE)、聚丙烯(polypropylene, PP)、聚氯乙烯(polyvinyl chloride, PVC)等塑料制品使用后难以在环境中降解,只能通过填埋、堆弃、焚烧等的方式处理,导致严重的白色污染现象[1-4]。近年来,由于对可再生材料需求的不断增加,环境保护、可持续发展以及废物管理得到立法的支持,这些因素均推动了市场开发生态友好型的生物降解材料[5-6]。其中,聚乳酸(polylactic acid, PLA)具有突出的生物相容性、完全无毒无害、可生物降解等优点而被广泛使用[4, 7]。但大多数生物可降解材料会添加一些添加剂,如增塑剂、抗氧化剂、热稳定剂、爽滑剂、增容剂等,来提高材料各方面的性能和加工性能[8]。
爽滑剂能够在增加聚合物链段运动的同时又不会影响聚合物的外观,因此,通常会向聚合物中添加少量的爽滑剂来提高加工过程的整体速率或在挤出、注塑、压缩成型等过程中提高表面脱模作用[9]。油酸酰胺、芥酸酰胺、硬脂酰胺及山嵛酰胺是几种常用的爽滑剂[9-11]。研究表明,硬脂酰胺添加到生物可降解材料中能够降低在加工过程中产生的摩擦剪切热,减少生物可降解材料的热降解[12]。芥酸酰胺能够提高聚烯烃薄膜的开口性能[9, 11, 13-14]。虽然爽滑剂的毒理学还没有完全得到评估,但研究表明爽滑剂有潜在的毒性,能够导致皮肤刺激等不良反应,其中芥酸酰胺能够使小鼠行动变缓,认知能力下降,而且芥酸酰胺容易水解成芥酸,引起皮肤损伤[15-16]。爽滑剂易从聚合物内迁移出来,并随温度和接触时间的增加而不断提高[9],因此研究生物降解食品接触材料中爽滑剂向食品中的迁移是很有必要的。
本文在前人研究爽滑剂的基础上[9-10, 15-18],建立PLA生物降解餐盒中2种爽滑剂硬脂酰胺和芥酸酰胺的气相色谱-质谱检测方法,研究2种爽滑剂从PLA发泡餐盒向食品模拟物中的迁移,并利用毒理学关注阈值方法(TTC)法对2种爽滑剂进行风险评估,为食品安全提供参考。
聚乳酸(PLA)生物可降解餐盒由国内某公司提供;甲醇、二氯甲烷、异辛烷(色谱纯),瑞典Oceanopak公司;无水乙醇(色谱纯),上海阿拉丁生化科技股份有限公司;硬脂酰胺标准品(>90%,CAS号:124-26-5),梯希爱(上海)化成工业发展有限公司;芥酸酰胺标准品(98%,CAS号:12-84-5),北京百灵威科技有限公司。
气相色谱-质谱联用仪(Agilent 7890A-5975C),美国安捷伦有限公司;电子分析天平(AL20),上海梅特勒-托利多仪器有限公司;样品自动浓缩工作站(Turbo VAP® II),美国Caliper公司;鼓风式烘箱(GZX-9420MBE),上海博迅有限公司;超纯水器(EPED-10TS),南京易普达科技发展有限公司。
色谱条件:色谱柱:Agilent HP-5MS (30.0 m×250 μm×0.25 μm);升温程序:初始温度为60 ℃,以40 ℃/min的速率升至200 ℃,再以20 ℃/min的速率升至280 ℃,保持5 min,载气(He)流速1 mL/min,进样量1 μL;分流比为20∶1。
质谱条件:电子轰击离子源;电子能量70 eV;传输线温度275 ℃;离子源温度230 ℃;选择离子扫描模式,硬脂酰胺定量离子为59,72,43,芥酸酰胺定量离子为59,72,55。
使用4种溶剂配制标准溶液,分别为V(二氯甲烷)∶V(甲醇)=1∶2溶液、异辛烷、无水乙醇、体积分数95%的乙醇。称取硬脂酰胺、芥酸酰胺各0.01 g(精确到0.000 1 g),分别溶解于10 mL V(二氯甲烷)∶V(甲醇)=1∶2溶液、无水乙醇或体积分数95%乙醇中,配制成质量浓度1 000 mg/L标准储备液。称取硬脂酰胺、芥酸酰胺各0.01 g(精确到0.000 1 g),溶解于100 mL异辛烷中,配制成质量浓度100 mg/L的标准储备液。将储备液密封后置于4 ℃冰箱中冷藏保存,使用时根据需要进行稀释。
(1)为检测餐盒中硬脂酰胺和芥酸酰胺的初始含量,对于硬脂酰胺,将标准储备液用V(二氯甲烷)∶V(甲醇)=1∶2溶液稀释成质量浓度为0.5、1、2、5、10和20 mg/L的工作液;对于芥酸酰胺,将标准储备液用V(二氯甲烷)∶V(甲醇)=1∶2溶液稀释成质量浓度为1.5、3、6、15、30和60 mg/L的工作液。
(2)为检测硬脂酰胺在异辛烷中的迁移,将标准储备液用异辛烷稀释成质量浓度为0.5、1、2、5、10和20 mg/L的工作液;为检测在无水乙醇和体积分数95%乙醇(体积分数95%乙醇无法直接上机检测,用无水乙醇的标曲来代替)中的迁移,将标准储备液用无水乙醇稀释成质量浓度为1、2、4、10、20和40 mg/L的工作液。
(3)为检测芥酸酰胺在异辛烷中的迁移,将标准储备液用异辛烷稀释成质量浓度为0.5、1、2、5、10、20 mg/L和质量浓度为1.5、3、6、15、30、60 mg/L的工作液;为检测在无水乙醇和体积分数95%乙醇中的迁移,将标准储备液用无水乙醇稀释成质量浓度为1、2、5、10、20和100 mg/L的工作液。
采用“溶解-沉淀”方法。将餐盒剪碎,称取0.1 g (精确到0.0001 g)放置于50 mL具塞三角瓶内,向其中加入10 mL二氯甲烷振荡,使其充分溶解,然后加入20 mL甲醇沉淀高聚物,静置24 h至上清液清澈,取适量上清液,过0.22 μm滤膜后,上机检测,取3个平行。
将发泡餐盒裁成1 cm×1 cm大小,在烘箱内干燥24 h,称取0.1 g(精确至0.000 1 g)放入10 mL模拟物中,在70 ℃下浸泡2 h,取出后擦拭干净放入恒温箱内干燥24 h后再次称重,比较不同模拟物对餐盒质量的影响,每组3个平行。餐盒的溶解程度为:
溶解程度![]()
(1)
式中:m0为浸泡前餐盒质量,mh为浸泡后餐盒质量。
依据欧盟法规NO 10/2011[19]进行迁移试验。迁移实验温度为40、70 ℃,食品模拟物选用异辛烷、95%体积分数的乙醇和无水乙醇,采用6 dm2食品接触材料及制品接触1 kg的食品或食品模拟物,将餐盒裁成1 cm×1 cm大小,充分混合均匀后,取3块置于具塞试管中(为避免餐盒片材浮起,片材用不锈钢丝穿过以使其完全浸泡于模拟物中),加入10 mL模拟物,盖好塞子并用保鲜膜密封后放入恒温箱内进行迁移实验。对于异辛烷和无水乙醇,每次到达设定的时间后,将试管充分振荡,用注射器吸取适量溶液,过0.22 μm有机滤膜,待GC-MS检测。对于95%体积分数的乙醇,每次到达设定的时间后,将试管充分振荡,用移液枪取2 mL进行氮吹,待溶剂吹干后,向其加入2 mL无水乙醇,充分振荡、静置10 min左右,用注射器吸取适量溶液,过0.22 μm有机滤膜,待GC-MS检测。每组3个平行。
为了验证迁移实验的可靠性,进行加标回收实验。向异辛烷、无水乙醇、95%体积分数的乙醇中添加质量浓度1,5和10 mg/L的标准溶液,样品溶液在70 ℃的条件下放置2 h(模拟欧盟法规中迁移的苛刻条件),每组3个平行,按照2.6节的迁移实验方法进行前处理,上机检测。
迁移量用食品模拟物中测得的硬脂酰胺(或芥酸酰胺)的质量与食品模拟物质量的比值表示[20],如公式(2)所示:
![]()
(2)
式中:M,硬脂酰胺(或芥酸酰胺)的迁移量,mg/kg;m1,硬脂酰胺(或芥酸酰胺)在食品模拟物中的质量,mg;m2,食品模拟物的质量,kg;ρ检测值,实验测得的硬脂酰胺(或芥酸酰胺)的质量浓度;V浸泡液,食品模拟物的体积,L;N,稀释倍数(若直接取食品模拟液上机,则N=1)。
迁移率用食品模拟物中测得的硬脂酰胺(或芥酸酰胺)的迁移量与餐盒中硬脂酰胺(或芥酸酰胺)的初始含量的比值表示,如公式(3)所示:
![]()
(3)
式中:MR,迁移率;M,硬脂酰胺(或芥酸酰胺)的迁移量,mg/kg;M0,餐盒中硬脂酰胺(或芥酸酰胺)的初始含量,mg/kg。
毒理学关注阈值(TTC)法是一种风险评估工具,适合评估极低暴露水平且缺少毒理数据或无毒理学数据物质[21]。TTC的原则是,为化学物(组)制定人体暴露水平阈值,人体摄入量低于该阈值,就不会对人体产生危害[22]。本文采用Toxtree(Version 2.6.13)中的Cramer决策树对2种爽滑剂的毒性进行预测,基于从TTC分析获得的安全阈值来计算2种爽滑剂的理论最大迁移量(mg/kg)。2种爽滑剂的暴露量根据美国食品药品监督管理局(Food and Drug Administration,FDA)提出的估计日摄入量(EDI)来计算,如
公式(4)所示[23]:
Migration=(f水+f酸)·M10%乙醇+f酒精·M50%乙醇+f脂肪·M脂肪
(4)
EDI/(mg/(人·d))=Migration×3kg×CF
(5)
式中:Migration为迁移量,mg/kg;Mi为在每种食品模拟物中的迁移量,mg/kg;CF为消费因子,是日常饮食中预期接触特定包装材料的部分。这里假设每人每天的食品及饮料的消费量为3 kg。食品种类分散因子(fT)反映接触每种包装材料的所有食品的不同类别,包括水性食品、酸性食品、酒精食品和脂肪性食品。
水性食品、酒精食品和脂肪类食品分别用体积分数为10%,50%和95%的乙醇作为食品模拟物,在这3种食品模拟物中的迁移实验与2.6节95%体积分数乙醇操作步骤一样,每种食品模拟物3个平行。
在配制标准储备液时发现,在70 ℃,5 min的条件下,V(二氯甲烷)∶V(甲醇)=1∶2、无水乙醇和体积分数95%的乙醇能够将硬脂酰胺和芥酸酰胺的标准品溶解;在70 ℃,15 min的条件下,异辛烷能够将芥酸酰胺标准品溶解,但硬脂酰胺的标准品不溶,当溶解的芥酸酰胺恢复到室温以后,溶液中充满了芥酸酰胺的絮状物,将溶液稀释后,絮状物消失。因此,将0.01 g(精确至0.001 g)标准品溶解在100 mL异辛烷中,芥酸酰胺在70 ℃,15 min条件下可以完全溶解且恢复室温以后没有絮状物产生,而硬脂酰胺要在70 ℃,数个小时才能够完全溶解,放在4 ℃条件下二者仍旧有絮状物质产生,每次配工作液时加热使其溶解,恢复室温后再进行稀释。说明硬脂酰胺、芥酸酰胺在乙醇中的溶解度远远高于在异辛烷中的溶解度。
硬脂酰胺、芥酸酰胺的线性方程、检出限、定量限如表1所示,Y表示峰面积,x表示分析物的浓度。
表1 硬脂酰胺和芥酸酰胺线性等式、检出限、定量限
Table 1 Linear equation, LOD, LOQ of stearmide and erucamide

注:a,b,c分别代表V(二氯甲烷)∶V(甲醇)=1∶2溶液(初始含量检测)、异辛烷(迁移实验)、无水乙醇(迁移实验,体积分数95%的乙醇标曲同乙醇)
PLA餐盒中硬脂酰胺、芥酸酰胺的含量分别为(1 881.597±59.10)和(11 123.46±202.67) mg/kg。
发泡餐盒在70 ℃,2 h条件下,在无水乙醇、体积分数95%乙醇和异辛烷中的溶解度分别为2.71%,2.62%,0.93%,相对标准偏差分别为6.67%,4.73%,7.58%。
迁移实验的加标回收率及相对标准偏差结果见表2。
表2 两种爽滑剂的加标回收率及相对标准偏差(n=3)
Table 2 Recoveries and RSDs of two slip agents(n=3)
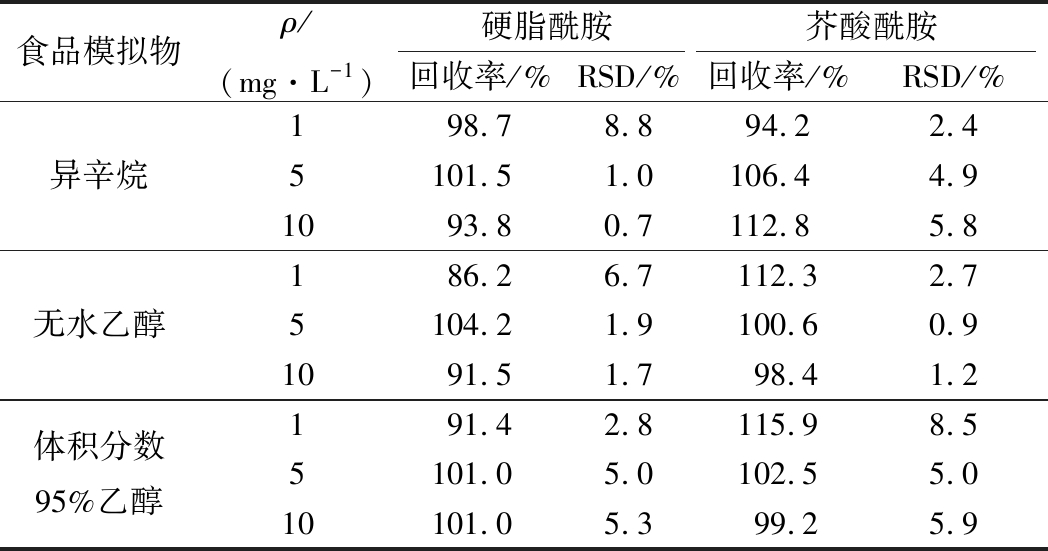
由表2可知,硬脂酰胺在异辛烷,无水乙醇和体积分数95%乙醇中的加标回收率分别为93.8%~101.5%,86.2%~104.2%,91.4%~101.0%,相对标准偏差分别为0.7%~8.8%,1.7 %~6.7%,2.8%~5.3%。芥酸酰胺在异辛烷,无水乙醇和体积分数95%乙醇的加标回收率分别为 94.2%~112.8%,98.4%~112.3%,99.2%~115.9%,相对标准偏差分别为2.4%~5.8%,0.9%~2.7%,5.0%~8.5%,说明该方法的准确度和精密度较好,满足实验要求。
3.6.1 两种爽滑剂在无水乙醇、体积分数95%乙醇中迁移量的对比
从图1可以看出,硬脂酰胺或芥酸酰胺在2种食品模拟物中的迁移量几乎相同,到达迁移平衡的时间也无明显差异。由3.4节餐盒溶解度实验可知,餐盒在乙醇和体积分数为95%乙醇中的溶解程度基本无差异,因此2种爽滑剂向乙醇和体积分数为95%乙醇中的迁移量几乎相同。而体积分数为95%乙醇在上机检测之前需要经过氮吹和复溶的操作过程,因此对于2种爽滑剂在70 ℃,95%体积分数的乙醇中迁移,只进行了2 h情况下的迁移。
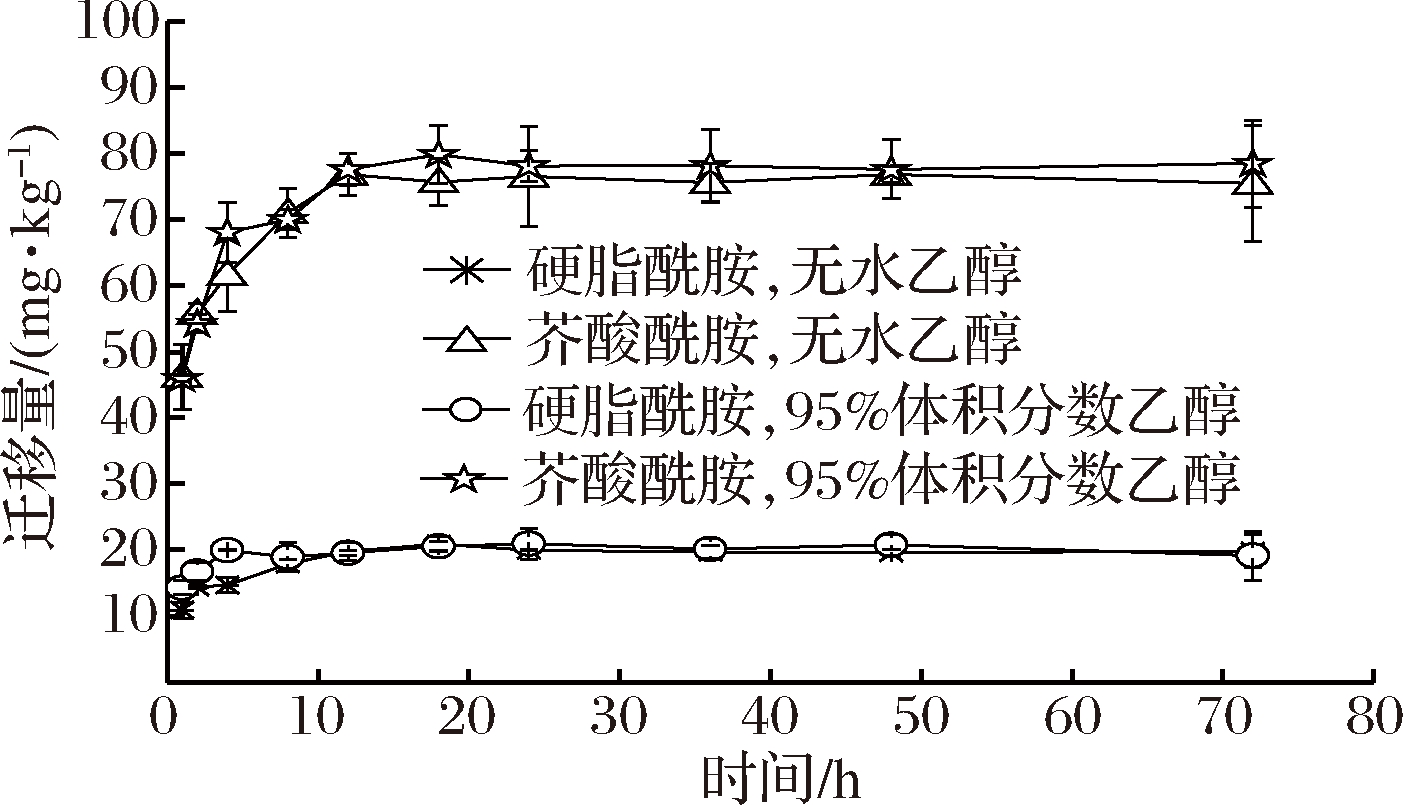
图1 两种爽滑剂向无水乙醇和95%体积分数乙醇中的迁移(40 ℃,n=3)
Fig.1 Migration of two slip agents in ethanol and 95% ethanol
3.6.2 食品模拟物对2种爽滑剂迁移的影响
实验对比了3种食品模拟物(异辛烷、无水乙醇、95%体积分数乙醇)对餐盒中2种爽滑剂迁移的影响。由图2可知,2种爽滑剂在异辛烷的迁移量均低于在无水乙醇和95%体积分数乙醇中的迁移。原因可能是:(1)2种爽滑剂在异辛烷中的溶解度较低,餐盒在异辛烷中的溶解度远远低于在无水乙醇和95%体积分数乙醇中的溶解度;(2)无水乙醇和95%体积分数的乙醇对PLA材料存在溶胀现象。

a-硬脂酰胺;b-芥酸酰胺
图2 两种爽滑剂在3种食品模拟物中的迁移(n=3)
Fig.2 Migration of two slip agents in three food simulants
研究表明,对体积分数50%的乙醇接触之前和接触之后的PLA薄膜进行扫描电子显微镜(scanning electron microscope, SEM)观察,发现无论是无定形的PLA还是半结晶的PLA,与50%体积分数乙醇接触以后,薄膜都会产生很大的孔腔,说明50%体积分数乙醇对薄膜强大的溶胀和渗透作用,在50%体积分数的乙醇中乳酸的迁移量会增加,也是因为50%体积分数乙醇对聚合物的强亲和力作用,对PLA产生溶胀现象,从而促进乳酸的迁移[24]。而95%体积分数乙醇和无水乙醇与50%体积分数乙醇相比含有更多的乙醇,对PLA的溶胀程度更大,因此迁移量也更大。
3.6.3 爽滑剂的物化特性对迁移的影响
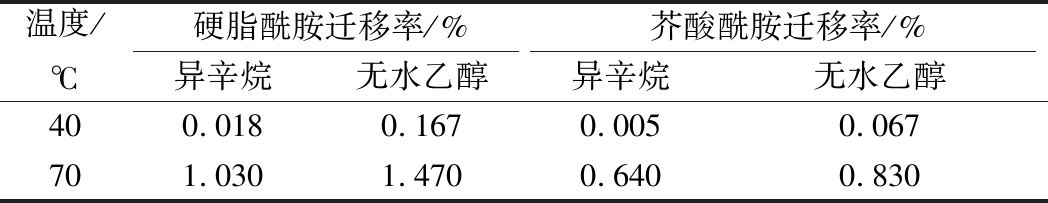
表3为2种爽滑剂在40 ℃和70 ℃下向异辛烷和无水乙醇迁移的最大迁移率。通过图2和表3可以看出,硬脂酰胺比芥酸酰胺到达迁移的平衡时间短,也更易迁移,这是因为硬脂酰胺的分子量(283.5)比芥酸酰胺的(337.6)小,爽滑剂迁移到表面的迁移速度很大程度上取决于添加剂碳链的长度和聚合物的结晶度,爽滑剂越大(碳原子越多),越易与聚合物相容,迁移的越少[9]。
表3 两种爽滑剂在异辛烷和无水乙醇中的最大迁移率(n=3)
Table 3 Maximum migration rates of two slip agentsinisooctane and ethanol
3.6.4 温度对两种爽滑剂的迁移影响
通过图2和表3可以看到,无论是哪种食品模拟物,在同一迁移时间下,40 ℃下2种爽滑剂的迁移量比70 ℃下的迁移量小,这是因为温度的升高会加快分子的热运动,而且高温提高了2种润滑剂在食品模拟物中的溶解度,从而提高2种爽滑剂在食品模拟物中的迁移量。
按TTC决策树将待评价的物质归类(使用Toxtree软件,将物质分为CramerⅠ、Ⅱ、Ⅲ类),从而得出该化学物质的TTC安全阈值,其中CramerⅠ、Ⅱ、Ⅲ类物质的安全阈值分别为1.8、0.54、0.09 mg/(人·d)[25]。通过Toxtree软件查得,2种爽滑剂均属于CramerⅢ类物质,因此安全阈值为0.09 mg/(人·d)。聚乳酸是以乳酸为原料聚合而成的聚酯,属于聚酯家族[26-27]。FDA提供的聚酯类的消费因子CF=0.05。2种爽滑剂在70 ℃,2 h条件下在各种食品模拟物中的迁移量以及聚酯中各种食品模拟物的分配系数见表4。
硬脂酰胺的估计日摄入量为EDI=0.34 mg/(人·d),芥酸酰胺的估计日摄入量EDI=0.73 mg/(人·d),均大于安全阈值0.09 mg/(人·d),说明此生物可降解餐盒中2种爽滑剂的迁移是远超过安全阈值的。
表4 两种爽滑剂在70 ℃,2 h下食品模拟物中的迁移量以及分配系数(n=3) 单位:mg/kg
Table 4 Migration quantity of two lubricants in foodsimulants and fT

注:“-”,公式中没有使用到酸性食品模拟物的迁移量,因此没有做2种物质在3%乙酸中的迁移;用95%乙醇代替橄榄油来模拟脂肪类食品。
建立了聚乳酸发泡餐盒中2种爽滑剂的检测方法,探究2种爽滑剂在3种食品模拟物中的迁移,结果表明,建立的方法简单,不需要对2种爽滑剂进行衍生化处理,具有良好的准确度和精密度,适用于PLA发泡餐盒中2种爽滑剂的检测。由于乙醇和95%体积分数乙醇存在溶胀和渗透作用,2种爽滑剂在异辛烷中的溶解度低于在乙醇和95%体积分数乙醇中的溶解度,因此2种爽滑剂在乙醇和95%体积分数乙醇中的迁移量更大,与芥酸酰胺相比,硬脂酰胺有更快的迁移速度和更高迁移率,更容易从餐盒迁移而进入食品。餐盒中2种爽滑剂的迁移均超过限量,建议企业在满足产品性能以及加工工艺的前提下,极大可能降低2种爽滑剂的添加量,使2种润滑剂的迁移量在安全阈值范围内。
参考文献
[1] ZHOU C, FANG W, XU W, et al. Characteristics and the recovery potential of plastic wastes obtained from landfill mining[J]. Journal of Cleaner Production, 2014, 80: 80-86.
[2] SALEEM J, ADIL RIAZ M, GORDON M. Oil sorbents from plastic wastes and polymers: A review[J]. Journal of Hazardous Materials, 2018, 341: 424-437.
[3] 韩巧臻. 白色垃圾污染现状及防治对策[J]. 阴山学刊, 2001(5): 29-30.
[4] FUKUSHIMA K, TABUANI D, ABBATE C, et al. Preparation, characterization and biodegradation of biopolymer nanocomposites based on fumed silica[J]. European Polymer Journal, 2011, 47(2): 139-152.
[5] SCARFATO P, DI-MAIO L, INCARNATO L. Recent advances and migration issues in biodegradable polymers from renewable sources for food packaging [J]. Journal of Applied Polymer Science, 2015, 132(48): 42 597
[6] 郭昊奇. 以白色化学污染为例浅析我国高分子可降解材料的应用现状及前景[J]. 化工管理, 2017(32): 59-60.
[7] Al-OTHMAN O, JAWAID M, SABA N. An overview on polylactic acid, its cellulosic composites and applications[J]. Current Organic Synthesis, 2017, 14(2):156-170.
[8] SYED ALI ASHTER. 6-additives and modifiers for biopolymers[M]. Oxford:William Andrew Publishing, 2016:153-178.
[9] FARAJZADEH M A, EBRAHIMI M, RANJ A, et al. HPLC and GC methods for determination of lubricants and their evaluation in analysis of real samples of polyethylene[J]. Microchimica Acta, 2006, 153(1-2): 73-78.
[10] 房宁,王子剑,赵劲松,等. 气相色谱-质谱法测定食品接触材料润滑剂在脂类食品模拟物中迁移量[J]. 中国食品卫生杂志, 2016,28(3): 319-322.
[11] 任晓兵. 开口爽滑剂在低密度聚乙烯薄膜中的应用[J]. 当代化工, 2017,46(1): 173-176.
[12] GUNNING M A, GEEVER L M, KILLION J A, et al. Melt processing of bioplastic composites via twin screw extrusion and injection molding[J]. Polymer-Plastics Technology and Engineering, 2014, 53(4): 379-386.
[13] 曹胜先,吕红丽,汪涵. 新型开口爽滑剂母料在聚烯烃薄膜中的应用[J]. 塑料科技, 2009,37(3): 59-63.
[14] 聂海平,吴剑,吴国岚. 爽滑剂和防粘开口剂在塑料薄膜中的应用[J]. 塑料助剂, 2017(3): 19-22.
[15] FEKETE Z, R FUSZ T, ANGYAL V, et al. Gas chromatographic-mass spectrometric analysis and subsequent quality improvement of plastic infusion packaging materials[J]. Journal of Pharmaceutical and Biomedical Analysis, 2014, 97: 111-115.
FUSZ T, ANGYAL V, et al. Gas chromatographic-mass spectrometric analysis and subsequent quality improvement of plastic infusion packaging materials[J]. Journal of Pharmaceutical and Biomedical Analysis, 2014, 97: 111-115.
[16] LV G, WANG L, LIU J, et al. Method for determination of fatty acid amides in polyethylene packaging materials—gas chromatography/mass spectrometry[J]. Journal of Chromatography A, 2009, 1 216(48): 8 545-8 548.
[17] 郝萍,王海,韩晓昱,等. 用气相色谱法测定高密度聚乙烯中爽滑剂芥酸酰胺的含量[J]. 石化技术与应用, 2013,31(1): 71-73.
[18] GARRIDO-L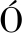 PEZ
PEZ 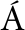 , ESQUIU V, TENA M T. Determination of oleamide and erucamide in polyethylene films by pressurised fluid extraction and gas chromatography[J]. Journal of Chromatography A, 2006, 1 124(1-2): 51-56.
, ESQUIU V, TENA M T. Determination of oleamide and erucamide in polyethylene films by pressurised fluid extraction and gas chromatography[J]. Journal of Chromatography A, 2006, 1 124(1-2): 51-56.
[19] Commission Regulation (EU) No 10/2011 of 14 January 2011 on plastic materials and articles intended to come into contact with food[S].Official Journal of the European Union,2011.
[20] 张明, 林勤保,单利君,等.石墨烯/低密度聚乙烯复合包装膜中2种抗氧化剂向食品模拟物异辛烷的迁移[J]. 食品科学,2017,38(20):209-214.
[21] HENNES E C. An overview of values for the threshold of toxicological concern[J]. Toxicology Letters, 2012, 211(3): 296-303.
[22] 杨岳平,胡长鹰,李克亚,等. 毒理学关注阈值方法在食品接触材料风险评估中的应用[J]. 食品科学, 2015,36(23): 334-339.
[23] Guidance Documents & Regulatory Information by Topic - Guidance for Industry: Preparation of Premarket Submissions for Food Contact Substances: Chemistry Recommendations[S].Offical of Food Additive Safety, 2007.
[24] SCARFATO P, DI MAIO L, MILANA M R, et al. Performance properties, lactic acid specific migration and swelling by simulant of biodegradable poly(lactic acid)/nanoclay multilayer films for food packaging[J]. Food Additives & Contaminants. Part A, Chemistry, Analysis, Control, Exposure & Risk Assessment. 2017, 34(10): 1 730-1 742.
[25] KROES R. Structure-based thresholds of toxicological concern (TTC): Guidance for application to substances present at low levels in the diet[J]. Toxicologic Pathology, 2016, 32(Suppl.2): 93.
[26] JABEEN N, MAJID I, NAYIK G A. Bioplastics and food packaging: A review[J]. Cogent Food & Agriculture, 2015, 1:117 749.
[27] 张龙翼,晏宸然,张崟,等. 聚乳酸的合成方法及其应用[J]. 农产品加工, 2018(10): 63-66.
HE Jinfeng1, LV Xinguang1*, LIN Qinbao1*, LI Zhong2, XU Caiyun2, XIE Deming3
1(Key Laboratory of Product Packaging and Logistics, Packaging Engineering Institute,Jinan University, Zhuhai 519070, China) 2(Gongbei Customs Technical Center, Zhuhai 519015, China) 3(College of Life Science and Technology, Jinan University, Guangzhou 510623, China)
Abstract A method using gas chromatography-mass spectrometry(GC-MS)to detect two slipping agents, stearic amide and erucic amide, in polyactic acid (PLA) foaming containers, was established. Migrations of two slipping agents into three food simulants (isooctane, ethanol, and 95% ethanol) were investigated at 40 ℃ and 70 ℃. PLA foaming containers were double-sided contacted with food simulants. Besides, threshold of toxicological concern (TTC) was introduced to assess the safety of two slipping agents in foods. It was shown that the migration amounts of two slipping agents into ethanol and 95% ethanol were almost the same, which were both higher than migrating to isooctane. Compared with erucic amide, stearic mide migrated faster into food simulants and had higher migration rate. However, since the initial content of erucic amide in PLA foaming containers was much higher than that of stearic amide, the migration amount of erucic amide was higher. Estimated daily intakes (EDI) of migrated stearic amide and erucic amide in food simulants were 0.34 mg/person/day and 0.73 mg/person/day, respectively. Both were higher than the safety threshold 0.09 mg/person/day, which means the amount of slipping agent used in this PLA foaming containers should be strictly controlled to ensure food safety.
Key words gas chromatography-mass spectrometry (GC-MS); polylactic acid; foaming containers; stearic amide; erucic amide; migration; threshold of toxicological concern (TTC)