高凤苑1,2,3,韦东来1,2,3,韦冬萍1,2,3,王冰1,2,3,吴吕归1,2,3,蓝平1,2,3*,廖安平1,2,3
1(广西民族大学 化学化工学院,广西 南宁,530006) 2(广西多糖材料及改性重点实验室(广西民族大学),广西 南宁,530006) 3(广西高校化学与生物转化过程新技术重点实验室(广西民族大学),广西 南宁,530006)
摘 要 以木薯淀粉为原料,丙烯酰胺为单体,N,N-亚甲基双丙烯酰胺为交联剂,过硫酸钾为引发剂,采用微波辐射技术辅助制备木薯淀粉基水凝胶。探究单体、交联剂、引发剂用量等因素对水凝胶溶胀性能的影响。当淀粉与丙烯酰胺用量比为1∶3,N,N-亚甲基双丙烯酰胺为0.02 g,过硫酸钾0.05 g时,微波400 W,60 s制得的木薯淀粉水凝胶达最高吸水倍率。通过傅里叶红外光谱仪(fourier transform infrared spectrometer,FTIR)、场发射扫描电子显微镜(field emission scanning electronic microscope,FESEM)等分析测试手段对其进行表征,结果表明已成功制备木薯淀粉基水凝胶。该水凝胶溶胀平衡比在35 ℃时达到最大,且在室温条件下保水性良好。该研究为淀粉水凝胶的制备应用提供了实验依据,提高了木薯淀粉的附加值。
关键词 木薯淀粉;水凝胶;温敏性;溶胀性能
第一作者:硕士(蓝平教授为通讯作者,E-mail:gxlanping@163.com)。
基金项目:广西生物多糖分离纯化及改性研究平台建设(桂科ZY18076005);广西大学生创新创业训练计划项目(201710608176);广西民族大学研究生教育创新计划项目重点项目(gxun-chxzs2017127)
收稿日期:2018-07-30,改回日期:2018-09-05
DOI:10.13995/j.cnki.11-1802/ts.018392
天然高分子,如多糖类,由于其无毒、良好的生物相容性、生物降解、来源丰富等特点正在被广泛关注[1-3]。木薯淀粉是一种天然高分子聚合物,也是自然界来源最丰富的多糖,且应用简便,不需提取,价格低廉,可以被广泛应用。高分子水凝胶材料是一类能迅速吸收大量水,并且可以保持水分而又不溶于水的材料,具有三维网络结构的功能高分子材料[4]。水凝胶可以感知外界刺激的微小变化,并对刺激产生敏感性响应,常通过体积溶胀或收缩来实现[5-6]。
水凝胶的制备方法很多,但很多都有局限性。物理法制备的水凝胶对环境友好、得率高,但普遍存在能耗高,结构不稳定的问题,应用性较差[7]。化学方法则是采用纯试剂制备水凝胶,产率低,响应性能差,且不利于环境保护。本实验采用微波法制备水凝胶,与化学方法相比,操作简单,热效率高,物质受热均匀,可在无溶剂或少溶剂条件下进行,可控性良好[8],且形成的水凝胶具有良好的溶胀性和温度敏感性。木薯淀粉基水凝胶不仅可以提高淀粉的使用价值,扩大淀粉应用范围,而且还可以改善合成高分子的性能。将分散的多糖材料引入合成高分子网络结构,形成多糖高分子复合水凝胶[1-3],这类研究已经成为当前热点。
木薯淀粉(工业级):广西武鸣安宁淀粉有限公司;丙烯酰胺(AM,化学纯):国药集团化学试剂有限公司;N,N-亚甲基双丙烯酰胺(NMBA,分析纯):阿达玛斯;过硫酸钾(KPS,分析纯):广东市金华大化学试剂有限公司;无水乙醇(分析纯),成都市科隆化学品有限公司;NaOH(分析纯),国药集团化学试剂有限公司。
JHS恒速数显控制器,杭州仪表电机有限公司;DF-101S集热式恒温加热磁力搅拌器,巩义市予华仪器有限责任公司;冷冻干燥机,埃朗科技国际贸易有限公司;BSA2245电子天平(0.0001g),赛多利斯科学仪器(北京)有限公司;MAGNA-1R550傅里叶变换红外光谱仪,美国Thermo公司; X’Pert PRO X-射线衍射仪,荷兰帕纳科公司PANalytical;STA449F3 TG-DSC同步热分析仪,德国耐驰仪器制造有限公司;SUPRA 55 Sapphire场发射扫描电子显微镜,德国卡尔蔡司公司;WBFY-205微电脑微波化学反应器,巩义市予华仪器有限责任公司。
称取2 g木薯淀粉加入15 mL 1 mol/L NaOH溶液,搅拌至黄色透明状,加入AM于混合物中,再加入5 mL蒸馏水以100 r/30 min的频率搅拌,加入一定量KPS,加入2 mL蒸馏水稀释,继续搅拌30 min,最后加入一定量NMBA和2 mL蒸馏水,继续搅拌至完全均匀[9]。搅拌结束后,放入培养皿中置于微波反应器中反应,过夜静置,放在蒸馏水中泡2 h,将粗产水凝胶在40 ℃烘箱中干燥24 h,备用。
2.2.1 引发剂用量对水凝胶溶胀性能的影响
固定木薯淀粉用量为2 g,NMBA用量为0.02 g,淀粉与AM用量比为1∶3,依次改变KPS用量:0.02、0.03、0.04、0.05、0.06 g,微波400 W,工作30 s。
2.2.2 交联剂用量对水凝胶溶胀性能的影响
固定木薯淀粉用量为2 g,淀粉与AM用量比为1∶3,KPS用量为0.05 g,依次改变NMBA用量:0.01、0.02、0.03、0.04、0.05 g,微波400 W,工作30 s。
2.2.3 原料与单体用量对水凝胶溶胀性能的影响
固定木薯淀粉用量为2 g,NMBA用量为0.02 g,KPS用量为0.05 g,依次改变淀粉与AM用量比:1∶1,1∶2,1∶3,1∶4,1∶5,微波400 W,工作30 s。
2.2.4 微波功率对水凝胶溶胀性能的影响
试剂用量最佳时,木薯淀粉用量为2 g,NMBA用量为0.02 g,KPS用量为0.05 g,淀粉与AM用量比为1∶3,改变微波功率:0、80、240、400、640、800 W,工作30 s。
2.2.5 微波时间对水凝胶溶胀性能的影响
试剂用量最佳时,木薯淀粉用量为2 g,NMBA用量为0.02 g,KPS用量为0.05 g,淀粉与AM用量比为1∶3,微波功率为400 W,改变工作时间:30、60、90 s。
2.3.1 水凝胶溶胀度测定
通过重量法测定水凝胶的溶胀程度。称取小块水凝胶样品于尼龙袋中,记做W0,完全浸入100 mL蒸馏水中,室温下每30 min测一次质量,浸泡3~4 h左右,取出水凝胶把尼龙袋中的水吸干,称取质量记做W[10]。按公式(1)计算室温下的平衡溶胀能力:
![]()
(1)
式中:SR为水凝胶溶胀平衡比;W0和W分别是溶胀前和溶胀后水凝胶的质量,g。
2.3.2 水凝胶脱水率测定
将达到溶胀平衡的水凝胶试样在室温下自然放置,每30 min测一次质量,记做Wn,直到水凝胶的质量保持基本稳定不变[11]。按公式(2)计算水凝胶脱水率:
脱水率![]()
(2)
式中:Wn和W0分别是溶胀平衡和溶胀前水凝胶的质量,g。
2.3.3 水凝胶温敏特性测定
称取一定量的干凝胶浸泡于100 mL蒸馏水中,分别将试样放在25、35、45、55 ℃水浴中,每个温度放置4 h达到溶胀平衡[11],按公式(1)计算溶胀百分比。
2.3.4 水凝胶溶胀-退胀性能测定[11]
把在35 ℃条件下平衡溶胀的水凝胶快速放到称有55 ℃的二次蒸馏水的烧杯中,水凝胶的体积会因失水而变小,每隔5 min将水凝胶从烧杯中取出并称重,计算溶胀百分比,直至水凝胶的质量不再发生变化[11],按公式(3)计算水的保留率。
![]()
(3)
式中:WR为水凝胶中水的保留率;Mt和M0分别是t时刻水凝胶的质量和达到溶胀平衡时水凝胶的质量,g。
2.4.1 红外(fourier transform infrared spectrometer,FTIR)表征
将溶胀后的水凝胶用液氮脆断,置于冷冻干燥器中完全冷冻干燥。取1~2 mg完全干燥的水凝胶样品,与50~100 mg干燥的KBr粉末混合,置于玛瑙研钵中充分研磨,将研磨好的混合物粉末放入压模中,在10 kPa的压力下压制成透明薄片,小心将压片取出,放入红外光谱仪进行测试,在4 000~500 cm-1波长范围内扫描。
2.4.2 扫描电镜(field emission scanning electronic microscope,SEM)表征
将溶胀后的水凝胶用液氮脆断,置于冷冻干燥器中完全冷冻干燥。取小块干燥后的样品四周贴好导电胶进行喷金处理,置于扫描电镜中观察其形貌。
2.4.3 X射线衍射(x-ray diffractometry,XRD)表征
将完全干燥的水凝胶研磨成粉末,压片后置于XRD中扫描得到XRD图。
2.4.4 热重分析(thermogravimetric,TG)表征
取200 mg样品粉末放入坩埚中,温度范围为35~800 ℃,在升温速率为10 ℃/min下进行检测。
3.1.1 引发剂用量对水凝胶溶胀性能的影响
引发剂KPS会引发大量活跃的自由基,促进淀粉结构与单体接枝共聚[8]。如图1所示,引发剂的量在0.05 g时,溶胀百分比达到最大,这是由于KPS浓度较小时,引发的自由基数量较少,使单体与原料接枝率不够,不利于凝胶吸水溶胀;而当KPS浓度过高时,自由基相对增加,引发单体与原料接枝过多,使凝胶的网络密度增大,致使水分子难于进入凝胶内部。此外,KPS的浓度过高可能会降解自由基,引起溶胀减少[12]。
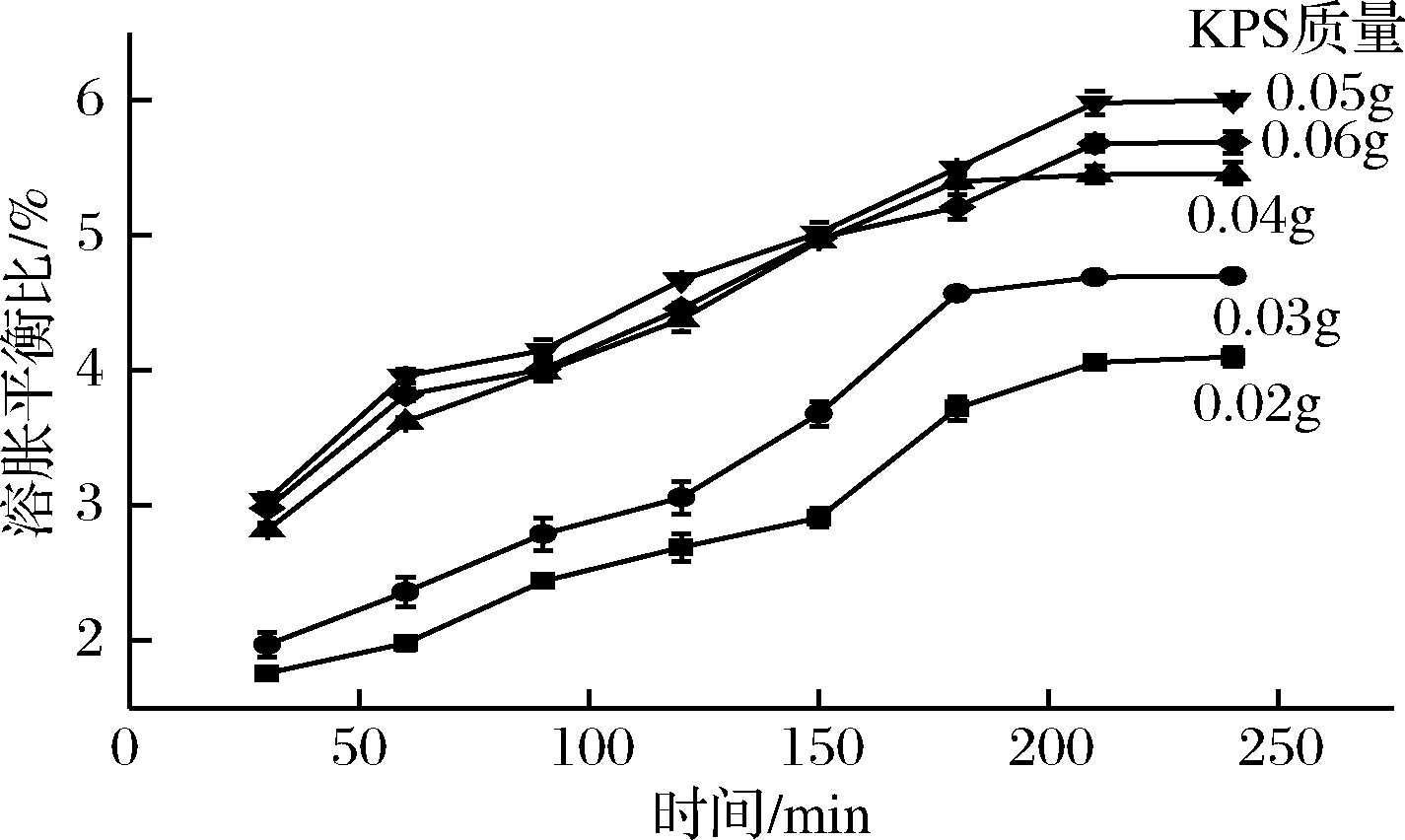
图1 KPS质量对水凝胶溶胀百分比影响
Fig.1 Effects of different concentrations of potassium persulfate on the swelling percentage of hydrogel
3.1.2 交联剂用量对水凝胶溶胀性能的影响
如图2所示,交联剂的最佳用量为0.02 g。交联剂量不足导致凝胶交联密度不足,强度不够,溶胀性能较低;当交联剂用量超过0.02 g时,交联剂用量过大,相应的交联密度过大,生成的水凝胶交联点增多,交联间距变小,交联更加密集,自由空间减少,水凝胶中的自由水变少,使得水凝胶的溶胀平衡比逐渐降低[13]。
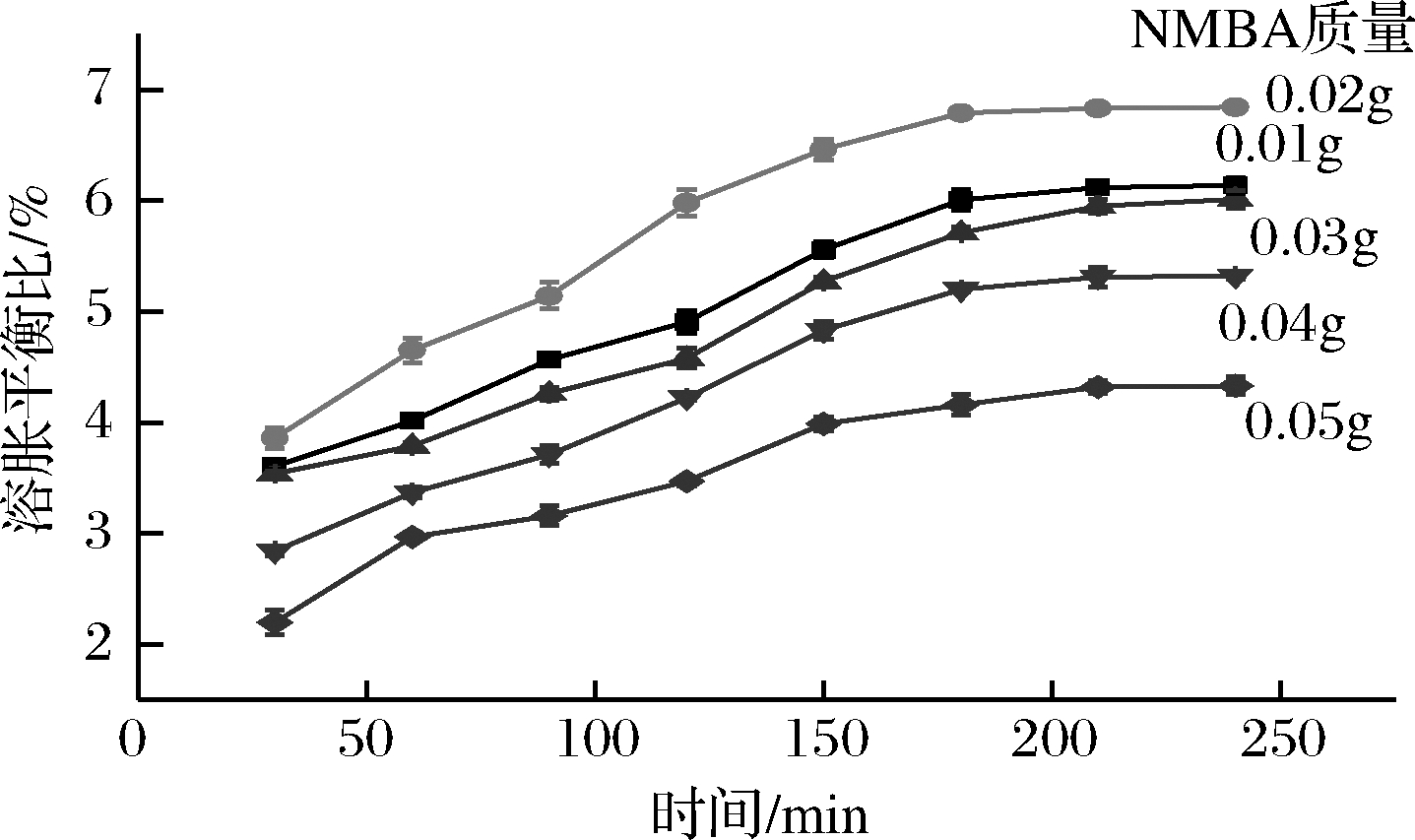
图2 NMBA质量对水凝胶溶胀百分比影响
Fig.2 Effects of different concentrations of N, N-methylenebisacrylamide on the swelling percentage of hydrogel
3.1.3 原料与单体用量对水凝胶溶胀性能的影响
随着单体Am浓度的增加,更多单体自由基接枝到淀粉上,更好地形成聚合物网络,使吸水性良好。如图3所示,当淀粉与Am用量比为1∶3时,溶胀性能最佳。再增加用量比使得溶胀性能大幅下降,因为介质黏度增加,阻碍了自由基和单体自由结合形成高效网络结构,所以使得吸水性下降[14]。
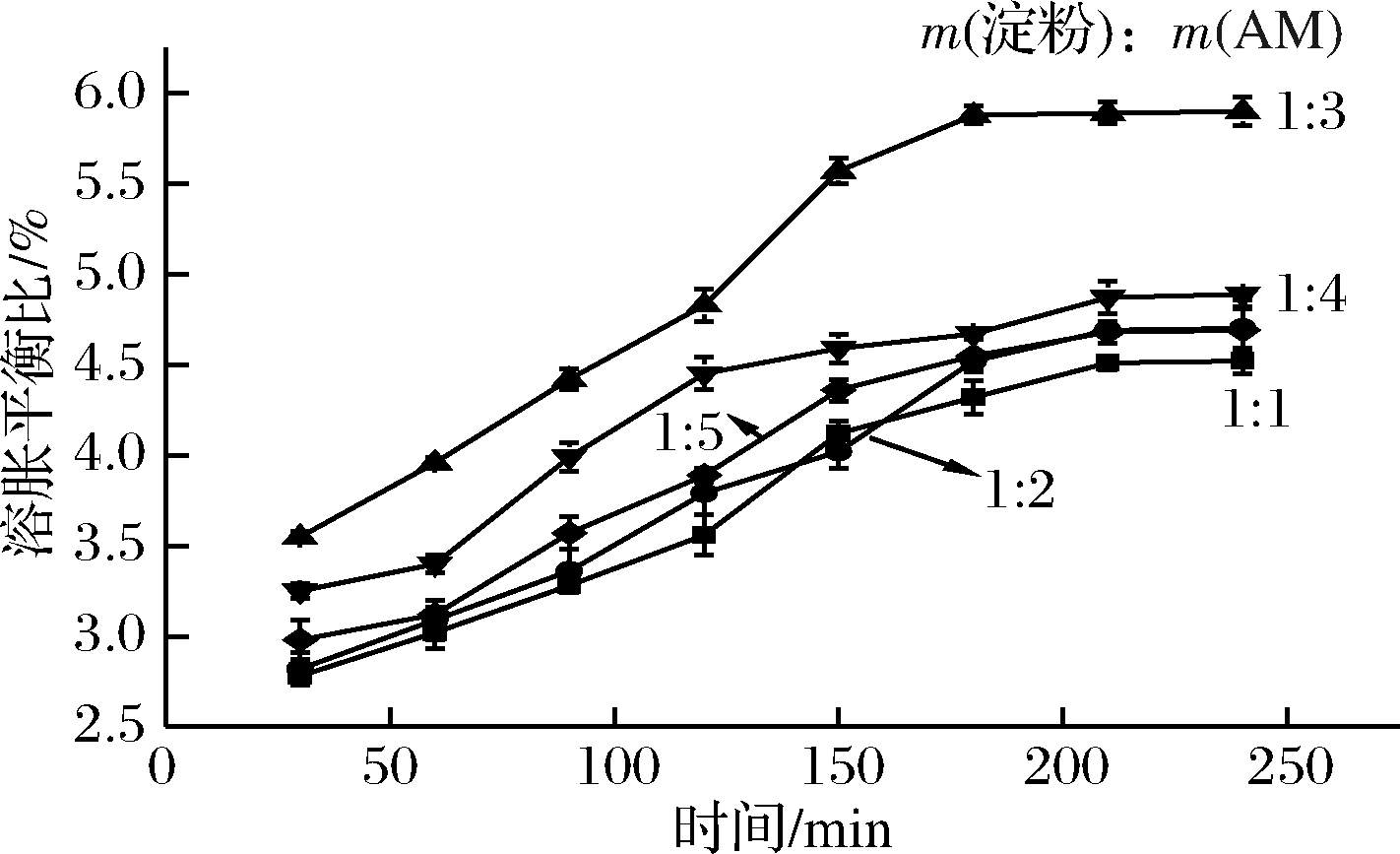
图3 淀粉与丙烯酰胺质量比对水凝胶溶胀百分比影响
Fig.3 Effects of different mass ratios of starch to acrylamide on the swelling percentage of hydrogel
3.1.4 微波功率对水凝胶溶胀性能的影响
如图4所示,随着微波功率的增加,反应温度升高,生成自由基的速率增加,加快淀粉与单体接枝,在微波功率为400 W时,水凝胶具有最佳溶胀百分比。微波功率过低,辐射不够,凝胶交联反应不完全,吸水性能不足;微波功率过大,自由基反应增加,聚合反应剧烈,部分反应物甚至喷出反应器,破坏形成的网络结构,吸水性降低[15]。
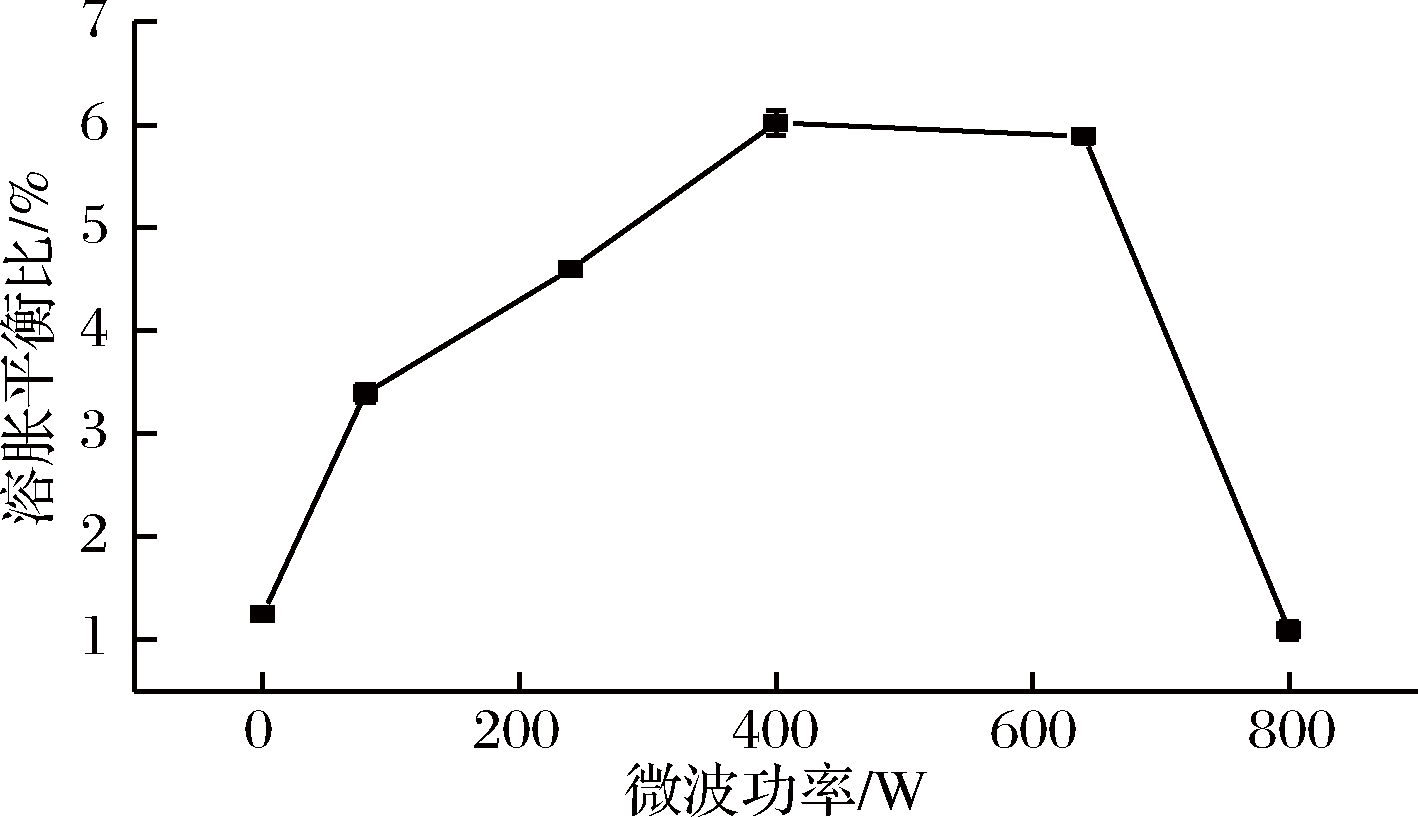
图4 微波功率对水凝胶溶胀百分比影响
Fig.4 Effects of microwave power on the swelling percentage of hydrogel
3.1.5 微波时间对水凝胶溶胀性能的影响
如图5所示,随着微波时间的延长,水凝胶的吸水性呈先增大后减小的趋势。反应时间的延长为反应体系提供更多的能量,有利于自由基的形成,促进三维网状结构的产生,促进溶胀度的平衡[16]。最佳反应时间为60 s,当微波时间过长时,热量过多,温度过高,引起爆聚反应,使聚合产物的交联网络体系变差,甚至喷出反应器,使溶胀性能下降。
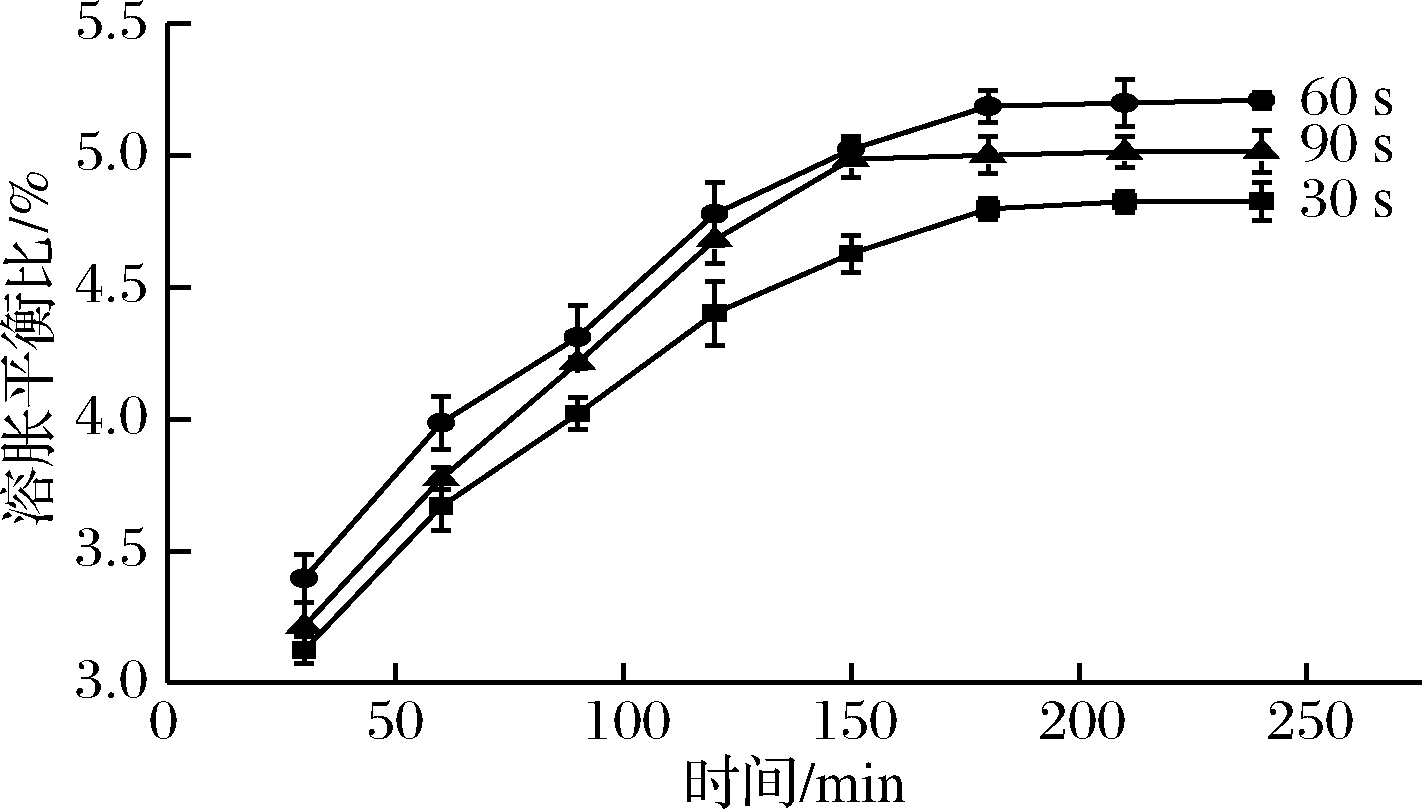
图5 微波时间对水凝胶溶胀百分比影响
Fig.5 Effects of microwave time on the swelling percentage of hydrogel
3.2.1 淀粉水凝胶的红外光谱解析
由图6可知,水凝胶除了有原淀粉本身的吸收峰,还在3 429 cm-1附近存在N—H对称和不对称宽峰,在2 943 cm-1附近存在C—H不对称伸缩振动和弯曲振动,在1 458 cm-1附近存在C![]() O伸缩振动峰,在1 670 cm-1附近出现C—N链的伸缩振动峰,是酰胺特征峰,说明AM成功嫁接到淀粉骨架上[17]。
O伸缩振动峰,在1 670 cm-1附近出现C—N链的伸缩振动峰,是酰胺特征峰,说明AM成功嫁接到淀粉骨架上[17]。
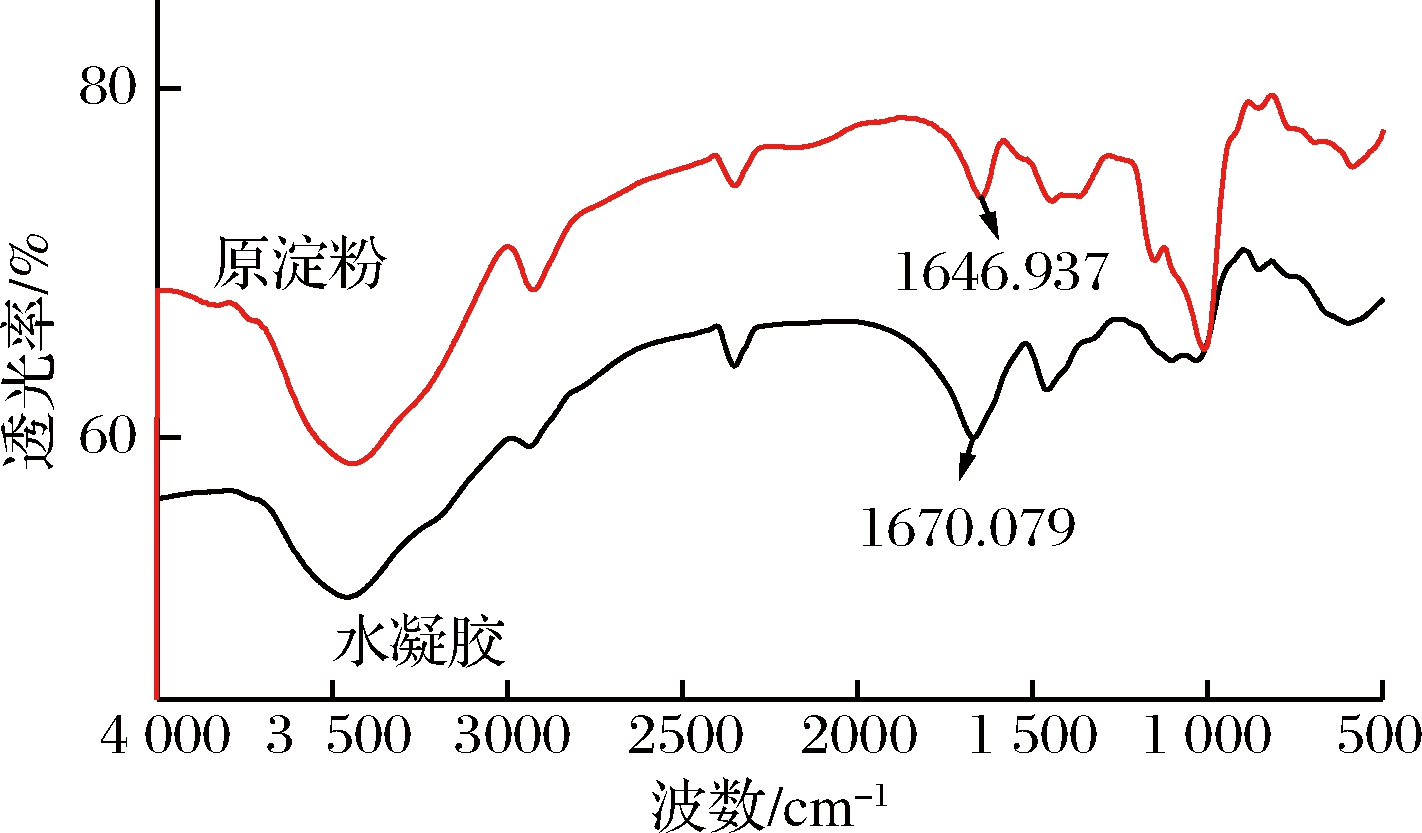
图6 木薯淀粉和水凝胶红外光谱图
Fig.6 Infrared spectrum of cassava starch and hydrogel
3.2.2 淀粉水凝胶表观形貌分析
由图7可知,原淀粉颗粒表面致密光滑,呈现略有缺陷的椭球状。发生交联形成水凝胶后,其颗粒形状完全消失,水凝胶呈现相互贯穿的三维多孔结构[10]。

a-木薯淀粉(×3 000);b-水凝胶(×2 000)
图7 木薯淀粉(a)和水凝胶(b)SEM图
Fig.7 SEM images of cassava starch (a) and hydrogel (b)
3.2.3 淀粉水凝胶X射线衍射图谱分析
从图8 XRD图谱分析可知,原淀粉XRD衍射图约在15°、17°、18°、23°附近有衍射峰,这是多结晶区域,水凝胶的XRD衍射图在20°左右,结晶进一步减少,分子间氢键被破坏,说明木薯淀粉发生反应成水凝胶后改变了原有的结晶。淀粉分子链上具有很多羟基,亲水性很强,但是淀粉颗粒不溶于水,这是因为羟基之间通过氢键结合,颗粒中水分也参与氢键形成的缘故。淀粉颗粒内部有结晶和无定形区域,后者具有较高的渗透性,化学反应主要发生在这个区域,反应后的水凝胶主要为无定形,渗透性升高,溶胀性能良好[18]。
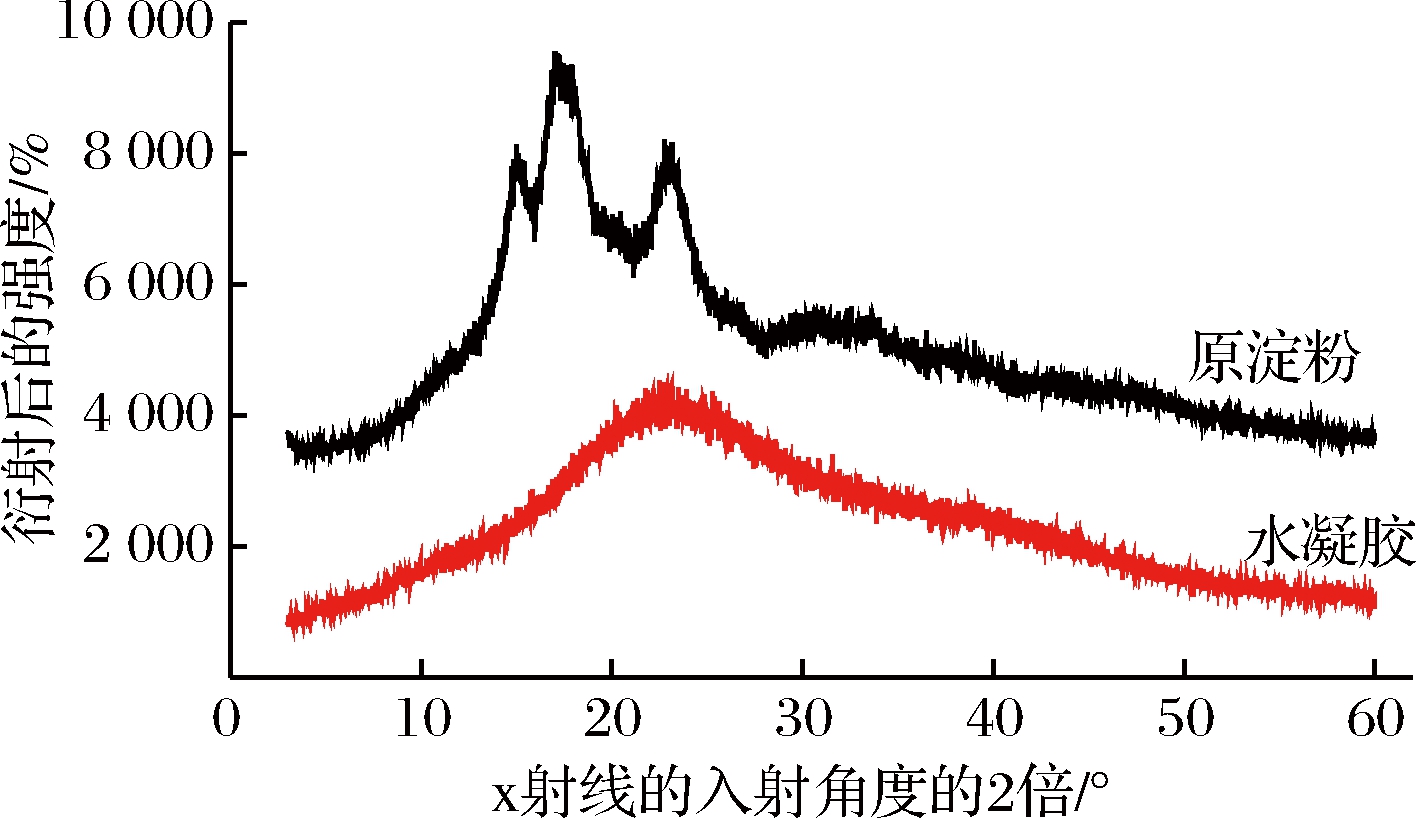
图8 木薯淀粉和水凝胶XRD图
Fig.8 XRD patterns of cassava starch and hydrogel
3.2.4 热失重分析
热重分析测试了物料耐高温性和分解温度。由图9可知,在35~165 ℃范围内,木薯淀粉及水凝胶的热失重约为4%~5%,较稳定,质量损失较少,这主要是样品中自由水分的蒸发。这一阶段水凝胶失水较少主要是由交联和较低结晶度所致,与实验结果相符。木薯淀粉在270~330 ℃范围内有显著的失重,主要是由于淀粉分解和微晶相转变所致[19]。与此同时,水凝胶在200~400 ℃范围内热损失较为明显,这是由于水凝胶中淀粉分子链的降解和交联结构解体所致。当温度达到800 ℃时,水凝胶和原淀粉的热失重残余分别为25%和21%。
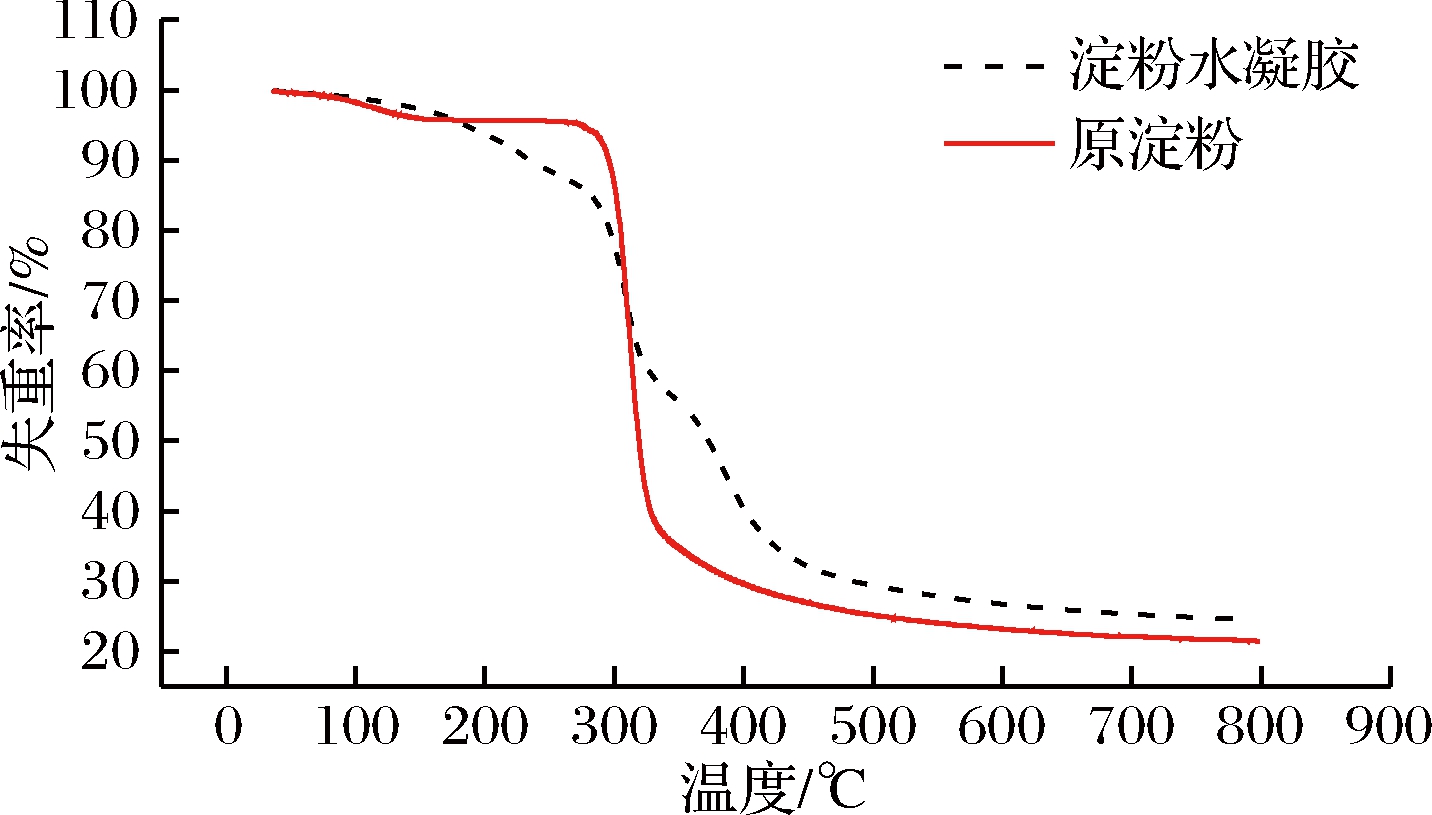
图9 木薯淀粉和水凝胶TG图
Fig.9 TG diagrams of cassava starch and hydrogel
3.3.1 水凝胶脱水率
由图10可知,水凝胶在室温下保水性能良好。在初始阶段,水凝胶的脱水率有明显的下降,是因为水凝胶表面的水分在空气中蒸发,致使脱水率降低。大约2 h以后,水凝胶表面水蒸发完全,脱水率接近平缓,说明水凝胶内部没有失水,保水性能良好。
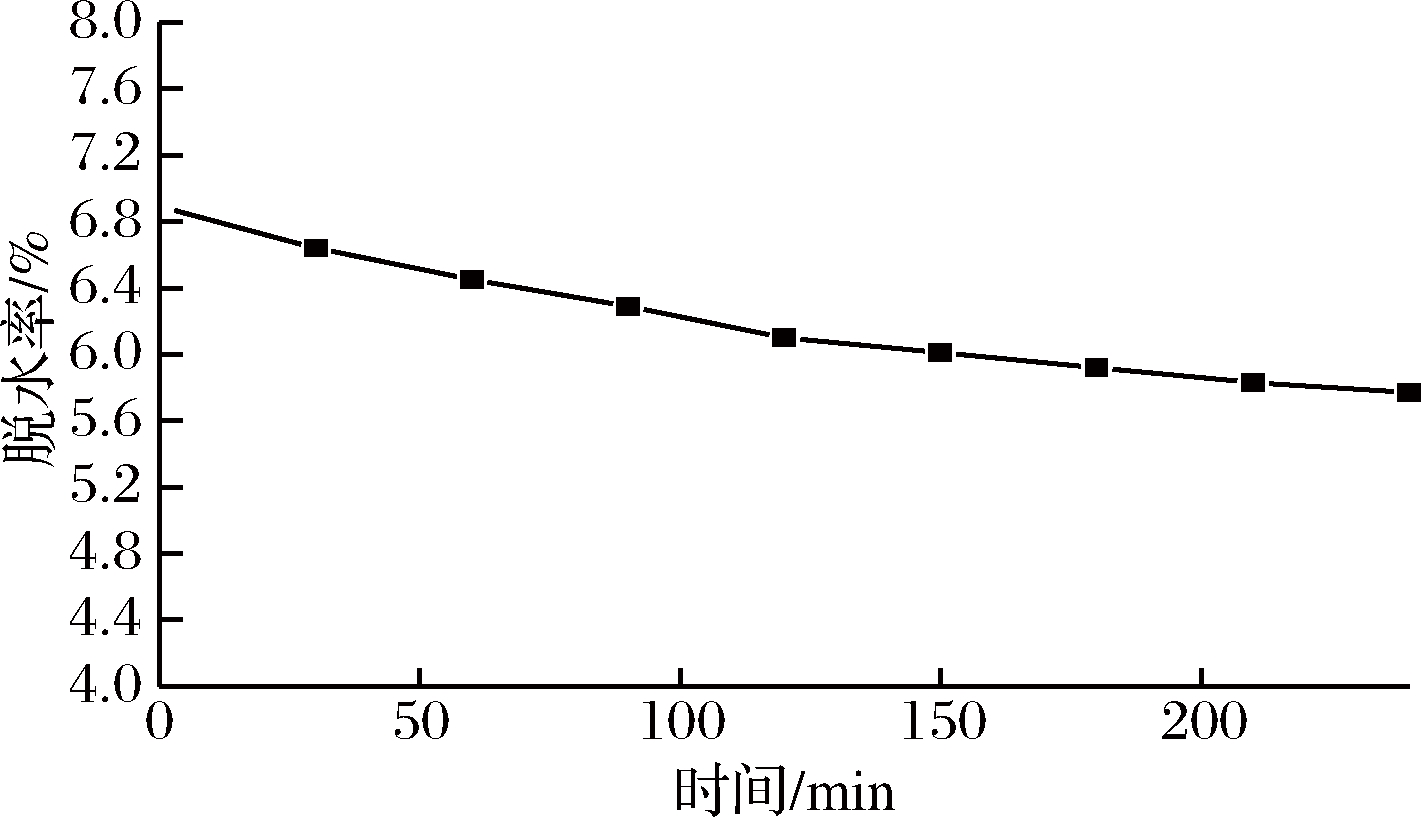
图10 水凝胶脱水率图
Fig.10 Hydrogel dehydration rate chart
3.3.2 水凝胶温敏性
温度对淀粉水凝胶溶胀平衡比的影响如图11所示。35 ℃为水凝胶的低临界转变温度。低于该温度时,亲水基团与水分子间形成的氢键占主导,水凝胶呈溶胀状态,利于吸水;温度高于该温度时,疏水基团间的相互作用力占主导,聚合物亲质子性作用增强,氢键作用减弱,水凝胶体积收缩,溶胀性能减弱[20-21]。
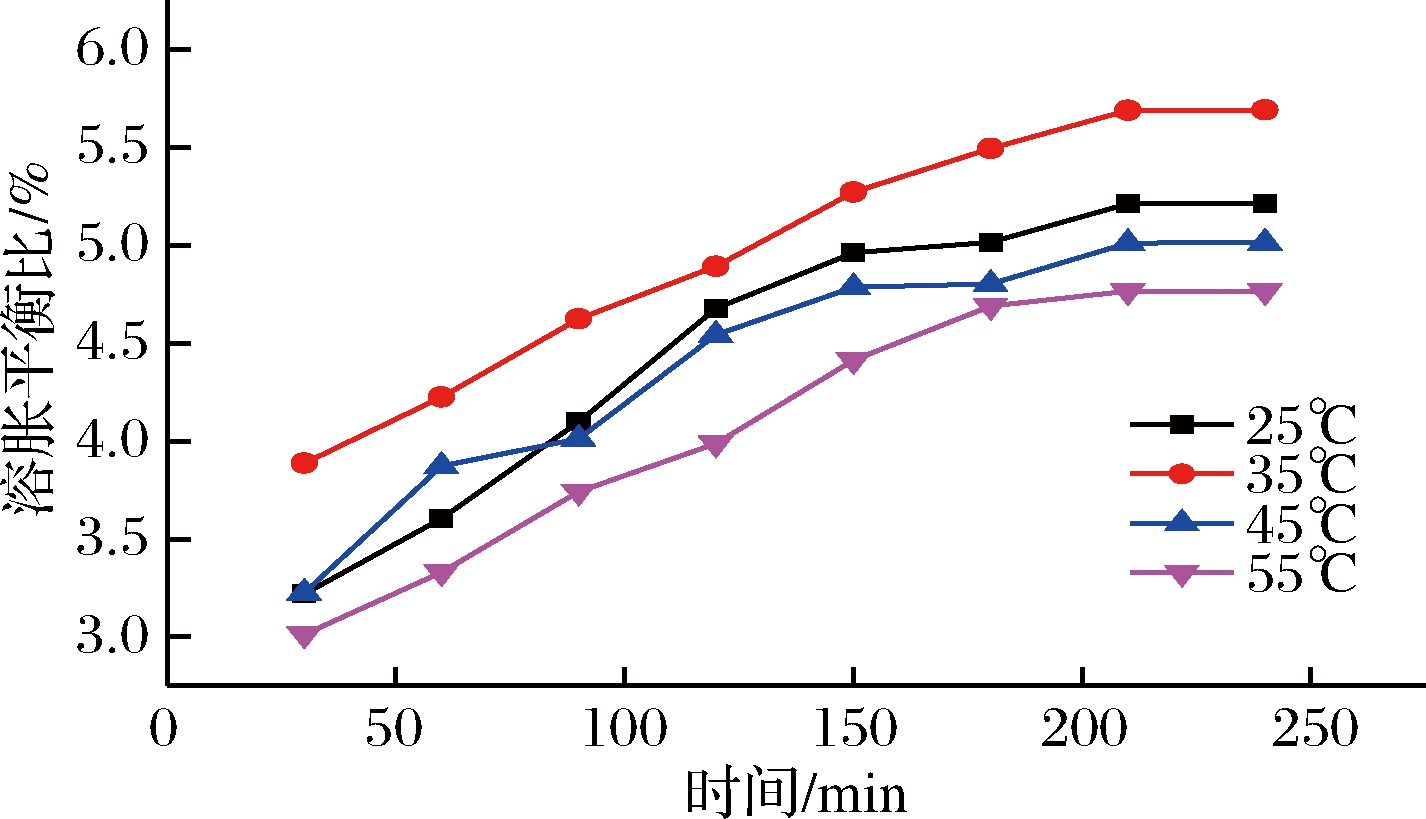
图11 温度对水凝胶溶胀平衡比影响
Fig.11 Effects of temperature on the swelling balance ratio of hydrogel
3.3.3 水凝胶溶胀-退溶性
从图12可以看出,完全溶胀后的水凝胶经历消溶胀。水凝胶的保水率迅速下降,随着时间延长,保水率下降速率变缓,到40 min后接近平缓,水凝胶不再退溶。温度迅速改变,偏离最低临界溶解温度,水分子与水凝胶链段之间氢键被破坏,分子间作用力减弱,链段运动能力变强,水凝胶中高分子链通过疏水作用互聚,水凝胶吸水率下降,一段时间后重新达到吸水-脱水平衡[22]。
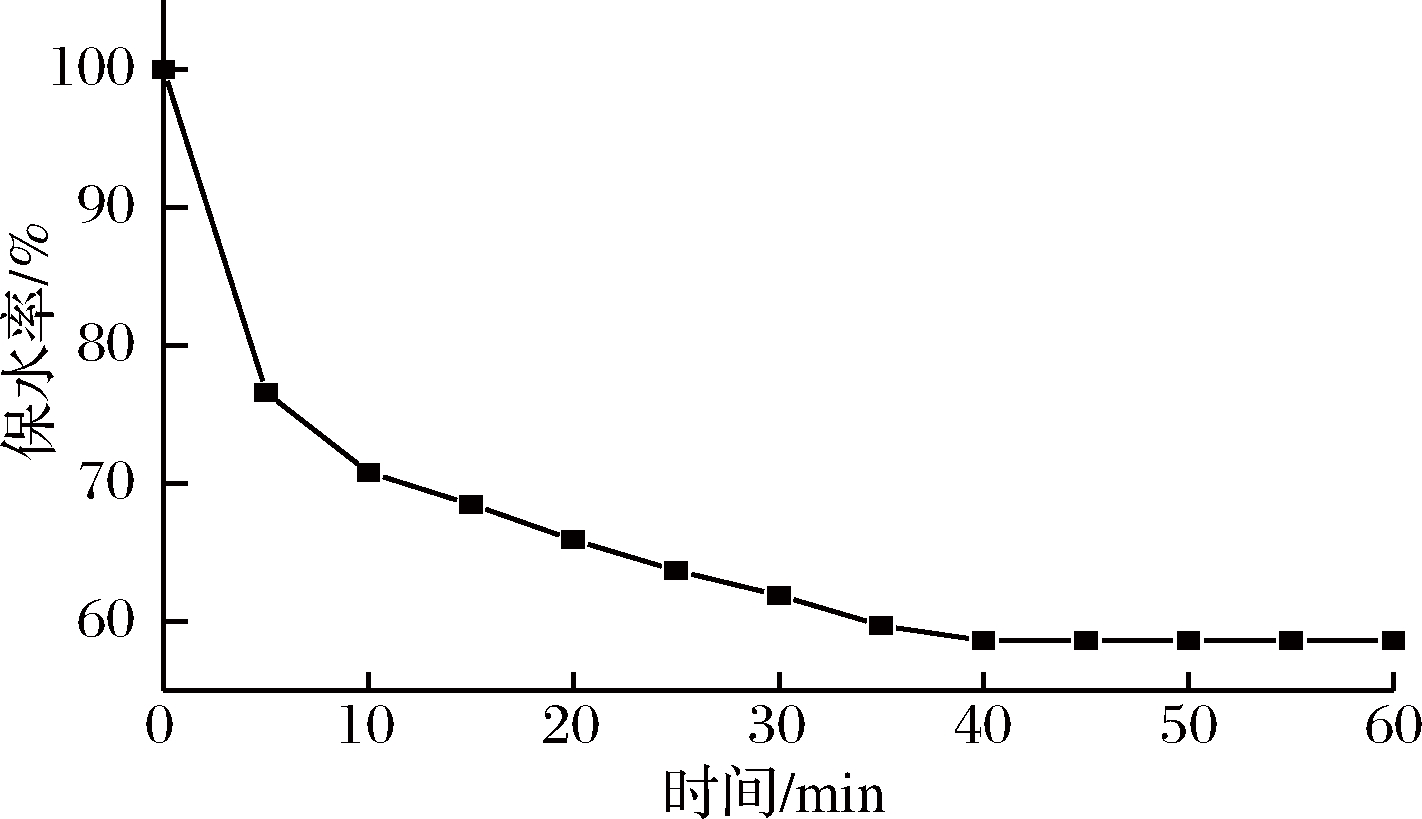
图12 水凝胶退溶平衡图
Fig.12 Hydrogel desolvation balance diagram
微波辐射制备水凝胶近来越来越得到广泛关注[12,23-25]。本实验用微波法制备水凝胶并对新生材料的结构进行表征,成功制备木薯淀粉基水凝胶。FTIR表明AM成功嫁接到淀粉骨架上;SEM显示水凝胶呈相互贯穿的三维多孔结构;XRD结果表明与原淀粉相比,淀粉水凝胶转化为无定形,相对结晶度明显降低。
对水凝胶性能进行研究,制备得到的水凝胶最高吸水倍率达600%,制备淀粉水凝胶的最佳条件为:木薯淀粉用量为2 g,AM 5 g,NMBA 0.06 g,KPS 0.03 g。水凝胶溶胀平衡比随着温度的改变而改变,在35 ℃时溶胀平衡比达到最大,而且水凝胶在室温条件下保水性良好。综合水凝胶溶胀比随着时间改变和溶胀-退溶曲线可以看出制备的水凝胶具有温度敏感性。该研究为淀粉水凝胶的制备应用提供依据,同时提高了木薯淀粉的附加值。
参考文献
[1] LIU C H, GAN X X, CHEN Y Q. A novel pH-sensitive hydrogels for potential colon-specific drug delivery: characterization and in vitro release studies[J]. Starch-Stärke, 2011, 63(8):503-511.
[2] 何领好,孙晓丽,宋锐,等.聚乙烯醇/壳聚糖凝胶的制备及性能研究[J].化工新型材料,2009,37(7):33-36.
[3] 黄怡,范晓东,张楠楠.聚乙烯醇固载β-环糊精线性高聚物的合成及其药物控制释放研究[J].高分子学报,2004(6):854-858.
[4] 赵志桩,王法,张晓阳,等.智能水凝胶研究进展[J].化学工程师,2014,28(1):33-36.
[5] 王薇,关国平,王璐.生物医用水凝胶研究进展[J].生物医学工程学进展,2015,36(4):221-225.
[6] 刘壮,谢锐,巨晓洁,等.环境刺激响应型高强度智能水凝胶研究进展[J].化工进展,2016,35(6):1 812-1 819.
[7] 王薇,关国平,王璐.生物医用水凝胶研究进展[J].生物医学工程学进展,2015,36(4):221-225.
[8] FAHANWI A N. Synthesis and characterization of superabsorbent chitosan-starch hydrogel and its application for removal of direct red 80 dye[J]. Eastern Mediterranean University (EMU), 2014,25(2):32-36.
[9] LIM W P, ASHRI A, MUNTAZ A B, et al. Preparation and characterization of starch/acrylamide-based hydrogel from Stemona curtissi tuber[J]. Malaysian Journal of Analytical Sciences, 2016,58(10): 157-170.
[10] 刘继伟,谷长生,宋文东,等.木薯淀粉基质水凝胶的制备及溶胀性能研究[J].安徽农业科学,2010,38(14):7 696-7 697;7 700.
[11] 谢松岩,周芳名,刘懿霆,等.温敏型水凝胶的制备及溶胀特性[J].当代化工,2015,44(4):702-705.
[12] NAMAZI H, DADKHAH A. Convenient method for preparation of hydrophobically modified starch nanocrystals with using fatty acids[J]. Carbohydrate Polymers, 2010, 79(3):731-737.
[13] 韦晓燕,谭军,欧阳玉霞,等.淀粉接枝丙烯酰胺吸附铜离子性能研究[J].工业水处理,2014,34(2):15-18.
[14] 刘子杰,梁兴唐,张海燕.壳聚糖接枝丙烯酸/丙烯酰胺水凝胶的微波快速合成及其响应性[J].化工新型材料,2015,43(5):202-205.
[15] 赵天勤,杜杰,张鹏,等.新型淀粉基pH值敏感水凝胶的微波法合成及性能表征[J].化工新型材料,2013,41(11):108-110;117.
[16] BAI C, ZHANG S F, HUANG L, et al. Starch-based hydrogel loading with carbendazim for controlled-release and water absorption.[J]. Carbohydrate Polymers, 2015, 125(9):376-383.
[17] 金海琴,张玉红,董勤政,等.壳聚糖接枝丙烯酸/丙烯酰胺水凝胶的制备及性能[J].高分子材料科学与工程,2009,25(11):129-132.
[18] 蓝平,何日梅,封余贤,等.木薯淀粉磁性微球的结构表征及其对溶菌酶的吸附性能[J].化工进展,2016,35(1):189-196.
[19] VAKILI M R, RAHNESHIN N. Synthesis and characterization of novel stimuli-responsive hydrogels based on starch and L-aspartic acid[J]. Carbohydrate Polymers, 2013, 98(2):1 624-1 630.
[20] DU J, ZHAO T Q, LIU Y, et al. Synthesis and characterization of a novel starch-based pH-sensitive hydrogel[J]. Applied Mechanics & Materials, 2013,30(6):2 602-2 605.
[21] ZHANG Y, GAO P Q, ZHAO L, et al. Preparation and swelling properties of a starch-g-poly(acrylic acid)/organo-mordenite hydrogel composite[J]. Frontiers of Chemical Science and Engineering, 2016, 10(1):147-161.
[22] 成瑾瑾. 温度敏感性水凝胶的制备及其在铜离子吸附中的应用[D].杭州:浙江大学,2017.
[23] PANDEY M, AMIN M C I M. Accelerated preparation of novel bacterial cellulose/acrylamide-based hydrogel by microwave irradiation[J]. International Journal of Polymeric Materials & Polymeric Biomaterials, 2013, 62(7):402-405.
[24] 谭德新,王艳丽,陈德磊,等. 高吸水树脂PAMPS的超声制备与性能研究[J]. 化工新型材料,2013,41(12):46-49.
[25] 董庆珍,熊国宣.超声法合成氨基酸型螯合树脂及其对铀的吸附[J]. 化工新型材料,2011,39(10):65-73.
GAO Fengyuan1,2,3, WEI Donglai1,2,3, WEI Dongping1,2,3,WANG Bing1,2,3,WU Lugui1,2,3, LAN Ping1,2,3*, LIAO Anping1,2,3
1 (College of Chemistry and Chemical Engineering, Guangxi University for Nationalities, Nanning 530006, China) 2 (Guangxi Key Laboratory of Polysaccharide Materials and Modification (Guangxi University for Nationalities), Nanning 530006, China) 3 (Guangxi Key Laboratory of Chemistry and Biotransformation Process (Guangxi University for Nationalities),Nanning 530006, China)
Abstract Tapioca starch was used as raw material, acrylamide as a monomer, N,N-methylenebisacrylamide as a cross-linking agent, potassium persulfate as an initiator, tapioca starch-based hydrogels were prepared by microwave irradiation technology. The effects of monomer, crosslinker, and initiator dosage on swelling properties of hydrogels were investigated. The results showed that when the ratio of starch to acrylamide was 1∶3, 0.02 g N,N-methylenebisacrylamide and 0.05 g potassium persulfate were used, the water absorption ratios of tapioca starch hydrogels prepared by microwaving at 400 W for 60 s reached the highest. FT-IR, field emission scanning electron microscope (FESEM), and other analytical methods were used for characterization. The results showed that the tapioca starch-based hydrogels were successfully prepared. The swelling balance ratios of hydrogels reached maximum at 35 ℃. Moreover, hydrogels had good water holding capacities at room temperature. This study provides certain experimental bases for preparing and applying starch hydrogel, which increases the added values of tapioca starch.
Key words tapioca starch; hydrogel; temperature sensitivity; swelling property