屎肠球菌Enterococcus faecium R2的分离鉴定及其在酸浆豆干加工中的应用
陈志娜*,叶韬,丁曼,尹琳琳,黄琳,夏悦,裴纪柳
(淮南师范学院 生物工程学院,安徽 淮南,232038)
摘 要为了获得黄浆水发酵优势菌种,通过平板涂布法和发酵培养法,以pH值和生物量为指标,从泡菜中分离筛选出1株可以高效利用黄浆水发酵产酸的菌株R2,对其进行菌株形态观察、生理生化鉴定及分子生物学鉴定,确定菌株R2属于屎肠球菌。对屎肠球菌R2的安全性及其发酵酸浆的品质特性进行分析,结果表明,屎肠球菌R2对几种常见抗生素敏感,具有一定的安全性;屎肠球菌R2纯种发酵制得的酸浆豆干与自然发酵酸浆豆干相比感官特性无显著差异,说明屎肠球菌R2可以作为一种新型酸浆纯种发酵剂进行开发利用。该研究可为黄浆水的高效开发利用及酸浆豆干(腐)的规范化生产提供理论依据。
关键词屎肠球菌;黄浆水;酸浆豆干
黄浆水是豆腐加工过程中产生的副产物,在豆腐加工过程中需加入10倍左右的水来将大豆研磨成浆,其中约有1/2~1/3的水在后续的加工过程中被沥出[1]。黄浆水中含有大豆异黄酮、蛋白质和VP、VK等营养物质,以及大量水溶性的糖类如水苏糖、棉籽糖等低聚糖,非常适宜微生物的生长[2],生产过程中直接排放不仅造成资源的浪费,而且会对周围的环境造成严重的污染。我国民间有利用黄浆水在自然条件下发酵产酸获得酸浆凝固剂,制得酸浆豆腐[3]。与石膏、卤水作为凝固剂的豆腐相比,酸浆豆腐具有质地细腻、保水性好、口感鲜嫩等特点,深受人们的喜爱。但是自然发酵条件下制备的酸浆,微生物菌群复杂,除了产酸的乳酸菌外,还可能污染致病菌和杂菌[4],造成酸浆质量不稳定,并对豆腐的安全性构成危害。而一些商用乳酸菌如干酪乳杆菌、嗜酸乳杆菌、植物乳杆菌在发酵利用黄浆水时需要前期补充蔗糖、葡萄糖等营养素或者在发酵结束后补充醋酸才能达到合适的酸度[5-6],增加了生产成本。因此,筛选出可以高效利用黄浆水的优质菌种对于黄浆水的开发利用及酸浆豆腐的规范化生产具有重要意义。
本研究采用平板涂布法从泡菜中分离乳酸菌,再将其转接至黄浆水培养基以pH值及生物量为指标筛选产酸能力最强的菌株,对其进行生理生化及分子生物鉴定,并用该菌种对黄浆水进行纯种发酵制备酸浆豆干,以发酵特性和感官评定为指标对其品质进行评价。
1 材料与方法
1.1 材料与试剂
食品级黄豆:淮南市苏果超市;细菌基因组DNA快速抽提试剂盒:生工生物工程(上海)股份有限公司;16S rDNA细菌鉴定PCR试剂盒:大连宝生物有限公司。
MRS培养基:蛋白胨10 g,酵母浸粉5 g,K2HPO4 2 g,柠檬酸二铵2 g,葡萄糖 20 g,牛肉膏10 g,无水乙酸钠5 g,MgSO40.2 g,MnSO40.05 g,琼脂粉 20 g,CaCO3 20 g,吐温-80 1 mL。
黄浆水培养基:黄浆水121 ℃灭菌15 min,冷却备用。
1.2 仪器与设备
ABI型PCR仪,美国ABI公司;pHS-3C pH计,上海仪电科学仪器股份有限公司;TA-XTPLUS物性测试仪,英国STABLE公司;DYY-6C型电泳仪,北京市六一仪器厂;GEL DOC XR凝胶成像系统,美国Bio-rad;SW-CJ-2D型超净工作台,苏州净化设备有限公司;LRH-250-A生化培养箱,广东泰宏君科学仪器股份有限公司;5804R型离心机,Eppendorf公司。
1.3 试验方法
1.3.1 乳酸菌的分离纯化
取泡菜样品10 g,置于90 mL无菌生理盐水中,均匀混合后用无菌生理盐水进行梯度稀释至10-3、10-4、10-5,取各稀释度样品200 μL均匀涂布于MRS分离培养基上,37 ℃静置培养48 h。挑取溶钙圈较大、培养基变黄的菌落,用平板划线法在MRS固体培养基上划线分离,如此重复直至分离纯化得到形态一致的、纯的单菌落,进行革兰氏染色和接触酶实验,淘汰非目标菌,目标菌采用25%的甘油保存待用。
1.3.2 乳酸菌的筛选
将纯化后的目标菌株分别转接到灭菌后的黄浆水培养基中,于37 ℃下静置培养72 h,以乳酸菌生物量和发酵液pH值为指标评价乳酸菌的发酵性能,筛选出1株生物量最高、pH值最低的乳酸菌菌株R2。
1.3.3 菌株鉴定
(1) 生理生化实验:参照《伯杰细菌鉴定手册》对菌株R2进行耐酸性试验、耐盐性试验和糖发酵试验等生理生化试验[7]。
(2)分子生物学鉴定:将菌株R2接种到MRS培养基中,37 ℃下静置培养16 h,离心收集沉淀,按照细菌基因组DNA快速抽提试剂盒方法提取菌株R2总DNA。将提取的DNA模板进行PCR扩增,采用正向引物:27F:5’-AGAGTTTGATCCTGGCTCAG-3’,反向引物1 492R:5’-ACGGCTACCTTGTTACGACTT-3’。PCR反应体系(25 μL):模板DNA 1 μL,正、反向引物 1 μL, Mix 12.5 μL,超纯水补足至25 μL。PCR反应条件为:预变性94 ℃ 5 min;变性 94 ℃ 30 s,退火55 ℃ 30 s; 延伸72 ℃ 1.5 min,共30个循环,最后72 ℃延伸5 min。 PCR产物经琼脂糖凝胶电泳检验后送通用生物系统(安徽)有限公司进行测序。所得序列通过BLAST(http://www.ncbi.nlm.nih.gov/blast)进行序列相关性分析,提交到GenBank获得序列号,采用MEGA 4.0软件、以Neighbor-joining法构建系统发育树。
1.3.4 药敏性测定
选用四环素、万古霉素、青霉素、链霉素4种药物对屎肠球菌E.faecium R2作药敏试验。采用Kirby-Bauer扩散法,将1.0 mL菌悬液(106~107CFU/mL)与15 mL含1.5%琼脂的MRS培养基混合后倾倒平板,待平板凝固后按照说明书要求贴放药敏纸片,于37 ℃恒温培养18~24 h后测量抑菌圈直径,参照美国临床和实验室标准协会(Clinical and Laboratory Standards Institute,CLSI)执行标准进行药敏性判断[7]。
1.3.5 纯种发酵酸浆的制作
以传统工艺制作的卤片黄浆水作为初级黄浆水,初级黄浆水接种屎肠球菌发酵剂(接种量3%)发酵36 h制得一代酸浆。以一代酸浆做为凝固剂制得二级豆腐黄浆水,再接种屎肠球菌发酵剂(接种量3%)发酵36 h制得二代酸浆。以二代酸浆做凝固剂制得三级豆腐黄浆水,实验以三级豆腐黄浆水为发酵基质制备酸浆与酸浆豆干,取消原卤盐凝固剂的影响[8]。
1.3.6 酸浆豆干的制作
取700 g食品级黄豆用蒸馏水于25 ℃下浸泡8 h, 豆水比1∶8(g∶mL)打浆,采用100目尼龙筛布过滤除渣,生豆浆煮沸并维持5 min,当降温至85 ℃时,轻轻搅动下徐徐加入酸浆,直至出现均匀脑花,添加量为16%(质量分数)左右。85 ℃下蹲脑20 min后,将豆花倒入豆腐模具中于5.5~6.0 kPa下压浆30 min成型,收集黄浆水,所得豆干切成小块[9]。
1.3.7 pH值测定
采用pH计测定纯种发酵和自然发酵过程中酸浆pH的变化规律。
1.3.8 微生物检验
参照GB/T 4789.35—2016和GB/T4789.3—2010方法测定纯种发酵酸浆和自然发酵酸浆中的乳酸菌含量和大肠菌群MPN。
1.3.9 感官评定
参照张影等[8]的方法及GB/T 22106—2008中 6.1的感官要求,略有修改。选取食品专业的10名同学组成感官评定小组,由小组讨论确定描述性感官指标术语和评分标准,然后将酸浆豆干样品按3位数编号后随机发放给评审员,参照表1对样品的感官属性进行打分(0~10分)。
表1 酸浆豆干感官评定标准
Table 1 Sensory attributes of acid slurry dried bean curds and their definitions

指标评分标准评分/分淡黄8~10色泽偏黄5~7暗黄0~4组织结构完整、质地细腻,弹性好,耐咀嚼,不易碎、表面不黏8~10质地组织结构较完整,质地较细腻,弹性较好,较耐咀嚼,不易碎、表面不黏5~7组织结构不完整,质地粗糙,弹性差,不耐咀嚼,易碎、表面有粘性0~4有豆香味,无豆腥味及其他异味8~10气味有豆香味,少许豆腥味及酸味5~7有较多豆腥味、酸味及其他异味0~4
续表1

指标评分标准评分/分口感细腻爽滑、弹性好、无酸味、不黏牙8~10口感口感较爽滑、弹性一般、少许酸味5~7粗糙或成浆糊状、无弹性、有异味0~4断面整齐、表面光滑8~10断面结构断面较整齐、表面较光滑5~7断面不整齐、表面粗糙0~4
1.4 数据统计与处理
结果以平均值±标准差表示,使用SPSS 18.0软件对结果进行统计分析(One-way ANOVA),用OriginPro 8.0 和Excel 2007软件绘图。
2 结果与分析
2.1 乳酸菌的分离筛选
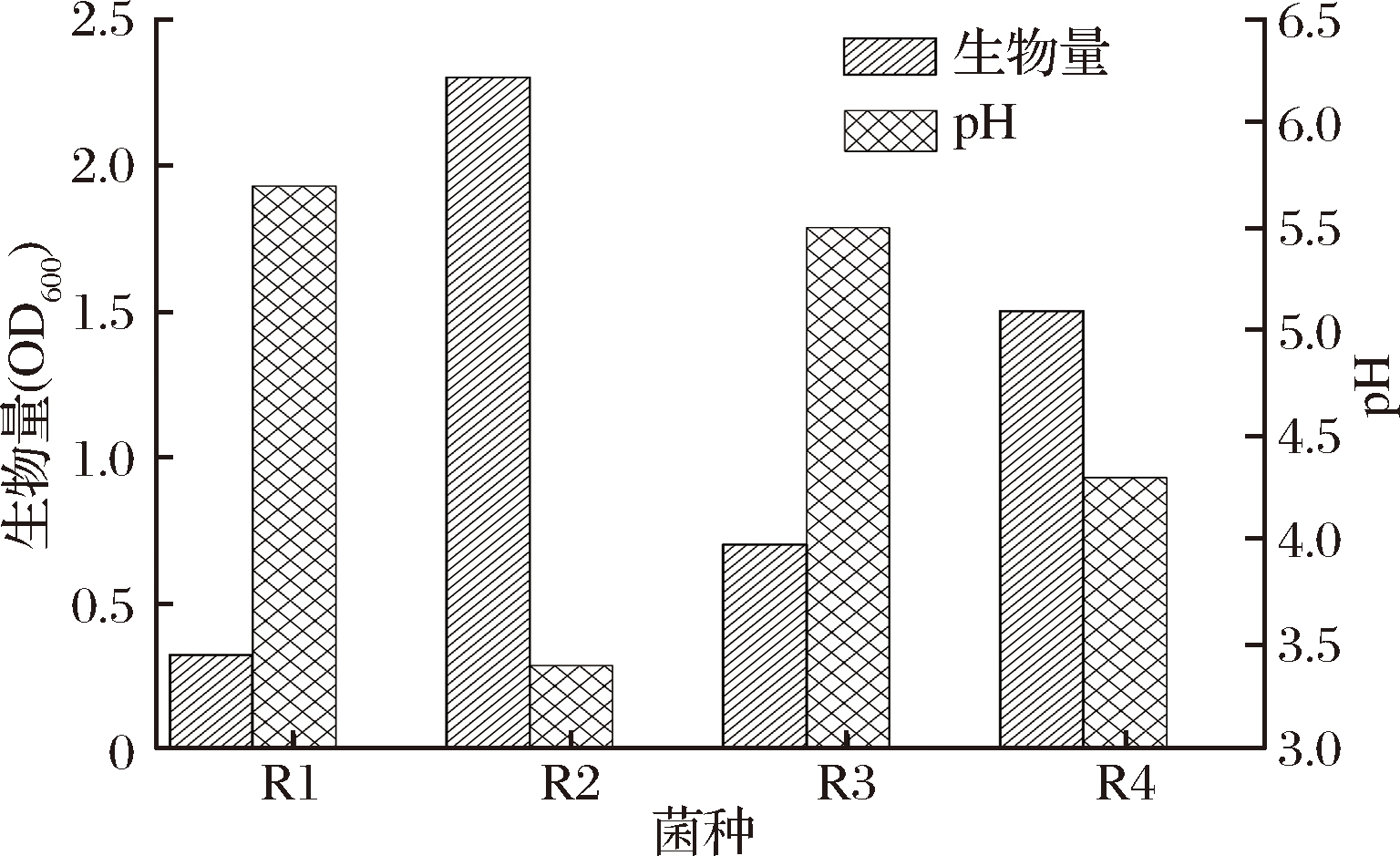
从泡菜样品中分离到4株溶钙圈较大的菌落,对其进行纯培养,革兰氏染色后显微镜观察菌体形态,确定为单菌落后将其分别转接至黄浆水培养基中,培养36 h后,测定生物量及发酵液pH值,结果如图1所示。
由图1可以看出,所选4株菌株对黄浆水的发酵性能的影响差别很大,其中菌株R2的发酵性能最强,在发酵36 h后,黄浆水的pH值下降到3.5左右,同时其菌体量OD600也达到2.0以上。一般当酸浆的pH值达到3.8~4.0时即可作为豆腐凝固剂[5],因此,菌株R2可以在无需补充蔗糖葡萄糖等营养素的前提下,直接利用黄浆水中的低聚糖发酵产酸,且在发酵结束后无需补充醋酸即可达到适宜的酸度。
2.2 菌株R2的鉴定
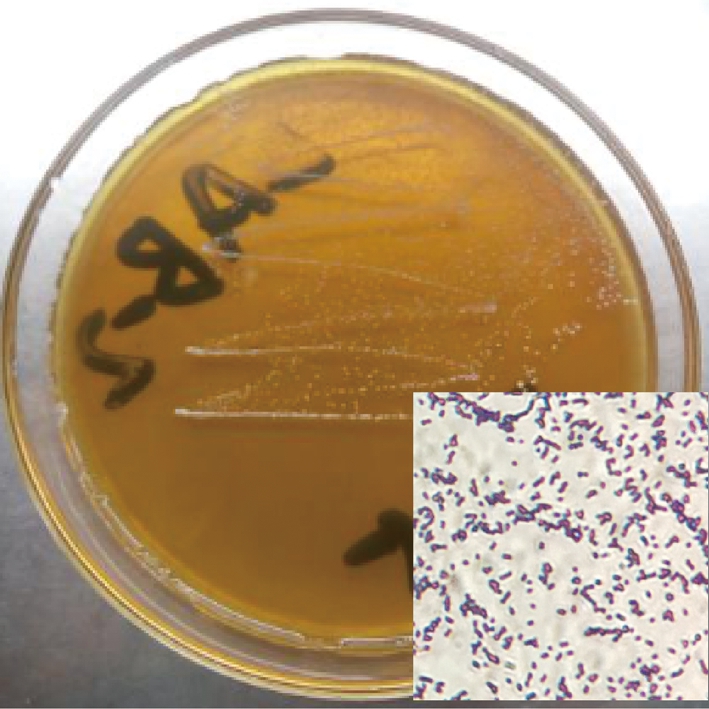
菌株R2菌落成圆形,乳白色、不透明、表面光滑湿润、凸起、边缘整齐、直径1 mm左右圆形菌落;油镜下观察其菌体呈椭圆形或圆形、无芽孢、成对成链或聚团排列(图2)。
菌株R2的生理生化鉴定结果详见表2。由表2可知,菌株R2可在pH 11.0、6.5%(质量分数)NaCl和40%(质量分数)胆汁环境中生长,不能分解可溶性淀粉、山梨醇,可以分解乳糖、半乳糖、蔗糖、麦芽糖、葡萄糖等,根据《伯杰细菌鉴定手册》和《乳酸菌的分类鉴定》,菌株R2的情况基本符合屎肠球菌的生理生化特征。
表2 屎肠球菌R2生理生化特征
Table 2 Physiologial and biochemical characterization of strain R2

项目结果项目结果乳糖+纤维二糖+麦芽糖+40%胆汁+果糖+6.5%NaCl+葡萄糖+触酶-山梨醇-pH 11.0生长+可溶性淀粉-
注:“+”实验结果为阳性;“-”试验结果为阴性。
进一步经PCR扩增和序列测定,获得菌株R2的16S rDNA序列片段,GenBank登录号为MG456825。进一步经过BLAST在线比对,与E.faecium(KY490552)的相似性达到99%,并利用MEGA 4.0软件与相近种构建系统发育树,如图3所示,确定菌种为屎肠球菌,命名为E.faecium R2。该菌种现保藏于中国微生物菌种保藏管理委员会普通微生物中心,保藏编号为CGMCC No.14944。
2.3 屎肠球菌R2对常见抗生素的敏感性
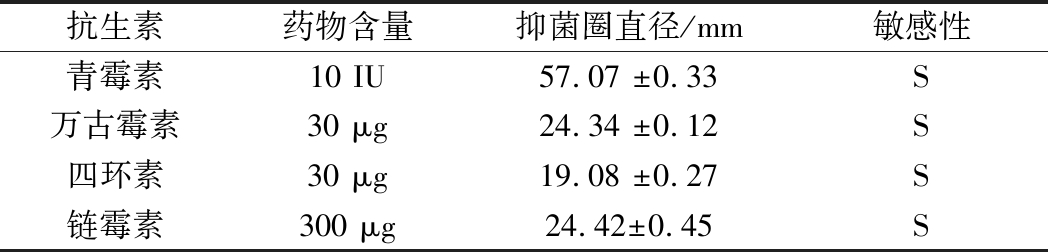
屎肠球菌属于乳酸菌的一种,是肠道内的正常菌群,广泛存在于传统乳制品[10]、泡菜[11]、豆酱[12]等发酵食品中,具有耐酸、耐热、肠道黏附能力强等特点,以及抑制病原菌、增强免疫力等作用[13-14]。但是近年来随着抗生素的广泛使用,屎肠球菌不断出现耐药性的现象,特别是对万古霉素的耐药性为临床治疗带来了很大的困难[15]。因此,对拟用于食品加工菌株的耐药性进行分析是十分必要的。由表3可看出,屎肠球菌R2对青霉素、万古霉素等4种常见的抗生素敏感,具有潜在的安全性。
表3 屎肠球菌R2药敏性图谱
Table 3 Antibiatic resistant profile ofE.faecium R2
抗生素药物含量抑菌圈直径/mm敏感性青霉素10 IU57.07 ±0.33S万古霉素30 μg24.34 ±0.12S四环素30 μg19.08 ±0.27S链霉素300 μg24.42±0.45S
注:药敏性判断结果参照美国临床和实验室标准协会(CLSI)执行标准;S:敏感;I:中介;R:耐药。
2.4 纯种发酵酸浆与自然发酵酸浆的pH变化规律
纯种发酵和自然发酵酸浆的pH变化规律如图4所示,由图4可以看出E.faecium R2纯种发酵酸浆的pH变化趋势与自然发酵酸浆的pH变化趋势基本一致,发酵速度稍有滞后,发酵前24 h阶段pH的下降速度较快,随后速度变慢。发酵30 h后两者的pH值达到4.0以下,随后进一步降到3.6以下并保持稳定。这一结果与赵贵丽等[16]的研究结果一致,其研究发现当发酵时间达到24 h后,pH下降变缓,在48 h后达到最低值3.6左右。
2.5 微生物检测
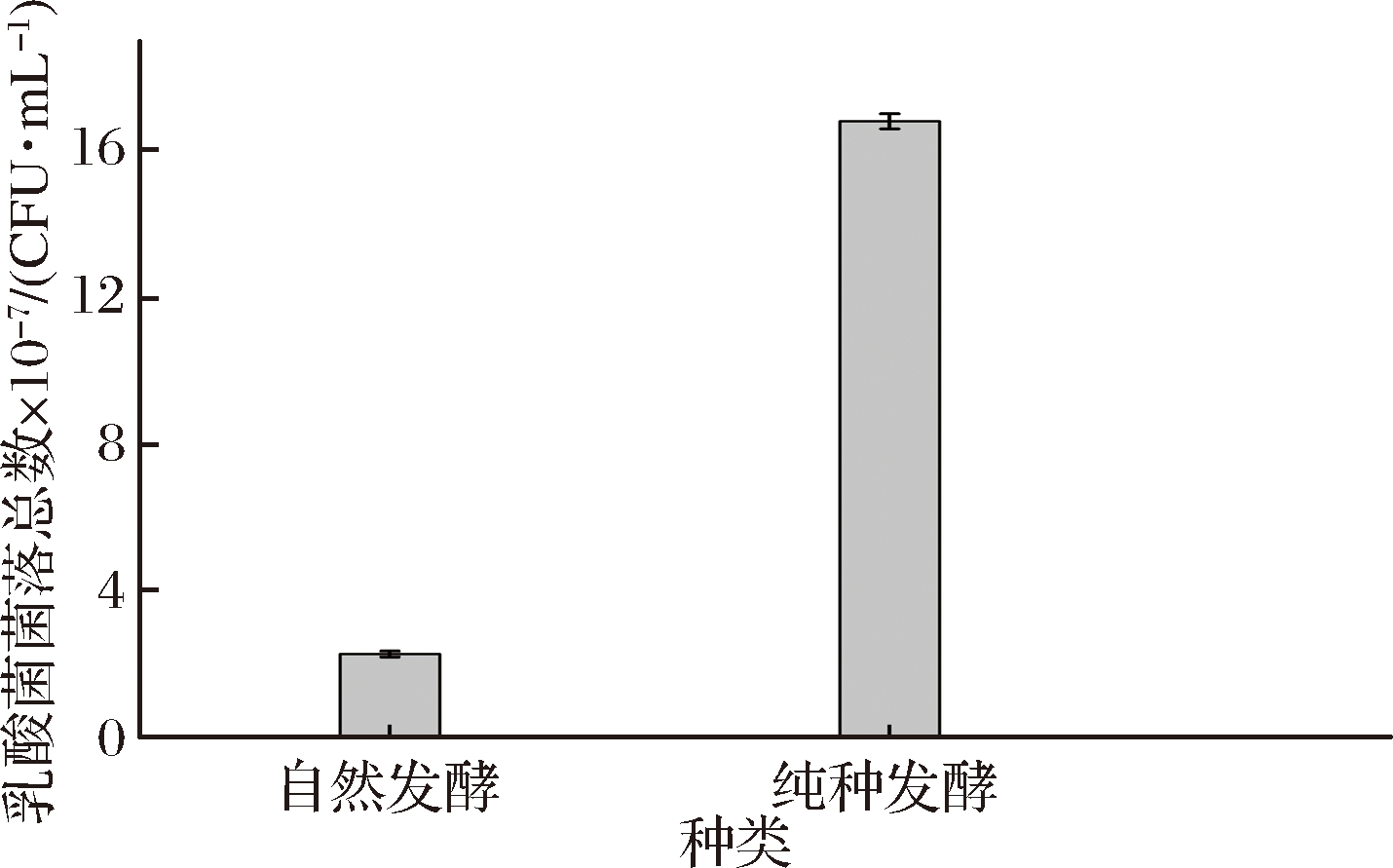
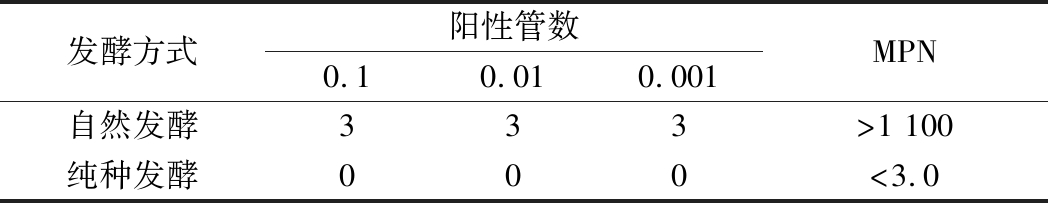
纯种发酵和自然发酵酸浆的乳酸菌菌落总数见图5,大肠菌群MPN见表4。由图5和表4可以看出纯种发酵酸浆中的乳酸菌含量明显高于自然发酵酸浆中的乳酸菌含量,同时纯种发酵酸浆中未检出大肠菌群。
杜欣等[17]研究发现在黄浆水中添加5%蔗糖后,不仅可以增强乳酸菌发酵黄浆水的能力,同时还提高了其抑菌效果。很多研究已经表明屎肠球菌具有良好的抑菌效果[18-20],其主要的抑菌活性物质除细菌素外还有乳酸等有机酸[21]。因此,采用E.faecium R2纯种发酵制备酸浆可以有效地抑制杂菌污染,提高酸浆的安全性。
表4 自然发酵和纯种发酵酸浆中大肠菌群MPN
Table 4 MPN value of the coliform bacteria ofE.faecium R2 fermental acid pulp and natural fermental acid pulp
发酵方式阳性管数0.10.010.001MPN自然发酵333>1 100纯种发酵000<3.0
2.6 感官评定
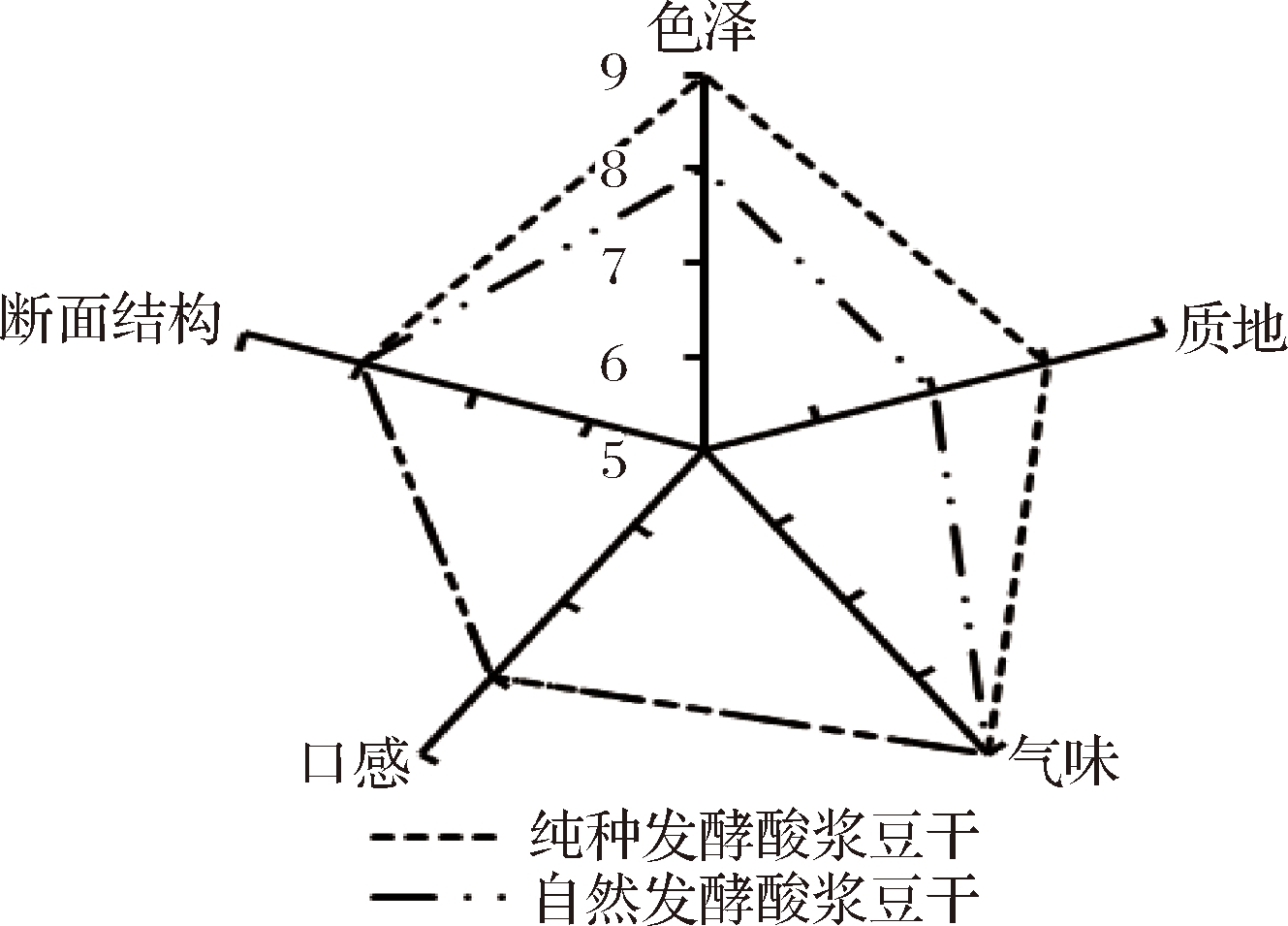
图6为纯种发酵酸浆豆干与自然发酵酸浆豆干感官特性玫瑰图。
由图6可知,纯种发酵酸浆豆干与自然发酵酸浆豆干的感官特性没有显著区别,2种酸浆制出的豆干色泽均呈现淡黄色,组织结构完整,质地细腻,弹性好,耐咀嚼,不易碎,表面不黏,断面较整齐表面光滑,无豆腥味无明显酸味。说明E.faecium R2纯种发酵酸浆豆干具有传统自然发酵酸浆豆干的色香味等感官品质。
3 结论
从泡菜中优选出1株可以直接利用黄浆水中的低聚糖发酵产酸的菌株R2,通过菌落形态、生理生化试验及分子生物学鉴定确定菌株R2为屎肠球菌,命名为E.faecium R2。该菌株可在无碳源添加前提下,发酵36 h后可使酸浆pH值达到3.6以下。E.faecium R2纯种发酵酸浆的乳酸菌数明显高于自然发酵酸浆,且无大肠杆菌检出,安全性更高。另外,E.faecium R2纯种发酵酸浆豆干的感官特性与自然发酵酸浆豆干无明显差异。
与现已报道的纯种发酵黄浆水产酸浆的乳酸菌相比,E.faecium R2培养条件更简单,产酸速度较快。利用该菌株进行酸浆豆腐及豆干等的生产,可以有效地生产乳酸菌等益生菌,减少污染致病菌及杂菌含量,保证酸浆的质量及稳定性,进而提高豆制品的安全性。在E.faecium R2发酵的过程中,无需补充蔗糖、葡萄糖等碳源,且在发酵结束后无需补充醋酸即可达到适宜的酸度,有效地降低了生产成本。因此,E.faecium R2作为一种酸浆纯种发酵剂会有较为广泛的应用前景。
参考文献
[1] 王爱伟,孙冰洁,刘玉,等. 酸浆豆腐废水中发酵假丝酵母的研究[J]. 中国酿造, 2009, 28(10): 44-46.
[2] FUNG W Y, LIONG M T. Evaluation of proteolytic and ACE-inhibitory activity ofLactobacillus acidophilus in soy whey growth medium via response surface methodology[J]. LWT - Food Science and Technology, 2010, 43(3): 563-567.
[3] 周婷婷, 易敏英,相大鹏,等. 白腐乳及其生产过程中蜡样芽孢杆菌的污染及防治[J]. 中国酿造, 2014, 33(5): 77-80.
[4] 刘力, 李理. 酸浆水中3种菌株的产酸能力及抗氧化活性[J]. 食品与机械, 2015(2): 11-15.
[5] 夏秀东,周剑忠,单成俊,等. 乳酸菌发酵黄浆水制备酸浆豆腐的工艺:中国, 201610211180.7 [P]. 2016-04-06.
[6] 张莉力, 许云贺,叶青,等. 一株乳酸菌及其在酸浆豆腐生产中的应用:中国, 201610811912.6 [P]. 2016-09-09.
[7] 郑伟. 屎肠球菌KQ2.6抑菌活性及其安全性研究[D]. 杭州:杭州师范大学, 2016.
[8] 张影, 刘志明,刘卫,等. 酸浆豆腐的工艺研究[J]. 农产品加工(学刊), 2014(4): 21-23.
[9] 叶青, 许云贺,张莉力. 豆腐酸浆中干酪乳杆菌的分离、鉴定及作为豆腐凝固剂的应用[J]. 食品工业科技, 2017, 38(18): 94-98.
[10] 夏玉, 郑华,林捷,等. 屎肠球菌发酵特性及其功能性研究[J]. 食品工业科技, 2014, 35(12): 123-126.
[11] 卢海强, 霍文敏,黄蕾,等. 一株具有潜在益生特性屎肠球菌的筛选及在酸菜中的应用[J]. 食品科技, 2017(7): 2-7.
[12] 王晓蕊, 邹婷婷,郭志富,等. 豆酱中产细菌素屎肠球菌的筛选及特性分析[J]. 食品与发酵工业, 2016, 42(4): 91-97.
[13] BANWO K, SANNI A, TAN H. Technological properties and probiotic potential ofEnterococcus faecium strains isolated from cow milk[J]. Journal of Applied Microbiology, 2013, 114(1): 229-241.
[14] SUN P, WANG J, JIANG Y. Effects ofEnterococcus faecium (SF68) on immune function in mice[J]. Food Chemistry, 2010, 123(1): 63-68.
[15] 王雪芹, 林海君,鞠世影,等. 两株粪肠球菌的安全性评价[J]. 食品工业科技, 2014, 35(8): 166-169.
[16] 赵贵丽, 罗爱平,廖娅凡,等. 酸浆最适自然发酵条件优化[J]. 食品科学, 2013, 34(17): 201-204.
[17] 杜欣, 李理,刘冬梅. 碳源对益生菌发酵黄浆水抗氧化和抑菌活性的影响[J]. 现代食品科技, 2014(2): 129-133.
[18] AHMADOVA A, TODOROV S D, CHOISET Y, et al. Evaluation of antimicrobial activity, probiotic properties and safety of wild strainEnterococcus faecium, AQ71 isolated from Azerbaijani Motal cheese[J]. Food Control, 2013, 30(2): 631-641.
[19] HADJI-SFAXI I, EL-GHAISH S, AHMADOVA A, et al. Antimicrobial activity and safety of use ofEnterococcus faecium PC4.1 isolated from Mongol yogurt[J]. Food Control, 2011, 22(12): 2 020-2 027.
[20] KIVANÇ S A, KIVANÇ M, T. Antibiotic susceptibility, antibacterial activity and characterisation ofEnterococcus faeciumstrains isolated from breast milk[J]. Experimental & Therapeutic Medicine, 2016, 12(3): 1 732-1 740.
T. Antibiotic susceptibility, antibacterial activity and characterisation ofEnterococcus faeciumstrains isolated from breast milk[J]. Experimental & Therapeutic Medicine, 2016, 12(3): 1 732-1 740.
[21] ZHENG W, ZHANG Y, LU H M, et al. Antimicrobial activity and safety evaluation ofEnterococcus faecium KQ 2.6 isolated from peacock feces[J]. Bmc Biotechnology, 2015, 15(1):30.
Isolation and identification of Enterococcus faecium R2 and its application in sour slurry dried bean curd processing
CHEN Zhina*, YE Tao, DING Man, YIN Linlin, HUANG Lin, XIA Yue, PEI Jiliu
(College of Biological Engineering, Huainan Normal University, Huainan 232038, China)
Abstract To select the predominant strains for bean curd water fermentation, a strain R2 that could efficiently ferment bean curd yellow water to produce acids was screened out from pickles using pH and biomass as indexes. The strain R2 was identified to beEnterococcus faecium by morphology, physiochemical, and molecular biological identifications. The safety ofE.faecium R2 and the quality of sour slurry fermented byE.faecium R2 were analyzed. The results showed thatE.faecium R2 was sensitive to several common antibiotics. Compared sour slurry dried bean curd fermented byE.faecium R2 against naturally fermented one, no significant differences were found regarding their sensory characteristics. The results indicated thatE.faecium R2 can be developed as a newly pure starter to produce sour slurry. This study provides theoretical basis for efficient utilization of bean curd water as well as standardized production of sour slurry dried bean curd.
Key words Enterococcus faecium; bean curd water; sour slurry dried bean curd
第一作者:博士,讲师(本文通讯作者,E-mail:chenzhina0625@163. com)。
基金项目:淮南市科技局科技计划项目(2018A365);淮南师范学院自然科学研究重点项目(2017xj03zd);淮南师范学院博士科研启动金(58886);地方高校国家级大学生创新创业训练项目(201710381017)
收稿日期:2018-11-10,改回日期:2019-01-04
DOI:10.13995/j.cnki.11-1802/ts.019283