坛紫菜(Porphyra haitanensis),系暖温带性种类[1],主要分布在福建、浙江和广东沿岸,是我国特有的原始大型经济海藻[2-3]。紫菜蛋白营养价值高,其总氨基酸含量高于浒苔、石莼、裙带菜、龙须菜、海带、马尾藻和麒麟藻[4],含8种必需氨基酸,富含天冬氨酸、谷氨酸、丙氨酸、亮氨酸、缬氨酸、精氨酸和赖氨酸,可弥补谷物蛋白中赖氨酸含量较低的缺陷。中国是世界紫菜的主要生产国和出口国,2016年养殖面积达73千公顷,年产量高达13.5万t[5],其中坛紫菜占我国紫菜总产量的50%以上[2],具有巨大的碳汇潜力[6]和经济开发价值。同时,随着陆地蛋白质资源的日益匮乏,海洋藻类作为新型蛋白质资源的来源已逐渐受到重视,充分利用坛紫菜的营养价值,满足人们对于高品质蛋白质的需求,为提高海洋资源开发能力和发展海洋经济提供一条可行之路。
随着生物技术的迅猛发展,新型提取方法如超声波辅助提取法、微波辅助提取法和液氮研磨法被应用到蛋白质的提取过程中,具有设备简单,安全环保,无化学残留,耗时短,效率高等优势[7-8]。超声波辅助提取法(ultrasonic-assisted extraction,UAE)通过在生物基质中产生热效应、机械效应和空化效应破碎植物组织细胞壁[9],已被广泛应用到蛋白质[10]、多糖[11]、多酚[12]、油脂[13]和黄酮类化合物[14]的提取制备。但目前对于紫菜水溶性蛋白质的提取、基础特性研究较少,多数研究中原料局限于条斑紫菜且提取率普遍低于50%[15-16],而且不同种类的紫菜蛋白在含量、组成等特性上存在一定差异,因此研究坛紫菜蛋白的提取、基础特性十分必要。2012年,姚兴存等[16]采用超声波提取条斑紫菜蛋白,在超声时间10 min、温度50 ℃、料液比10∶1(mg∶mL)条件下提取率为37.6%。 紫菜的采收期一般可分为4次,即头水、二水、三水和四水,一般越往后营养品质越低,三水和四水等相对低值的坛紫菜资源是总产量的主要组成部分,一般较少用于食用[17]。本研究以广东南澳产三水坛紫菜为原料,优化超声波结合水提酸沉法提取坛紫菜蛋白工艺条件,并对其基础特性进行测定,旨在为低值坛紫菜的精深加工提供一定科学依据与理论基础。
第三次采收期坛紫菜,收获于广东省南澳汕头市澄海区培隆紫菜养殖区,在50 ℃烘干至质量恒定,过100目筛,干燥保存。凯氏定氮法测得其蛋白质含量为34%。
0.1 mol/L NaOH标准溶液、浓H2SO4、0.1 mol/L HCl标准溶液、K2SO4、H3BO3、CuSO4,上海碧云天生物技术有限公司。
Kjeltec TM 2300型蛋白自动分析仪,丹麦Foss公司;BioTek全自动酶标仪,美国Bio-Tek公司;JY 99LLDN超声波细胞粉碎仪,宁波新芝生物科技股份有限公司;日立835-50型高速氨基酸自动分析仪,日本日立公司;TDZ4-WS台式低速离心机,上海卢湘仪离心机仪器公司;Delta320精密pH计,梅特勒-托利多仪器(上海)公司。
1.3.1 工艺流程
准确称取1 g紫菜粉,加入100 mL蒸馏水混合均匀,设置一定的超声功率,设置频率参数为20 kHz,变幅杆25 mm,超声一定时间,4 500 r/min离心10 min, 将上清液pH调至等电点4.2,静置1 h,4 500 r/min离心10 min,收集粗蛋白并真空冷冻干燥24 h。坛紫菜蛋白含量的测定采用凯氏定氮法[18],提取率计算见公式(1)。
蛋白质提取率![]()
(1)
式中:m1,粗蛋白中蛋白质质量,mg;m0,样品原料中蛋白质质量,mg。
1.3.2 单因素试验设计
依据SPSS 20.0软件,采用单因素方差分析法(ANOVE,Tukey检验)进行显著性检验,并通过Dunbcan’s法进行单因素多重比较分析,以获得影响蛋白提取率的显著性因素。本实验分别考察了料液比(5∶1、7.5∶1、10∶1、12.5∶1、15∶1(mg∶mL))、功率(720、900、1 080、1 260、1 440 W)、超声发出时间(2、4、6、8、10 s)和超声全程时间(15、30、45、60、75 min)对坛紫菜蛋白提取率的影响。由于超声发生时间高于超声间歇时间时,提取液局部易形成高温、高压,易导致蛋白变性,因此本实验采用相同的超声发生时间和超声间歇时间。
1.3.3 响应面试验工艺优化
依据Design Expert 8.0.5 Trial软件,采用Box-Behnken中心组合实验设计及响应面(response surface methodology,RSM)试验优化关键因素,以获得紫菜蛋白的最佳提取工艺条件。根据单因素试验结果,以功率(A)、超声发出时间(B)、超声全程时间(C)3个关键因素为自变量,以1、0、-1分别代表自变量的高、中、低水平,共设立17个处理组。试验因素水平见表1。
表1 响应面试验因素水平表
Table 1 Response surface test factor level
Table

水平因素A(功率)/WB(超声发出时间)/sC(超声全程时间)/min-11 08043001 26064511 440860
1.3.4 等电点的测定
准确称取2 g坛紫菜蛋白,溶于200 mL去离子水中,取上清液20 mL并分别调至pH值为3.4、3.6、3.8、4.0、4.2、4.4、4.6、4.8、5.0,静置1 h,4 500 r/min离心10 min,取1 mL上清液加入3 mL考马斯亮蓝(G-250)试剂,混匀并-静置10 min,于595 nm波长处测定吸光度,坛紫菜蛋白的等电点(isoelectric point,pI) 为吸光度值最低点[19]。
1.3.5 紫外-可见分光光度计测定
配制5 mg/mL的蛋白溶液,用紫外-可见分光光度计在200~700 nm进行扫描测定。
1.3.6 氨基酸分析
色氨酸参考GB/T 18246—2000[20]法,其他氨基酸则参考GB/T 5009.124—2016[21]法。
根据1973年FAO/WHO提出的每克氮氨基酸评分模式和中国预防医学科学院营养与食品卫生研究所提出的鸡蛋蛋白氨基酸评分模式对比分析[22-23]。氨基酸评分(amino acid score,AAS)和化学评分(chemical score,CS)的计算见公式(3)和(4)。
![]()
(3)
![]()
(4)
被测样品蛋白质中氨基酸含量![]()
(5)
2.1.1 料液比对蛋白质提取率的影响
由图1可知,蛋白质的提取率随着料液比的增加先上升后下降,在 10∶1 (mg∶mL)时提取率达到最大,且各处理组无显著差异(P>0.05);这是因为溶液的黏度较低,分子扩散速率较高,传质推动力越大,提取率上升;随着料液比的增加,细胞内容物的大量溶出使得溶液的黏度较高,体系分散不均匀,影响了蛋白质的溶出量,因而提取率下降。综合考虑,料液比选择10∶1 (mg∶mL)较为合适。

图1 料液比蛋白质提取率的影响
Fig.1 Effect of solid-to-solvent ratio on the extraction yield of protein
2.1.2 功率对蛋白质提取率的影响
由图2可知,蛋白质的提取率随着功率的增加先迅速上升后缓慢上升,在超声功率1 440 W时达到最大,各处理组存在显著差异(P<0.05);这是因为空化效应和机械效应的增强了蛋白质分子与水分子之间相互作用,促进蛋白质的溶解[24],因此提取率迅速上升;随着功率的增加,由于超声产生的大量微气泡无法达到完全溃陷造成空化效应和机械效应的减弱,因此提取率上升缓慢。考虑到生产成本和仪器使用寿命,超声波功率选择1 080~1 440 W较为合适。

图2 功率对蛋白质提取率的影响
Fig.2 Effect of power on the extraction yield of protein
2.1.3 超声发出时间对蛋白质提取率的影响
由图3可知,蛋白质的提取率随着超声发出时间的增加先缓慢上升后迅速下降,在超声发出时间6s时达到最大,且处理组存在显著差异(P<0.05);这是因为持续的超声促进了蛋白质分子与水分子之间的相互作用,有利于蛋白质的溶出,因此提取率增加;随着超声发出时间的增加,超声局部产生的热效应使得蛋白质空间构象的次级键被破坏,促进了蛋白质分子间相互结合而形成沉淀[25],不利于蛋白质的溶出,且超声探头工作时间过长影响其使用寿命。综合考虑,超声发出时间选择4~8 s较为合适。
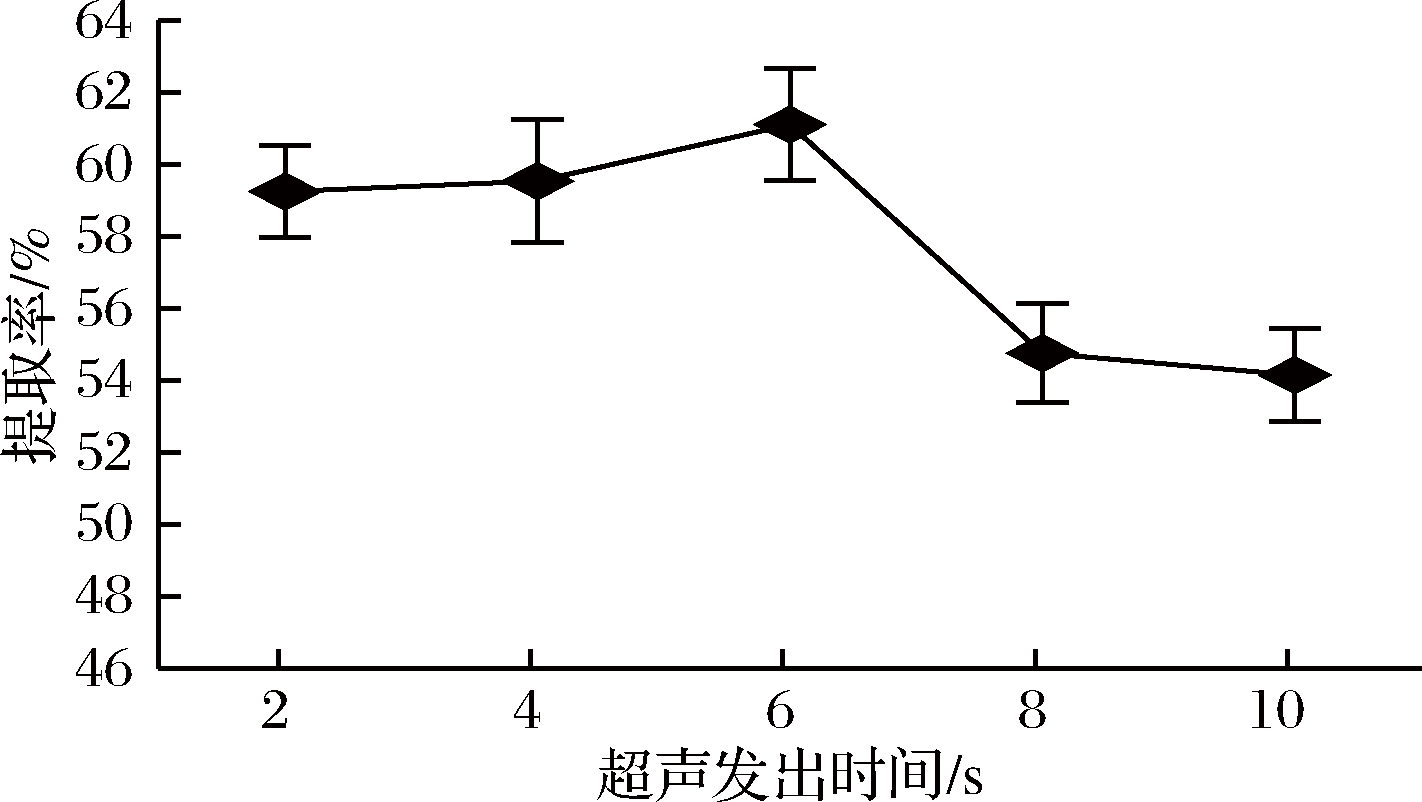
图3 超声发出时间对蛋白质提取率的影响
Fig.3 Effect of ultrasound emit time on the extraction yield of protein
2.1.4 超声全程时间对蛋白质提取率的影响
由图4可知,蛋白质的提取率随着超声全程时间的增加先迅速上升后迅速下降,在超声全程时间达到45 min时达到最大,且处理组存在显著差异(P<0.05); 这是因为超声波增强了水分子配位能力,促进了蛋白质分子和水分子的交互作用,因此提取率上升;随着超声全程时间的增加,蛋白质疏水集团暴露而巯基被掩埋在分子内部,通过非共价键形成了蛋白质聚集体,因此蛋白质提取率下降[26]。综合考虑,超声全程时间选择30~60 min较为合适。

图4 超声全程时间对蛋白质提取率的影响
Fig.4 Effect of ultrasound full time on the extraction yield of protein
2.2.1 数学模型的建立与显著性分析
经Design-Expert 8.0.5软件对表2结果进行分析,得到紫菜蛋白提取率的二次回归模型:Y/%= 61.17+0.91A+0.58B+3.53C-0.01AB-0.06AC+1.02BC-4.63A2-2.89B2-3.86C2
方差分析和显著性分析见表3。模型的P值小于0.000 1,失拟项(P=0.992 2大于0.05)不显著,表明该回归模型极显著;该模型R2值为0.992 1大于![]() 为0.982 0大于0.95,表明回归模型与试验结果的拟合度高,可用于坛紫菜蛋白质提取率的分析和预测。一次项系数A、B、C和二次项系数A2、B2、C2的P值小于0.05,表明这些因素对坛紫菜蛋白提取率的影响显著。
为0.982 0大于0.95,表明回归模型与试验结果的拟合度高,可用于坛紫菜蛋白质提取率的分析和预测。一次项系数A、B、C和二次项系数A2、B2、C2的P值小于0.05,表明这些因素对坛紫菜蛋白提取率的影响显著。
表2 响应面实验设计及结果
Table 2 Experimenal design and correspongding results for respond surface analysis

序号功率/W超声发出时间/s超声全程时间/s提取率/%1-1-1052.0921-1054.033-11053.26411055.245-10-148.22610-150.017-10155.48800157.0290-1-151.371001-150.48110-1156.331200059.501300062.011400062.011500060.341600060.591700060.90
由A、B、C的F值大小可以推断出,3个因素对坛紫菜蛋白提取率影响主次顺序为C>A>B。由表2可知,平行试验中数据存在一定的波动性,这可能是由于变幅杆的超声探头作为一种耗材,长时间的工作模式会使其变幅杆探头逐渐磨损,超声效果变差,因此认为不同磨损程度上的超声探头发出超声的强度略有差异。
表3 回归方程的方差分析
Table 3 Analysis of variance for the fitted regression model
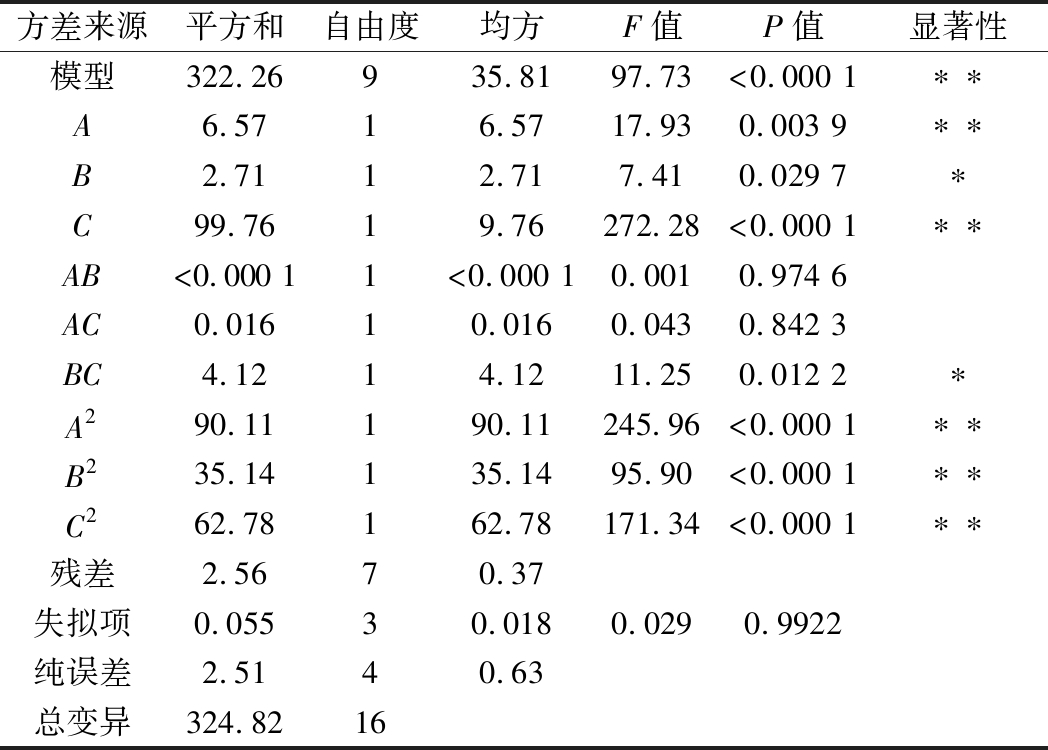
方差来源平方和自由度均方F值P值显著性模型322.26935.8197.73<0.000 1∗∗A6.5716.5717.930.003 9∗∗B2.7112.717.410.029 7∗C99.7619.76272.28<0.000 1∗∗AB<0.000 11<0.000 10.0010.974 6AC0.01610.0160.0430.842 3BC4.1214.1211.250.012 2∗A290.11190.11245.96<0.000 1∗∗B235.14135.1495.90<0.000 1∗∗C262.78162.78171.34<0.000 1∗∗残差2.5670.37失拟项0.05530.0180.0290.9922纯误差2.5140.63总变异324.8216
注:**,P<0.01,差异极显著;*,P<0.05,差异显著。
2.2.2 因素间交互作用影响结果
经过Design-Expert 8.0.5软件处理,得到功率(A)、超声发生时间(B)、超声全程时间(C)交互作用的响应面和等高线图。如图5~图7所示,超声全程时间和超声发生时间(BC)对坛紫菜蛋白提取率的影响显著,功率和超声发出时间(AB)、功率和超声全程时间(AC)交互作用不显著,与显著性分析结果相符。
根据所得到的响应面模型,经Design-Expert 8.0.5软件处理得到最优工艺为功率1 276.73 W、超声发生时间6.37 s、超声全程时间52.22 min,在此条件下坛紫菜蛋白提取率为62.12%。考虑到实际可操作性,调整工艺参数为功率1 278 W、超声发生时间6 s、超声全程时间52 min,在此条件下进行3组验证实验,坛紫菜蛋白提取率为61.13%、60.96%、61.50%,取平均值为61.20%,与理论值较为接近,表明响应面模型对优化坛紫菜蛋白的提取工艺可行。

图5 功率和超声发出时间交互作用的响应面和等高线图
Fig.5 Response surface and contour plots of interactions between power andultrasonic emission time

图6 功率和超声全程时间交互作用的响应面和等高线图
Fig.6 Response surface and contour plots of interactions between power and ultrasound full tme
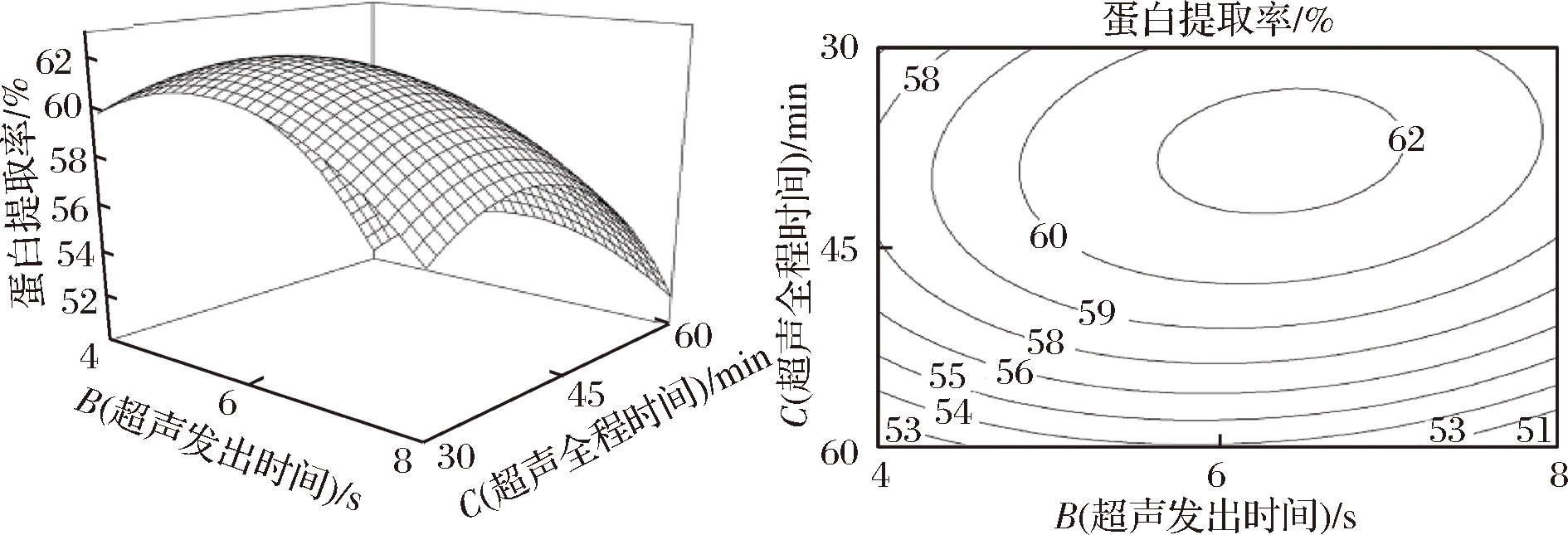
图7 超声发出时间和超声全程时间交互作用的响应面和等高线图
Fig.7 Response surface and contour plots of interactions between ultrasonic emission time and ultrasonic full time
2.3.1 等电点分析
由图8可知,pH值在3.4~5.0变化时,样品上清液吸光度呈现先下降后上升的趋势,在pH 4.2时吸光度最低,上清液中蛋白溶解度最小,即坛紫菜蛋白的等电点pI为4.2;这是因为pH靠近等电点时,蛋白质之间的疏水相互作用增强,蛋白质无序聚集,溶解度部分丧失或全部丧失[27]。
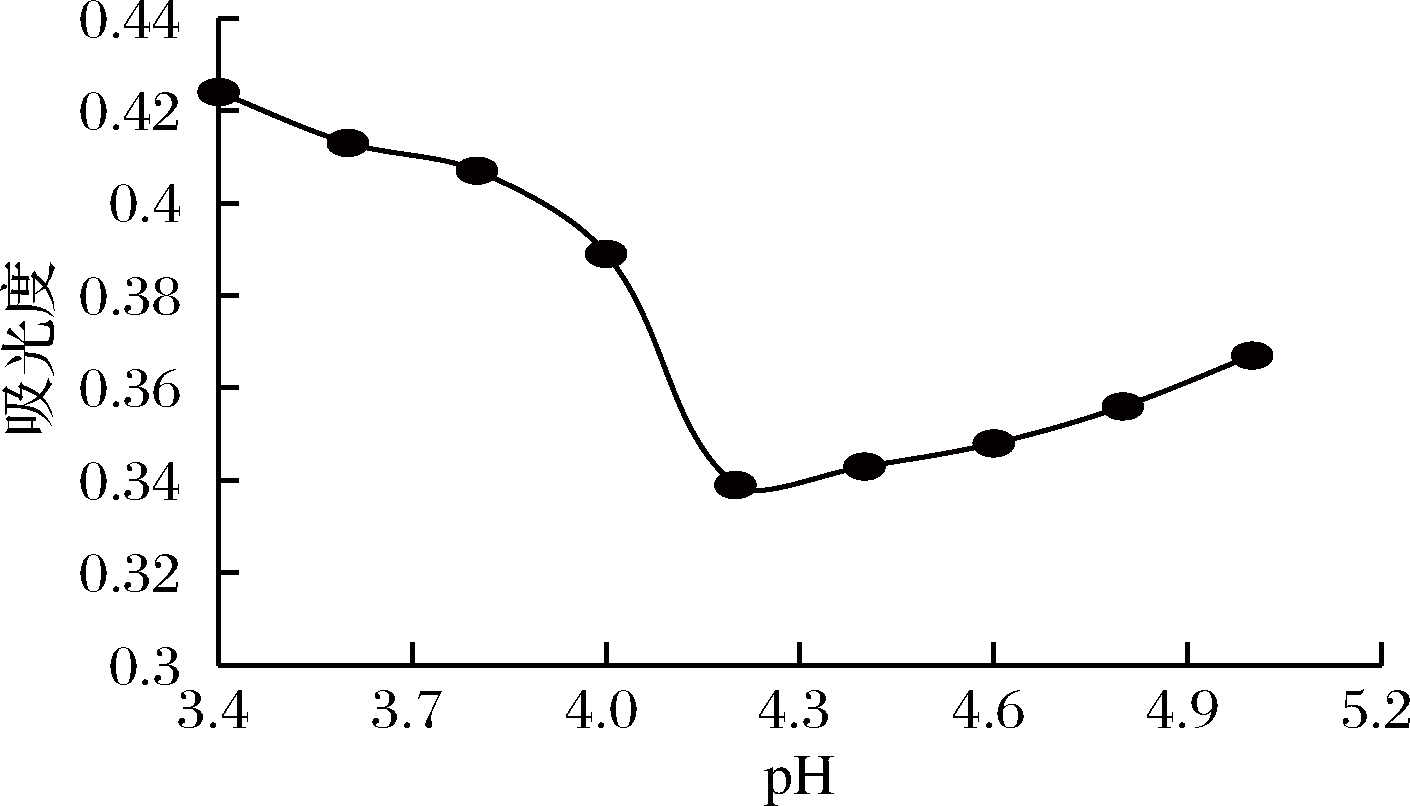
图8 蛋白等电点测定结果
Fig.8 Isoelectric point of the protein
2.3.2 紫外光谱分析
大部分氨基酸在紫外区仅有一个吸收峰,吸收峰多集中在200~220 nm,而Phe的吸收峰在222 nm 与259 nm,Tyr的吸收峰在231 nm及272 nm,Trp的吸收峰在227 nm与279 nm[28]。由图9可知,在200~700 nm对蛋白溶液进行紫外-可见光谱扫描时,220~280 nm曲线吸收较高,在260 nm 出现最大吸收峰,且未见明显杂峰;这是因为坛紫菜蛋白质氨基酸组成种类较多,Phe含量高于Tyr和Trp,因此最大吸收峰靠近Phe的最大吸收峰波长为259 nm。
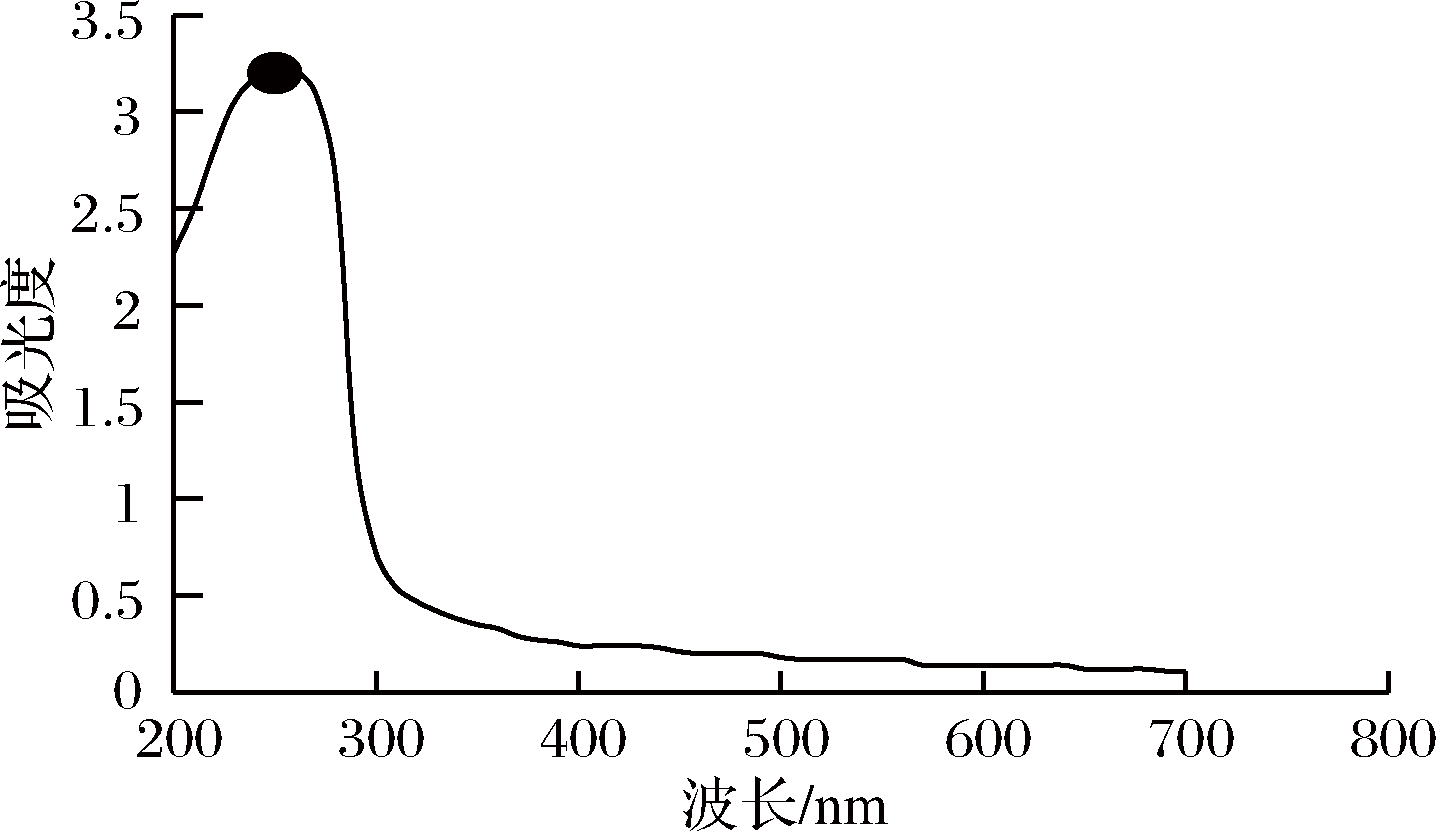
图9 蛋白溶液紫外-可见光谱扫描
Fig.9 UV-visible spectrum of the protein solution
2.3.3 氨基酸组成分析
由表4可知,检测到坛紫菜蛋白中共17种氨基酸(半胱氨酸未检测),种类齐全,Glu、Asp和Ala含量最高,必需氨基酸质量分数为40.29%,非必需氨基酸质量分数为59.71%,必需氨基酸和非必需氨基酸的比例为0.675,高于世界卫生组织规定值0.666,表明坛紫菜蛋白氨基酸组成合理[29]。仅根据必需氨基酸与非必需氨基酸的比例无法完全评估坛紫菜蛋白质的营养价值[30],因此采用FAO/WHO联合推荐的必需氨基酸模式和鸡蛋蛋白模式评估蛋白质营养价值。由表5可知,坛紫菜蛋白中Val、Lys、Leu、Thr和Phe+Tyr高于FAO/WHO氨基酸标准模式;Val、Leu、Thr和Phe+Tyr高于鸡蛋蛋白氨基酸模式,表明坛紫菜蛋白氨基酸组成与人体需求模式基本平衡,是一种理想蛋白源。Met的必需氨基酸评分(AAS)和化学评分(CS)评分最低,是第一限制性氨基酸。坛紫菜蛋白质的氨基酸组成比例与EUN-SUN等[31]测定结果相比,氨基酸组成较为相似,但氨基酸占总氨基酸含量比例却不同,这可能与紫菜的品种、生长环境、生长季节有关。
表4 坛紫菜蛋白氨基酸组成
Table 4 Amino acid of composition of Algal protein
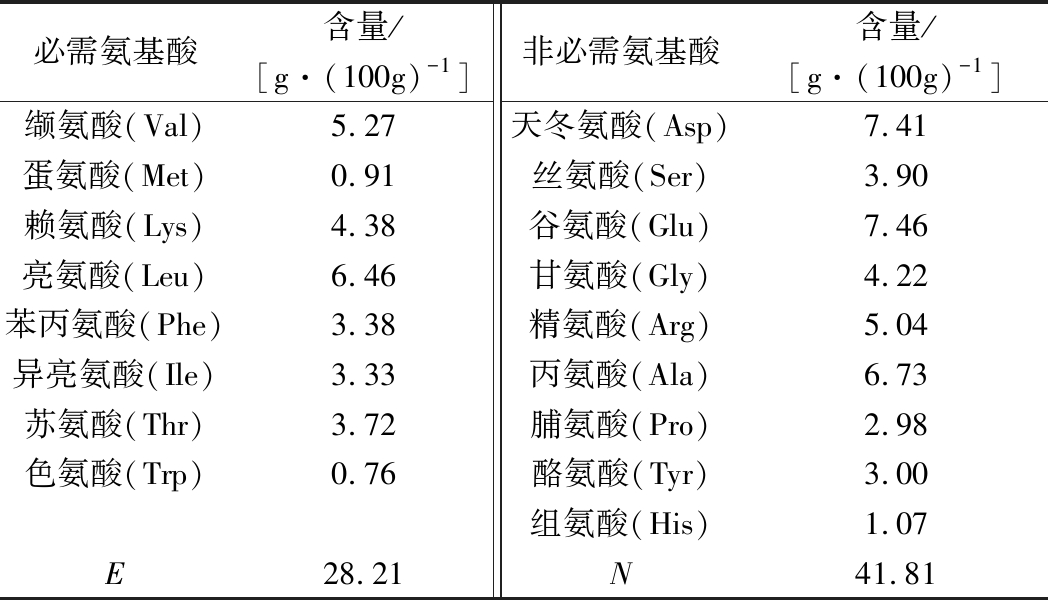
必需氨基酸含量/[g·(100g)-1]非必需氨基酸含量/[g·(100g)-1]缬氨酸(Val)5.27天冬氨酸(Asp)7.41蛋氨酸(Met)0.91丝氨酸(Ser)3.90赖氨酸(Lys)4.38谷氨酸(Glu)7.46亮氨酸(Leu)6.46甘氨酸(Gly)4.22苯丙氨酸(Phe)3.38精氨酸(Arg)5.04异亮氨酸(Ile)3.33丙氨酸(Ala)6.73苏氨酸(Thr)3.72脯氨酸(Pro)2.98色氨酸(Trp)0.76酪氨酸(Tyr)3.00组氨酸(His)1.07E28.21N41.81
注:E为必需氨基酸总和;N为非必需氨基酸总和。
表5 蛋白模式及必需氨基酸分析
Table 5 Protein mode and essential amino acid analysis
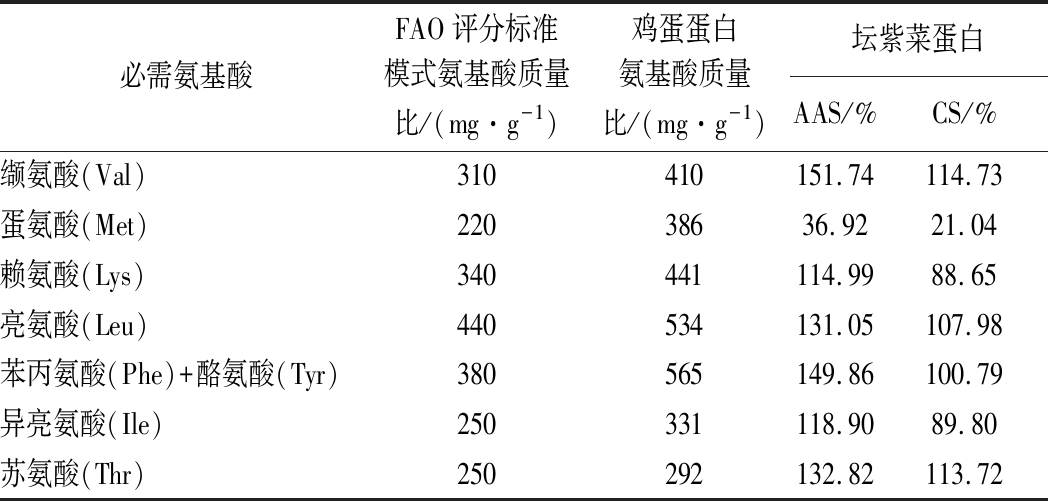
必需氨基酸FAO评分标准模式氨基酸质量比/(mg·g-1)鸡蛋蛋白氨基酸质量比/(mg·g-1)坛紫菜蛋白AAS/%CS/%缬氨酸(Val)310410151.74114.73蛋氨酸(Met)22038636.9221.04赖氨酸(Lys)340441114.9988.65亮氨酸(Leu)440534131.05107.98苯丙氨酸(Phe)+酪氨酸(Tyr)380565149.86100.79异亮氨酸(Ile)250331118.9089.80苏氨酸(Thr)250292132.82113.72
本实验选用三水紫菜作为原料,采用UAE进行坛紫菜蛋白的制备,运用单因素试验、响应面模型进行坛紫菜蛋白工艺的优化,同时对坛紫菜蛋白基础特性进行研究,旨在为低值坛紫菜的精深加工提供一定理论依据。通过3因素3水平的响应面实验设计,坛紫菜蛋白最佳提取工艺为超声功率为1 278 W、超声发出时间为6 s、超声全程时间为52 min,得率最高为61.20%,同时测定了坛紫菜蛋白的等电点、紫外最大吸收波长和氨基酸种类与含量,本研究为低值坛紫菜的研究开发提供了一定的科学依据和理论支持。
[1] 李锋,李清仙,程志远,等. 坛紫菜多酚抗氧化及抑制UVB致HSF细胞氧化损伤作用[J]. 食品科学, 2017, 38(17): 190-197.
[2] 白露. 坛紫菜多肽的分离纯化及其抗肿瘤活性研究[D]. 广州:华南理工大学, 2016.
[3] 陈伟洲, 吴文婷,许俊宾,等. 不同生态因子对皱紫菜生长及生理组分的影响[J]. 南方水产科学, 2013, 9(2): 14-19.
[4] 黄永连, 黄柳霞,陈晓嘉. 氨基酸自动分析仪测定不同藻类的氨基酸组成[J]. 粮食流通技术, 2016(11):100-104.
[5] 农业部渔业渔政管理局. 2017年中国渔业统计年鉴[M]. 北京:中国农业出版社. 2017: 28-50.
[6] 齐占会, 王珺,黄洪辉,等. 广东省海水养殖贝藻类碳汇潜力评估[J]. 南方水产科学, 2012, 8(1): 30-35.
[7] YU M, LIU H, SHI A, et al. Preparation of resveratrol-enriched and poor allergic protein peanut sprout from ultrasound treated peanut seeds[J]. Ultrasonics Sonochemistry, 2016, 28:334.
[8] ROLD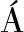 NGUTIÉRREZ J M, RUIZJIMÉNEZ J, CASTRO L D. Ultrasound-assisted dynamic extraction of valuable compounds from aromatic plants and flowers as compared with steam distillation and superheated liquid extraction[J]. Talanta, 2008, 75(5):1 369.
NGUTIÉRREZ J M, RUIZJIMÉNEZ J, CASTRO L D. Ultrasound-assisted dynamic extraction of valuable compounds from aromatic plants and flowers as compared with steam distillation and superheated liquid extraction[J]. Talanta, 2008, 75(5):1 369.
[9] KADAM S U, TIWARI B K, LVAREZ C, et al. Ultrasound applications for the extraction, identification and delivery of food proteins and bioactive peptides [J]. Trends in Food Science & Technology, 2015, 46(1): 60-67.
LVAREZ C, et al. Ultrasound applications for the extraction, identification and delivery of food proteins and bioactive peptides [J]. Trends in Food Science & Technology, 2015, 46(1): 60-67.
[10] PREECE K E, HOOSHYAR N, KRIJGSMAN A J, et al. Pilot-scale ultrasound-assisted extraction of protein from soybean processing materials is not recommended for industrial usage[J]. Journal of Food Engineering, 2017: 206.
[11] ZHANG D Y, WAN Y, XU J Y, et al. Ultrasound extraction of polysaccharides from mulberry leaves and their effect on enhancing antioxidant activity[J]. Carbohydr Polym, 2016, 137:473-479.
[12] PRADAL D, VAUCHEL P, DECOSSIN S, et al. Kinetics of ultrasound-assisted extraction of antioxidant polyphenols from food by-products: Extraction and energy consumption optimization[J]. Ultrasonics Sonochemistry, 2016, 32:137.
[13] KHOEI M, CHEKIN F. The ultrasound-assisted aqueous extraction of rice bran oil[J]. Food Chemistry, 2016, 194:503.
[14] CHEN Y Y, ZHANG D J. Optimization of ultrasound/microwave assisted extraction(UMAE)of flavones from Vaccinium Bracteatum Thunb Leaves[J]. Food & Machinery, 2016,32(1):148-153.
[15] 王婷, 马海乐,曲文娟,等. 条斑紫菜蛋白和多糖的逆流脉冲超声辅助提取技术研究[J]. 食品工业科技, 2012, 33(13):228-230.
[16] 姚兴存, 舒留泉,盘赛昆,等. 条斑紫菜蛋白提取与抗氧化活性[J]. 食品科学, 2012, 33(20):113-118.
[17] 陈美珍, 徐景燕,潘群文,等. 末水残次坛紫菜的营养成分及多糖组成分析[J]. 食品科学, 2011, 32(20):230-234.
[18] 中华人民共和国卫生部. GB/T 5009.5食品中蛋白质的测定[S]. 北京:中国标准出版社, 2010.
[19] 孙媛, 蔡迪,向琴,等. 麦麸中四种蛋白的Osborne法提取分离及性能研究[J]. 食品工业科技, 2015, 36(9): 136-139.
[20] 国家质量技术监督局. GB/T 18246饲料中氨基酸的测定[S]. 北京:中国标准出版社, 2000.
[21] 中华人民共和国国家卫生和计划生育委员会, 国家食品药品监督管理总局. GB/T 5009.124食品中氨基酸的测定[S]. 北京:中国标准出版社, 2016.
[22] VINAY B J, SIDHU KANYA T C. Effect of detoxification on the functional and nutritional quality of proteins of karanja seed meal [J]. Food Chemistry, 2008, 106(1): 77-84.
[23] 于刚, 张洪杰,杨少玲,等. 南海鸢乌贼营养成分分析与评价[J]. 食品工业科技, 2014, 35(18): 358-361.
[24] 刘高梅, 任海伟. 不同功率超声波对芸豆蛋白理化和功能性质的影响[J]. 中国粮油学报, 2012, 27(12): 17-21.
[25] 徐飞. 花生球蛋白亚基缺失对热特性的影响[D]. 北京:中国农业科学院, 2016.
[26] 毕爽, 马文君,李杨,等. 脉冲电场-超声波作用对黑豆球蛋白功能性质的影响[J]. 食品科学, 2016, 37(9):7-12.
[27] 周心雅, 贺稚非,李洪军,等. 酸碱度对兔肉肌原纤维蛋白功能性质的影响[J]. 食品与发酵工业, 2017,43(11):172-179.
[28] 董欣, 王丽燕. 氨基酸紫外光谱的再测定[J]. 德州学院学报, 2015(2): 44-46.
[29] 刘婷婷, 刘阳,张晶,等. 分蘖葱头蛋白提取工艺优化及其基础特性[J]. 食品科学, 2018, 39(2): 267-272.
[30] LUO T, XIE Y, DONG Y, et al. Quality assessment of soy sauce using underivatized amino acids by capillary electrophoresis[J]. International Journal of Food Properties, 2018:1-10.
[31] EUN-SUN H, KYUNG-NAM K, HA-YULL C. Proximate composition, amino acid, mineral, and heavy metal content of dried laver[J]. Prev Nutr Food Sci, 2013, 18(2):139-144.