
根据《可再生能源发展“十三五”规划》,到2020年,全国可再生能源年利用量折合7.3亿t标准煤,相当于减少CO2排放量约14亿t,减少SO2排放量约1 000万t,减少氮氧化物排放约430万t,减少烟尘排放约580万t,年节约用水约38亿m3[1-2]。可再生绿色能源的研发已逐渐成为国内外研究的热点[3-5]。
根据《全国农村沼气发展“十三五”规划》测算,中国每年产生农作物秸秆10.4亿t,可收集资源量约9亿t,约有1.8亿t的秸秆未得到有效利用,导致了环境污染和资源浪费。利用农作物秸秆厌氧发酵产沼气可以有效地解决该问题。沼气是一种清洁可再生能源,可为城镇提供电力和热力,也可经提纯得到的生物天然气并入天然气管网,进一步推动可再生绿色能源——沼气融入到当今的能源供应体系中[6]。沼气的主要成分为60%~70%的CH4和30%~40%的CO2,同时还含有0.1%~3%的H2S和少量水汽[7]。在沼气净化、运输、储存和使用的过程中,H2S会造成沼气净化设备、运输管道、储气柜等设备的腐蚀,利用效率的降低,使用寿命缩短,导致严重的安全问题[8-9]。沼气作为车用压缩天然气燃料时,H2S浓度应不高于15 mg/m3[10];并入天然气管网时,一类天然气对H2S含量要求为不高于6 mg/m3,二类天然气对H2S含量要求为不高于20 mg/m3[11]。而厌氧发酵产生的沼气中H2S的浓度远远高于此标准,因此,无论工业还是民用过程中,都必须对沼气进行脱硫处理[12]。
脱硫方法大致上可以分为干法脱硫、湿法脱硫以及一些其他脱硫方法,如生物脱硫、电化学再生脱硫、原位脱硫等[13-18]。其中,干法、湿法脱硫都属于目前工业应用中传统的脱硫方法[19]。这些方法脱硫效率较低,但沼气发酵工程规模逐年增大,亟需寻求一种低运行成本、高处理效率、操作简单的新型脱硫方法[20]。微氧法原位脱硫是一种新兴的脱硫方法,即向发酵罐中通入微量的氧气,使之与沼气中的H2S反应生成单质硫或硫酸盐[21-24]。随着国内外对微氧法原位脱硫技术研究的不断深入,往发酵罐顶部连续通入氧气已成为最佳选择方式。本实验通过微氧发酵的方法,探究了不同底物对发酵的影响,并研究了其对产气规律、沼气组分、脱硫效率以及对发酵液挥发性脂肪酸(volatile fatty acids, VFAS)VFAs的影响。
实验分别选用水稻秸秆和小麦秸秆(取自江苏省宿迁市归仁镇墩伦村)作为发酵原料,其中水稻秸秆总固体(total solid,TS)为(93.3±0.2)%,挥发性固体(volatile solid,VS)为(84.5±0.4)%,小麦秸秆总固体为(91.8±0.4)%,挥发性固体为(86.7±0.5)%, 使用前先用粉碎机将其粉碎。沼液作为接种物,取自杭州正兴牧业有限公司,总固体为(3.0±0.2)%, 挥发性固体为(1.8±0.2)%。
本实验建立了能连续导入O2的实验装置,使得氧气能够连续通入沼气厌氧发酵系统。实验在30 L带搅拌的序批式发酵罐中进行,发酵罐外部装有循环热水套,以维持反应过程中所需要的温度,并由热电偶测定与显示;发酵罐一侧装有可拆卸的pH电极,可从设备操作面板上直接读取沼液的pH值;同时,数字控制装置与发酵罐的搅拌装置相连,用来控制搅拌速度。发酵罐与滑动式集气柜相连,用来收集发酵过程中产生的气体。
实验选用水稻秸秆和小麦秸秆分别作为发酵底物,以沼液为接种物,向发酵罐中分别装入963 g水稻秸秆和978 g小麦秸秆,并向其中各加入12 L沼液和8 L水,控制总TS为(8±0.1)%,发酵温度设置为55 ℃,搅拌速度设定为100 r/min。发酵罐密封后用高纯氩驱赶发酵罐内残余的空气,使之处于完全厌氧状态。氧气自钢瓶出来,经转子流量计、蠕动泵、分气头控制气量后,从发酵罐的上部通入。由前期预实验可知产生沼气中H2S的含量,在高温发酵条件下,设置连续的O2通入量分别为体系中H2S产生量的1、 2、3倍,由此可得,水稻秸秆作为发酵底物时,发酵罐中O2通入量分别为75、150、225 mL/(L·d);小麦秸秆作为发酵底物时,发酵罐中O2通入量分别为39、78、117 mL/(L·d), 并各自设置不通O2的对照组实验。
在发酵产气的第9天通入O2(即发酵产气保持相对平稳的时期),设置发酵周期为30 d,每日计量沼气产生量;每5 d取罐中发酵液,测定pH值,且每10 d测定发酵液中VFAs的含量;每5 d采沼气样,测定其中CH4、CO2、O2、H2S的体积分数;测定发酵开始前和结束后沼液中的COD、TS和VS。
秸秆和沼液的TS、VS根据参考文献[25]测定。沼气中CH4、CO2、O2含量的检测方法如下:采用六通阀进样器进样,即采用铝箔采样袋将试样从进样孔注射至2 mL定量环,待定量环充满后,以高纯氩为载气携带试样进入气相色谱(GC-1690N,Agilent)的填充柱TDX-01内,最后采用热导检测器TCD检测。沼气中H2S含量的检测方法如下:进样方式同上,O2作为助燃气体,H2点火,以N2为载气携带试样进入气相色谱(GC-2014,岛津)的毛细管柱SH-Rtx-1(60 m×0.32 mm×5 μm)内,采用火焰光度检测器(FPD)检测。沼液中VFAs浓度的测定方法如下:通过微量进样针自动吸取进样瓶中的试样,经过气化室将样品汽化,氧气作为助燃气体,氢气点火,以氮气为载气携带汽化样品进入气相色谱(GC-6890N,Agilent Technologies)的毛细管柱AT-FFAP(30 m×0.32 mm×0.5 μm)内,采用火焰离子化检测器(FID)检测。
由图1可知,水稻秸秆和小麦秸秆分别作为发酵底物时,其产气规律极为相似。相比对照组,两种秸秆发酵的沼气总产量在连续通氧量为理论需氧量1、2倍时相对升高;而在通氧量为理论需氧量3倍时,两种秸秆的沼气总产量均低于对照组,可能是因为实验组发酵前期产气速率较高,底物消耗较快,且由于通入氧气过多,在发酵后期抑制了产甲烷菌的活性,导致产气量下降。但从总体上来说,氧气的通入对两种底物在整个发酵周期的沼气总产量变化不大,且水稻秸秆发酵的总产气量及产气速率均高于小麦秸秆。连续通入的O2量不同,对两种底物微氧发酵产气规律的影响几乎一致,且不改变沼气的产气规律。

a-小麦秸秆;b-水稻秸秆
图1 不同发酵底物中沼气总产量变化
Fig.1 Cumulative biogas production using different fermentation substrates
由图2和图3可知,对比发酵稳定期的沼气产量,实验发现对于不同底物,连续通氧量达到理论需氧量的2倍时产量最高,且小麦秸秆和水稻秸秆的产量分别升高约13%和23%。当通氧量升高到理论需氧量的3倍时,二者在发酵稳定期的产气量都不再升高。但相较于对照组,实验组中沼气的发酵稳定期天数相对延长,且呈现出较高的沼气产量,小麦秸秆和水稻秸秆发酵稳定期沼气产量分别升高约10%和12%,说明发酵体系中微量的氧气可以提高产甲烷菌的活性[26]。在本实验条件下,通氧量为理论需氧量2倍时,可达到较好的产气效果。

图2 不同发酵底物中沼气总产量(1~30 d)
Fig.2 The total gas production of biogas under different fermentation substrates under different fermentation substrates
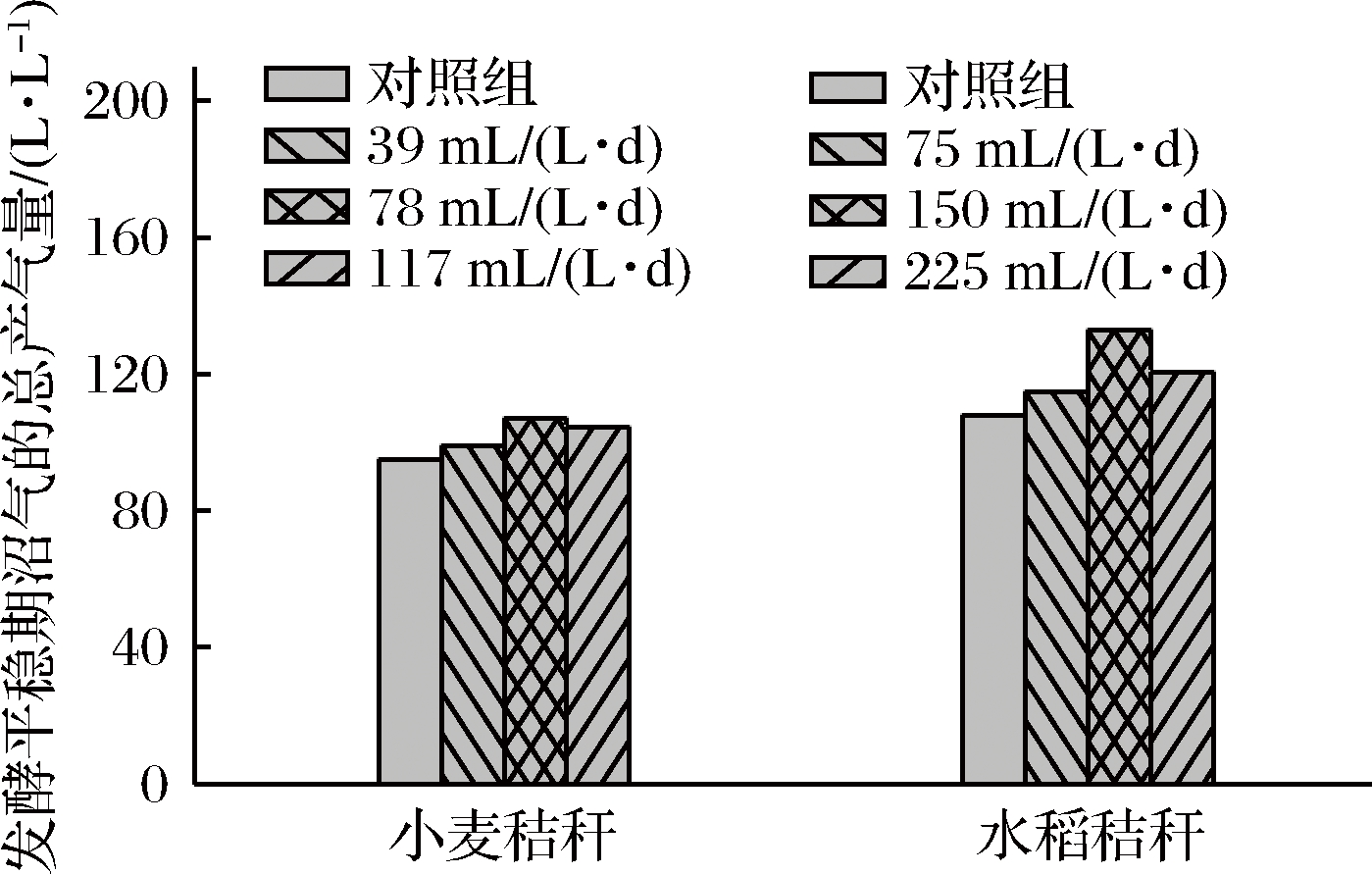
图3 不同发酵底物中发酵平稳期沼气产量(10~20 d)
Fig.3 The gas production of biogas during stable fermentation
由表1可知,小麦和水稻秸秆的沼气总产量在通氧量为理论需氧量2倍时,相较对照组分别升高约5.5%和4.6%,但通氧量升高到需氧量的3倍时,相较对照组分别降低约2.7%和1.5%,沼气总产量变化不大。随着通氧量的增大,小麦秸秆和水稻秸秆发酵沼气中CH4产量呈现出相同的变化趋势,且通氧量为理论需氧量的2倍时达到最大,分别达到12.6、14.0 L/(L·d),体积分数分别达到(63.9±3.1)%和(66.1±3.6)%,CH4产量相较对照组分别升高约10.5%和8.5%。
表1 不同发酵底物下沼气中各组分情况
Table 1 Biogas composition percentage under different fermentation substrates

组分小麦秸秆通氧量/[mL·(L·d)-1]水稻秸秆通氧量/[mL·(L·d)-1]03978117075150225沼气总产量/(L·L-1)558.7581.8589.5543.6605.6636.5633.6596.7平稳期沼气产量/(L·L-1)94.899.2106.9104.5108.1114.7132.9120.7沼气组成/%CH461.2±6.162.6±4.763.9±3.163.2±8.563.9±3.2 64.5±2.166.1±3.666.8±4.2CO237.5±5.436.1±4.834.9±6.835.1±5.232.9±3.931.2±4.330.9±5.627.6±3.9O20.26±0.070.26±0.040.28±0.030.37±0.080.24±0.030.25±0.020.32±0.040.55±0.01CH4产量/[L·(L·d)-1]11.412.112.611.512.913.714.013.3
注:表中水稻秸秆发酵产气平稳期取第10~20天数据;小麦秸秆发酵产气平稳期取第9~19天数据。
连续通氧量为117 mL/(L·d)时,与通氧量78 mL/(L·d) 相比,小麦秸秆发酵沼气CH4的体积分数基本不变,但平稳期沼气产量呈现出略微下降的趋势,下降约2.2%,而CH4产量和沼气总产量下降幅度较大,约为8.7%和7.8%;但相比对照组,均呈现出升高的趋势。沼气中氧气的体积分数整体维持在0.5%以下。
水稻秸秆作为发酵底物,连续通氧量为理论需氧量的1、2倍时,沼气中各组分体积分数、沼气总产量及平稳期产量、CH4产量的变化趋势均与小麦秸秆相似。当通氧量达到225 mL/(L·d)时,与通氧量150 mL/(L·d)相比,沼气总产量与CH4产量分别下降约5.8%和5.0%,此时,氧气体积分数略微超过了0.5%,这可能是因为通氧倍数不变,向水稻秸秆发酵罐中引入的氧气量较大,通氧速率较快,但气液传质较慢,造成部分O2不能及时被沼液中的硫氧化细菌和兼性厌氧菌利用,从而导致其残留在沼气中,造成O2体积分数整体略高于小麦发酵沼气中O2的体积分数;但在该条件下,平稳期沼气产量及CH4产量均高于对照组,说明连续通入的氧气没有对发酵系统产生抑制作用。
由表2、表3对比可知,小麦和水稻秸秆发酵沼气中H2S浓度波动范围分别为3 500~4 500 mg/m3和6 500~7 000 mg/m3,后者H2S浓度更高。对比H2S去除率可知,连续通氧量为相同倍数理论需氧量下,水稻秸秆发酵体系中H2S去除率略高于小麦秸秆发酵体系,可能是因为小麦秸秆发酵沼气中H2S浓度波动范围比水稻秸秆大,氧气连续通入量保持不变,使得水稻秸秆发酵沼气中H2S更能够稳定地与O2反应,从而保持相对较高的脱硫效率。
表2 小麦秸秆作为发酵底物沼气发酵过程中H2S去除效果
Table 2 The concentration and removal efficiency of H2S during biogas fermentation of wheat straw as fermentation substrate
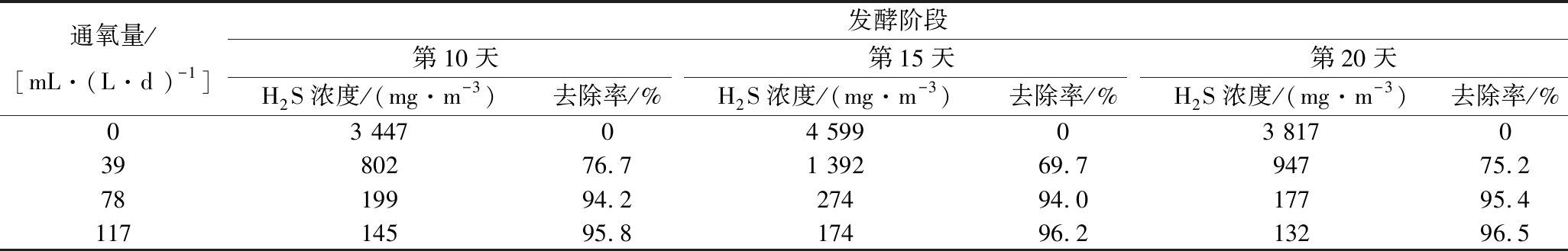
通氧量/[mL·(L·d )-1]发酵阶段第10天第15天第20天H2S浓度/(mg·m-3)去除率/%H2S浓度/(mg·m-3)去除率/%H2S浓度/(mg·m-3)去除率/%03 44704 59903 81703980276.71 39269.794775.27819994.227494.017795.411714595.817496.213296.5
表3 水稻秸秆作为发酵底物沼气发酵过程中H2S去除效果
Table 3 The concentration and removal efficiency of H2S during biogas fermentation of rice straw as fermentation substrate
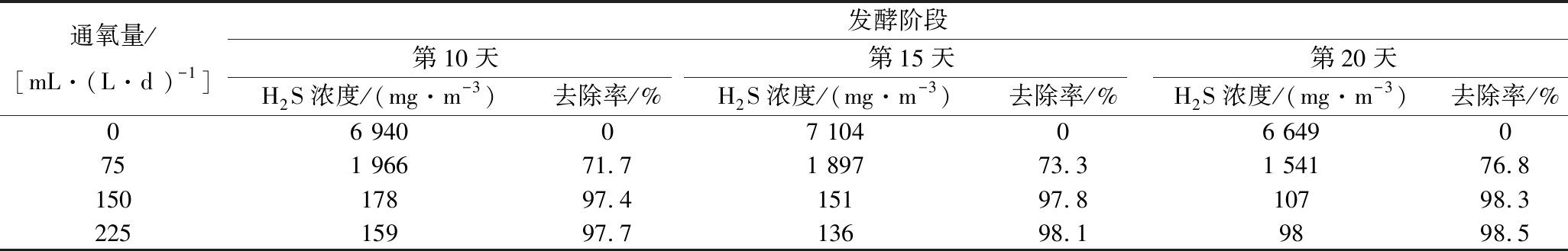
通氧量/[mL·(L·d )-1]发酵阶段第10天第15天第20天H2S浓度/(mg·m-3)去除率/%H2S浓度/(mg·m-3)去除率/%H2S浓度/(mg·m-3)去除率/%06 94007 10406 6490751 96671.71 89773.31 54176.815017897.415197.810798.322515997.713698.19898.5
连续通氧量由1倍增加到2倍,H2S的脱除效率明显增高。小麦和水稻秸秆发酵体系中H2S脱除效率由74%分别增加到95%和98%左右。由图4可知,两种不同底物的发酵体系中,O2体积分数也随着连续通氧量的增大而增大,小麦秸秆发酵体系中O2体积分数始终维持在0.5%以下。水稻秸秆发酵体系中,通氧量增加到理论需氧量的3倍时,H2S脱除效率增加不明显,但沼气中O2体积分数明显增加,且略微超过了0.5%,可能是因为氧气在发酵罐中不能及时分散,限制了与H2S的接触,残留于沼气且被带出发酵罐。

图4 不同发酵底物中发酵平稳期沼气中的
O2平均体积分数
Fig.4 Average O2 content in biogas during stable fermentation under different fermentation substrates
相关研究表明[27],发酵体系中的异养甲烷营养细菌会与氧化H2S的微生物竞争O2,导致O2不能完全用于氧化H2S,因而通氧量为1倍时,O2并不能完全用于氧化H2S,导致整体的脱硫效率较低。当连续通氧量达到理论需氧量的3倍时,可能是因为发酵罐中兼性厌氧菌和好氧菌利用氧气的能力有限,用于氧化H2S的O2量达到其利用的最高限值,导致脱硫效率提高不明显,且由于气液传质速率较小,O2不能及时被其充分利用而残留在沼气中,导致O2体积分数明显升高。
由表4、表5及图5可以看出,发酵第3天,乙酸浓度较高,可能是处于厌氧发酵初期,微生物将大分子有机物分解为小分子有机物和脂肪酸,而后进入酸化阶段,产氢产乙酸菌将第一阶段的有机酸如挥发性短链脂肪酸(丁酸、丙酸)和乙醇等水溶性小分子转化为乙酸、H2和CO2,其中乙酸所占比例最大,故大量乙酸存在于发酵液中。随着发酵不断进行,底物不断被消耗,微生物活性逐渐降低,VFAs浓度逐渐减小,最后趋于稳定,由此可知,微量氧气的通入未对发酵液中VFAs的降解造成明显的影响。
由表4、表5可以看出,水稻秸秆发酵液中VFAs的浓度及降解速率均高于小麦秸秆,且VFAs中乙酸浓度远高于其他酸,这可能是造成水稻秸秆发酵沼气中CH4体积分数高于小麦秸秆的原因。水稻秸秆发酵后期,连续通氧量达到225 mL/(L·d)时,相较于1、2倍通氧量的发酵,沼液中VFAs积累明显,可能是由于过量O2的通入,提高了发酵体系中好氧菌及兼性厌氧菌的活跃度,从而产生了较多的VFAS,同时过量的O2抑制了产甲烷菌等严格厌氧菌的活性,使得VFAs的降解受到了一定程度的抑制。
表4 小麦秸秆作为发酵底物发酵过程中发酵液中的VFAs浓度变化 单位:mg/L
Table 4 Variation of VFAs concentration in biogas slurry during fermentation

发酵时间/d通氧量/[mL·(L·d)-1]03978117乙酸丙酸异丁酸正丁酸乙酸丙酸异丁酸正丁酸乙酸丙酸异丁酸正丁酸乙酸丙酸异丁酸正丁酸3619386142473589351131502601406192409593441142473109812217501081468728102132244611215321392082341128795315208234112091349283062143953206753185115823513
表5 水稻秸秆作为发酵底物发酵过程中发酵液中的VFAs浓度变化 单位:mg/L
Table 5 Variation of VFAs concentration in biogas slurry during fermentation

发酵时间/d通氧量/[mL·(L·d)-1]075150225乙酸丙酸异丁酸正丁酸乙酸丙酸异丁酸正丁酸乙酸丙酸异丁酸正丁酸乙酸丙酸异丁酸正丁酸31 5646186649361 8765145697761 7816805318291 73256160373010163261541641832848712320826781982332901147520797216286853212570492019786510263047105104021819581781383231225

a-小麦秸杆;b-水稻秸杆
图5 不同发酵底物下发酵液中总VFAs浓度变化图
Fig.5 The concertration of total VFAs under different fermentation substrates
本实验以小麦秸秆和水稻秸秆作为底物,考察了连续通氧对原位脱除H2S的效果,及其对厌氧消化性能的影响。结论如下:
(1)两种秸秆进行高温微氧发酵,产气规律极为相似,沼气总产量基本不变,说明微量氧气的通入不改变沼气产气规律,且可提升稳定期沼气和CH4的产量,通氧量为理论需氧量2倍时皆达到最高。
(2)通氧量为理论需氧量2倍时,水稻和小麦秸秆发酵沼气中H2S的脱除率分别达到98%和95%,前者脱硫率略高。通氧量为理论需氧量3倍时,H2S脱除效率达到最高,此时,小麦秸秆发酵体系中O2体积分数较低,但水稻秸秆发酵体系中,O2的体积分数较难控制在0.5%以下。
(3)两种秸秆发酵液中VFAs浓度变化趋势极其相似,但小麦秸秆发酵液中VFAs浓度及其降解速率均远低于水稻秸秆,VFAs主要成分为乙酸。
[1] 邹才能,赵群,张国生,等.能源革命:从化石能源到新能源[J].天然气工业,2016,36(1):1-10.
[2] 国家发展改革委.可再生能源发展“十三五”规划[J].太阳能,2017(1):78.
[3] 张伟,李文,赵继东,等.小麦秸秆同步糖化发酵制取燃料乙醇[J].食品与发酵工业,2012,38(12):50-54.
[4] 石笑羽,王宁,陈钦冬,等.生物炭加速餐厨垃圾厌氧消化的机理[J].环境工程学报,2018,12(11):3 204-3 212.
[5] 艾平,张济韬,席江,等.纤维素乙醇糟液对稻秸猪粪厌氧发酵的促进机制[J].环境工程学报,2017,11(12):6 404-6 414.
[6] 赵伟,黄小美,谭顺民.沼气混入天然气管网使用的可行性探讨[J].煤气与热力,2012,32(12):8-11.
[7] 林春绵,章祎玛,叶媛媛,等.沼气的微氧法原位脱硫试验[J].浙江工业大学学报,2017,45(1):37-42.
[8] 龚甍.天然气的脱硫净化研究[D].西安:西安石油大学,2017:1-9.
[9] 罗新爱.天然气脱硫装置中硫化氢对设备的腐蚀问题浅析[J].四川化工,2014,17(3):26-29.
[10] GB 17820—2012,天然气[S].北京:中国标准出版社, 2012.
[11] GB 18047—2000,车用压缩天然气[S].北京:中国标准出版社,2000:414-451.
[12] 陈沛全,曾彩明,李娴,等.沼气净化脱硫工艺的研究进展[J].环境科学与管理,2010,35(4):125-129.
[13] LI X,LI W,WANG L,et al.Investigation on the selection of flue gas dry and wet desulfurization processes[J].Coal Chemical Industry,2018,46(3):17-21.
[14] 董长青,陆强,田伟强,等.一种石灰石石膏湿法烟气脱硫添加剂:中国,CN104941429 B[P],2017.
[15] MESCIA D,HERN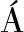 NDEZ S P,CONOCI A,et al.MSW landfill biogas desulfurization[J].International Journal of Hydrogen Energy,2011,36(13):7 884-7 890.
NDEZ S P,CONOCI A,et al.MSW landfill biogas desulfurization[J].International Journal of Hydrogen Energy,2011,36(13):7 884-7 890.
[16] MAKARUK A,MILTNER M,HARASEK M.Biogas desulfurization and biogas upgrading using a hybrid membrane system - modeling study[J].Water Science & Technology,2013,67(2):326-32.
[17] WEI Z S,NING X N.Development and application of the bio-desulfurization technology[J].Advanced Materials Research,2012,518:178-182.
[18] 甄峰,李东,孙永明,等.沼气高值化利用与净化提纯技术[J].环境科学与技术,2012,35(11):103-108.
[19] 韩文彪,王毅琪,徐霞,等.沼气提纯净化与高值利用技术研究进展[J].中国沼气,2017,35(5):57-61.
[20] 尹雅芳,张伟.沼气生物脱硫工艺设计及运行条件分析[J].环境科技,2017,30(2):12-16.
[21] 吴檬檬.微氧法原位脱除沼气中硫化氢的实验研究[D].杭州:浙江工业大学,2014:31-37.
[22] WU M,ZHANG Y,YE Y,et al.In situ removal of hydrogen sulfide during biogas fermentation at microaerobic condition[J].Appl Biochem Biotechnol,2016,180(5):1-9.
[23] D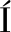 AZ I,LOPES A C,PÉREZ S I,et al.Determination of the optimal rate for the microaerobic treatment of several H2S concentrations in biogas from sludge digesters[J].Water Science & Technology,2011,64(1):233.
AZ I,LOPES A C,PÉREZ S I,et al.Determination of the optimal rate for the microaerobic treatment of several H2S concentrations in biogas from sludge digesters[J].Water Science & Technology,2011,64(1):233.
[24] KRÜGER K I,RUPF M,LEIFHEIT M,et al.Biological desulfurization of biogas,comprises directly performing desulfurization in biogas fermenter during anaerobic fermentation of biomass,and forming artificial functional layer at interface between liquid phase and gas phase:Germany,DE102011081522[P].2013-02-28.
[25] CLESCERL L S.Standard Methods for the Examination of Water and Wastewater[M]. 20th Ed.Washington DC: Amer Public Health Assn,1998.
[26] RODR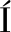 GUEZ E,LOPES A,FDZ-POLANCO M,et al.Molecular analysis of the biomass of a fluidized bed reactor treating synthetic vinasse at anaerobic and micro-aerobic conditions[J]. Applied Microbiology & Biotechnology,2012,93(5):2 181-2 191.
GUEZ E,LOPES A,FDZ-POLANCO M,et al.Molecular analysis of the biomass of a fluidized bed reactor treating synthetic vinasse at anaerobic and micro-aerobic conditions[J]. Applied Microbiology & Biotechnology,2012,93(5):2 181-2 191.
[27] POKORNAKRAYZELOVA L,BARTACEK J,THEURI S N,et al.Microaeration through biomembrane for biogas desulfurization: lab-scale and pilot-scale experiences[J]. Environmental Science Water Research & Technology,2018,4(8):1 190-1 200.