余甘子又名油柑子、滇橄榄、鱼木果等[1],广泛分布于(亚)热带,在中国主要分布于云南、福建、广东、广西和海南等几个省区[2-3]。余甘子性凉,味甘、酸、苦、涩,含有多种有益成分,如多酚类、氨基酸类、维生素类和微量矿物元素等[4-5]。研究表明,余甘子果肉中含有丰富的酚类物质,含量可达到11.4%[5-6],并且其VC含量在水果中仅次于刺梨[7]。余甘子是联合国卫生组织指定的在世界范围内推广种植的3种保健植物之一,在1998年被国家卫生部列入首批药食兼用名单[3-4,8],具有抗氧化、抗菌、抗病毒、降血脂、抗肿瘤、抗诱变突变等生理和药用功能,且无明显的毒副作用[9]。
食用酵素是以动物、植物、食用菌等为原料,经微生物发酵制得的含有特定生物活性成分可食用的酵素产品[10],包含多酚、氨基酸、功效酶、有机酸、维生素、益生菌等有益成分[11],这些成分为食用酵素提供了抑菌消炎、美容养颜、维持机体平衡、解酒护肝、改善肠胃、提高免疫力等生理功能[12-22]。
本文以余甘子为实验原料,选取食品发酵常用霉菌作为菌种,采用前发酵加主发酵的两段发酵法,以游离氨基酸含量和总酚含量为主要指标,结合还原糖含量、蛋白质含量以及1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl,DPPH)自由基清除能力等其他指标,研究1种新型余甘子酵素的发酵工艺,制备品质良好的余甘子酵素饮品,为余甘子鲜果的开发利用提供了新的途径和科学依据,有助于提高余甘子的经济及社会价值。
1 材料与方法
1.1 材料与试剂
余甘子、黄砂糖、麸皮,市售;米根霉、米曲霉、黑曲霉,广东省微生物菌种保藏中心。
L-亮氨酸、DPPH:色谱纯;福林酚,生物试剂;甲基红、亚甲基蓝:指示剂;3,5-二硝基水杨酸,化学纯;其他试剂,分析纯;高效凯氏定氮催化剂片,北京金元兴科科技有限公司。
1.2 主要仪器与设备
SW-CJ-1FD超净工作台,苏州智净净化设备有限公司;YX-2800手提式压力蒸汽灭菌器,合肥华泰医疗设备有限公司;LRH生化培养箱,上海一恒科技有限公司;JW-3024HR高速冷冻离心机,安徽嘉文仪器装备有限公司;UV-1800紫外分光光度计,Shimadzu Suzhou Instruments Mfg. CO., Ltd;FE20 pH计,梅特勒-托利多仪器(上海)有限公司;SH220F石墨消解仪,山东海能科学仪器有限公司;KjeltecTM 8100凯氏定氮仪,福斯分析仪器有限公司;PAL-1手持式糖度计,ATAGO Co., Ltd.。
1.3 实验方法
1.3.1 工艺流程
菌种→活化→制曲 糖水(ω=40%)
↓ ↓
余甘子处理→前发酵→主发酵→过滤离心→上清液巴氏杀菌→余甘子酵素
1.3.2 操作要点
1.3.2.1 原辅料处理
挑选新鲜、无腐烂、无霉变的余甘子,用无菌水洗净后晾干,去核,破碎成小于5 mm的果块,整个操作在无菌操作台内进行。糖水:黄砂糖在紫外下灭菌30 min后用无菌水调配成ω=40%。
1.3.2.2 菌种活化和制曲
菌种活化:按照广东省微生物菌种保藏中心提供的操作说明活化2代后制成孢子悬浮液备用。
制曲[23-24]:首先将麸皮与水以质量比1∶1混合拌匀并装入三角瓶中,经0.098 MPa蒸汽灭菌30 min,冷却至35 ℃左右,加入质量分数1%~2%的孢子悬浮液;然后28~30 ℃保温培养至长出菌丝,摇瓶;再培养1~2 d,扣瓶,培养12~24 h;最后装入无菌纸袋,37~40 ℃下干燥至含水量(10±1)%后装入无菌密闭容器,低温干燥保存不超过1个月。
1.3.2.3 前发酵
本工艺选取的菌种是食品发酵常用霉菌,均为好氧菌,根据微生物在对数生长期时酶系活跃的特性[25],为了产生足够的酶对原辅料进行分解,缩短发酵周期,需要先让霉菌在合适的温度和有氧的条件下生长一定时间。调节前发酵的温度为28 ℃,并用透气膜包住发酵容器口使空气流通和隔离环境微生物,保证霉菌的生长。
1.3.2.4 主发酵
为了防止霉菌过量生长消耗营养物质,并让前发酵产生的各种酶充分作用,把发酵物中的大分子物质水解为易于被吸收利用的生物活性小分子物质,同时改善酵素的气味、口感等,从而需要在前发酵结束时对霉菌进行抑制并继续发酵一段时间。按m(原料)∶m(糖水)=1∶1加入质量分数为40%的糖水,使发酵物体积占发酵容器总体积的90%~95%,调节主发酵的温度为23 ℃,密封发酵。
1.3.3 单因素试验
在单因素试验中,先后考察发酵曲种(无曲种、米根霉、米曲霉、黑曲霉、米根霉+米曲霉、米根霉+黑曲霉、米曲霉+黑曲霉、米根霉+米曲霉+黑曲霉),前发酵时间(0、12、24、36、48、60、72、84、96、108、120 h),主发酵时间(0、15、30、45、60、75、90 d),黑曲霉曲种添加量(ω=0.25%、0.50%、0.75%、1.00%、1.25%、1.50%,ω为黑曲霉曲种质量与黑曲霉曲种和余甘子果肉的总质量之比)和米根霉曲种添加量(ω=0.25%、0.50%、0.75%、1.00%、1.25%、1.50%,ω为米根霉曲种质量与米根霉曲种和余甘子果肉的总质量之比)对余甘子酵素游离氨基酸含量和总酚含量的影响。
1.3.4 响应面优化试验
在上述单因素试验结果的基础上,采用Box-Behnken设计方法[26-28],选择前发酵时间、主发酵时间、黑曲霉曲种添加量和米根霉曲种添加量为自变量,以游离氨基酸含量和总酚含量的综合评分为响应值,设计4因素3水平的响应面试验,从而获得最佳的发酵工艺条件。设计的因素水平见表1。
表1 Box-Behnken试验因素水平设计
Table 1 Factors and levels used in Box-Behnken design
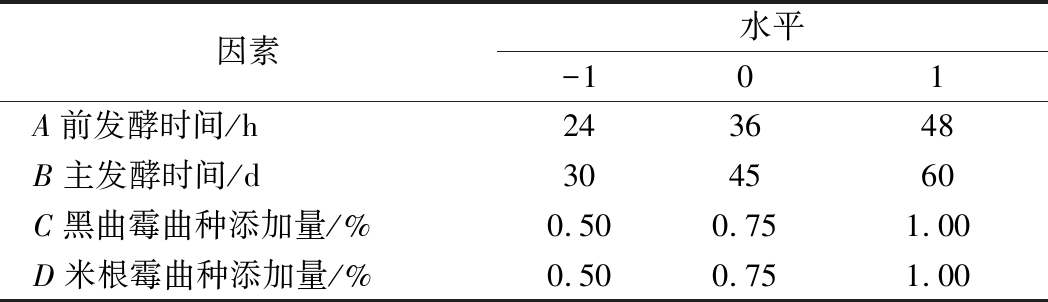
因素水平-101A前发酵时间/h243648B主发酵时间/d304560C黑曲霉曲种添加量/%0.500.751.00D米根霉曲种添加量/%0.500.751.00
通过运用隶属度综合评分法和加权计算对所得酵素进行综合评分[29],其中隶属度按公式(1)计算,综合评分按公式(2)计算:
![]()
(1)
式中: Ci,指标值;Cmin,指标最小值;Cmax,指标最大值。
S=aL氮+bL酚
(2)
式中:L氨,游离氨基酸含量隶属度;L酚,总酚含量隶属度;a,游离氨基酸含量权重,赋予a=0.5;b,总酚含量权重,赋予b=0.5。
1.3.5 余甘子酵素的理化特性及感官评价
1.3.5.1 游离氨基酸含量
采用茚三酮比色法测定游离氨基酸含量[30]。游离氨基酸含量用亮氨酸等价物表示,亮氨酸标准曲线回归方程如公式(3)所示:
y=7.236 6x-0.019 7,R2=0.999 1
(3)
1.3.5.2 总酚含量
采用福林酚法测定总酚含量[31-32],取2.00 mL余甘子酵素,加入1 mL福林酚试剂(1∶5 H2O),3 min后加入20% Na2CO3溶液2 mL,混合后在30 ℃避光静置30 min,765 nm处测定吸光度。总酚含量用没食子酸等价物表示,没食子酸标准曲线回归方程如式(4)所示:
y=34.149x+0.013 5,R2=0.999 1
(4)
1.3.5.3 其他特性
蛋白质含量:凯氏定氮法[33]。还原糖含量:3,5-二硝基水杨酸法[12]。pH值:pH计直接测定。可溶性固形物:手持式糖度计直接测定。DPPH自由基清除能力:参照管章瑞等[34]的方法测定。羟自由基清除能力:参照蒋增良等[35]的方法测定。
1.3.5.4 感官评价
感官评价小组由10人组成,单独对余甘子酵素进行观察、嗅闻和品尝后,根据表2的感官评价标准进行综合打分,同一样品的最终得分为10人总数的平均值。
表2 新型余甘子酵素感官评价标准
Table 2 Sensory evaluation standards of novelPhyllanthus emblica jiaosu

项目评价标准满分/分外观亮黄色,澄清,无肉眼可见沉淀和悬浮物30气味清香,无酒味,无明显霉味,无其他刺激性气味30滋味酸甜适中,无涩味,无异味,口感柔顺40
1.3.6 数据处理
所有试验均重复3次,结果取平均值。采用SPSS、Origin和Design-Expert软件进行数据处理分析及绘图。
2 结果与讨论
2.1 单因素试验结果与分析
2.1.1 发酵曲种对余甘子酵素游离氨基酸和总酚含量的影响
在固定前发酵36 h、主发酵45 d、各曲种的添加量为质量分数0.75%的条件下,改变发酵曲种,测定主发酵45 d后的余甘子酵素的游离氨基酸和总酚含量,结果见图1。
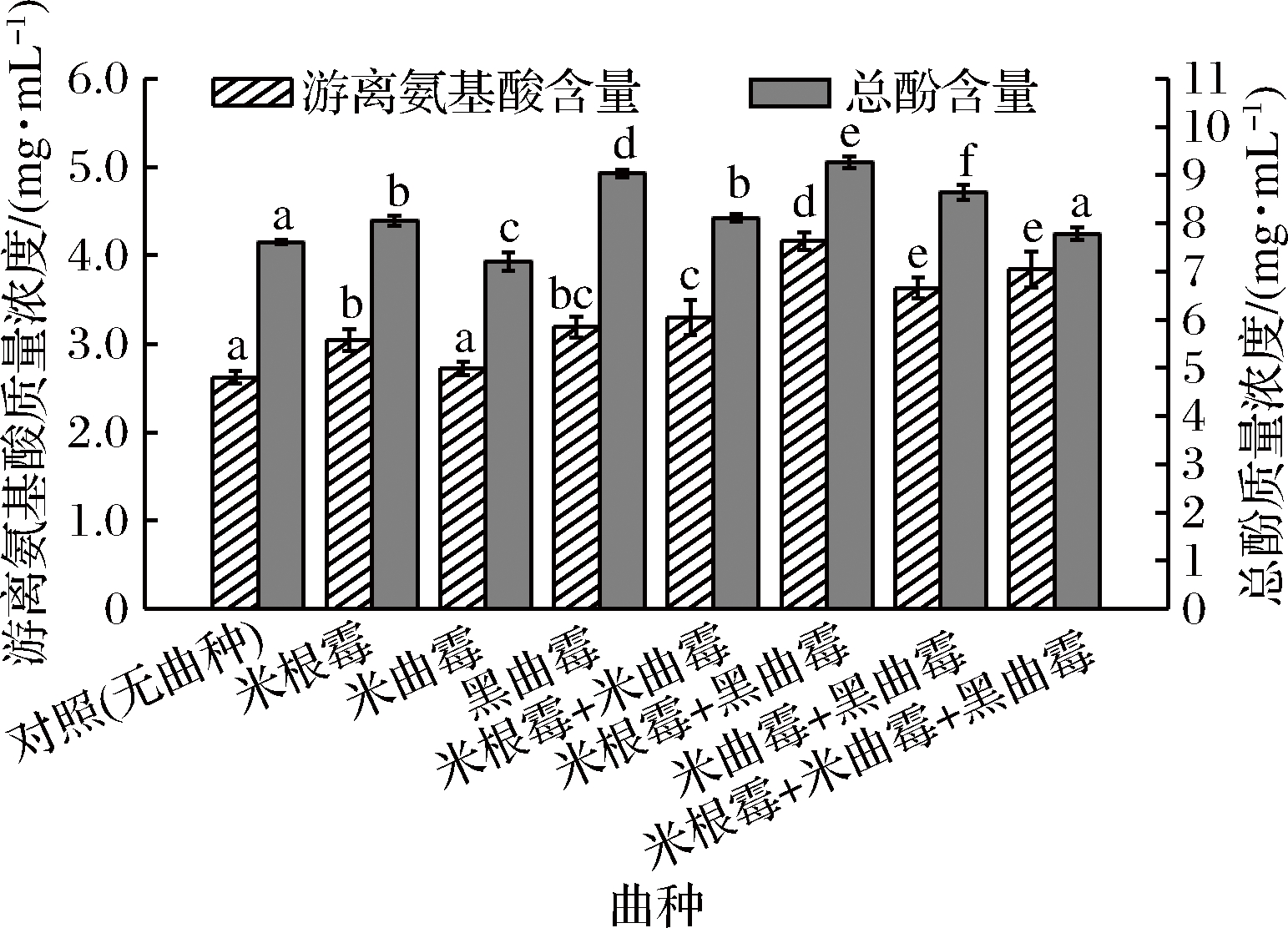
图1 发酵曲种对余甘子酵素游离氨基酸和总酚含量的影响
Fig.1 Effect of fermentation strains on free amino acid content and total phenol content of Phyllanthus
emblica jiaosu
注:图中同一指标的不同小写字母表示两者差异显著(P<0.05)。下同。
由图1可知,米根霉+黑曲霉发酵得到的余甘子酵素的游离氨基酸含量最高,为4.16 mg/mL,显著高于对照组和其他曲种(P<0.05);在总酚含量上,米根霉+黑曲霉的发酵得到的余甘子酵素最高,为9.27 mg/mL,米曲霉的最低,为7.20 mg/mL,米根霉+黑曲霉发酵得到的余甘子酵素的总酚含量与其他组之间均差异显著(P<0.05)。因此,米根霉+黑曲霉的发酵效果最好,确定为最佳的发酵曲种。
2.1.2 前发酵时间对余甘子酵素游离氨基酸和总酚含量的影响
在固定发酵曲种为米根霉+黑曲霉、主发酵45 d、各曲种的添加量为质量分数0.75%的条件下,改变前发酵时间,测定主发酵45 d后的余甘子酵素的游离氨基酸和总酚含量,结果见图2。
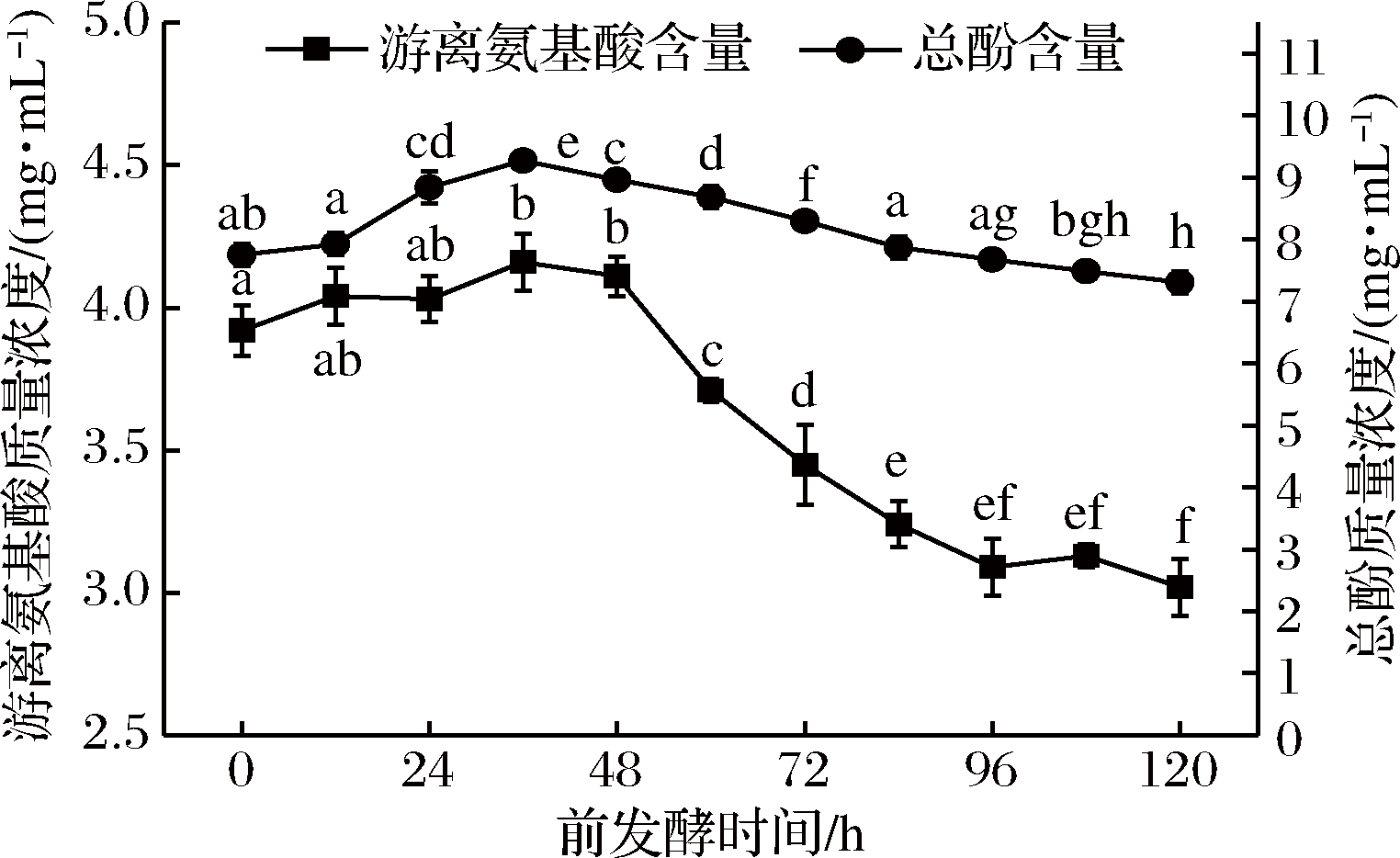
图2 前发酵时间对余甘子酵素游离氨基酸和总酚含量的影响
Fig.2 Effect of pre-fermentation time on free amino acid content and total phenol content of Phyllanthusemblica jiaosu
由图2可知,游离氨基酸含量和总酚含量的变化趋势均为先上升后下降,余甘子酵素在前发酵为36 h,再经过主发酵45 d后,其中的游离氨基酸含量达到最高值4.16 mg/mL,总酚含量也达到最高值9.27 mg/mL。这可能是因为米根霉和黑曲霉产生了具有破坏植物细胞结构、水解蛋白质和结合态多酚作用的果胶酶、纤维素酶和蛋白酶等,使果实细胞中的游离氨基酸和游离多酚得以释放,以及水解了蛋白质和结合态多酚,所以两者的含量均上升;另一方面,可能因为随着前发酵时间增加,微生物生长过量,对游离氨基酸和总酚的消耗大于生成[36-38],导致当前发酵超过36 h后,经过45 d主发酵得到的余甘子酵素的游离氨基酸和总酚含量都开始下降。因此最佳前发酵时间为36 h。
2.1.3 主发酵时间对余甘子酵素游离氨基酸和总酚含量的影响
在固定发酵曲种为米根霉+黑曲霉、前发酵36 h、各曲种的添加量为质量分数0.75%的条件下,改变主发酵时间,测定主发酵结束后的余甘子酵素的游离氨基酸和总酚含量,结果见图3。
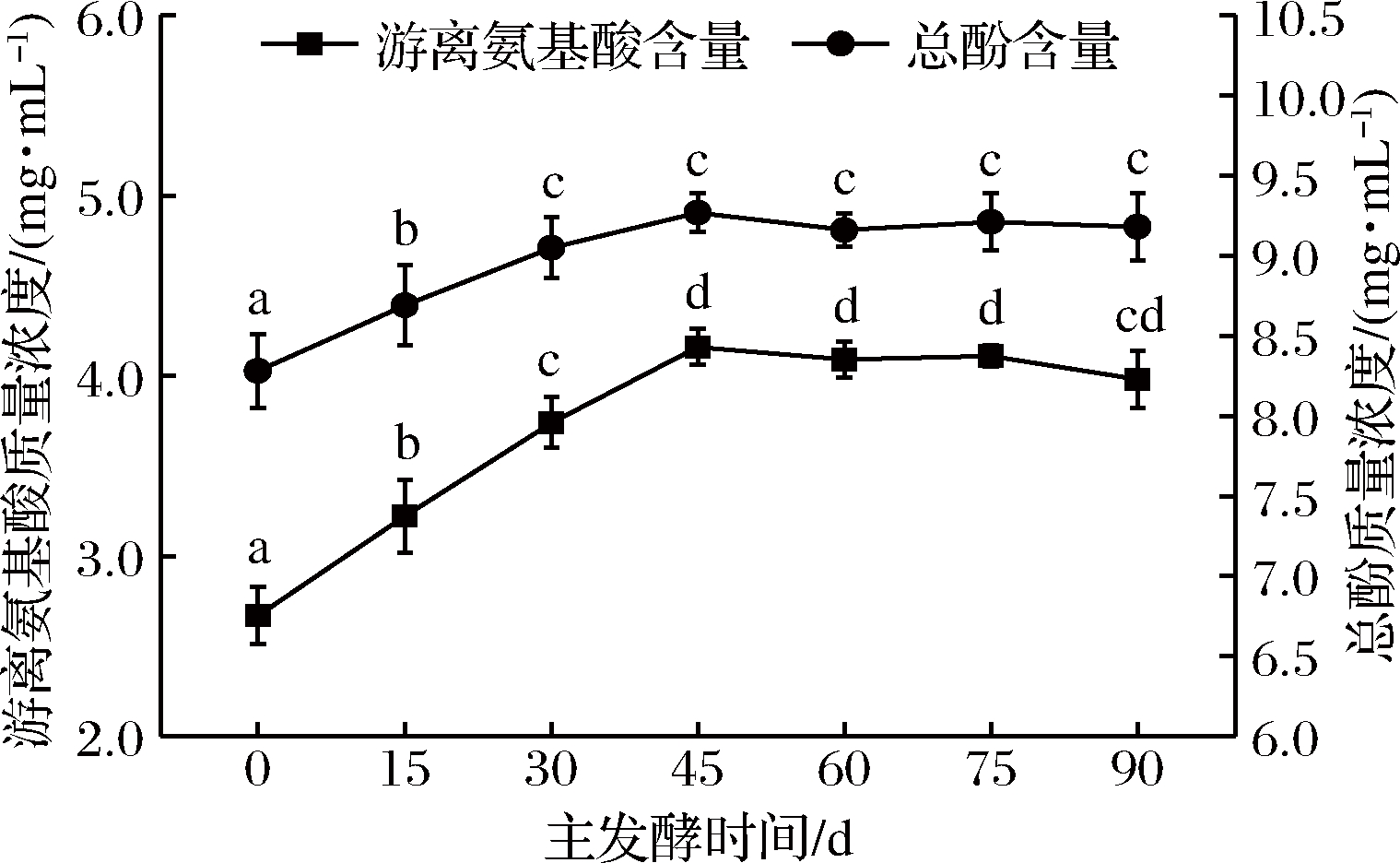
图3 主发酵时间对余甘子酵素游离氨基酸和总酚含量的影响
Fig.3 Effect of main fermentation time on free amino acid content and total phenol content of Phyllanthusemblica jiaosu
如图3所示,在经过36 h前发酵后,随着主发酵时间增加,余甘子酵素的游离氨基酸和总酚含量显著上升(P<0.05),到45 d时最高,分别为4.16 mg/mL和9.27 mg/mL,这可能是因为前发酵所产生的蛋白酶和果胶酶等在主发酵期间继续对原辅料作用。主发酵时间继续增加,游离氨基酸和总酚含量变化无显著性差异,保持在较高的水平,出现此现象的原因可能是45 d后原辅料中的游离氨基酸和多酚已经在酶的作用下被释放完全。因此最适的主发酵时间定为45 d。
2.1.4 黑曲霉曲种添加量对余甘子酵素游离氨基酸和总酚含量的影响
黑曲霉可产生蛋白酶、果胶酶和纤维素酶等,这些酶具有水解蛋白质、果胶质和纤维素等作用[39]。在固定发酵曲种为米根霉+黑曲霉、前发酵36 h,主发酵45 d、米根霉曲种添加量为质量分数0.75%的条件下,改变黑曲霉曲种添加量,测定主发酵45 d后的余甘子酵素的游离氨基酸和总酚含量,结果见图4。

图4 黑曲霉曲种添加量对余甘子酵素游离氨基酸和总酚含量的影响
Fig.4 Effect of the addition amount of Aspergillus niger on free amino acid content and total phenol content ofPhyllanthus emblica jiaosu
由图4可知,当黑曲霉曲种添加量由质量分数0.25%增加至0.75%时,余甘子酵素的游离氨基酸含量由2.05 mg/mL上升至4.16 mg/mL(P<0.05),总酚含量由8.96 mg/mL上升至9.27 mg/mL(P<0.05)。当继续添加黑曲霉曲种时,可能是因为发酵体系内存活的微生物数量有所上升,其维持生长需要消耗的营养物质也随之增加,从而导致游离氨基酸和总酚含量的总体趋势下降。所以,最佳的黑曲霉曲种添加量为质量分数0.75%。
2.1.5 米根霉曲种添加量对余甘子酵素游离氨基酸和总酚含量的影响
米根霉可产生糖化酶、蔗糖酶和蛋白酶等,能够将淀粉、蔗糖、蛋白质等大分子有机物酶解为葡萄糖、氨基酸等小分子物质[39]。在固定发酵曲种为米根霉+黑曲霉、前发酵36 h,主发酵45 d、黑曲霉曲种添加量为质量分数0.75%的条件下,改变米根霉曲种添加量,测定主发酵45 d后的余甘子酵素的游离氨基酸和总酚含量,结果见图5。
如图5所示,随着米根霉曲种添加量增加,余甘子酵素的游离氨基酸含量由3.70 mg/mL增加至4.16 mg/mL(P<0.05),总酚含量由8.54 mg/mL增加至9.27 mg/mL(P<0.05),此时米根霉曲种添加量为质量分数0.75%。
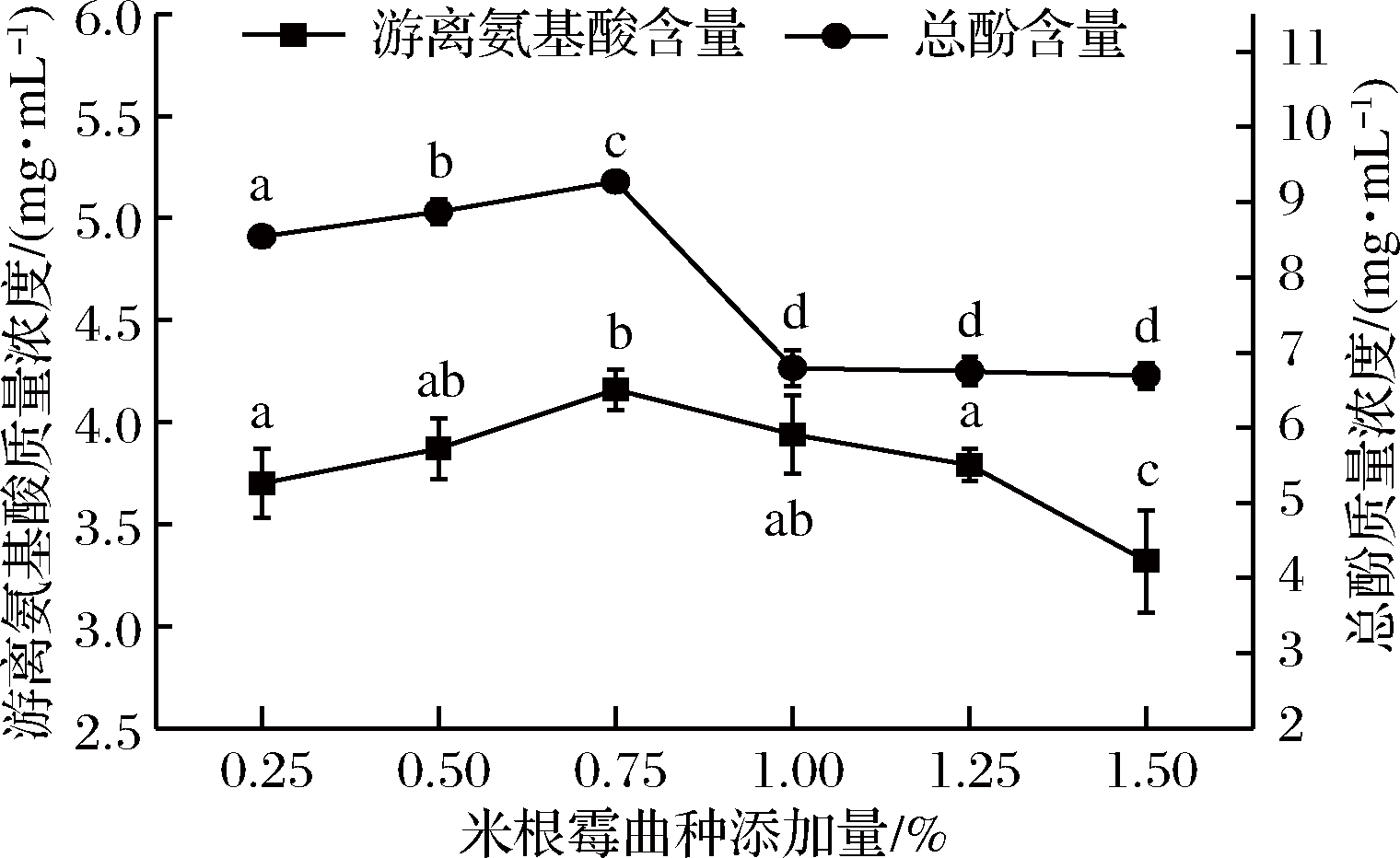
图5 米根霉曲种添加量对余甘子酵素游离氨基酸和总酚含量的影响
Fig.5 Effect of the addition amount of Rhizopus oryzae on free amino acid content and total phenol content ofPhyllanthus emblica jiaosu
当继续添加米根霉曲种,游离氨基酸含量开始逐渐下降,总酚含量则显著降低(P<0.05)后趋于平稳,推测其原因可能与继续添加黑曲霉曲种相似。所以,确定最佳的米根霉曲种添加量为质量分数0.75%。
2.2 响应面优化试验结果与分析
2.2.1 响应面试验设计与结果
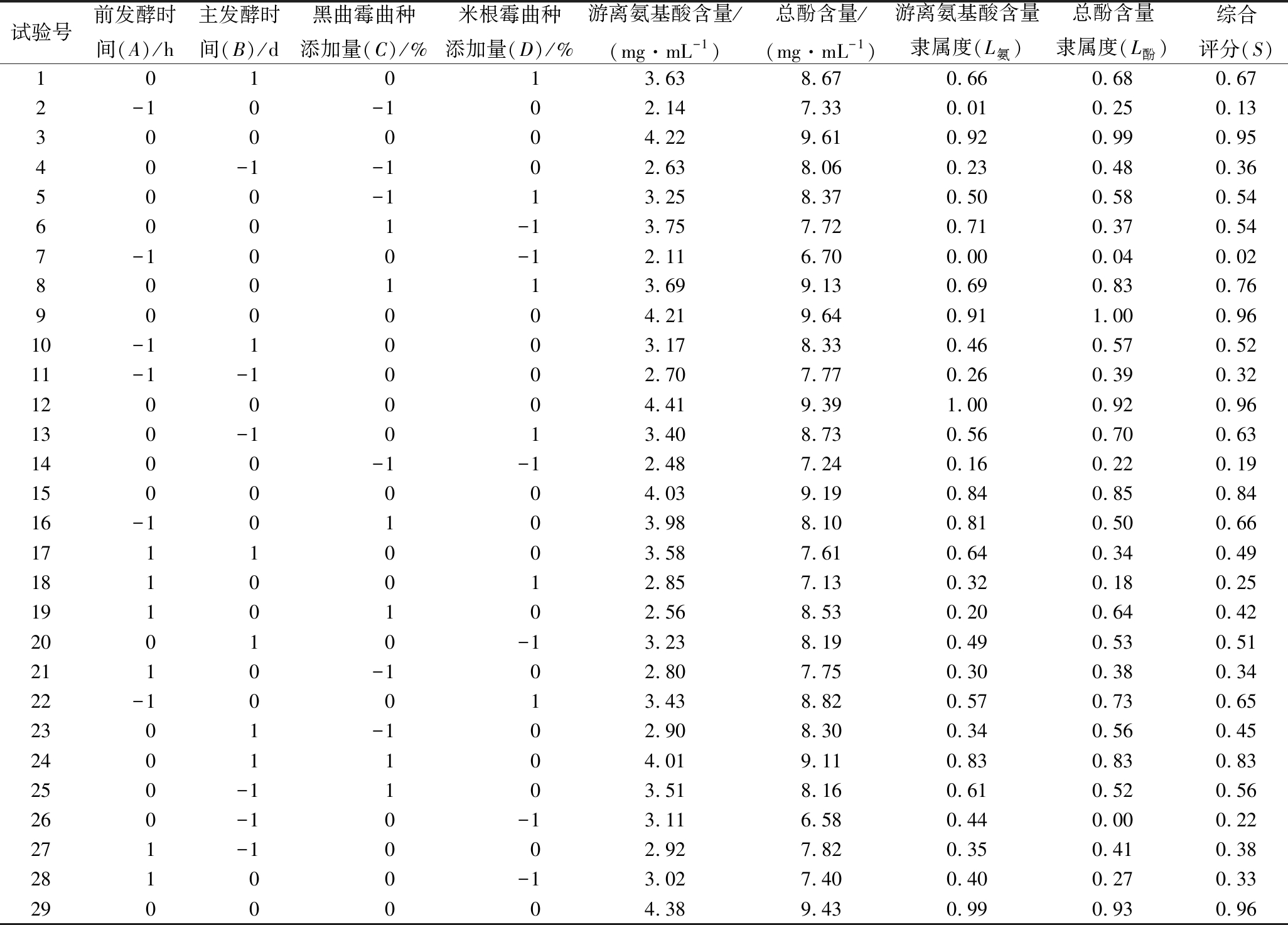
根据表1的Box-Behnken试验因素水平设计,共制作了29组余甘子酵素,测定其游离氨基酸含量和总酚含量,并计算综合评分。相关结果如表3所示。
利用Design-Expert软件对表3的数据进行分析,以综合评分为响应值进行二次多项回归拟合,得到综合评分(S)对前发酵时间(A)、主发酵时间(B)、黑曲霉曲种添加量(C)、米根霉曲种添加量(D)的回归模型方程:
S=0.93-0.007 5A+0.083B+0.15C+0.14D-0.021AB-0.11AC-0.18AD+0.042BC-0.062BD-0.034CD-0.35A2-0.17B2-0.19C2-0.25D2
表3 Box-Behnken试验设计及结果
Table 3 Box-Behnken design and results
试验号前发酵时间(A)/h主发酵时间(B)/d黑曲霉曲种添加量(C)/%米根霉曲种添加量(D)/%游离氨基酸含量/(mg·mL-1)总酚含量/(mg·mL-1)游离氨基酸含量隶属度(L氨)总酚含量隶属度(L酚)综合评分(S)101013.638.670.660.680.672-10-102.147.330.010.250.13300004.229.610.920.990.9540-1-102.638.060.230.480.36500-113.258.370.500.580.546001-13.757.720.710.370.547-100-12.116.700.000.040.02800113.699.130.690.830.76900004.219.640.911.000.9610-11003.178.330.460.570.5211-1-1002.707.770.260.390.321200004.419.391.000.920.96130-1013.408.730.560.700.631400-1-12.487.240.160.220.191500004.039.190.840.850.8416-10103.988.100.810.500.661711003.587.610.640.340.491810012.857.130.320.180.251910102.568.530.200.640.4220010-13.238.190.490.530.512110-102.807.750.300.380.3422-10013.438.820.570.730.652301-102.908.300.340.560.452401104.019.110.830.830.83250-1103.518.160.610.520.56260-10-13.116.580.440.000.22271-1002.927.820.350.410.3828100-13.027.400.400.270.332900004.389.430.990.930.96
2.2.2 方差分析
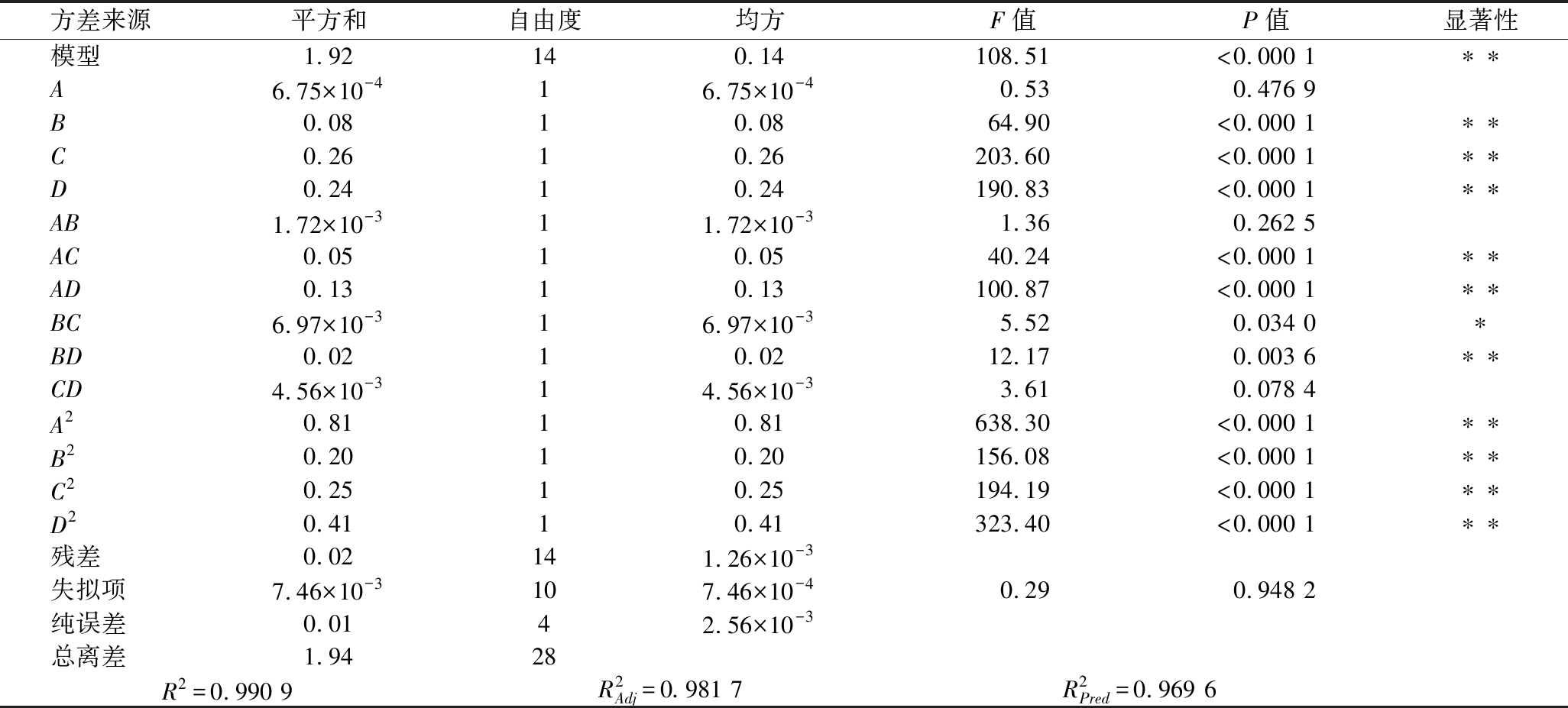
对得到的回归模型进行方差分析,结果如表4所示。
由表4可知,模型P<0.000 1,说明该模型极其显著;失拟项不显著(P>0.05),说明该模型拟合得较好;R2=0.990 9,说明该模型对综合评分的预测值与实际值的拟合程度较高;![]() 说明该模型能解释98.17%响应值的变化;
说明该模型能解释98.17%响应值的变化;![]() 说明该模型的预测能力好。在所有作用因素中,对综合评分影响显著(P<0.05)的因素有:BC;影响极其显著(P<0.01)的因素有:B、C、D、AC、AD、BD、A2、B2、C2、D2。4个单因素对综合评分的影响顺序依次为C>D>B>A。
说明该模型的预测能力好。在所有作用因素中,对综合评分影响显著(P<0.05)的因素有:BC;影响极其显著(P<0.01)的因素有:B、C、D、AC、AD、BD、A2、B2、C2、D2。4个单因素对综合评分的影响顺序依次为C>D>B>A。
表4 回归模型方差分析
Table 4 Variance analysis of regression model
方差来源平方和自由度均方F值P值显著性模型1.92140.14108.51<0.000 1∗∗A6.75×10-416.75×10-40.530.476 9B0.0810.0864.90<0.000 1∗∗C0.2610.26203.60<0.000 1∗∗D0.2410.24190.83<0.000 1∗∗AB1.72×10-311.72×10-31.360.262 5AC0.0510.0540.24<0.000 1∗∗AD0.1310.13100.87<0.000 1∗∗BC6.97×10-316.97×10-35.520.034 0∗BD0.0210.0212.170.003 6∗∗CD4.56×10-314.56×10-33.610.078 4A20.8110.81638.30<0.000 1∗∗B20.2010.20156.08<0.000 1∗∗C20.2510.25194.19<0.000 1∗∗D20.4110.41323.40<0.000 1∗∗残差0.02141.26×10-3失拟项7.46×10-3107.46×10-40.290.948 2纯误差0.0142.56×10-3总离差1.9428R2=0.990 9R2Adj=0.981 7R2Pred=0.969 6
注:*表示差异显著(P<0.05);**表示差异极显著(P<0.01)。
2.2.3 最优发酵工艺条件确定及验证
通过Design-Expert软件的进一步分析,得到了最优的发酵工艺条件为:黑曲霉曲种添加量0.86%,米根霉曲种添加量0.82%,前发酵34.12 h,主发酵48.71 d,此时余甘子酵素的综合评分为0.99。为了验证最优工艺的准确性,考虑实际情况,将发酵条件修正为:前发酵时间34 h,主发酵时间49 d,黑曲霉曲种添加量0.85%,米根霉曲种添加量0.80%。以修正后的工艺条件进行3次平行验证试验,结果取平均值,得到余甘子酵素的游离氨基酸含量为4.36 mg/mL,总酚含量为9.52 mg/mL,综合评分为0.97,接近模型预测值。
2.3 余甘子酵素的理化特性及感官评价结果
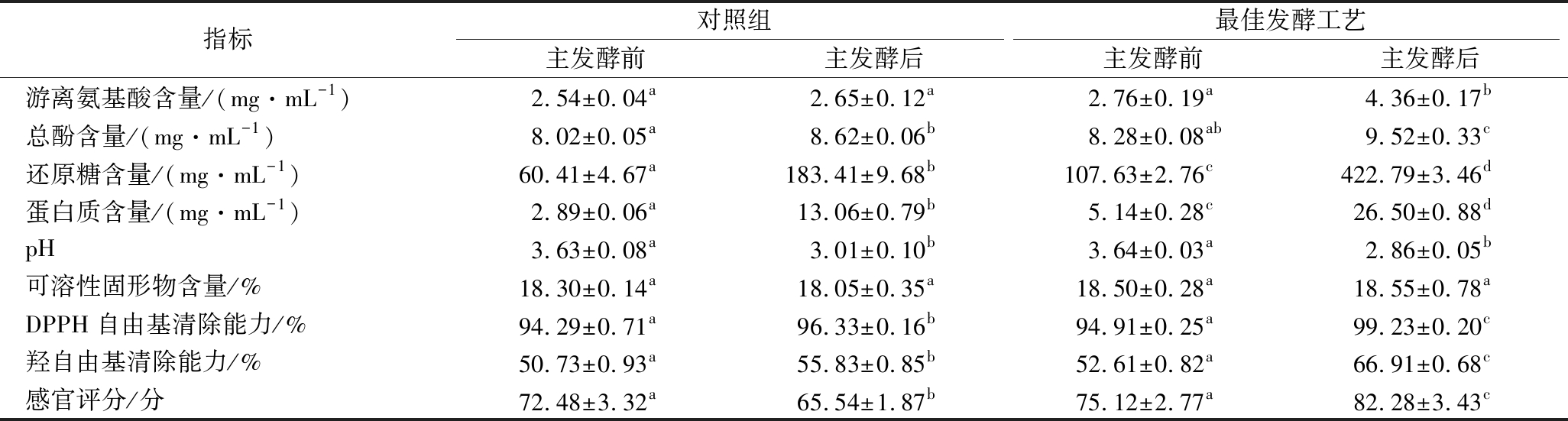
根据2.2.3修正后的最佳工艺条件,测定对照组(无曲种)和最佳发酵工艺各自主发酵前后所得的余甘子酵素的理化特性和感官评分,进一步验证最佳发酵工艺的优劣。结果见表5。
表5 对照组与最佳发酵工艺各自主发酵前后所得余甘子酵素的理化特性和感官评分
Table 5 Physicochemical properties and sensory scores of Phyllanthus emblica jiaosu obtained before and after the mainfermentation in the control group and the optimal fermentation process
指标对照组最佳发酵工艺主发酵前主发酵后主发酵前主发酵后游离氨基酸含量/(mg·mL-1)2.54±0.04a2.65±0.12a2.76±0.19a4.36±0.17b总酚含量/(mg·mL-1)8.02±0.05a8.62±0.06b8.28±0.08ab9.52±0.33c还原糖含量/(mg·mL-1)60.41±4.67a183.41±9.68b107.63±2.76c422.79±3.46d蛋白质含量/(mg·mL-1)2.89±0.06a13.06±0.79b5.14±0.28c26.50±0.88dpH3.63±0.08a3.01±0.10b3.64±0.03a2.86±0.05b可溶性固形物含量/%18.30±0.14a18.05±0.35a18.50±0.28a18.55±0.78aDPPH自由基清除能力/%94.29±0.71a96.33±0.16b94.91±0.25a99.23±0.20c羟自由基清除能力/%50.73±0.93a55.83±0.85b52.61±0.82a66.91±0.68c感官评分/分72.48±3.32a65.54±1.87b75.12±2.77a82.28±3.43c
注:在同一指标中,字母相同表示无显著性差异(P>0.05),字母不同表示存在显著性差异(P<0.05)。
表5中的数据显示,与对照组相比,最佳发酵工艺主发酵后得到的余甘子酵素的游离氨基酸含量、总酚含量、还原糖含量、蛋白质含量、DPPH自由基清除能力、羟自由基清除能力和感官得分都显著高于对照组主发酵前、后得到的余甘子酵素(P<0.05),而最佳发酵工艺主发酵前得到的余甘子酵素的还原糖含量和蛋白质含量也显著高于对照组主发酵前得到的(P<0.05),这说明曲种的添加和前发酵对提高余甘子酵素中多种成分的含量和抗氧化性具有促进作用,这可能是因为米根霉和黑曲霉在前发酵期间产生了足够的果胶酶、纤维素酶、蛋白酶、蔗糖酶等,这些酶本身既是蛋白质,又能作用于相应的底物,破坏余甘子果实细胞结构和水解大分子物质,使蛋白质和总酚等物质的含量升高。在最佳发酵工艺中,除pH和可溶性固形物含量之外,余甘子酵素的其他指标在经过主发酵后对比未经主发酵的均得到了明显改善(P<0.05),说明主发酵阶段对获得品质良好的余甘子酵素是必要的。无论是对照组还是最佳发酵工艺,主发酵后的余甘子酵素的pH值均降低,这可能是发酵过程中微生物产酸导致的。
氨基酸具有良好的营养价值和生理功能,可参与物质的合成、转化、提供能量等,对机体代谢具有重要作用,同时也是影响食品风味和感官的重要成分[40-41]。酚类物质是重要的生物活性物质之一,有较强的抗氧化活性,因其很容易给出1个氢离子并通过共振杂化而稳定,所以自由基清除能力很高[14],此外,酚类物质也是挥发性风味物质中的一类。本实验最优发酵工艺条件制得的余甘子酵素含游离氨基酸4.36 mg/mL、总酚9.52 mg/mL,远高于其他研究者开发的同类发酵食品,如杨志鹏等[42]的海棠果酵素含氨基酸1.83 mg/mL和多酚0.573 mg/mL;蒋增良[14]的树莓、蓝莓和葡萄酵素的总酚含量最大值依次为2.813、2.308和1.739 mg/mL,陈犇等[43]的栀子花酵素营养液含游离氨基酸0.42 mg/mL和总酚1.83 mg/mL,玉兰花酵素营养液含游离氨基酸0.44 mg/mL和总酚2.68 mg/mL;李杰等[44]的核桃青皮果蔬酵素含多酚0.188 mg/mL。所以本实验最优发酵工艺条件制得的余甘子酵素含有丰富的游离氨基酸和酚类物质,营养价值高。
3 结论
本研究先通过单因素和响应面优化试验及修正,确定了新型余甘子酵素的最佳发酵工艺条件:原料∶糖水(ω=40%)=1∶1,米根霉曲种添加量0.80%,黑曲霉曲种添加量0.85%,前发酵34 h,主发酵49 d。其中在响应面设计及分析中,得到主发酵时间、黑曲霉曲种添加量和米根霉曲种添加量对产品的综合评分均影响极显著(P<0.01),影响程度由高到低依次为黑曲霉曲种添加量>米根霉曲种添加量>主发酵时间>前发酵时间;修正条件后的余甘子酵素的综合评分为0.97(满分为1)。然后进一步通过分别比较对照组与最佳发酵工艺制得的新型余甘子酵素、最佳发酵工艺制得的新型余甘子酵素与其他植物类发酵食品,验证了此最佳发酵工艺是比较好的工艺,可制作出品质良好的新型余甘子酵素饮品,其含有游离氨基酸4.36 mg/mL,总酚9.52 mg/mL,还原糖422.79 mg/mL,蛋白质26.50 mg/mL,可溶性固形物18.55%,pH为2.86,DPPH自由基清除能力和羟自由基清除能力分别为99.23%和66.91%,感官得分为82.28分,产品澄清透明呈亮黄色,气味清香,口感柔顺、酸甜可口,符合市场需求,发展前景良好。此外,本研究结果显示了新型余甘子酵素的游离氨基酸和总酚含量发生了较明显的改变,这2类物质与食品的风味密切相关,因此对本产品在发酵过程中其游离氨基酸和酚类物质的种类和含量的详细变化还有待更进一步的研究。
[1] 徐义侠.余甘子化学成分及总酚提取工艺研究[D].北京:北京中医药大学,2009.
[2] 罗维.余甘子干果活性成分的分离鉴定与生理活性研究[D].广州:华南理工大学,2010.
[3] 陈智毅,刘学铭,吴继军,等.余甘子生物学特性及营养成分[J].中国南方果树,2003,32(6):71-73.
[4] 李明玺,黄卫锋,姚亮亮,等.余甘子提取物降血糖活性及其主要成分研究[J].现代食品科技,2017,33(9):96-101.
[5] 吴雪辉,谢治芳,黄永芳.余甘子的化学成分和保健功能作用[J].中国野生植物资源,2003,22(6):69-71.
[6] 孙忠文,刘汉清,黄一平,等.藏药余甘子中总鞣质和没食子酸的含量测定[J].现代中药研究与实践,2010,24(3):60-62.
[7] 杨顺楷,杨亚力,杨维力,等.余甘子资源植物的研究与开发进展[J].应用与环境生物学报,2008,14(6):846-854.
[8] 张福平.余甘子的营养价值[J].中国食物与营养,2004 (1):25.
[9] 李昌玲.余甘子的药理研究[J].药学进展,2001,25(4):210-213.
[10] 中国生物发酵产业协会.T/CBFIA 08001-2016 酵素产品分类导则[S].北京:中国标准出版社,2016.
[11] OKADA H, KAWAZOE N, YAMAMORI A, et al.Structural analysis and synthesis of oligosaccharides isolated from fermented beverage of plant extract[J].Journal of Applied Glycoscience,2008,55(2):143-148.
[12] 李杰.酵素饮品质量控制标准研究[D].昆明:昆明理工大学,2016.
[13] 杨培青.蓝莓果渣酵素制备工艺的研究[D].沈阳:沈阳农业大学,2016.
[14] 蒋增良.天然微生物酵素发酵机理、代谢过程及生物活性研究[D].杭州:浙江理工大学,2013.
[15] 张静雯.组合菌发酵过程中产生的微生物酵素及其生物活性研究[D].武汉:武汉轻工大学,2015.
[16] 赵芳芳,莫雅雯,蒋增良,等.功能性微生物酵素产品的研究进展[J].食品与发酵工业,2016,42(7):283-287.
[17] 朱继元.天然酵素在运动食品中的应用及市场前景分析[J].食品研究与开发,2016,37(18):209-212.
[18] 刘加友,王振斌.微生物酵素食品研究进展[J].食品与发酵工业,2016,42(1):273-276.
[19] 刘祺,陈朝银,赵声兰.酵素化妆品的研发与展望[J].药物生物技术,2016,23(5):462-466.
[20] 敖梅英,王鑫,范友隆,等.食用型酵素产品的研究进展[J].安徽农业科学,2016,44(30):64-66;145.
[21] 王子丹.微生物酵素的研究进展[J].农业科技与装备,2015(8):67-68.
[22] 毛建卫,吴元锋,方晟.微生物酵素研究进展[J].发酵科技通讯,2010,39(3):42-44.
[23] 李文德.应用于食醋生产的糖化麸曲各制作工序设备与工艺操作[J].中国调味品,2002(3):26-29;33.
[24] 曾洁,郑华艳.果酒米酒生产[M].北京:化学工业出版社,2014:45-48.
[25] 何国庆,贾英民,丁立孝.食品微生物学[M].第2版.北京:中国农业大学出版社,2009:110-114.
[26] 海金萍,刘钰娜,邱松山.三华李果酒发酵工艺的优化及香气成分分析[J].食品科学,2016,37(23):222-229.
[27] 吴灿,夏延斌,唐鑫.响应面法优化莲子黄酒的发酵工艺条件[J].现代食品科技,2013,29(7):1 675-1 679.
[28] 崔国庭,王缎,刘向丽,等.响应面法优化苹果酵素的发酵工艺及其生物活性初探[J].食品工业,2018,39(6):187-192.
[29] 张黎骅,张文,吕珍珍,等.响应面法优化酒糟微波间歇干燥工艺[J].农业工程学报,2011,27(3):369-374.
[30] 彭真汾,王威,谢倩,等.橄榄果实游离氨基酸测定方法的优化[J].食品工业科技,2017,38(22):263-267.
[31] SECZYK  ,
,![]() M,GAWLIKDZIKI U.Effect of carob (Ceratonia siliqua L.) flour on the antioxidant potential,nutritional quality,and sensory characteristics of fortified durum wheat pasta[J].Food Chemistry,2016,194(B11):637-642.
M,GAWLIKDZIKI U.Effect of carob (Ceratonia siliqua L.) flour on the antioxidant potential,nutritional quality,and sensory characteristics of fortified durum wheat pasta[J].Food Chemistry,2016,194(B11):637-642.
[32] 吴敏.包装和贮藏条件对荔枝果汁品质的影响研究[D].广州:华南农业大学,2016.
[33] 国家食品药品监督管理总局.GB 5009.5—2016 食品中蛋白质的测定[S].北京:中国标准出版社,2016.
[34] 管章瑞,田裕,赵娜,等.蓝莓酵素发酵过程中的抗氧化活性变化研究[J].现代食品科技,2016,32(12):74-80.
[35] 蒋增良,毛建卫,黄俊,等.蓝莓酵素在天然发酵过程中抗氧化性能的变化[J].食品工业科技,2013,34(2):194-197;201.
[36] KAUR C,KAPOOR HC.Antioxidants in fruits and vegetables-the millennium’s health[J].International Journal of Food Science & Technology,2010,36(7):703-725.
[37] MUTABARUKA R,HAIRIAH K,CADISCH G.Microbial degradation of hydrolysable and condensed tannin polyphenol-protein complexes in soils from different land-use histories[J].Soil Biology and Biochemistry,2007,39(7):1 479-1 492.
[38] 张晓松,孙艳梅,胡振生,等.都柿果酒在酿制过程中总酚和花色苷含量和抗氧化活性[J].东北农业大学学报,2010,41(3):120-124.
[39] 郭勇.酶的生产与应用[M].北京:化学工业出版社,2003:45-47.
[40] 程勇杰,陈小伟,张沙沙,等.柘树植物酵素中氨基酸分析及抗氧化性能研究[J].食品工业科技,2018,39(6):1-7;12.
[41] 刘姗,杨柳,何述栋,等.杏鲍菇料酒的研制及风味研究[J].食品与发酵工业,2019,45(4):131-136.
[42] 杨志鹏,王婷,袁峰,等.海棠果酵素产品开发及其生物活性研究[J].中国调味品,2018,43(1):48-51;83.
[43] 陈犇,方晟,张佳城,等.栀子花和玉兰花酵素营养液发酵过程中营养成分的动态分析[J].农业工程,2018,8(3):122-126.
[44] 李杰,赵声兰,陈朝银.核桃青皮果蔬酵素的成分组成及体外抗氧化活性研究[J].食品工业科技,2016,37(10):117-122.