真空低温烹饪技术(sous vide cooking, SVC)源于法国,是19世纪70年代中期Georges Pralus为Troisgros餐厅研发的一种新派烹饪方式,即将食物原料在热稳定真空装置中以可控温度与时间进行蒸煮加热[1]。低温烹饪温度一般控制在50~80 ℃,在低温环境下设定较长时间去加热食材,可消灭绝大部分有害菌。RINALDI等[2]研究表明,60~70 ℃的加热温度能抑制大部分细菌的生长,适用于鱼肉、牛肉、羊肉的烹饪加工,71~80 ℃的加热温度则适用于禽类和猪肉的加工。
牛肉是世界三大肉类消耗品之一,含有丰富的蛋白质、肽类及氨基酸,相比于其他肉类更接近人体摄入营养素的需求[3]。传统的高温加热不仅造成牛肉的口感下降,还易造成各类风味、营养物质的严重损失,而真空低温技术在基于牛肉安全烹饪温度的基础上,采用真空包装隔绝氧气,既可有效保证食材内外温度的均匀性,又可确保牛肉食用的安全性。同时,真空低温烹饪能够极大限度地减少食材的质量损失及水分流失,较好地保留住食材本身的风味与营养,使烹饪后的食物具有更好的口感,符合现代人们对膳食品质的高要求[4]。
本试验以澳洲西冷牛肉为研究对象,将其真空处理后分别在不同低温环境下加热,探究真空低温烹饪对牛肉微观结构与理化性质的影响,以期为我国传统肉制品的加工技术提供新思路与方向。
1 材料与方法
1.1 材料与试剂
澳洲冰鲜牛西冷(婆罗门牛),泰氏澳洲宾利市有限公司;多聚甲醛、无水乙醇、二甲苯、中性树胶、伊红染液、苏木精染液均为分析纯,国药集团化学试剂有限公司;盐酸、冰醋酸均为分析纯,南京博尔迪生物科技有限公司。
1.2 仪器与设备
MK-301型热电偶接触式测温仪,杭州美控自动化技术有限公司;GTR16-2型高速冷冻离心机,北京时代北利离心机有限公司;TMS-Pro物性测定仪,美国FTC公司;SC-80C型全自动色差计,北京康光光学仪器有限公司;HH-6型电热恒温水浴锅,山东博科生物产业有限公司;BS210S(1/1000)型电子天平,北京赛多斯仪器系统有限公司;ZH型真空包装机,上海铸衡电子科技有限公司;MEV冷冻切片机,德国SLEE公司;Optika XDS-3FL4型倒置荧光显微镜,上海长方光学仪器有限公司;KD-BM型石蜡包埋机、KD-BL型样品冷却台,浙江科迪仪器设备有限公司;KPJ-1A型展片机、ZPJ-1A型烤片机,天津天利航空机电有限公司。
1.3 试验方法
1.3.1 样品处理
剔除西冷牛肉表面筋腱、肌膜,将其切割成规格为5 cm×5 cm×1.5 cm的整块肉样。将肉样分为5组,每组6块。先将热电偶温度探头插入未经真空包装的样品中心位置,按组分别置于60、65、70、75和100 ℃的恒温水浴锅中加热,密封袋开口朝上,开始加热并计时,实时监控样品的中心温度变化,记录样品中心温度分别达到对应水浴温度时所需的加热时间,每个条件重复3次,取平均值。后将测试肉样真空包装后,利用每组样品达到对应中心温度所需时间进行水浴加热,当肉样中心温度达到60 ℃(加热28~32 min)、65 ℃(加热46~50 min)、70 ℃(加热60~65min)、75 ℃(加热82~86 min)和100 ℃(加热165~170 min)时取出肉样,冷却至室温(20±2) ℃,待测。
1.3.2 微观结构
1.3.2.1 石蜡切片制备
取出已固定好的牛肉组织,切割成2.5 mm×2.5 mm×3 mm大小,进行组织脱水,包埋和切片。
具体步骤:70%乙醇3 h→80%乙醇45 min→95%乙醇Ⅰ 40 min→95%乙醇Ⅱ 40 min→无水乙醇Ⅰ 40 min→无水乙醇Ⅱ 30 min→二甲苯Ⅰ 30 min→二甲苯Ⅱ 40 min→石蜡Ⅰ 1 h→石蜡Ⅱ 1 h→石蜡Ⅲ 1 h。
包埋:将熔化的石蜡倒入包埋框再将组织块放入,放入时不能有气泡,冷却30 min。
常规石蜡切片:厚度4 μm,连续切片。
烤片:60 ℃烤片30 min,室温保存。
1.3.2.2 HE染色和封片
采用组织学HEMATOXYLIN & EOSIN (H.E.)[5]染色方法,具体步骤:
(1)选取待染色切片,62 ℃烤片1 h。
(2)对切片进行脱蜡,复水。
二甲苯Ⅰ 10 min→二甲苯Ⅱ 10 min→二甲苯:无水乙醇(1∶1) 10 min→无水乙醇Ⅰ 5 min→无水乙醇Ⅱ 5 min→95%乙醇Ⅰ 2 min→95%乙醇Ⅱ 2 min→80%乙醇2 min→70%乙醇2 min→双蒸水5 min。
(3)苏木精液染色
苏木精液染色4 min,流水冲洗2 min,1%盐酸酒精溶液分色1~3 s,流水冲洗至返蓝,镜检。
(4)伊红液染色
伊红液染色90 s,蒸馏水稍洗,镜检。
(5)脱水、透明、封片
95%乙醇Ⅰ 30 s→95%乙醇Ⅱ 1 min→无水乙醇 3 min→二甲苯:无水乙醇(1∶1) 3 min→二甲苯Ⅰ 5 min→二甲苯Ⅱ 5 min→中性树胶封片。
1.3.3 理化性质
1.3.3.1 质构特性
采用TMS-Pro物质分析仪,对牛肉样品的硬度、弹性、咀嚼性、胶黏性、内聚性和黏附性进行测定。设置测定参数为:P/36.5柱形探头,测前速度60 mm/min,测试速度120 mm/min,测试形变量50%,触发力0.4 N。
1.3.3.2 嫩度
选用国产C-LM2型肌肉嫩度仪进行牛肉样品嫩度的测定。将肉样用直径1.27 cm的圆形取样器沿与肌纤维平行的方向钻取肉样(避开筋腱),孔样长度不少于2.5 cm,取样位置距离样品边缘不少于5 mm,两个取样的边缘间距不少于5 mm,剔除有明显缺陷的孔样,测定样品数量不少于3个,取样后立即测定。
1.3.3.3 色泽
将便携式色差仪经白板校准后,测定牛肉样品的L*值(亮度)、a*值(红度)、b*值(黄度)、C值(色彩强度)。将色差仪镜头垂直放置于牛肉表面测量,镜口紧贴肉面(避免漏光),记录显示屏上的各个值,每个样品选取不同的截面测定3次,测量时要有意识地将色差仪测定位置均匀,分布在牛肉肌肉表面,记录L*、a*、b*及C值(a*2+b*2)0.5。
1.3.3.4 pH
参照GB 5009.237—2016采用pH仪测定。取10.0 g牛肉样品剪碎,加入90 mL pH为7.0的蒸馏水浸泡30 min并不停搅拌,再用pH仪进行检测,待数值稳定后读数,测定样品数量不少于3个,取平均值。
1.3.3.5 持水力(WHC)
参照ZHOU YANZI等人[6]的离心方法,略作修改。取10.0 g左右的牛肉样品切碎放入离心管中,记为Wa,置于转速为7 000 r/min的冷冻离心机中离心20 min,离心结束后将肉样取出并用滤纸吸干样品表面水分并称重,记为Wb。按公式(1)计算牛肉的持水力:
![]()
(1)
1.3.3.6 消化特性
采用胃蛋白酶-胰蛋白酶两步消化法模拟胃及肠部的消化过程,测定牛肉蛋白质的胃消化率和胃肠总消化率。参照杨万君[7]、ESCUDERO等人[8]的方法,略作修改。先用蛋白质BCA试剂盒测定牛肉原始样品中的蛋白质含量,记为P0。准确称取5.0 g牛肉样品置于50 mL离心管中,每个消化样品同时准备2组,在每组样品中各加入20 mL双蒸水,在冰浴环境下首先于9 500 r/min条件匀浆2次,每次30 s,后于13 500 r/min条件匀浆2次,每次30 s,每次匀浆前需间隔30 s对样品进行冷却处理。匀浆结束后,用1 mol/L的HCl将待测样品pH调至2.0±0.1,以肉的质量为基准,按31.25∶1的比例加入0.16 g的胃蛋白酶(酶活≥400 U/g),将此混合样品置于37 ℃的恒温摇床中振摇2 h,反应结束后迅速加适量1 mol/L的NaOH溶液将酶解液pH调至7.5±0.1灭活胃蛋白酶,离心后弃上清液,用蛋白质BCA试剂盒测残渣中的蛋白含量,记为P1,求出胃消化率。另一组从摇床中取出,加适量1 mol/L的NaOH溶液灭活后,以肉的重量为基准,按50∶1的比例加入0.1 g胰蛋白酶(酶活≥1 645 U/g),将混合样品置于37 ℃的恒温摇床中继续振摇2 h,反应结束后迅速将消化样品置于95 ℃恒温水浴锅中加热5 min终止酶解反应,完成样品的消化。将消化好的样品于4 ℃冷冻离心机中离心20 min,离心力10 000×g,去除上清液,用蛋白质BCA试剂盒测定残渣的蛋白质含量,记为P2,求得胃肠总消化率。按公式(2)、(3)计算牛肉的体外消化率:
胃消化率![]()
(2)
胃肠总消化率![]()
(3)
1.3.4 数据处理
所有数据用平均值±标准差表示。采用Microsoft Office Excel 2003制表和绘图,SPSS 17.0全因子模型对测定结果进行显著性分析和方差分析。差异显著水平α为0.05。
2 结果与分析
2.1 真空低温烹饪对牛肉微观结构的影响
图1显示了不同真空低温加热条件下牛肉微观结构的变化情况,红色为肌纤维,白色为肌内膜,呈网状结构[9]。肌肉组织结构是影响肉品质的重要内在因素,结缔组织、肌纤维直径、密度、面积比例、肌节长度等都会影响肌肉品质[10],通常肌纤维越细、密度越大,肉质越嫩。由图1可知,在60~65 ℃低温加热条件下,牛肉组织结构较为松散,肌束膜与肌纤维分离度较小,肌肉细胞分布紧密,肉质较为细嫩。随着加热温度的升高,牛肉中由胶原纤维组成的肌膜与结缔组织进一步发生热收缩,原来卷曲包绕在肌纤维四周的肌内膜和肌束膜与肌纤维发生分离,肌纤维逐渐沿横、纵向伸长膨胀,肌纤维直径显著增大,肌束膜紧密包裹肌纤维,肌肉组织变得更加紧致,宏观上表现为肌肉嫩度的降低,在60~70 ℃低温加热的牛肉中尤为明显。由于加热温度的进一步升高,在75、100 ℃加热条件下,牛肉肌纤维继续拉伸膨胀,热溶性胶原纤维生成的膜结构内收缩张力逐渐消失[11],肌纤维之间产生孔洞,肌内膜发生断裂,肌纤维间隙不断增加,可溶性胶原蛋白和结缔组织发生液体化,随水分一起流出[12],肌纤维也因此变得松散与不规则。

a-60 ℃加热;b-65 ℃加热;c-70 ℃加热;d-75 ℃加热;e-100 ℃加热
图1 真空低温烹饪过程中牛肉微观结构的变化(× 400) Fig.1 The changes in microstructure of beef during
sous vide cooking (× 400)
2.2 真空低温烹饪对牛肉理化性质的影响
2.2.1 质构特性
由表1可知,牛肉的质构特性在不同真空低温加热条件下变化显著(P<0.05)。内聚性主要反映对食物咀嚼时的抵抗性指标[13],牛肉的内聚性在75 ℃加热条件下达到最高值,在60 ℃加热条件下最低。弹性主要反映食物在撤去外力后的恢复程度[14],60 ℃加热条件下牛肉的弹性最小,与其他温度组差异显著(P<0.05)。胶黏性是指将半固体食品咀嚼至可吞咽时需做的功[13],牛肉在65、70、100 ℃加热条件下的胶黏性无显著差异(P<0.05),与60、75 ℃差异显著(P<0.05)。咀嚼性是指将固体食品咀嚼至可吞咽时需做的功[15],牛肉在70与100 ℃加热条件下表现出较高的咀嚼性,在60 ℃加热条件下咀嚼性最低,比70 ℃时减少22.78 mJ。硬度主要表示牙齿间压迫样品所需的最大力,能较好反映出牛肉的嫩度[15]。60 ℃加热条件下牛肉的硬度最小,仅为46.00 N,到70 ℃升至71.63 N,随后又有明显减小(P<0.05)。综合看来,以常温100 ℃为对照,在真空低温加热过程中,牛肉的弹性、胶黏性、咀嚼性、硬度随温度的升高呈先增大后减小趋势,分别在60、70 ℃加热条件下有极小值和极大值,主要与肌原蛋白在60~70 ℃加热过程中逐渐变性并收缩有关。已知弹性、硬度和咀嚼性对产品的综合评价影响最大[16],结果显示60、65 ℃加热条件下的牛肉具有较好的质构特性。
表1 真空低温烹饪过程中牛肉质构特性的变化
Table 1 The changes in texture properties of beef during sous vide cooking

温度/℃内聚性弹性/mm胶黏性/N咀嚼性/mJ硬度/N1000.37±0.01b3.59±0.27a32.03±0.91a75.13±4.62a55.80±3.22b600.29±0.02c2.28±0.09b28.23±3.09b55.14±2.11c46.00±1.37c650.45±0.02a3.82±0.28a32.20±3.73a61.14±1.30c66.20±3.14a700.39±0.03b3.50±0.36a33.73±2.06a77.92±2.51a71.63±3.76a750.46±0.01a3.67±0.28a26.30±1.97b68.09±5.67b55.97±3.46b
注:同列肩标字母不同表示差异显著(P<0.05),相同表示差异不显著(P>0.05)。
2.2.2 嫩度
剪切力大小可直观反映肉品的嫩度好坏,是评价牛肉嫩度的首要指标[17]。肉品剪切力参数大小主要与其蛋白结构在加热过程中的变化有关[18]。由图2可知,以常温100 ℃为对照,在不同真空低温加热条件下,牛肉的剪切力值随温度的升高呈先增大后减小趋势,于70 ℃产生峰值,75 ℃又有明显减小(P<0.05)。前人研究表明,在60~70 ℃加热条件下牛肉剪切力逐渐增大主要与其肌原纤维蛋白的热变性和肌肉结缔组织发生热收缩有关[19]。在75 ℃、100 ℃牛肉剪切力的减小主要由于加热温度的升高使得肌间胶原蛋白发生热变性而使肌束膜和肌内膜的完整性遭到破坏,肌肉纤维变得更加松散和不规则,同时肌肉可溶性胶原蛋白的溶解度增加,这与PALKA[20]、孙红霞等人[21]的研究结果一致。
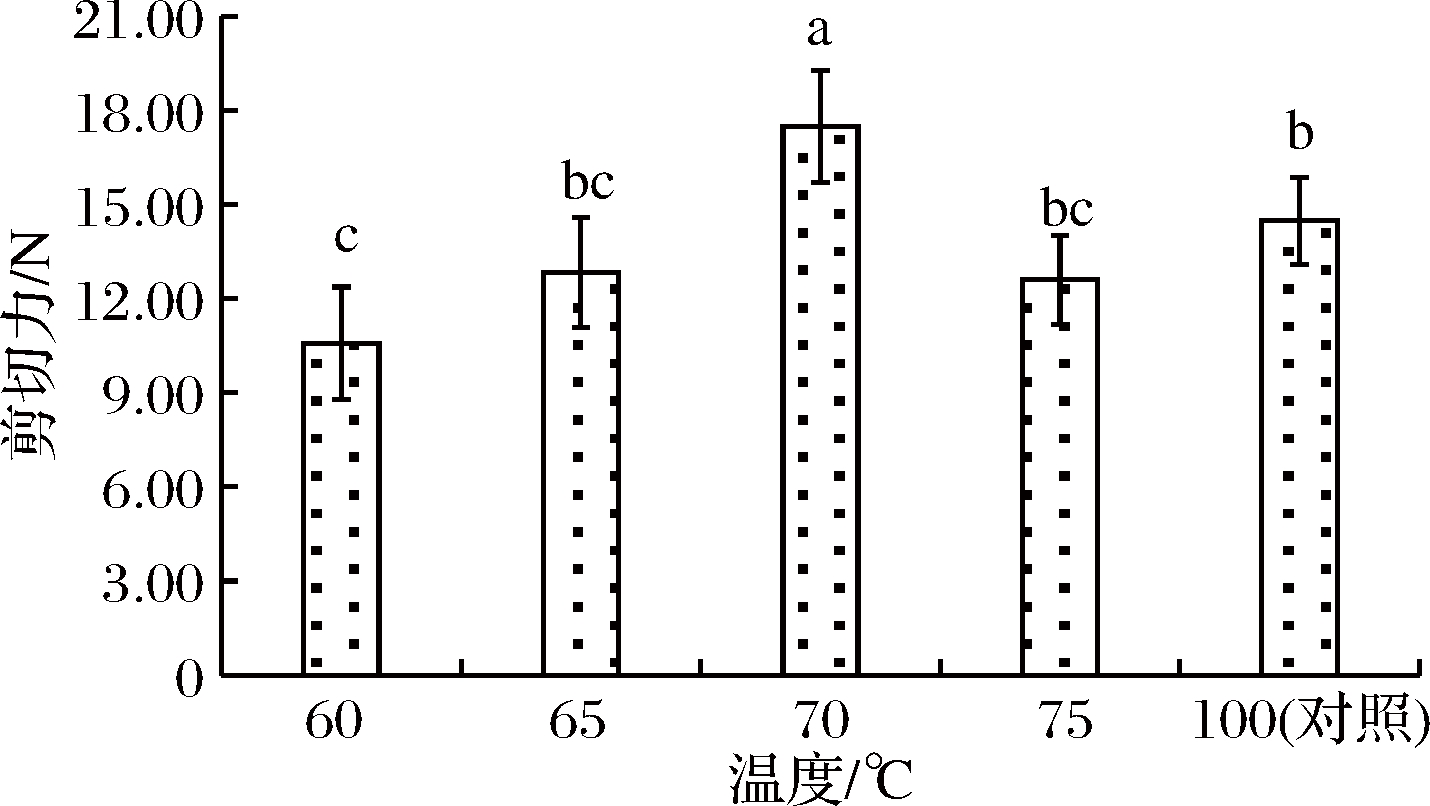
图2 真空低温烹饪过程中牛肉嫩度的变化
Fig.2 The changes in tendernes of beef during sous vide
cooking
2.2.3 色泽
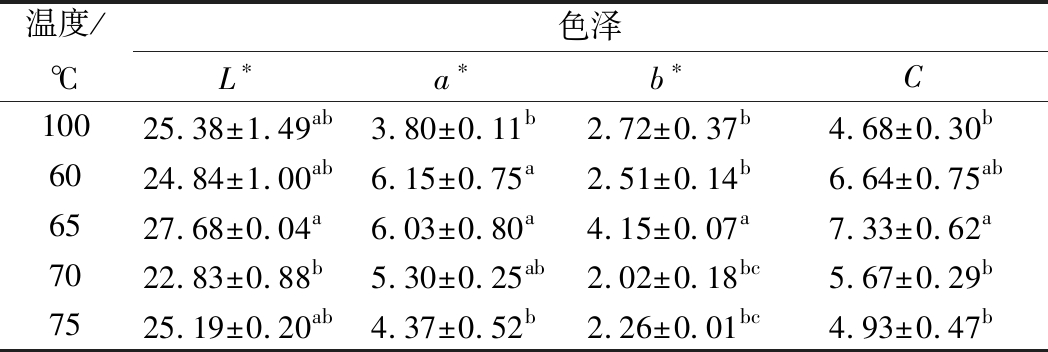
色泽是消费者在决定购买牛肉产品前首先考虑的重要属性[22]。由表2可得,随着加热温度的升高,亮度L*值总体呈先增大后减小再增大趋势,在65 ℃加热条件下牛肉的L*值显著高于其他样品组(P<0.05),70 ℃加热条件下的牛肉L*值最小,仅为22.83,随后有缓慢增大,主要由加热过程中牛肉内部水分流失至表面的程度有关。牛肉的红度a*值随加热温度的升高逐渐减小(P<0.05),75 ℃与100 ℃加热条件下的牛肉a*值显著小于其他样品组,而60与65 ℃加热条件下的牛肉样品具有较高的a*值,主要由于低温加热极大减少了对肌红蛋白的破坏,而高温加热导致肌红蛋白周围失水后生成高铁肌红蛋白[23],肌肉也由鲜红色变为棕褐色。低温烹饪过程中牛肉黄度b*值的变化趋势与L*值基本保持一致,牛肉的b*值在65 ℃加热条件下达到最大,为4.15,而在70 ℃加热条件下减小至2.02。C值主要表示肌肉的色彩强度,牛肉的C值随加热温度的升高呈先增大后减小趋势,在60~65、70~75及100 ℃加热条件下具有显著差异(P<0.05),65 ℃加热条件下的牛肉具有最好的色彩强度,常温100 ℃对照组的牛肉色彩强度最差,显示随着加热温度的升高,牛肉会逐渐变得黯淡、无光泽。
表2 真空低温烹饪过程中牛肉色泽的变化
Table 2 The changes in colour of beef during sous
vide cooking
温度/℃色泽L∗a∗b∗C10025.38±1.49ab3.80±0.11b2.72±0.37b4.68±0.30b6024.84±1.00ab6.15±0.75a2.51±0.14b6.64±0.75ab6527.68±0.04a6.03±0.80a4.15±0.07a7.33±0.62a7022.83±0.88b5.30±0.25ab2.02±0.18bc5.67±0.29b7525.19±0.20ab4.37±0.52b2.26±0.01bc4.93±0.47b
注:同列肩标字母不同表示差异显著(P<0.05),相同表示差异不显著(P>0.05)。
2.2.4 pH与持水力(WHC)
pH值是衡量牛肉品质的关键参数[24]。由表3可知,真空低温烹饪对牛肉的pH有显著影响(P<0.05),在65 ℃加热条件下牛肉的pH明显降低,到70 ℃又有明显升高,这可能与温度破坏稳定蛋白质结构的化学键使其在加热后酸性基团减少有关[25]。70 ℃后牛肉的pH略有降低并趋于稳定,可能因肌肉中的脂肪在加热过程中发生部分水解生成脂肪酸而使pH降低[26]。
表3 真空低温烹饪过程中牛肉pH和WHC的变化
Table 3 The changes in pH and WHC of beef during
sous vide cooking

温度/℃pHWHC/%1006.24±0.03b 76.32±3.05d606.35±0.03a83.03±2.00b656.08±0.04c86.71±1.54a 706.31±0.04a84.71±1.22ab756.21±0.03b80.85±0.79bc
注:同列肩标字母不同表示差异显著(P<0.05),相同表示差异不显著(P>0.05)。
持水力(water holding capacity, WHC)可以反映肉品的保水性能,除了影响肉的食用品质外,还具有重要的经济学意义[27]。当加热温度在60~65 ℃之间,牛肉的WHC有显著提高(P<0.05)。65 ℃后牛肉的WHC随着加热温度的升高逐渐下降,且差异明显(P<0.05)。牛肉的WHC在65 ℃低温加热条件下高达86.71%,而在100 ℃常温加热条件下降低至76.32%,主要与加热过程中牛肉的肌纤维结构逐渐变得松散与不规则,使得肌肉内部水分在外力作用下易流失所致。
2.2.5 消化特性
为模拟人体胃肠消化环境,采用两步消化法构建牛肉的体外消化模型。由图3可知,真空低温烹饪对牛肉的体外消化率具有显著影响(P<0.05)。当加热温度在60~70 ℃之间,牛肉蛋白质的胃消化率无显著差异(P<0.05)。随着加热温度的继续升高,牛肉蛋白质的胃消化率开始有了明显下降(P<0.05),而75与100 ℃加热条件下的胃消化率并无显著差异(P>0.05),可能因为热诱导氧化和肌原纤维蛋白表面疏水性的增加引起蛋白质聚集,进一步降低胃蛋白酶消化率[28]。与胃消化率相比,牛肉蛋白质的总体消化率均有明显增大,主要因为食物从胃进入小肠后,蛋白质不完全水解产物会在肠液中进一步被分解,且胰蛋白酶酶解作用更强,可将蛋白质、肽彻底分解为氨基酸[29]。常温100 ℃对照组除外,经胃蛋白酶-胰蛋白酶联合处理的牛肉蛋白质总消化率均在90%以上,且随加热温度的升高呈先增大后下降趋势,差异显著(P<0.05)。低温65 ℃牛肉蛋白质的总消化率高达96.27%,而在75、100 ℃加热条件下,牛肉蛋白质的总消化率下降明显(P<0.05),与PROMEYRAT[30]、WEN等[31]的研究结果一致。
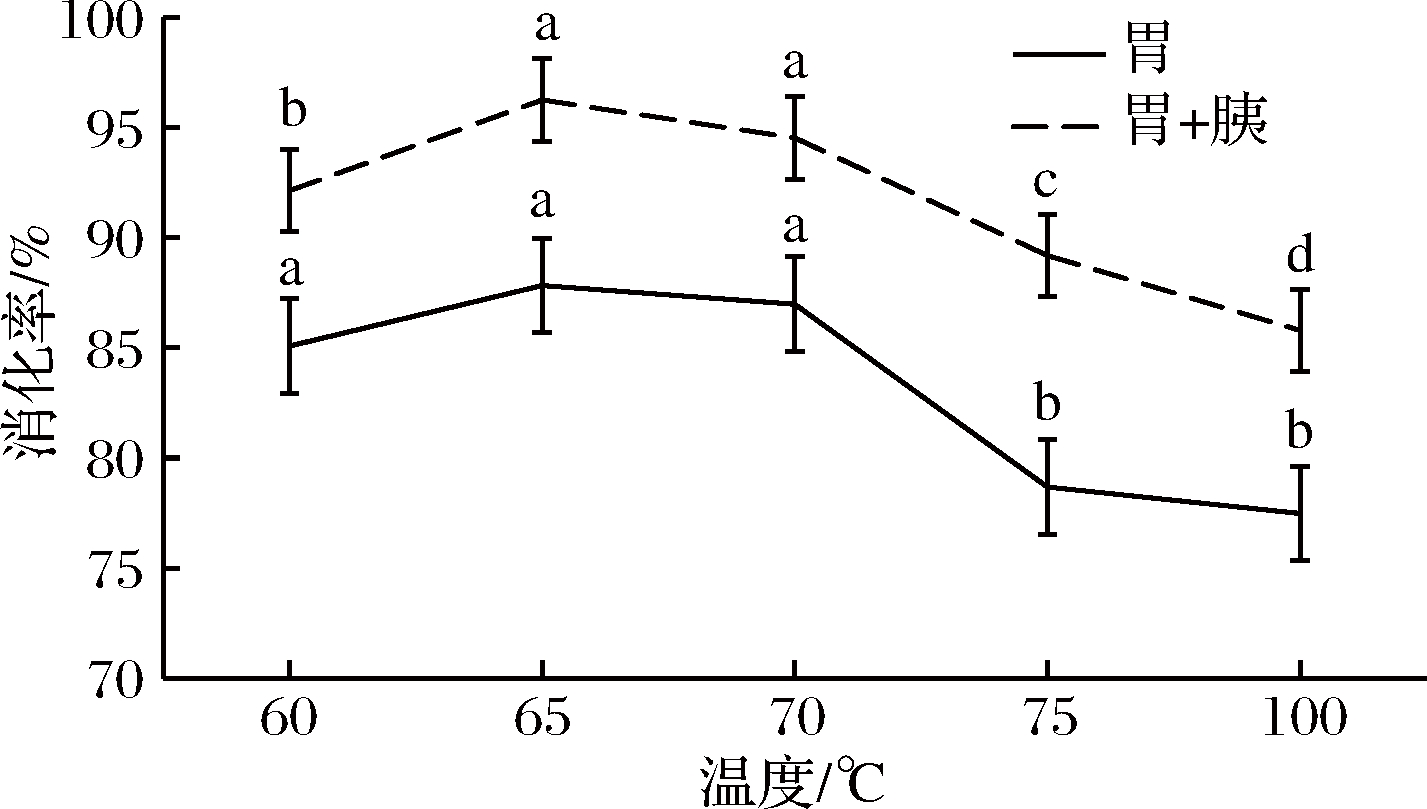
图3 真空低温烹饪过程中牛肉消化特性的变化
Fig.3 The changes in digestion characteristics of beef during sous vide cooking
3 结论
真空低温烹饪对与牛肉微观结构和理化性质相关的各项指标均有显著影响。以常温100 ℃为对照,在不同真空低温烹饪条件下,对产品综合评价影响最大的弹性、硬度和咀嚼性随着温度的升高呈先增大后减小趋势,结果显示低温60、65 ℃加热条件下的牛肉具有较好的质构特性。低温70 ℃加热条件下牛肉的嫩度较差,主要与其肌原纤维蛋白的热变性和肌肉结缔组织发生热收缩有关,而继续升高温度会引起肌束膜和肌内膜的完整性遭到破坏,肌肉纤维变得松散和不规则,使得牛肉的嫩度得到改善,与微观结构的结果一致。色泽受加热温度的影响较大,低温60、65 ℃加热条件下的牛肉具有较好的色泽,随着加热温度的升高,牛肉逐渐变得黯淡、无光泽。真空低温烹饪对牛肉的pH与WHC均有显著影响,低温65 ℃加热条件下的牛肉保水性最好,且此时牛肉蛋白质的体外消化率远高于常温100 ℃加热的,显示经低温烹饪后的牛肉产品更利于机体的消化吸收。
[1] SCHELLEKENS M. New research issues in sous-vide cooking[J]. Trends in Food Science and Technology, 1996, 7(8): 256-262.
[2] MASSIMILIANO R, CHIARA D, FEDERICA M, et al. Physicochemical and microbiological quality of sous-vide-processed carrots and brussels sprouts[J]. Food Bioprocess Technology, 2013, 18(6): 3 076-3 087.
[3] 王笑丹, 刘爱阳,孙永海,等. 基于自组织神经网络模型与质构特性的牛肉嫩度评定方法[J]. 农业工程学报, 2015, 31(18):262-268.
[4] BALDWIN D E. Sous vide cooking: a review[J]. International Journal of Gastronomy and Food Science, 2012, 1(1): 15-30.
[5] FAUSTINO H. Fluorescence and confocal laser scanning microscopy imaging of elastic fibers in hematoxylin-eosin stained sections[J]. Cell Biology, 1996, 106: 587-592.
[6] ZHOU YANZI, CHEN CONGGUI, CHEN XING, et al. Contribution of three ionic types of polysaccharides to the thermal gelling properties of chicken breast myosin[J]. Journal of Agricultural and Food Chemistry, 2014, 62(12): 2 655-2 662.
[7] 杨万君. 三种品牌酱排骨中蛋白质体外消化研究[J]. 肉类工业, 2017(3): 17-23.
[8] ESCUDERO E, SENTANDREU MA, TOLDRA F. Characterization of peptides released by in vitro digestion of pork meat[J]. Journal of Agricultural and Food Chemistry, 2010, 58(8): 5 160-5 165.
[9] 王水清. 乌珠穆沁羊生长过程中肌纤维结构特性变化研究[D]. 呼和浩特:内蒙古农业大学, 2012.
[10] 秦召, 康相涛,李国喜. 肌纤维组织学特性与肌肉品质的关系[J]. 安徽农业科学, 2006, 34(22): 5 872-5 873.
[11] 张立彦, 吴兵,包丽坤. 加热对三黄鸡胸肉嫩度、质构及微观结构的影响[J]. 华南理工大学学报, 2012, 40(8): 116-121.
[12] TORNBERG E. Effects of heat on meat proteins-Implications on structure and quality of meat products[J]. Meat Science, 2005, 70(3): 493-508.
[13] 李里特. 食品物性学[M]. 北京:中国农业出版社, 1998: 107-109.
[14] 张馨木. 质构仪测定冷鲜肉新鲜度方法的研究[D]. 吉林:吉林大学, 2012.
[15] 夏军军, 李洪军,贺稚非,等. 不同腌制方式对牛肉品质特性的影响[J]. 西南大学学报(自然科学版), 2016, 38(2): 12-19.
[16] 张志清, 熊善波,李远志,等. 工程重组米质构测定(TPA)与感官评价相关分析[J].中国粮油学报, 2011, 26(10): 1-5.
[17] HILDRUM K I, RØDBOTTEN R, HØY M, et al. Classification of different bovine muscles according to sensory characteristics and Warner Bratzler shear force[J]. Meat Science, 2009, 83(2): 302-307.
[18] HUANG F, HUANG M, XU X, et al. Influence of heat on protein degradation, ultrastructure and eating quality indicators of pork[J]. Journal of the Science of Food & Agriculture, 2011, 91(3): 443-448.
[19] CHRISTENSEN M, PURSLOW P P, LARSEN L M. The effect of cooking temperature on mechanical properties of whole meat, single muscle fibres and perimysial connective tissue[J]. Meat Science, 2000, 55(3): 301-307.
[20] PALKA K. Changes in intramuscular connective tissue and collagen solubility of bovine M. semitendinosus during retorting[J]. Meat Science, 1999, 53(3): 189-194.
[21] 孙红霞, 黄峰,丁振江,等. 不同加热条件下牛肉嫩度和保水性的变化及机理[J]. 食品科学, 2018, 39(1): 84-90.
[22] ENGCHUAN W, JITTANIT W, GARNJANAGOONCHORN W. The ohmic heating of meatball: Modeling and quality determination[J]. Innovative Food Science & Emerging Technologies, 2014, 23: 121-130.
[23] 郎玉苗, 谢鹏,李敬,等. 熟制温度及切割方式对牛排食用品质的影响[J]. 农业工程学报, 2015, 31(1): 317-323.
[24] 李梦熹, 黄斯,关荣发,等. 牛肉品质性状与感官指标关系的研究[J]. 畜牧与饲料科学, 2011, 32(7): 91-93.
[25] MA HANJUN, LEDWARD D A. High pressure / thermal treatment on the texture of beef muscle[J]. Meat Science, 2004, 68: 347-355.
[26] JOSEPH J K, AWOSANYA B, et al. The effects of endpoint internal cooking temperature on the meat quality attributes of selected Nigerian poultry meats[J]. Food Quality and Preference, 1997(8): 57-61.
[27] 李鸣, 邢通,王虎虎,等. 加工工艺对白切鸡品质及微生物状况的影响[J]. 食品科学, 2018, 39(11): 32-38.
[28] BAX ML, SAYD T, AUBry L, et al. Muscle composition slightly affects in vitro digestion of aged and cooked meat: Identification of associated proteomic markers[J]. Food Chemistry, 2013, 136(3): 1 249-1 262.
[29] 王君翠. 微波和水浴低温加热对牛肉品质的影响研究[D]. 广东:华南理工大学, 2016.
[30] PROMEYRAT A, BAX ML, TRAOREÉ S et al. Changed dynamics in myofibrillar protein aggregation as a consequence of heating time and temperature[J]. Meat Science, 2010, 85(4): 625-631.
[31] SIYING W, GUANGHONG Z, LI L, et al. Effect of Cooking on in vitro digestion of pork proteins:A peptidomic perspective[J]. Journal of Agricultural and Food Chemistry, 2015, 63(1): 250-261.