大菱鲆(Scophthalmus maximus)属于鲽形目鲆科,在我国被称作“多宝鱼”,作为我国北方主要的海水养殖鱼类,年产量达8.5万t,销售价值超过40亿元人民币[1]。大菱鲆因其高蛋白、低脂肪、营养丰富等特点为消费者喜爱[2]。目前,大菱鲆以活鱼销售为主,随着生鲜电商的迅猛发展,冰鲜大菱鲆已成为未来销售流通的重要途径之一。然而,由于受到微生物繁殖和体内酶活性的影响,大菱鲆在贮藏期间易发生蛋白质氧化和降解,导致鱼肉品质劣变,产品货架期缩短。
近年来,涂膜作为一种新型安全的保鲜方法得到了外界广泛的关注。其中,复合涂膜技术发展迅速,具有加强涂膜抑菌和抗氧化等方面的性能,是一种经济、有效、安全的保鲜方法[3]。亚麻籽胶(flaxseed gum,FSG)因具有良好的成膜性、功能特性和营养价值而成为一种具有广泛前景的成膜材料[4]。YOUSUF等[5]将亚麻籽胶与柠檬草精油结合处理即食石榴,结果表明,相比于对照组,用亚麻籽胶-柠檬草精油复合涂膜处理显著抑制了微生物的生长,并且更好地保持了石榴的色泽和水分。柠檬马鞭草精油(verbena oil)是一种由柠檬马鞭草萃取而制得的植物精油,主要成分为柠檬醛、苧烯和芳姜黄烯,具有很强的抗氧化和抗菌能力[6-7]。ISHKEH等[7]用柠檬马鞭草精油处理树莓果实,发现用柠檬马鞭草精油处理的树莓果实具有较高的抗氧化能力、酚类和花青素含量,抑制了真菌的生长,延长了果实的货架期。因此,将亚麻籽胶与柠檬马鞭草精油复合使用涂膜就能够既具备良好的成膜性,又具有强抑菌和抑制蛋白氧化的效果,延长产品货架期。
本研究利用不同浓度的柠檬马鞭草精油结合亚麻籽胶制作复合涂膜液处理冰温贮藏下的大菱鲆鱼片,研究冰温贮藏期间大菱鲆肌原纤维蛋白生化特性及结构的变化,以期筛选出一种有效的柠檬马鞭草精油-亚麻籽胶复合涂膜的配方,为今后的大菱鲆保鲜提供一种全新的方法。
1 材料与方法
1.1 实验试剂及仪器
1.1.1 实验试剂
三羟甲基氨基甲烷(Tris)、马来酸、KCl、三氯乙酸、尿素、SDS、EDTA、DTNB、CaCl2、戊二醛、甘油、无水乙醇、KBr、二甲胂酸钠、四氧化锇、环氧树脂、乙酸双氧铀、柠檬酸铅,生工生物工程(上海)股份有限公司;Bradford法蛋白测试盒、超微量Ca2+-ATP酶测定试剂盒,南京建成生物工程研究所;柠檬马鞭草精油,广州粤渝精油公司;亚麻籽胶(食品级),河南万邦实业有限公司。
1.1.2 实验仪器
H1850R型高速冷冻离心机,湖南湘仪离心机仪器有限公司;XEBJ-1000超声波均质机,济宁谐成超声波设备有限公司;DJ1C-60增力电动搅拌器,青岛聚创环保设备有限公司;FEI Tecnai G2 SpiritBiotwin透射电子显微镜,美国Thermo Scientific公司;Hitachi L-8800全自动氨基酸分析仪,天美(中国)科学仪器有限公司;Hitachi F-7100荧光分光光度计,上海斯迈欧分析仪器有限公司;BOC Edwards Lyofast真空冷冻干燥机,北京天利联合科技有限公司;BioTek多功能酶标仪,上海京工实业有限公司;BPS-100CB恒温恒湿箱,上海一恒科学仪器有限公司。
1.2 实验方法
1.2.1 柠檬马鞭草精油-亚麻籽胶复合涂膜的制备及鱼样的处理
将亚麻籽胶粉末以0.6%的质量浓度溶解在蒸馏水中[5],使用磁力搅拌器以3 000 r/min匀速搅拌3 h,加入甘油(25%,w/v)进行适当乳化,待溶液冷却后,将柠檬马鞭草精油分别以0、0.128%、0.64%和1.28%的质量浓度渗入到FSG溶液中继续以3 000 r/min匀速搅拌0.5 h,最后在超声波均质机中均质0.5 h,制得柠檬马鞭草精油-亚麻籽胶复合涂膜液。
鲜活大菱鲆于2019年6月购于上海市芦潮港水产品批发市场,体态均匀、健康,每条大菱鲆的平均体重为(700±50)g,平均体长为(30±2)cm。活鱼宰杀后,去除鱼鳃和内脏,清洗干净后把鱼体切分成质量大小均一的鱼块。
分别对鱼块进行浸泡,浸泡时间为3 min。未涂膜处理的鱼块作为对照组CK,仅用FSG溶液涂覆的样品为实验组C1,用渗入0.128%、0.64%和1.28%质量浓度柠檬马鞭草精油的FSG溶液涂覆的样品为实验组C2,C3和C4。鱼样沥干后随机分装在聚乙烯袋中,-1 ℃下贮藏,每隔5 d取一次样。
1.2.2 肌原纤维蛋白的制备与含量测定
参考LV等[8]的方法提取肌原纤维蛋白溶液(myofibril protein,MP)。称取2 g剁碎的鱼肉于50 mL离心管中,加入20 mL缓冲液A(20 mmol/L Tris-maleate,pH 7.0,0.05 mol/L KCl),4 ℃下匀浆,匀浆液以10 000 r/min离心15 min,收集沉淀。沉淀加入20 mL缓冲液B(20 mmol/L Tris-maleate,pH 7.0,0.6 mol/L KCl),匀浆后于4 ℃下浸提1 h,10 000 r/min离心15 min,上清液即肌原纤维蛋白溶液。根据Bradford试剂盒法测定蛋白浓度。
1.2.3 总巯基含量的测定
参照BENJAKUL等[9]的方法测定。
1.2.4 Ca2+-ATPase活性的测定
根据鲁耀彬等[10]的方法测定。
1.2.5 蛋白质二级结构
根据LI等[11]的方法,将MP干粉样品与KBr充分混合并研磨,然后用Thermo FT-IR光谱仪在25 ℃下扫描整个条带,将每个样品的红外光谱图设置为32次扫描的叠加,仪器分辨率为4 cm-1,每个样品以空气为背景进行扫描。实验进行3次测量。用Omnic 9.2.106光谱软件处理FT-IR原始数据,用Peckfit v4.12光谱分析拟合软件对谱峰进行拟合。
1.2.6 蛋白质三级结构
根据SUN等[12]的方法,稍作修改。使用F-7100荧光分光光度计测量蛋白质溶液的固有荧光发射光谱,发射波长为295 nm,狭缝宽度为5 nm,发射光谱范围为310~400 nm,扫描速度为1 200 nm/min。记录荧光发射光谱的最大荧光波长。
1.2.7 游离氨基酸含量的测定
参照YU等[13]的方法进行。使用Hitachi L-8800全自动氨基酸分析仪分析。
1.2.8 透射电子显微镜观察
参照CHEN等[14]的方法,稍作修改。将各样品沿着平行于肌原纤维的方向切成5 mm×3 mm×2 mm的方形小块,用预冷的2.5%体积浓度戊二醛固定并置于0.1 mol/L磷酸缓冲液中(pH 7.4),然后将样品在pH 7.4的二甲胂酸钠缓冲液中洗涤,四氧化锇固定2 h。然后,样品分别经30%、50%和70%(体积分数)的乙醇梯度脱水,在环氧丙烷中交换后包埋在Spurr树脂中,使用超薄切片机平行切割纤维。超薄切片(70 nm)用乙酸双氧铀和柠檬酸铅染色,最后使用FEI Tecnai G2 SpiritBiotwin透射电子显微镜拍照观察。
1.3 数据分析
以上每个指标做3次平行实验,采用Origin 8.5绘图,并利用SPSS Statistics 24软件对组间数据进行显著性分析,P<0.05表示存在显著差异。
2 结果与分析
2.1 总巯基含量的变化
巯基是蛋白质中最主要的官能团之一,其含量变化是评价肌肉蛋白质氧化的有效指标[15]。如图1所示,随着贮藏时间的增加,所有组样品的巯基含量均不断下降,这是因为贮藏期间巯基发生氧化形成二硫键[16]。CK组的巯基含量在整个贮藏期间下降迅速,贮藏至15 d时,CK组的巯基含量下降了38.74%,而C1、C2、C3和C4组的巯基含量分别下降了32.31%、16.70%、22.25%和23.68%,结果表明,涂有柠檬马鞭草精油-亚麻籽胶复合涂膜样品的巯基含量要显著高于其他组(P<0.05),这可能是因为复合涂膜里的柠檬马鞭草精油具有较强抗氧化能力,抑制了巯基的氧化,从而保护蛋白质免于变性。另外,C2组的巯基含量在贮藏结束时显著高于C3和C4组(P<0.05),这可能是因为较高浓度的柠檬马鞭草精油的促氧化作用引起的[17]。NIETO等[18]发现,与较低质量浓度(0.05%)相比,向猪肉饼中添加更高质量浓度(0.4%)的牛至精油会导致更高的蛋白质氧化。因此,以上结果表明添加0.128%(质量浓度)柠檬马鞭草精油的复合涂膜能更有效地抑制肌肉蛋白质的氧化。
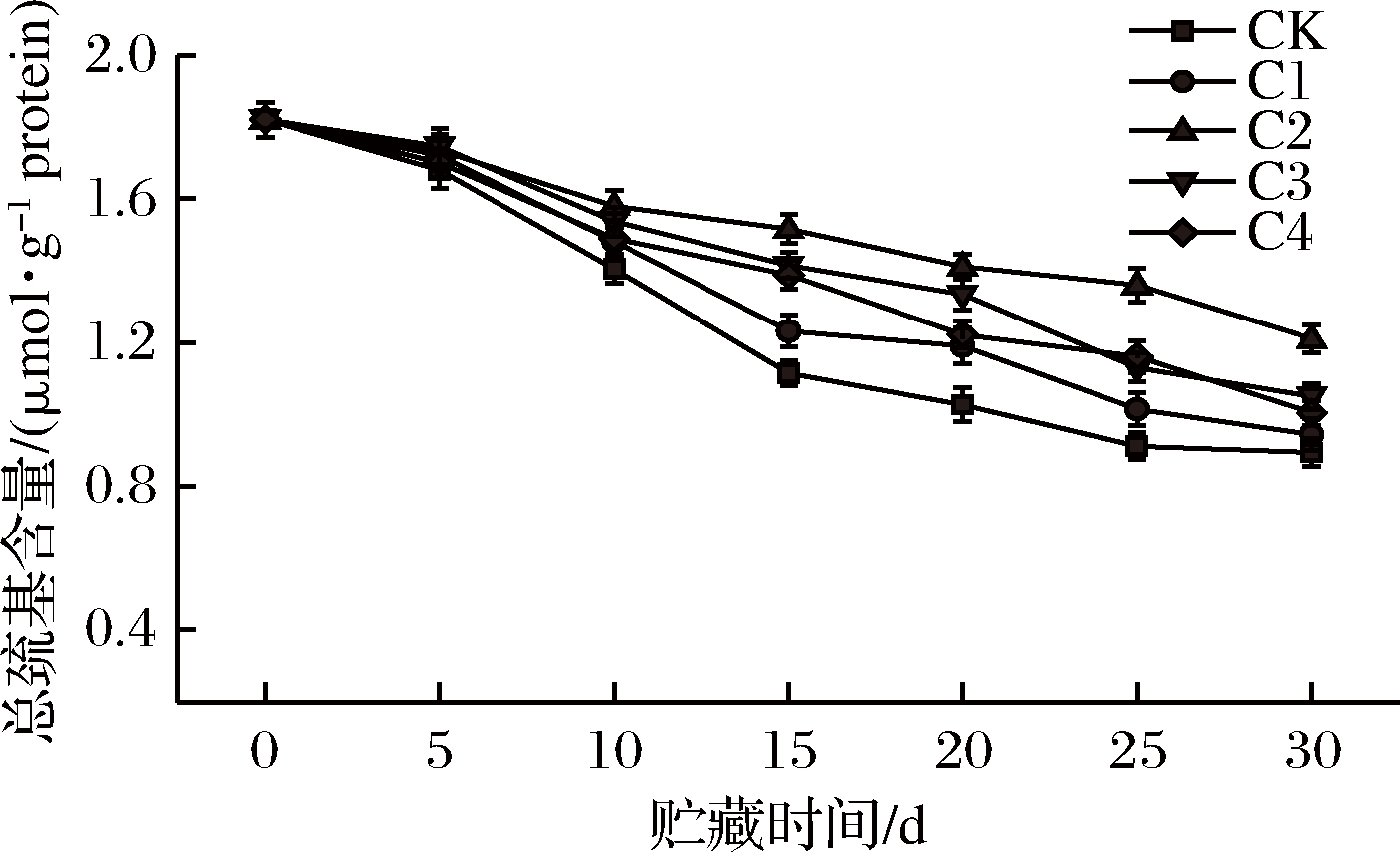
图1 不同处理条件下大菱鲆肌原纤维蛋白总巯基含量的变化
Fig.1 Changes in total sulfhydryl content of myofibril protein in turbot under different treatments
2.2 Ca2+-ATPase活性的变化
Ca2+-ATPase活性是用来评价肌球蛋白完整性的指标,蛋白质的变性会导致酶活力发生改变[19]。图2显示了不同处理组的大菱鲆的Ca2+-ATPase活性在整个贮藏期间的变化,可以得出,随着贮藏时间的增加,所有组的Ca2+-ATPase活性均呈下降趋势,这可能是由于肌球蛋白的球状头部上的巯基发生氧化和肌球蛋白的聚集引起的[20]。其中,相比于其他处理组的样品,对照组样品的Ca2+-ATPase活性急剧下降,贮藏至15 d时,其Ca2+-ATPase活性从0.148降低至0.1 μmol Pi/(mg protein·min),显著低于用亚麻籽胶和柠檬马鞭草精油-亚麻籽胶复合涂膜处理的样品(P<0.05)。贮藏30 d后,C2组样品的Ca2+-ATPase活性显著高于其他处理组的样品(P<0.05),这可能是因为这种复合涂膜能更有效地抑制肌球蛋白中的巯基发生氧化,该结果与总巯基含量的变化保持一致。
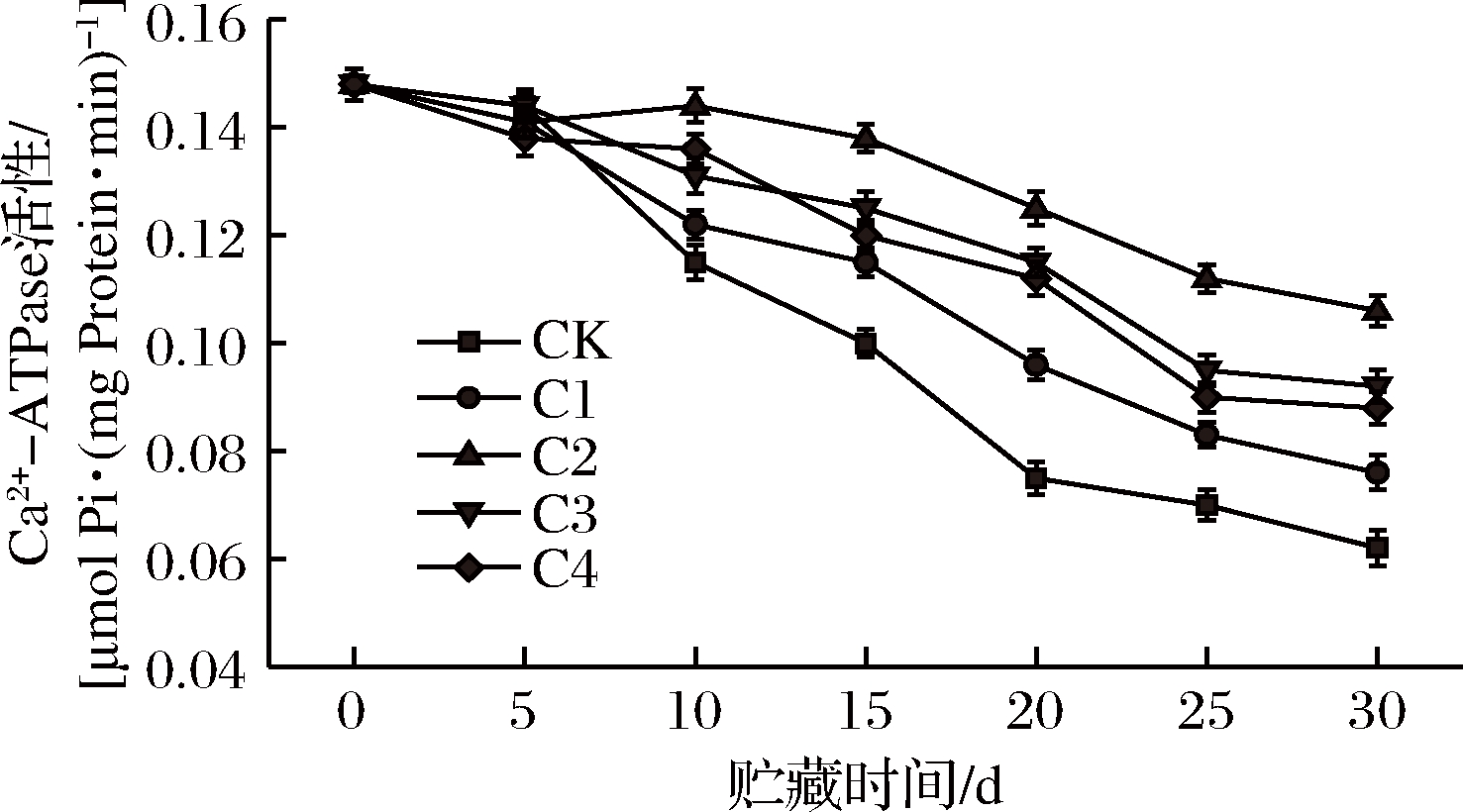
图2 不同处理条件下大菱鲆肌原纤维蛋白Ca2+ATPase活性的变化
Fig.2 Changes in Ca2+-ATPase of myofibril protein in turbot under different treatments
YU等[13]将不同浓度的丁香精油与壳聚糖涂膜结合处理草鱼,发现添加较高浓度精油的涂膜能更好地减弱氧化损伤,更好地保持鱼片的完整性。然而,本实验得到较低浓度的柠檬马鞭草精油保护蛋白效果更佳,可能是因为高浓度的柠檬马鞭草精油会引起促氧化作用。MARIO[21]等用迷迭香精油处理法兰克福香肠时也发现迷迭香精油在低浓度时抗氧化效果更好。
2.3 大菱鲆肌原纤维蛋白的红外光谱和二级结构
蛋白质二级结构变化与C—H、N—H和C![]() O等的振动方式有关,这些振动方式使红外在多个波段均有吸收[22]。其中,酰胺I带(1 700~1 600 cm-1)是肌原纤维谱中最主要的谱带,它主要受C
O等的振动方式有关,这些振动方式使红外在多个波段均有吸收[22]。其中,酰胺I带(1 700~1 600 cm-1)是肌原纤维谱中最主要的谱带,它主要受C![]() O伸缩振动的影响,常被用来分析肌原纤维二级结构的变化[23]。FT-IR因其操作简单、扫描快速、波长精确、灵敏度高等优点,可快速准确地分析蛋白质的二级结构,包括α-螺旋、β-折叠、β-转角和无规则卷曲[24]。图3-a和图3-b显示了冰温贮藏期间大菱鲆肌原纤维蛋白在4 000~400 cm-1范围内的红外光谱图,图3-c和图3-d显示了1 700~1 600 cm-1范围内光谱的二阶导数。从图3-a可以看出,新鲜鱼样的酰胺I带波数为1 644 cm-1,贮藏至15 d后,CK、C1和C4的酰胺I带发生了变化,波数分别为1 645、1 643和1 642 cm-1,可能是因为蛋白质降解导致了二级结构的改变,而C2和C3的样品保持不变;贮藏30 d后,不同组大菱鲆MP酰胺I区的光谱差异是由于多肽链的构象随着贮藏时间的增加而变化[25]。
O伸缩振动的影响,常被用来分析肌原纤维二级结构的变化[23]。FT-IR因其操作简单、扫描快速、波长精确、灵敏度高等优点,可快速准确地分析蛋白质的二级结构,包括α-螺旋、β-折叠、β-转角和无规则卷曲[24]。图3-a和图3-b显示了冰温贮藏期间大菱鲆肌原纤维蛋白在4 000~400 cm-1范围内的红外光谱图,图3-c和图3-d显示了1 700~1 600 cm-1范围内光谱的二阶导数。从图3-a可以看出,新鲜鱼样的酰胺I带波数为1 644 cm-1,贮藏至15 d后,CK、C1和C4的酰胺I带发生了变化,波数分别为1 645、1 643和1 642 cm-1,可能是因为蛋白质降解导致了二级结构的改变,而C2和C3的样品保持不变;贮藏30 d后,不同组大菱鲆MP酰胺I区的光谱差异是由于多肽链的构象随着贮藏时间的增加而变化[25]。
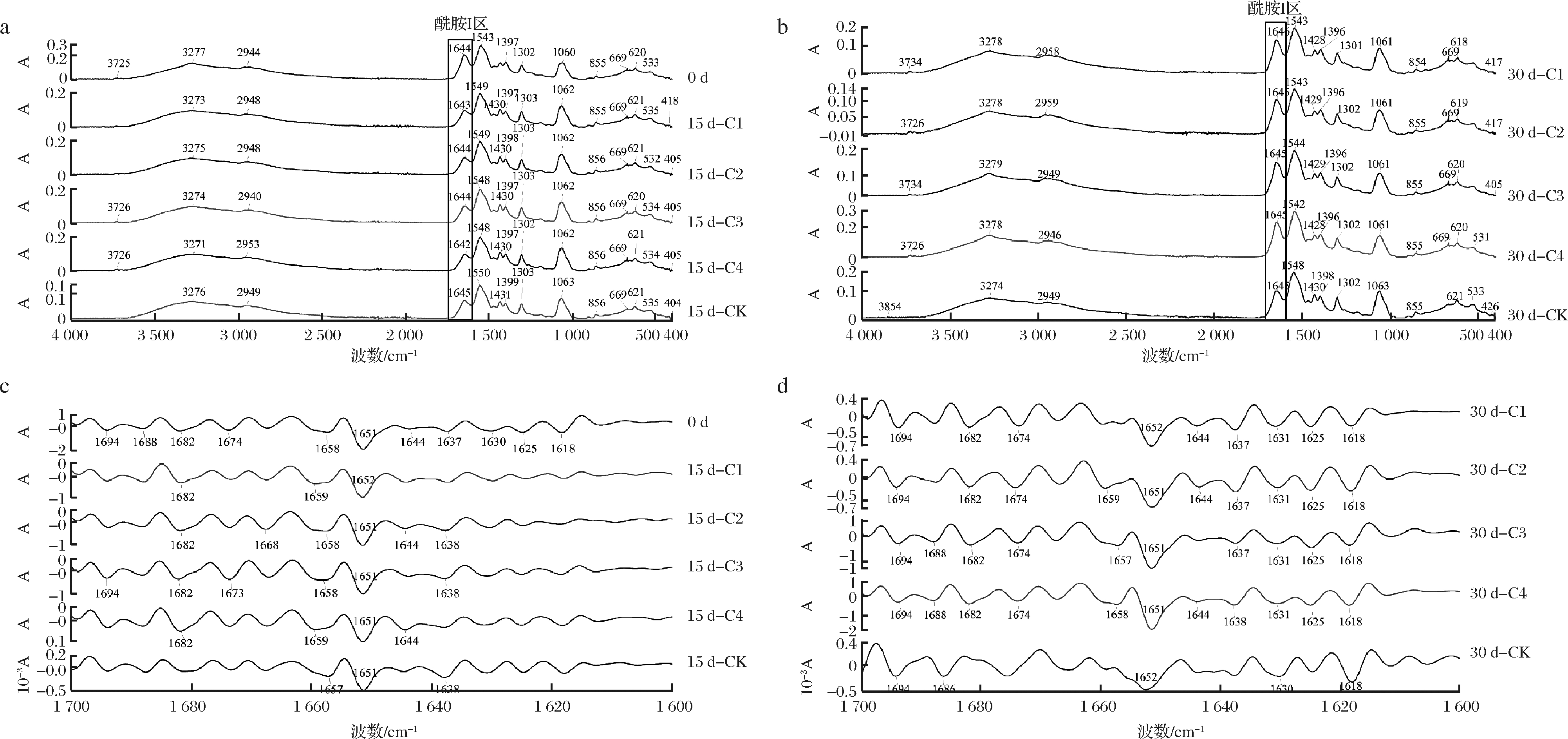
图3 不同处理条件下大菱鲆肌原纤维蛋白在0、15和30 d的红外光谱图,如(a)和(b);贮藏在0、15和30 d大菱鲆肌原纤维蛋白在1 700~1 600 cm-1区域的二阶导数,如(c)和(d)
Fig.3 FT-IR spectra of myofibrillar protein in tubot with different treatments stored at 0,15 and 30 d,shown as (a) and (b);Second derivative of the 1700-1600 cm-1 region of the spectra of myofibrillar protein in tubot stored at 0,15 and 30 d,shown as (c) and (d)
图4显示了不同方式处理的大菱鲆肌原纤维的二级结构的定量分析。新鲜鱼样包含37.62%的β-折叠、25.27%的无规则卷曲、16.85%的α-螺旋和20.26%的β-转角。随着贮藏时间的增加,α-螺旋的比例出现下降,β-折叠的比例上升,表明低温下α-螺旋向β-折叠的转变[26]。其中,α-螺旋的减少可能与冰藏期间螺旋结构的部分解折叠有关,包括维持二级结构的氢键被破坏[27]。在贮藏结束时,用柠檬马鞭草精油-亚麻籽胶复合涂膜处理的样品相比于空气组的样品,有规则的二级结构(α-螺旋和β-折叠)的总比例显著增加(P<0.05),表明这种复合涂膜在冰藏期间能够很好地稳定大菱鲆的肌原纤维结构。并且,相比于仅用亚麻籽胶处理的样品,复合涂膜处理能够更好地促进肌原纤维蛋白的稳定化,这很可能是因为柠檬马鞭草精油具有的强抗氧化性,保护蛋白被降解。ZHAO[28]等用鱼明胶结合葡萄籽提取物处理罗非鱼鱼片,结果表明这种复合涂膜处理有助于罗非鱼在贮藏期间维持更有规则的二级结构,促进肌原纤维蛋白结构的稳定。
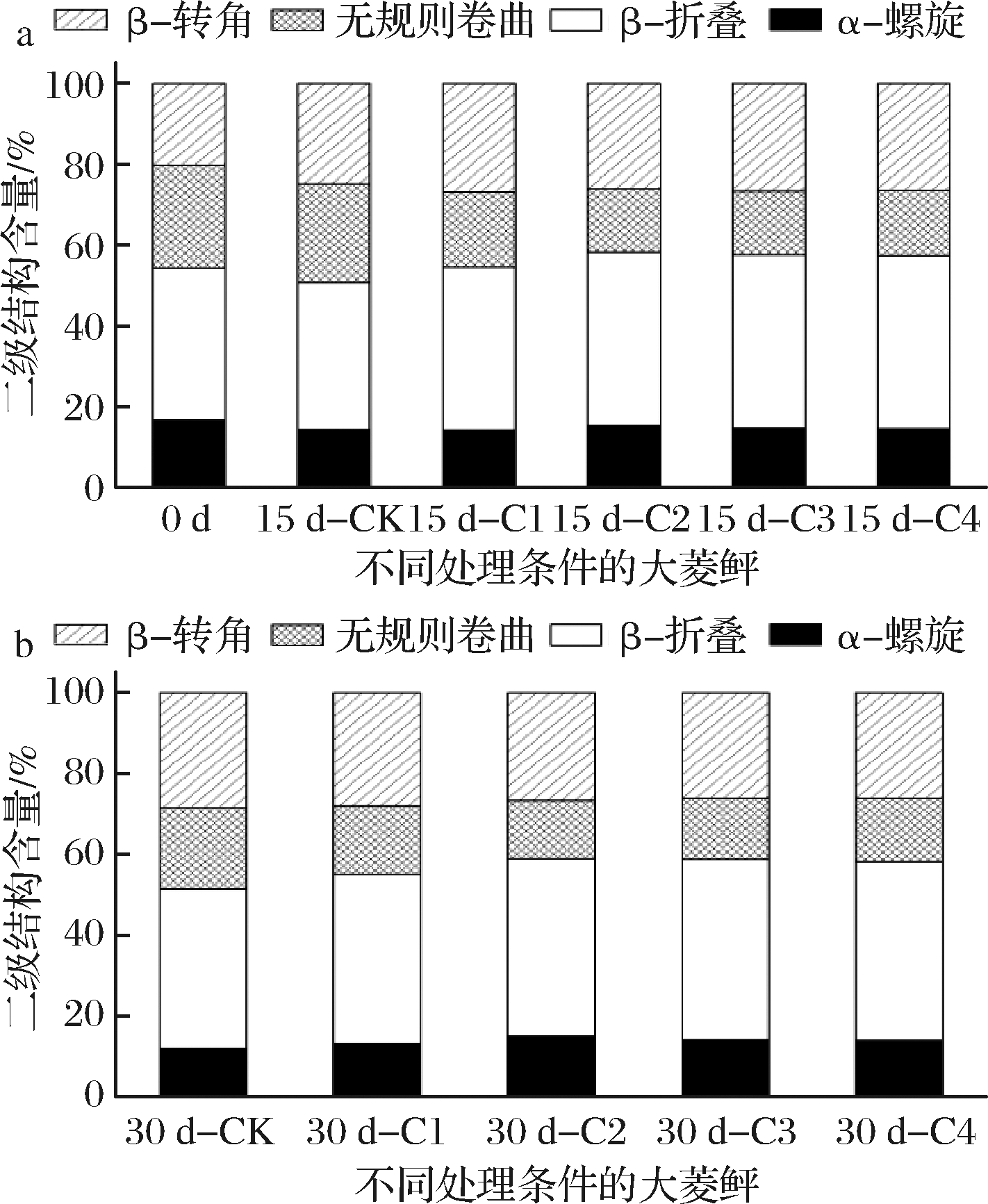
图4 不同处理条件下大菱鲆肌原纤维蛋白二级结构含量的变化
Fig.4 Changes of the secondary structure contents of myofibrillar protein in tubot with different treatments
2.4 蛋白质三级结构
蛋白质的内源荧光是指蛋白质分子内的荧光基团暴露在紫外线时发出荧光的现象。荧光强度的降低通常是因为发色团在溶剂中或在蛋白质自身中与猝灭剂发生相互作用,蛋白质内部的荧光转移到表面,从而发生荧光猝灭[29]。因此,蛋白质内源荧光的变化可以反映其构象的变化[30]。色氨酸作为一种芳香族氨基酸,存在于蛋白质内核中,可以发出可通过荧光光谱法测定的荧光,它们的出现表明蛋白质展开的程度[31]。冰温贮藏期间经不同处理方式处理的大菱鲆肌原纤维蛋白的荧光光谱如图5所示。结果表明,第0天的新鲜鱼样在波长为336 nm处显示出最高的荧光强度。对照组中大菱鲆肌原纤维蛋白的内源荧光强度在整个贮藏期间急剧下降,可能是因为大菱鲆在贮藏过程氧化严重,肌原纤维蛋白结构逐渐展开,色氨酸残基等荧光物质暴露在极性环境中,其内源荧光强度降低[32]。然而,用亚麻籽胶和柠檬马鞭草精油-亚麻籽胶复合涂膜处理的样品的内源荧光强度在贮藏前期下降较慢,尤其是C2组的下降速率要显著低于其他组(P<0.05),表明添加质量浓度为0.128%柠檬马鞭草精油的复合涂膜可以保护蛋白质在冰温贮藏期间免于变性和结构的变化,提高大菱鲆的品质。并且,贮藏结束时C3和C4组的荧光强度显著低于C2组(P<0.05),这是因为较高浓度的柠檬马鞭草精油引起的促氧化作用加快了内源荧光物质的转移。SHI[31]等用迷迭香提取物作为上釉材料处理泥虾,结果表明,与迷迭香釉虾相比,未上釉虾的内源荧光强度在整个贮藏期间急剧下降,表明上釉处理保护蛋白质在冷冻贮藏期间免于结构的变化。

图5 不同处理方式对贮藏期间大菱鲆肌原纤维蛋白内源荧光强度的影响
Fig.5 Effects of different treatments on intrinsic fluorescence of myofibrillar protein in tubot during storage
2.5 游离氨基酸含量的变化
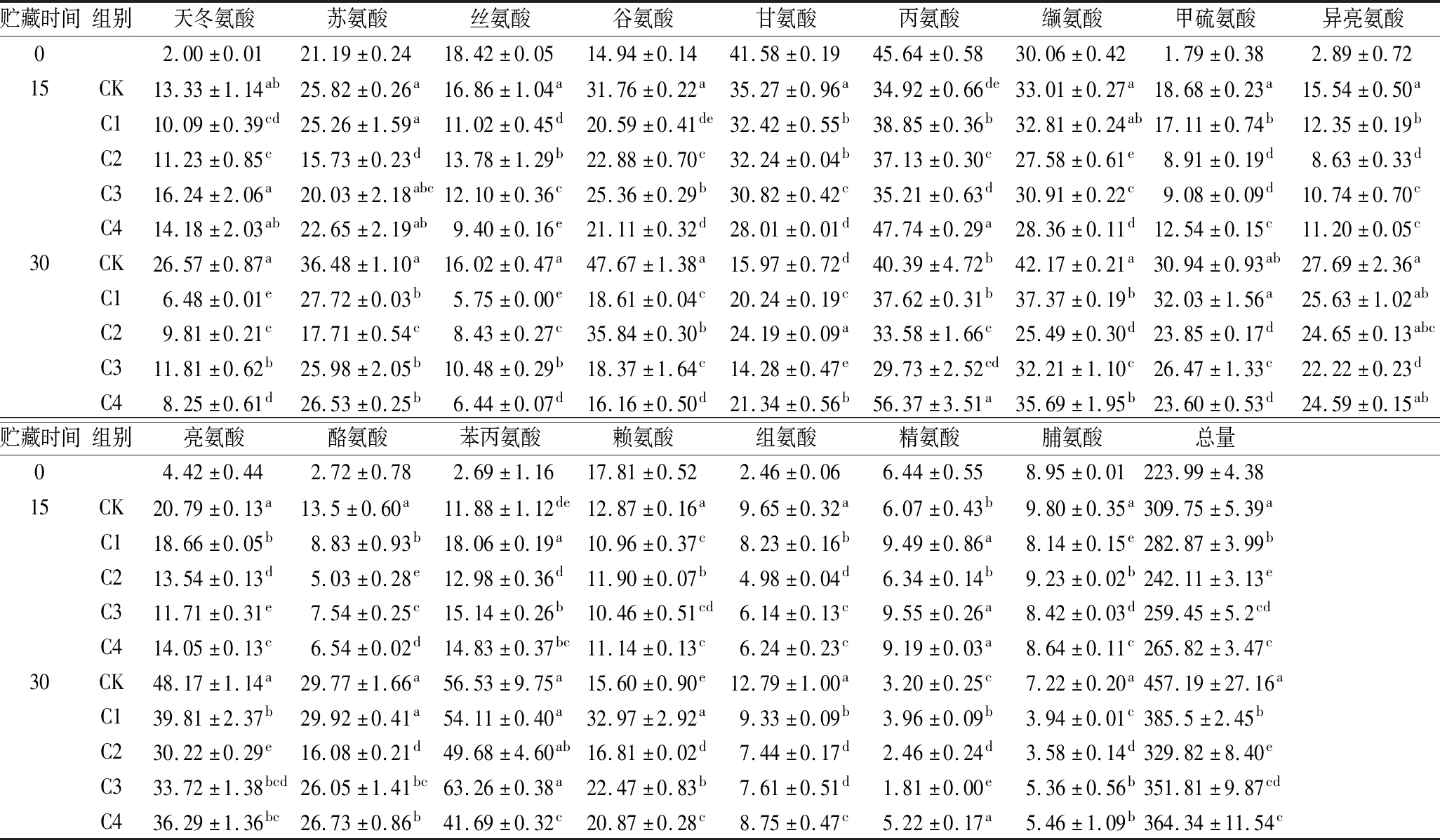
游离氨基酸与鱼片贮藏期间风味的形成密切相关,一些游离氨基酸更是有害生物胺的前体[33],如组氨酸在组氨去羧酶的作用下转变成组胺。蛋白质的降解导致了游离氨基酸的形成[34],因此游离氨基酸的含量变化可以反映蛋白质的降解程度。不同处理方式的大菱鲆冰温贮藏0、15和30 d后游离氨基酸含量如表1所示。在整个贮藏期间,所有组大菱鲆的游离氨基酸的总含量均不断增加,表明随着贮藏时间的增加,大菱鲆因受到自身酶和微生物的作用,导致蛋白质被降解,其中CK组蛋白质降解速度最快。而亚麻籽胶和柠檬马鞭草精油-亚麻籽胶复合涂膜抑制了蛋白质的降解,并且C2组抑制效果最好,这可能是因为柠檬马鞭草精油具有的强抗氧化性抑制了蛋白质的降解。另外,CK组中的谷氨酸、缬氨酸、异亮氨酸、亮氨酸和组氨酸的含量在整个贮藏期间均高于其他处理组,作为异味氨基酸,较多的组氨酸含量会导致CK组中的大菱鲆产生更多的苦味,口味下降。SUN等[35]研究富含CUR/βCD乳液的鱼明胶涂层对4 ℃下贮藏的草鱼鱼片的保鲜效果,结果表明,鱼明胶涂层处理抑制了草鱼蛋白质的降解,并且经鱼明胶涂层处理的鱼片风味更佳。
表1 不同处理组的大菱鲆在贮藏期间游离氨基酸含量(mg/100 g)的变化
Table 1 Changes in FAA content (mg/100 g) of turbot with different treatments during storage period
贮藏时间组别天冬氨酸苏氨酸丝氨酸谷氨酸甘氨酸丙氨酸缬氨酸甲硫氨酸异亮氨酸02.00±0.0121.19±0.2418.42±0.0514.94±0.1441.58±0.1945.64±0.5830.06±0.421.79±0.382.89±0.7215CK13.33±1.14ab25.82±0.26a16.86±1.04a31.76±0.22a35.27±0.96a34.92±0.66de33.01±0.27a18.68±0.23a15.54±0.50aC110.09±0.39cd25.26±1.59a11.02±0.45d20.59±0.41de32.42±0.55b38.85±0.36b32.81±0.24ab17.11±0.74b12.35±0.19bC211.23±0.85c15.73±0.23d13.78±1.29b22.88±0.70c32.24±0.04b37.13±0.30c27.58±0.61e8.91±0.19d8.63±0.33dC316.24±2.06a20.03±2.18abc12.10±0.36c25.36±0.29b30.82±0.42c35.21±0.63d30.91±0.22c9.08±0.09d10.74±0.70cC414.18±2.03ab22.65±2.19ab9.40±0.16e21.11±0.32d28.01±0.01d47.74±0.29a28.36±0.11d12.54±0.15c11.20±0.05c30CK26.57±0.87a36.48±1.10a16.02±0.47a47.67±1.38a15.97±0.72d40.39±4.72b42.17±0.21a30.94±0.93ab27.69±2.36aC16.48±0.01e27.72±0.03b5.75±0.00e18.61±0.04c20.24±0.19c37.62±0.31b37.37±0.19b32.03±1.56a25.63±1.02abC29.81±0.21c17.71±0.54c8.43±0.27c35.84±0.30b24.19±0.09a33.58±1.66c25.49±0.30d23.85±0.17d24.65±0.13abcC311.81±0.62b25.98±2.05b10.48±0.29b18.37±1.64c14.28±0.47e29.73±2.52cd32.21±1.10c26.47±1.33c22.22±0.23dC48.25±0.61d26.53±0.25b6.44±0.07d16.16±0.50d21.34±0.56b56.37±3.51a35.69±1.95b23.60±0.53d24.59±0.15ab贮藏时间组别亮氨酸酪氨酸苯丙氨酸赖氨酸组氨酸精氨酸脯氨酸总量04.42±0.442.72±0.782.69±1.1617.81±0.522.46±0.066.44±0.558.95±0.01223.99±4.3815CK20.79±0.13a13.5±0.60a11.88±1.12de12.87±0.16a9.65±0.32a6.07±0.43b9.80±0.35a309.75±5.39aC118.66±0.05b8.83±0.93b18.06±0.19a10.96±0.37c8.23±0.16b9.49±0.86a8.14±0.15e282.87±3.99bC213.54±0.13d5.03±0.28e12.98±0.36d11.90±0.07b4.98±0.04d6.34±0.14b9.23±0.02b242.11±3.13eC311.71±0.31e7.54±0.25c15.14±0.26b10.46±0.51cd6.14±0.13c9.55±0.26a8.42±0.03d259.45±5.2cdC414.05±0.13c6.54±0.02d14.83±0.37bc11.14±0.13c6.24±0.23c9.19±0.03a8.64±0.11c265.82±3.47c30CK48.17±1.14a29.77±1.66a56.53±9.75a15.60±0.90e12.79±1.00a3.20±0.25c7.22±0.20a457.19±27.16aC139.81±2.37b29.92±0.41a54.11±0.40a32.97±2.92a9.33±0.09b3.96±0.09b3.94±0.01c385.5±2.45bC230.22±0.29e16.08±0.21d49.68±4.60ab16.81±0.02d7.44±0.17d2.46±0.24d3.58±0.14d329.82±8.40eC333.72±1.38bcd26.05±1.41bc63.26±0.38a22.47±0.83b7.61±0.51d1.81±0.00e5.36±0.56b351.81±9.87cdC436.29±1.36bc26.73±0.86b41.69±0.32c20.87±0.28c8.75±0.47c5.22±0.17a5.46±1.09b364.34±11.54c
注:同一贮藏时间不同组别之间不同小写字母表示具有显著性差异(P<0.05)。
2.6 肌原纤维蛋白的超微结构观察
已有文献[36]表明,肌原纤维的结构变化是由几种主要的肌原纤维蛋白(肌联蛋白、肌间线蛋白等)降解而导致的。本研究主要观察了第0天的新鲜样品以及贮藏20 d后不同处理组样品的肌原纤维结构变化。如图6-A所示,新鲜大菱鲆的肌原纤维结构完整、肌节规则、肌丝条纹清晰,并且Z线、M线、A带和I带清晰可见。贮藏20 d后,对照组CK和仅用亚麻籽胶处理的C1组样品的超微结构发生较大变化,如图6-B和图6-C。对照组的肌原纤维结构降解严重,主要表现为Z线、M线基本消失,A带和I带严重模糊,肌节发生崩解;C1组样品的肌原纤维结构破坏较严重,Z线和M线弱化,部分出现降解,A带和I带难以区分,肌节逐渐崩解;然而观察图6-D、图6-E、图6-F可以得出,用柠檬马鞭草精油-亚麻籽胶复合涂膜处理的样品的肌原纤维结构依然保持完整,Z线和M线出现轻微弱化,肌节部分紊乱,邻近Z线的I带减弱,这可能是由肌原纤维结合的钙蛋白酶对肌肉纤维蛋白质的水解作用造成的[37]。与对照组相比,用柠檬马鞭草精油-亚麻籽胶复合涂膜处理样品在贮藏期间较好地保持了大菱鲆肌原纤维超微结构的完整性,表明这种复合涂膜很好地抑制了肌原纤维蛋白的降解,这可能是因为柠檬马鞭草精油具有较强抗氧化性,能够保护蛋白免于变性。

A代表新鲜鱼样;B、C、D、E和F分别代表贮藏20 d后CK、C1、C2、C3和C4组的样品。比例尺为0.5 μm
图6 贮藏期间不同处理组大菱鲆肌肉超微结构的透射电镜观察
Fig.6 Transmission electron micrographs of the ultrastructure of the turbot muscle with different treatments during storage
3 结论
本实验研究了不同浓度的柠檬马鞭草精油结合亚麻籽胶形成的复合涂膜对冰温贮藏期间大菱鲆肌原纤维蛋白的影响。结果表明,与对照组相比,用柠檬马鞭草精油-亚麻籽胶复合涂膜处理鱼样能有效抑制蛋白质氧化,包括延缓总巯基含量的减少和更好地保持Ca2+-ATPase活性。同时,复合涂膜处理抑制了α-螺旋的减少和内源荧光强度的降低,稳定了蛋白质的二级结构和三级结构,以及较低的游离氨基酸含量表明复合涂膜有效地抑制了蛋白质降解。此外,通过透射电子显微镜观察可得,复合涂膜处理的样品在贮藏后期依然保持较完整的肌原纤维结构。其中,以添加质量浓度为0.128%柠檬马鞭草精油的复合涂膜保鲜效果最佳。另外,精油作为植物的次级代谢产物,对于人类消费而言是安全的,因此,柠檬马鞭草精油与亚麻籽胶结合是一种有效且具有应用前景的保鲜大菱鲆的方法。
[1] 聂小宝,杜明溪,陈东杰,等.复合保鲜剂结合冰温对大菱鲆鱼片品质的影响[J].食品研究与开发,2018,39(21):210-217.
[2] 李学鹏,陈杨,王金厢,等.冷藏大菱鲆质量指数法的建立及其货架期[J].食品科学,2016,37(14):219-224.
[3] 刘小霞,安学明,贠建民,等.蜂胶、蜂蜡复合涂膜对双孢蘑菇的保鲜研究[J].食品与发酵工业,2019,45(16):187-194.
[4] LIU J,SHIM Y Y,POTH A G,et al.Conlinin in flaxseed (Linum usitatissimum L.) gum and its contribution to emulsification properties[J].Food Hydrocolloids,2016,52:963-971.
[5] YOUSUF B,SRIVASTAVA A K.Flaxseed gum in combination with lemongrass essential oil as an effective edible coating for ready-to-eat pomeg ranate arils[J].International Journal of Biological Macromolecules,2017,104:1 030-1 038.
[6] 沈校军,姚雷,黄健.柠檬马鞭草精油含油率、组份及其抗菌作用的研究[J].香料香精化妆品,2003,(5):16-18.
[7] ISHKEH S R,ASGHARI M,SHIRZAD H,et al.Lemon verbena (Lippia citrodora) essential oil effects on antioxidant capacity and phytochemical content of raspberry (Rubus ulmifolius subsp.sanctus)[J].Scientia Horticulturae,2019,248(5):297-304.
[8] LV M C,MEI K L,ZHANG H,et al.Effects of electron beam irradiation on the biochemical properties and structure of myofibrillar protein from Tegillarca granosa meat[J].Food Chemistry,2018,254:64-69.
[9] BENJAKUL S,VISESSANQUAN W,THONQKAEW C,et al.Comparative study on physicochemical changes of muscle proteins from some tropical fish during frozen storage[J].Food Research International,2003,36(8):790-795.
[10] 鲁耀彬,熊光权,李新,等.葡聚糖延缓草鱼肌原纤维蛋白冷冻变性的机理分析[J].食品科学,2016,37(10):289-294.
[11] LI C L,PENG A,HE L C,et al.Emulsifying properties development of pork myofibrillar and sacroplasmic protein irradiated at different dose:a combined FT-IR spectroscopy and Low-field NMR study[J].Food Chemistry,2018,252:108-114.
[12] SUN Q X,CHEN Q,XIA X F,et al.Effects of ultrasound-assisted freezing at different power levels on the structure and thermal stability of common carp (Cyprinus carpio) proteins[J].Ultrasonics-Sonochemistry,2019,54(3):311-320.
[13] YU D W,XU Y S,REGENSTEIN J M,et al.The effects of edible chitosan-based coatings on flavor quality of raw grass carp (Ctenopharyngodon idellus) fillets during refrigerated storage[J].Food Chemistry,2018,242:412-420.
[14] CHEN L,FENG X C,ZHANG Y Y,et al.Effects of ultrasonic processing on caspase-3,calpain expression and myofibrillar structure of chicken during post-mortem ageing[J].Food Chemistry,2015,177(11):280-287.
[15] CHEN Q,KONG B H,HAN Q,et al.The role of bacterial fermentation in the hydrolysis and oxidation of sarcoplasmic and myofibrillar proteins in Harbin dry sausages[J].Meat Science,2016,121:196-206.
[16] PAN S K,WU S J.Effect of chitooligosaccharides on the denaturation of weever myofibrillar protein during frozen storage[J].International Journal of Biological Macromolecules,2014,65:549-552.
[17] FANG Z X,LIN D,WARNER R D,et al.Effect of gallic acid/chitosan coating on fresh pork quality in modified atmosphere packaging[J].Food Chemistry,2018,260:90-96.
[18] NIETO G,JONGBERG S,ANDERSEN M L,et al.Thiol oxidation and protein cross-link formation during chill storage of pork patties added essential oil of oregano,rosemary,or garlic[J].Meat Science,2013,95(2):177-184.
[19] 张晗,高星,宣仕芬,等.电子束辐照对鲈鱼肉肌原纤维蛋白生化特性及其构象的影响[J].食品科学,2019,40(13):81-86.
[20] KONG B H,GUO Y Y,XIA X F,et al.Cryoprotectants reduce protein oxidation and structure deterioration induced by freeze-thaw cycles in common carp (Cyprinus carpio) surimi[J].Food Biophysics,2013,8(2):104-111.
[21] MARIO E,RAMON C.Effectiveness of rosemary essential oil as an inhibitor of lipid and protein oxidation:Contradictory effects in different types of frankfurters[J].Meat Science,2006,72(2):348-355.
[22] 刁小琴,关海宁,李杨,等.高压均质对肌原纤维蛋白乳化特性及结构的影响[J].食品与机械,2019,35(4):26-30;36.
[23] HAN Z Y,ZHANG J L,ZHENG J Y,et al.The study of protein conformation and hydration characteristics of meat batters at various phase transition temperatures combined with Low-field nuclear magnetic resonance and Fourier transform infrared spectroscopy[J].Food chemistry,2019,280(9):263-269.
[24] 张秋会,黄现青,李苗云,等.傅里叶红外光谱法研究肌肉蛋白质的二级结构[J].食品与发酵工业,2015,41(10):247-251.
[25] WANG X Y,XIE J.Evaluation of water dynamics and protein changes in bigeye tuna (Thunnus obesus) during cold storage[J].LWT,2019,108(3):289-296.
[26] LIU S C,FAN W,ZHONG S Y,et al.Quality evaluation of tray-packed tilapia fillets stored at 0 ℃ based on sensory,microbiological,biochemical and physical attributes[J].African Journal of Biotechnology,2010,9(5):692-701.
[27] MARTINEZ M A,VELAZQUEZ G,CANDO D,et al.Effects of high pressure processing on protein fractions of blue crab(Callinectes sapidus) meat[J].Innovative Food Science &Emerging Technologies,2017,41(2):323-329.
[28] ZHAO X,ZHOU Y G,ZHAO L,et al.Vacuum impregnation of fish gelatin combined with grape seed extract inhibits protein oxidation and degradation of chilled tilapia fillets[J].Food Chemistry,2019,294:316-325.
[29] DONG Z Y,LI M Y,TIAN G,et al.Effects of ultrasonic pretreatment on the structure and functionality of chicken bone protein prepared by enzymatic method[J].Food Chemistry,2019,299:125 103.
[30] WANG C Y,XU F,LI D,et al.Physico-chemical and structural properties of four rice bran protein fractions based on the multiple solvent extraction method[J].Czech Journal of Food Sciences,2015,33(3):283-291.
[31] SHI J,LEI Y T,SHEN H X,et al.Effect of glazing and rosemary (Rosmarinus officinalis) extract on preservation of mud shrimp (Solenocera melantho) during frozen storage[J].Food Chemistry,2019,272(2):604-612.
[32] 曹云刚,马文慧,艾娜丝,等.不同氧化强度对肌原纤维蛋白结构及凝胶性能的影响[J].食品科学,2019,40(20):21-27.
[33] LI N,MEI J,SHEN Y,et al.Quality improvement of half-smooth tongue sole (Cynoglossus Semilaevis) fillets by chitosan coatings containing rosmarinic acid during storage[J].CyTA-Journal of Food,2018,16(1):1 018-1 029.
[34] 郝紫娜,李振兴,王甜甜,等.一卤鲜鲈鱼加工过程中蛋白质降解的分析[J].食品工业科技,2015,36(19):68-77.
[35] SUN X Y,GUO X B,JI M Y,et al.Preservative effects of fish gelatin oating eniched with CUR/βCD emulsion on grass carp (Ctenopharyngodon idellus) fillets during storage at 4 ℃[J].Food Chemistry,2019,272:643-652.
[36] KOOHMARAIE M.Biochemical factors regulating the toughening and tenderization processes of meat[J].Meat Science,1996,43(Suppl 1):0-201.
[37] HUANG M,HUANG F,XUE M,et al.The effect of active caspase-3 on degradation of chicken myofibrillar proteins and structure of myofibrils[J].Food Chemistry,2011,128(1):22-27.