块菌(truffle)是一类与树木共生的地下真菌的统称,商业上也叫做松露。在生物学分类上隶属于真菌界(Eumycetes)、子囊菌亚门(Ascomycotina)、块菌目(Tuberales)、块菌科(Tuberaceae)、块菌属(Tuber)[1]。在国外,块菌主要分布在北纬 40°~47°,海拔 100~1 000 m的地区。其中,法国北温带的科梅尔西、意大利和西班牙的温带地区等最为广泛。常见的块菌有黑孢块菌(Tuber melanosporum)、意大利白块菌(T.magnatum)、印度块菌(T.indicum)等,通常与多种宿主树种如法国的橡树(Quercus pubescens)、栎树(Q.ilex)、榛子树(Corylus avellana)等共生[2]。块菌价格昂贵,每千克达1000 美元仍然供不应求,在法国、美国和意大利块菌均享有“地下黄金”和“厨房里钻石”的美誉[3]。
在我国,块菌主要成熟于每年 10~12月。据调查,集中成熟和采收过后的块菌,由于保鲜方法不当所造成的损失率可超过 30%。块菌采后由于具有生理后熟作用,仍然能进行呼吸作用,加上子实体表面没有明显的保护结构,容易蒸腾失水,且易受到微生物的侵染而腐烂变质,失去色、香、味等,造成品质下降,为块菌产业发展带来较大的经济损失。目前,国内外对块菌储藏的方法主要是低温保鲜。研究显示,在不发生冷害的情况下,块菌子实体的保鲜时间随着温度的下降而延长,其香气成分也能更好地保留[4-7]。但是,目前却鲜有关于块菌的保鲜剂贮藏效果研究的报道[8]。因此,研究开发成本低、方便操作、安全有效的块菌保鲜剂,具有重要的应用前景。
油橄榄(Olea europaea)又名齐墩果,是世界著名的木本油料树种。20世纪 60 年代,国内开始大量引种,主栽地区涉及四川、甘肃、广西、湖北等地[9]。油橄榄鲜果被开发利用和榨油的过程中,产生的大量加工下脚料(枝、叶)却未被利用。研究显示,油橄榄枝叶中含有大量的酚类物质,具有抗菌、抗氧化等作用,却鲜有应用方面的报道[10-13]。壳聚糖是以自然界中广泛存在的甲壳素(chitin)为原料,经过脱乙酰作用得到的,是迄今为止发现的唯一天然碱性多糖,具有很好的抑菌效果和成膜性,被广泛用于水果、蔬菜以及肉类的保鲜中,具有较高的研究价值[14-17]。因此,本试验以印度块菌为研究对象,探讨橄榄叶提取物和壳聚糖复配对其保鲜效果的影响,为开发天然保鲜剂提供参考,也可为油橄榄树枝叶的高值化利用提供参考。
1 材料与方法
1.1 试验材料
新鲜印度块菌:采自凉山州会东县,挑选成熟度一致、无机械损伤、无病虫害、大小基本一致的子实体进行试验。
橄榄叶粗提物,实验室自提(多酚含量为 100 mg/g);壳聚糖(脱乙酰度>90%),索莱宝试剂公司;浓硫酸、苯酚、葡萄糖、2,6-二氯靛酚、草酸、抗坏血酸、氯化钡、酚酞、NaOH等均为分析纯,西昌迪安实业公司。
1.2 主要仪器
Tu1810紫外可见分光光度计,北京普析通用仪器有限责任公司;ME203TE电子天平,梅特勒-托利多仪器(上海)有限公司;SHB-B95真空抽滤机,上海振捷实验设备有限公司;79-2恒温磁力搅拌器,常州国华电器有限公司。
1.3 试验方法
1.3.1 橄榄叶粗提物浓度初筛及抑菌活性测定
1.3.1.1 橄榄叶粗提物质量浓度初筛
配制质量浓度为 10、20、30、40、50 g/L的橄榄叶粗提物溶液,将块菌在溶液中浸渍 20 s,取出风干,用 PE 保鲜膜包裹,于 4 ℃条件下贮藏。以无菌水处理的块菌为空白对照,储藏到第10天取样测定其失重率和总糖含量。
1.3.1.2 橄榄叶粗提物抑菌活性测定
采用滤纸片法,验证最佳浓度橄榄叶粗提物对大肠杆菌、金黄色普通球菌、白色念珠菌的抑菌活性。将 5×108 CFU/mL各菌悬液在营养琼脂培养基表面均匀涂抹 3 次,静置 15 min后,把吸有 10 μL提取液的灭菌滤纸圆片贴于涂布好菌液的培养基上,以去离子水为对照,每组 5 个平板,每个平板 3 个滤纸片,于 37 ℃培养 18 h后,测量抑菌圈直径并进行比较。
1.3.2 壳聚糖浓度初筛
配制质量浓度为5、10、15、20、25 g/L的壳聚糖溶液,并添加适量摩尔浓度为0.1 mol/L的乙酸溶液,置于磁力搅拌器上搅拌,使其充分溶解。将块菌在溶液中浸渍20 s,取出风干,用PE保鲜膜包裹,于4 ℃条件下贮藏。以无菌水处理的块菌为空白对照,储藏到第10天取样测定其失重率和总糖含量。
1.3.3 复配保鲜剂的配方筛选
在单因素试验基础上,以橄榄叶粗提物浓度和壳聚糖浓度进行两两复配,以无菌水处理的块菌为空白对照,每隔 5 d 测定失重率、总糖、Vc含量及呼吸强度,复配保鲜剂配方见表1。
表1 复配保鲜剂配方 单位:g/L
Table 1 Compounding preservative formula
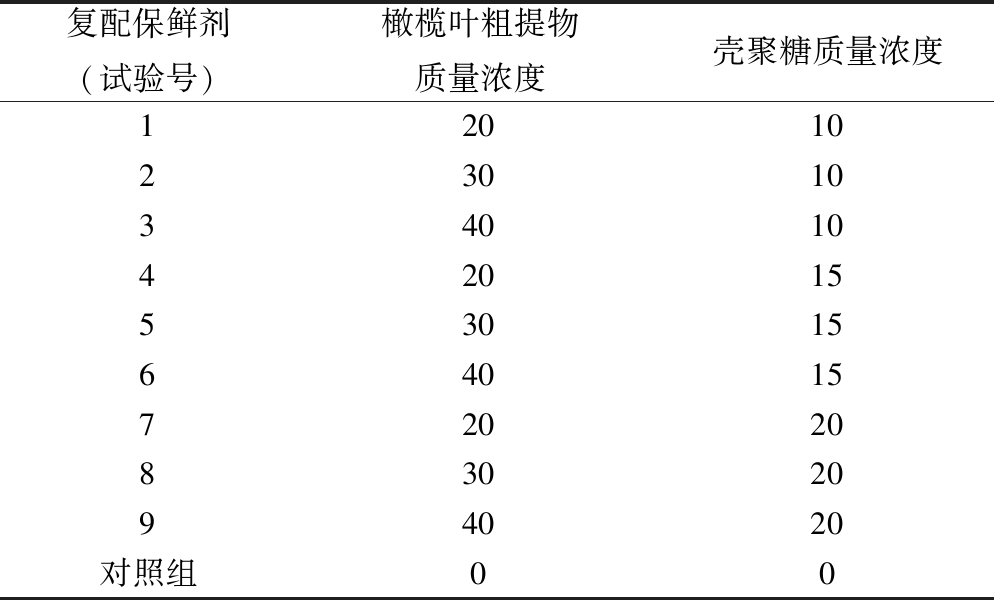
复配保鲜剂(试验号)橄榄叶粗提物质量浓度壳聚糖质量浓度120102301034010420155301564015720208302094020对照组00
1.4 测定指标和方法
1.4.1 失重率及质量保留率
采用称重法统计失重率[18]如公式(1),公式(2)所示:
失重率![]()
(1)
质量保留率/%=100%-失重率
(2)
1.4.2 总糖含量
采用硫酸苯酚比色法测定[19]。
1.4.3 Vc含量的检测
采用2,6-二氯酚靛酚法测定[20]。
1.4.4 呼吸强度的检测
采用静置法测定,室温下借助干燥器代替呼吸室[21]。
1.5 货架期品质变化模型
大多数食品的质量与时间关系表现出零级或一级的反应[22]。其中,零级和一级动力学方程分别按公式(3),公式(4)计算:
Q=Q0-k1t
(3)
Q=Q0exp(-k2t)
(4)
式中:Q,t 时刻块菌的某项指标测定值;k,块菌的某项指标测变化速率常数;Q0,块菌的某项指标测初始值。
1.6 数据分析
本试验用 SPSS 20.0 进行方差分析和多重比较,块菌货架期品质变化模型中参数值用MATLAB 2014估计。
2 结果与分析
2.1 橄榄叶粗提物浓度对块菌保鲜效果的影响
不同浓度橄榄叶粗提物处理的块菌在 4 ℃条件下贮藏 10 d 后的失重率和总糖含量变化如图1 所示。橄榄叶粗提物质量浓度在 20~40 g/L 时,与对照组相比,块菌失重率较低,而总糖含量较高。通过多重比较分析可知,橄榄叶提取物各试验组与对照组均呈显著性差异(P<0.05),其中橄榄叶粗提物浓度为 30 g/L 时,块菌的失重率最低,总糖含量最高。
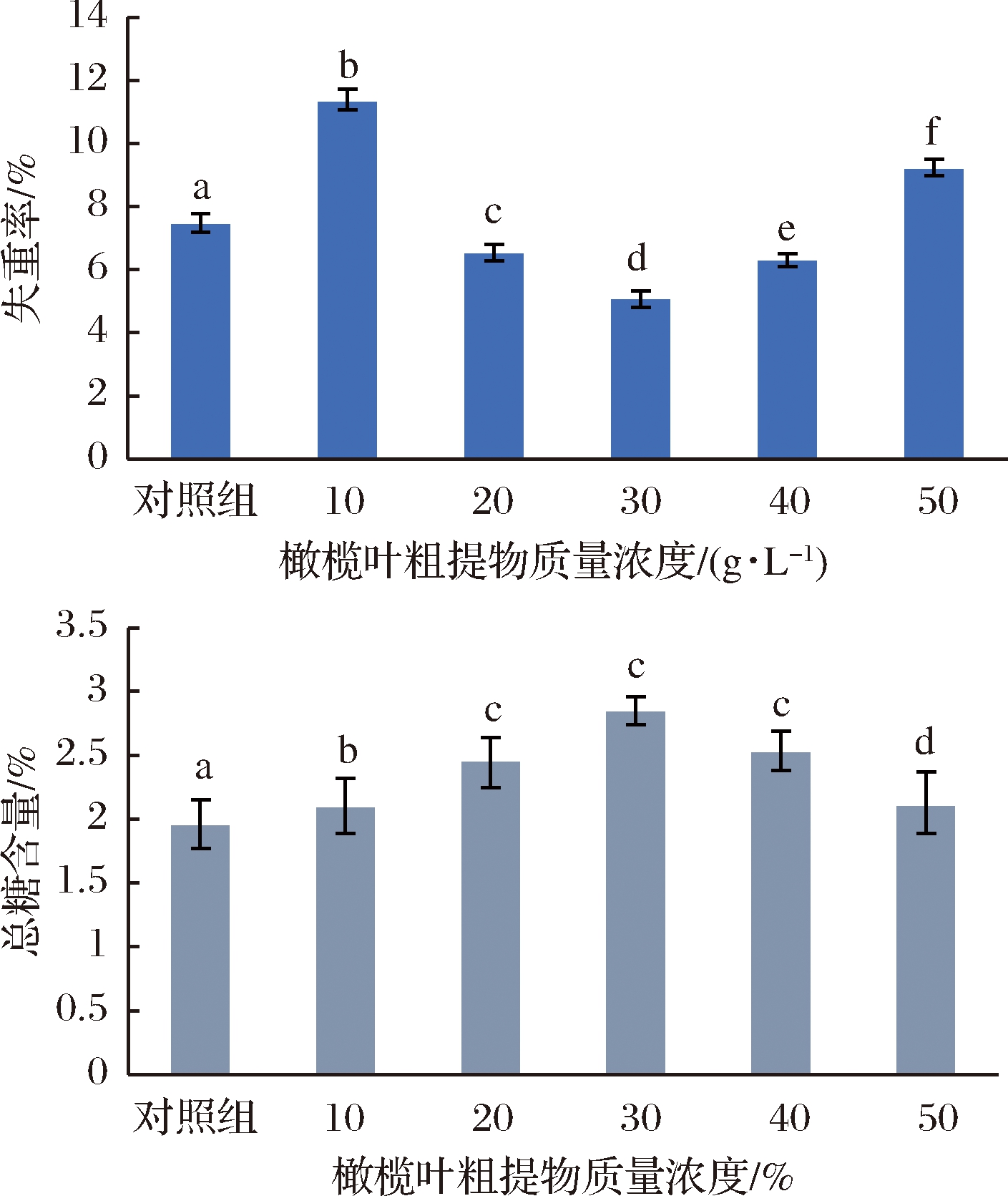
图1 不同质量浓度橄榄叶提取物对块菌失重率、总糖含量的影响
Fig.1 Effects of different concentrations of olive leaves extracts on weight loss rate and total sugar content of truffles
注:不同小写字母表示具有显著性差异(P<0.05)。下同。
2.2 橄榄叶粗提物的抑菌活性分析
橄榄叶粗提物溶液对大肠杆菌、金黄色葡萄球菌和白色念珠菌的抑菌试验结果见表2。30 g/L 橄榄叶粗提物溶液有明显抑制大肠杆菌、金黄色葡萄球菌的作用,抑菌圈直径均高于去离子水组(P<0.05)。其中,对金黄色葡萄球菌的抑制作用高于大肠杆菌。
表2 橄榄叶粗提物溶液的抑菌能力
Table 2 The antimicrobial activity of crude extracts from olive leaves
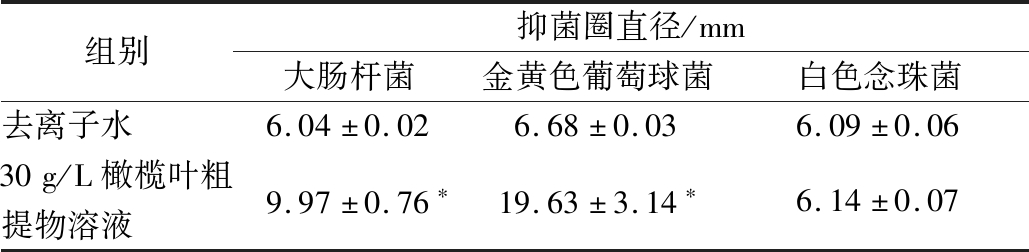
组别抑菌圈直径/mm大肠杆菌金黄色葡萄球菌白色念珠菌去离子水6.04±0.026.68±0.036.09±0.0630g/L橄榄叶粗提物溶液9.97±0.76∗19.63±3.14∗6.14±0.07
注:与去离子水组比较*表示P<0.05。
2.3 壳聚糖浓度对块菌保鲜效果的影响
不同浓度壳聚糖处理的块菌在 4 ℃条件下贮藏 10 d 后的失重率和总糖含量变化如图2所示。壳聚糖质量浓度在5~25 g/L时,与对照组相比,块菌失重率较低,而总糖含量较高。通过多重比较分析可知,壳聚糖各试验组与对照组均呈显著性差异(P<0.05)。其中,壳聚糖质量浓度为10和15 g/L 时,块菌的失重率最低,且无显著性差异,而壳聚糖质量浓度为15 g/L时,块菌总糖含量最高则更优。
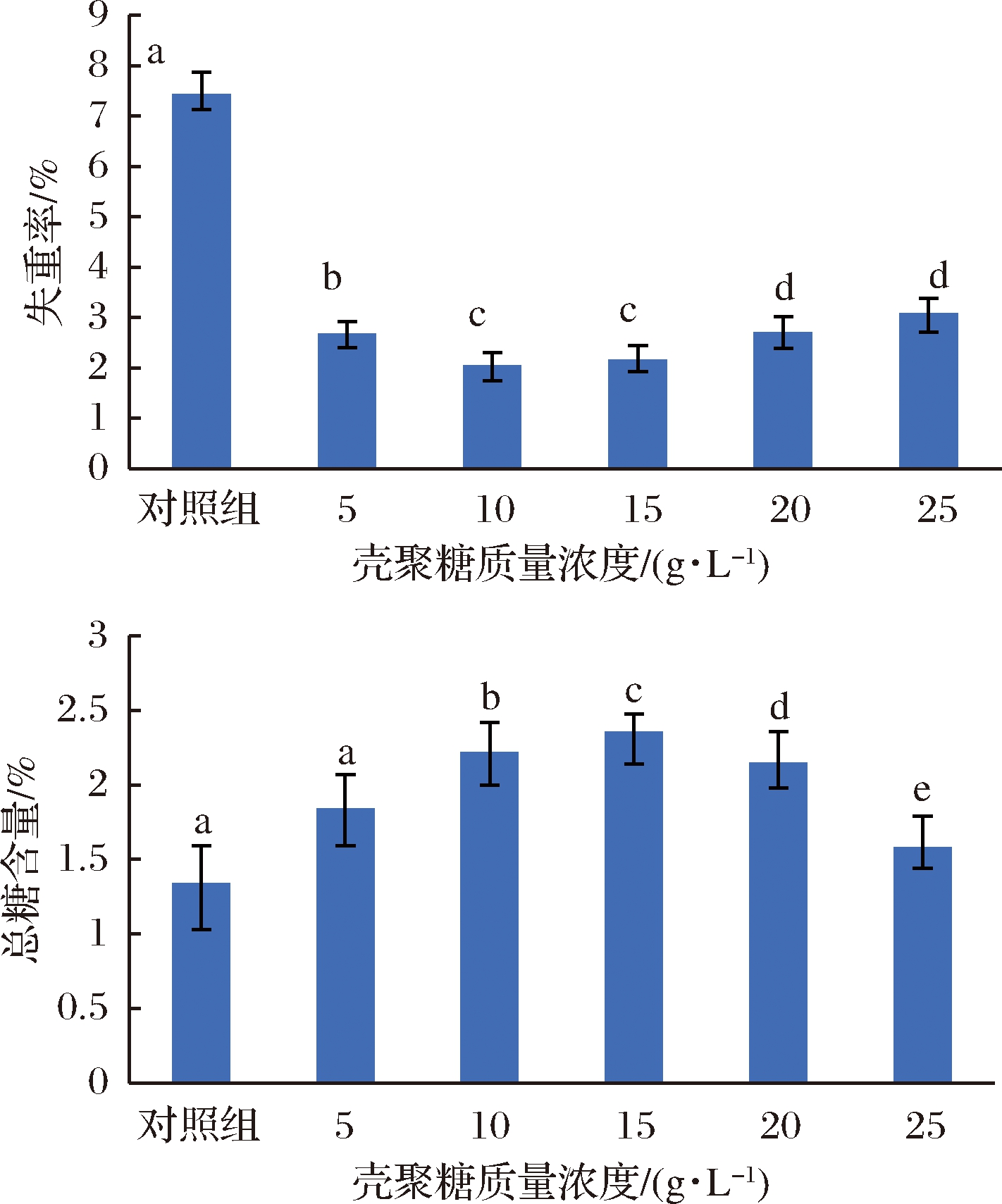
图2 不同浓度壳聚糖对块菌失重率、总糖含量的影响
Fig.2 Effects of different concentrations of chitosan on weight loss rate and total sugar content of truffles
2.4 复配保鲜剂的配方优化
2.4.1 复配保鲜剂对块菌失重率的影响
由表3 可知,随着储藏天数的增加,各组块菌的失重率也增加。但是,对照组块菌的失重率增加速度最快,与各试验组相比呈显著性差异(P<0.05)。
表3 不同复配保鲜剂配方对块菌失重率的影响
Table 3 Effects of different compounding preservatives on the weight loss rate of truffles
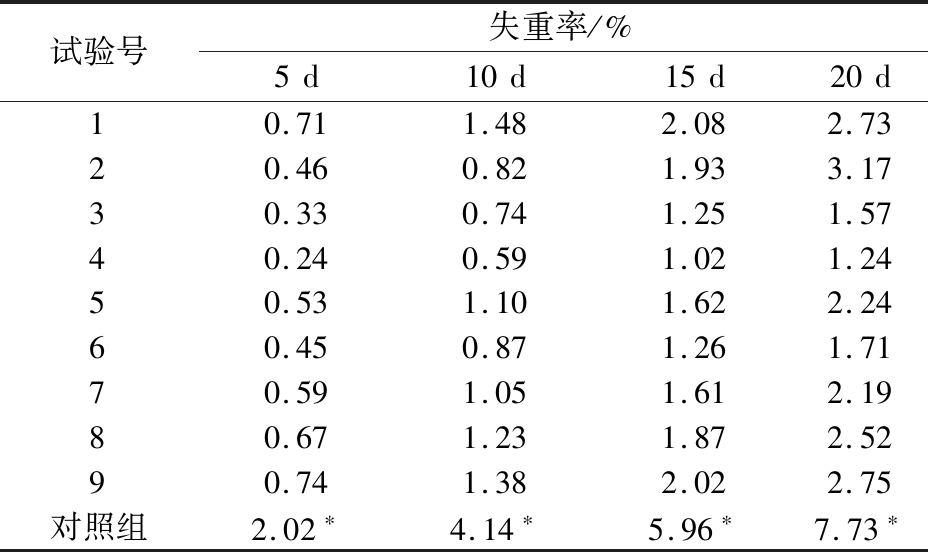
试验号失重率/%5d10d15d20d10.711.482.082.7320.460.821.933.1730.330.741.251.5740.240.591.021.2450.531.101.622.2460.450.871.261.7170.591.051.612.1980.671.231.872.5290.741.382.022.75对照组2.02∗4.14∗5.96∗7.73∗
注:与试验组比较,*表示差异显著(P<0.05)。
由此可见,橄榄叶粗提物与壳聚糖复配的保鲜剂能有效减少储藏过程中块菌水分的流失,延缓失重率的增加。其中,试验 4 组在第20天的失重率仅为 1.24%,较其他组更低。利用各试验组第20天的失重率进行交叉分组的两因素方差分析,橄榄叶粗提物与壳聚糖的交互作用如图3 所示,当橄榄叶粗提物浓度为 20 g/L、壳聚糖浓度为 15 g/L 时,块菌失重率最低,为最佳复配组合。
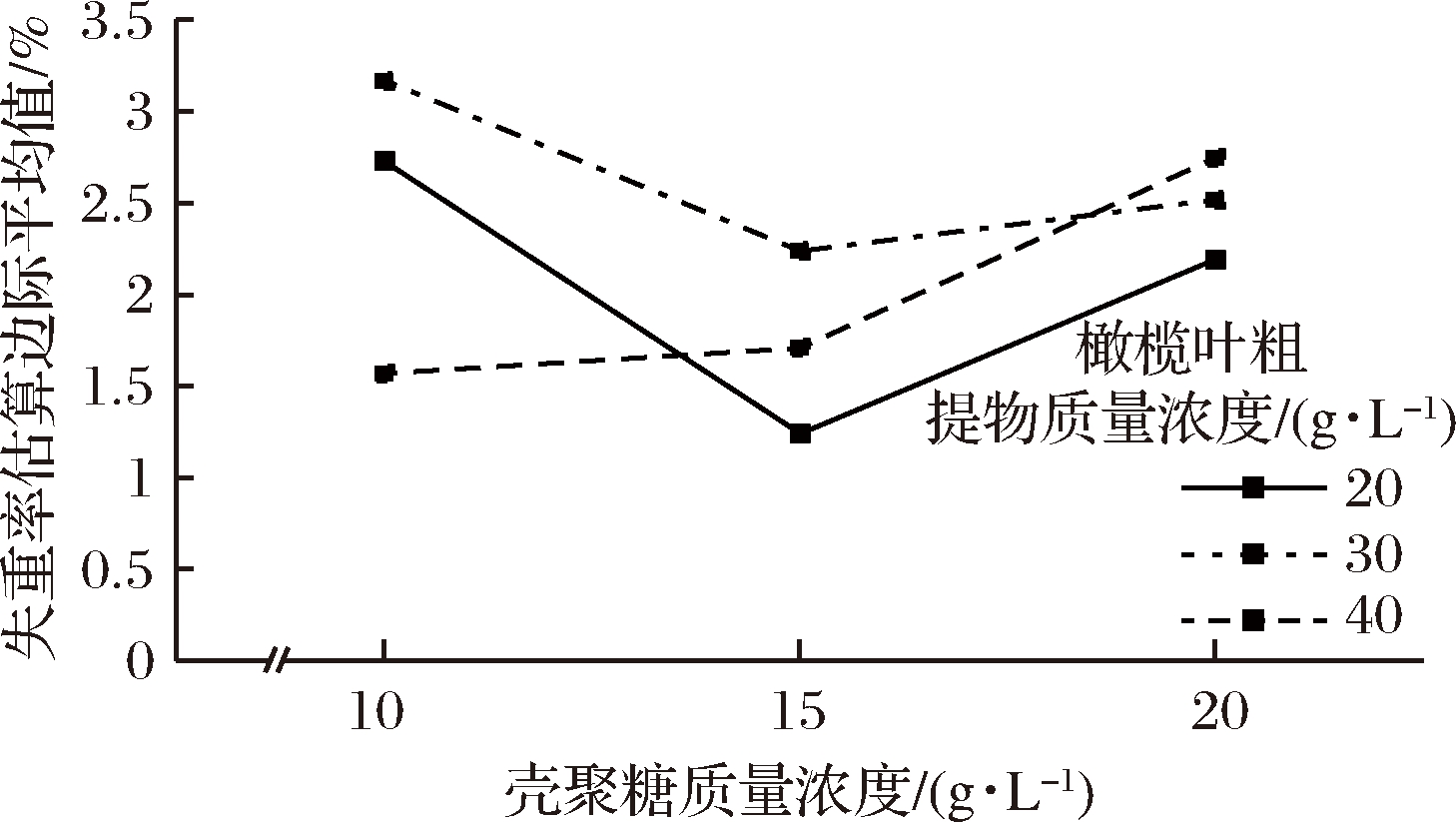
图3 复配保鲜剂对块菌失重率的交互作用
Fig.3 Interaction diagram of weight loss rate of truffles with the compound preservative
2.4.2 复配保鲜剂对块菌总糖含量的影响
由表4 可知,随着储藏天数的增加,各组块菌的总糖含量下降。与对照组相比,第 9 组无显著性差异,其他各试验组均呈显著差异(P<0.05)。橄榄叶粗提物与壳聚糖复配的保鲜剂能有效降低块菌的代谢率,降低总糖含量的损失。其中,试验4组在第20天的总糖含量为1.93%,较其他组更高。
表4 不同复配保鲜剂配方对块菌总糖含量的影响
Table 4 Effects of different compounding preservatives on total sugar content of truffles
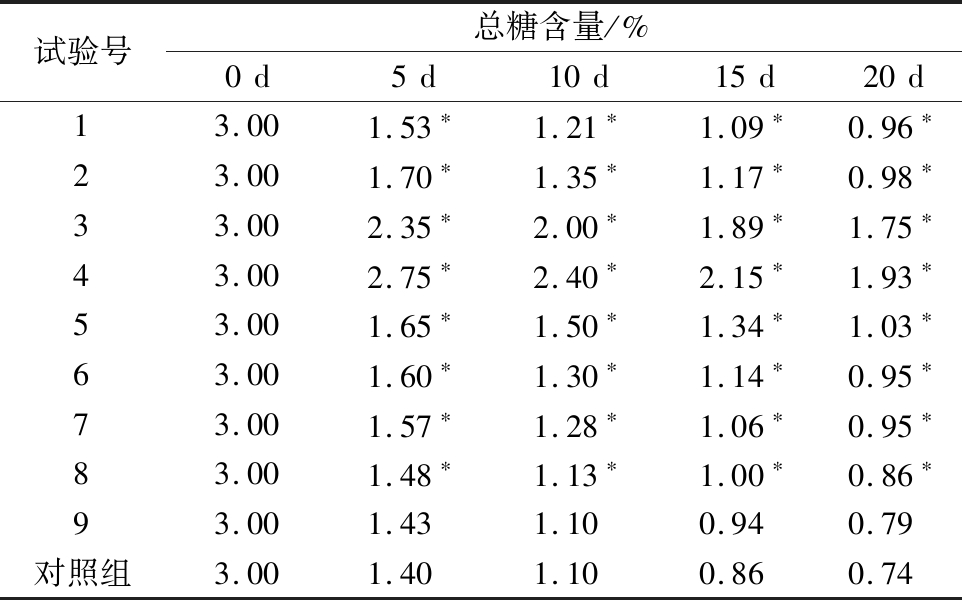
试验号总糖含量/%0d5d10d15d20d13.001.53∗1.21∗1.09∗0.96∗23.001.70∗1.35∗1.17∗0.98∗33.002.35∗2.00∗1.89∗1.75∗43.002.75∗2.40∗2.15∗1.93∗53.001.65∗1.50∗1.34∗1.03∗63.001.60∗1.30∗1.14∗0.95∗73.001.57∗1.28∗1.06∗0.95∗83.001.48∗1.13∗1.00∗0.86∗93.001.431.100.940.79对照组3.001.401.100.860.74
注:与对照组比较*P<0.05
利用各试验组第20天的总糖含量进行交叉分组的两因素方差分析,橄榄叶粗提物与壳聚糖的交互作用如图4所示,当橄榄叶粗提物浓度为20 g/L、壳聚糖浓度为15 g/L时,块菌总糖含量最高,为最佳复配组合。
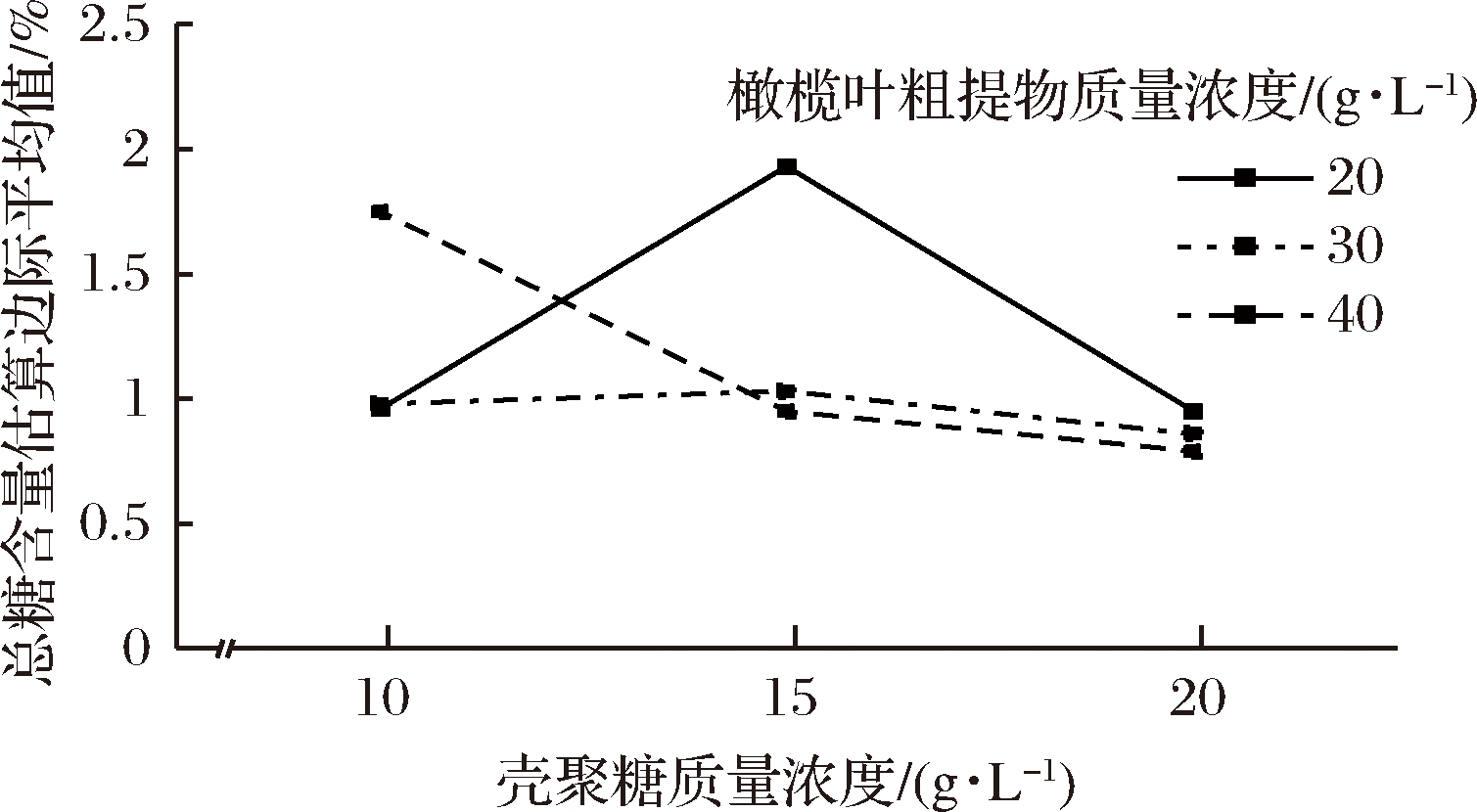
图4 复配保鲜剂对块菌总糖含量的交互作用
Fig.4 Interaction diagram of total sugar content of truffles with compound preservative
2.4.3 复配保鲜剂对块菌Vc含量的影响
由表5可知,随着储藏天数的增加,各组块菌的 Vc 含量下降。与对照组相比,第 7、8、9 组无显著性差异,其他各试验组均呈显著差异(P<0.05)。橄榄叶粗提物与壳聚糖复配的保鲜剂可以有效的抑制块菌在储藏期间 Vc 的分解。其中,试验 4 组在第20天的 Vc 含量为 1.8 mg/100 g,较其他组更高。
表5 不同复配保鲜剂对块菌Vc含量影响
Table 5 Effects of different compounding preservatives on Vc content of truffles
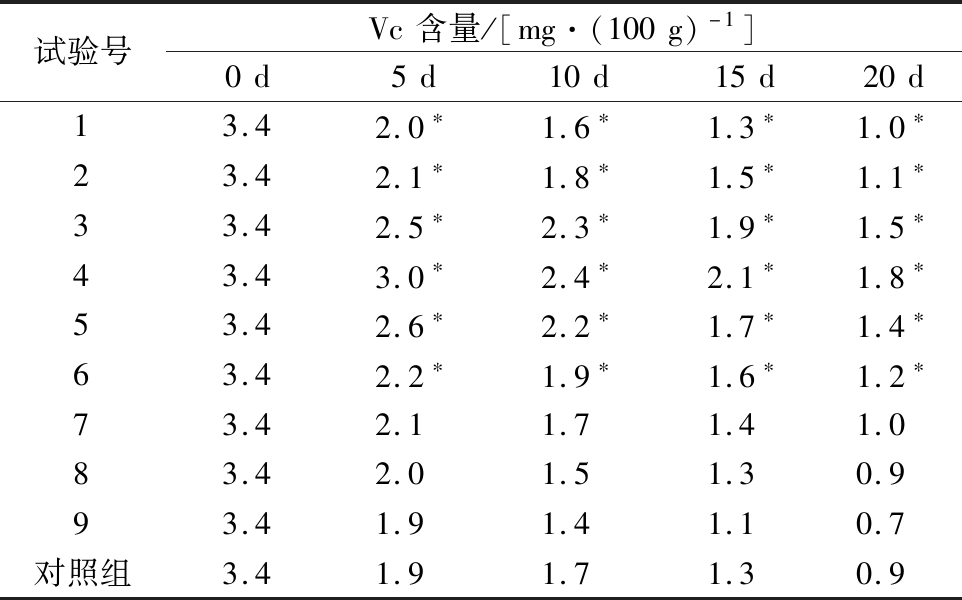
试验号Vc含量/[mg·(100g)-1]0d5d10d15d20d13.42.0∗1.6∗1.3∗1.0∗23.42.1∗1.8∗1.5∗1.1∗33.42.5∗2.3∗1.9∗1.5∗43.43.0∗2.4∗2.1∗1.8∗53.42.6∗2.2∗1.7∗1.4∗63.42.2∗1.9∗1.6∗1.2∗73.42.11.71.41.083.42.01.51.30.993.41.91.41.10.7对照组3.41.91.71.30.9
注:与对照组比较*P<0.05
利用各试验组第20天的Vc含量进行交叉分组的两因素方差分析,橄榄叶粗提物与壳聚糖的交互作用如图5所示,当橄榄叶粗提物浓度为20 g/L、壳聚糖浓度为15 g/L时,块菌Vc含量最高,为最佳复配组合。
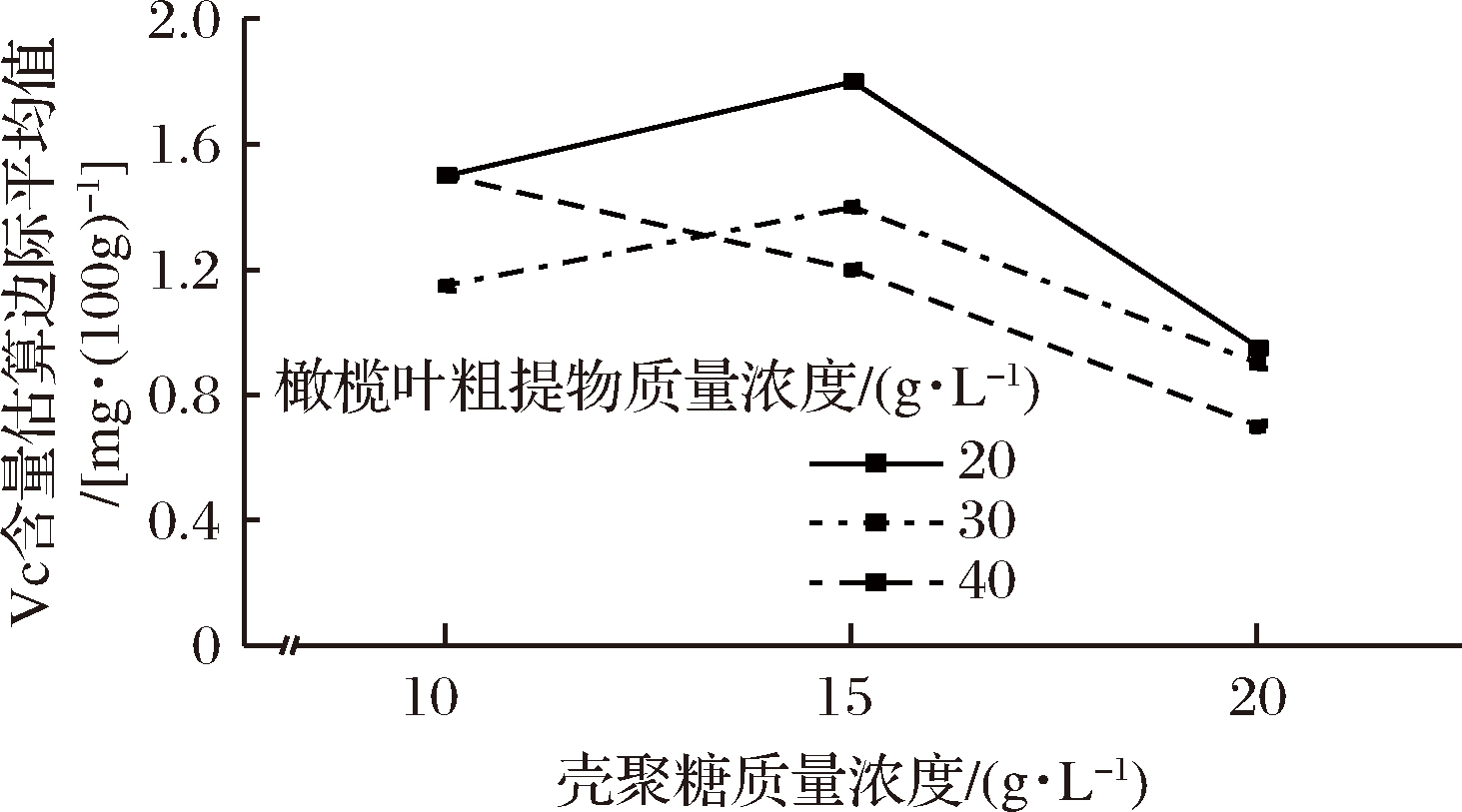
图5 复配保鲜剂对块菌Vc含量的交互作用
Fig.5 Interaction diagram of Vc content in truffles with compound preservative
2.4.4 复配保鲜剂对块菌呼吸强度的影响
由表6可知,随着储藏天数的增加,各组块菌的呼吸强度也增加,而对照组块菌的呼吸强度上升速度最快。与对照组相比,橄榄叶粗提物与壳聚糖复配的保鲜剂能抑制块菌的呼吸作用,但无显著性差异。其中,试验3组在第20天的呼吸强度为161 mg/(kg·h),较其他组更低。
表6 不同复配保鲜剂对块菌呼吸强度影响
Table 6 Effects of different compounding preservatives on respiratory intensity of truffles
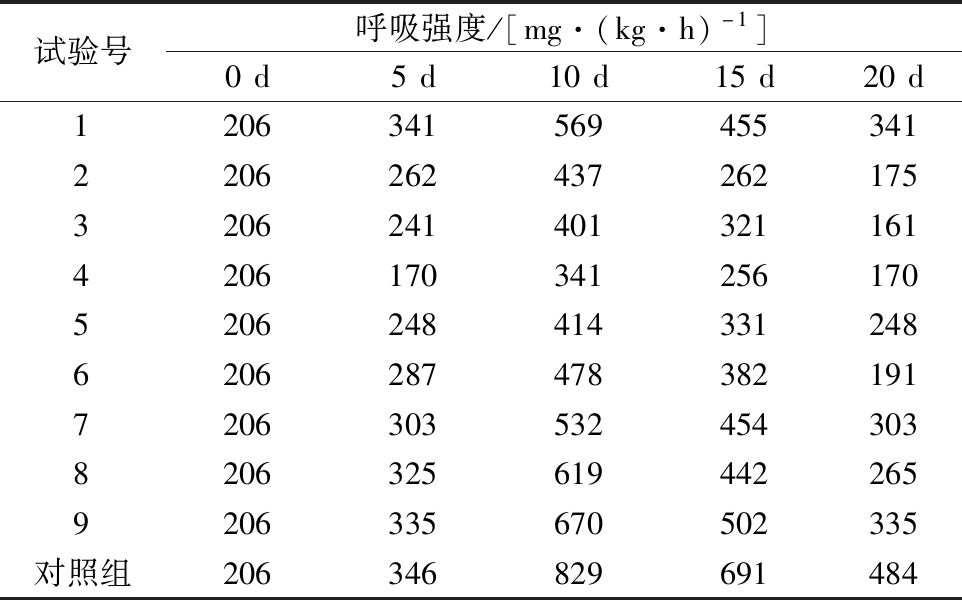
试验号呼吸强度/[mg·(kg·h)-1]0d5d10d15d20d120634156945534122062624372621753206241401321161420617034125617052062484143312486206287478382191720630353245430382063256194422659206335670502335对照组206346829691484
利用各试验组第20天的Vc含量进行交叉分组的两因素方差分析,橄榄叶粗提物与壳聚糖的交互作用如图6所示,当橄榄叶粗提物浓度为40 g/L、壳聚糖浓度为10 g/L时,块菌的呼吸强度最低。结合储藏过程中失重率、总糖含量、Vc含量的变化,确定最佳复配组合为橄榄叶粗提物20 g/L、壳聚糖 15 g/L。
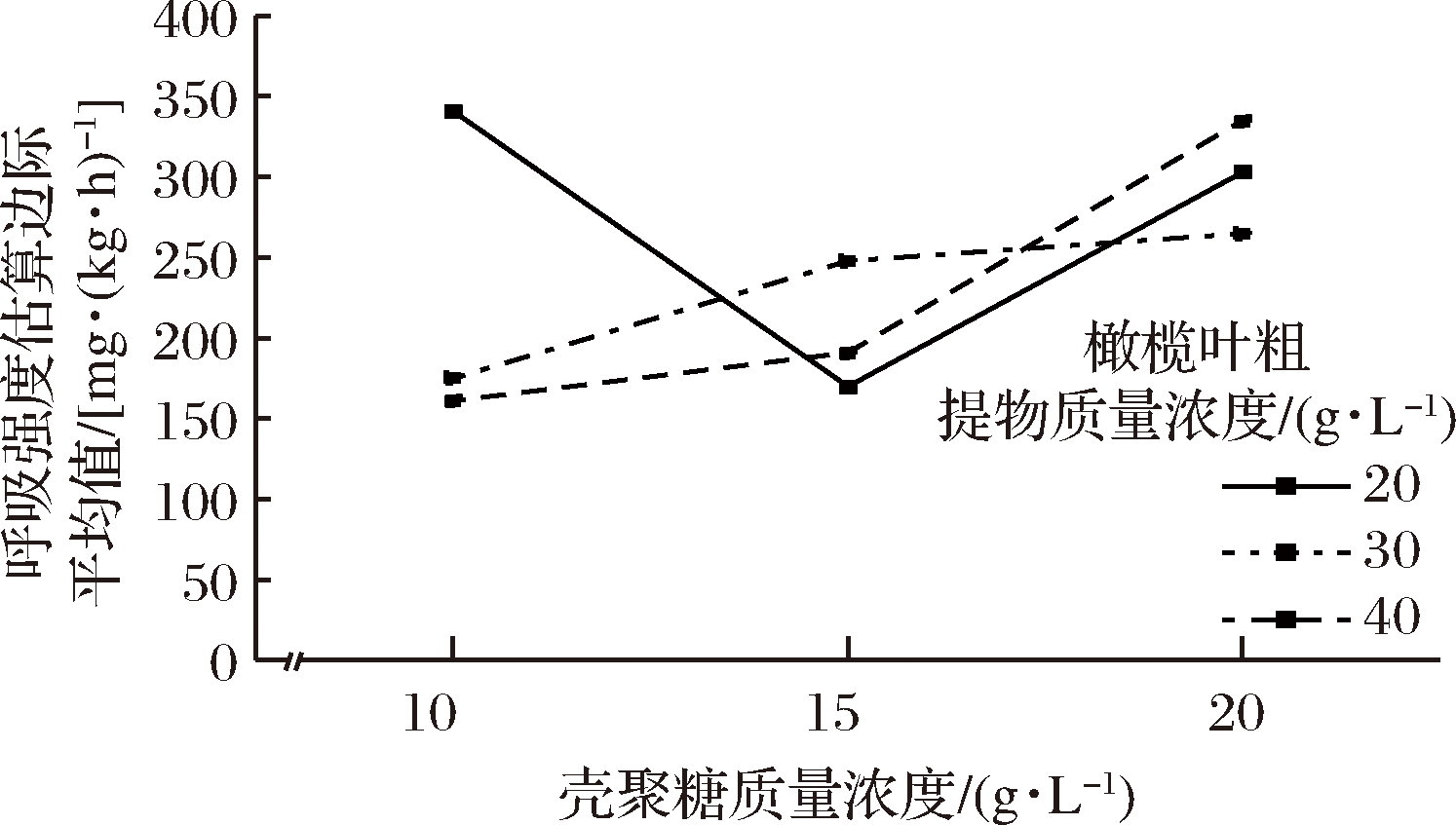
图6 复配保鲜剂对块菌呼吸强度的交互作用
Fig.6 Interaction diagram of respiratory intensity of truffles with compound preservative
2.5 复配保鲜剂对块菌货架期品质变化模型的预测结果
通过 MATLAB 软件对块菌的质量保留率、总糖含量、Vc 含量和呼吸强度进行货架期拟合。其中,在储藏期内块菌质量保留率的变化符合零级动力学模型,Vc 含量的变化符合一级动力学模型。因此,以质量保留率、Vc 含量计算最佳复配保鲜剂处理后,块菌的货架期如表7 所示。以块菌质量保留率下降3%为品质终点时的货架期为44 d,与对照组相比,货架期延长了36 d;以块菌Vc含量下降50%为品质终点时的货架期为 21 d,与对照组相比,货架期延长了11 d。分析结果表明,橄榄叶粗提物 20 g/L,壳聚糖 15 g/L的复配保鲜剂能有效地对块菌进行保鲜,提升品质,延长块菌的货架期。
表7 不同品质终点的块菌货架期
Table 7 Shelf life of truffles with different quality end points

处理质量保留率k1值Vc含量k2值货架期/d(质量保留率下降3%)货架期/d(Vc含量下降50%)橄榄叶粗提物20g/L+壳聚糖15g/L0.06860.03284421对照组0.37900.0677810
3 结论
本试验主要研究橄榄叶粗提物与壳聚糖复配的复合保鲜剂对块菌保鲜效果的影响。以块菌的失重率和总糖含量为指标,通过单因素试验筛选,确定最佳橄榄叶粗提物浓度为 30 g/L,最佳壳聚糖浓度为 15 g/L。通过抑菌试验研究发现,30 g/L 橄榄叶提取物对大肠杆菌、金黄色葡萄球菌均有显著的抑制效果(P<0.05),对金黄色葡萄球菌的抑制作用高于大肠杆菌,具有作为天然抑菌保鲜剂研究和开发的价值。由于复配处理的最佳组合并非单个最佳剂量的简单相加,而常表现出不同用量的协同增效作用,因而两两组合采用单因素试验获得的最好水平并适当扩大剂量范围。
通过复配试验研究发现,当橄榄叶粗提物浓度为20 g/L、壳聚糖为 15 g/L 时能有效提升块菌在储藏过程中的品质,降低块菌失重率和呼吸强度,维持其总糖含量和 Vc 含量。对该配方的货架期预测显示,与未处理块菌相比,以质量保留率下降 3% 为品质终点的货架期预计可延长 36 d,以 Vc 含量下降 50% 为品质终点的货架期预计可延长 11 d,具有进一步研究和开发的价值。
[1] 清源,戢林,李廷轩,等.适宜印度块菌生长的地形和土壤因子[J].应用生态学报,2015,26(6):1 793-1 800.
[2] 陈娟,邓晓娟,刘培贵.块菌属研究概况和重要进展[J].微生物学通报,2009,36(7):1 013-1 018.
[3] 过敏,唐丽薇,严金平,等.块菌主要生理活性及活性物质生产的研究进展[J].食品工业科技,2012,33(21):403-407.
[4] SAVINI S,LOIZZO M R,TUNDIS R,et al.Fresh refrigerated Tuber melanosporum truffle:effect of the storage conditions on the antioxidant profile,antioxidant activity and volatile profile[J].European Food Research and Technology,2017,243(12):2 255-2 263.
[5] MARCO P,CAMPO E,ORIA R,et al.Effect of lyophilisation in the black truffle (Tuber melanosporum) aroma:a comparison with other long-term preservation treatments (freezing and sterilization)[J].Acta Horticulturae,2018(1 194):831-838.
[6] 唐平,柳成益,杨梅,等.印度块菌冷库保鲜技术研究[J].食用菌,2014,36(3):70-72.
[7] SALTARELLI R,CECCAROLI P,CESARI P,et al.Effect of storage on biochemical and microbiological parameters of edible truffle species[J].Food Chemistry,2008,109(1):8-16.
[8] 陈存坤,李少华,熊海宽,等.云南楚雄松露的采后贮藏保鲜品质研究初探[C]//第八届云南省科协学术年会论文集.中国云南楚雄彝族自治州:云南省科学技术协会,2018:212-222.
[9] 王成章,陈强,罗建军,等.中国油橄榄发展历程与产业展望[J].生物质化学工程,2013,47(2):41-46.
[10] 梁剑.三种油橄榄叶片中多酚含量的季节动态变化研究[J].北方园艺,2010(1):57-59.
[11] ORAK H ![]() M,AMAROWICZ R,et al.Genotype-related differences in the phenolic compound profile and antioxidant activity of extracts from olive (Olea europaea L.) leaves[J].Molecules,2019,24(6):1 130-1 144.
M,AMAROWICZ R,et al.Genotype-related differences in the phenolic compound profile and antioxidant activity of extracts from olive (Olea europaea L.) leaves[J].Molecules,2019,24(6):1 130-1 144.
[12] HANNACHI H,BENMOUSSA H,SAADAOUI E,et al.Optimization of ultrasound and microwave-assisted extraction of phenolic compounds from olive leaves by response surface methodology[J].Research Journal of Biotechnology,2019,14(7):28-32.
[13] PEREIRA A,FERREIRA I,MARCELINO F,et al.Phenolic compounds and antimicrobial activity of olive (Olea europaea L.Cv.Cobrançosa) leaves[J].Molecules,2007,12(5):1 153-1 162.
[14] 孙彦峰,罗爱国,冯佳,等.壳聚糖/绿球藻多糖复合膜的制备及性能研究[J].食品与发酵工业,2019,45(5):170-176.
[15] 高晓冉,刘程惠,陈立国,等.壳寡糖与茶多酚复合保鲜剂对冷鲜牛肉的保鲜效果[J].食品与发酵工业,2019,45(11):172-178.
[16] 杨涛,原双进,张润光,等.壳聚糖和噻苯咪唑处理对晋枣鲜果贮藏品质的影响[J].食品与发酵工业,2019,45(8):109-114.
[17] 范林林,李萌萌,冯叙桥,等.壳聚糖涂膜对鲜切苹果贮藏品质的影响 [J].食品科学,2014,35(22):350-355.
[18] 刘开华,邢淑婕.含茶多酚的壳聚糖涂膜对青椒的保鲜效果研究[J].中国食品添加剂,2013(2):224-228.
[19] 谢丽源,郑林用,彭卫红,等.不同包装膜对杏鲍菇冷藏品质和贮藏效果的影响[J].食品科学,2015,36(22):197-202.
[20] 刘开华,张宇航,邢淑婕.含茶多酚的壳聚糖涂膜对圣女果保鲜效果的影响[J].食品研究与开发,2014,35(2):109-112.
[21] 汪东风,张一妹,徐莹,等.壳聚糖复合膜处理对蓝莓保鲜效果的影响[J].现代食品科技,2014,30(2):62-65;41.
[22] 汪琳,应铁进.番茄果实采后贮藏过程中的颜色动力学模型及其应用[J].农业工程学报,2001,17(3):118-121.