美藤果油是一种含有丰富α-亚麻酸的功能性植物油,其α-亚麻酸含量分别是橄榄油的67.09倍、茶籽油的175.46倍、花生油的506.89倍,不饱和脂肪酸质量分数可达93%,多不饱和脂肪酸质量分数为83.73%[1-2]。研究表明,美藤果油在调节人体血脂、预防心血管疾病、增强免疫力、抗菌消炎、保养肌肤等方面具有显著疗效[3]。然而,由于美藤果油中不饱和脂肪酸含量极高,其在贮藏加工中极易发生氧化,且又因为油类物质具有水溶性差、口服利用率低等不足,大大限制了其作为功能油脂在食品中的开发应用。
纳米乳液(nanoemulsions),多指平均粒径为50~500 nm的乳液体系[4-5],是由水、油、表面活性剂或助表面活性剂等按一定比例混合,经过一定的外部能量输入(如搅拌、均质、分散、超声等)所形成的热力学稳定的胶体分散体系[6]。纳米乳液可以改善功能性油脂在水相食品中的溶解性和分散性,使功能性油脂可以应用到多相多组分的油水分散体系,如蛋黄酱、色拉酱、酸奶、功能性饮料、护肤乳液等[7-9]。除此之外,功能性油脂由于乳化后界面面积增大,有利于与消化液作用,改善了生物利用度[10]。LANE等[11]利用超声乳化法制备了藻油纳米乳液,并添加到草莓酸奶中,发现纳米乳液体系改善了DHA的吸收速率、吸收量和生物利用度。SALVIA-TRUJILLO等[12]发现番茄红素纳米乳液与番茄汁相比,更有利于番茄红素向胶束相转移,提高生物利用度。纳米乳液还可改善功能性油脂贮藏过程中的氧化程度。郑景霞等[13]报道了鱼油经纳米乳液包埋可显著提高鱼油氧化稳定性,张建润[14]也发现了南极磷虾油纳米乳液可以提高南极磷虾油的氧化稳定性。纳米乳液与其他乳液体系相比,在乳液稳定性和食品安全性等方面具有较好的优势[15-16]。
将美藤果油制作成美藤果油纳米乳液,可以解决其水溶性差、口服利用率低、贮藏和加工过程中易发生氧化变质等加工应用方面的难题,同时保留美藤果油作为功能性油脂的营养价值,有利于其作为功能性辅料在食品领域进行广泛应用。目前,有关美藤果油纳米乳液的研究鲜有报道,本实验以复合乳化剂为基质,利用高压均质法制备美藤果油纳米乳液,研究均质压力、均质次数、乳化剂的用量以及油添加量对美藤果油纳米乳液的平均粒径、多分散系数(polydispersity index, PDI)、Zeta电位和分光比(split ratio, SRI)的影响,优化制备工艺条件,并进一步评价美藤果油添加量对纳米乳液的物理稳定性和贮藏稳定性的影响,为美藤果油纳米乳液应用开发提供数据参考。
1 材料与方法
1.1 材料与仪器设备
美藤果油,普洱联众生物资源开发有限公司;硬脂酰乳酸钠、蒸馏单硬脂酸甘油脂(均为食品级),印尼春金集团;卵磷脂(食品级),安庆市中创工程技术有限责任公司。
85-2WS型磁力搅拌器,上海沪析实业有限公司;FJ200型高速分散均质搅拌器,上海弗鲁克流体机械制造有限公司;scientz-150型高压均质机,宁波新芝生物科技股份有限公司;UV-1200型紫外可见分光光度计,上海美普达仪器有限公司;Zetasizer Nano ZS90型纳米粒度及Zeta电位分析仪,英国Malvern公司;LUM6112型LUMiSizer稳定性分析测试仪,德国罗姆公司。
1.2 实验方法
1.2.1 美藤果油纳米乳液的制备
在室温25 ℃条件下,以美藤果油为油相,卵磷脂、蒸馏单硬脂酸甘油脂和硬脂酰乳酸钠以2∶2∶1的质量比混合,作为复合乳化剂制备纳米乳液。先将蒸馏单硬脂酸甘油脂和硬脂酰乳酸钠添加到70 ℃的去离子水中,利用磁力搅拌器搅拌15 min,然后添加卵磷脂进行搅拌5 min,最后添加美藤果油,进行磁力搅拌乳化15 min,搅拌过程中,转速保持在2 000 r/min。利用高速分散机10 000 r/min 分散5 min,形成粗乳液。再将制得的粗乳液在不同高压均质压力下均质不同次数, 得到相应的美藤果油纳米乳液。
1.2.2 美藤果油纳米乳液平均粒径、PDI和Zeta电位测定方法
取适量的待测乳液用去离子水稀释1 000倍后,摇晃均匀,利用Zetasizer Nano ZS90型纳米粒度及Zeta电位分析仪测定纳米乳液的粒径,PDI和Zeta电位。每个待测样品平行测定3次,取平均值。贮藏90 d粒径增长率按公式(1)计算:
粒径增长率![]()
(1)
1.2.3 美藤果油纳米乳液SRI的测定方法
用去离子水将适量的待测纳米乳液稀释1 000倍以后,利用紫外分光光度计分别在400、800 nm波长下测其吸光度A,用分光比SRI=A800/A400表示美藤果油纳米乳液的稳定性,每个待测样品平行测定3次,取平均值。
1.2.4 单因素实验
采用1.2.1所述方法制备美藤果油纳米乳液, 进行单因素实验, 考察以下因素对纳米乳液乳化性能的影响。
1.2.4.1 均质压力
固定制备条件为美藤果油添加量15%(质量分数,下同),去离子水的添加量83.25%,复合乳化剂添加量1.75%,均质2次,考察不同高压均质压力(60、70、80、90、100 MPa)对纳米乳液粒径、电位、PDI和SRI的影响。
1.2.4.2 均质次数
固定制备条件为美藤果油添加量为15%,去离子水的添加量为83.25%,复合乳化剂添加量为1.75%,取1.2.4.1得到的最优的均质压力,考察不同均质次数(2、3、4、5、6、7)对纳米乳液粒径、电位、PDI和SRI的影响。
1.2.4.3 乳化剂含量
固定制备条件为美藤果油添加量为15%,去离子水的添加量为83.25%,取1.2.4.1和1.2.4.2得到的最优的均质压力和均质次数,考察不同的复合乳化剂含量(1.5%、1.75%、2.00%、2.25%、2.50%)对纳米乳液粒径、电位、PDI和SRI的影响。
1.2.4.4 美藤果油添加量
均质压力、均质次数和乳化剂含量取1.2.4.1、1.2.4.2和1.2.4.3实验中所得到的最优值,考察不同的美藤果油添加量(5%、10%和15%)对纳米乳液粒径、电位、PDI和SRI的影响。
1.2.5 不同美藤果油添加量的纳米乳液长期物理稳定性评价
利用单因素实验得到的最优工艺制作3种美藤果油添加量(5%、10%和15%)的纳米乳液,通过LUMiSizer稳定性分析仪评估美藤果油纳米乳液的模拟长期物理稳定性。取400 μL待测纳米乳液样品均匀注入到PC管样品皿底部,温度设定为40 ℃,离心转速为4 000 r/min,样品的透射率的特征线每 30 s 记录1次,共 255 次。通过得到不同时间的样品透光率-位置图谱(指纹图),可定性分析纳米乳液的相分离行为;通过不稳定指数柱状图和曲线图,可定性分析纳米乳液样品的模拟长期物理稳定性。
1.2.6 不同美藤果油添加量的纳米乳液90 d贮藏稳定性评价
利用单因素实验得到的最优工艺制作3种美藤果油添加量(5%、10%和15%)的纳米乳液,分别在室温25 ℃和4 ℃下密封避光贮藏90 d,在0、10、20、30、40、50、60和90 d的时候,单独取出2管测定纳米乳液的粒径、电位、PDI和SRI,观察贮藏稳定性。
2 结果与分析
2.1 美藤果油纳米乳液单因素实验结果
2.1.1 均质压力对纳米乳液性质的影响
由图1可知,随着高压均质压力的增加,美藤果油纳米乳液的粒径、PDI和SRI呈现下降的趋势,Zeta电位呈现上升的趋势,表明在一定范围内随着均质压力的增加,乳液的粒径会趋向更小和更稳定。这可能是因为在高压均质过程中,均质压力越大,粗乳液受到的作用力越大,乳液乳化、细化越明显,所形成的纳米乳液的粒径就越小且均一,有利于形成均相分散体系,纳米乳液稳定性提高[13]。由于均质压力为100 MPa时对高压均质机的设备要求较高,且均质压力过高会导致乳液温度显著升高,加大油脂被氧化的风险,考虑到90与100 MPa对纳米乳液各项指标的影响相差不大,所以最终选定的高压均质压力为90 MPa。
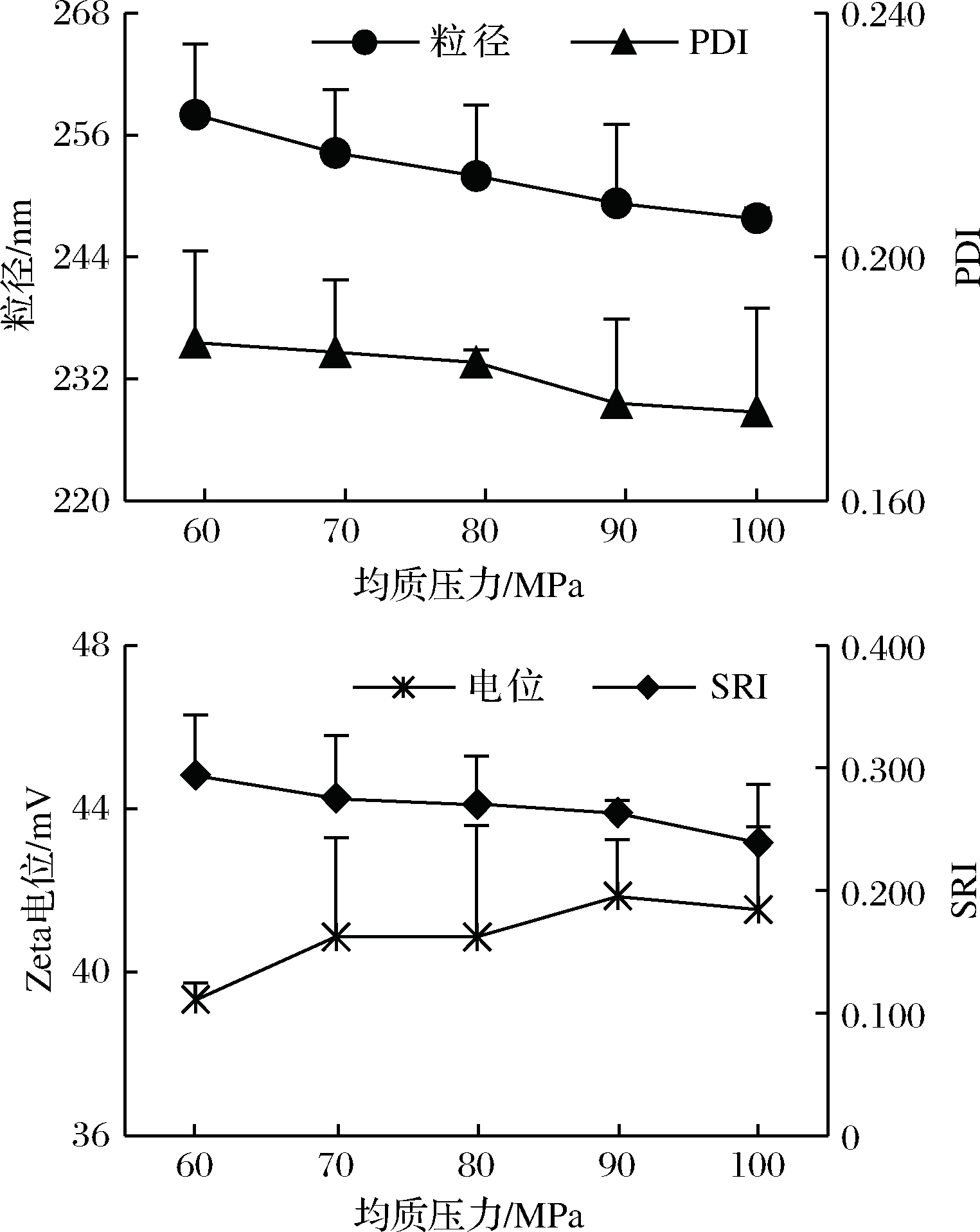
图1 不同高压均质压力下纳米乳液的平均粒径和
分散系数(PDI)、电位和分光比(SRI)
Fig.1 Effects of homogenization pressure on particle size
and PDI, zeta-potential and SRI of nanoemulsions
2.1.2 均质次数对纳米乳液性质的影响
由图2可知,随着均质次数的增加,美藤果油纳米乳液的粒径、PDI和SRI呈现下降的趋势,Zeta电位呈现上升的趋势,表明在一定范围内随着均质次数的增加,乳液的粒径会趋向更小和更稳定。这可能是因为高压均质机均质一次具有一定的破碎颗粒概率,压力在均质阀中产生的能量并不均匀,处于高能区的粒子就被破碎,而低能区的粒子不能被破碎,因此需要多次均质使得粒径破碎更均匀[17]。乳液在均质5次时,Zeta电位达到最大,SRI达到最小,随后继续增加均质次数,尽管粒径会继续减小,但是乳液会逐渐呈现一个不稳定的状态。这可能是因为随着高压均质机运转次数的增加,机械产热的温度升高,破坏了本已形成的纳米包埋运载体系,导致了乳液稳定性下降。综合考虑,最终选定均质次数为5次。
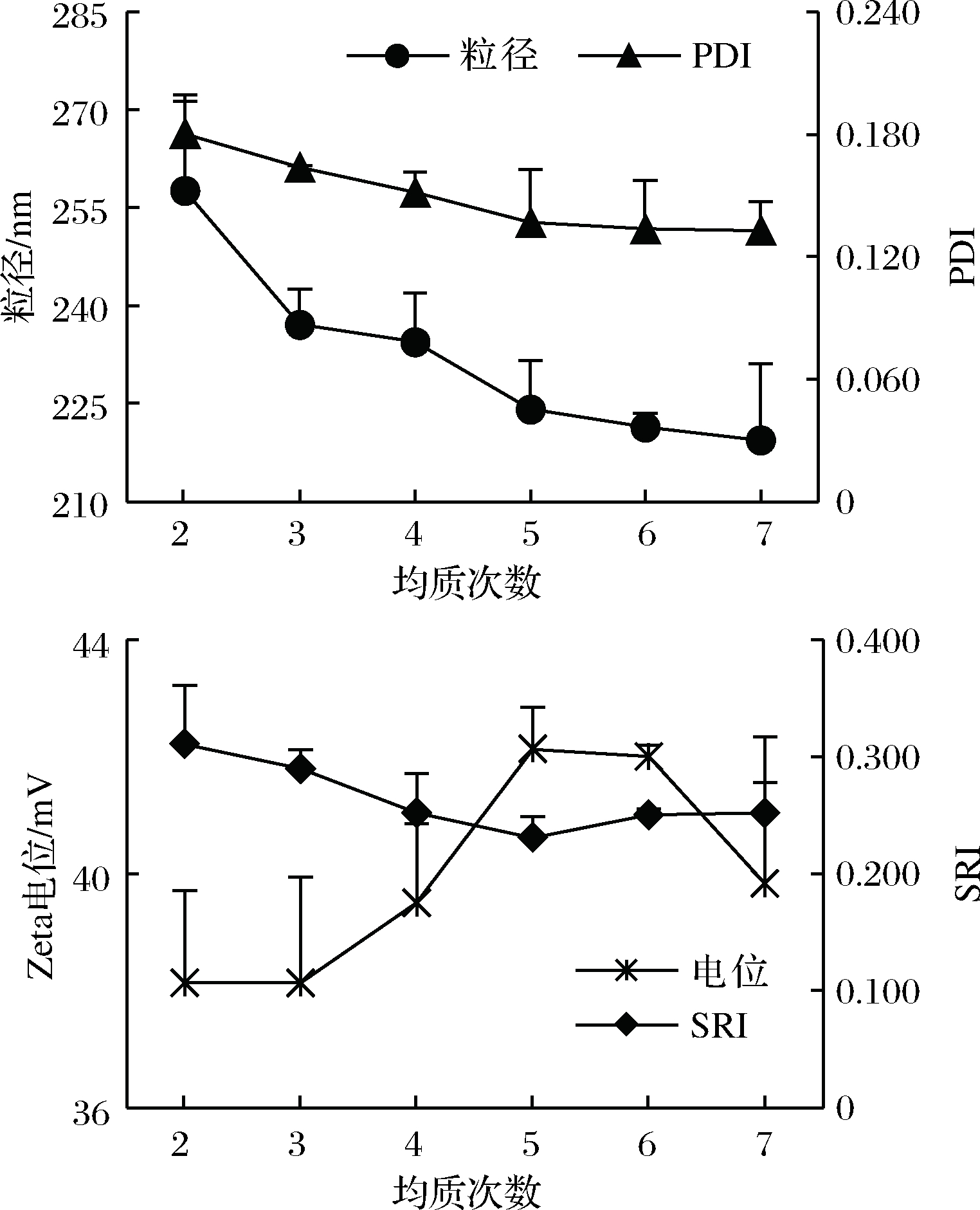
图2 不同均质次数下纳米乳液的平均粒径和
分散系数(PDI)、电位和分光比(SRI)
Fig.2 Effects of homogenization number of cycles on particle
size and PDI, zeta-potential and SRI of nanoemulsions
2.1.3 复合乳化剂含量对纳米乳液性质的影响
由图3可知,随着复合乳化剂含量的增加,美藤果油纳米乳液的粒径、PDI和SRI呈现下降的趋势,Zeta电位呈现上升的趋势,表明在一定范围内乳液的粒径会随着乳化剂含量的增加而趋向更小和更稳定。这可能是因为乳化剂可降低油水界面的界面张力,提高了界面膜的强度,并且随着浓度的增加,能够紧密包裹在油滴的表面,防止油滴发生聚合现象,增强纳米乳液的稳定性[18]。由图3可知,复合乳化剂质量分数为2.5%时,乳液的粒径最小,乳液性能最稳定,因此选定复合乳化剂质量分数为2.5%。
2.1.4 美藤果油添加量对纳米乳液性质的影响
由图4可知,随着美藤果油添加量的增加,美藤果油纳米乳液的粒径、PDI和SRI呈现上升的趋势,Zeta电位呈现下降的趋势,表明美藤果油纳米乳液的粒径会随着油添加量的增加而趋向更大和更不稳定。这可能是因为随着美藤果油添加量的增加,定量的乳化剂为了能乳化更多的油脂,需要增大所乳化的油滴体积,降低油滴与水相的接触面积,从而导致乳液体系的粒径增大,乳液稳定性下降[17, 19-20]。
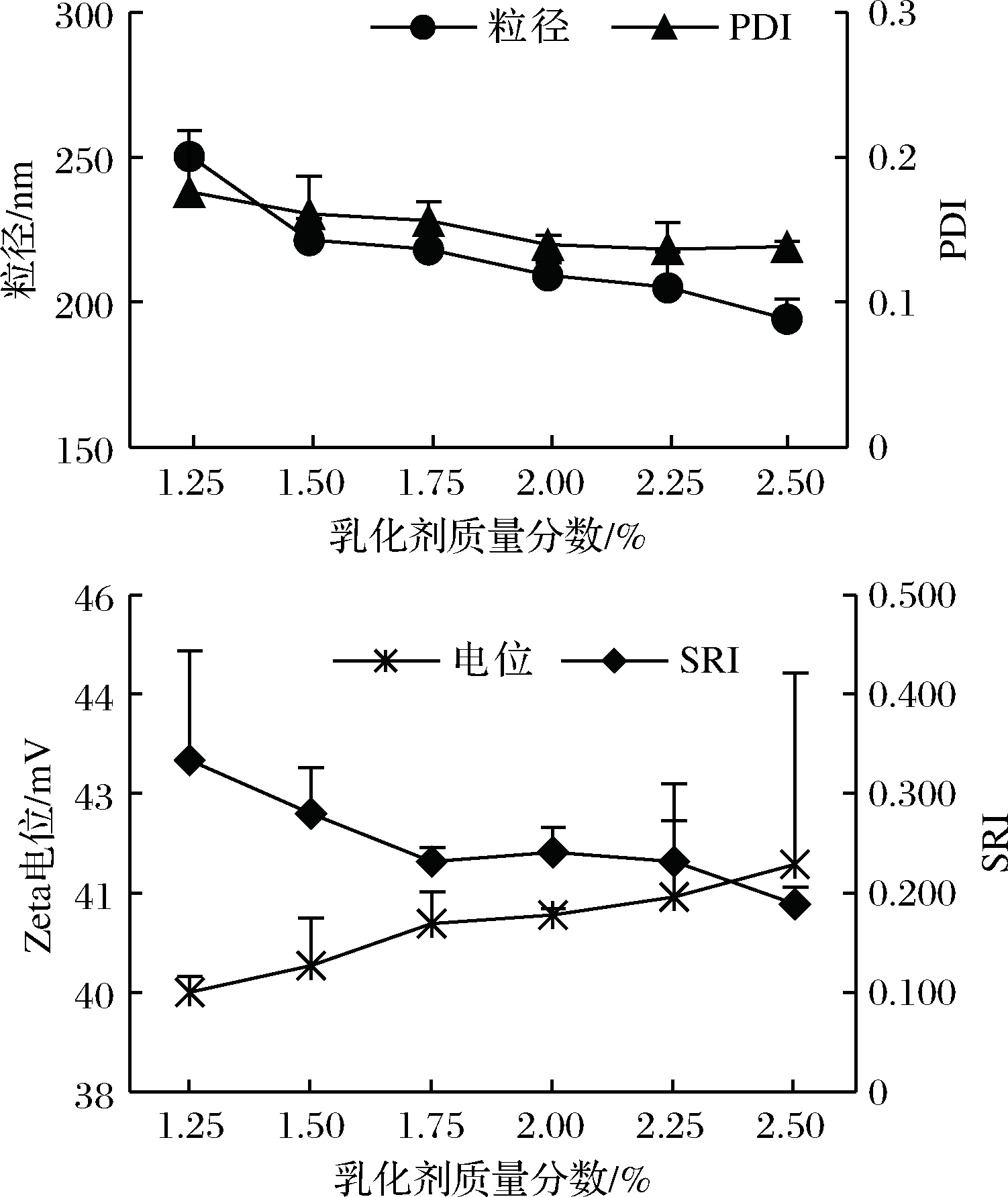
图3 不同乳化剂含量下的纳米乳液的平均粒径和
分散系数、电位和分光比
Fig.3 Effects of different emulsifier content on particle size
and PDI, zeta-potential and SRI of nanoemulsions
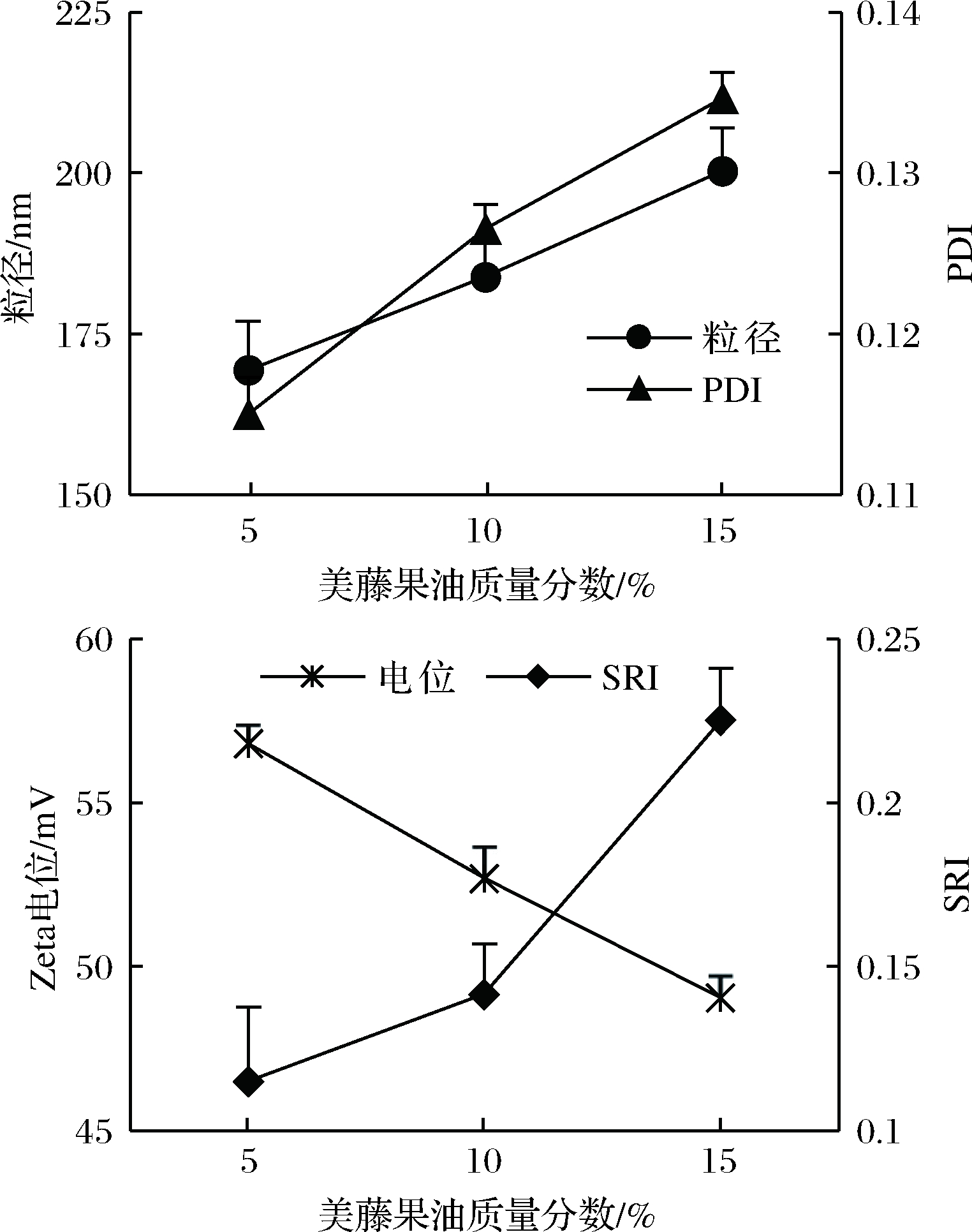
图4 不同美藤果油添加量下的纳米乳液的平均粒径和
分散系数(PDI)、电位和分光比(SRI)
Fig.4 Effects of different oil content on particle size and
PDI,zeta-potential and SRI of nanoemulsions
由图4可知,油质量分数为5%时,乳液的粒径、PDI和SRI最小,Zeta电位最大,乳液最稳定,因此最佳的美藤果油添加量为5%。
2.2 LUMiSizer分析美藤果油纳米乳液模拟长期物理稳定性结果
美藤果油添加质量分数为5%、10%和15%纳米乳液的指纹图谱见图5,透光率曲线随着时间变化由红色转变为绿色。图谱变化越大,表明纳米乳液的稳定性就越差[21]。由图5-a~5-c可以看出,美藤果油添加量为15%的纳米乳液的透光率变化最大,5%油添加量和10%油添加量透光率变化相当,表明5%和10%油添加量的纳米乳液较为稳定。乳液的稳定性还可利用不稳定指数值来量化,它与纳米乳液的稳定性成反相关,即不稳定指数越小,乳液越稳定[22]。由图5-d可以看出,随着时间的增加,3种不同美藤果油添加量的纳米乳液的不稳定指数逐渐增加,其中15%油添加量的纳米乳液不稳定性指数增加最快。由图5-e可以看出,15%油添加量的纳米乳液不稳定指数(0.631)最大,5%油添加量(0.483)和10%油添加量(0.424)的不稳定指数相当。综上结果表明,美藤果油添加量为5%和10%的纳米乳液的长期物理稳定性相对更好。
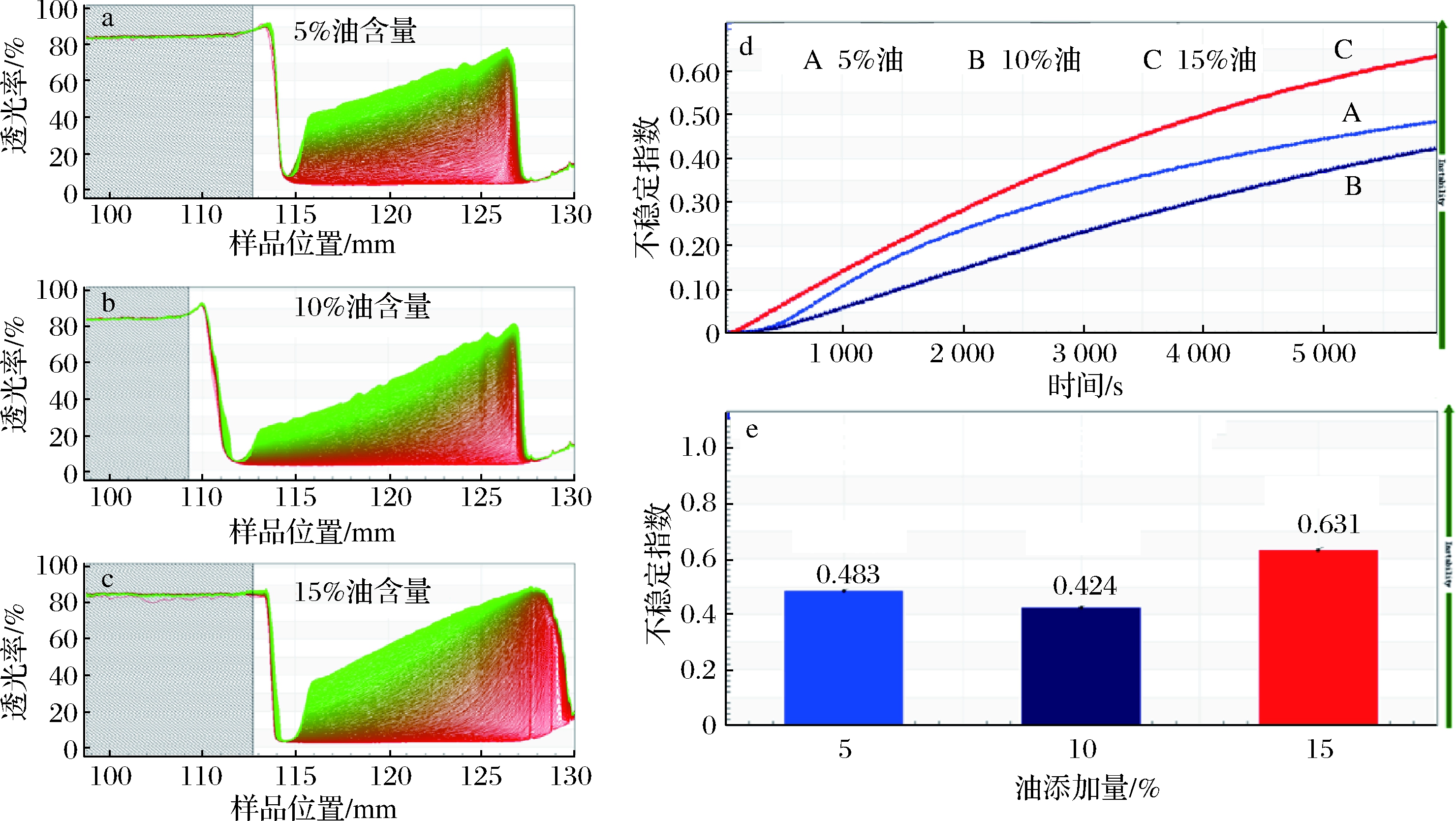
a~c-指纹图谱;d-纳米乳液的不稳定指数时间曲线图;e-柱状图
图5 LUMiSizer稳定性分析仪评价不同美藤果油添加量的纳米乳液长期物理稳定性结果
Fig.5 Physical stability test results of nanoemulsions with different oil contents
2.3 不同美藤果油添加量的纳米乳液90 d贮藏稳定性结果分析
2.3.1 粒径
由图6-a可知,随着贮藏时间的增加,不同美藤果油添加量和不同贮藏温度的纳米乳液的粒径都呈上升趋势,90 d后乳液粒径上升范围最终在18~55 nm。由图6-b可知,贮藏90 d后不同贮藏温度不同油添加量的纳米乳液粒径增长率大小排列为:4 ℃ 15%(粒径增长37.08%)>4 ℃ 10%(27.52%)>室温15%(26.77%)>4 ℃ 5%(24.74%)>室温10%(20.04%)>室温5%(10.67%)。以上结果表明,无论是室温还是4 ℃冷藏,在美藤果油添加量为5%~15%范围内,美藤果油添加量越少,纳米乳液的粒径增长越少,乳液越稳定;在贮藏温度影响方面,4 ℃冷藏乳液的粒径增长要比室温贮藏的粒径增长要大,表明美藤果油纳米乳液更适合在室温下保存。从总体上来看,所有乳液贮藏90 d后,肉眼观察没有发生分层现象,平均粒径均在300 nm以下,表明所制美藤果油纳米乳液的贮藏稳定性较好,粒径变化较少,其中美藤果油添加量为5%和10%在室温下贮藏90 d的粒径增长相对较少,表明美藤果油添加量为5%和10%的纳米乳液在室温下贮藏更为稳定。
2.3.2 PDI
PDI值表示纳米乳液的粒子分布情况,PDI值越小表示乳液粒子分布越均匀。由图7可知,随着贮藏时间的增加,不同油添加量,不同贮藏温度的纳米乳液的粒径分散系数PDI都呈现上升的趋势,表明随着贮藏时间的增加,乳液粒子逐渐变大,乳液变得不均匀。在油添加量影响方面,无论是室温还是4 ℃冷藏,美藤果油添加量为5%和10%的乳液PDI值较为接近。在贮藏温度影响方面,4 ℃冷藏的PDI增长要比室温贮藏增长要多,表明所制美藤果油纳米乳液在室温下保存粒径更均匀稳定。
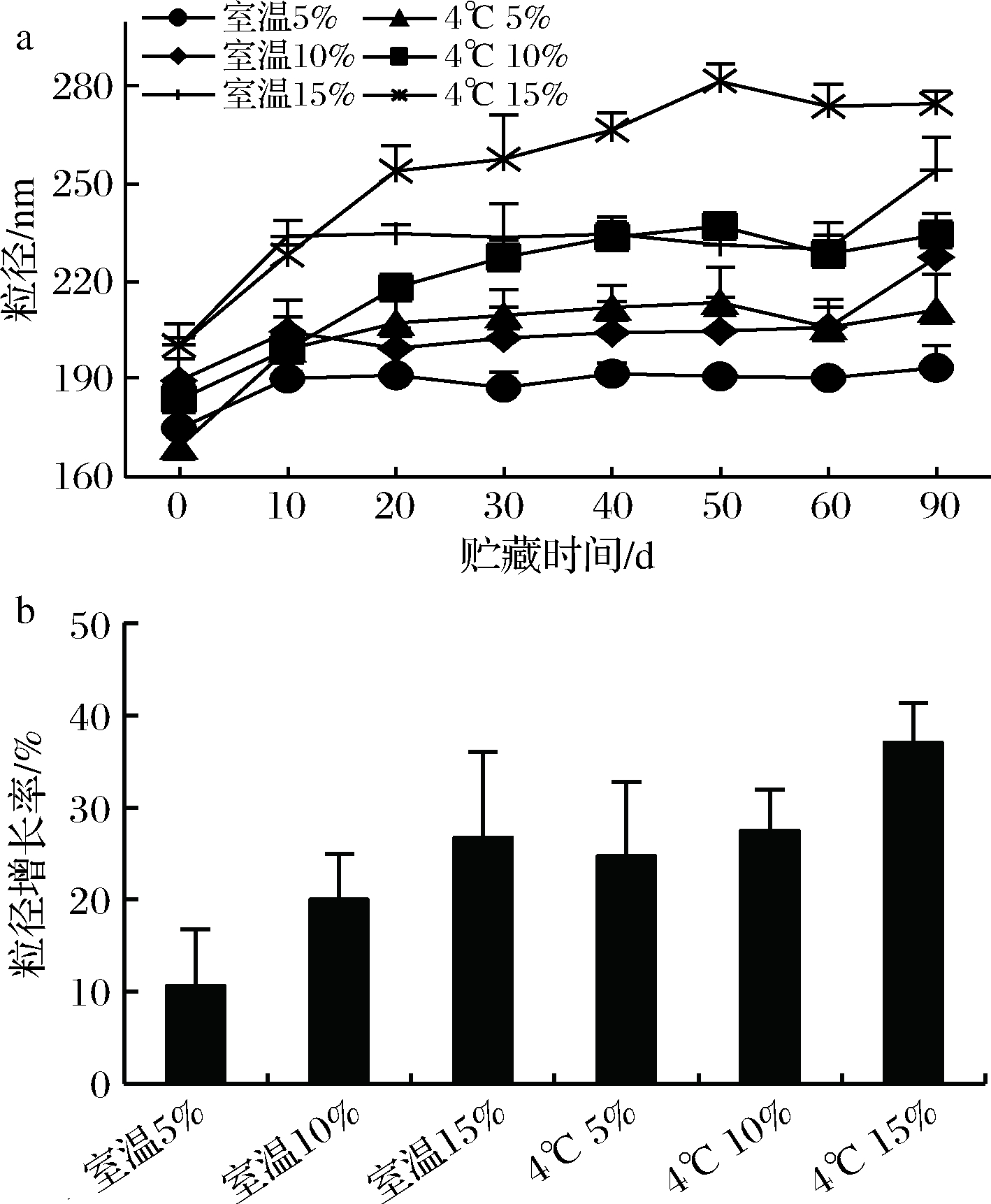
图6 不同美藤果油添加量的纳米乳液室温和4 ℃
贮藏期间粒径变化图(a)和粒径增长率(b)
Fig.6 Particle size change of sacha inchi oil nanoemulsion
with different oil content at room temperature and 4 ℃(a),
particle size charge rate(b)
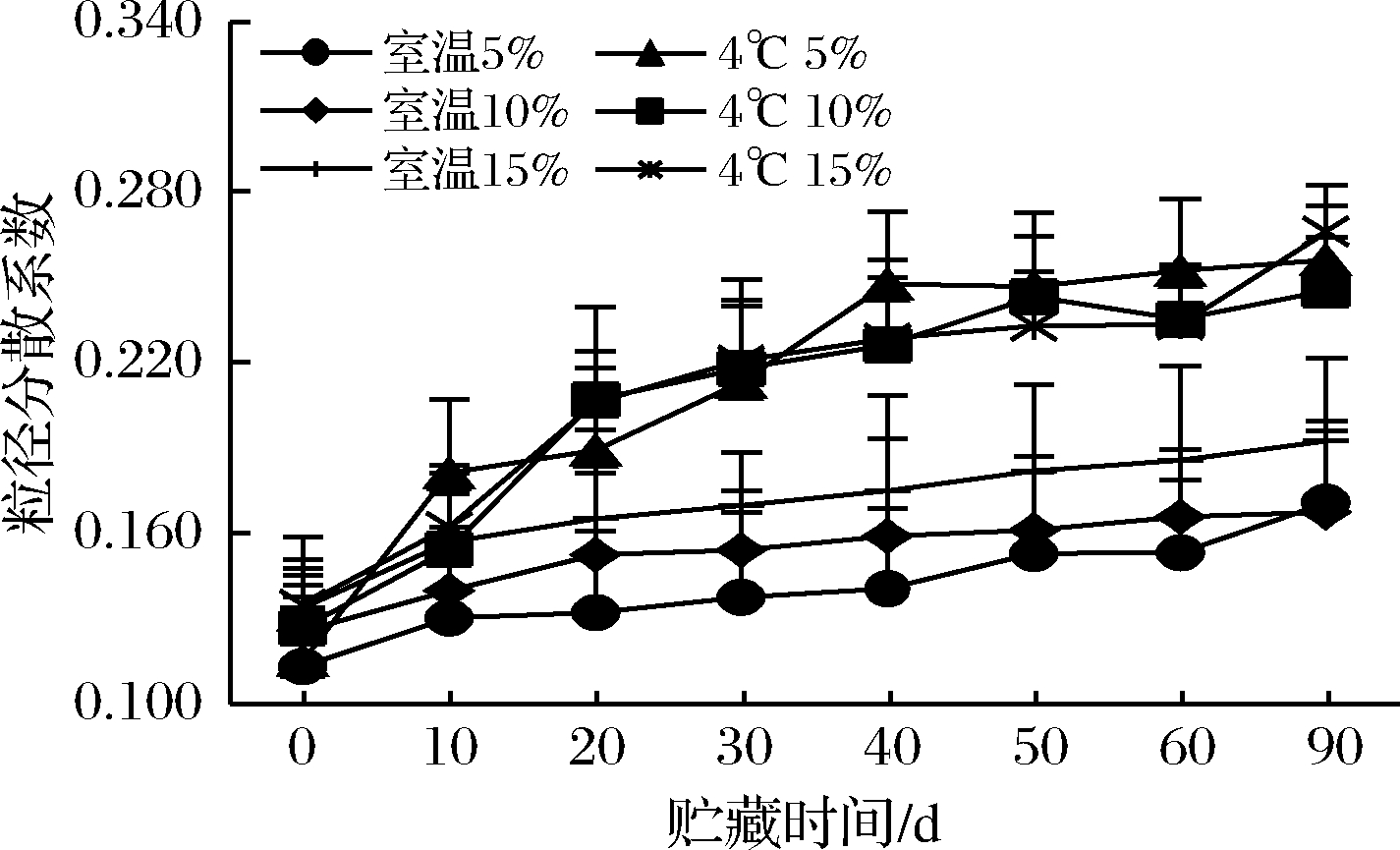
图7 不同美藤果油添加量的纳米乳液室温和4℃
贮藏期间粒径分散系数(PDI)变化图
Fig.7 PDI change of sacha inchi oil nanoemulsion
with different oil content at room temperature
and 4 ℃
从总体上来看,所有乳液贮藏90 d后,PDI值均小于0.3,表明所制美藤果油纳米乳液的分布还是相对均匀和稳定的,其中美藤果油添加量为5%和10%时,在室温下贮藏90 d的纳米乳液的PDI结果相对更好,表明美藤果油添加量为5%和10%的纳米乳液在室温下贮藏更为稳定。
2.3.3 Zeta电位
Zeta电位是用来表征油滴之间静电斥力的一种方法。从理论上来说,Zeta电位的绝对值>30 mV,表明乳液的稳定性较强。由图8可知,随着贮藏时间的增加,不同美藤果油添加量,不同贮藏温度的纳米乳液的Zeta电位都呈现下降的趋势,表明随着贮藏时间的增加,乳液粒子之间的静电斥力在逐渐变小,乳液的稳定性逐渐下降。在油添加影响方面,无论是室温还是4 ℃冷藏,5%与10%油添加量的Zeta电位较为接近,且都>15%油添加量乳液。在贮藏温度影响方面,4 ℃冷藏的纳米乳液的Zeta电位要比室温贮藏下降的多,表明所制美藤果油纳米乳液在室温下保存粒径较为稳定。从总体上来看,所有乳液贮藏90 d后,Zeta电位的绝对值均>30 mV,表明所制美藤果油纳米乳液的贮藏稳定性相对较强[23],其中美藤果油添加量为5%和10%在室温下贮藏90 d后的纳米乳液的Zeta电位相对更高,表明美藤果油添加量为5%和10%的纳米乳液在室温下贮藏更为稳定。
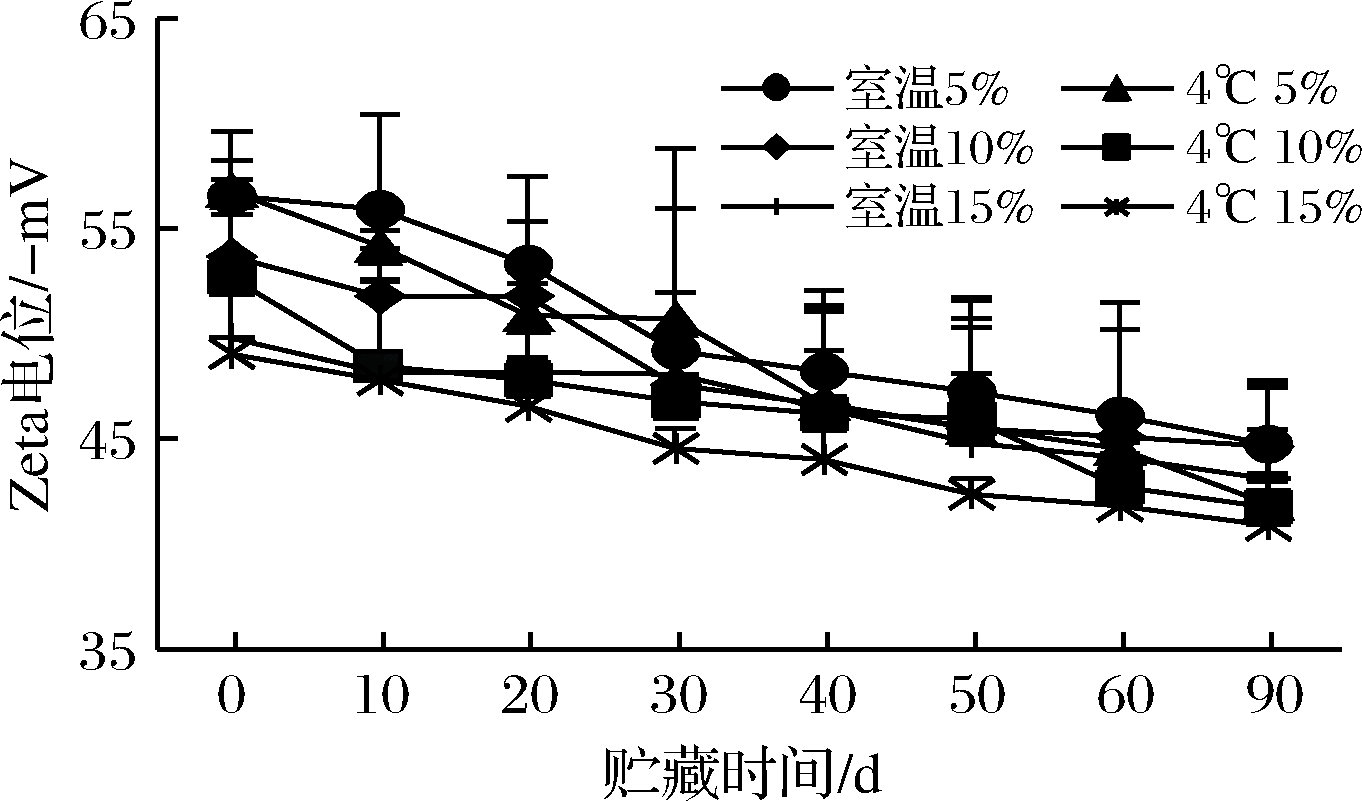
图8 不同美藤果油添加量的纳米乳液室温和4 ℃
贮藏期间Zeta电位变化图
Fig.8 Zeta-potentia change of sacha inchi oil
nanoemulsion with different oil content at room
temperature and 4 ℃
2.3.4 SRI
由图9可知,随着贮藏时间的增加,不同美藤果油添加量,不同贮藏温度的纳米乳液的SRI呈现上升的趋势,表明随着贮藏时间的增加,乳液的稳定性在逐渐下降,SRI在逐渐升高。
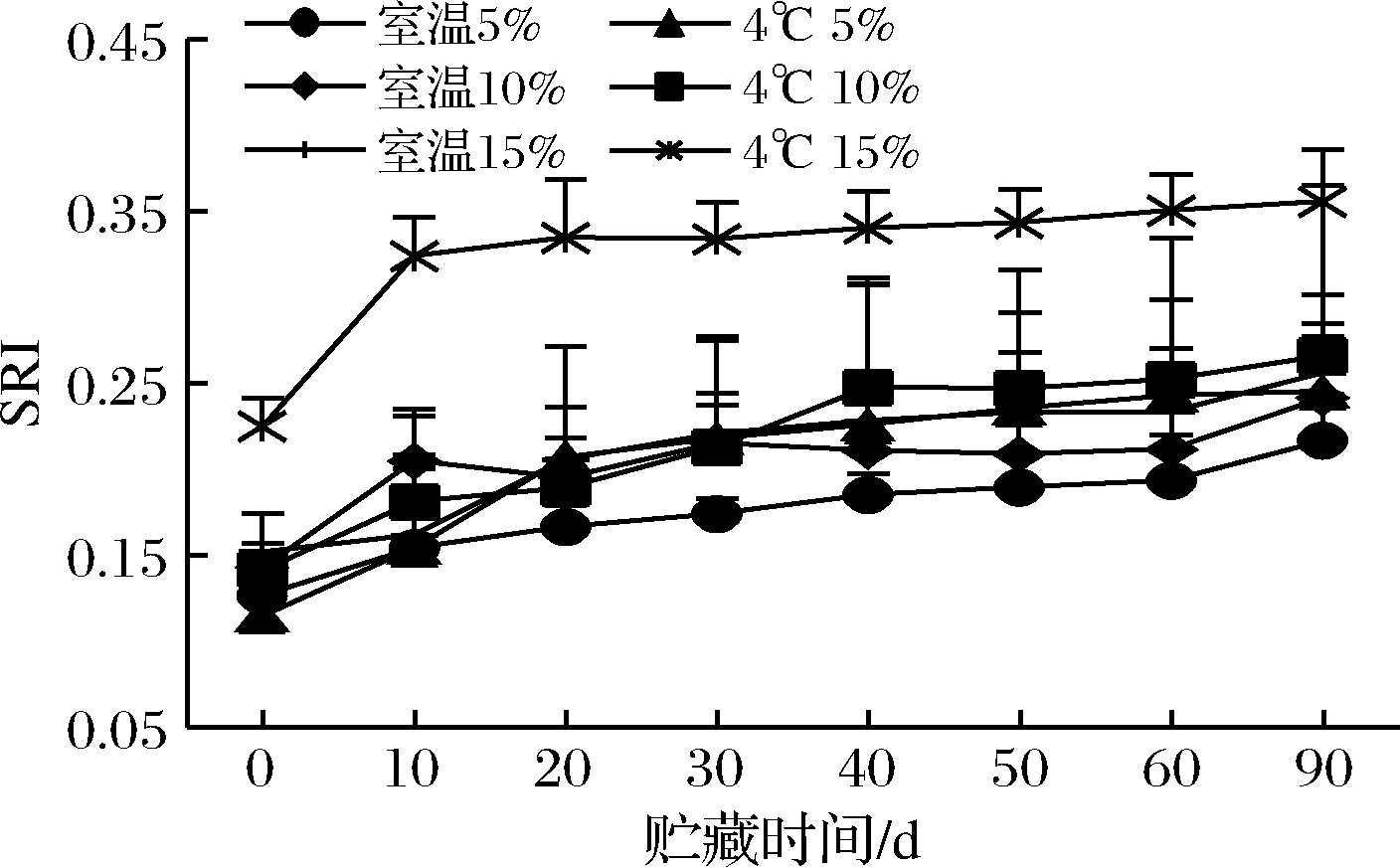
图9 不同美藤油添加量纳米乳液室温和4 ℃
贮藏期间分光比(SRI)变化图
Fig.9 Absorption ratio SRI change of sacha inchi Oil
nanoemulsion with different oil content at room
temperature and 4 ℃
在美藤果油添加量影响方面,无论是室温还是4 ℃冷藏,5%与10%油添加量的SRI较为接近,且都<15%油添加量的乳液,表明油添加量为5%和10%的纳米乳液较为稳定。在贮藏温度影响方面,4 ℃冷藏的纳米乳液的SRI要比室温贮藏高很多,表明所制美藤果油纳米乳液在室温下保存会较为稳定,所得结论与粒径、PDI、Zeta电位变化相一致。从总体上来看,所有乳液贮藏90 d后,除4 ℃冷藏油添加量为15%的纳米乳液的SRI>0.3之外,其他乳液SRI均<0.3,表明所制美藤果油纳米乳液的贮藏稳定性相对较强[24],其中美藤果油添加量为5%和10%在室温下贮藏90 d后的纳米乳液的SRI相对更小,表明美藤果油添加量为5%和10%的纳米乳液在室温下贮藏更为稳定。
3 结论
本研究经过单因素实验得到美藤果油纳米乳液的最佳工艺参数为:高压均质压力90 MPa,均质次数5次,复合乳化剂含量2.5%(蒸馏单硬脂酸甘油酯1%、卵磷脂1%、硬脂酰乳酸钠0.5%),美藤果油添加量为5%。在最佳工艺参数下制备的美藤果油纳米乳液的平均粒径为(169.33±7.60) nm,PDI为(0.115±0.02),Zeta电位为(-56.8±0.56) mV,SRI为(0.12±0.02);LUMiSizer稳定性分析、90 d室温和4 ℃贮藏稳定性实验结果显示,美藤果油添加量为5%和10%的纳米乳液的不稳定指数、粒径、PDI和SRI相对更小,Zeta电位相对更大,表明美藤果油添加量为5%和10%的纳米乳液的长期物理稳定性和贮藏稳定性更好,其中以室温下进行贮藏质量更佳。本研究所得结果为美藤果油纳米乳液产品开发及其稳定性研究提供了实验数据,同时促进了美藤果油在食品加工领域中的应用。
[1] LI P, DENG J, XIAO N, et al. Identification of polyunsaturated triacylglycerols and C![]() C location isomers in sacha inchi oil by photochemical reaction mass spectrometry combined with nuclear magnetic resonance spectroscopy[J].Food Chemistry,2020,307:125 568.
C location isomers in sacha inchi oil by photochemical reaction mass spectrometry combined with nuclear magnetic resonance spectroscopy[J].Food Chemistry,2020,307:125 568.
[2] 韩本勇,周志梅,赵鹏,等.美藤果油的组成、性质及功能特性研究进展[J].中国野生植物资源, 2019,38(3):59-64.
[3] 谢蓝华,杨勇福,陈佳,等.美藤果油的研究进展及综合利用价值分析[J].食品工业,2019,40(3):223-226.
[4] 李季楠,吴艳,胡浩,等.食品纳米乳液的研究进展[J].食品与机械,2019,35(2):217-225.
[5] ROOHINEJAD S, GREINER R, OEY I, et al. Emulsion-based systems for delivery of food active compounds: Formation, application, health and safety[M]. Hoboken: Wiley Online Library,2018.
[6] ANTON N, BENOIT J P, SAULNIER P. Design and production of nanoparticles formulated from nano-emulsion templates—a review[J].Journal of Controlled Release,2008,128(3):185-199.
[7] KWAK M, AHN H, SONG K. Rheological investigation of body cream and body lotion in actual application conditions[J].Korea-Australia Rheology Journal,2015(3):241-251.
[8] TORO-FUNES N, BOSCH-FUSTÉ J, LATORRE-MORATALLA M L, et al. Isoflavone profile and protein quality during storage of sterilised soymilk treated by ultra high pressure homogenisation[J].Food Chemistry,2015,167:78-83.
[9] 郭永生,马传国,刘君,等.美藤果油水包油型乳液的制备及其稳定性研究[J].中国油脂,2019,44(10):23-28.
[10] BOREL T, SABLIOV C M. Nanodelivery of bioactive components for food applications: types of delivery systems, properties, and their effect on ADME profiles and toxicity of nanoparticles[J].Annual Review of Food Science and Technology,2014,5:197-213.
[11] LANE K E, LI W, SMITH C, et al. The bioavailability of an omega-3-rich algal oil is improved by nanoemulsion technology using yogurt as a food vehicle[J].International Journal of Food Science & Technology,2014,49(5):1 264-1 271.
[12] SALVIA-TRUJILLO L, MCCLEMENTS D J. Enhancement of lycopene bioaccessibility from tomato juice using excipient emulsions: Influence of lipid droplet size[J].Food Chemistry,2016,210:295-304.
[13] 郑景霞,白春清,陆天洋,等.鱼油纳米乳的制备及贮藏稳定性研究[J].中国油脂,2017,42(4):47-52.
[14] 张建润.南极磷虾油纳米乳的制备及其氧化稳定性研究[D].大连:大连工业大学,2018.
[15] TADROS T, IZQUIERDO P, ESQUENA J, et al. Formation and stability of nano-emulsions[J].Advances in Colloid and Interface Science,2004,108:303-318.
[16] BOUCHEMAL K, BRIANCON S, PERRIER E, et al. Nano-emulsion formulation using spontaneous emulsification: solvent, oil and surfactant optimisation[J].International Journal of Pharmaceutics,2004,280(1-2):241-251.
[17] 吴婉仪,李璐,解新安,等.基于响应面法构建虾青素纳米乳液[J].食品工业科技,2018,39(10):204-210.
[18] 李杨,胡淼,谢凤英,等.超高压均质对紫苏油纳米乳液稳定性的影响[J].农业机械学报,2018,49(8):381-387.
[19] 杨贵妃,杨柳,钟金锋,等.超声均质法制备以乳清蛋白-OSA变性淀粉为乳化剂的纳米乳液[J].食品与发酵工业,2019,45(12):169-175.
[20] 綦玉曼,寻崇荣,车佳玲,等.薄荷油纳米乳液的制备及其性质分析[J].食品科学,2019,40(10):29-35.
[21] SOBISCH T, LERCHE D. Thickener performance traced by multisample analytical centrifugation[J].Colloids and Surfaces A: Physicochemical and Engineering Aspects,2008,331(1-2SI):114-118.
[22] PETZOLD G, GOLTZSCHE C, MENDE M, et al. Monitoring the stability of nanosized silica dispersions in presence of polycations by a novel centrifugal sedimentation method[J].Journal of Applied Polymer Science,2009,114(2):696-704.
[23] VALLAR S, HOUIVET D, EL FALLAH J, et al. Oxide slurries stability and powders dispersion: Optimization with zeta potential and rheological measurements[J].Journal of The European Ceramic Society,1999,19(6-7):1 017-1 021.
![]() E, STABIECKA A, MASZEWSKA M. Effect of oil phase concentration on rheological properties and stability of beverage emulsion[J].Acta Scientiarum Polonorum Technologia Alimentaria,2006,5(2):147-156.
E, STABIECKA A, MASZEWSKA M. Effect of oil phase concentration on rheological properties and stability of beverage emulsion[J].Acta Scientiarum Polonorum Technologia Alimentaria,2006,5(2):147-156.