密蒙花,又名黄饭花、染饭花、米汤花和小锦花等,是马钱科醉鱼草属落叶灌木植物密蒙花树的干燥花絮和花蕾[1]。密蒙花最早出现在《开宝本草》中,作为传统中药至今已有一千多年的使用历史[2]。同时,密蒙花作为药食两用植物,在我国西南少数民族地区常用来染制糯米饭,其黄色素鲜亮、自然,气味清香,备受欢迎[3]。研究表明,密蒙花黄色素是主要由蒙花苷、芹菜素、木犀草素及藏红花素等组成,具有抗炎、护肝、抗氧化、抗抑郁、抗肿瘤、神经保护、改善记忆及治疗糖尿病等多种功能[4-11]。可见,密蒙花黄色素是一种具有保健功效的新型植物源天然色素,作为食品添加剂应用前景广阔。当前,密蒙花黄色素制备工艺还不成熟,提取研究多集中在通过正交或响应面设计等方法进行一般提取工艺的优化[2-3,12-15],试验结果不能很好反映某一因素变化对其提取效果的影响,而从动力学角度研究其浸提过程,建立提取模型,可以提高提取工艺筛选效率,通过不断矫正和优化进而达到指导工业化生产的目的[15]。为此,本实验以Fick第二定律为基础,建立了密蒙花黄色素提取动力学模型、求解了相关动力学和热力学参数,并优化了其糯米饭的染制工艺,以期为密蒙花黄色素提取工业化放大及其相关民族传统食品产业化提供一定的依据。
1 材料与方法
1.1 实验材料
密蒙花,广西百色市金三角农贸市场,经百色学院苏仕林教授鉴定确认;糯米,广西靖西鸿丰大米加工厂;无水乙醇,天津市富宇精细化工有限公司。
1.2 仪器设备
UV-2700紫外可见分光光度计,日本岛津公司;FD5系列真空冷冻干燥机,金西蒙(北京)仪器有限公司;AL204电子分析天平,德国梅特勒公司;RE-52A旋转蒸发仪和SHZ-Ⅲ循环水真空泵,上海亚荣生化仪器厂;DL-3000循环水冷器,郑州长城科工贸公司;3H20RI智能冷冻高速离心机,湖南赫西仪器装备有限公司。
1.3 实验方法
1.3.1 黄色素制备与光谱扫描
密蒙花50 ℃干燥粉碎后,按料液比1∶20加去离子水室温避光浸提。浸提后,抽滤,加无水乙醇至体积分数80%,醇沉过夜,8 000 r/min、4 ℃离心20 min,弃沉淀,上清液浓缩后转至塑料烧杯内,-80 ℃预冷24 h后,进行低温真空冷冻干燥。干燥所得密蒙花黄色素用去离子水配制一定质量浓度后,进行光谱扫描(400~800 nm),其特征吸收峰在435 nm处(图1-a)。
1.3.2 黄色素标准曲线绘制
先取1.3.1所制备的密蒙花黄色素,配制质量浓度分别为0.05、0.1、0.2、0.3、0.4、0.5和0.6 mg/mL溶液,再在435 nm处测定各自吸光度。以吸光度为纵坐标,以质量浓度为横坐标,绘制标准曲线。由图1-b可知,密蒙花黄色素质量浓度在0.05~0.6 mg/mL时,线性关系良好。
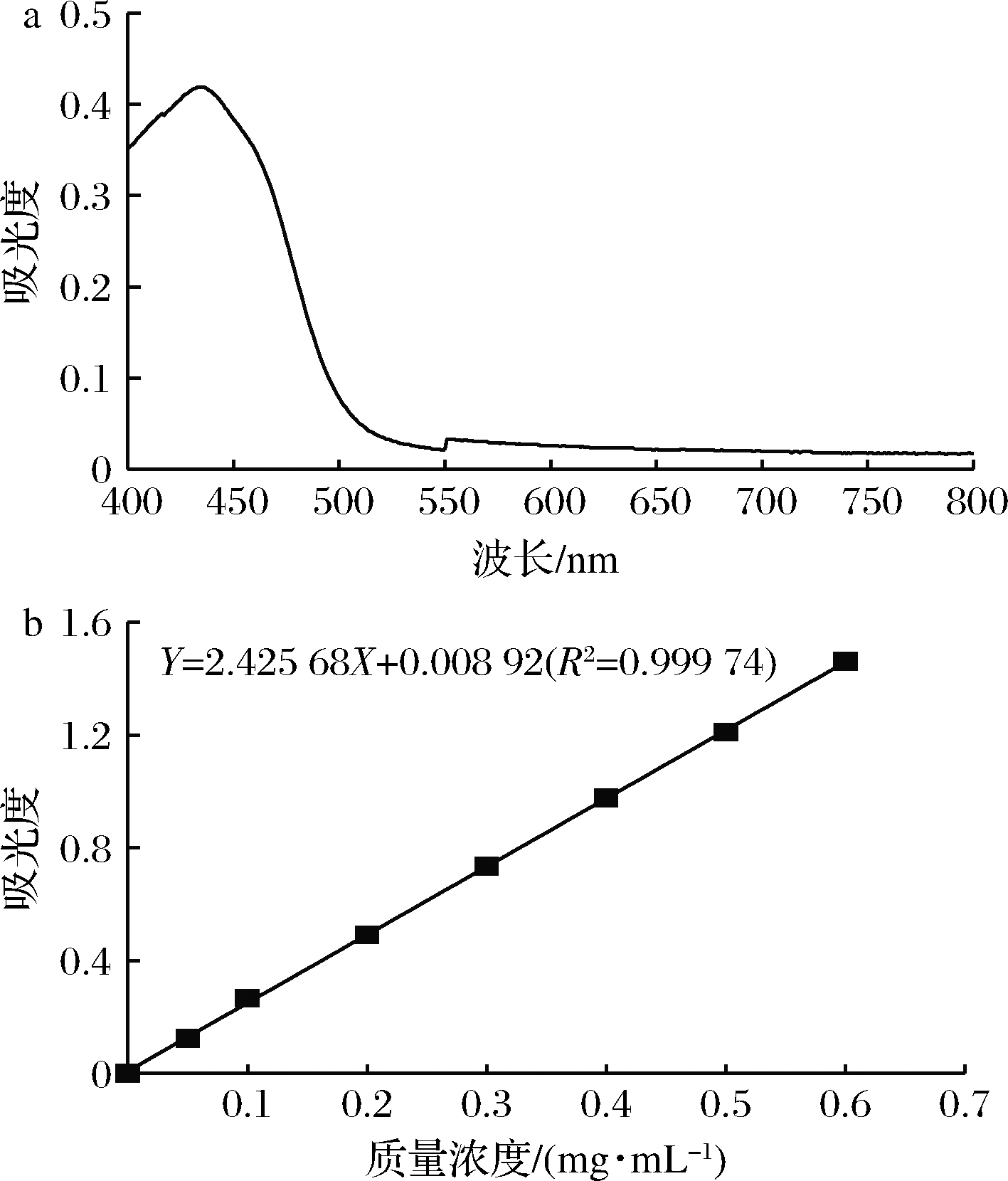
a-可见光光谱;b-标准曲线
图1 密蒙花黄色素可见光光谱图及其标准曲线
Fig.1 Visible spectrogram and standard curve of yellow pigment from Buddleja officinalis flower
1.3.3 黄色素提取与测定
取10 g密蒙花颗粒(半径约为0.125 mm)置于250 mL三口烧瓶中,缓慢加入不同温度(303、313、323和333 K)的去离子水200 mL,搅拌。相应温度下提取密蒙花黄色素,分别在2.5、5、10、15、20、25、30、40、50、60、80和100 min时取样0.1 mL,适当稀释后再在435 nm处直接测定其吸光度,并带入标曲中求得黄色素质量浓度。重复3次,求其平均值。由于提取过程中取样造成了体积的变化,故需按照公式(1)对实测黄色素质量浓度进行校正:
(1)
式中:Cn为第n次取样黄色素质量浓度修正值,mg/mL;Ci为第n次取样黄色素质量浓度实测值,mg/mL;n为取样次数。
1.3.4 黄色素浸提动力学模型
密蒙花黄色素的浸提过程实质是溶质的固液物理传质过程,为不稳定扩散过程。以单粒密蒙花颗粒为计算对象,假设密蒙花颗粒均匀球形、黄色素进行径向扩散、提取过程中球形内部黄色素均匀分布、黄色素质量浓度和扩散系数保持不变、密蒙花颗粒表面传质阻力忽略不计、提取体系温度相同且均匀分布。那么,密蒙花黄色素传质过程的扩散系数可由Fick第二扩散定律计算,如公式(2)所示[16-17]:
(2)
对公式(2)取对数可得:
(3)
式中:C∞为浸提平衡时提取液中黄色素的质量浓度,mg/mL;C0为提取液中黄色素初始质量浓度,mg/mL;Ct为浸提t min时提取液中黄色素的质量浓度,mg/mL;κ为浸提速率常数;Ds为有效扩散系数,mm2/s;R为颗粒半径,mm。
公式(2)和(3)即为根据Fick第二定律建立的黄色素浸提动力学模型。该模型反映了密蒙花颗粒尺寸、提取时间和提取温度与其黄色素质量浓度之间的关系。
1.3.5 黄色糯米饭染制工艺
1.3.5.1 糯米饭染制工艺操作要点
糯米饭染制工艺如下:
1.3.5.2 单因素实验
米饭品质既受大米本身营养成分组成及结构的影响,又和蒸煮条件如加水量、浸泡与否、蒸煮方式等因素有关[18]。结合百色地区壮族五色糯米饭的传统染制工艺,在室温条件下,实验选取料液比(加水量)、染色时间和色素浓度3个关键步骤进行单因素实验。在预实验的基础上,固定色素质量浓度(0.6 mg/mL)和染色时间(8 h),考察料液比(1∶1、1∶2、1∶3、1∶4、1∶5和1∶6)对黄色糯米饭品质的影响;固定料液比(1∶4)和色素质量浓度(0.6 mg/mL),考察染色时间(6、8、10、12、14和16 h)对黄色糯米饭品质的影响;固定染色时间(10 h)和料液比(1∶4),考察黄色素质量浓度(0.2、0.4、0.6、0.8和1.2 mg/mL)对黄色糯米饭品质的影响。
1.3.5.3 正交实验
根据单因素实验结果,选择色素质量浓度(A)、浸泡时间(B)和料液比(C)最佳水平及其上下梯度为考察水平,采用3因素3水平正交实验,对密蒙花黄色素染制糯米饭工艺进行优化(表1)。
表1 正交实验设计表
Table 1 Design of orthogonal experiment
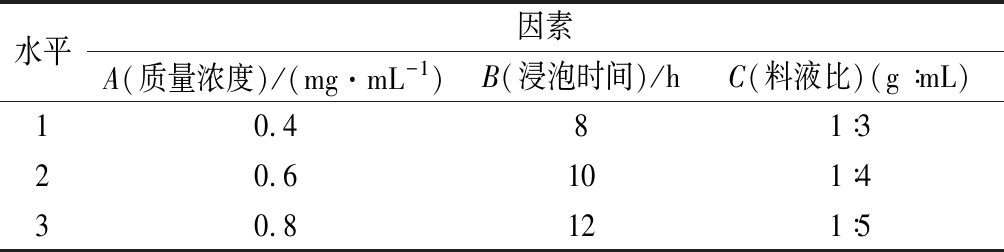
水平因素A(质量浓度)/(mg·mL-1)B(浸泡时间)/hC(料液比)(g∶mL)10.481∶320.6101∶430.8121∶5
1.3.5.4 感官评价方法和标准
黄色糯米饭品质由其感官评价分值表示。糯米染色蒸煮冷却后,选取经食品感官评价技术培训的10人(男女各半)组成评定小组,从气味、外观结构、适口性、滋味及冷饭质地等方面对其进行评价,满分100,最后结果为10人评分的平均值。具体评价标准见表2。
表2 黄色糯米饭感官评价标准
Table 2 Sensory evaluation criteria of yellow glutinous rice

项目评价标准分值/分气味(20分)米饭特有的香气浓郁,带有密蒙花的香味16~20米饭的香气清淡,密蒙花的香味较重15~11米饭的香气不明显,全是密蒙花香味<10外观结构(20分)饭粒完整性好,黄色适当,色泽均匀一致16~20饭粒略有爆花,黄色较淡,色泽较差15~11饭粒大部分爆花,黄色淡,色泽不均匀<10适口性(30分)饭粒有黏性,不粘牙,具有嚼劲,软硬适中16~30有黏性,基本不粘牙,稍有嚼劲,略硬或略软15~11有黏性或黏性,粘牙,米饭疏松,偏软或偏硬<10滋味(20分)咀嚼时,具有密蒙花和糯米的浓郁清香和甜味16~20咀嚼时,有淡淡的密蒙花和糯米清香和甜味15~10咀嚼时,无清香滋味,有异味或无异味<10冷饭质地(10分)松散和黏弹性较好,硬度合适8~10易结团,黏弹性稍差,较硬6~7易板结,黏弹性差,偏硬<5
1.3.6 数据处理
采用Origin 8.0对数据进行分析处理和做图。
2 结果与分析
2.1 密蒙花黄色素提取动力学分析
2.1.1 浸提速率常数求解
不同提取温度和时间下,密蒙花提取液中的黄色素浓度如表3所示。由表3可知,密蒙花黄色素质量浓度达到平衡的时间随着提取温度升高而减少;而在达到质量浓度平衡前,相同提取时间的黄色素质量浓度随提取温度升高而增加。提取温度303 K时,密蒙花黄色素质量浓度在100 min时才趋于平衡,为5.75 mg/mL;而在313、323和333 K时,其平衡时间依次降低到40、30和25 min,但其质量浓度却依次增加到5.84、6.00和7.40 mg/mL。密蒙花黄色素提取过程中,提取温度升高,分子运动速度加快,有利于扩散传质,故黄色素分子与提取溶剂间动态平衡所需时间缩短、平衡前相同提取时间的质量浓度较高。然而,由于密蒙花黄色素的热不稳定性[19],造成在提取温度313、323和333 K时达到质量浓度平衡的后期,其浓度有明显下降。
表3 不同提取温度和时间下提取液中黄色素质量浓度 单位:mg/mL
Table 3 Yellow pigment content of extract at different temperature and time
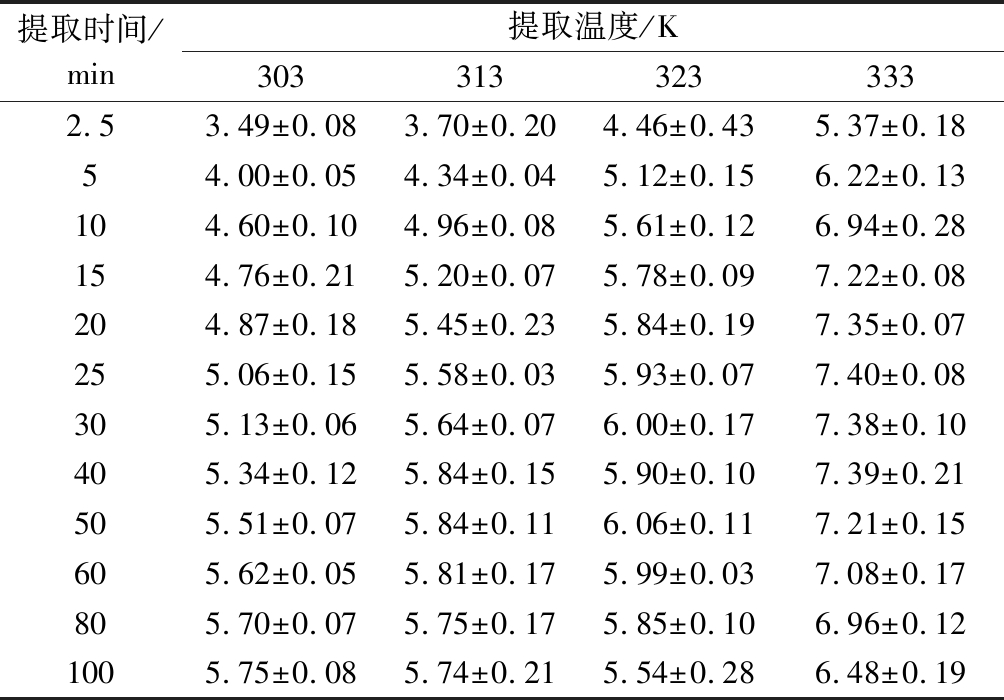
提取时间/min提取温度/K3033133233332.53.49±0.083.70±0.204.46±0.435.37±0.1854.00±0.054.34±0.045.12±0.156.22±0.13104.60±0.104.96±0.085.61±0.126.94±0.28154.76±0.215.20±0.075.78±0.097.22±0.08204.87±0.185.45±0.235.84±0.197.35±0.07255.06±0.155.58±0.035.93±0.077.40±0.08305.13±0.065.64±0.076.00±0.177.38±0.10405.34±0.125.84±0.155.90±0.107.39±0.21505.51±0.075.84±0.116.06±0.117.21±0.15605.62±0.055.81±0.175.99±0.037.08±0.17805.70±0.075.75±0.175.85±0.106.96±0.121005.75±0.085.74±0.215.54±0.286.48±0.19
利用表3实验数据,做ln[C∞/(C∞-Ct)]与时间t的关系函数,得出回归方程和提取速率常数(表4)。
表4 不同温度下ln[C∞/(C∞-Ct)]与t关系
Table 4 Relation of ln[C∞/(C∞-Ct)] and t at different temperature
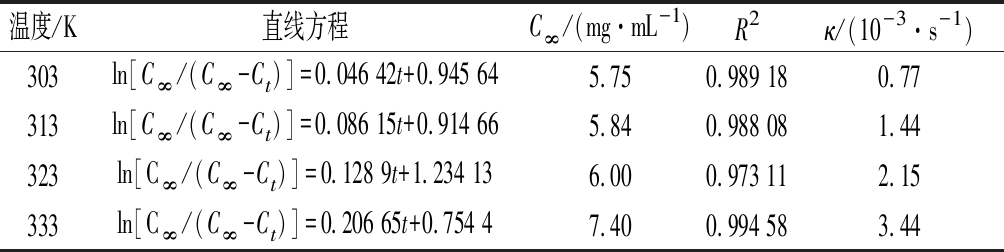
温度/K直线方程C∞/(mg·mL-1)R2κ/(10-3·s-1)303ln[C∞/(C∞-Ct)]=0.046 42t+0.945 645.750.989 180.77313ln[C∞/(C∞-Ct)]=0.086 15t+0.914 665.840.988 081.44323ln[C∞/(C∞-Ct)]=0.128 9t+1.234 136.000.973 112.15333ln[C∞/(C∞-Ct)]=0.206 65t+0.754 47.400.994 583.44
由表4可以看出,提取速率常数κ随温度的升高而增加,在0.77×10-3/s~3.44×10-3/s,说明升温有助于密蒙花黄色素的溶出。此外,其回归方程的拟合系数R2均在0.97以上,说明ln[C∞/(C∞-Ct)]与t之间线性关系良好,密蒙花黄色素的热浸提取行为符合准一级动力学方程。
2.1.2 相对萃余率求解
相对萃余率为(C∞-Ct)/C∞。由于密蒙花黄色素提取之前没有经过浸泡,故其初始提取浓度C0=0,公式(2)可变为(C∞-Ct)/C∞=(6/π2)exp(-κt)。利用表1数据,做(C∞-Ct)/C∞与提取时间t的关系函数,可得不同提取温度下的相对萃余率方程(表5)。
表5 不同温度下相对萃余率与时间的关系
Table 5 Relation of (C∞-Ct)/C∞ and t at different temperature
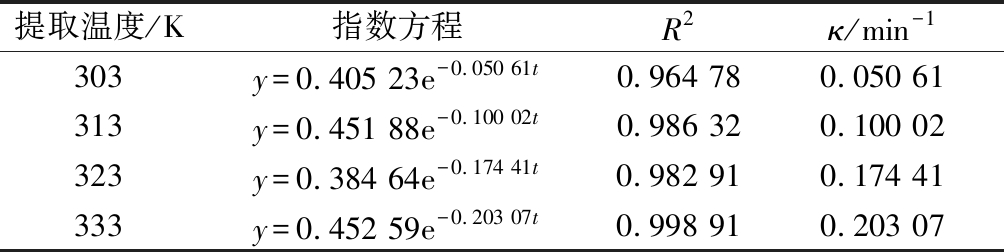
提取温度/K指数方程R2κ/min-1303y=0.405 23e-0.050 61t0.964 780.050 61313y=0.451 88e-0.100 02t0.986 320.100 02323y=0.384 64e-0.174 41t0.982 910.174 41333y=0.452 59e-0.203 07t0.998 910.203 07
由表5可知,拟合方程相关系数均在0.96以上,表明拟合方程精度较高,密蒙花黄色素提取过程可以用指数模型进行解释,但提取温度在303和313 K时利用一级动力学方程进行解释更加合理。此外,由于采用了不同模型对密蒙花黄色素提取过程进行拟合分析,故表4和表5中的提取速率常数κ有一定偏差。
2.1.3 活化能求解
由化学反应动力学可知,低温下的溶质扩散速率常数与温度有关,一般遵循Arrhenius方程。通过对Arrihenius公式两端取对数可得到公式lnκ=lnA-(Ea/RT)。其中κ为黄色素的提取速率常数,s-1;A为前指因子;Ea为表观活化能,J/mol;R为气体常数,8.314 J/mol;T为提取温度,K。
利用表4中κ,对-lnκ与1/T做图(图2),进行回归拟合,其方程为-lnκ=(4 933.26/T)×9.151 49,R2为0.992 8。可求得活化能为Ea=41.02 kJ/mol。
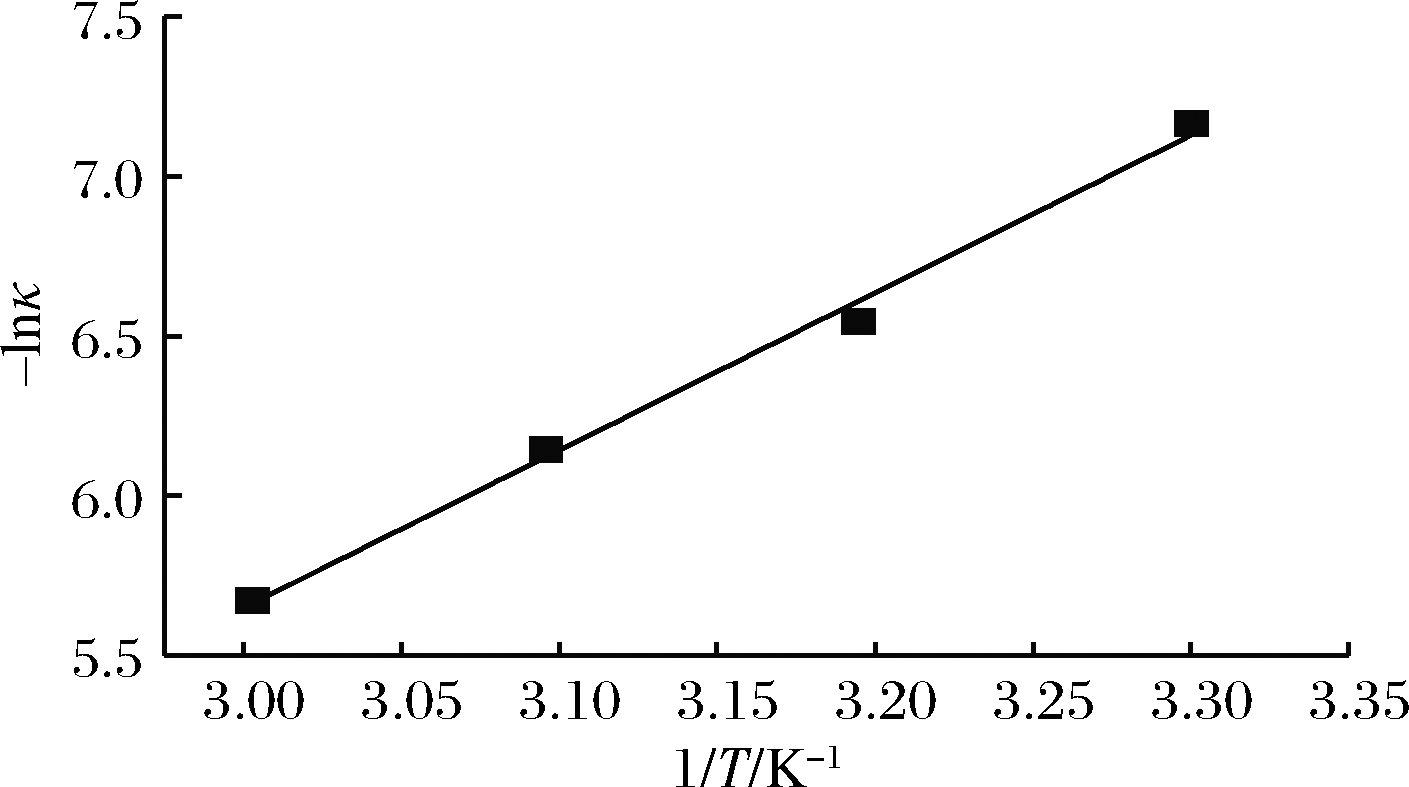
图2 -lnκ与1/T的关系
Fig.2 Relation of -lnκ and 1/T
2.1.4 半衰期求解
当密蒙花提取液中黄色素质量浓度达到平衡浓度一半所需要的时间为其半衰期,可以通过对t1/2=ln2/κ和温度T做图求得(图3)。通过指数拟合可得其方程为t1/2=1.266 9×108exp(-0.052 7T),R2=0.987 71。由该方程可知,随着温度增加,密蒙花黄色素提取半衰期逐渐减小,提取效率逐渐增加,提取过程逐渐加快。
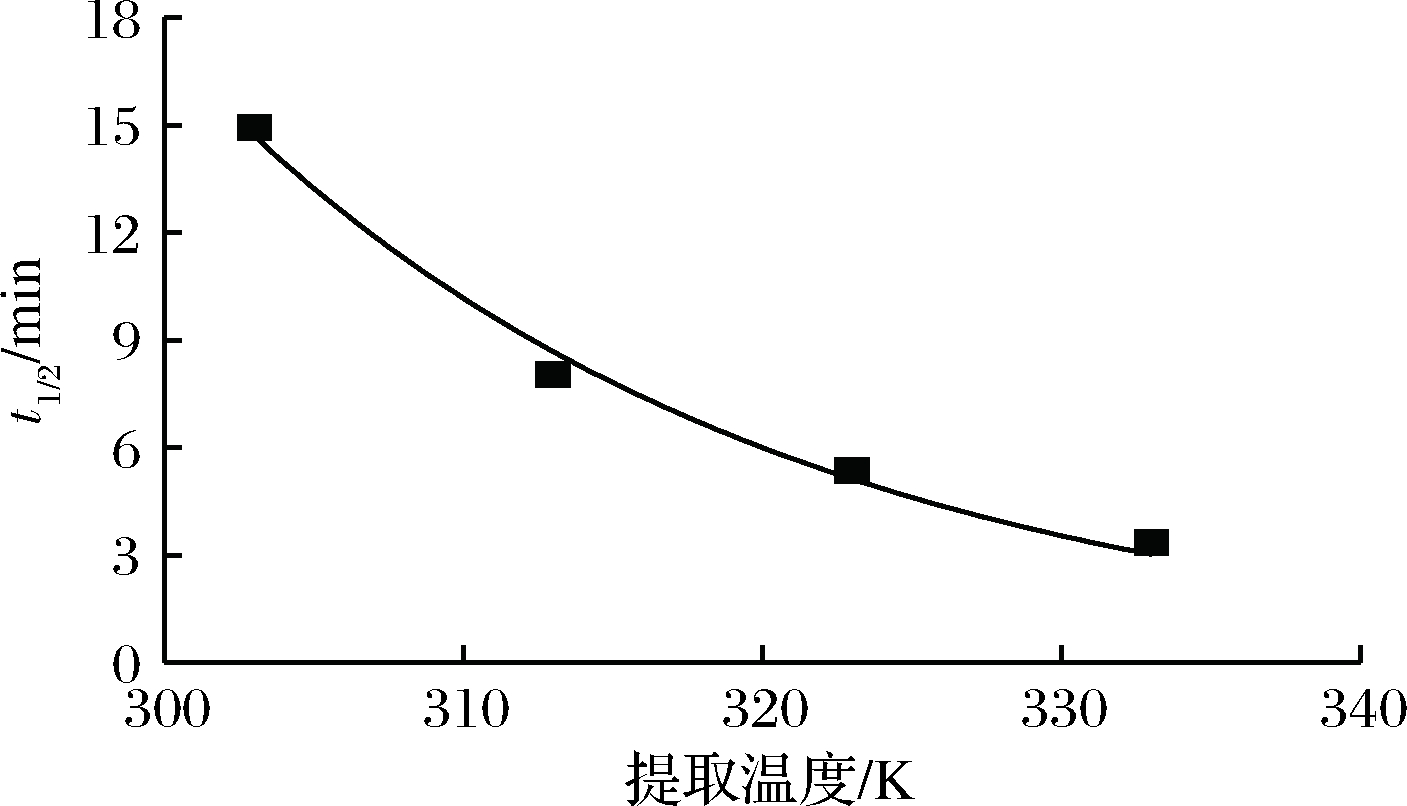
图3 半衰期t1/2与提取温度κ的关系
Fig.3 Relation of half-life and extract temperature
2.1.5 有效扩散系数Ds求解
有效扩散系数Ds可由公式(3)κ=π2Ds/R2推导出Ds=κR2/π2。通过对Ds和提取温度T做图(图4),并进行指数方程拟合可得:108Ds=0.005 71exp(0.046 73T),R2=0.995 23。由此方程可计算不同提取温度下密蒙花黄色素的有效扩散系数。
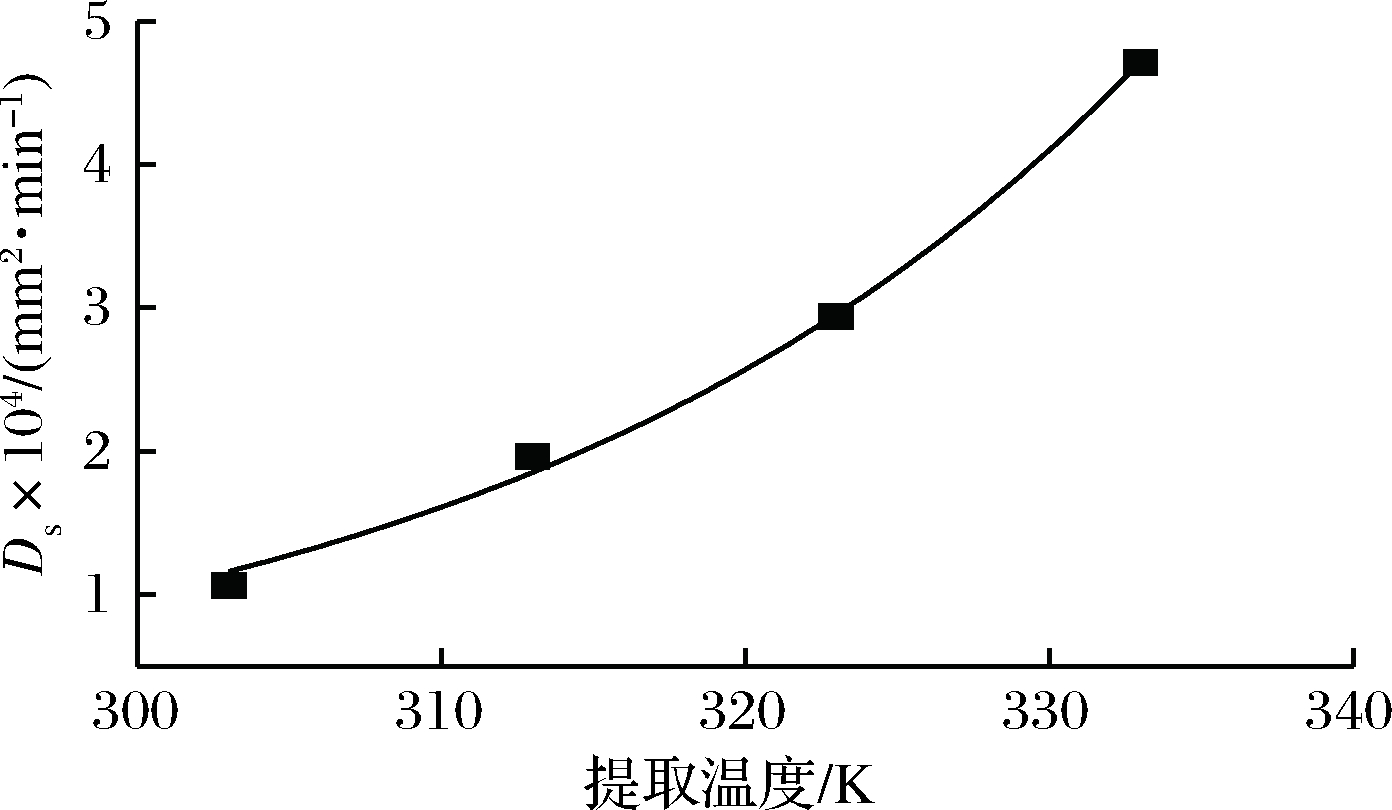
图4 有效扩散系数Ds与提取温度的关系
Fig.4 Relation of Ds and extract temperature
2.2 密蒙花黄色糯米饭染制工艺
2.2.1 料液比(加水量)对糯米饭品质的影响
加水量是影响糯米饭品质的重要因素。糯米中水分的含量、分布及存在状态会使米饭呈现不同的物性,故可以通过控制水量来提高米饭的食味品质[20]。由图5可知,随料液比增大,黄色糯米饭品质感官得分先上升后下降。在料液比1∶4时,感官分值最高,为82.21。这是因为料液比较低时,水量不足,糯米内外层淀粉糊化不均匀,糯米饭硬度大,饭粒松散,适口性差;饭粒黄色较淡,偶见着色不均;料液比过大时,糯米龟裂,蒸煮后饭粒弹性差,较软、偶见粘牙;同时,从糯米粒龟裂处渗入黄色素的量增加,密蒙花香味较重。故选择糯米浸泡料液比为1∶4。
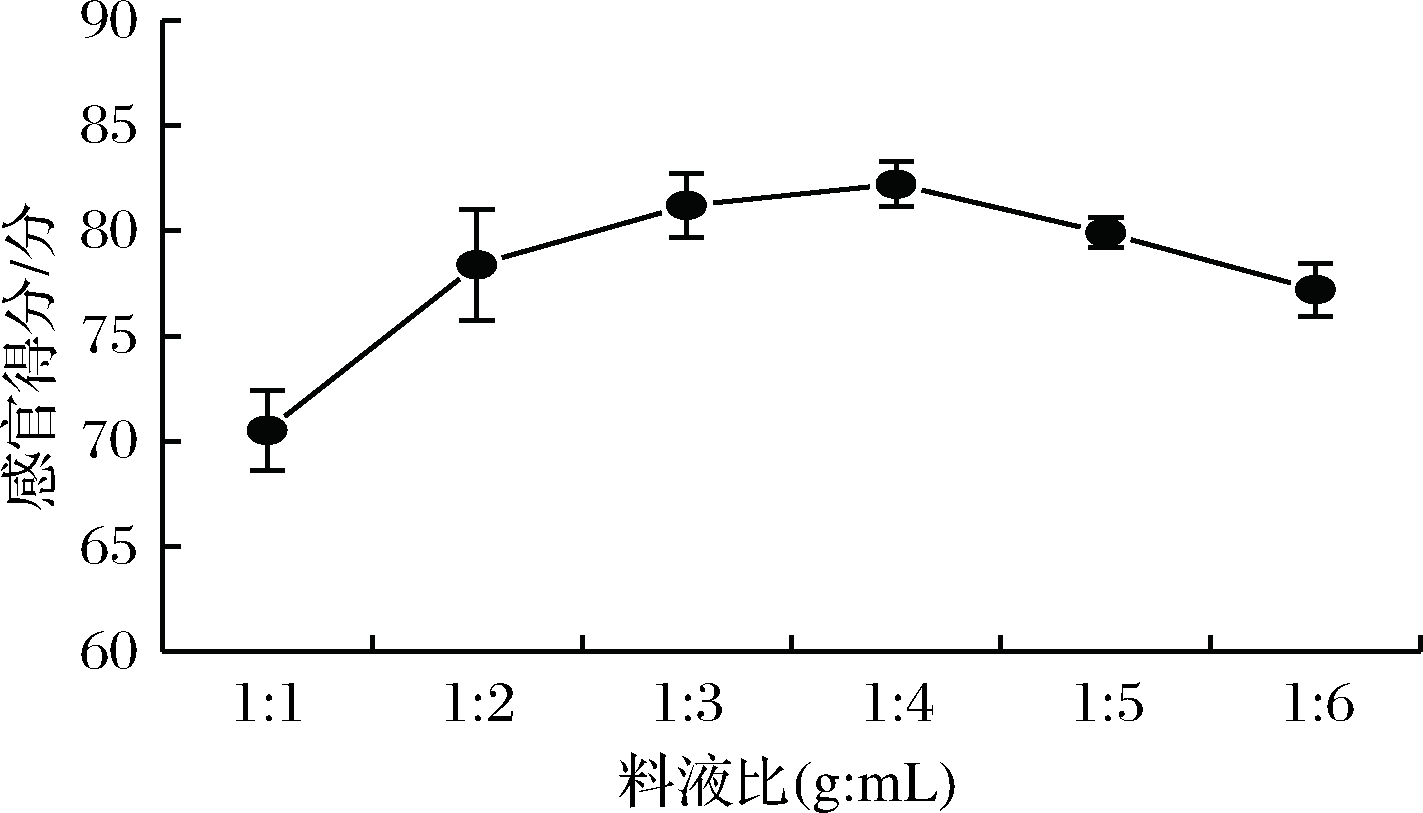
图5 料液比对对黄色糯米饭品质的影响
Fig.5 Effect of solid-liquid ratio on the quality of yellow milled glutinous rice
2.2.2 染色时间对糯米饭品质的影响
浸泡染色是五色糯米饭制作的必需环节,其目的是使糯米粒充分吸水膨胀,促进加热过程热量在组分间传递,糊化均一,米粒松软。研究表明,大米中水分迁移由外至内、沿着淀粉细胞间隙进行的,而米粒腹部细胞间隙较大,是其渗透的主要路线[21-22]。此外,浸泡也能够促进密蒙花水溶性黄色素随着水分的迁移而更好地与米粒中的蛋白、淀粉等成分结合着色。染色时间对黄色糯米饭品质影响如图6所示。
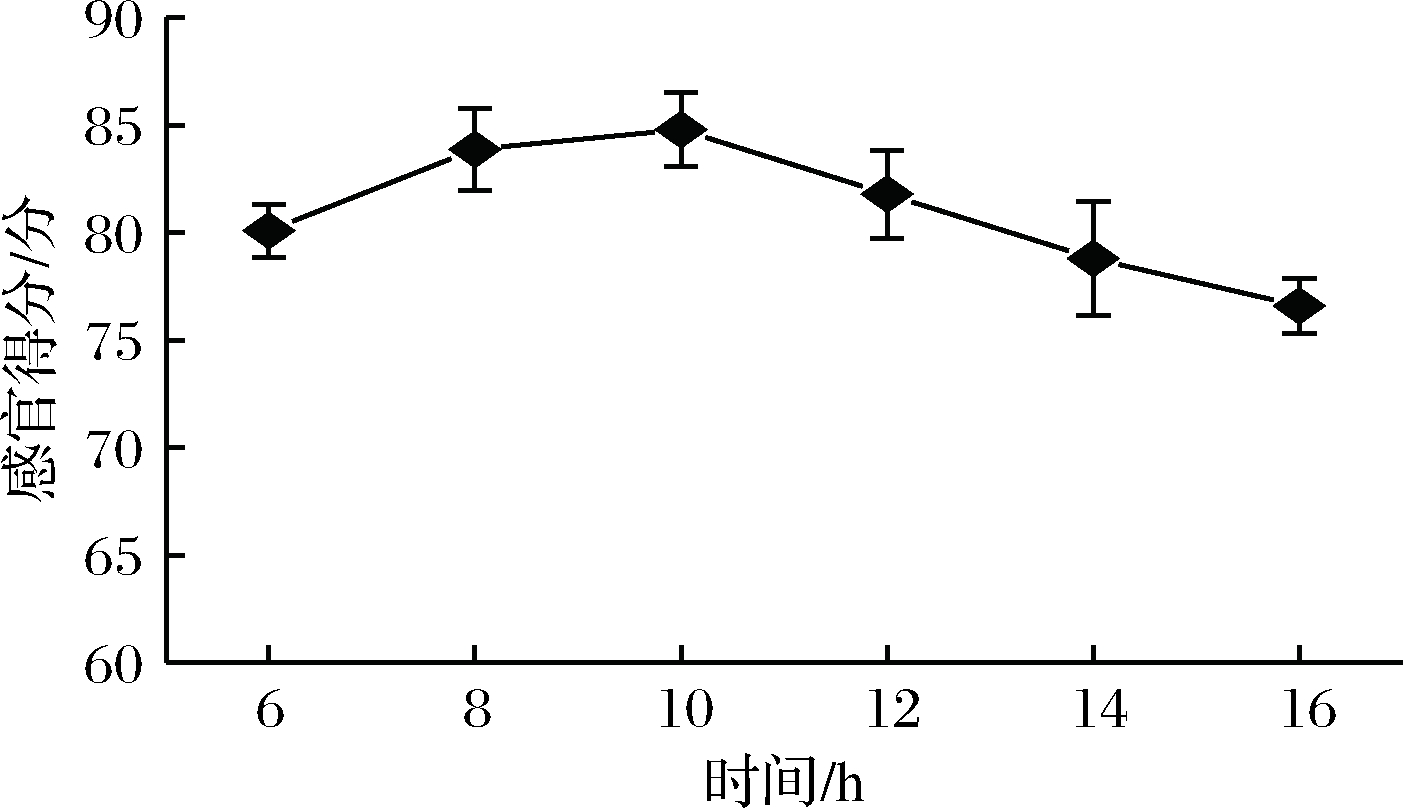
图6 染色时间对对黄色糯米饭品质的影响
Fig.6 Effect of dyeing time on the quality of yellow milled glutinous rice
由图6可知,染色时间在10 h时,黄色糯米饭品质最好,感官分值最高,为84.85。当染色6 h时,糯米饭呈淡黄色,且密蒙花花香不明显。这是由于糯米着色滞后于水分渗透,染色时间较短,色素吸附量不够。当染色12 h时,糯米饭呈暗黄色,且密蒙花花香较重;当染色14 h和16 h时,由于糯米在色素溶液中浸泡过久,米粒偶见开裂、不完整、淀粉脱落,糯米饭口感较软、易结团、粘牙。故选择染色时间为10 h。
2.2.3 色素质量浓度对糯米饭品质的影响
色素溶液质量浓度影响糯米着色效率。由图7可知,密蒙花黄色素质量浓度在0.2~0.6 mg/mL时,黄色糯米饭品质随色素质量浓度增加而提升,感官分值逐渐升高;质量浓度超过0.6 mg/mL时,其感官分值逐渐下降,食味品质变差。主要是因为高浓度色素溶液中糯米吸附色素量增加,糯米饭呈暗黄色,且密蒙花花香掩盖了糯米本有的清香。这与曹昌伟等人的报道一致[23],故选择密蒙花黄色素质量浓度为0.6 mg/mL。
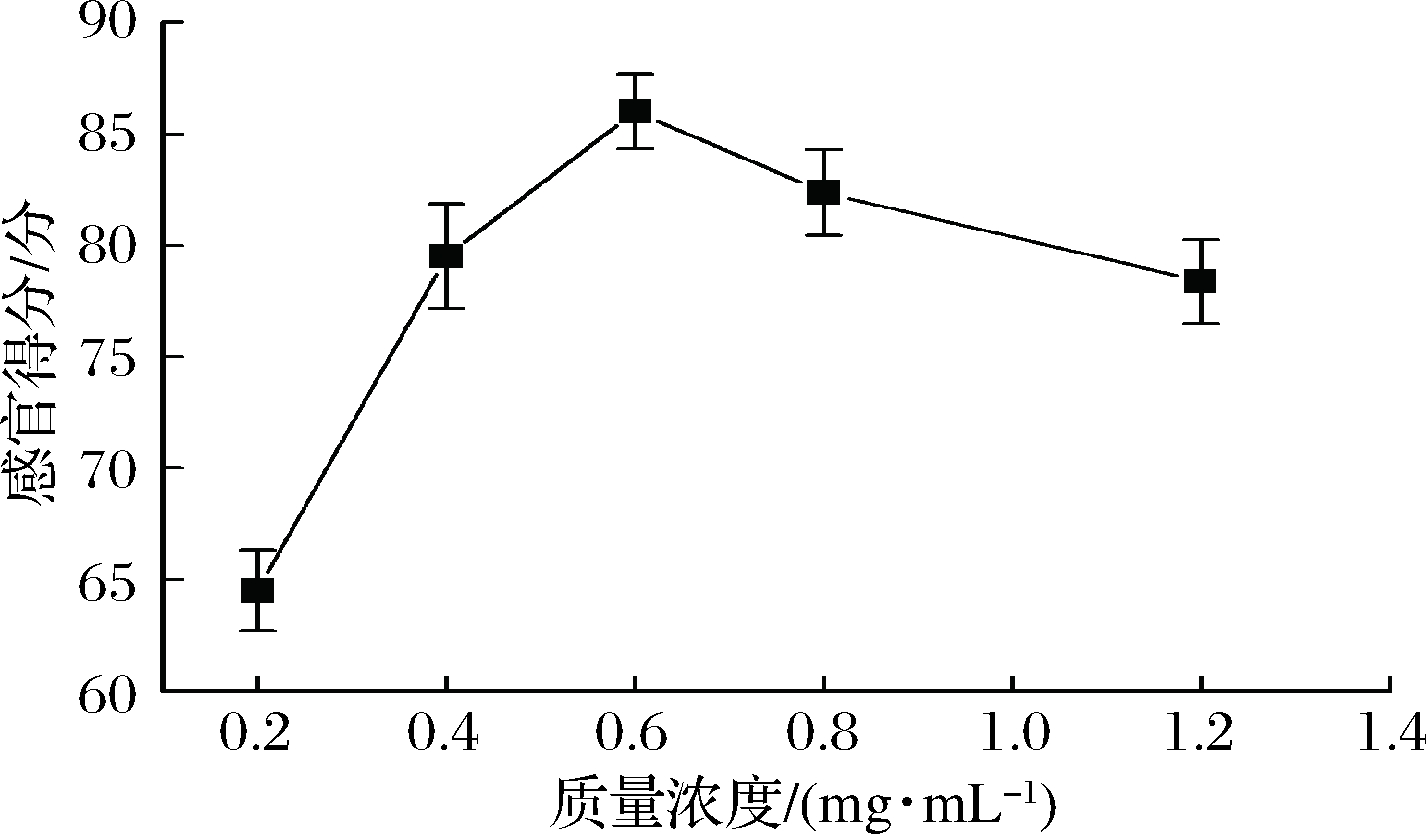
图7 色素质量浓度对黄色糯米饭品质的影响
Fig.7 Effect of pigment content on the quality of yellow milled glutinous rice
2.2.4 正交实验结果分析及验证
由表7的极差可知,对黄色糯米饭品质贡献大小的各因素依次为A、B和C,即色素质量浓度、料液比和浸泡时间,最佳染制工艺条件为A2B3C2,即色素质量浓度0.6 mg/mL、料液比1∶4(g∶mL)和浸泡12 h。由于最佳工艺组合不在正交实验表中,故需对最佳工艺进行验证试验。验证结果表明,3次验证实验的感官平均得分为85.02,高于正交实验表中的组合最高感官得分,可见正交实验达到了优化目的。因此,密蒙花黄色素染制糯米饭的最佳工艺为黄色素质量浓度0.6 mg/mL、料液比1∶4(g∶mL)浸泡12 h后,蒸煮20 min。
表7 正交实验结果
Table 7 Result of f orthogonal experiment
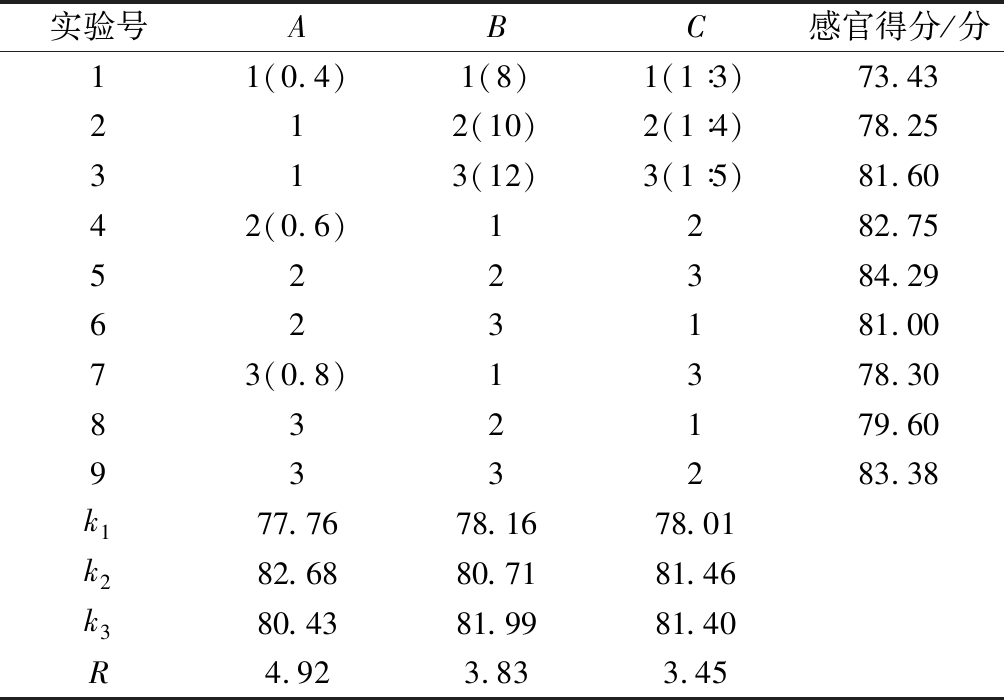
实验号ABC感官得分/分11(0.4)1(8)1(1∶3)73.43212(10)2(1∶4)78.25313(12)3(1∶5)81.6042(0.6)1282.75522384.29623181.0073(0.8)1378.30832179.60933283.38k177.7678.1678.01k282.6880.7181.46k380.4381.9981.40R4.923.833.45
3 结论
密蒙花黄色素的提取过程是一个复杂的物理溶解过程,与提取条件和自身性质有关。实验以Fick第二定律为基础,采用球形模型,建立了密蒙花黄色素的浸提动力学方程,求解了相关动力学参数。其中,浸提速率随温度上升而增加,而半衰期随温度上升而减小;活化能为41.02 kJ/mol。此外,根据壮族传统五色糯米饭染制工艺,选取色素浓度、浸泡时间和料液比等3个因素进行单因素试验,进而采用3因素3水平的正交试验。结果显示,对密蒙花黄色素糯米饭品质影响大小的各因素依次为色素质量浓度、浸泡时间和料液比;其最佳染制工艺为用0.6 mg/mL的黄色素溶液,按照料液比1∶4(g∶mL)染色12 h。本实验可以为密蒙花黄色素的生产工艺设计与操作条件选择和优化提供理论依据,也可以为民族传统食品产业化提供数据支撑。
[1] 国家药典委员会. 中华人民共和国药典[M]. 一部. 北京: 北京医药科技出版社, 2015.
[2] XIE GY, LI R, HAN Y, et al. Optimization of the extraction conditions for Buddleja officinalis maxim. Using response surface methodology and exploration of the optimum harvest time[J]. Molecules, 2017, 22(11): 1877.
[3] 许海棠,廖艳娟, 欧小辉, 等. 密蒙花黄色素的提取及其稳定性研究[J]. 食品与发酵工业, 2015, 41(6): 218-222.
[4] XIE G Y, XU Q H, LI R, et al. Chemical profiles and quality evaluation of Buddleja officinalis flowers by HPLC-DAD and HPLC-Q-TOF-MS/MS[J]. Journal of Pharmaceutical and Biomedical Analysis, 2019, 164: 283-295.
[5] ROH C, PARK M-K., SHIN H-J, et al. Buddleja officinalis Maximowicz extract inhibits lipid accumulation on adipocyte differentiation in 3T3-L1 cells and high-fat mice[J]. Molecules, 2012, 17: 8 687-8 695.
[6] SUN M H, LUO Z Q, LIU Y, et al. Identification of the major components of Buddleja officinalis extract and their metabolites in rat urine by UHPLC-LTQ-orbitrap[J]. Journal of Food Science, 2016, 81: H2 587-H2 596.
[7] YAO X L, PENG Q H, PENG J, et al. Effects of extract of Buddleja officinalis on partial inflammation of lacrimal gland in castrated rabbits with dry eye[J]. International Journal of Ophthalmol. 2010, 3(2):114-119.
[8] SALAMA R M, ABDEL-LATIF G A, ABBAS S S, et al. Neuroprotective effect of crocin against rotenone-induced Parkinson's disease in rats: Interplay between PI3K/Akt/mTOR signaling pathway and enhanced expression of miRNA-7 and miRNA-221[J]. Neuropharmacology, 2020, 164: 107 900.
[9] DUAN Z, LI H, QI X, et al. Crocin attenuation of neurological deficits in a mouse model of intracerebral hemorrhage[J]. Brain Research Bulletin, 2019, 150: 186-195.
[10] AHMADI M, RAJAEI Z, HADJZADEH M A, et al. Crocin improves spatial learning and memory deficits in the Morris water maze via attenuating cortical oxidative damage in diabetic rats[J]. Neuroscience Letters, 2017, 642: 1-6.
[11] RAHAIEE S, HASHEMI M, SHOJAOSADATI S A, et al. Nanoparticles based on crocin loaded chitosan-alginate biopolymers: Antioxidant activities, bioavailability and anticancer properties[J]. International Journal of Biological Macromolecules, 2017, 99: 401-408.
[12] 罗堾子, 孔永强, 张弘, 等. 响应面分析法优化超声波提取密蒙花黄色素工艺[J]. 食品科学, 2010, 31(22): 352-356.
[13] 杨胜远,李卓文, 方晓旋, 等. 密蒙花黄色素的提取及其紫外可见光谱指纹图谱研究[J]. 食品科技, 2013, 38(6): 281-285.
[14] 张姣姣,杜超, 杨维弘, 等. 微波辅助提取密蒙花黄色素及稳定性分析[J]. 中国食品添加剂, 2018, 1: 67-71.
[15] 张晋,李存新, 葛亮, 等. 水煎煮法提取骨碎补总黄酮的动力学模型适应性研究[J]. 北京中医药大学学报, 2014, 37(2): 121-125.
[16] 刘存菊, 赵立党, 李稳宏, 等.飞天蜈蚣七中黄酮提取的动力学[J]. 化工进展, 2012, 31(6): 1 302-1 305;1 313.
[17] WANG YG, ZHANG X, MA XQ, et al. Study on the kinetic model, thermodynamic and physicochemical properties of Glycyrrhiza polysaccharide by ultrasonic assisted extraction [J]. Ultrasonics Sonochemistry,2019, 51: 249-257.
[18] 周显青, 邓灵珠, 张玉荣. 米饭物性与食味形成机理研究进展[J]. 粮油食品科技, 2012, 20(4): 1-6.
[19] RAHAIEE S, SHOJAOSADATI S A, HASHEMI M, et al. Improvement of crocin stability by biodegradeble nanoparticles of chitosan-alginate[J]. International Journal of Biological Macromolecules, 2015, 79: 423-432.
[20] ZHU L, CHENG L L, ZHANG H, et al. Research on migration path and structuring role of water in rice grain during soaking[J].Food Hydrocolloids, 2019, 92: 41-50.
[21] AKEMI K H, HITOSHI T, SACHIO M, et al. Water penetration into rice grains during soaking observed by gradient echo magnetic resonance imaging[J]. Journal of Cereal Science, 2006, 44(3): 307-316.
[22] CHEN X, ZHANG X X, WANG B Y, et al. Investigation of water migration and its impacts on eating qualities of black rice during cooking process[J]. Journal of Cereal Science, 2019, 89: 102 810.
[23] 曹昌伟, 杨越超, 张建跃, 等. 响应面法优化密蒙花黄色素染制黄米饭工艺研究[J]. 食品研究与开发, 2017, 10(20): 75-79.