藻类食品富含人体必需的氨基酸、蛋白质、微量元素、小分子多糖等生物活性物质,具有重要的营养、保健和医疗价值[1]。如被日本誉为“长寿菜”的羊栖菜以及“人类最理想的蛋白源”的螺旋藻就具有抗氧化、抗肿瘤、免疫调节等功效[2]。但由于受水源、农药等影响,易被重金属污染,所以测定藻类食品中金属元素含量具有重要意义[3]。周小瑞等[4]用微波消解-原子吸收法测定铜藻中多种微量元素。胡越等[5]用微波消解-电感耦合等离子体质谱法测定螺旋藻中16种矿物元素含量。电感耦合等离子质谱法(inductively coupled plasma mass spectrometry,ICP-MS)因其灵敏度高、检出限低、抗干扰性强、可同时测定多元素,而被广泛应用[6]。
目前,常用的藻类样品中矿物元素分析的前处理方法主要有干法灰化、湿法消解、微波消解等。干法灰化和湿法消解操作繁琐,待测组分易被损失和污染;微波消解法用酸量大,反应剧烈,污染环境,不利于实验人员的健康[7]。近年来高效、环保的超声酶解法陆续被报道[8-10]。超声酶解技术将超声波萃取技术与酶萃取技术相结合,酶的生化作用可将蛋白质断裂为氨基酸从而释放出其中的金属元素,超声波的空化效应、机械效应以及热效应能够促进酶解反应[11-12]。超声酶解法具有提取率高、待测物不易挥发损失、反应过程温和、提取条件绿色环保等优点,在食品检测、土壤分析等方面有较多应用[13-14]。YILMAZ等[15]用超声胃蛋白酶解-原子吸收法测定青葱中的锰,试验通过比较胃蛋白酶、淀粉酶和胰蛋白酶的提取效果,确定胃蛋白酶为最佳提取剂,之后对pH值、酶的用量、超声温度等提取条件进行优化,从而得到青葱中锰的最佳提取方案。
本工作通过螺旋藻超声酶解条件的优化,建立一种超声酶提取-ICP-MS分析螺旋藻样品中锰(Mn)、锌(Zn)、锶(Sr)、镉(Cd)的方法,以期为藻类样品中矿物元素的分析提供一种温和、绿色、快速且准确的测定方法。
1 材料与方法
1.1 材料与试剂
多元素标准溶液:质量浓度为10 μg/mL;调谐溶液:Ce、Co、Li、Mg、Tl、Y,质量浓度为1 μg/L;内标溶液:Sc、Ge、Rh、In,质量浓度为100 μg/mL,均购于美国Agilent公司;胃蛋白酶、纤维素酶,上海源叶生物科技有限公司;螺旋藻标准物质(GBW10025),地球物理地球化学勘查研究所;HNO3(AR),德国Merck;盐酸(GR),国药试剂;螺旋藻片、羊栖菜、海发菜、冰藻,市售。
1.2 仪器与设备
7900型电感耦合等离子体质谱仪,美国Agilent公司;微波消解仪,意大利Milestone公司;VB24 up赶酸仪,北京莱伯泰科公司;涡旋振荡器,德国IKA公司;KQ-700DE型数控超声波清洗机,昆山市超声仪器有限公司;雷磁pHS-3C型PH计,上海精密科学仪器有限公司;TDL-40B高速台式离心机,上海安亭科学仪器厂;FW-100高速万能粉碎机,北京市永光明医疗仪器有限公司;电子分析天平,METLER TOLEDO。优化后的ICP-MS工作条件如表1所示。
表1 ICP-MS工作条件
Table 1 ICP-MS operating parameters

工作条件设定值射频功率/W1 550等离子气体流量/(L·min-1)15雾化室温度/ ℃2雾化气体流量/(L·min-1)0.99氦气流量/(mL·min-1)4.8
1.3 实验方法
1.3.1 样品前处理
样品经高速粉碎机粉碎后过80目筛,置于干燥器中备用。
1.3.1.1 超声胃蛋白酶提取法
称取0.2 g(精确到0.001 g)螺旋藻样品于15 mL离心管中,加入20 mg胃蛋白酶,再加入7.0 mL超纯水,用0.1 mol/L HCl调节pH至1.0,涡旋混匀1 min,然后于45 ℃的超声仪中水浴超声20 min,在4 000 r/min的条件下离心10 min,取其上清液,用超纯水定容至10 mL备用。测定前经0.45 μm的水系滤膜过滤。同时做试剂空白试验。
1.3.1.2 超声纤维素酶提取法
称取0.2 g(精确到0.001 g)螺旋藻样品于15 mL离心管中,加入20 mg纤维素酶,再加入7.0 mL超纯水,用0.1 mmol/L HCl调节pH至4.0,涡旋混匀1 min,然后于55 ℃的超声仪中水浴超声20 min,在4 000 r/min的条件下离心10 min,取其上清液,用超纯水定容至10 mL备用。测定前经0.45 μm的水系滤膜过滤。同时做试剂空白试验。
1.3.1.3 超声稀HCl(pH=1.0)提取法
与1.3.1.1相同的试验条件下,不加入胃蛋白酶进行试验。同时做试剂空白试验。
1.3.1.4 微波消解法
称取0.2 g(精确到0.001 g)螺旋藻样品于消解管中,参考GB 5009.268—2016[16]中第一法(ICP-MS法)的微波消解法进行消解。同时做试剂空白试验。
2 结果与分析
2.1 前处理条件的优化
本研究采用超声酶解法提取藻类中的Mn、Zn、Sr和Cd。由于不同的提取剂、pH值、超声温度、酶的质量、超声时间和液料比对提取Mn、Zn、Sr、Cd会产生不同的影响,所以实验比较了螺旋藻样品在不同提取条件时的提取效率。以传统的微波消解法为对照,提取效率为不同提取条件下测定的样品含量值与微波消解法测定的样品含量值的比率,从而选择出最佳配比组合。
2.1.1 提取剂的选择
根据螺旋藻蛋白质含量高且具有细胞壁的特性,分别选择胃蛋白酶、纤维素酶和稀HCl(pH=1.0)作为提取剂,考察不同的提取剂对螺旋藻中Mn、Zn、Sr、Cd提取效果的影响。结果如图1所示,结果表明,采用胃蛋白酶的提取效果最佳,提取效率为93%~100%;稀HCl(pH=1.0)的提取效率为83%~91%;纤维素酶的提取效率均低于60%。选择胃蛋白酶为提取剂作进一步的实验优化。
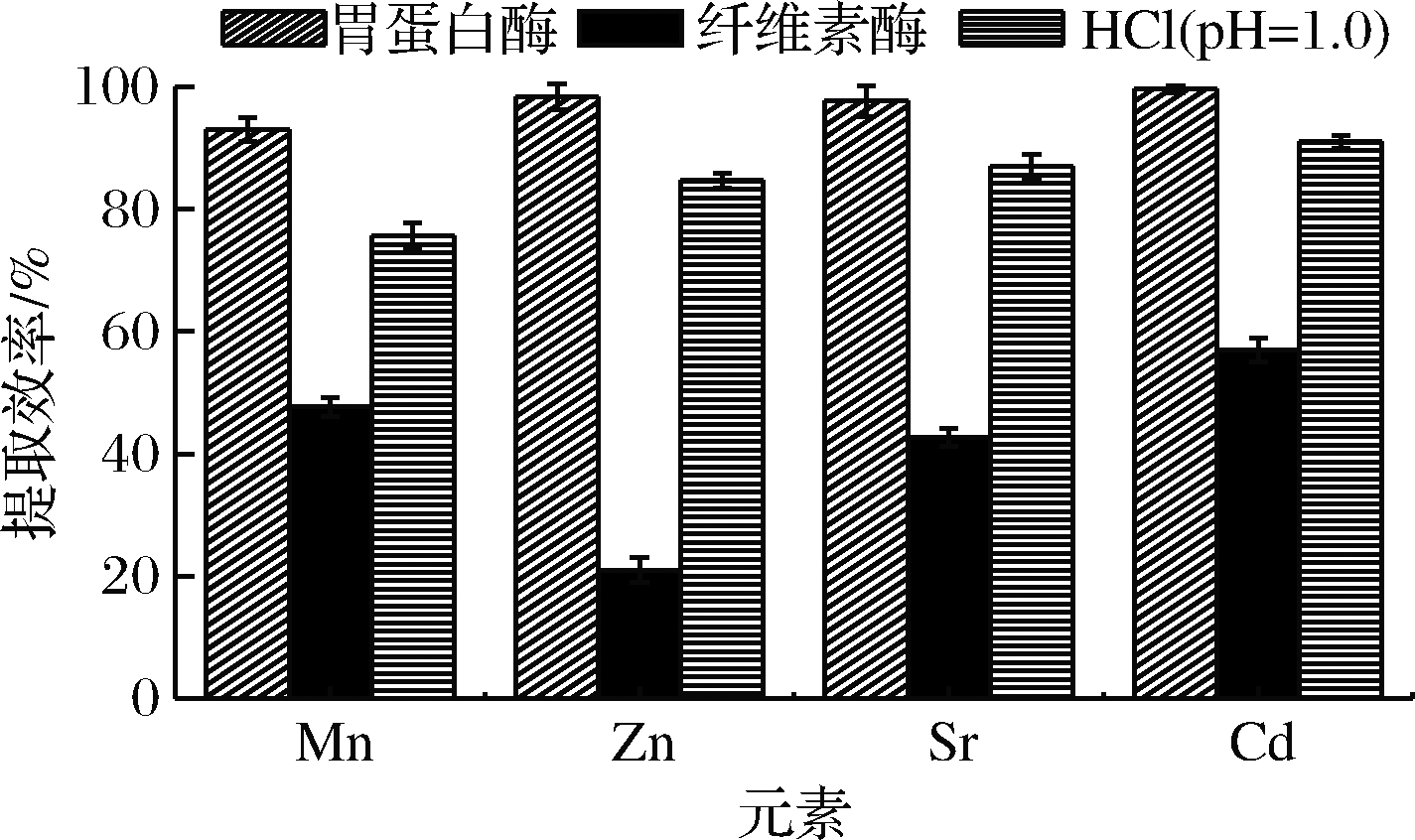
图1 提取剂对Mn、Zn、Sr、Cd提取效率的影响
Fig.1 Influence of extracting agent on extraction efficiency of Mn, Zn, Sr and Cd
2.1.2 pH值的优化
按照1.3.1.1试验方法,在其他条件不变的情况下,考察pH为1.0、1.5、2.0、2.5、3.0、4.0时,螺旋藻中Mn、Zn、Sr、Cd的提取效率。结果如图2所示,结果表明,提取效率随pH值的增加而降低后趋于平稳。pH值对酶反应速率的影响较大,胃蛋白酶的最适pH为1~2[17],过高的pH值环境会导致酶蛋白的变性。选择pH值为1.0最优。

图2 pH值对Mn、Zn、Sr、Cd提取效率的影响
Fig.2 Influence of pH on extraction efficiency of Mn, Zn, Sr and Cd
2.1.3 超声水解温度的优化
相同的试验条件下,考察超声水解温度为25、35、40、45、50和60 ℃时对Mn、Zn、Sr、Cd提取效果的影响。结果如图3所示,结果表明,当温度为45或50 ℃时,Mn、Zn、Sr、Cd提取率均在95%以上,但温度过低或过高时提取率均呈下降趋势。温度过低会使胃蛋白酶的活性受到抑制,过高会破坏胃蛋白酶分子中多肽链的链接。选择最佳超声水解温度为45 ℃。

图3 超声温度对Mn、Zn、Sr、Cd提取效率的影响
Fig.3 Influence of extraction temperature on extraction efficiency of Mn, Zn, Sr and Cd
2.1.4 酶添加量的优化
分别在样品中加入5、10、20、30、40、50 mg的胃蛋白酶。结果如图4所示,酶用量为20 mg时各元素提取效率均能在96%以上;酶添加量为5 mg时,提取效率低于86%,酶量过低不利于酶与底物的充分反应;酶量增加提取速率也不再提高,过量的酶会包裹原料颗粒,不利于产物的溶出。结合经济性最终选择酶添加量为20 mg。
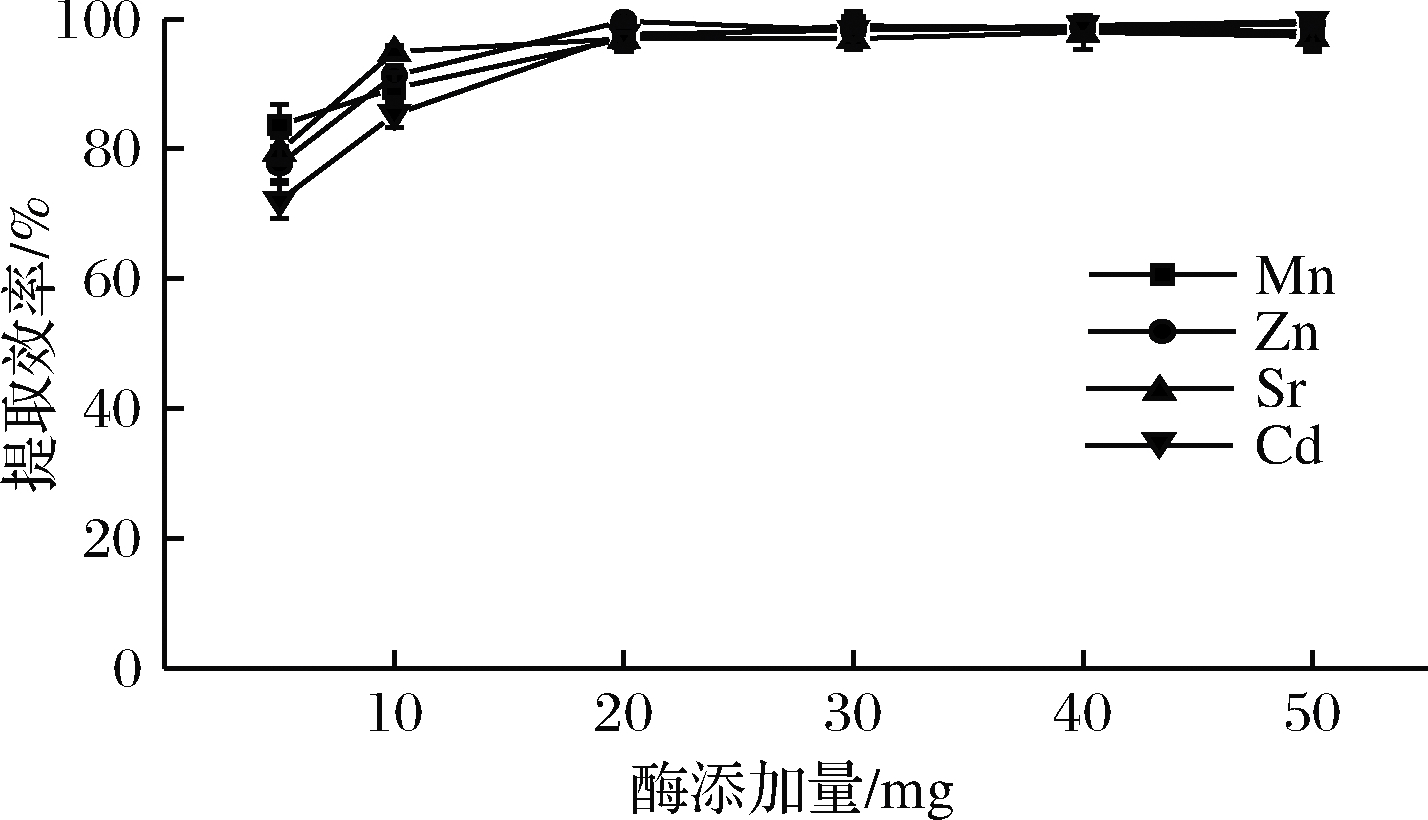
图4 酶添加量对Mn、Zn、Sr、Cd提取效率的影响
Fig.4 Influence of amount of enzyme on extraction efficiency of Mn, Zn, Sr and Cd
2.1.5 超声时间的优化
分别超声酶解样品5、10、20、30、40、50 min。结果如图5所示,结果表明,随着超声时间的增加Mn、Zn提取效率也提高,并在20 min后趋于平稳,超声时间延长可增加原料与提取液的接触时间。Sr、Cd随超声时间的变化无明显差异。选择最优超声时间为20 min。
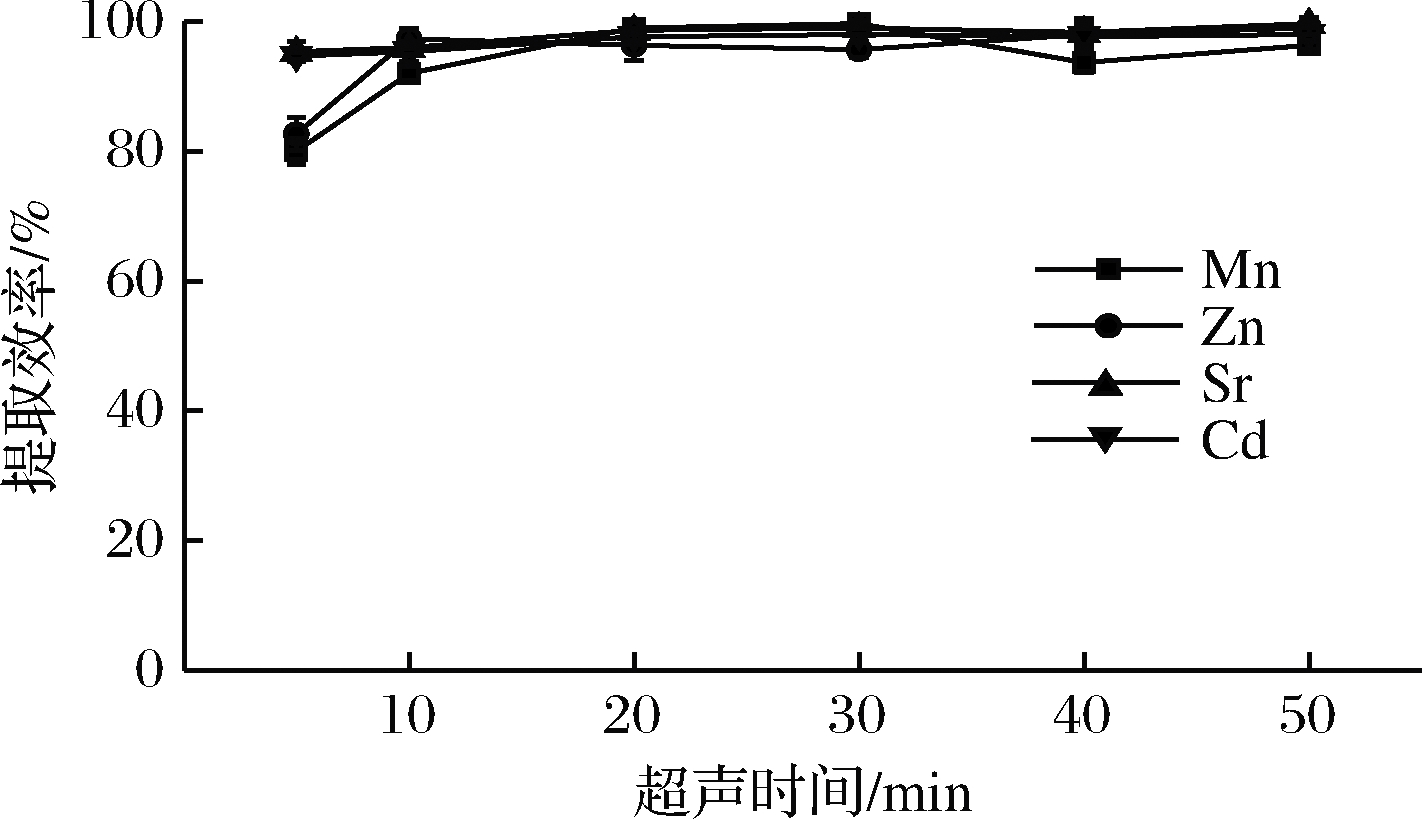
图5 超声时间对Mn、Zn、Sr、Cd提取效率的影响
Fig.5 Influence of ultrasonic time on extraction efficiency of Mn, Zn, Sr and Cd
2.1.6 液料比的优化
不同的液料比对Mn、Zn、Sr、Cd提取效率的影响如图6所示。当液料比(mL∶g)为2∶0.2和4∶0.2时,Mn的提取效率低于80%,当液料比(mL∶g)为6∶0.2时,Mn提取效率迅速提高,达最大值98%;Zn的提取效率随液料比的增加而增加,并在液料比(mL∶g)为7∶0.2时趋于稳定;Sr的提取效率在液料比(mL∶g)为4∶0.2时趋于稳定并且达90%以上;当液料比(mL∶g)为2∶0.2时,Cd提取效率低于50%,当液料比(mL∶g)为7∶0.2及以上时,Cd提取效率达100%。综合考虑提取效率和成本,选择最佳液料比(mL∶g)为7∶0.2。
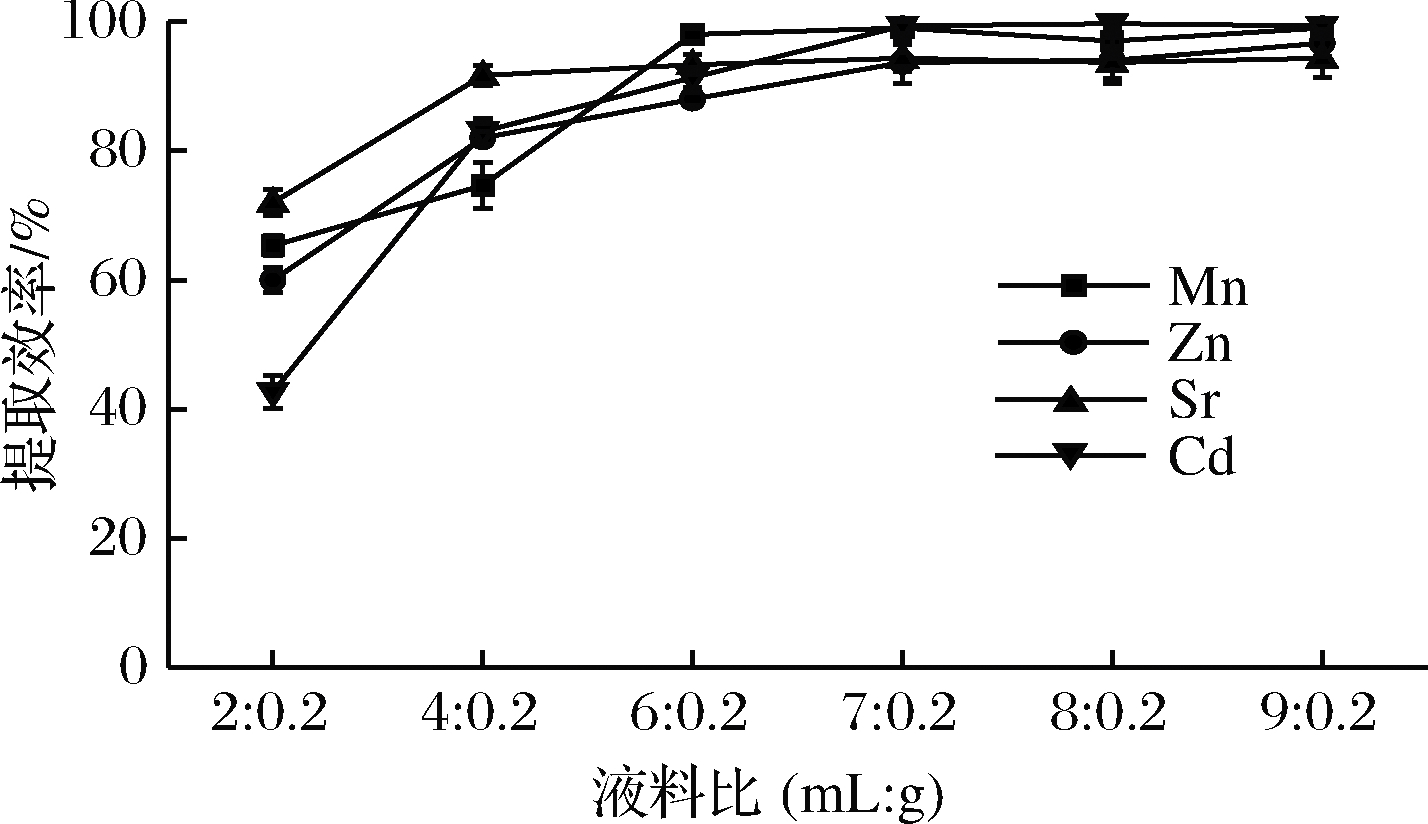
图6 液料比对Mn、Zn、Sr、Cd提取效率的影响
Fig.6 Influence of solvent to substrate ratio on extraction efficiency of Mn, Zn, Sr and Cd
2.2 ICP-MS的干扰及校正
本实验选用7Li、89Y和205Tl作为矫正因子使仪器分辨率在0.65~0.80 amu,氧化物(156/140)≤2%,双电荷(70/140)≤3.0%,根据丰度高、干扰小的原则选择最佳同位素55Mn、66Zn、88Sr、111Cd,使用八级杆氦模式及四级杆质量过滤器消除质谱型干扰。通过加入1 μg/mL的45Sc、72Ge、103Rh、115In内标混合溶液,采用与样品溶液相同浓度的盐酸配制标准溶液进行基体匹配消除基体效应。
2.3 线性关系与检出限
分别配制0.0、1.0、5.0、10.0、20.0、50.0 μg/L的Cd元素标准溶液系列和0.0、20.0、100.0、200.0、500.0、1 000.0 μg/L的Mn、Zn、Sr元素混合标准溶液系列,以质量浓度为1 000 μg/L的115In、45Sc、72Ge、103Rh分别作为111Cd、55Mn、66Zn、88Sr的内标元素进行校正。对试剂空白溶液连续进行11次测定,计算方法检出限。线性回归方程、相关系数及检出限如表2所示。结果表明,在最佳实验条件下,各元素线性良好,相关系数均≥0.999 6。超声酶解法对酸的需求量少,反应温和,检出限为0.001 5~0.086 2 mg/kg。
表2 线性回归方程、相关系数和检出限
Table 2 The linear regression equation, correlation coefficients and detection limit
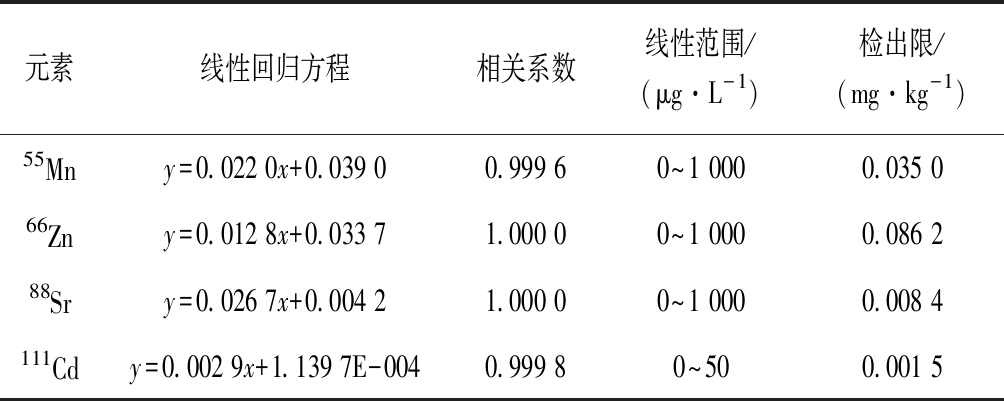
元素线性回归方程相关系数线性范围/(μg·L-1)检出限/(mg·kg-1)55Mny=0.022 0x+0.039 00.999 60~1 0000.035 066Zny=0.012 8x+0.033 71.000 00~1 0000.086 288Sry=0.026 7x+0.004 21.000 00~1 0000.008 4111Cdy=0.002 9x+1.139 7E-0040.999 80~500.001 5
2.4 重复性试验
按照优化的超声酶解条件,对螺旋藻样品进行6份平行试验,分别测定55Mn、66Zn、88Sr、111Cd元素含量,并计算相对标准偏差(relative standard deviation, RSD)。结果如表3所示,结果表明,优化的超声酶解法用于螺旋藻中55Mn、66Zn、88Sr、111Cd的测定其RSD在0.36%~3.51%,测定结果有较好的一致性,方法重复性良好。
表3 超声酶解法测定结果及精密度(n=6)
Table 3 The determination results and precision by ultrasonic enzyme extraction(n=6)

元素元素含量平均值/(mg·kg-1)RSD/%55Mn30.9400.3666Zn9.5773.5188Sr5.6930.40111Cd0.0552.58
2.5 加标回收试验
取螺旋藻样品0.2 g,置于离心管中,分别加入3个浓度水平的55Mn、66Zn、88Sr、111Cd混合标准溶液,在相同的试验条件下进行测定,计算样品加标回收率。结果如表4所示,超声酶解提取法的加标回收率在89.5%~107.8%,回收率较好,说明该法准确可靠。
表4 超声酶解法的加标回收率(n=3)
Table 4 Recovery rate of ultrasonic enzyme extraction(n=3)

元素本底值/(μg·L-1)加标量/(μg·L-1)测定值/(μg·L-1)平均回收率/%RSD/%50.0663.370~687.83089.51.9855Mn634.030200.0810.360~837.08094.81.62500.01 065.530~1 123.56092.72.6950.0241.038~244.58292.30.7366Zn196.782200.0392.982~400.23198.71.38500.0697.006~704.065100.70.5050.0165.303~168.998101.31.1188Sr116.505200.0306.688~314.32597.41.29500.0652.236~658.505107.80.480.51.568~1.68899.83.73111Cd1.1241.02.051~2.12598.62.545.05.476~5.79290.22.80
2.6 质控样品校验
为进一步验证方法的准确性,按照优化的样品前处理方法对国家标准物质螺旋藻(GBW10025)进行测定,标准物质中的55Mn、66Zn、88Sr、111Cd测定值均在标准值范围之内,符合证书要求。结果如表5所示。
表5 螺旋藻(GBW10025)测定结果(n=3)
Table 5 Determination results of spirulina (GBW10025)(n=3)
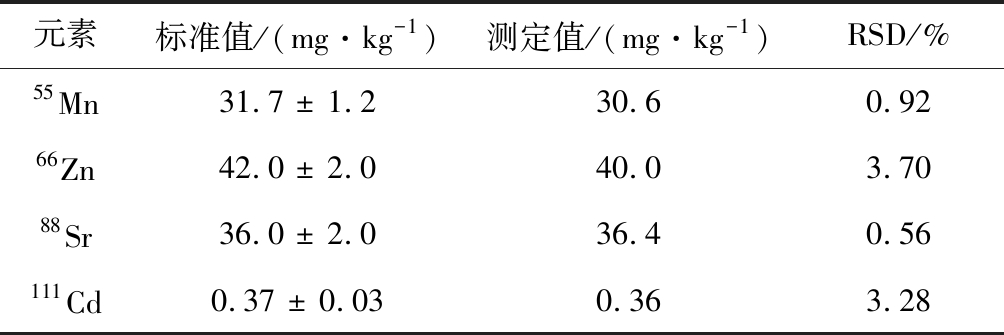
元素标准值/(mg·kg-1)测定值/(mg·kg-1)RSD/%55Mn31.7 ± 1.230.60.9266Zn42.0 ± 2.040.03.7088Sr36.0 ± 2.036.40.56111Cd0.37 ± 0.030.363.28
2.7 藻类样品的测定
采用优化好的前处理及检测方法,对市售的藻类食品(羊栖菜、冰藻、海发菜)中的55Mn、66Zn、88Sr、111Cd进行测定。并与微波消解法的测定值相比计算提取效率,测定结果如表6所示。结果显示,羊栖菜、冰藻、海发菜中的55Mn、66Zn元素提取率均在84%以上,88Sr、111Cd元素均在94%以上。相较传统的微波消解法,超声酶解法用酸量少、耗时短且反应过程温和,测定结果准确可靠,用于藻类食品中Mn、Zn、Sr、Cd的提取具有一定的普适性。
表6 藻类样品测定结果(n=3)
Table 6 Determination results of algal samples(n=3)
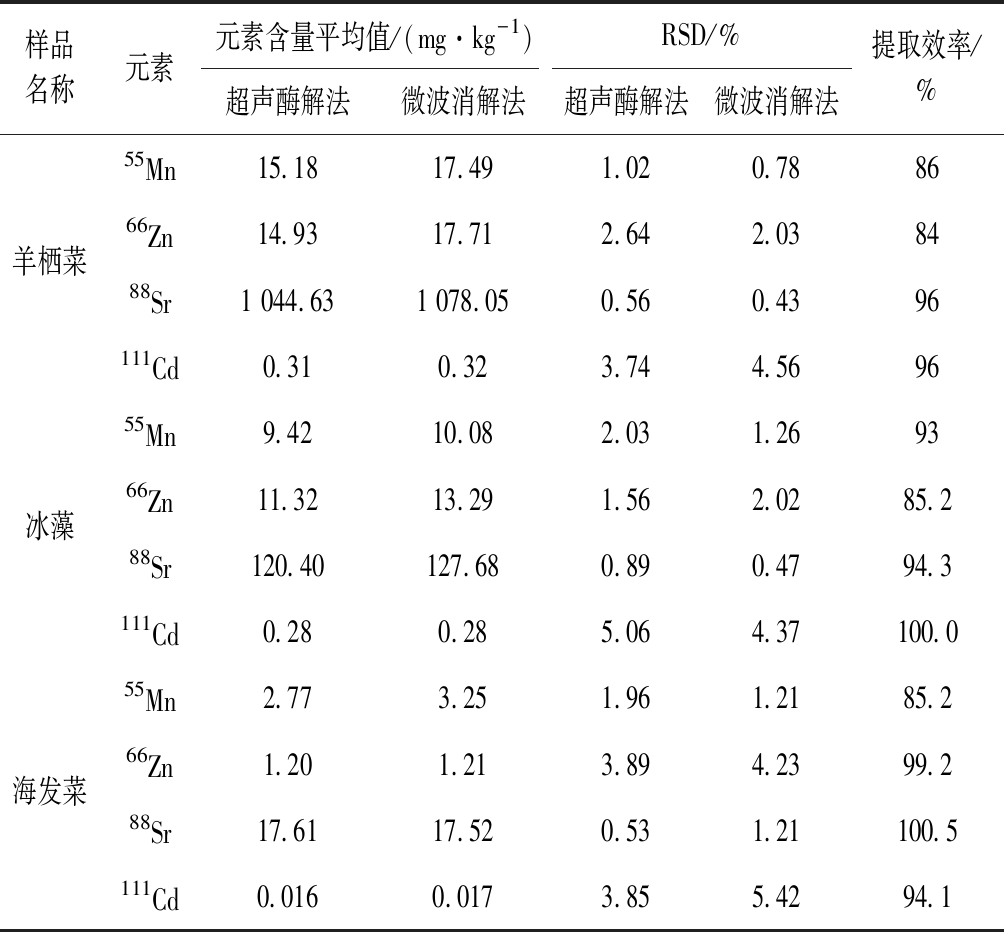
样品名称元素元素含量平均值/(mg·kg-1)RSD/%超声酶解法微波消解法超声酶解法微波消解法提取效率/%55Mn15.1817.491.020.7886羊栖菜66Zn14.9317.712.642.038488Sr1 044.631 078.050.560.4396111Cd0.310.323.744.569655Mn9.4210.082.031.2693冰藻66Zn11.3213.291.562.0285.288Sr120.40127.680.890.4794.3111Cd0.280.285.064.37100.055Mn2.773.251.961.2185.2海发菜66Zn1.201.213.894.2399.288Sr17.6117.520.531.21100.5111Cd0.0160.0173.855.4294.1
3 结论
本研究建立了超声酶解提取-ICP-MS法测定藻类中Mn、Zn、Sr、Cd含量的分析方法。通过选择合适的提取剂及优化酶解条件获得了元素的最佳提取效果。该法精密度和准确度良好,对国家标准物质螺旋藻(GBW10025)进行处理,测定结果均在参考值范围内。与国家标准中的微波消解法相比,藻类食品中Mn、Zn、Sr、Cd的提取率均在84%以上。与传统的前处理方法相比,该法操作简单,用酸量少,绿色节能,反应过程无物料损失且无副反应发生。整个前处理过程可在40 min内完成,且不需要赶酸,更加高效快速。超声酶解提取技术具有广阔的应用前景,在以后的工作中可以进一步开展不同的酶在其他食品元素中提取的研究。
[1] 郑海阳,苑婷婷,谢艳姣,等.16种食用菌类及藻类食品的营养分析[J].中国食用菌,2016,35(6):69-72.
[2] 杨春花,毕健梁,周美丽,等.快速石墨消解-电感耦合等离子体质谱法测定海菜中13种无机元素[J].食品与发酵工业,2019,45(16):281-285.
[3] 周美丽,杨子秋,杨伟,等.3种前处理方法在电感耦合等离子体质谱测定螺旋藻中铅、镉含量的比较[J].食品与发酵工业,2018,44(12):256-260.
[4] 周小瑞,于凤文,韦一,等.不同前处理对原子吸收光谱法测定铜藻中微量元素的对比[J].化学世界,2018,59(5):283-287.
[5] 胡越,丁宏,李梦怡,等.电感耦合等离子体质谱同时测定螺旋藻保健品中16种元素含量[J].食品安全质量检测学报,2019,10(1):111-116.
[6] 胥佳佳,冯鑫,汤静,等.超声辅助提取-高相液相色谱-电感耦合等离子体质谱法测定香菇中6种形态砷化合物[J].食品科学,2016,37(24):216-221.
[7] 袁嫣昊,胡曙光,苏祖俭,等.食品中重金属检测快速前处理技术研究进展[J].食品安全质量检测学报,2019,10(14):4 483-4 491.
[8] 张颜,王一淳,倪莹莹,等.超声辅助酶提取-高效液相原子荧光测定抗癌类海洋中药中硒的形态[J].分析试验室,2019,38(7):850-853.
[9] 裘一婧,贾彦博,方玲,等.超声酶水解提取/高效液相色谱-原子荧光光谱联用法测定动物源性中药中的砷形态[J].中国现代应用药学,2020,36(23):130-136.
[10] 陈绍占,唐德剑,李晓玉,等.超声酶提取-高效液相色谱-电感耦合等离子体质谱法测定谷类食品中硒形态[J].中国公共卫生,2020,36(1):130-136.
[11] 未敏.砷和汞的超声酶萃及其磁固相萃取富集技术研究[D].马鞍山:安徽工业大学,2018.
[12] VALE G, RIAL-OTERO R, MOTA A M, et al. Ultrasonic-assisted enzymatic digestion (USAED) for total elemental determination and elemental speciation: A tutorial[J]. Talanta, 2007, 75(4): 872-884.
[13] MADURO C, VALE G, ALVES S, et al. Determination of Cd and Pb in biological reference materials by electrothermal atomic absorption spectrometry: A comparison of three ultrasonic-based sample treatment procedures[J]. Talanta, 2005, 68(4): 1 156-1 161.
[14] PENA-FARFAL C, MOREDA-PINERO A, BERMEJO-BARRERA A, et al. Speeding up enzymatic hydrolysis procedures for the multi-element determination in edible seaweed[J]. Analytica Chimica Acta, 2005, 548(1): 183-191.
[15] YILMAZ E, SOYLAK M. Innovative, simple and green ultrasound assisted-enzyme based hydrolytic microextraction method for manganese at trace levels in food samples[J]. Talanta, 2017, 174: 605-609.
[16] GB 5009.268—2016 食品安全国家标准食品中多元素的测定[S].北京:中国标准出版社,2017.
[17] 程贤,毕良武,赵振东,等.酶辅助提取技术在天然产物提取中的应用研究进展[J].生物质化学工程,2016,50(3):71-76.