马铃薯是全世界重要的粮食作物之一,由于光照、贮藏不当,致使马铃薯发芽或皮变绿,在这一过程中产生了一类甾体糖苷类生物碱[1],被称为龙葵素,其成分为α-茄碱、β-茄碱、γ-茄碱、α-卡茄碱、β-卡茄碱、γ-卡茄碱6种成分,主要以α-茄碱、α-卡茄碱的形式存在,占总的糖苷生物碱的95%。这类生物碱有较强的毒性[2-12],当成年人一次摄入龙葵素超过200 mg时就会引起中毒[2],含量更高时就会导致舌头发麻、呕吐、腹泻、头晕目眩,甚至昏迷、抽搐、呼吸困难、死亡。科学准确地检测马铃薯中α-茄碱、α-卡茄碱的含量对保障我们每一个人的身体健康具有重要的实际意义。
目前已报道的马铃薯中α-茄碱、α-卡茄碱检测方法主要有比色法[13]、液相色谱法[14-25]、液相色谱-质谱法[26-30],后两种方法研究的比较多。邵慧凯等[15]用异丁醇萃取-高效液相色谱法测定马铃薯中的α-茄碱,运用异丁醇萃取,在210 nm波长处检测,从检测谱图可以看出其检测限偏高,达不到实际检测的需求。赵丹青等[16]用V(乙醇)∶V(乙酸)=100∶30溶液提取,过SPE NH2小柱,V(甲醇)∶V(二氯甲烷)=5∶95洗脱用液相检测,只检测了α-茄碱,没有完全将α-茄碱和α-卡茄碱分开,不能准确地测定α-茄碱和α-卡茄碱的各自含量。张舵[21]用无水乙醇-乙酸提取后液相色谱检测,检测的峰型不好,并且有双头峰。王建凤等[26]用V(1%甲酸)∶V(甲醇)=1∶1提取,采用液质法检测。刘红河等[27]用超高液相色谱串联质谱法检测马铃薯及制品中α-茄碱,用V(甲酸)∶V(甲醇)=1∶1作为溶剂提取,并且用MCX固相萃取柱萃取过程复杂,提取效果不是很理想。戴超等[29]运用液质联用法分析贮藏对马铃薯中α-茄碱含量的影响中用V(乙酸)∶V(乙醇)=1∶10混合溶剂振荡提取,其提取效果不佳。现有的液相色谱普遍存在前处理复杂,提取效果差,检出限偏高,检测结果不理想的问题,而现有的液相-质谱联用法则存在提取不完全,对仪器性能要求高等问题。
本研究在综合分析现有方法的基础上,创新了前处理方法,采用液相色谱法分析检测,同时与液相色谱-质谱联用法进行分析比对,该方法操作简单、检测灵敏度高、稳定性好,能有效监测马铃薯龙葵素的含量,为防止食物中毒提供技术支撑,尤其是可以普及应用到基层的检测机构。
1 材料与方法
1.1 材料与试剂
马铃薯,市购。
甲醇、乙腈(均为色谱纯),默克股份两合公司;甲酸(色谱纯),天津市科密欧化学试剂有限公司;无水硫酸钠、无水乙酸镁、无水硫酸镁、无水乙酸钠、乙酸、乙醇、异丁醇(分析纯),天津市科密欧化学试剂有限公司;磷酸二氢钾(色谱纯),天津市科密欧化学试剂有限公司;α-茄碱(C45H73NO15,CAS号:20562-02-1,纯度≥99.9%),多伦多研究化学公司;α-卡茄碱(C45H73NO14,CAS号:20562-03-2,纯度≥99.9%),ChromaDex公司。
1.2 仪器与设备
岛津LC-20AT型液相色谱仪,日本岛津公司;艾柯Advanced-Ⅱ-12型高纯水机,成都唐氏康宁科技发展有限公司;宁波新芝SB25-12DTD型超声波清洗机,宁波新芝生物科技有限公司;长沙英泰TG16型离心机,长沙英泰仪器有限公司;IKA MS3型涡旋混合器,IKA公司;赛多利斯SQP型电子天平,赛多利斯科学仪器(北京)有限公司;梅特勒PL602E/02便携式天平,梅特勒-托利多仪器(上海)有限公司。
1.3 实验方法
1.3.1 HPLC条件
色谱柱:Hubble C18液相色谱柱(250 mm×4.6 mm,5 μm);流动相A为0.02 mol/L磷酸二氢钾溶液,流动相B为乙腈,流动相比例:A为70%,B为30%,流速0.2 mL/min,柱温30 ℃,进样量10 μL,二级管阵列检测器检测范围190~810nm,检测波长195 nm。
1.3.2 标准曲线溶液的配制
分别称取10 mg α-茄碱和α-卡茄碱于10 mL容量瓶中,用甲醇溶解并定容,配制成1mg/mL的标准储备液;用甲醇逐级稀释成0.2、2、10、20、50、100、200 μg/mL的混合标准系列溶液。
1.3.3 样品前处理
用均质器将样品充分打碎混匀,放入分装容器中,密封并标记,于-20 ℃以下冷冻存放。
称取试样1~2 g(精确至0.001 g)于50 mL具塞离心管中,加入3.0~5.0 mL水涡旋混匀1 min,再准确加入25.0 mL酸化甲醇[V(甲酸)∶V(甲醇)=1∶99],涡旋混匀1 min。之后,向离心管中加入1.0~2.0 g 无水硫酸钠,1.0 g 无水乙酸镁。手动剧烈摇动1 min后涡旋混匀1 min。再将离心管置于离心机中,在室温条件下以10 000 r/min的速度,离心5 min。试样为芽和绿皮时取1 mL上清液于10 mL容量瓶中,加入甲醇水溶液[40%(体积分数)甲醇]定容至刻度;试样为马铃薯肉和制品时取5 mL上清液于试管中氮吹浓缩近干,然后加入1 mL甲醇水溶液[40%(体积分数)甲醇]复溶;过微孔滤膜(0.22 μm,尼龙)后上机测定。
1.3.4 定性、定量方法
在以α-茄碱和α-卡茄碱保留时间定性的基础上,与全扫描光谱定性和色谱峰纯度分析相结合的多重定性方法。以外标法对α-茄碱和α-卡茄碱进行定量分析。
2 结果与分析
2.1 提取方式的选择
马铃薯中α-茄碱、α-卡茄碱的常用提取方法有乙醇法、乙醇-乙酸混合剂法、异丁醇萃取法、乙酸-乙腈法、乙醇-乙腈法等,虽然均能不同程度的提取,但是提取效果均不能达到最佳理想状态。本研究先加入少量水再用酸化甲醇提取,通过加入无水硫酸钠、无水乙酸镁这2种在提取中不参加反应而吸收多余的水,最后在高速离心机上离心。由表1可以看出,通过不同方法的对比得出酸化甲醇能够最大限度地提取α-茄碱、α-卡茄碱,同时与吸水性较弱的无水硫酸镁、无水乙酸钠对比,无水硫酸钠和无水乙酸镁的吸水性更强。这是由于在酸性、含水量少的环境中α-茄碱、α-卡茄碱易溶于甲醇,无水硫酸镁、无水乙酸钠有很强的的吸水能力,致使大量的水分被吸收。
表1 不同试剂提取效果的对比 单位:μg/mL
Table 1 Comparison of extraction effects of different reagents
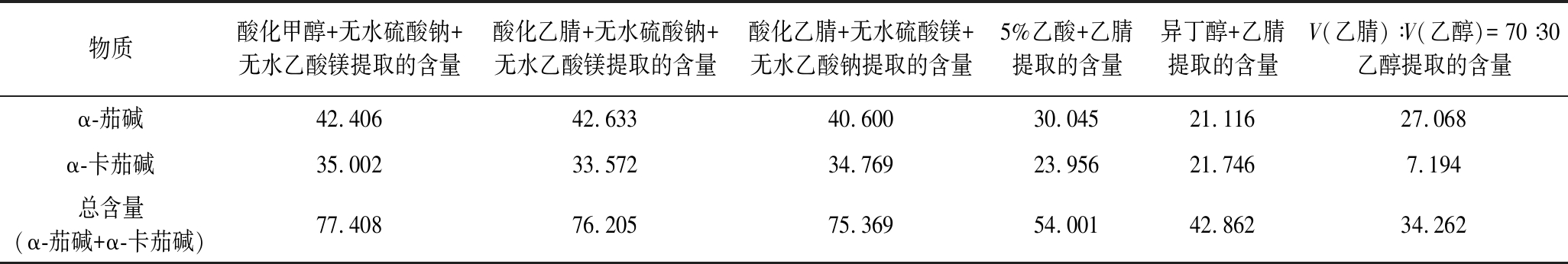
物质酸化甲醇+无水硫酸钠+无水乙酸镁提取的含量酸化乙腈+无水硫酸钠+无水乙酸镁提取的含量酸化乙腈+无水硫酸镁+无水乙酸钠提取的含量5%乙酸+乙腈提取的含量异丁醇+乙腈提取的含量V(乙腈)∶V(乙醇)=70∶30乙醇提取的含量α-茄碱42.40642.63340.60030.04521.11627.068α-卡茄碱35.00233.57234.76923.95621.7467.194总含量(α-茄碱+α-卡茄碱)77.40876.20575.36954.00142.86234.262
2.2 色谱条件的选择
2.2.1 检测波长的选择
马铃薯淀粉含量高,在酸性介质中样品易水解,检测基质复杂,同时α-茄碱和α-卡茄碱保留时间相近,仅依据保留时间定性易出现假阳性。二极管阵列检测可进行全波长扫面,通过对待测样品谱图与α-茄碱和α-卡茄碱标准谱图的扫描光谱和最大吸收波长进行比较,同时可进行色谱峰的纯度分析,利用多重定性方法,排除了基质的干扰,防止假阳性结果的出现,提高了定性分析的准确度。
采用二极管阵列检测器的全波长3D扫描功能,在190~810 nm对α-茄碱和α-卡茄碱进行扫描。扫描结果表明α-茄碱和α-卡茄碱的全波长扫描图基本一致,在190~205 nm时扫描图差别较小,在特征波长195 nm处α-茄碱和α-卡茄碱均有最强的紫外吸收,峰面积和峰高度均达到最高值,具体对比结果见图1,因此本研究确定195 nm作为本方法的定性检测波长。
2.2.2 色谱柱的选择
液相色谱法最常用的多为反相色谱C18柱,因为α-茄碱和α-卡茄碱为疏水性物质,并且在提取介质中加入了甲酸,致使提取液的酸性较强,一般的C18柱无法有效分离,本方法采用了OmniBond HPLC Column Hubble C18 (250 mm×4.6 mm,5 μm),它采用了超纯硅胶和深度键合这2种技术,具有高柱效,高选择性,高pH稳定性。同时对同类型Hubble C18 (150 mm×4.6 mm,5μm)进行对比试验发现无法分离α-茄碱和α-卡茄碱。结果表明HubbleC18 (250 mm×4.6 mm,5 μm)色谱柱能够很好的分离、检测α-茄碱和α-卡茄碱,色谱峰的基线平稳。
2.2.3 流动相体系的选择
检测α-茄碱和α-卡茄碱的流动相体系一般由0.4%磷酸/乙腈、0.1%甲酸水溶液/乙腈、甲醇/甲酸铵、甲醇/乙酸铵、甲醇/甲酸、乙腈/磷酸二氢钾。通过比较乙腈体系的基线噪音比甲醇体系小,分离效果更佳,同时,磷酸二氢钾比乙酸铵、甲酸铵、磷酸、甲酸有更好的分离效果。因此,选用乙腈/磷酸二氢钾作为流动相的体系,并且对磷酸二氢钾的浓度和乙腈的配比进行了对比,发现0.2 mol/L磷酸二氢钾能够很好的调节流动相体系的pH,而当V(磷酸二氢钾)∶V(乙腈)=70∶30时流动相体系的pH为6.0,α-茄碱和α-卡茄碱可以完全分开,并且峰型良好,是最佳的分析条件。

a-190 nm波长的谱图;b-195 nm波长的谱图;c-200 nm波长的谱图;d-190、195、200 nm波长下色谱峰的相关信息
图1 不同波长时α-茄碱和α-卡茄碱的色谱图及峰表
Fig.1 Chromatogram and peak table of α-solanine and α-chaconine at different wavelengths
2.2.4 流动相淋洗方式的选择
流动相采用梯度淋洗时能够较早的出峰,但是基线不平稳,致使α-卡茄碱分离的效果不佳。因为α-茄碱和α-卡茄碱出峰时间相差很小,用等度淋洗时,可以保持流动相体系的酸性环境稳定,在有效分离α-茄碱的同时也可有效分离α-卡茄碱。
2.2.5 流动相流速的选择
分别对0.10、0.15、0.20、0.25、0.30、0.40、0.50、0.60、0.80、1.00 mL/min时的分离效果进行了比对。研究结果表明,随着流速的增大,保留时间缩短,峰宽变窄,峰面积降低,α-茄碱和α-卡茄碱的峰重叠越严重。综合保留时间、峰面积、分离度等因素,最终确定流动相流速为0.2 mL/min,。在此优化条件下,α-茄碱和α-卡茄碱分离效果良好,标准谱图见图2,马铃薯芽样品中的α-茄碱和α-卡茄碱谱图见图3。
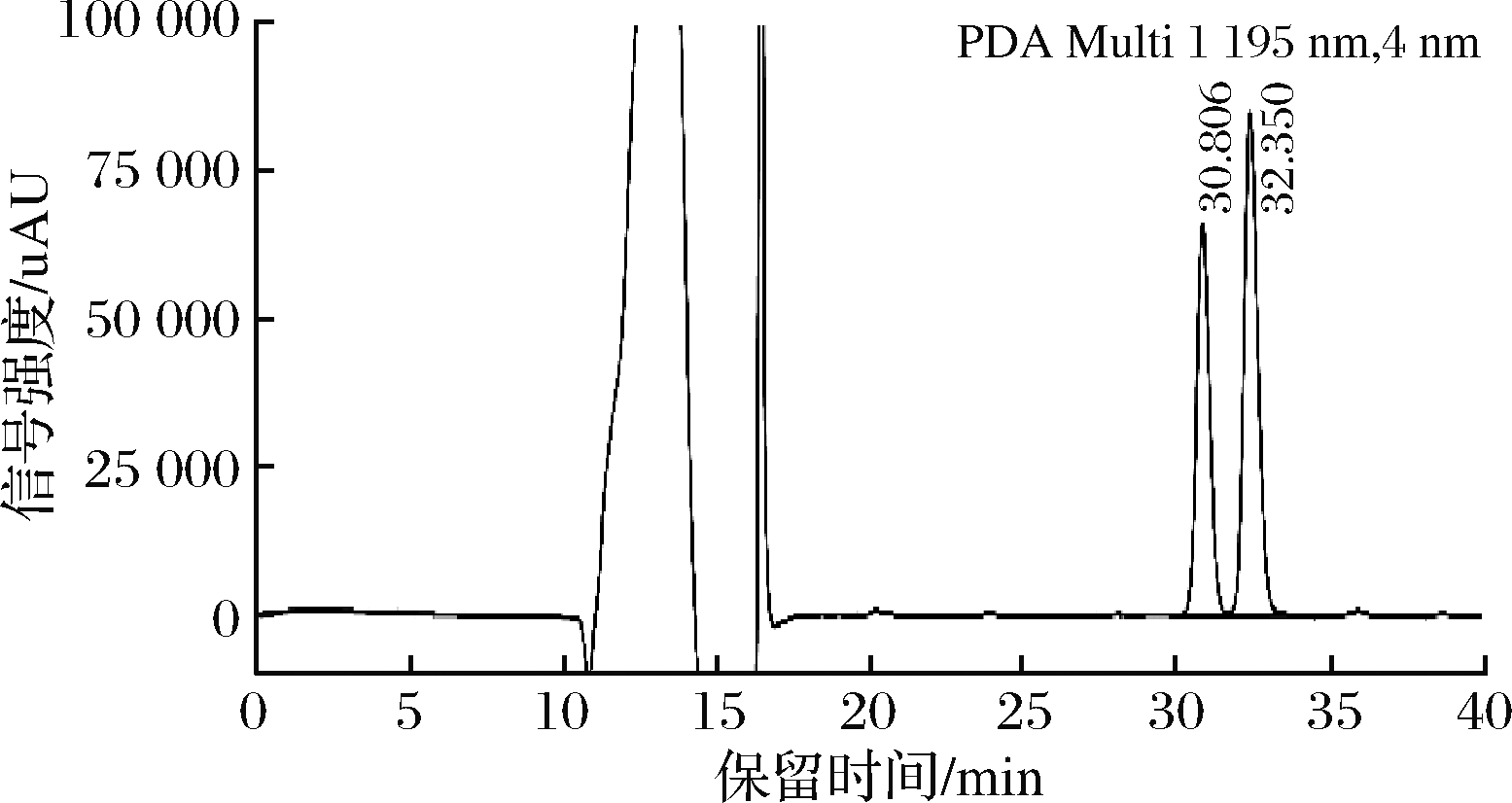
图2 100.0 μg/mL α-茄碱和α-卡茄碱标准溶液液相色谱图
Fig.2 Liquid chromatogram of 100.0 μg/mL α - solanine and α-chaconine standard solution
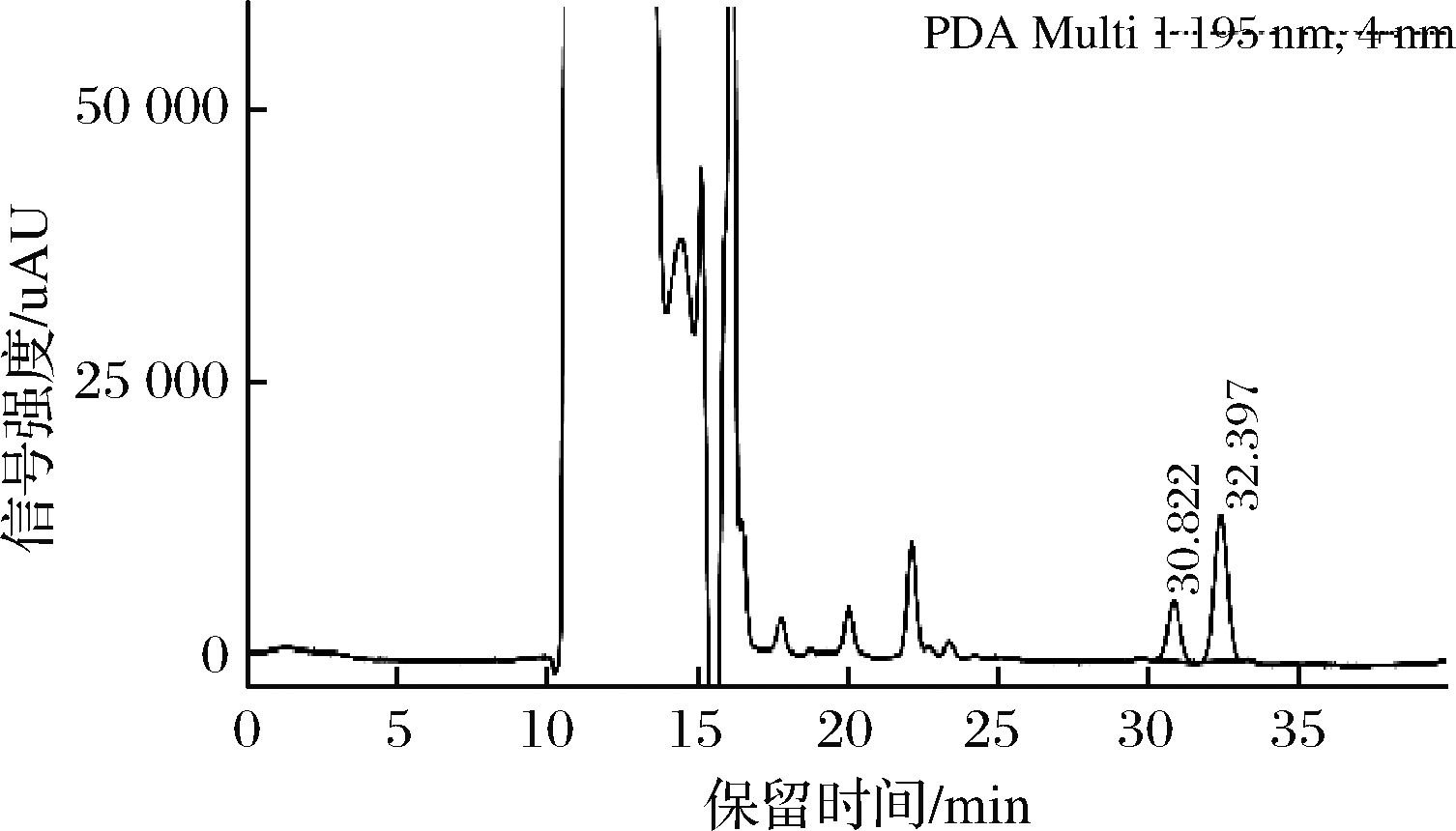
图3 马铃薯芽中α-茄碱和α-卡茄碱的色谱图
Fig.3 Chromatogram of α - solanine and α-chaconine in potato bud
2.3 标准曲线与检出限
分别以质量浓度(X, μg/mL)为横坐标、峰面积(Y)为纵坐标绘制标准曲线,α-茄碱和α-卡茄碱的线性方程及其相关系数见表2。由表2可以看出在质量浓度0.20~200 μg/mL时,2种茄碱的线性关系良好,相关系数(R2)为0.999 3~0.999 8,满足定量分析的要求。
表2 α-茄碱和α-卡茄碱的线性方程、相关系数(R2)、 及其方法检出限
Table 2 Linear equation, correlation coefficient (R2) and detection limit of α-solanine and α-chaconine

化合物保留时间/min线性方程相关系数(R2)检出限/(mg·kg-1)α-茄碱30.806y=19 320.3x+0.00.999 80.5α-卡茄碱32.352y=26 370.5x+0.00.999 30.5
以不含茄碱的新鲜马铃薯肉作为空白基质,在其中加入低浓度α-茄碱和α-卡茄碱,按照本研究的上述方法进行前处理和分析检测,以3倍、10倍信噪比分别计算得到本方法中α-茄碱和α-卡茄碱的检出限均为0.5 mg/kg,定量限均为1.7 mg/kg,说明本方法的灵敏度很高。
2.4 回收率和精密度
选用已测定α-茄碱和α-卡茄碱含量的马铃薯芽,分别添加4.0、6.0、10.0 μg/mL 三个质量浓度水平的α-茄碱和α-卡茄碱混合标准溶液,配成加标样品,按照上述方法进行前处理,每个加标水平的样品平行测定6次,结果加标回收率为98%~107%,相对标准偏差为0.05%~0.44%(表3),说明本方法有较高的准确度和精密度,完全适合马铃薯中α-茄碱和α-卡茄碱的分析检测。
表3 α-茄碱和α-卡茄碱的回收率和精密度
Table 3 Recoveries and RSDs of α-solanine and α-chaconine

化合物加标浓度4.0 μg/mL加标浓度6.0 μg/mL加标浓度10.0 μg/mL回收率/%相对标准偏差RSD/%回收率/%相对标准偏差RSD/%回收率/%相对标准偏差RSD/%α-茄碱1050.051070.12980.33α-卡茄碱1070.061020.14990.44
2.5 马铃薯样品分析
用本方法对马铃薯的芽、绿皮、肉、马铃薯淀粉、马铃薯粉条的5种样品平行测定2次,平均结果见图4,由检测结果可看出,马铃薯芽中的α-茄碱和α-卡茄碱含量是很高的,在马铃薯芽、绿皮、肉、淀粉、粉条依次降低。

图4 马铃薯样品中龙葵素含量(α-茄碱+α-卡茄碱) 柱形图
Fig.4 Column chart of α-solanine and α-chaconine content in potato samples
2.6 与液-质法的对比
对马铃薯的肉、白芽、绿芽分别用本研究方法和土豆及其制品中α-茄碱和α-卡茄碱的测定补充方法中液相色谱-串联质谱仪法(BJS201806)进行提取、测定,检测结果见表4,可以看出2种方法的检测结果的相对偏差为4.0%~8.8%,本研究的液相色谱法检测的含量均比补充方法BJS201806高。说明本方法能够更加科学准确地测定α-茄碱和α-卡茄碱的含量。
表4 液相色谱法与液相-质谱法检测结果的对比
Table 4 Comparison between the results of liquid chromatography and liquid mass spectrometry

名称马铃薯肉马铃薯白芽马铃薯绿芽液-质法测含量/(mg·kg-1)液相法测含量/(mg·kg-1)相对偏差/%液-质法测含量/(mg·kg-1)液相法测含量/(mg·kg-1)相对偏差/%液-质法测含量/(mg·kg-1)液相法测含量/(mg·kg-1)相对偏差/%α-茄碱12.312.84.03183.03460.28.32207.82342.05.9α-卡茄碱27.028.86.53588.53896.28.22594.02831.58.8
3 结论
本研究建立了高效液相色谱-二极管阵列检测器测定马铃薯中α-茄碱和α-卡茄碱的方法。利用酸化甲醇提取,以二极管阵列检测器的全扫描和色谱纯度分析进行定性,很大程度解决了现有报道文献方法中提取不完全、分析检测不准确的问题。该方法前处理简单、灵敏度高,具有良好的精密度、准确度,可作为马铃薯及其制品中α-茄碱和α-卡茄碱监测分析,防止马铃薯存储不善而食用后引起的食物中毒事件发生,该方法可普及到市、县级基层检验检测机构,对于食品安全监管具有重要的现实意义。
[1] MENDEL FRIEDMAN,CAROL E LEVIN. α-Tomatine content in tomato and tomato products determined by hplc with pulsed amperomet-ric detection[J]. J Agric Food Chem,1995,43(6):1 507-1 511.
[2] 徐敏慧,刘珂伟,张晓慧,等.马铃薯中龙葵素的研究进展[J].保鲜与加工,2017,17(1):112-116.
[3] FRIEDMAN M. Analysis of biologically active compounds in pota-toes (Solanum tuberosum), tomatoes(Lycopersicon esculen-tum), and jimson weed (Datura stramonium) seeds[J]. J. Chro-matogr A,2004,1054(1~2):143-155.
[4] MENDEL FRIEDMAN. Tomato glycoalkaloids: Role in the plant and in the diet[J]. J Agric Food Chem,2002,50(21):5 751-5 780.
[5] FRIEDMAN M, MCDONALD G. Potato glycoalkaloids: Chemistry, analysis, safety,and plant physiology[J].Crit Rev Plant Sci,1997, 16:55-132.
[6] CATCHPOLE G S, BECKMANN M, ENOT D P, et al. Hierarchical metabolomics demonstrates substantial compositional similarity between genetically modified and conventional potato crops[J]. P Natl Acad Sci USA,2005,102(40):14 458-14 462.
[7] 吴延.马铃薯主粮化的关键与种植技术[J].农村新技术,2015,(4):4-6.
[8] 李彦杰,杨俊年,刘仁华,等.芽期和发酵期马铃薯中龙葵素含量动态及组分分析[J].黑龙江畜牧兽医,2014(13):114-116.
[9] 平华,马智宏,李杨,等.不同发芽天数及芽周不同深度马铃薯中α-茄碱含量变化规律[J].食品科技,2017,42(1):55-59.
[10] 李志文,王娜,刘翔,等.马铃薯中a-茄碱提取工艺优化[J].食品与机械,2016,32 (8):167-172.
[11] 赵建宗,申建平.我国马铃薯种薯质量监督控制体系现状、问题与建议[J].种子, 2017,36(12):92-94.
[12] 马全胜.马铃薯中毒的防治措施[J].中兽医学杂志, 2017(5):32-32.
[13] 王运雷,张辉.马铃薯皮、马铃薯渣、块茎中α-茄碱含量的测定[J].畜牧与饲料科学, 2018,39(5):19-21.
[14] 曾凡逵,周添红,康宪学,等. HPLC法测定马铃薯块茎中糖苷生物碱的含量[J].中国马铃薯, 2015,29(5):263-268.
[15] 邵慧凯,丘汾,何佳平,等.异丁醇萃取-高效液相色谱法测定马铃薯中a-卡茄碱[J].中国食品卫生杂志, 2015,27(5): 517-520.
[16] 赵丹青,张锋锋,吴燕,等.宁夏不同地区不同品种马铃薯中龙葵素在不同生长期的积累含量测定[J].中国野生植物资源, 2017,36(6):29-31.
[17] 商婷婷,邝梦婷,胡新喜,等. HPLC-ELSD法同时测定马铃薯中α-茄碱和α-卡茄碱含量[J].食品与机械, 2015,31(4):55-58.
[18] 罗爱花,徐美蓉,陆立银,等.利用HPLC法测定不同马铃薯品种茎叶中的α-茄碱含量[J].中国马铃薯,2014,28(6):331-334.
[19] 王守兰,朱佳.高效液相色谱法测定马铃薯中α-茄碱的含量[J].食品科学,1996,17(6):60-61.
[20] 肖文军,李勤,熊兴耀,等.高效液相色谱法分析马铃薯中α-茄碱[J].分析化学, 2011,39(9):1 459-1 460.
[21] 张舵.反相高效液相色潽法检测马铃薯中龙葵素含量[J].齐齐哈尔大学学报, 2013,29(5):24-25.
[22] FANG L, WAN M, PENNACCHIO M, et al. Evaluation of evaporative light- scattering detector for combinatorial library quantitation by reversed phase HPLC[J].J Comb Chem,2000,2(3):254-257.
[23] ROBERT J HOUBEN, KOMMER BRUNT. Determination of glycoalka-loids in potato tubers by reversed high-performance liquid chromatography[J].Journal of Chromatography A,1994,661(1-2):169-174.
[24] LAN DAO, MENDEL FRIEDMAN. Comparison of glycoalkaloid content of fresh and freeze- dried potato leaves determined by HPLC and colormetry[J]. Agric Food Chem,1996(8):2 287-2 291.
[25] SOTELO A, SERRANO B. High-performance liquid chromatographic determination of the glycoalkaloids alpha-solanine and alpha-chaconine in 12 commercial varieties of Mexican potato [J]. Agric Food Chem,2000,48(6):2 472-2 475.
[26] 王建凤,范筱京,贾丽,等.超高液相色谱串联质谱法检测土豆及土豆制品中α-茄碱[J].食品安全质量检测学报,2017,8(7): 2 756-2 761.
[27] 刘红河,康莉,廖仕成,等.超高效液相色谱-质谱法测定食物中毒样品中α-茄碱和α-卡茄碱[J].华南预防医学,2016,42(5): 435-442.
[28] 伍慧敏,曾静,李美,等.液相色谱-质谱联用法检测马铃薯中α-茄碱含量[J].食品科学,2013,34(24):121-124.
[29] 戴超,郑鹭飞,刘佳萌,等.液质联用法分析贮藏因素对马铃薯中α-茄碱含量的影响[J].核农学报,2017,31(11):2 200-2 205.
[30] 王丹,丁颢,程莉,等.超高效液相色谱-三重四级杆串联质谱法测定土豆中α-茄碱与α-卡茄碱含量[J].中国食品卫生杂志, 2014,26(3):233-237.