苹果是世界四大水果之冠,汁甜肉脆,富含铁、钾、有机酸等营养成分,有清热化痰,补中益气的功效[1]。鲜切苹果是指苹果经去皮、去核、切分、保鲜等工艺处理的轻加工产品,很大程度上保持了苹果肉脆、多汁、味美的特征[2]。随着生活方式的改变,鲜切苹果等营养、健康、安全,方便的轻加工食品已经形成并深受消费者喜爱,然而加工过程中的机械损伤加速了鲜切苹果水分及营养物质流失,同时促进酶促褐变、组织软化、果片表面微生物生长,严重降低鲜切苹果的营养价值和商品价值,极大地缩短了鲜切苹果的货架期[3-5]。目前,通过物理保藏方法,如低温贮藏、食用涂膜、气调保鲜、紫外辐照等方式处理鲜切苹果,不同程度地延长了鲜切苹果的货架期,但这类方法对贮藏环境要求严苛,投入成本过高,技术要求复杂,难以控制[6-8]。化学保鲜方法成本低廉、操作简便、保鲜效果好,被人们广泛接受。例如,抗坏血酸(Vc)等抗氧化剂是防止鲜切水果褐变,保持水果品质的重要方法,但Vc性质不稳定,易氧化,当Vc被完全氧化成脱氢抗坏血酸时就会丧失抑制褐变的能力,同时可能会引起鲜切苹果的氧化损伤[9-10]。因此,开发稳定、安全的抗氧化剂是目前果蔬保鲜的重要工作。
硒(selenium,Se)被誉为“生命元素”,是人体必须的微量营养元素及一些抗氧化酶(谷胱甘肽过氧化物酶、谷氨酸还原酶等)的重要组成成分[11],有增强免疫、抗氧化、预防心血管疾病、拮抗重金属毒性等功效[12-14]。因此富硒农产品开发已然成为热潮,但是硒的活性与毒性之间的作用范围较窄,相比于无机硒和有机硒,纳米硒(SeNPs)具有毒性小,生物利用度高,生物活性好的优势[15-16]。目前SeNPs主要用于药物开发,在果蔬保鲜方面的研究鲜有报道。本试验以Vc还原亚硒酸钠制得Vc修饰纳米硒(Vc modified nano selenium,Vc@SeNPs),通过测定体外抗氧化指标及鲜切苹果褐变,失重率、平均散失率和总酚含量,初步评价Vc@SeNPs对鲜切苹果品质的影响,以期获得即可膳食补硒,又可保持鲜切苹果品质的果蔬保鲜剂,并为开发更加安全有效的果蔬保鲜剂提供理论依据。
红富士苹果:选取大小均一,八至九成熟,无机械损伤和病虫害,购买后保存于4 ℃冰箱。
Vc、30% H2O2、FeSO3、水杨酸、邻苯三酚,均为分析纯,天津永大化学试剂厂;亚硒酸钠,郑州红祥化工有限公司;聚乙烯吡咯烷酮(polyvinyl pyrrolidone,PVP)、亚硒酸钠、Na2CO3、1,1-二苯基-2-三硝基苯肼(1,1-diphenyl-2-picrylhydrazyl,DPPH),2,2-连氮基-双-(3-乙基苯并二氢噻唑啉-6-磺酸)[2,2-azino-bis(3-ethylbenzothiazoline-6-sulfonic acid),ABTS]、福林酚,北京索莱宝科技有限公司;其他试剂,国药集团化学试剂有限公司。
Titan透射电镜,中国FEI公司;多功能酶标仪,Moecular Devices;UV-5200型UV-可见分光光度计,上海元析仪器有限公司;傅里叶变换红外光谱,美国Thermo公司;AUY120型电子天平,岛津公司;CL-3型磁力搅拌器,巩义市予华仪器有限责任公司;KQ-250DE型数控超声波清洗器,昆山市超声仪器有限公司。
1.2.1 Vc@SeNPs的制备
依据软模板法制备Vc@SeNPs并适当调整[17]。以PVP为模板剂,Vc为还原剂。将200 μL Vc溶液(0.2 mol/L)加入小烧杯中,并用磁力搅拌器轻轻搅拌,然后将100 μL亚硒酸钠溶液(0.1 mol/L)和50 μL PVP(5.0 g/L)溶液滴入Vc溶液中,搅拌至颜色由无色变至砖红色,将所得溶液离心,弃去上清液,将沉淀复溶后定容至10 mL,4 ℃保存。
1.2.2 Vc@SeNPs的化学表征
1.2.2.1 紫外-可见光谱(ultraviolet-visible absorption spectrometry, UV-Vis)测定
将Vc与Vc@SeNPs稀释至适当浓度后,在190~450 nm波长范围内检测紫外扫描吸收峰。
1.2.2.2 傅里叶变换红外光谱(Fourier transform infrared spectroscopy, FT-IR)测定
FT-IR测定采用溴化钾压片法,取适量冷冻干燥的Vc@SeNPs粉末与溴化钾按照1∶100质量比混合,测定红外吸收峰。
1.2.2.3 透射电镜(transmission electron microscope,TEM)表征
取10 μL Vc@SeNPs滴至TEM专用铜网上,室温放置至干燥,于FEI透射电子显微镜上观察并拍照。
1.2.3 Vc@SeNPs体外抗氧化活性测定
1.2.3.1 还原力测定
参考OYZIAU[18]测定还原力的方法并适当调整。不同浓度的Vc@SeNPs溶液及Vc溶液1 mL,加入2.5 mL磷酸盐缓冲液(0.2 mmol/L,pH 6.6)、2.5 mL K3Fe(CN)6(10 g/L)溶液,50 ℃水浴20 min,然后加入2.5 mL三氯乙酸(100 g/L)溶液,终止反应后3 000 r/min离心10 min, 取上清液2.5 mL,加入2.5 mL蒸馏水和0.5 mL FeCl3(1.0 g/L),测定700 nm处混合物的吸光度。
1.2.3.2 超氧阴离子自由基![]() 清除能力测定
清除能力测定
参照MARKLUND[19]测定![]() 取不同浓度Vc@SeNPs溶液1 mL分别与4.5 mL Tris-HCl(50 mmol/L,pH 8.2)混匀,25 ℃水浴20 min,随后加入0.4 mL邻苯三酚(25 mmol/L),25 ℃反应5 min后立即加入1 mL HCl溶液(8 mmol/L)终止反应,以Tirs-HCl为空白对照,Vc为阳性对照,测定325 nm处吸光度,各组均为3个平行,取平均值,按公式(1)计算清除率:
取不同浓度Vc@SeNPs溶液1 mL分别与4.5 mL Tris-HCl(50 mmol/L,pH 8.2)混匀,25 ℃水浴20 min,随后加入0.4 mL邻苯三酚(25 mmol/L),25 ℃反应5 min后立即加入1 mL HCl溶液(8 mmol/L)终止反应,以Tirs-HCl为空白对照,Vc为阳性对照,测定325 nm处吸光度,各组均为3个平行,取平均值,按公式(1)计算清除率:
(1)
式中:E,清除率,%;A0,空白吸光度;A1,样品吸光度;A2,显色剂本底吸光度。
1.2.3.3 羟自由基(·OH)清除能力测定
参照LI等[20]的方法测定·OH清除能力。取不同浓度的Vc@SeNPs溶液1 mL分别与FeSO4(9 nmol/L,1 mL)、水杨酸-乙酸溶液(9 nmol/L,1 mL)、H2O2溶液(9 nmol/L,1 mL)混匀,37 ℃水浴30 min,以超纯水为空白, Vc为阳性对照,510 nm处测定吸光值,各组均为3个平行,取平均值,根据1.2.3.2中公式(1)计算清除率。
1.2.3.4 DPPH自由基清除能力测定
参照MA等[21]的方法稍作改动。取不同浓度的Vc@SeNPs溶液及DPPH-乙酸溶液各2 mL,摇匀,25 ℃避光放置30 min,在517 nm处测定吸光度,以无水乙醇替代样品溶液为空白对照,以不同浓度Vc溶液作为阳性对照,各组均为3个平行,取平均值。根据1.2.3.2中公式(1)计算清除率。
1.2.4 Vc@SeNPs对鲜切水果的保鲜试验
1.2.4.1 鲜切苹果的处理
将置于4 ℃的苹果在室温(22 ~25 ℃)条件下放置2 h后清洗、去皮、去核、切块(切为1cm左右厚度的苹果片),分别用蒸馏水、10、30、50 g/L Vc@SeNPs或Vc浸泡后,测定各个时间段的相关指标。
1.2.4.2 感官评价
参照管磬馨等[22]的方法。请10位具备食品感官评定专业知识的人员对苹果切片的色泽、气味、组织状态等指标进行评分,评定标准如表1所示。
表1 鲜切苹果感官评分细则
Table 1 Fresh-cut apple sensory score rules

评分项目评分标准分数色泽外观(30分)白色或微黄色,颜色分布均匀黄色, 某些部位颜色较深棕褐色, 颜色分布不均匀21~3011~2010分以下气味(30分)具有明显的苹果香味,无不良气味无苹果香味,略有不良气味16~3015分以下组织状态(40分)组织状态完整,结构紧密组织状态不完整,结构松散21~4020分以下
1.2.4.3 褐变度测定
称取2 g鲜切苹果,分别放入30 mL 10、30、50 g/L Vc或Vc@SeNPs溶液及蒸馏水中浸泡,观察不同时间段内鲜切苹果的褐变情况,并拍照。
1.2.4.4 失重率和平均散失率测定
将鲜切苹果分别放入装有30 mL 10、30、50 g/L Vc或Vc@SeNPs溶液及蒸馏水中,浸泡30 min后用滤纸吸干其表面附着的水分,室温(25 ℃)置于保鲜膜上,每隔30 min称重并记录数值。按公式(2)计算失重率,按公式(3)计算平均散失速率:
失重率![]()
(2)
平均散失速率![]()
(3)
1.2.4.5 总酚含量测定
参照韩菊等[23]的方法。称取0.5 g鲜切苹果放入研砵中,分别加入100 μL 10、30、50 g/L Vc@SeNPs溶液,研磨成浆后定容至10 mL容量瓶中,取250 μL的样液于10 mL试管中,再加入1.25 mL福林酚试剂,摇匀,3 min后加入75 g/L的Na2CO3溶液1 mL,振荡。静置1 h后在765 nm处测定吸光值,以10、30、50 g/L Vc溶液为阳性对照,蒸馏水代替Vc@SeNPs做空白测定,以没食子酸做标准品测定标准曲线。每组重复测量3次,取平均值。
试验所得数据均采用SPSS 22.0软件进行分析,结果表示为均值±标准差(Mean±SD),P<0.05表示显著差异。运用Origin 2018进行绘图。
2.1.1 紫外-可见光谱分析
Vc及Vc@SeNPs的UV-Vis光谱如图1所示。在220 nm以下的远紫外区,Vc及Vc@SeNPs均有最大吸收峰,Vc的最大吸收峰位于266 nm处,Vc@SeNPs的最大吸收峰位于256 nm处。最大吸收峰蓝移10 nm。依据王娜等[24]以没食子酸修饰纳米硒的紫外光谱,杨志恒等[25]对纳米TiO2/β-CDP复合物的紫外光谱,可以推测Vc还原亚硒酸钠后Vc侧链的羟基(—OH)与SeO结合形成Se—O共价键,从而影响—OH吸收峰,导致Vc@SeNPs特征峰蓝移。
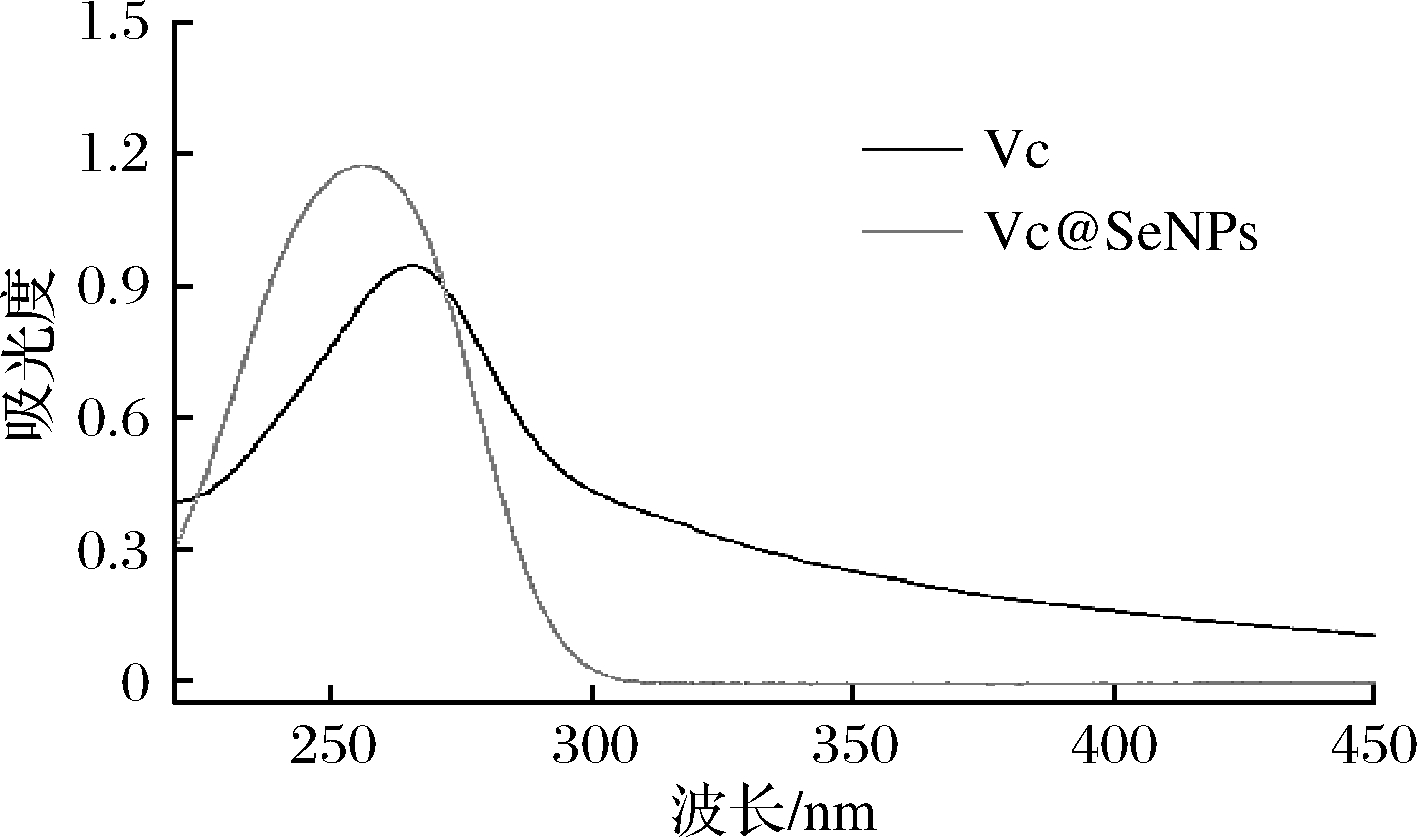
图1 Vc@SeNPs的紫外-可见光谱
Fig.1 UV-Vis spectra of Vc@SeNPs
2.1.2 FT-IR光谱分析
Vc@SeNPs红外光谱如图2所示。

图2 Vc@SeNPs红外图谱表征
Fig.2 Vc@SeNPs characterization of FT-IR
Vc图谱中3 410.65 cm-1为—OH伸缩振动,1 029.56 cm-1为—OH面内弯曲振动峰[26]。对比Vc图谱发现,Vc@SeNPs图谱中的上述特征峰均发生移动,这是由于Vc侧链中的—OH与SeO结合后形成Se—O共价键,分子间氢键作用增强,表明Vc与SeNPs结合形成Vc@SeNPs[27]。
2.1.3 TEM表征
Vc@SeNPs的形貌如图3所示。Vc@SeNPs呈明显单分散球状颗粒,分散性良好,粒径分布均匀。粒径分布如图4所示,通过Nano Measurer 1.2软件分析得出Vc@SeNPs平均粒径为64.80 nm。

图3 Vc@SeNPs透射电镜表征
Fig.3 TEM characterization of Vc@SeNPs
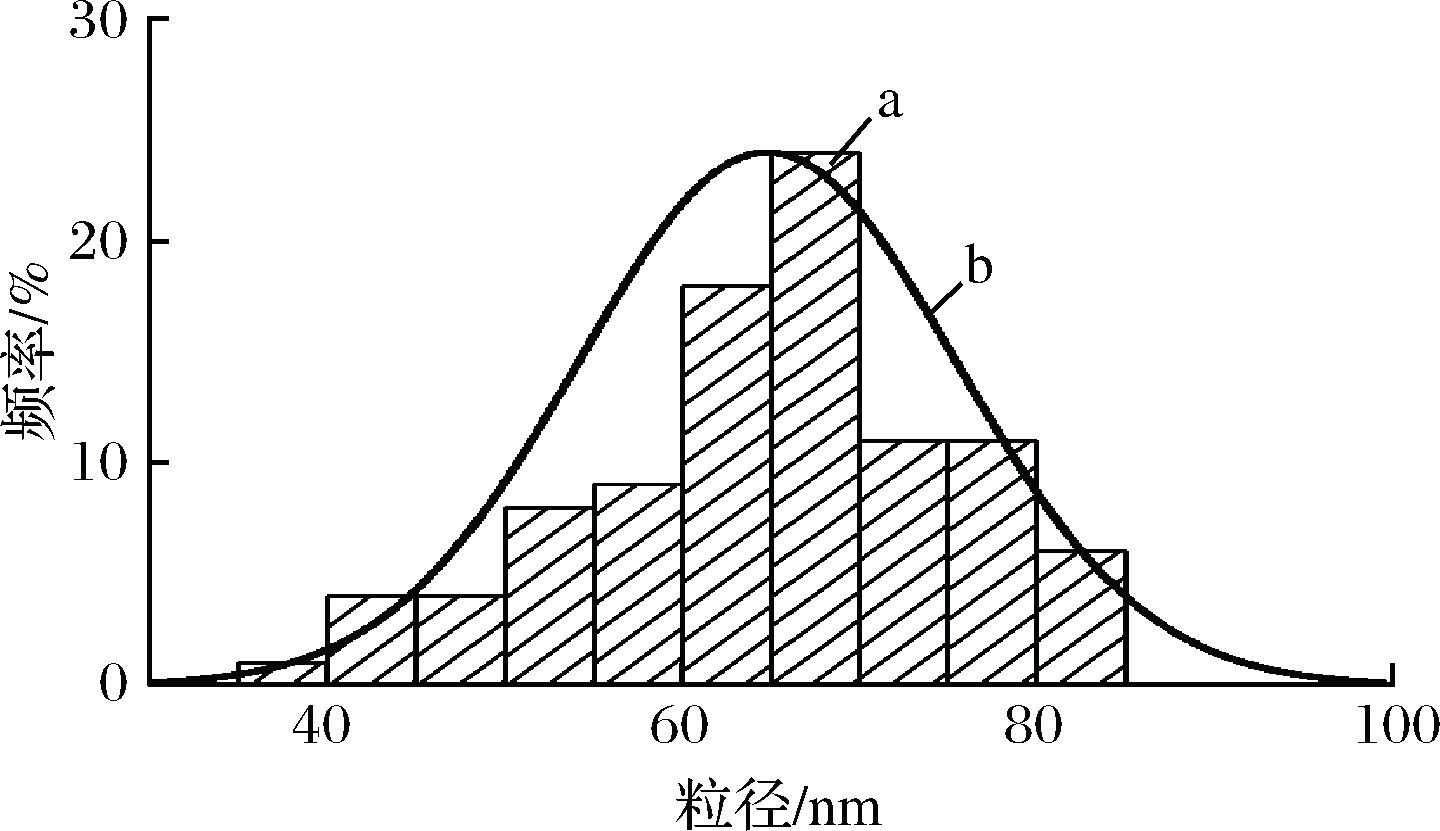
图4 Vc@SeNPs粒度分布柱状图(a)及分布曲线(b)
Fig.4 Vc@SeNPs particle size distribution histogram(a) and distribution curve(b)
2.2.1 Vc@SeNPs还原力活性评价
还原力被认为是评价抗氧化能力最重要的指标,直接反映了抗氧化剂清除自由基能力的强弱[18]。Vc@SeNPs的还原能力如图5所示。
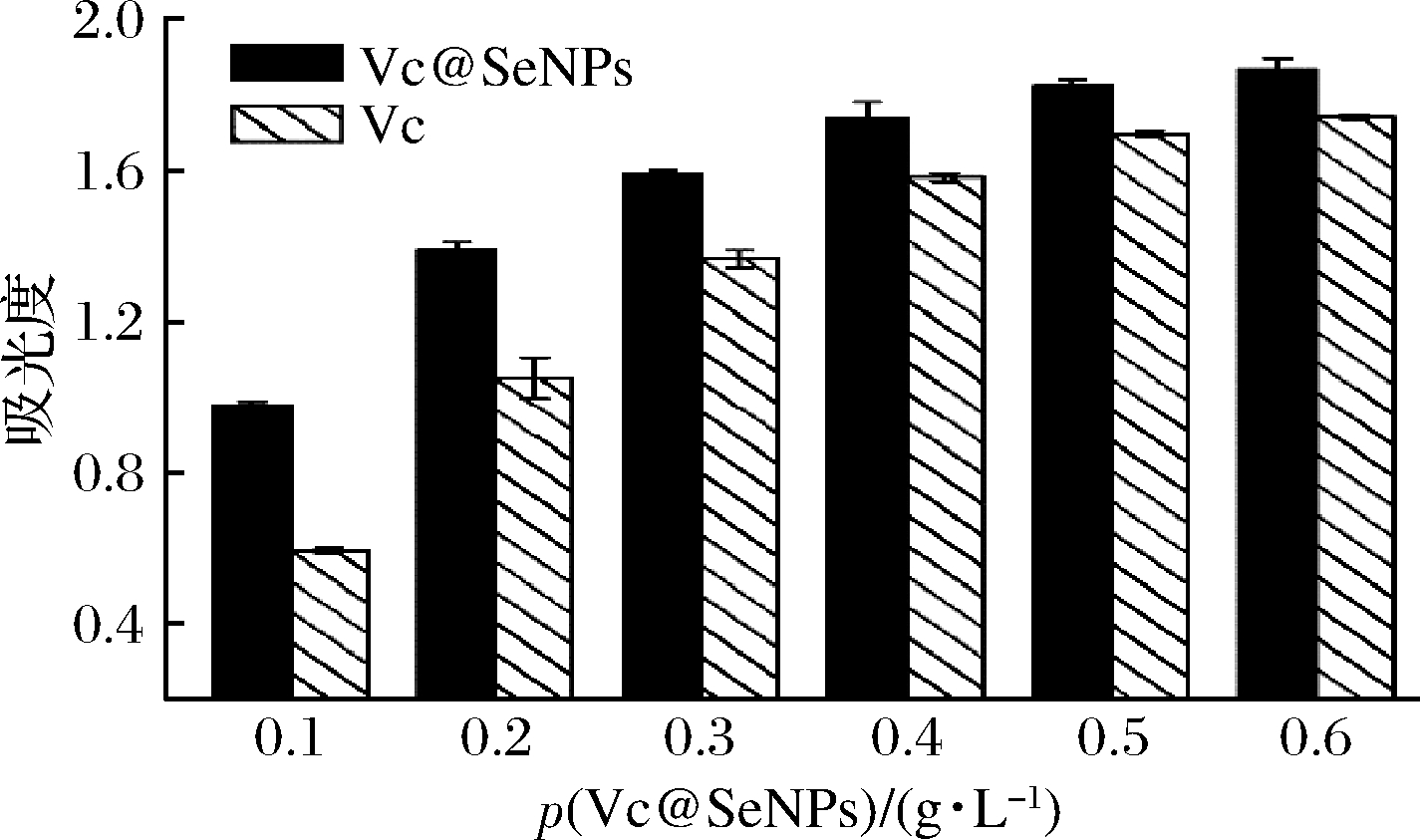
图5 Vc@SeNPs对还原力的影响
Fig.5 Effect of Vc@SeNPs on reducing power
在一定浓度范围内,Vc@SeNPs的还原能力随浓度的增大而增加,呈浓度依赖性。当样品质量浓度为0.1 g/L时,Vc@SeNPs的还原力是Vc的1.65倍,表明在低浓度时Vc@SeNPs还原力较强,当质量浓度升高至0.6 g/L时,Vc@SeNPs还原力为1.87,仍高于相同浓度下Vc的还原力,表明Vc@SeNPs具有较强的还原能力。
2.2.2 Vc@SeNPs清除·OH活性评价
·OH被认为是最活泼的氧化剂,可以与细胞中的蛋白质、核酸以及糖类等各种大分子物质作用导致细胞损伤[28]。Vc具有较强的还原能力,可以与·OH发生氧化还原反应以降低自由基对机体的危害[29]。Vc@SeNPs对·OH的清除能力如图6所示。在0.1~0.6 g/L质量浓度范围内,Vc@SeNPs对·OH的清除能力与Vc相当,IC50为0.10 g/L,且有明显的量效关系。当Vc@SeNPs质量浓度为0.6 g/L时对·OH的清除率为77.9%,是Vc的90%。由此可见,Vc@SeNPs对·OH的清除能力较强。此外,郑晓凤[30]研究发现,当SeNPs及Vc质量浓度为10 g/L时,SeNPs对·OH的清除能力与Vc相当,但在低浓度时Vc对·OH的清除能力高于SeNPs,与本文结果相似。
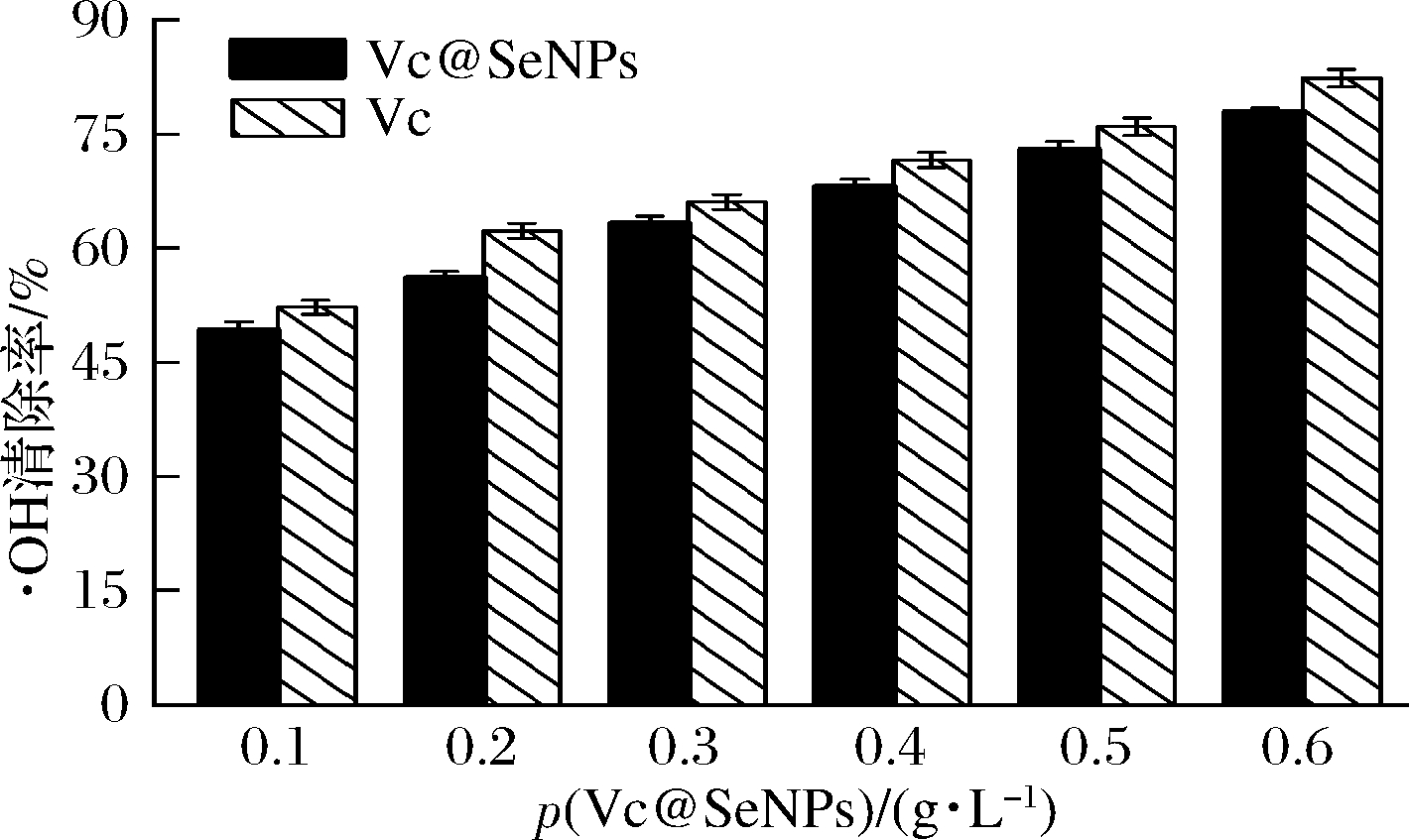
图6 Vc@SeNPs对·OH的清除率
Fig.6 Effect of Vc@SeNPs on the scavenging rate of ·OH
2.2.3 Vc@SeNPs清除![]() 活性评价
活性评价
![]() 在活性氧形成过程中起着重要作用,主要损害细胞膜及亚显微结构,并引起一系列有害的生化反应[19]。Vc@SeNPs对
在活性氧形成过程中起着重要作用,主要损害细胞膜及亚显微结构,并引起一系列有害的生化反应[19]。Vc@SeNPs对![]() 的清除能力如图7所示。在一定浓度范围内,Vc@SeNPs对
的清除能力如图7所示。在一定浓度范围内,Vc@SeNPs对![]() 的清除率呈线性增长,具有量效关系,IC50为0.25 g/L。当质量浓度≥0.5 g/L时,Vc@SeNPs对
的清除率呈线性增长,具有量效关系,IC50为0.25 g/L。当质量浓度≥0.5 g/L时,Vc@SeNPs对![]() 的清除率是Vc的97%,且趋于稳定,这与罗海英等[31]制备的纳米硒-氨基酸溶胶有类似的
的清除率是Vc的97%,且趋于稳定,这与罗海英等[31]制备的纳米硒-氨基酸溶胶有类似的![]() 清除效果。
清除效果。
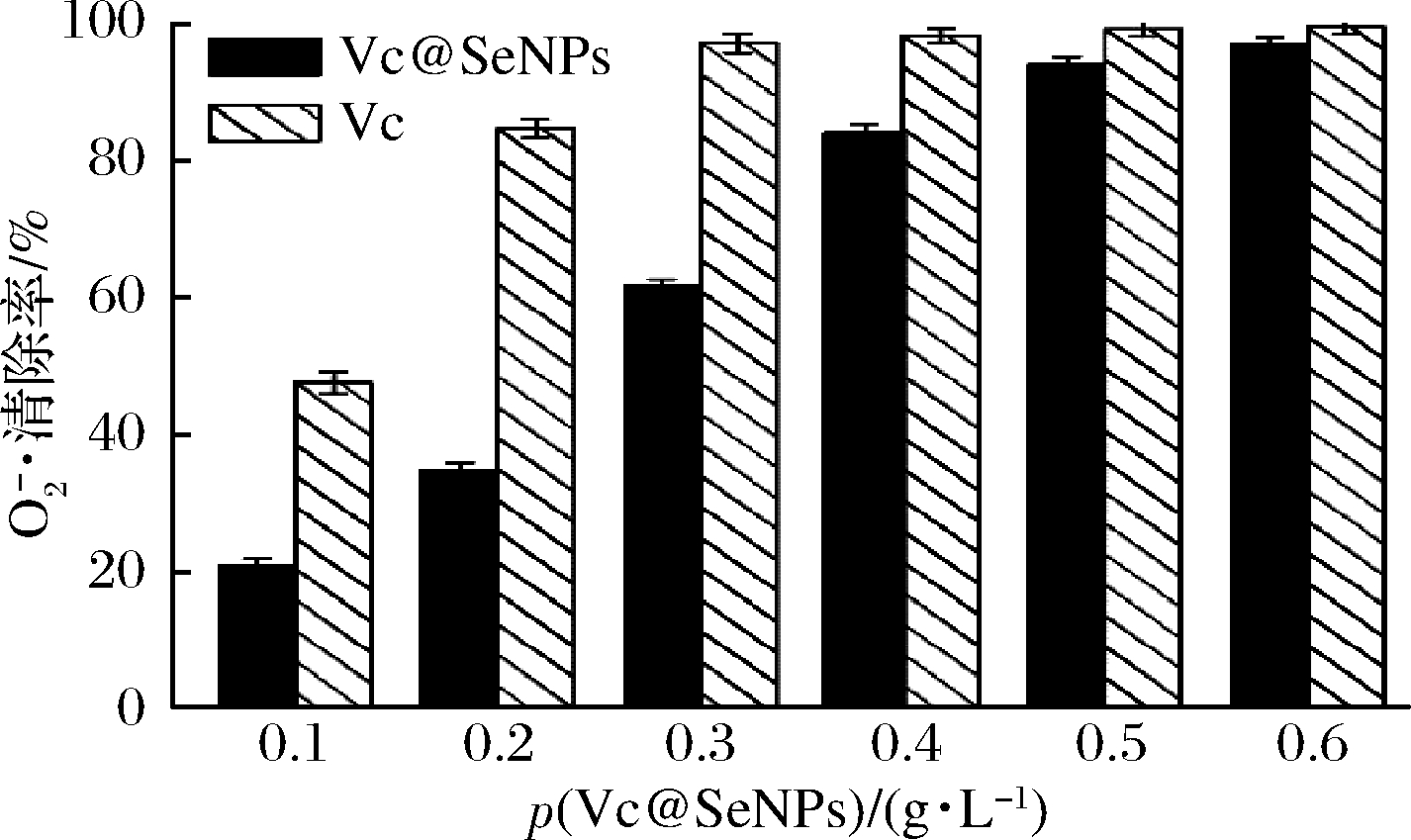
图7 Vc@SeNPs对![]() 清除率的影响
清除率的影响
Fig.7 Effect of Vc@SeNPs on the scavenging rate of ![]()
2.2.4 Vc@SeNPs清除DPPH自由基活性评价
DPPH被广泛用于评估各种抗氧化剂对自由基清除作用。在抗氧化剂存在的情况下,DPPH自由基可以接受电子或氢原子以减少自由基损伤[32]。如图8所示,Vc@SeNPs对DPPH自由基的清除能力随着浓度的增大而增加,具有明显的量效关系,IC50为0.51 g/L。当质量浓度为0.1 g/L时,Vc@SeNPs对DPPH清除率是Vc的62%,当质量浓度增高至0.4 g/L时,Vc@SeNPs对DPPH的清除率是Vc的45%,表明Vc@SeNPs在0.1~0.6 g/L范围内均能有效清除DPPH自由基。

图8 Vc@SeNPs对DPPH清除率的影响
Fig.8 Effect of Vc@SeNPs on the scavenging rate of DPPH
2.3.1 Vc@SeNPs对鲜切苹果感官品质的影响
感官品质是综合评价鲜切苹果品质的重要指标。不同浓度Vc@SeNPs或Vc溶液对鲜切苹果感官品质影响如图9所示,10、30、50 g/L Vc@SeNPs或Vc溶液处理后鲜切苹果感官评分随贮藏时间的延长而降低。10、30、50 g/L Vc@SeNPs溶液处理鲜切苹果感官评分明显优于Vc溶液处理组及蒸馏水处理组。处理2 h内,Vc@SeNPs及Vc处理组状态良好,未表现出色泽变黄,有不良气味等症状。处理4 h以后,Vc处理组均出现色泽变黄,有些部位出现棕褐色,苹果香味变淡,而10、30、50 g/L Vc@SeNPs处理组感官评分均大于60分,且未出现褐变,气味变淡等不良状态。6 h以后蒸馏水处理组苹果切面出现严重褐变,切面表层发黏,几乎无苹果香味。而Vc@SeNPs处理组感官评分虽有所下降,但组织状态,苹果香味以及色泽等均表现良好。综合比较发现, 30、50 g/L Vc@SeNPs处理均可较好的保持鲜切苹果的新鲜度,延长鲜切苹果的货架期,其中50 g/L Vc@SeNPs处理组效果最佳。
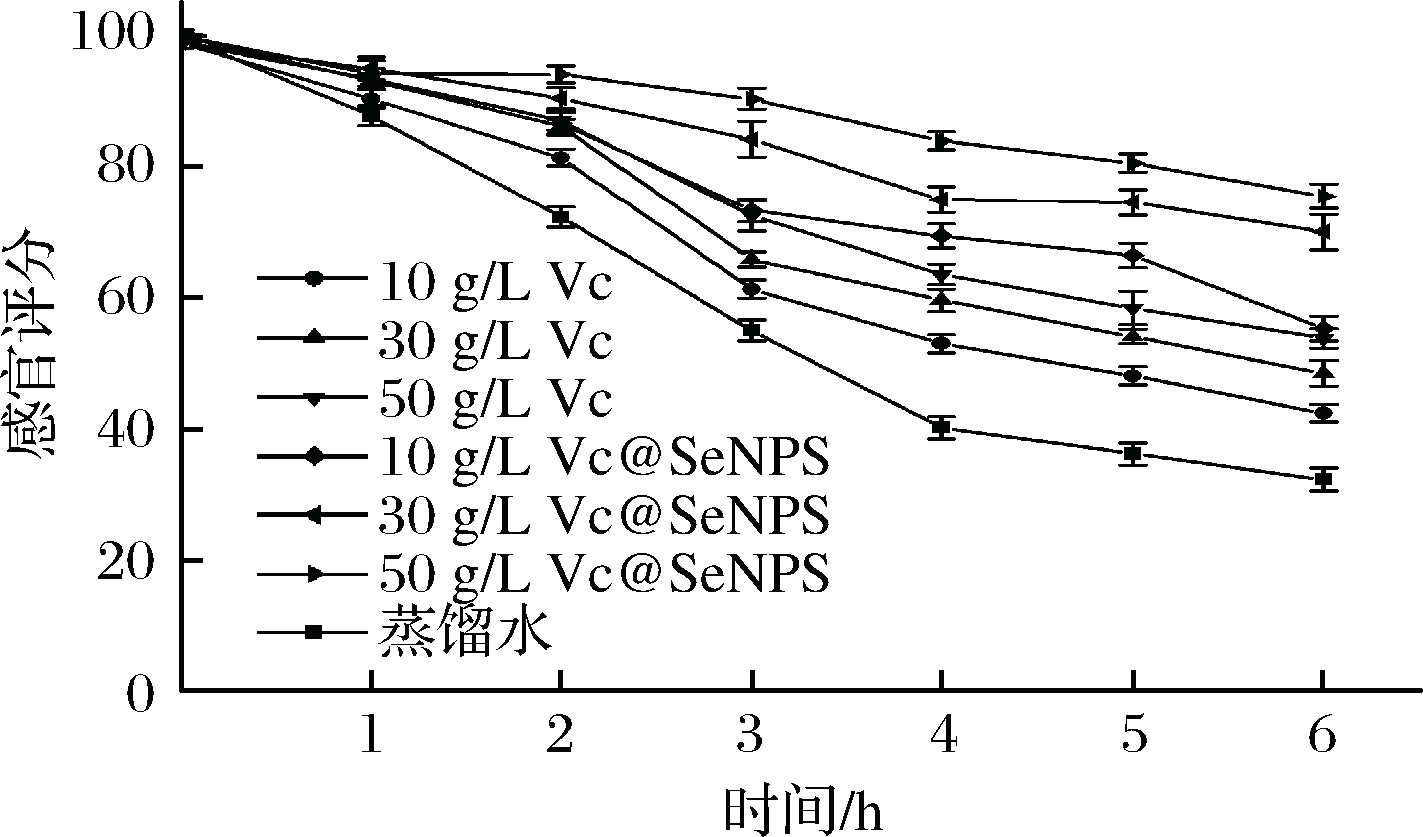
图9 不同处理对鲜切苹果感官品质的影响
Fig.9 Effects of different treatments on sensory quality of fresh-cut apples
2.3.2 Vc@SeNPs对鲜切苹果褐变的影响
色泽是消费者评估鲜切果蔬外观品质的重要指标,也从一定程度上反映了鲜切果蔬的营养价值变化。蒸馏水处理后,苹果褐变程度随储藏时间的延长而加剧。这可能是由于机械切割破坏苹果组织结构,诱导产生大量活性氧,过量的活性氧加剧膜脂质过氧化,膜渗透性增大,进而加剧酶促褐变[33-34]。对比蒸馏水,30、50 g/L Vc@SeNPs及Vc均可显著抑制鲜切苹果褐变,但两者并无明显差异,而10 g/L Vc@SeNPs及10 g/L Vc对防止鲜切苹果褐变的效果差异较大。如图10所示,处理6 h后,10 g/L Vc@SeNPs处理组鲜切苹果仅有轻微褐变,10 g/L Vc处理组鲜切苹果褐变程度加深,显著优于蒸馏水处理组。表明Vc@SeNPs能有效延缓鲜切苹果发生褐变。

图10 处理6 h时鲜切苹果的褐变情况
Fig.10 Browning of fresh-cut apples at 6 h
由于Vc@SeNPs具有较好的自由基清除效果,因此,Vc@SeNPs可能通过自身抗氧化特性清除机械损伤中产生的大量自由基,从而延缓苹果切片褐变。
2.3.3 Vc@SeNPs对鲜切苹果失重率的影响
水分是影响鲜切水果品质的重要因素,直接反映了鲜切苹果的新鲜状况[35]。鲜切苹果在加工过程中细胞受损,呼吸强度增大,蒸腾作用加剧,导致营养物质流失,果品品质下降,货架期缩短[36]。由图11可知,鲜切苹果在贮藏期间质量变化较大,说明贮藏期间鲜切苹果呼吸强度较高,水分散失较多。对比不同处理组发现,蒸馏水处理组失重率增长最快,Vc及Vc@SeNPs处理组均能有效减缓鲜切苹果水分散失,其中50 g/L Vc@SeNPs处理组对鲜切苹果的水分维持明显优于蒸馏水及50 g/L Vc处理组(P<0.05)。这是由于Vc@SeNPs有效降低了鲜切苹果面水膜的透过率,阻断了水蒸气散失[37]。表明Vc@SeNPs可以减缓苹果质量的下降速度,较好地保持苹果的水分。
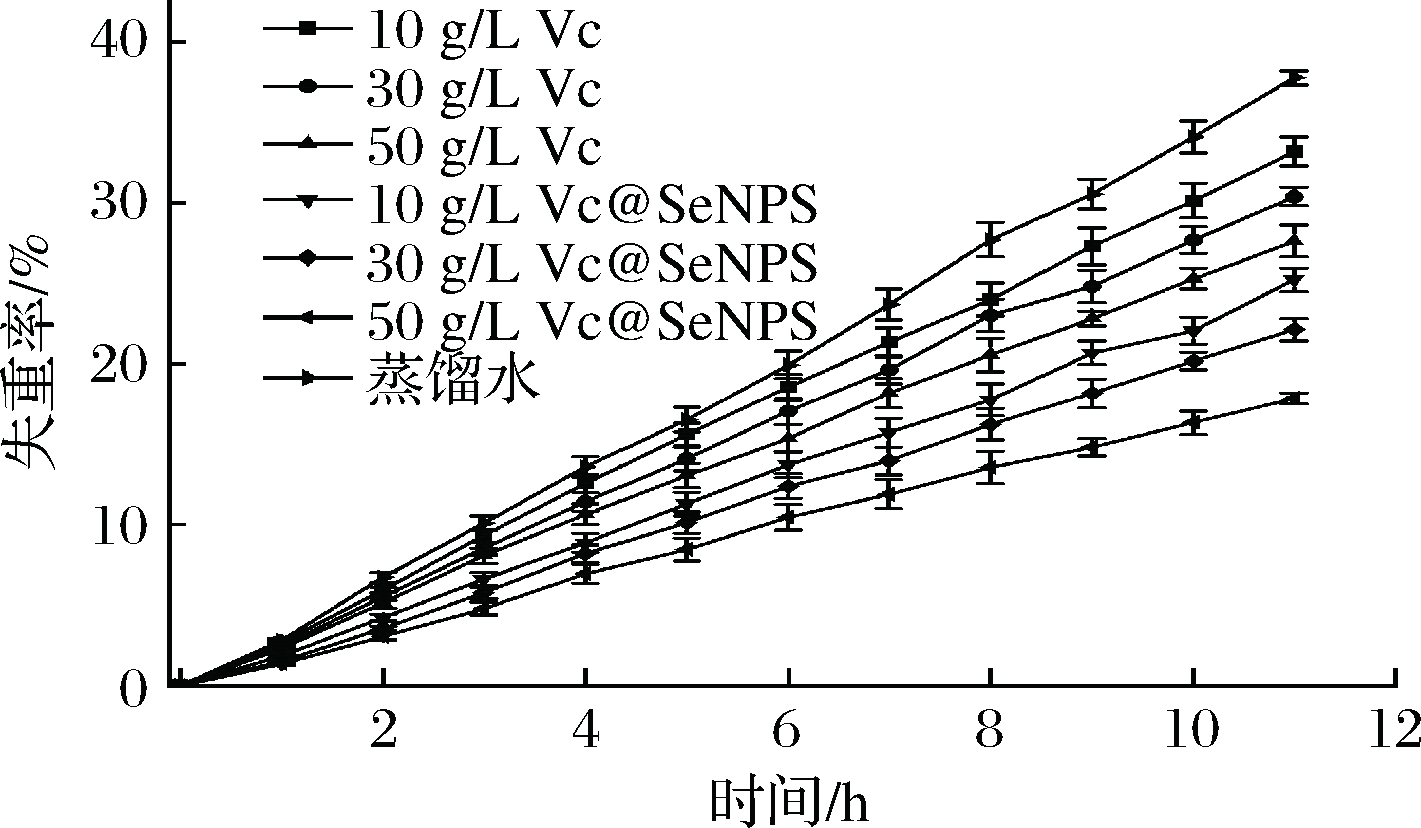
图11 不同处理对鲜切苹果失重率的影响
Fig.11 Effect of different treatments on the weight loss rate of fresh-cut apples
2.3.4 Vc@SeNPs对鲜切苹果水分平均散失率影响
鲜切苹果的水分平均散失率如图12所示,所有处理组均在贮藏前1 h内急剧升高,1~3 h内各组平均散失率均有所延缓,之后平缓下降。这表明苹果切片在贮藏前3 h内水分散失较快,应在此阶段做好保鲜措施。
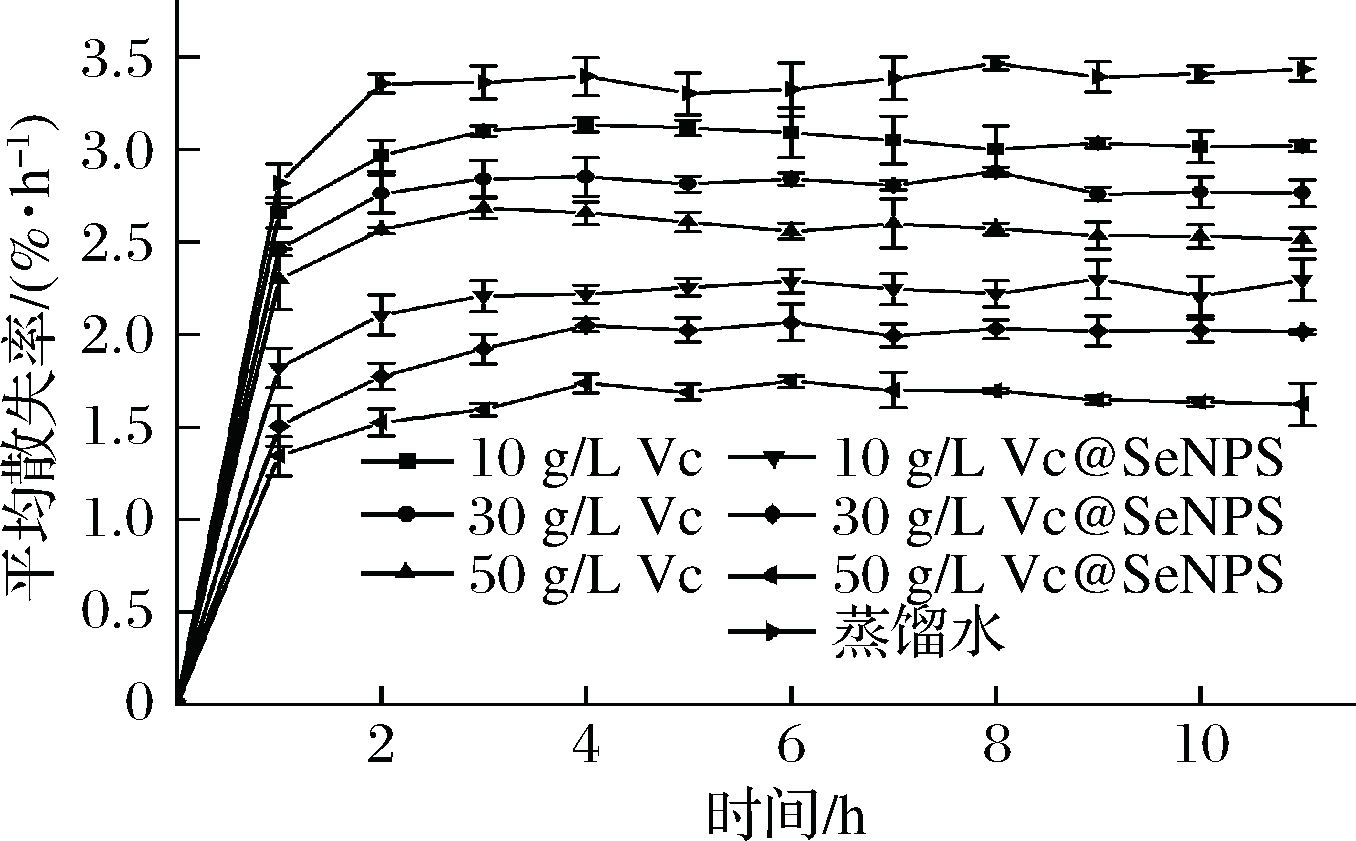
图12 不同处理对鲜切苹果水分平均散失率的影响
Fig.12 Effect of different treatments on the average loss rate of fresh-cut apples
对比不同处理组发现,不同浓度Vc处理组平均散失率存在差异,其中,50 g/L Vc处理组优于10 g/L Vc处理,这与杨巍等[38]的研究一致。对比不同浓度Vc和Vc@SeNPs处理组发现,Vc@SeNPs处理明显优于蒸馏水和Vc处理组,其中50 g/L Vc@SeNPs处理水分平均散失率最低,是50 g/L Vc处理的58%(P<0.05)。这表明50 g/L Vc@SeNPs处理鲜切苹果能有效防止水分散失。
2.3.5 Vc@SeNPs对鲜切苹果总酚含量的影响
苹果多酚是苹果生长过程中产生的次生代谢产物,是苹果及其加工产品重要的呈味物质及显色物质。如图13所示,贮藏期间不同处理鲜切苹果总酚含量均呈下降趋势。贮藏0 h,鲜切苹果总酚含量为1 410 mg/kg,贮藏7 h,鲜切苹果总酚含量为634.65~1 134.00 mg/kg,与LI等[4]和CHEN等[37]研究一致。对比不同浓度Vc及Vc@SeNPs处理组发现,不同处理组存在差异,10、30、50 g/L Vc@SeNPs处理组总酚含量均高于Vc及蒸馏水处理组,其中50 g/L Vc@SeNPs处理组总酚含量仅下降19.5%,是蒸馏水处理组的1.79倍, 是50 g/L Vc处理组的1.42倍,这可能是由于Vc及Vc@SeNPs均属于抗氧化性物质,当Vc及Vc@SeNPs含量较高时不仅抑制了鲜切苹果多酚氧化,而且促进酚类物质生成,因而Vc@SeNPs可有效延缓鲜切苹果多酚氧化[38]。
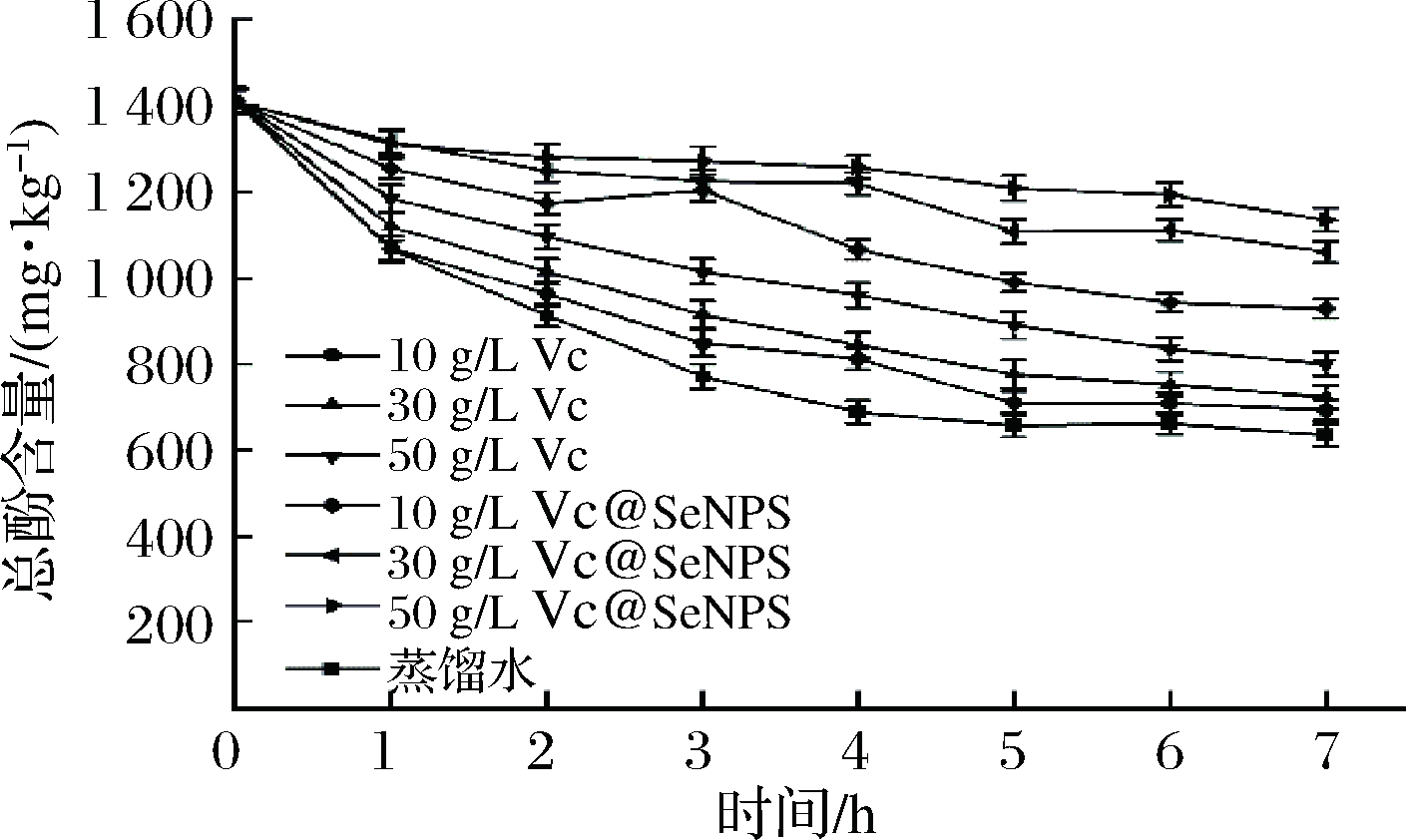
图13 不同处理对鲜切苹果总酚含量的影响
Fig.13 Effect of different treatments on total phenolic content of fresh-cut apples
目前SeNPs或SeNPs修饰物在果蔬保鲜方面的研究鲜有报道,本文以Vc为还原剂成功制备了分散均匀,平均粒径为64.80 nm的球形Vc@SeNPs。通过还原力,![]() 和DPPH自由基指标表明Vc@SeNPs在0.1~0.6 mg/mL浓度范围内均具有量效关系,且清除率随浓度的增大呈上升趋势,能有效清除自由基。在鲜切苹果保鲜方面,Vc@SeNPs处理鲜切苹果后能有效防止鲜切苹果发生褐变,较好地保持水分,延缓苹果质量的损失和鲜切苹果多酚氧化。此外,Vc和Se均为无污染食品添加剂,因此Vc@SeNPs作为果蔬保鲜剂,即可膳食补硒,又能起到保鲜作用,有望成为理想的鲜切苹果保鲜剂。
和DPPH自由基指标表明Vc@SeNPs在0.1~0.6 mg/mL浓度范围内均具有量效关系,且清除率随浓度的增大呈上升趋势,能有效清除自由基。在鲜切苹果保鲜方面,Vc@SeNPs处理鲜切苹果后能有效防止鲜切苹果发生褐变,较好地保持水分,延缓苹果质量的损失和鲜切苹果多酚氧化。此外,Vc和Se均为无污染食品添加剂,因此Vc@SeNPs作为果蔬保鲜剂,即可膳食补硒,又能起到保鲜作用,有望成为理想的鲜切苹果保鲜剂。
[1] 郭倩.浓缩苹果汁的褐变因素及控制措施[J].食品安全导刊,2016(6):72.
[2] OLAIMAT A,HOLLEY R.Factors influencing the microbial safety of fresh-produce: a review[J].Food Microbiol,2012,32(1):1-19.
[3] 陈春,黎家妍,黄泽鹏,等.氧化白藜芦醇对鲜切苹果及果汁褐变的影响[J].食品工业科技,2019,40(20):285-289;295.
[4] LI W, LI L,CAO Y,et al.Effects of PLA film incorporated with ZnO nanoparticle on the quality attributes of fresh-cut apple[J]. Nanomaterials (Basel), 2017,7(8):207-227.
[5] MORERIRA MR,CASSAN I,CMARTIN-BELLOSO O, et al.Effects of polysaccharide-based edible coatings enriched with dietary fiber on quality attributes of fresh-cut apples[J]. J Food Sci Technol,2015,52(12):7 795-7 805.
[6] 李文瀚,刘紫韫,李喜宏,等.不同包装方式对鲜切秦冠苹果贮藏品质的影响[J].食品研究与开发,2019,40(15):97-101.
[7] CORTELLINO G, GOBBI S, BIANCHI G, et al.Modified atmosphere packaging for shelf life extension of fresh-cut apples [J].Food Science & Technology, 2015,11(88):177-183.
[8] 曹文娟,张媛媛,崔金香.鲜切果蔬保鲜技术研究[J].农业装备技术,2009,35(5):13-15.
[9] OMS O G, ROJAS G M A, ALANDES G L,et al.Recent approaches using chemical treatments to preserve quality of fresh-cut fruit: A review[J]. Postharvest Biology and TechnoLogy,2010,57(3):139-148.
[10] CHRISTIAN L,DOLORS U,YOLANDA S,et al.Oxidative behavior of fresh-cut ‘Fuji’ apples treated with stabilising substances[J]. Journal of the Science of Food &Agriculture, 2010,88(10):1 770-1 776.
[11] MISHRA B, HASSAN P A, PRIUADARSINI K, et al. Reactions of biological oxidants with selenourea: Formation of redox active nanoselenium[J]. J Phys Chem B,2005,109(26):12 718-12 723.
[12] ZHAI X,ZHANG C,ZHAO G,et al.Antioxidant capacities of the selenium nanoparticles stabilized by chitosan[J]. J Nanobiotechnology,2017,15(1):4-19.
[13] SHOEIBI S,MOZDZAK PGOLKAR,NARENJI A. Biogenesis of selenium nanoparticles using green chemistry[J].Top Curr Chem,2017,375(88):1-22.
[14] FAIRWEATHER T,BAO Y,BROADLEY M R,et al.Selenium in human health and disease[J].Antioxid. Redox Sign,2011,14(7):1 337-1 383.
[15] LANCTOT CM,CRESSWELL T, CALLAGHAN PD,et al.Bioaccumulation and biodistribution of selenium in metamorphosing tadpoles[J].Environ Sci Technol,2017,51(10):5 764-5 773
[16] ZHANG J,WANG X,XU T.Elemental selenium at nano size (Nano-Se) as a potential chemo preventive agent with reduced risk of selenium toxicity: comparison with se-methylselenocysteine in mice[J].Toxicol Sci,2008,101(1):22-31.
[17] JIA X W, LIU Q, ZOU S W, et al.Construction of selenium nanoparticles/-glucan composites for enhancement of the antitumor activity[J].Carbohydrate Polymers, 2015,117:434-442.
[18] OYAIZU M.Studies on products of browning reaction: antioxidative activities of products of browning reaction prepared from glucosamine[J].Nutr,1986,44:307-315.
[19] MARKLUND S.Involvement of the superoxide anion radical in the autoxidation of pyrogallol and a convenient assay for superoxide dismutase[J].Eur J Biochem, 1974, 47(3):469-474.
[20] LI Q,YU N,WANG Y,et al.Extraction optimization of Bruguiera gymnorrhiza polysaccharides with radical scavenging activities[J].Carbohydrate Polymers,2013,96(1):148-155.
[21] MA L,ZHAO Y, YU J, et al. Characterization of Se-enriched Pleurotus ostreatus polysaccharides and their antioxidant effects in vitro[J].Int J Biol Macromol,2018(111):421-429.
[22] 管磬馨,胡文忠,李婉莹,等.毛茶茶多酚提取工艺优化及其对鲜切苹果品质的影响[J].食品工业科技,2019,40(23):124-129.
[23] 韩菊,魏福祥.Folin-Ciocalteu比色法测定苹果渣中的多酚[J].食品科学,2010,31(4):179-182.
[24] 王娜,褚路路,徐梦,等.没食子酸修饰纳米硒的制备表征及其抑菌活性研究[J].食品科技,2019,44(1):302-307.
[25] 杨志恒,武伟,刘泽华,等.纳米TiO2/β-CDP复合物的制备及表征[J].天津科技大学学报,2018,33(2):38-42.
[26] 冯笑颜,武玉洁,周冠霖,等.抗坏血酸红外及变温红外光谱研究[J].煤炭与化工,2019,42(8):146-150.
[27] BAI K K,HONG B H,HONG Z,et al.Selenium nanoparticles-loaded chitosan/citrate complex and its protection against oxidative stress in D-galactose-induced aging mice[J]. J Nanobiotechnol,2017,15:92-106.
[28] 杨少辉,宋英今,王洁华,等.雪莲果体外抗氧化和自由基清除能力[J].食品科学,2010,31(17):166-169.
[29] 郝婧玮,索莲宦,杨斯棋,等.橘皮与橙皮精油抑菌、抗氧化、抗肿瘤活性研究[J].中医药学报,2019,47(4):37-41.
[30] 郑晓凤. 桔梗多糖软模板法制备纳米硒及其活性研究[D].佳木斯:佳木斯大学,2017.
[31] 罗海英,周艳晖,白燕,等.纳米硒-氨基酸溶胶的抗氧化作用[J].食品科技,2011,36(4):202-206;210.
[32] SHIMARMURA T,SUMIKURA Y,YAMZAKI T,et al.Applicability of the DPPH assay for evaluating the antioxidant capacity of food additives-inter-Laboratory evaluation study[J].AnaL Sci,2014,30(7):717-721.
[33] DEG E,GUIDI L,PARDOSSI A,et al.Biochemical study of leaf browning in minimally processed leaves of lettuce (Lactuca satival. var.acephala[J].Agric Food Chem,2005,N53(26): 9 980-9 984.
[34] ZHANG J S,WANG H L,BAO Y L,et al.Nano red elemental selenium has no size effect in the induction of selenoenzymes in both cultured cells and mice[J].Life Science,2004,75(2):237-244.
[35] 管玉格,胡文忠,姜爱丽,等.阔叶凤尾蕨提取工艺优化及对鲜切苹果保鲜的影响[J].食品与发酵工业,2018,44(12):166-173.
[36] 宋欣纯,管磬馨,陈晨,等.鲜切苹果褐变机理及物理保鲜技术研究进展[J].现代园艺,2019(3):7-8.
[37] CHEN H,HU X,CHEN E,et al. Preparation characterization, and properties of chitosan films with cinnamaldehyde nanoemulsions[J].Food Hydrocoll,2016,6(1):662-671.
[38] 杨巍,刘晶,吕春晶,等.氯化钙和抗坏血酸处理对鲜切苹果品质和褐变的影响[J].中国农业科学,2010,43(16):3 402-3 410.