慈姑(Sagittaria sagittifolia L.),又称茨菰、慈菰,泽泻科水生慈姑属,盛产于北美、欧洲和亚洲,尤其常见于中国、印度尼西亚、马来西亚及尼泊尔等地[1]。慈姑为低脂肪、高碳水化合物的食品,干燥的慈姑球茎主要含有约54.60%的淀粉及16.47%的蛋白质[2]。新鲜慈姑含水量较大且淀粉含量较高,不易长期储存。在中国,因为其独特口感和营养,慈姑多被当作应季蔬菜进行食用。对慈姑淀粉进行研究成为慈姑资源应用的重要途径。淀粉的理化性质会影响其在食品和非食品工业中的应用。慈姑淀粉的直链淀粉、支链淀粉含量约为27%和73%,其糊化温度范围较小、不易溶解、易凝沉、冻融稳定性差,但透明度较高[3-4]。对淀粉进行改性后应用于工业生产是常见的淀粉利用方式[5]。
利用化学方法对淀粉进行改性是最经典和最有效的方法,常见方法有氧化、交联、醚化、羟丙基化和乙酰化改性等[6-7]。氧化和交联反应可通过将功能单元引入淀粉分子,从而改变淀粉热力学性质和糊化性能[8]。氧化淀粉近年来广泛应用于食品和工业应用中,例如提供膜产品和黏合特性产品[9]。目前还没有关于慈姑氧化淀粉制备的研究,本研究旨在利用过氧化氢(H2O2)将慈姑淀粉进行氧化处理,探讨氧化前后淀粉性质的变化,从而提高慈姑淀粉的综合利用性能。
1 材料和方法
1.1 材料与设备
慈姑淀粉,弥勒市竹园镇蔗林食品厂;H2O2(30%)、HCl、NaOH、CuSO4、NaHSO3,均为分析纯,成都市科龙化工试剂。
DZKW-S-8 恒温水浴锅,北京市永光明医疗仪器有限公司;STARTER 3100 pH计,奥豪斯仪器有限公司;DF-101S 集热式恒温加热磁力搅拌器,巩义市予-华仪器有限责任公司;UV8100紫外分光光度计,北京莱伯泰科仪器有限公司;101 电热鼓风干燥器、分析天平,常州衡正电子仪器有限公司;HD场发射扫描电子显微镜,德国SIGMA;Nicolet is 50 傅立叶变换红外光谱仪,美国赛默飞;Rigaku smartlab9 X-衍射仪,日本理学。
1.2 试验方法
1.2.1 氧化慈姑淀粉的制备
称取40 g慈姑淀粉,加入去离子水配成质量分数40% 的淀粉乳悬浮液[10],加入CuSO4,调节pH,搅拌均匀后,在45 ℃下与H2O2反应。反应结束后,加入质量分数10% NaHSO3溶液以终止反应。用 1 mol/L NaOH调节溶液 pH 值至中性,然后抽滤、洗涤,将反应后淀粉放置于45 ℃烘箱内,干燥,研磨制得氧化慈姑淀粉。
1.2.2 H2O2氧化淀粉工艺单因素试验
基础反应条件为CuSO4取干基0.02(相对于干基淀粉的质量,g/g,下同),调节pH至7.0,加入16 mL H2O2,反应4 h。分别考察不同H2O2(8、16、24、32、40 mL)用量、不同CuSO4取干基(0、0.01%、0.02%、0.03%、0.04%)用量、不同pH(3.0、5.0、7.0、9.0、11.0)及不同反应时间(2、3、4、5、6 h)对氧化慈姑淀粉的羧基含量及透明度的影响。
1.2.3 羧基含量的测定
羧基含量的测定参照GB/T 20374—2006《变性淀粉 氧化淀粉羧基含量的测定》,总的羧基质量分数,以%计算。
1.2.4 透明度的测定
参考WU等[11]的测定方式略作调整,用去离子水配制质量分数1%的慈姑淀粉乳,于沸水浴中回流加热至糊化20 min后停止,冷却至室温,以去离子水为空白,在 620 nm 波长下测定透光率,透光率与透明度成正比。
1.2.5 溶解度和膨胀度测定
参考王素雅等[12]的实验方法略作调整,分别在55、65、75、85、95 ℃温度下进行水浴加热处理,测定淀粉在设定温度的溶解度和膨胀度。
1.2.6 凝沉性的测定
参考李鑫等[13]的实验方法略作调整,称取慈姑淀粉及氧化淀粉0.5 g(以干基计),加入蒸馏水50 mL,配制成质量分数为1%的慈姑淀粉悬浮液,置于沸水浴中不断搅拌使其充分糊化后冷却至室温,倒入刻度量筒中静置沉淀,保鲜膜封口,观察淀粉糊上层清液体积,以上清液体积分数随时间的变化情况来表征其凝沉性质。
1.2.7 冻融稳定性的测定
准确称取一定质量的氧化慈姑淀粉及原淀粉,加入一定量蒸馏水配制成质量浓度为60 g/L的淀粉悬浮液(以干基计),在沸水浴中加热至充分糊化,称取15 g冷却后的样品装入离心管中,盖紧盖子后置于冰箱(-18 ℃)冷冻20 h后将样品取出[14],在室温下解冻,在3 000 r/min条件下离心30 min,弃去上清液后称取沉淀物的质量。如此反复冻融3次并测定每次的析水率。
1.2.8 淀粉黏度测定
参考GB/T 22427.7—2008《淀粉黏度测定》,使温度控制在50、55、60、65、70、75、80、85、90 ℃,用旋转黏度仪测量每个温度的黏度值。
1.2.9 电镜分析
将2种淀粉进行真空冷冻干燥后,样品进行研碎,然后均匀分散于双面胶上并固定在铜台上,喷金后扫描电镜观察。
1.2.10 红外光谱分析
采用KBr压片法处理后进行红外光谱仪测定。
1.2.11 X射线衍射分析
使用X射线衍射仪测定氧化前后慈姑淀粉的X射线衍射图,测试条件:淀粉过300目筛,利用Cu-Kα辐射,波长为1.540 56 nm,衍射扫描范围为5~40°,管压为40 kV,电流为150 mA,扫描速度为2 °/min。
1.3 数据统计分析
实验数据采用Excel、Origin及Jade进行处理。
2 结果与分析
2.1 单因素实验
2.1.1 H2O2用量对氧化淀粉性质的影响
可以用羧基含量来衡量氧化淀粉的氧化程度,羧基含量越高,氧化程度就越深。氧化淀粉的淀粉糊透明度与老化度有相关性,易老化者透明度较差,淀粉的透明度与淀粉的溶解度也有关。在CuSO4添加量为0.02%,pH为7.0,反应时间为4 h的条件下H2O2添加量对氧化淀粉羧基含量及透光率影响如图1所示,羧基含量与透明度受H2O2添加量影响的趋势相似。通过氧化作用,慈姑淀粉中部分还原性的链端被氧化成羧基[15],增加氧化剂用量,氧化剂与淀粉的接触越频繁,反应程度越深。由图1可知,当氧化剂添加量逐渐增加,羧基含量及透明度明显增加,氧化程度增大,羧基含量及透明度在H2O2添加量为32 mL时达到最大,此时H2O2与慈姑淀粉结合趋于饱和。
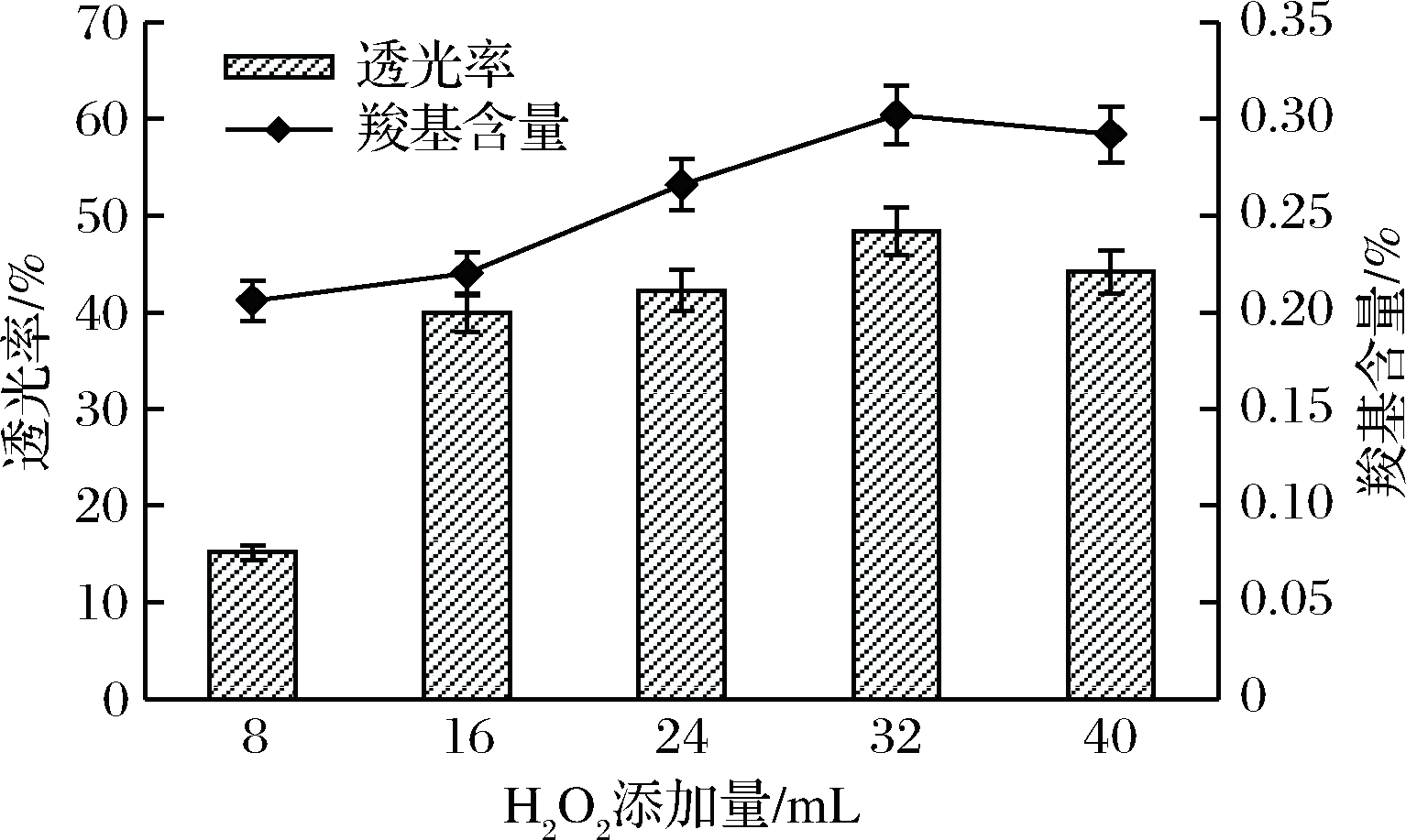
图1 H2O2添加量对氧化淀粉性质的影响
Fig.1 Effect of H2O2 content on properties of oxidized starch
2.1.2 催化剂CuSO4对氧化淀粉的影响
在H2O2添加量为16 mL,pH为7.0,反应时间为4 h的条件下,CuSO4添加量对氧化淀粉羧基含量及透明度的影响如图2所示。催化剂的使用可以明显改变慈姑淀粉的氧化程度,在未添加CuSO4的情况下,H2O2与慈姑淀粉的反应缓慢,与加工前原料相比,羧基含量的增加不明显。随着CuSO4的加入,H2O2对慈姑淀粉的氧化效果明显提升,反应逐渐剧烈,慈姑淀粉的羧基含量及透明度明显增加。在CuSO4添加量为淀粉干基的0.03%时,达到相对较好的透光率及羧基含量。持续增加催化剂,羧基含量反而略微减少,可能是随着 Cu2+浓度的增加,淀粉与 Cu2+发生配位反应的几率增大,使得可用于氧化反应的慈姑淀粉量减少。
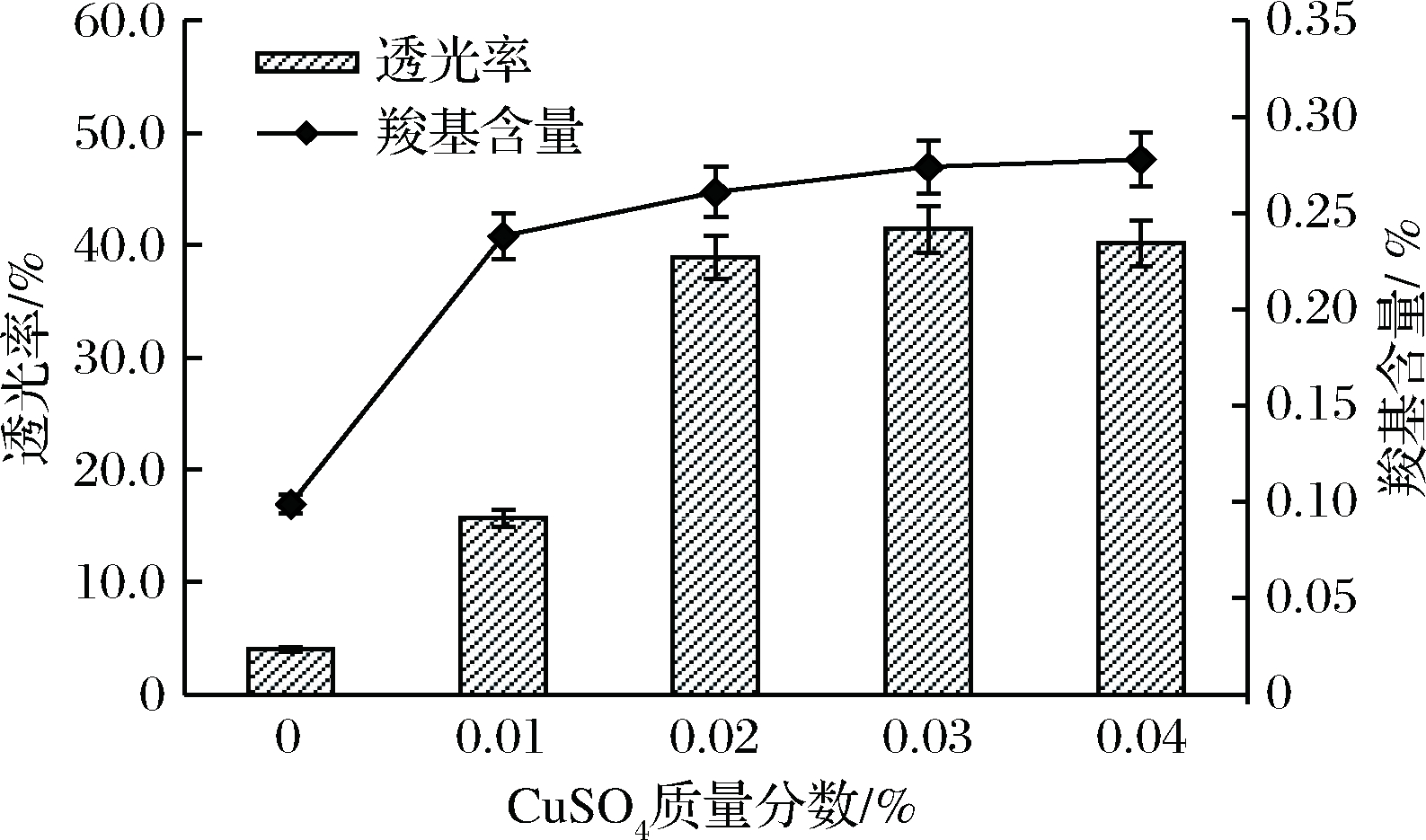
图2 CuSO4质量分数对氧化淀粉性质的影响
Fig.2 Effect of CuSO4 content on properties of oxidized starch
2.1.3 pH值对氧化淀粉的影响
不同pH值条件下慈姑氧化淀粉的羧基含量及透光率结果见图3。整体而言,以CuSO4作催化剂条件下,中性或碱性环境更有利于H2O2对慈姑淀粉进行氧化作用,氧化效果明显较酸性条件更好。就淀粉透明度而言,中性条件相对要优于酸性或碱性条件。淀粉与H2O2在CuSO4存在下多发生自由基反应[16],虽然酸性条件下H2O2的氧化能力增强,但同时淀粉分子间的氢键作用也加强,不利于自由基反应中链的传递。碱性增强,不利于淀粉氢键的形成,但随着OH-浓度增大,会使得催化剂中的Cu2+转化为Cu(OH)2沉淀,整体催化能力下降,不利于氧化反应的发生。因此为获得氧化程度较高且透明度较好的氧化慈姑淀粉,控制反应在中性或偏弱碱性范围。

图3 pH值对氧化淀粉性质的影响
Fig.3 Effect of pH on properties of oxidized starch
2.1.4 氧化时间对氧化淀粉的影响
反应时间对H2O2氧化慈姑淀粉的影响结果见图4。

图4 反应时间对氧化淀粉性质的影响
Fig.4 Effect of reaction time on properties of oxidized starch
随着反应时间的增加,H2O2在较短时间内表现出较为稳定的氧化性,氧化后慈姑淀粉的羧基含量先增加,随着时间的推移,部分H2O2发生降解同时淀粉分子中易发生局部反应,致羧基含量减少。慈姑淀粉的透明度随着时间的增加先增大后减小,在5 h时达到最大值,继续反应,透明度反而降低,且4 h的反应效果略优于6 h。与已有研究结果基本一致[15],反应时间较短时部分淀粉来不及参加反应,随着反应时间的增加反应进一步加深,部分H2O2氧化分解而失去氧化性,且淀粉分子内部发生局部反应,导致淀粉分子高度降解。综合考虑羧基含量及透明度的结果,故下一步试验设计中固定氧化反应的时间为4 h。
2.2 响应面优化试验结果
2.2.1 响应面试验设计及回归模型的建立与分析
根据淀粉氧化的单因素试验结果,固定反应时间为4 h,选取介质 pH(A)、CuSO4添加量(B)及H2O2添加量(C) 3 个因素为响应面的试验因素,氧化淀粉羧基含量、透明度为响应值响应面试验设计见表1,试验结果见表2。
表1 响应面试验因素与水平
Table 1 Factors and levels of response surface test
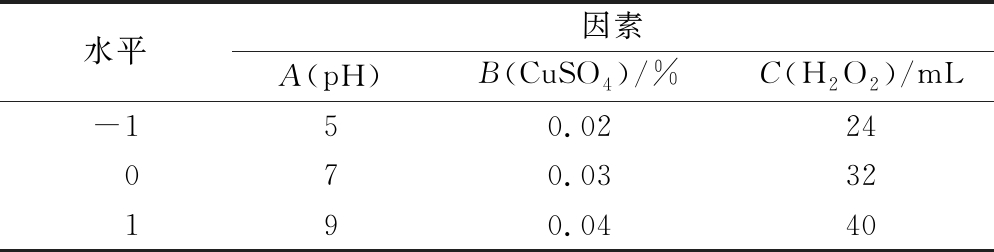
水平因素A(pH)B(CuSO4)/%C(H2O2)/mL-150.0224070.0332190.0440
表2 Box-Behnken试验设计及结果
Table 2 Box-Behnken test design and results

实验号pHCuSO4/%H2O2/mL羧基含量/%透光率/%170.03320.337±0.01249.4±3.4290.03400.332±0.01240.3±2.0350.02320.259±0.00133.0±1.9470.02240.287±0.00431.1±4.3550.04320.252±0.01226.0±0.7690.04320.356±0.00449.9±3.4770.02400.317±0.00235.0±3.1890.02320.280±0.00938.6±1.5970.03320.346±0.00745.4±5.11070.03320.339±0.00953.4±3.61170.04240.335±0.00948.4±2.61270.03320.318±0.01652.7±2.41370.04400.340±0.00944.1±1.21470.03320.327±0.01751.7±1.11550.03400.263±0.00330.2±0.21650.03240.251±0.00733.7±1.41790.03240.328±0.01552.2±1.6
采用Design-Expert 8.0.6软件对表2的响应面结果进行多元回归拟合、方差分析及显著性检验,分别得到羧基含量(Y1)及表征透明度的透光率(Y2)与3个因素的二次多项回归方程为:Y1=0.33+0.034A+0.018B+0.006C+0.021AB-0.002AC-0.006BC-0.036A2-0.010B2-0.003C2;Y2=0.51+0.073A+0.038B-0.020C+0.046AB-0.021AC-0.020BC-0.071A2-0.065B2-0.043C2。对羧基含量模型进行方差分析结果见表3,对透光率模型进行方差分析结果见表4。
表4 透光率模型的显著性检验
Table 4 Significance test of transmittance model
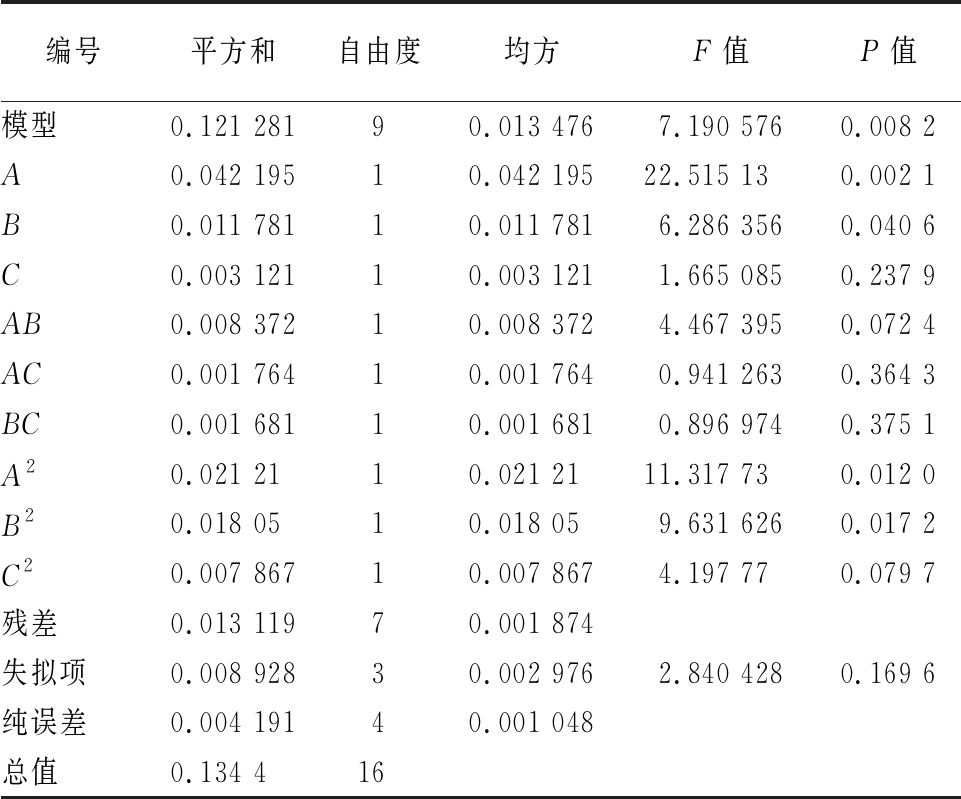
编号平方和自由度均方F值P值模型0.121 28190.013 4767.190 5760.008 2A0.042 19510.042 19522.515 130.002 1B0.011 78110.011 7816.286 3560.040 6C0.003 12110.003 1211.665 0850.237 9AB0.008 37210.008 3724.467 3950.072 4AC0.001 76410.001 7640.941 2630.364 3BC0.001 68110.001 6810.896 9740.375 1A20.021 2110.021 2111.317 730.012 0B20.018 0510.018 059.631 6260.017 2C20.007 86710.007 8674.197 770.079 7残差0.013 11970.001 874失拟项0.008 92830.002 9762.840 4280.169 6纯误差0.004 19140.001 048总值0.134 416
表3 羧基含量模型的显著性检验
Table 3 Significance test of carboxyl content model
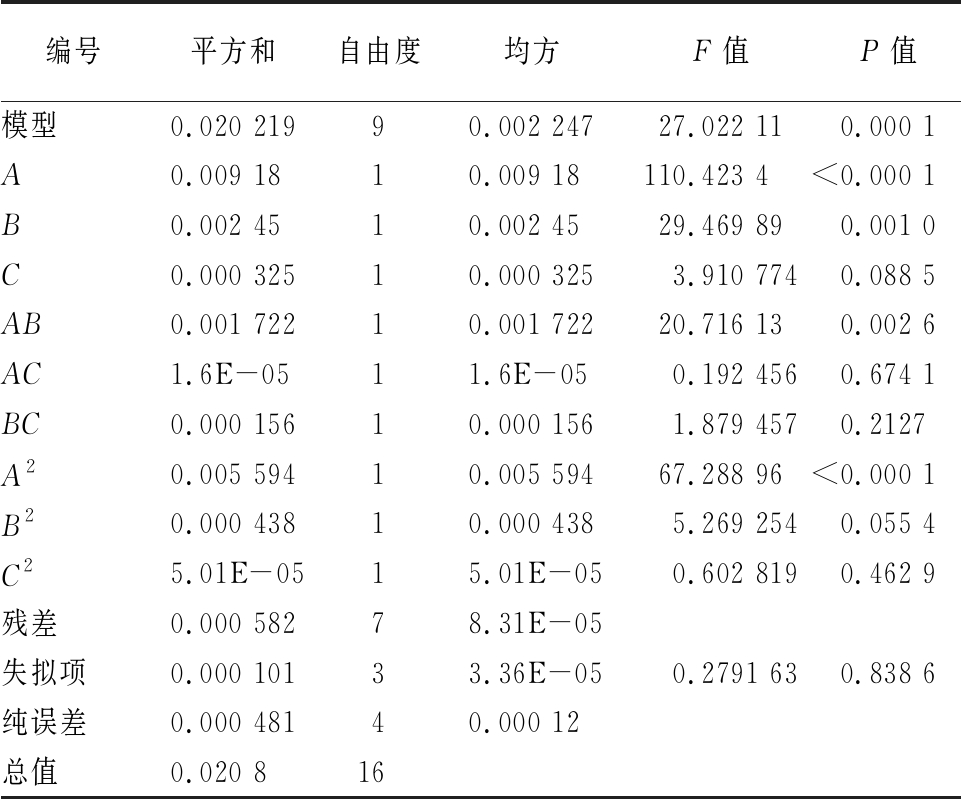
注:P<0.000 1为极显著性差异,P<0.05为显著性差异(下同)
编号平方和自由度均方F值P值模型0.020 21990.002 24727.022 110.000 1A0.009 1810.009 18110.423 4<0.000 1B0.002 4510.002 4529.469 890.001 0C0.000 32510.000 3253.910 7740.088 5AB0.001 72210.001 72220.716 130.002 6AC1.6E-0511.6E-050.192 4560.674 1BC0.000 15610.000 1561.879 4570.2127A20.005 59410.005 59467.288 96<0.000 1B20.000 43810.000 4385.269 2540.055 4C25.01E-0515.01E-050.602 8190.462 9残差0.000 58278.31E-05失拟项0.000 10133.36E-050.2791 630.838 6纯误差0.000 48140.000 12总值0.020 816
由表3可看出,氧化慈姑淀粉羧基含量的多元回归拟合中P=0.000 1,表明此回归模型准确度高、合理性强。失拟项P=0.838 6,说明模型失拟项不显著,因此可用此回归方程代替试验点对实验结果进行分析和预测。对羧基含量的影响大小依次为:A>B>C。
由表4可看出,氧化慈姑淀粉透明度的多元回归拟合中P=0.008 2,表明此回归模型准确度较高。失拟项P=0.169 6>0.05,说明模型失拟项不显著,因此可用此回归方程代替试验点对实验结果进行分析和预测。模型项A、B对透明度的影响均显著,影响大小依次为:A>B>C。
2.2.2 响应面交互作用
在表2的基础上得出各因素交互作用对羧基含量影响的响应曲面图见图5,对透明度影响的响应曲面图见图6。

a-pH和CuSO4的交互作用;b-pH和H2O2的交互作用;c-CuSO4和H2O2的交互作用(下同)
图5 各因素交互作用对羧基含量影响的响应面分析
Fig.5 Response surface analysis of the influence of interaction of various factors on carboxyl content

图6 各因素交互作用对淀粉透明度影响的响应面分析
Fig.6 Response surface analysis of the effect of interaction of various factors on starch transparency
固定CuSO4添加量,变性淀粉羧基含量随pH增加先上升后下降,固定反应pH,变性淀粉羧基含量及透明度随CuSO4添加先上升后下降,两者交互作用显著,见图5-a和图6-a。固定H2O2添加量,变性淀粉羧基含量及透明度随pH增加先上升后下降,固定反应pH,变性淀粉羧基含量及透明度随H2O2添加缓慢上升后下降,但两者交互的等高线图均接近圆形,交互作用不显著(图5-b、图6-b)。固定H2O2添加量,变性淀粉羧基含量及透明度随pH增加先上升后下降,固定反应pH,变性淀粉羧基含量及透明度随H2O2添加先上升后下降,两者交互作用等高线图接近圆形(图5-c、图6-c),说明两者交互作用不显著。结合方差分析结果,可以看出所选H2O2体积范围均已满足化学计量上氧化剂的用量要求,此时起主要作用的是催化剂的添加量以及提供反应环境介质的pH,方差分析结果及响应面曲线与反应实际相符。
用响应面优化法测定出最佳优化工艺,即H2O2用量31.6 mL,反应pH为8.35,CuSO4用量取干基的0.04%,45 ℃条件下反应4 h。所选取的慈姑淀粉的羧基含量为0.049%,透明度为2.98%;而优化后所制得氧化慈姑淀粉的羧基含量为0.355%,透明度为52.6%,相对于单因素实验(羧基含量为0.302%,透明度为48.4%)有一定程度的提高。
2.3 氧化前后慈姑淀粉的性质对比
2.3.1 溶解度和膨胀度测定结果
从图7~图8可知,H2O2氧化慈姑淀粉在最初温度下溶解度和膨润度与原淀粉差异不大,但随着温度的升高差异变大,当温度升高到65 ℃,氧化慈姑淀粉的溶解度显著升高,远大于慈姑原淀粉的溶解度。随着温度的升高,氧化淀粉的膨润度逐渐高于原慈姑淀粉。
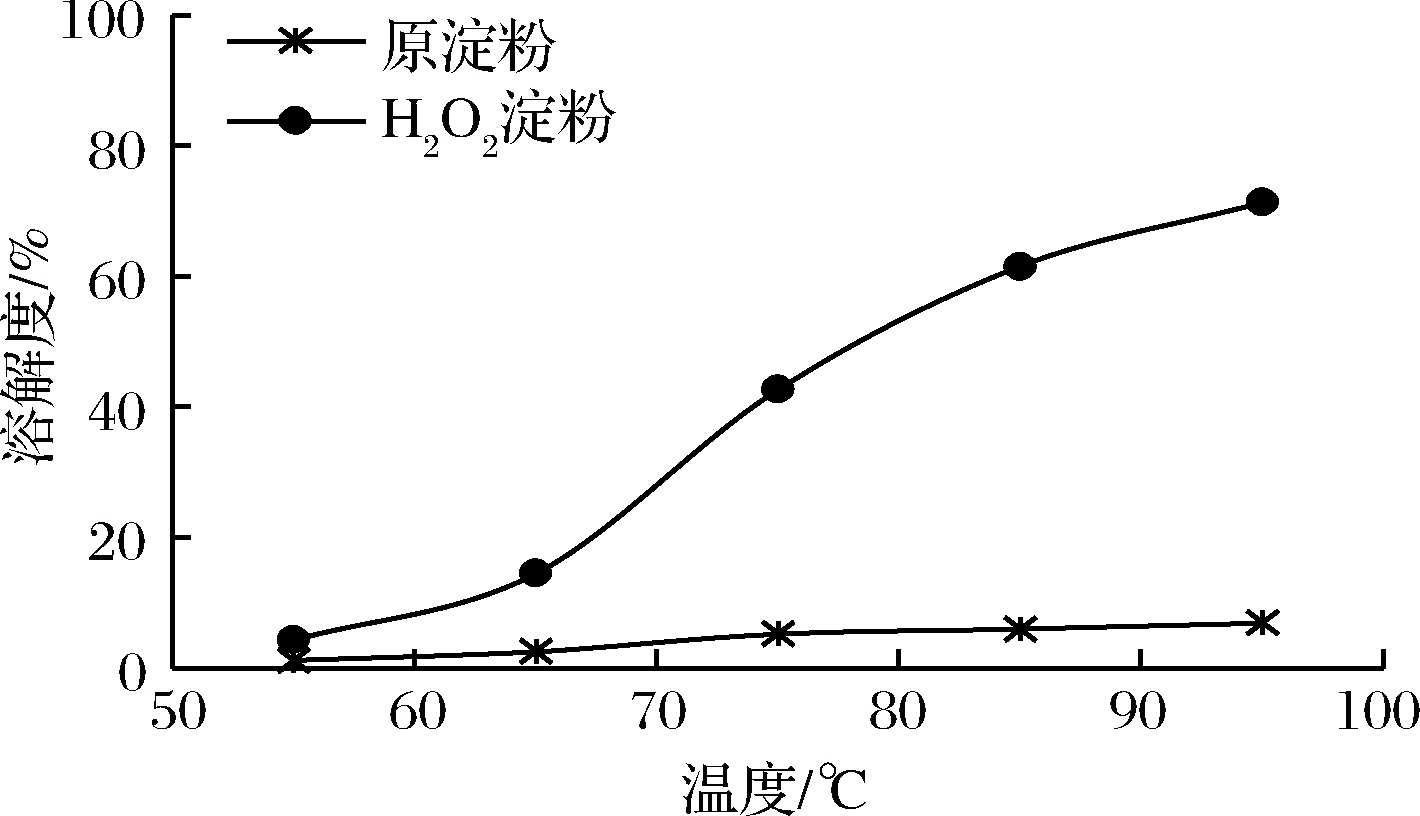
图7 H2O2氧化反应对慈姑淀粉溶解度的影响
Fig.7 Effect of H2O2 oxidation on the solubility of arrowhead starch

图8 H2O2氧化反应对慈姑淀粉膨润度的影响
Fig.8 Effect of H2O2 oxidation on swelling degree of arrowhead starch
已有文献报道[4],慈姑淀粉相对于荸荠、马铃薯、玉米及木薯等几种常见的淀粉,溶解度明显偏低,而利用H2O2/CuSO4对慈姑淀粉进行氧化改性,能明显提高其溶解度。
2.3.2 凝沉性测定结果
氧化前后慈姑淀粉凝沉性的对比结果见图9,测定实验中,上清液体积以透明液体体积计。原慈姑淀粉在3 h后就开始出现明显析水分层现象,在10 h时慈姑淀粉糊析出减少且后期基本无变化,说明对所选慈姑淀粉糊的凝沉特性的影响主要发生在前10 h。H2O2氧化的淀粉在观察时间内均表现出良好的稳定性且优于原慈姑淀粉。凝沉性的现象与溶解度的结论保持一致。
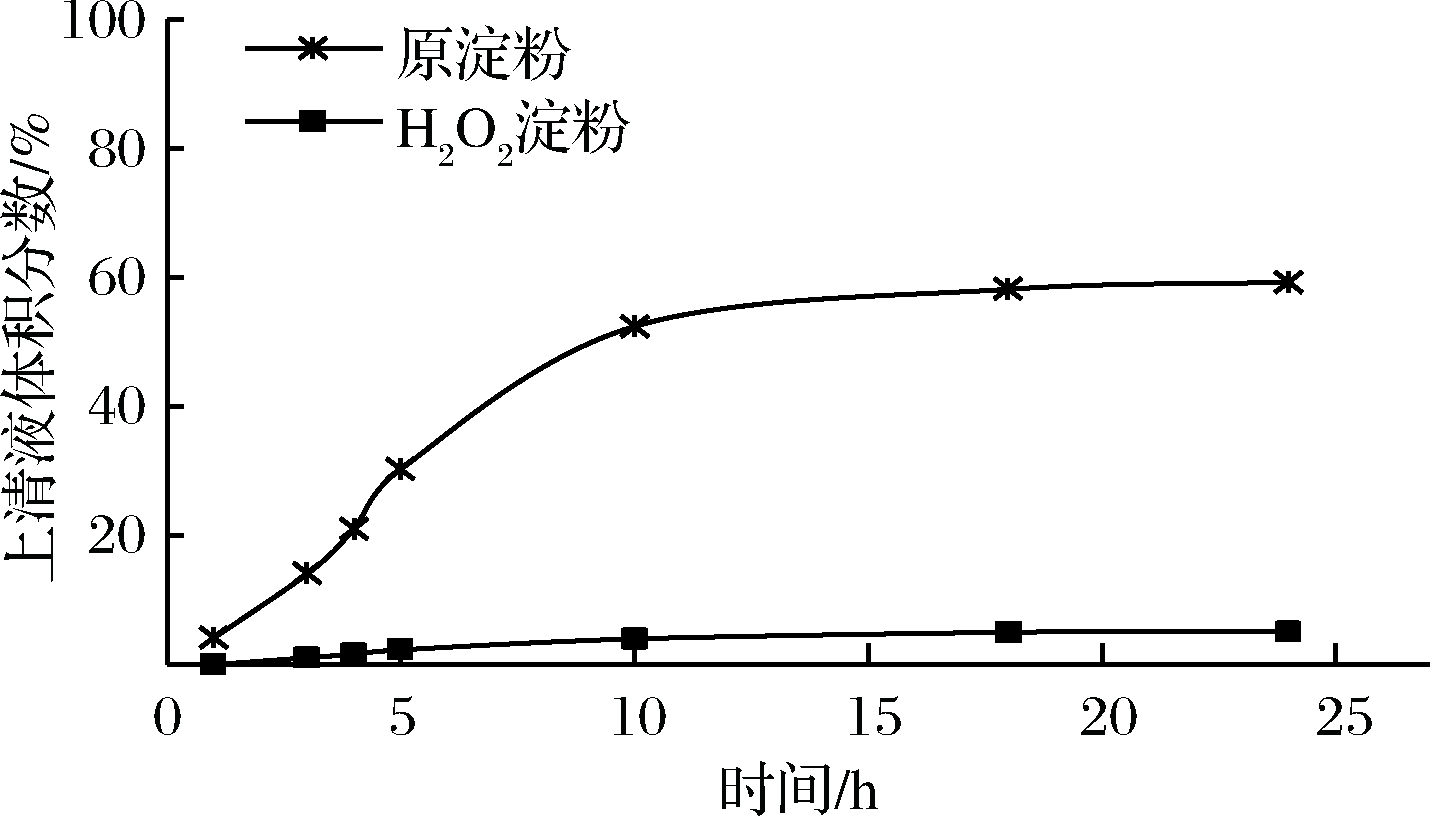
图9 H2O2氧化反应对慈姑淀粉凝沉性的影响
Fig.9 Effect of H2O2 oxidation on the retrogradation of arrowhead starch
可以推测氧化后淀粉空间结构可能发生了变化,导致可溶性淀粉量增加,也可能是支链淀粉的结构受到破坏,溶解性发生变化导致,具体原因及更长时间范围的凝沉性特性有待进一步研究。
2.3.3 冻融稳定性测定结果
冻融稳定性指糊化后的淀粉在经过冷冻和解冻后保持原来淀粉糊胶体结构的性质。冻融后淀粉糊的析水率越低表明淀粉糊的冻融稳定性越好,从图10中可以看出, 所选慈姑淀粉的第2、3、4次冻融析水率差值较小,而氧化后淀粉析水率高于慈姑淀粉,且每次冻融与前一次差异较明显。H2O2氧化的慈姑淀粉冻融实验中表现出较差的冻融稳定性。

图10 H2O2氧化反应对慈姑淀粉冻融稳定性的影响
Fig.10 Effect of H2O2 oxidation on the freeze-thaw stability of arrowhead starch
2.3.4 黏度测定结果
淀粉的黏度指淀粉在水溶液中抗流动性的性质,从图11可以看出,氧化淀粉的黏度低于原淀粉的黏度,淀粉的糊化温度变低。慈姑淀粉经过H2O2/CuSO4氧化后,羧基含量增加,相较于原淀粉,对直链淀粉分子间氢键缔合的抑制作用增强[17],糊化温度降低,淀粉分子链断裂,聚合度降低,溶解度增大,黏度也随即减小。
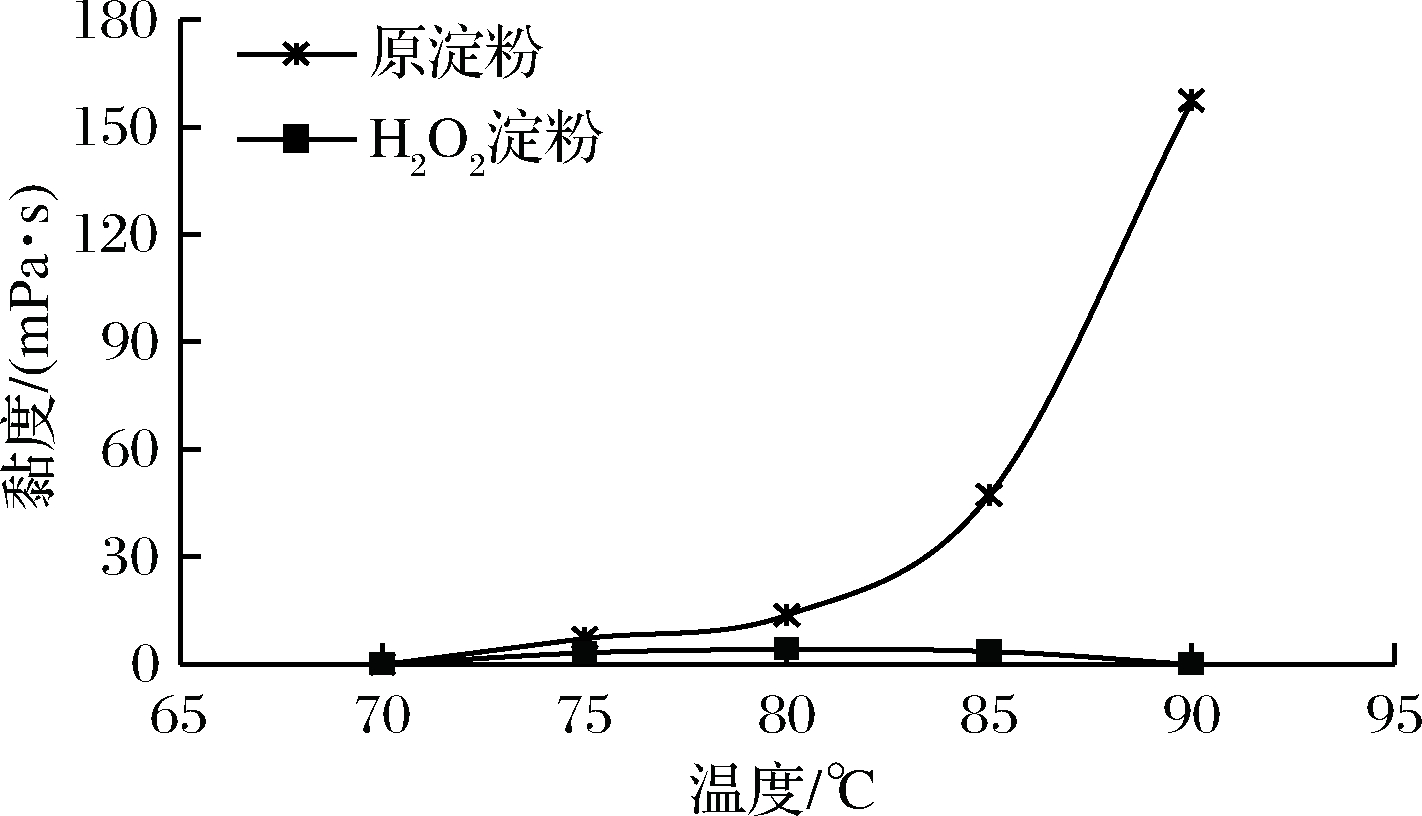
图11 H2O2氧化反应对慈姑淀粉黏度的影响
Fig.11 Effect of H2O2 oxidation on the viscosity of arrowhead starch
2.3.5 扫描电镜测定结果
由图12可知,对比H2O2/CuSO4氧化前后慈姑淀粉的扫描电镜图,从颗粒的破碎情况和光滑程度可以看出,原淀粉的颗粒饱满,表面光滑,没有明显的破碎,经过改性的慈姑淀粉,颗粒破碎严重,呈现不同规则的形状并且表面出不同程度的粗糙情况。从淀粉颗粒的形状和大小比较:慈姑淀粉主要呈椭圆形和球形,经过H2O2/CuSO4氧化的慈姑淀粉,形状增多,说明H2O2/CuSO4氧化条件使得慈姑淀粉颗粒形态发生改变。

a-氧化前(×500);b-氧化前(×1 000);c-氧化后(×500);d-氧化后(×1 000)
图12 淀粉的颗粒电镜结果图
Fig.12 Results of starch granule electron microscope
2.3.6 红外光谱分析
图13为改性前与H2O2/CuSO4改性后的慈姑淀粉的红外光谱图对比,在3 200~2 400cm-1范围内,羧基二聚体强氢键使O—H伸缩振动变成弥散的宽谱带,改性慈姑淀粉的分子中和分子间的O—H基团形成的氢键作用力强,O—H伸缩振动向低频移动,吸收谱比原淀粉更加弥散。谱带弥散的原因可能是,淀粉分子在不断的运动中,氢键O—H…O中的距离在不断变化,且H…O之间的距离越短,氢键力越强,O—H键的键长就越长,因而O—H伸缩振动的频率也就越低,H…O之间的距离在一定范围内,变化的范围越大,谱带就越弥散[18]。在1 760~1 660 cm-1的范围内,H2O2改性淀粉在这个吸收峰更尖且更强,表明分子结构中有更多的羰基振动[19]。常用1 047 cm-1与1 022 cm-1两处的吸光度的比值来反映淀粉链的有序化程度和相对结晶度[20],氧化慈姑淀粉在1 047、1 022 cm-1处吸光度比值增大,说明有序度提高,淀粉中晶体结构发生改变,无定形结构减少,同时结晶淀粉的量也减少。
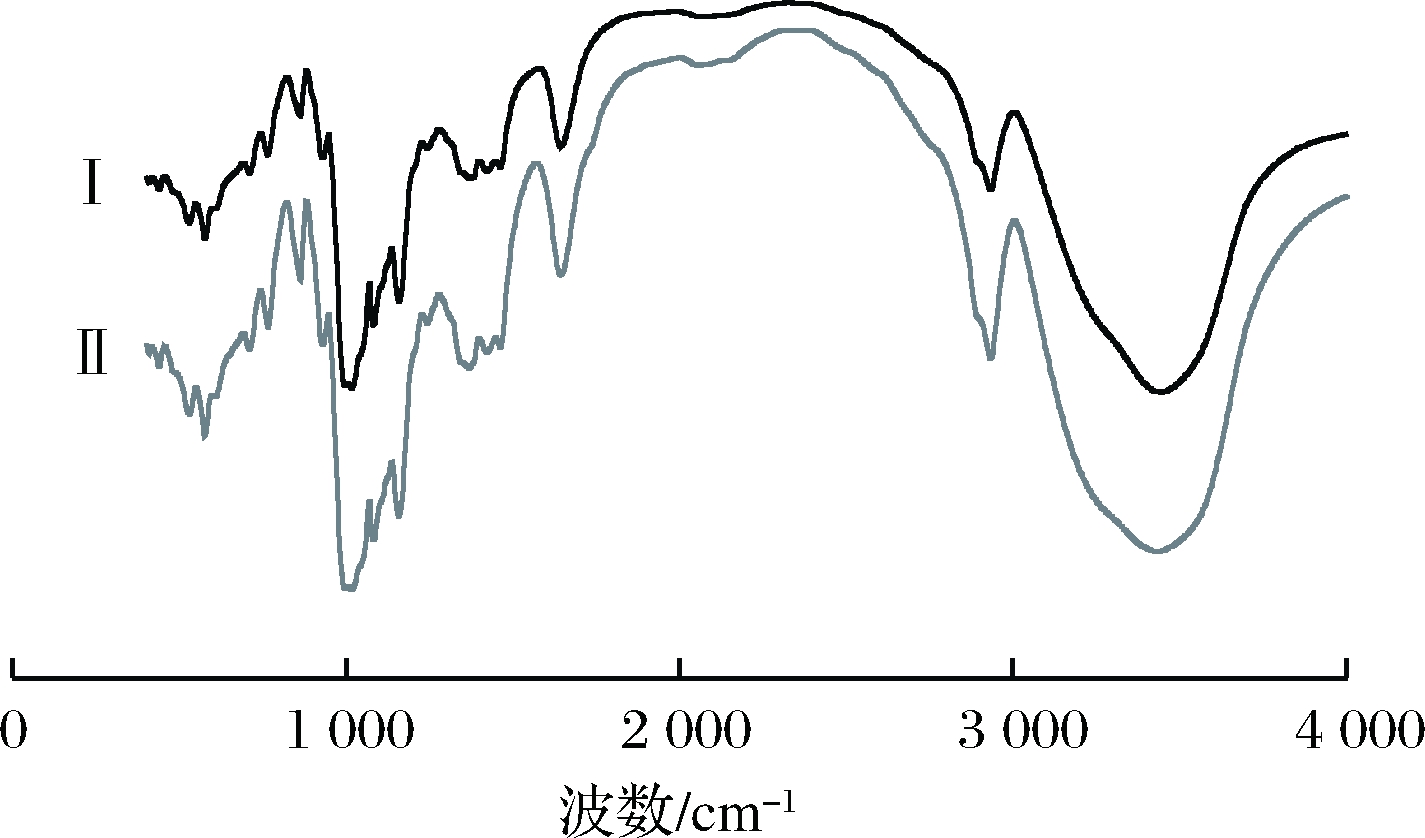
图13 氧化对慈姑淀粉红外结果的影响
Fig.13 Effect of oxidation on the infrared results of arrowhead starch
注:Ⅰ为慈姑淀粉;Ⅱ为H2O2/CuSO4改性后的慈姑淀粉(下同)
2.3.7 X-衍射结果
根据X-衍射结果,慈姑原淀粉在15.16°、17.10°、17.92°和22.99°处出现了明显的吸收峰,属于典型的A型射线衍射谱图,从图14可知,经过H2O2/CuSO4改性的慈姑淀粉的衍射峰变高但位置与氧化前基本一致,说明是部分结晶结构发生改变[21]。原淀粉的结晶度为44.8%,经H2O2/CuSO4改性的慈姑淀粉结晶度升高至55.11%,说明氧化改性破坏了原淀粉颗粒的晶体结构,主要原因是淀粉的结晶度基于支链淀粉分子链中双螺旋的形成[22]。X-衍射的测定结果与红外测试的结果一致。
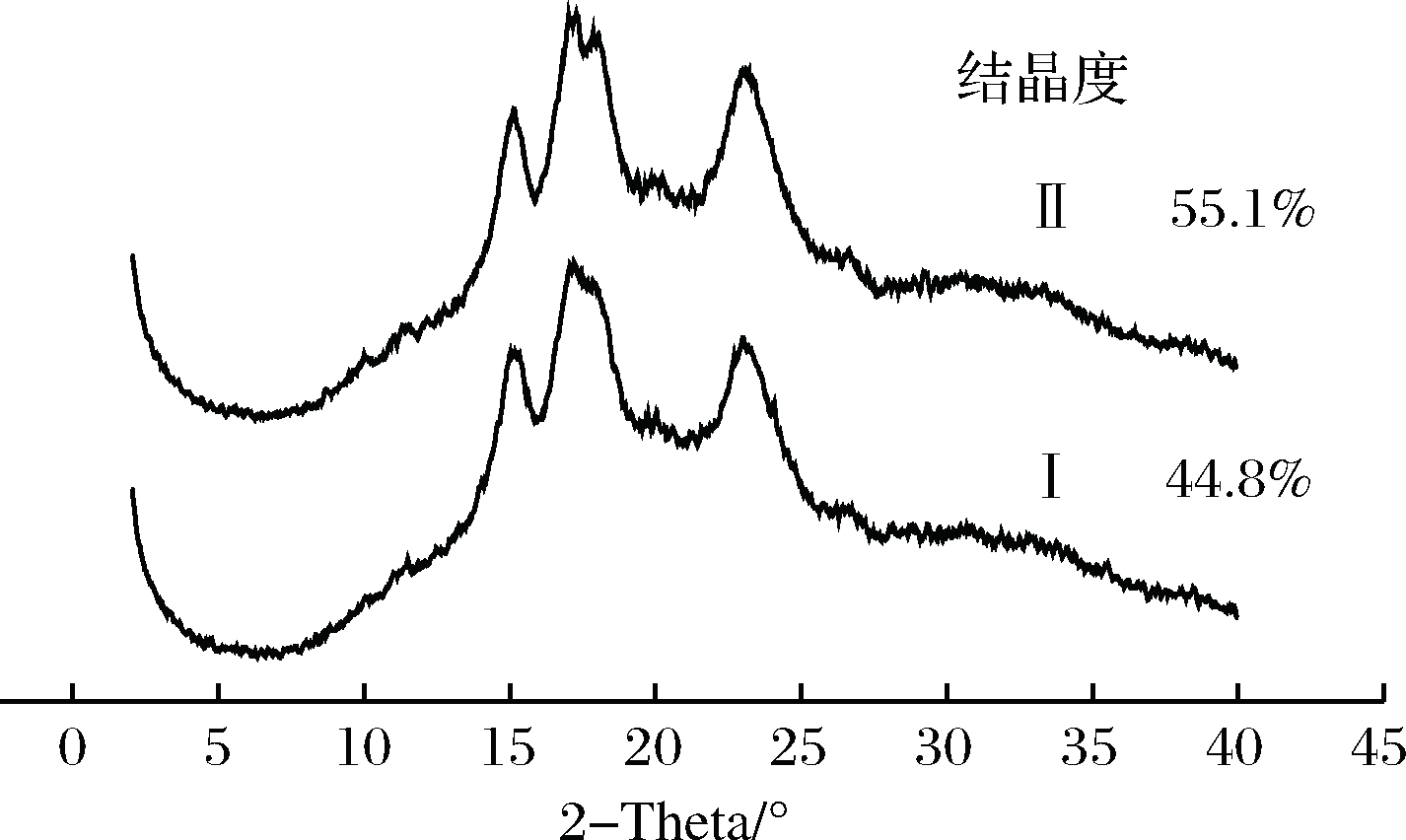
图14 氧化对慈姑淀粉X-衍射结果的影响
Fig.14 Effect of oxidation on X-diffraction results of arrowhead starch
3 结论
优化得到慈姑变性淀粉条件,即H2O2体积31.6 mL,反应pH为8.35,CuSO4用量取干基的0.04%,45 ℃条件下反应4 h,经过氧化后,慈姑淀粉的羧基含量由0.049%提升为0.355%,透明度由3.0%提升到52.6%,得到高羧基含量、高透明度的慈姑淀粉,红外光谱中的对应吸收峰型明显尖且强,羰基振动增强,氧化后淀粉的溶解度、透明度均比原慈姑淀粉高,拥有较好的凝沉性能、较低的黏度,但其冻融稳定性变差,微观颗粒破损严重,形状增多。结合红外及X-衍射测定结果显示,慈姑淀粉的结晶度从44.80%升高至55.11%,晶体结构发生了一定的改变。此方法反应条件温和,对环境友好,且与原慈姑淀粉相比,增加了淀粉的部分性能,扩展了慈姑淀粉的利用可能性。
[1] WANI A A, WANI I A, HUSSAIN P R, et al. Physicochemical properties of native and γ-irradiated wild arrowhead (Sagittaria sagittifolia L.) tuber starch[J]. International Journal of Biological Macromolecules, 2015, 77:360-368.
[2] LI A, ZHANG Y, ZHANG Y, et al. Comparison of morphology and physicochemical properties of starch among 3 arrowhead varieties[J]. Journal of Food Science, 2016, 81(5):C1 110-C1 117.
[3] 杜征, 赵力超, 肖苏尧, 等. 慈姑淀粉的理化特性及其比较研究[J]. 食品科技, 2010,35(9):70-75.
[4] 王素雅, 秦天仓, 杨玉玲,等. 慈姑直链淀粉的分离与分子结构[J]. 食品与发酵工业, 2009,35(3):41-44.
[5] ANDREEV P V. Using modified starch in russian pharmaceutical industry (A review)[J]. Pharmaceutical Chemistry Journal, 2004, 38(8):447-450.
[6] OSUNDAHUNSI O F , SEIDU K T , MUELLER R . Effect of presence of sulphurdioxide on acetylation and sorption isotherm of acetylated starches from cultivars of cassava[J]. Food Chemistry, 2014, 151(15):168-174.
[7] KAUR L, SINGH N, SINGH J. Factors inflfluencing the properties of hydroxypropylated potato starches[J]. Carbohydrate Polymers, 2003,55(2): 211-223.
[8] MAULANI R R , FARDIAZ D , KUSNANDAR F , et al. Characterization of chemical and physical properties of hydroxypropylated and cross-linked arrowroot (Marantha arundinacea) starch[J]. Journal of Engineering and Technological Ences, 2013, 45(3):207-221.
[9] 肖俊, 张燕萍. 不同原料双氧水氧化淀粉的制备及性能[J]. 食品与发酵工业, 2007,33(11):85-88.
[10] SHANISE L M E H, ROSANA C, VANIA Z P, et al. Structure, morphology and functionality of acetylated and oxidised barley starches[J]. Food Chemistry, 2015, 168:247-256.
[11] WU S H, SEIB P A. Acetylated and hydroxypropylated distarch phosphates from waxy barley: paste properties and freeze-thaw stability [J]. Cereal chemistry, 1990, 67(2):202-208.
[12] 王素雅, 曹崇江, 杨晓蓉, 等. 慈姑淀粉的性质研究[J]. 食品与发酵工业, 2008,34(10):40-43.
[13] 李鑫, 赵燕, 廖斌, 等. 甘薯淀粉糊透明度及凝沉性初探[J]. 食品研究与开发, 2011, 32(3):34-37.
[14] MUADKLAY J, CHAROENREIN S. Effects of hydrocolloids andfreezing rates on freeze-thaw stability of tapioca starch gels[J]. Food Hydrocolloids, 2008, 22: 1 268-1 272.
[15] 赵文恩, 张晓阁, 胡水涛, 等. 双氧水氧化橡实淀粉的实验研究[J]. 郑州大学学报(工学版), 2010, 31(2):72-75.
[16] ZHANG Y R, WANG X L, ZHAO G M, et al. Preparation and properties of oxidized starch with high degree of oxidation[J]. Carbohydrate Polymers, 2012, 87(4):2 554-2 562.
[17] 周雪, 张本山. 高透明度氧化蜡质玉米淀粉性质研究[J]. 粮食与油脂, 2010(4):9-11.
[18] 翁诗甫.傅里叶变换红外光谱分析[M]. 第三版. 北京:化学工业出版社, 2016: 38-42.
[19] SUN F, LIU J, LIU X, et al. Effect of the phytate and hydrogen peroxide chemical modifications on the physicochemical and functional properties of wheat starch[J]. Food Research International, 2017, 100(Pt 1):180-192.
[20] VAN SOEST J J G, TOURNOIS H, DE WTT W, et al. Short-range structure in (partially) crystalline potato starch determined with attenuated total reflectance Fourier-transform IR spectroscopy[J]. Carbohydrate Research, 1995,279:201-214.
[21] 杨莹琦, 田双起, 王新伟, 等. 苹果酸玉米淀粉酯理化性质及消化特性研究[J]. 河南工业大学学报(自然科学版), 2019, 40(3):1-6.
[22] DIOP C I K, LI H L, XIE B J, et al. Effects of acetic acid/acetic anhydride ratios on the properties of corn starch acetates[J]. Food Chemistry, 2011, 126(4):1 662-1 669.