代谢组学(metabolomics)这一概念在20世纪70年代被DEVAUX第一次提出[1],随后在1999年英国伦敦大学NICHOLSON教授将其重新定义[2]。代谢组学又称代谢物组学,是继基因组学、蛋白质组学、转录组学后出现的新兴“组学”。它能够对生物体内相对分子质量1 000以内的代谢物进行定性和定量的分析。代谢组学最主要的技术手段包括质谱、气相色谱、液相色谱、液相色谱-质谱联用(liquid chromatograph-mass spectrometer,LC-MS)、气相色谱-质谱联用(gas chromatography-mass spectrograph,GC-MS)、核磁共振(nuclear magnetic resonance,NMR),而目前使用的分析手段多为组合式联用型仪器,如超高效液相色谱-四级杆串联飞行时间质谱(ultra performance liquid chromatography-quadrupole-time of flight-mass spectrometry,UPLC-QTOF-MS)、超高效液相色谱-串联质谱(ultra performance liquid chromatography-tandem mass spectrometry,UPLC-MS/MS)等。依靠其高通量、高灵敏度、检测范围广的特点,可以对因各种外界因素刺激而引起的植物表型变化、生理活动变化以及代谢变化进行检测分析,通过代谢物的变化探讨引起植物出现差异的原因[3]。完整的代谢组学研究过程,包括样品采集、代谢物提取、代谢物分离、代谢物检测和数据分析,要求尽可能地保留代谢物信息。代谢组学的研究方法主要分为非靶向代谢组学分析和靶向代谢组学分析[4]。二者研究目的不同,各有特点。在实际运用中,通常在前者发现差异代谢物之后,再利用后者进行进一步的确证,常常结合使用,优势互补。
植物多酚是植物中一类化学物的总称,其作为人体“第七类营养素”广泛存在于植物性食物中,人体不能通过自身合成,需从食物中获取[5]。多酚类化合物作为植物代谢过程中的次生代谢物,已经被分离鉴定出八千多种,是自然界最常见的一大类植物活性物质[6]。因其种类繁多,结构不尽相同,通常可将多酚分为类黄酮类(flavonoids)、酚酸类(phenolic acids)、芪类(stilbenes)以及木脂素类(lignans),这些结构上的差异导致其生物利用率、功能活性也均存在差异。研究表明,多酚类物质作用于人体的生理功能主要包括抗氧化[7]、抗炎[8]、抗癌[9]、降血脂[10]、降血糖[11]等。随着人们对天然产物的开发利用,对多酚类物质的研究也将更为深入,挖掘其更多的功能活性作用。
因植物中的多酚类物质易受品种、种植条件、储藏条件、加工过程等方面的影响,从而导致其功能活性也发生变化,所以依靠代谢组学技术对植物中多酚类物质的检测分析能够帮助人们建立代谢物与功能活性变化的联系。本文主要论述了代谢组学作为一种工具在植物多酚定性定量,植物食品质量、种类筛选、加工贮藏及其功能活性方面的应用研究。
1 代谢组学技术在多酚定性定量检测中的应用
代谢组学技术在植物多酚定性定量分析方面占据主导地位,目前主要应用在果蔬、杂粮、茶叶、油脂等植物源性食品方面[12-17],通过高通量的检测和开放式数据库,可以对植物中多酚类物质进行定性和定量,还可以发现新型多酚类物质,有助于对植物多酚领域的深入研究。谢佳函等[18]利用HPLC技术将经过超声辅助提取的红豆皮多酚进行定性分析,通过与各标准品的色谱峰保留时间相比对,最终定性了金丝桃苷、没食子酸、芦丁等13种单体酚,其中主成分峰对应的物质是金丝桃苷。胡会刚等[19]采用液相色谱-四级杆-飞行时间质谱(liquid chromatography-quadrupole-time of flight-mass spectrometry,LC-Q-TOF-MS)对经过分离纯化的芒果皮渣多酚组分进行初步定性分析,共检测出与已知数据库相对应的17个色谱峰,其中正离子模式下为槐角苷等3种多酚化合物,负离子模式下为6-O-没食子酰葡萄糖等14种多酚化合物。邹梦瑜等[20]进行了葡萄酒中多酚类化合物的体内外成分分析,使用了高效液相色谱-傅立叶变换离子回旋共振质谱(high performance liquid chromatography-fourier transform ion cyclotron resonance mass spectrometry,HPLC-FT-ICR MS)和超高效液相色谱(ultra performance liquid chromatography,UPLC)鉴定了葡萄酒多酚提取物中的41种酚类化合物和灌胃入血后的9种多酚原型及代谢物,并利用UPLC快速、灵敏的特点,对这9种潜在活性物质基础成分进行了含量测定,但具体探究其功能活性的机制还有待研究。张云[21]和焦阳[22]分别研究了猕猴桃果实及其种植中的副产物猕猴桃疏果,分别运用高速逆流色谱(high-speed countercurrent chromatography, HSCCC)与制备型高效液相色谱(high performance liquid chromatography,HPLC)联用技术和超高效液相色谱-三重四级杆串联质谱(UPLC-QQQ-MS/MS)。前者通过筛选建立的HSCCC溶剂体系对纯化后猕猴桃多酚提取物具有较好的分离效果,基于此分离出一种非常罕见的酚酸类结构:2-O-咖啡酰基苏糖酸;后者成功实现了在22 min运行时间内对15种酚类化合物进行有效的分离和精确定量,从而确定表儿茶酸是猕猴桃疏果中含量最高的多酚化合物,此类方法显著缩短了测量时间,高效且灵敏。潘汇[23]将荷叶在2种溶剂系统中分离纯化的3种多酚进行HPLC检测分析,结果表明这3种多酚物质分别为紫云英苷、异槲皮苷和槲皮素。
代谢组学技术在植物多酚定性定量分析中的应用逐渐增多,相比于气相色谱和液相色谱灵敏度更高,对于多酚物质的定性更准确。通过组学平台虽然可以对多酚类物质进行检测,但多样化的检测仪器所得到的检测结果也是不同的,而且对于植物样本的前处理也没有规范的方法,所以目前急需建立系统性的多酚高通量检测平台,规范植物样本前处理的方法,形成完整检测分析体系。
2 代谢组学技术定性定量多酚的应用
2.1 定性定量多酚在不同加工方式研究中的应用
日常生活中植物性食品通常会经过不同方式的处理被加工成食物,以提升其食用品质。多酚类物质不稳定,如加热可导致其结构受到破坏,降低其功能性质。而在发酵中多酚可促进有益菌的生长,抑制有害菌的繁殖等,此过程中多酚的含量会发生变化或被转化成其他类物质等。植物食品在不同加工过程中多酚物质的含量和结构均会发生改变,进而影响其功能作用。通过代谢组学手段可以对多酚物质进行检测,从而分析不同处理方式下多酚的变化情况。ZHAO等[24]将光电二极管阵列检测器(photo-diode array, PDA)和质谱仪与超高效液相色谱结合使用,研究了烘烤,煮沸和微波处理方法对蓝莓中多酚的影响。在蓝莓中发现了28个特征峰,其中25个峰受烹饪的影响很大,咖啡酰奎尼酸、儿茶素和槲皮素糖苷在加工中最稳定,该研究比较得出微波烹饪对多酚类物质的影响最大。LONG等[25]为研究堆发酵过程中茶叶活性物质的变化,采用液相色谱-串联质谱联用技术(LC-MS),通过非靶向代谢组学分析表明,堆发酵的第一阶段使黄酮-3-醇和没食子酸的含量降低。靶向代谢组学分析表明,在堆发酵第一阶段之后,葛根素(N-乙基-2-吡咯烷酮取代的没食子儿茶素和儿茶素)的含量显著增加,但是长期的堆发酵会使黄酮糖苷,原花青素和没食子酸的水平明显降低。姜丽等[26]的研究采用气相-飞行时间质谱联用(GC-TOF-MS)对传统曲和新基质曲酿造的黑糯米酒进行差异代谢物的分析,并对发酵72 h内的黑糯米酒进行了跟踪研究,发现苯酚为2种曲酿酒后差异最大的物质,并在发酵60 h时,代谢物积累量最大且差异代谢物数目最多。ERICA等[27]利用核磁共振对酵母菌发酵的苹果酒的生产过程进行实时监测,代谢谱的研究中发现酵母菌种类不同对表儿茶素、儿茶素等酚类物质的种类及含量均有影响,为苹果酒生产中涉及的酵母种类之间的代谢差异提供了初步见解。张灵敏等[28]利用HPLC建立了快速有效的多酚定量分析方法,确定了3个酿酒葡萄品种中的16种单体酚含量,从多酚成分含量角度对酿酒葡萄进行评价提供了依据。PINTO等[29]将顶空固相微萃取与气相色谱-质谱(HS-SPME-GC/MS)相结合和质子核磁共振(1H NMR)光谱研究了霞多丽葡萄在橡木桶中储存时间对多酚类物质变化的影响,发现了多酚变化与葡萄酒褐变的关系。
2.2 定性定量多酚在品种、产地区分中的应用
每种植物都有不同的品种,而且种植范围广,不同的品种和产地导致植物中多酚类物质产生差异。如市售的不同品种的苹果,颜色外观,口味营养各不相同,这些差异与多酚的种类与含量密不可分。通过代谢组学手段可以对多酚物质进行检测,从而分析不同品种、产地的植物产品中多酚的差异情况。FRANCINI等[30]利用1H NMR技术结合主成分分析(principal component analysis, PCA),对不同品种的苹果干中的多酚类物质进行研究分析,发现了苹果干中儿茶素、表儿茶素、绿原酸等活性物质及其抗氧化能力是区别其品种的判断依据。ALESSIO等[31]为区别不同产地的特级初榨橄榄油,对多个样品进行了分析目标气相色谱-质谱联用(GC-MS)和综合二维气相色谱-质谱(GC/GC-TOF-MS)的非目标谱分析,发现各产地的橄榄油之间在多酚的特征方面的差异是显著的。对不同产地植物性食品中的多酚类物质进行代谢组学分析有助于建立成熟的食品溯源体系[32-33]。KASHIF等[34]使用PCA和偏最小二乘判别分析(partial least squares discrimination analysis, PLS-DA)等相关多元数据分析与1H NMR相联系对3个品种的葡萄的4个发育阶段进行多变量数据分析以识别总体代谢差异,发现“Trincadeira”较其他2个品种酚类含量低,并且此类葡萄发育初始阶段显示出较高的酚类含量,这在生理学上增加了人们对葡萄生长发育的理解。
2.3 定性定量多酚在品质、等级区分中的应用
多酚类物质的种类和含量对植物性食品的风味和品质具有重要影响,也逐渐成为评价和衡量植物食品等级的重要指标之一。通过代谢组学手段可以对多酚物质进行检测,从而分析不同品质、等级下多酚的变化情况。在茶叶中,人们通常会忽略除儿茶素和黄酮醇以外的多酚对茶涩性的影响。ZHUANG等[35]使用液相色谱-质谱法,通过靶向代谢谱分析评估了多酚的贡献,从47种绿茶样品中鉴定出86种多酚,其涩味评分各不相同,结果表明,多酚的单羟基黄酮醇和酰基衍生物与除没食子酸和儿茶素以外的多酚呈负相关,与其他多酚呈现明显的分离,反映出此类物质多茶涩味的独特作用。郭雪梅[36]采用HPLC对8个不同等级的祁门红茶进行多酚定量分析,发现高等级红茶中,表没食子儿茶素没食子酸酯(epigallocatechin gallate, EGCG)明显高于低等级,同时通过高分辨质谱(LC-LTQ-Orbitrap)对不同等级红茶样品进行非靶标代谢组学分析,在多元统计分析方法下从不同等级的红茶中共筛选出17个差异代谢物,通过相关性分析最终确定3个代谢物作为判断红茶等级的标准物。
通过代谢组学的方法可对加工后的植物食品中的多酚物质进行检测,探讨不同处理对多酚含量和结构的影响。品种和产地的不同,导致植物中多酚含量存在差异,反之通过对多酚物质的检测分析,可将不同品种和不同产地的植物产品进行区分。对于品质的差异也可以用多酚的含量与种类进行区分。但目前这些研究仅停留在代谢物含量的分析上,对于出现差异的机理研究并不多,关于代谢通路的分析也较少,代谢途径的分析将更全面的解释这些现象。
2.4 定性定量多酚在多酚功能活性研究中的应用
植物多酚具有较好的功能活性,对于疾病的预防和治疗有很好的功效,目前多酚的功能活性主要体现在抗氧化、抗炎、降血糖、降血脂方面。通过动物实验对多酚功能活性的研究较多,体内实验的研究将多酚在临床治疗、保健药品、食品的推广趋向于安全化、可应用化,也提升了多酚的应用价值。SEVERINA等[37] 对来自意大利坎帕尼亚地区的鼠尾草叶应用液相色谱-串联质谱法(liquid chromatographytandem mass spectrometry,LC-MS/MS)进行定性和定量分析,并首次发现木质素寡聚物,此类物质对抑制AChE酶能力较强,为评估“坎帕尼亚”鼠尾草在动物模型中预防中枢神经系统疾病提供了可能性。与此类似的还有浆果多酚对人体代谢的贡献[38]。苏天霞等[39]通过高效液相色谱法,在猕猴桃皮多酚中发现了原儿茶酸、表儿茶素、七叶亭等多酚类物质,并对脂代谢紊乱的小鼠进行代谢分析,发现此类多酚物质具有正向调控的作用。CHANG等[40]通过代谢组学研究发现黑豆种皮中的花青素可以降低PGE2、NO以及抑制大鼠中COX-2和iNOS基因的表达而发挥抗炎症活性。MA等[41]利用LC-MS/MS技术分析了假木霉和黑根霉混合培养发酵液对猕猴桃根际土壤处理后,对其货架期和果实品质的影响。代谢组学数据显示,在采摘后室温(25℃)储藏条件下,0、10、15 d不同程度地提高了总酚含量,混合培养发酵液处理改变了几种类黄酮代谢物,对延长保质期和改善水果质量有帮助。汤小芳[42]利用超高液相色谱-四级杆串联飞行时间质谱(UPLC-QTOF-MS)代谢组学分析手段,对EGCG干预下的衰老小鼠的血清、尿液、肠道、脑组织进行代谢组学研究,通过差异代谢物的筛选及代谢通路的分析,最终发现了与EGCG抗衰老作用有关的代谢通路及相应代谢物。
目前研究已经证实了植物多酚的许多功能活性,通过代谢组学的方法可以对不同功能活性的多酚进行检测分析,探究关键代谢物及其作用机理,证实多酚单体具有的功能活性,但仍然需要利用尖端的仪器设备进行解析,并逐渐完善分析体系。另外,由于植物多酚中的结合态酚的提取和鉴定操作繁琐,在研究多酚功能活性中,代谢组学技术主要集中在对游离酚的检测分析上。未来应进一步研究不同多酚单体的功能评价,以更好地提升多酚的应用价值。
3 多组学技术在多酚功能活性研究中的应用
在对多酚功能活性的研究中,一些植物多酚如白藜芦醇、EGCG、迷迭香多酚、姜黄素等所表达的抗肿瘤活性逐渐引起人们的注意[43]。代谢组学技术可以发现多酚类物质的更多功能活性成分,但对多酚类物质的抗肿瘤活性的研究则需要其他组学技术和细胞实验技术的支撑,所以应用多组学技术对多酚类物质功能活性的研究正在逐渐展开。蛋白质组学技术可以从肿瘤信号传导途径、肿瘤细胞凋亡等多方面阐明这些活性的产生与癌细胞体内蛋白的差异表达之间的关系,在多酚的功能活性研究中同样发挥着重要的作用。ZHANG等[44]的研究为确定EGCG对人体肝细胞癌的作用及其分子机制,通过二维凝胶电泳(two-dimensional gel electrophoresis, 2-DE)和基质辅助激光解吸/电离飞行时间质谱法(matrix-assisted laser desorption ionization-time of flight-mass spectrometry, MALDI-TOF-MS)分析得知,EGCG有诱导细胞凋亡,抑制人体肝癌细胞转移的能力,其抗转移作用与抑制基质金属蛋白酶MMP-2和MMP-9活性有关。MENORET等[45]经十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(sodium dodecyl sulfatepolyacrylamide gelelectrophoresis,SDS-PAGE)、LC-MS/MS分析发现白藜芦醇具有调节结肠癌细胞HCT116的细胞周期的作用,肌动蛋白、Hsp60等均受到白藜芦醇的影响。也有研究者将代谢组学与转录组学结合使用,利用GC-MS及逆转录-聚合酶链反应(reverse transcription-polymerase chain reaction,RT-PCR)检测分析手段研究了迷迭香多酚提取物和鼠尾草酸对HT-29结肠癌细胞转录组和胆固醇代谢的影响。研究表明在迷迭香多酚和鼠尾草酸处理下,HT-29细胞激活了调节因子的转录活性,在脂质代谢中起关键作用。迷迭香多酚处理可诱导HT-29细胞中以活性氧产生和内质网应激下UPR信号通路协调为主导的相关代谢和转录变化[46]。
单一的组学技术因其本身技术的局限,只能从特定的角度分析植物多酚的作用机理,目前多组学联用在植物多酚研究中仍鲜有报道,且均为多酚类物质抗肿瘤活性的研究。对于多酚类物质更多功能活性的研究必须进行体外细胞实验和小鼠等模型的体内实验,代谢组学仅是众多研究平台中的一部分,多组学平台联用将会对植物多酚功能活性的具体、清晰、完整的作用机制研究提供更多可能。
4 总结与展望
随着组学技术的不断发展和完善,代谢组学技术将在植物多酚检测分析中发挥越来越重要的作用,此类技术在帮助人们了解植物中化学成分,并在动态中把握成分变化及其带来的影响等方面具有重要指导意义。在研究植物性食品的不同品种产地、加工贮藏方式下,可以找出关键的代谢物质及代谢途径中的关键节点,可以从更深的角度去阐明代谢物的变化,以及此变化对功能活性、感官品质、机体健康所带来的影响。目前对于植物多酚类物质的功能活性研究大多是在宏观意义上的,鲜有对具体多酚物质的研究。利用代谢组学技术可以在探究植物的功能活性上准确找出关键的多酚类物质。目前代谢组学仍属于一种具备潜力、尚待开发的新兴学科领域,同时也有很多因素制约了代谢组学在食品科学方面的应用。同时,因其发展时间较短,存在着样品分析结果不稳定、仪器分析范围有局限等问题,又因数据库不完善等原因,导致仅有一部分的代谢产物能够被识别,未识别的代谢产物仍占比巨大。如何将各种实验技术和多组学平台结合起来,对多酚类物质的功能活性进行深入研究,以上述存在的问题。
[1] DEVAUX P G,HORNINA M, G,HORNING E C.Benyzl-oxime derivative of steroids: a new metabolic profile procedure for human urinary steroids[J].Analytical Letters,1971,4(3):151-160.
[2] NICHOLSON J K,LINDON J C,HOLMES E.Metabonomics: understanding the metabolic responses of living systems to pathophysiological stimuli via multivariate statistical analysis of biological NMR spectroscopic data[J].Xenobiotica,1999,29(11):1 181-1 189.
[3] 朱超,梁琼麟,王义明,等.代谢组学的整合化发展及其新进展[J].分析化学,2010,38(7):1 060-1 068.
[4] CEVALLOS-CEVALLOS J M,REYES-DE-CORCUERA J I,ETXEBERRIA E,et al.Metabolomic analysis in food science:a review[J].Trends in Food Science & Technology,2009,20(11):557-566.
[5] MANDAL S M,CHAKRABORTY D,DEY S.Phenolic acids act as signaling molecules in plant-microbe symbioses[J].Plant Signaling and Behavior,2010,5(4):359-368.
[6] 左玉.多酚类化合物研究进展[J].粮食与油脂,2013,26(4):6-10.
[7] DIAO Jianxin,OU Jinying,DAI Huan,et al.Antioxidant and antiapoptotic polyphenols from Green tea extract ameliorate CCL4-induced acute liver injury in mice[J].Chinese Journal of Integrative Medicine, 2019.DOI:10.1007/S11655-019-3034-5.
[8] LEONG D J,CHOUDHURY M,HANSTEIN R,et al.Correction to: Green tea polyphenol treatment is chondroprotective, anti-inflammatory and palliative in a mouse posttraumatic osteoarthritis model[J].Arthritis Research & Therapy,2019,21(1).DOI:10.1186/S13075-018-1791-9.
[9] MIYATA Y,SHIDA Y,HAKARIYA T,et al.Anti-cancer effects of green tea polyphenols against prostate cancer[J].Molecules (Basel,Switzerland),2019,24(1):193.
[10] QI Rong,LIAN Guan,YU Maomao,et al.Study on hypolipidemic and anti-atherosclerosis effects of grapeseed polyphenols[J].Atherosclerosis,2017,263:168.
[11] 韦芳媚.桑叶提取物、茶多酚及其复配物的抗氧化和降血糖活性[D].广州:华南理工大学,2019.
[12] XUE Ying,XU Xianshun,LI Yong,et al.Optimization of vortex-assisted dispersive liquid-liquid microextraction for the simultaneous quantitation of eleven non-anthocyanin polyphenols in commercial blueberry using the multi-objective response surface methodology and desirability function approach[J]. Molecules (Basel,Switzerland),2018,23(11):2 921.
[13] 李文婷.六种豆类中不同结合态多酚组成、胃肠道生物可接受率及其抗氧化活性研究[D].南昌:南昌大学,2018.
[14] PARK J E,KIM T E,SHIN K H.Quantitative analysis of four catechins from green tea extract in human plasma using ultra-performance liquid chromatography-tandem mass spectrometry for pharmacokinetic studies[J].Molecules (Basel,Switzerland),2018,23(4):984.
[15] IRENE D,SERENELLA S,ANTONELLO S,et al.Development and validation of an analytical method for total polyphenols quantification in extra virgin olive oils[J].Food Analytical Methods,2020,13(2):457-464.
[16] G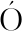 MEZ M E,ROSALES C N,LE
MEZ M E,ROSALES C N,LE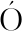 N G M E,et al.Citrus peels waste as a source of value-added compounds:Extraction and quantification of bioactive polyphenols[J].Food Chemistry,2019,295:289-299.
N G M E,et al.Citrus peels waste as a source of value-added compounds:Extraction and quantification of bioactive polyphenols[J].Food Chemistry,2019,295:289-299.
[17] MA Sihui,KIM C,NEILSON A P,et al.Comparison of common analytical methods for the quantification of total polyphenols and flavanols in fruit juices and ciders[J].Journal of Food Science,2019,84(8):2 147-2 158.
[18] 谢佳函,刘回民,刘美宏,等.红豆皮多酚提取工艺优化及抗氧化活性分析[J].中国食品学报,2020,20(1):147-157.
[19] 胡会刚,赵巧丽.芒果皮渣多酚的提取分离及抗氧化活性分析[J].现代食品科技,2020,36(2):53-62.
[20] 邹梦瑜,吕慧婕,崔艳,等.葡萄酒中多酚类化合物的体内外成分分析[J].沈阳药科大学学报,2019,36(11):1 033-1 040.
[21] 张云.猕猴桃多酚分离鉴定及抗氧化活性研究[D].长沙:中南林业科技大学,2019.
[22] 焦阳.基于UPLC-QQQ-MS/MS和循环伏安法的猕猴桃疏果多酚鉴定及功能特性研究[D].杨凌:西北农林科技大学,2019.
[23] 潘汇.荷叶中多酚类物质的提取,分离及抗氧化构效关系的研究[D].芜湖:安徽工程大学,2018.
[24] ZHAO Yang,WU Xianli,YU Liangli,et al.Retention of polyphenols in blueberries (Vaccinium corymbosum) after different cooking methods,using UHPLC-DAD-MS based metabolomics[J].Journal of Food Composition and Analysis,2017,56:55-56.
[25] LONG Piaopiao,WEN Mingchun,DANIEL G,et al.Untargeted and targeted metabolomics reveal the chemical characteristic of pu-erh tea(Camellia assamica)during pile-fermentation[J].Food Chemistry,2020,311:125 895.
[26] 姜丽,苏伟,母应春,等.基于GC-TOF-MS代谢组学研究高度黑糯米酒后发酵阶段代谢差异[J/OL].食品科学:1-16[2020-02-19].https://kns.cnki.net/KCMS/detail/11.2206.TS.20191025.1701.015.html.
[27] ERICA C,LAURA R C,ROBERTO C,et al.NMR-based metabolic profiling of different yeast fermented apple juices[J].LWT,2020,118:108 711.
[28] 张灵敏,周培羽,张舒婷,等.酿酒葡萄多酚含量及抗氧化活性分析[J].沈阳药科大学学报,2019,36(6):539-548.
[29] PINTO J,OLIVEIRA A S,AZEVEDO J,et al.Assessment of oxidation compounds in oaked Chardonnay wines: A GC-MS and 1H NMR metabolomics approach[J].Food Chemistry,2018,257:120-127.
[30] FRANCINI A, ROMES S, CIFELLI M, et al.1H NMR and PCA-based analysis revealed variety dependent changes in phenolic contents of apple fruit after drying[J].Food Chemistry,2017,221:1 206-1 213.
[31] ALESSIO D R,MASUERO D,RICCADONNA S,et al.Complementary untargeted and targeted metabolomics for differentiation of extra virgin olive oils of different origin of purchase based on volatile and phenolic composition and sensory quality[J].Molecules(Basel, Switzerland),2019,24(16):2 896.
[32] 祝爱艳.基于代谢组学技术构建赣南脐橙产地溯源体系[D].南昌:南昌大学,2018.
[33] 冯玉超.基于GC-MS技术的黑龙江省主产区水稻(Oryza sativa L)代谢组学分析[D].大庆:黑龙江八一农垦大学,2019.
[34] KASHIF A,FEDERICA M,ANA M F,et al.Monitoring biochemical changes during grape berry development in Portuguese cultivars by NMR spectroscopy[J].Food Chemistry,2010,124(4):1 760-1 769.
[35] ZHUANG Juhua,DAI Xinlong,ZHU Mengqing,et al.Evaluation of astringent taste of green tea through mass spectrometry-based targeted metabolic profiling of polyphenols[J].Food Chemistry,2020,305:125 507.
[36] 郭雪梅.不同等级红茶样品主要成分分析和代谢组学研究[D].合肥:安徽农业大学,2018.
[37] SEVERINA P,SIMONA P,ANNAMARIA L,et al.A metabolic profiling approach to an Italian sage leaf extract (SoA541) defines its antioxidant and anti-acetylcholinesterase properties[J].Journal of Functional Foods,2017:29:1-9.
[38] SUH D H,JUNG E S,LEE G M,et al.Distinguishing six edible berries based on metabolic pathway and bioactivity correlations by non-targeted metabolite profiling[J].Frontiers in Plant Science,2018,9:1 462.
[39] 苏天霞,袁敏兰,周艳,等.猕猴桃皮多酚对高脂膳食大鼠脂代谢紊乱的调节作用[J/OL].食品科学:1-9[2020-02-15].https://kns.cnki.net/KCMS/detail/11.2206.TS.20200109.1110.036.html.
[40] HYE J K,IRINA T,JUNG M P,et al.Anthocyanins from soybean seed coat inhibit the expression of TNF-α-induced genes associated with ischemia/reperfusion in endothelial cell by NF-κB-dependent pathway and reduce rat myocardial damages incurred by ischemia and reperfusion in vivo[J].FEBS Letters,2006,580(5):1 391-1 397.
[41] MA Qunfei,CONG Yunzhe,WANG Jiayue,et al.Pre-harvest treatment of kiwifruit trees with mixed culture fermentation broth of Trichoderma pseudokoningii and Rhizopus nigricans prolonged the shelf life and improved the quality of fruit[J].Postharvest Biology and Technology,2020,162:111 099.
[42] 汤小芳.基于生物信息学研究茶多酚EGCG对小鼠肠道菌群及代谢的影响[D].南昌:南昌大学,2019.
[43] 李谣,廖霞,肖星凝,等.基于蛋白质组学的植物多酚抗肿瘤作用机制研究进展[J].食品科学,2016,37(3):235-240.
[44] ZHANG Yunjuan,OWUSU L,DUAN Wei,et al.Anti-metastatic and differential effects on protein expression of epigallocatechin-3-gallate in HCCLM6 hepatocellular carcinoma cells[J].International Journal of Molecular Medicine,2013,32(4):959-964.
[45] MENORET A,DREW D A,MIYAMOTO S,et al.Differential proteomics identifies PDIA3 as a novel chemoprevention target in human colon cancer cells[J].Molecular Carcinogenesis,2014,53(1):11-22.
[46] ALBERTO V,GIUSEPPE S,ELENA I,et al.Rosemary polyphenols induce unfolded protein response and changes in cholesterol metabolism in colon cancer cells[J].Journal of Functional Foods,2015,15:429-239.