红酸汤是以红辣椒(鲜品)、番茄、生姜、大蒜、精盐和糯米等为原料[1],由酵母菌、乳酸菌、醋酸菌[2]等微生物发酵而成的一种地方特色调味品,具有开胃健脾、帮助消化,防止腹泻等功效,还能起到除惑提神的作用,深受广大消费者喜爱。目前对红酸汤的研究主要集中在工艺优化[2]、生理功能[3]和营养分析[4]等方面,在风味分类方面研究较少。
气-质联用技术(gas chromatography-mass spectrometry,GC-MS) 是气相色谱加质谱技术的简称,二者结合可以实现复杂有机化合物的分离和定性,作为分析挥发性物质的有效工具,具有操作简便、高效、高灵敏度等特点。目前广泛应用于调味品[5]、乳类[6]、酒类[7]、茶叶[8]、肉类[9]等。电子鼻是一种模拟人生理嗅觉从整体评价食品气味的技术,其样品前处理简便快捷,检测速度快,结果易读,目前主要应用于调味品[10]、乳类[11]等研究领域。本文拟以GC-MS检测结果结合主成分综合评分法建立评价模型,对红酸汤的气味物质进行识别。另外,在已有研究中还未见电子鼻应用于分析红酸汤的相关报道。
本研究以不同品牌红酸汤为研究对象,探索利用电子鼻和GC-MS,结合主成分分析不同红酸汤挥发性风味物质的异同,以GC-MS分析结果结合主成分综合评分方法建立红酸汤挥发性物质的评价模型,为红酸汤的识别提供理论依据。
1 材料与方法
1.1 材料与试剂
所有样品购于京东超市,具体见表1。
表1 样品信息
Table 1 Sample information

样品产地配料冠想源(A)贵州毕节市 西红柿、红辣椒、食用盐、大豆油、菜籽油、味精、食用香料、山梨酸钾、D-异抗坏血酸钠、柠檬酸、黄原胶、乙二胺四乙酸二钠、焦亚硫酸钠、苯甲酸钠玉梦(B) 贵州黔东南州西红柿、红辣椒、食用盐、大豆油、味精、鸡精、生姜、白砂糖、花椒、胡椒、木姜油、脱氢乙酸钠、羧甲基纤维素钠、D-异抗坏血酸钠、山梨酸钾亮欢寨(C)贵州黔东南州西红柿、红辣椒、食用盐、白酒、山梨酸钾、脱氢乙酸钠刘胡子(D)贵州遵义市 西红柿、红辣椒、食用盐、大蒜、糯米、生姜、黄原胶、柠檬酸
1.2 仪器与设备
SQ680气质联用仪、色谱柱Elite-5MS(30 m×0.25 mm×0.25 μm),美国PerkinElmer;PC-420D专用磁力加热搅拌装置、75 μm CAR/PDMS手动萃取头,美国Supelco公司;FOX 4000电子鼻,法国Alpha MOS公司;其他为实验室常用仪器设备。
1.3 电子鼻检测
FOX 4000电子鼻由3个矩阵室,18根金属氧化物传感器组成,每根传感器对一类或几类物质敏感[11],其传感器具体特性见表2。样品处理:准确称取2.00 g样品于10 mL顶空瓶,密封待用;顶空加热300 s;进样量1 000 μL。电子鼻检测参数设置:手动进样速度1 000 μL/s;分析时间300 s,分析器清洁180 s,每个样品平行检测6次,取后4次传感器在第300 s时获得的稳定信号进行分析。
表2 电子鼻传感器性能特点
Table 2 The performance characteristics of electronic nose sensor
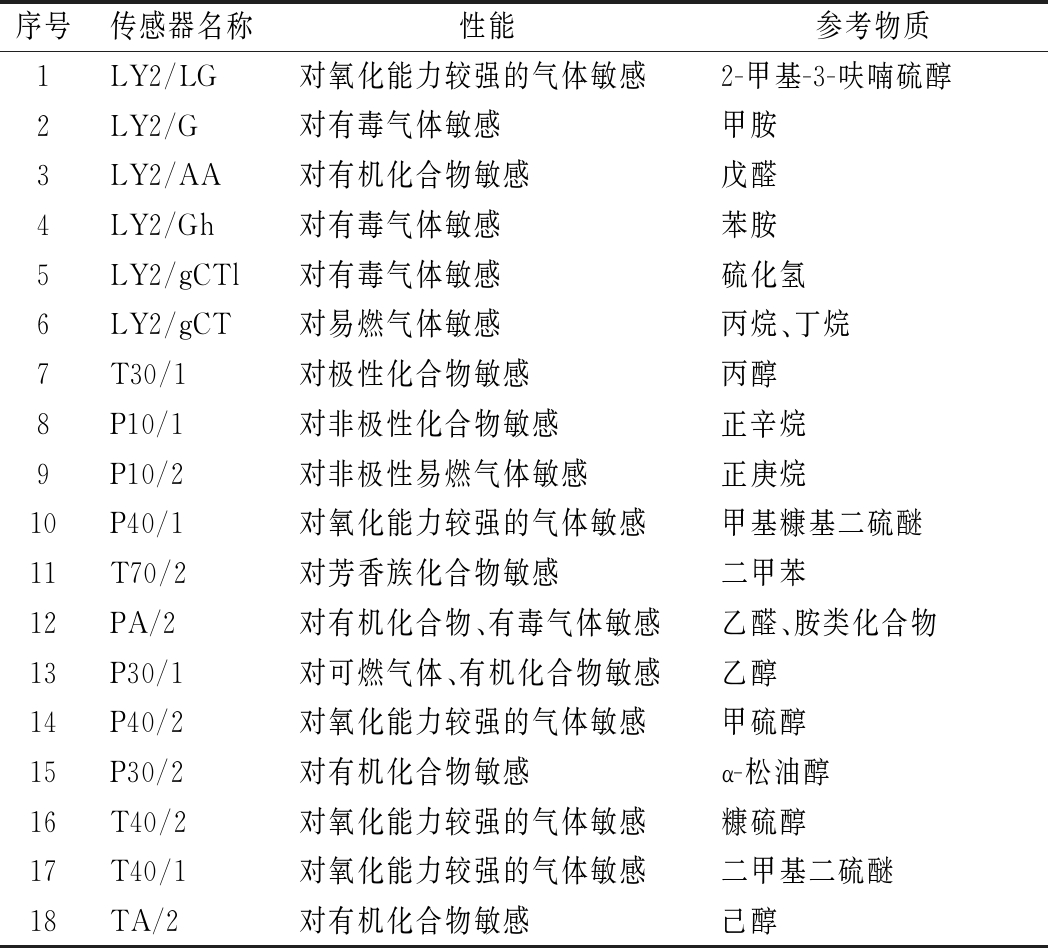
序号传感器名称性能参考物质1LY2/LG对氧化能力较强的气体敏感2-甲基-3-呋喃硫醇2LY2/G对有毒气体敏感甲胺3LY2/AA对有机化合物敏感戊醛4LY2/Gh对有毒气体敏感苯胺5LY2/gCTl对有毒气体敏感硫化氢6LY2/gCT对易燃气体敏感丙烷、丁烷7T30/1对极性化合物敏感丙醇8P10/1对非极性化合物敏感正辛烷9P10/2对非极性易燃气体敏感正庚烷10P40/1对氧化能力较强的气体敏感甲基糠基二硫醚11T70/2对芳香族化合物敏感二甲苯12PA/2对有机化合物、有毒气体敏感乙醛、胺类化合物13P30/1对可燃气体、有机化合物敏感乙醇14P40/2对氧化能力较强的气体敏感甲硫醇15P30/2对有机化合物敏感α-松油醇16T40/2对氧化能力较强的气体敏感糠硫醇17T40/1对氧化能力较强的气体敏感二甲基二硫醚18TA/2对有机化合物敏感己醇
1.4 GC-MS检测
顶空固相微萃取(headspace solid-phase micro extraction,SPME)条件:取样品2.00 g置于15 mL样品瓶中,加入搅拌子(聚四氟乙烯)密封,磁力搅拌装置温度70 ℃,转速1 r/s,平衡600 s,然后将老化(250 ℃,600 s)的萃取头插入样品瓶萃取2 400 s,随后插入GC-MS进样口,解析600 s。
色谱条件[2]:色谱柱Elite-5MS(30 m×0.25 mm×0.25 μm);升温程序:起始温度40 ℃,保留2 min,以4 ℃/min升温至250 ℃,保留1 min。载气(99.999% He)流速1.0mL/min; 流速1 mL/min,分流比5∶1。
MS条件:EI离子源,电子轰击能量为70 eV,离子源温度230 ℃,电子倍增电压1 350 V;全扫描;质量扫描范围45~400 m/z;扫描延迟70 s;标准调谐文件。
定性方法:选取正反匹配度均>700,参考NIST 2011谱库同时结合人工解谱和参考文献。
1.5 数据处理
电子鼻数据分析采用Origin 2018作图;GC-MS数据分析采用SPSS 22.0对样品进行主成分分析。
2 结果与分析
2.1 电子鼻雷达图分析
图1为4种红酸汤电子鼻传感器平均值制作的雷达图。(如图1所示)所有传感器对红酸汤均有响应且有差异,说明4种样品在气味上存在差异。
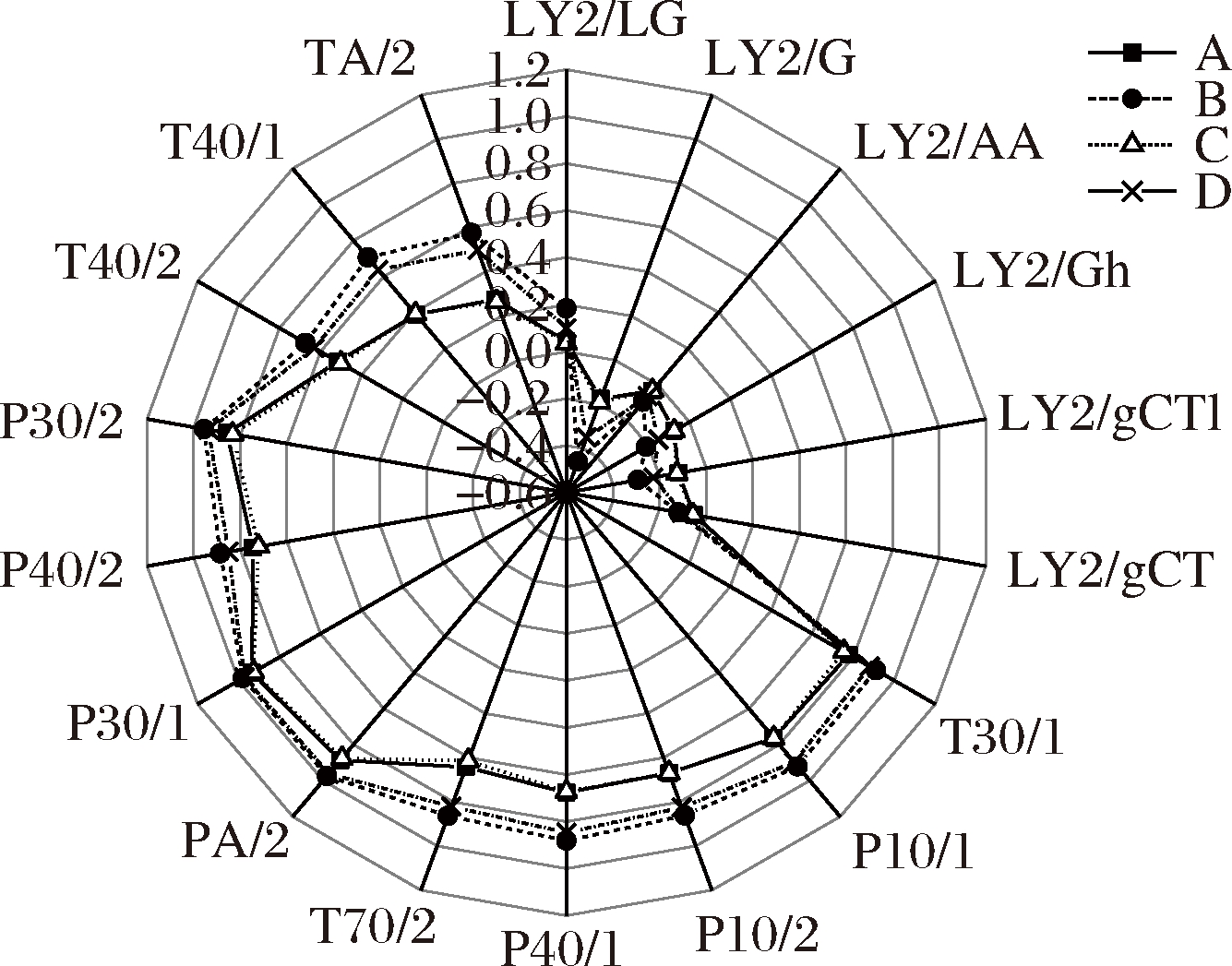
图1 四种红酸汤电子鼻雷达图
Fig.1 The radar map of E-nose responses of 4 Red sore soup
通过比较发现,在所有传感器上A、C样品响应值较为接近且较低,B、D较为接近且较高;可以推测A、C较为相似,B、D较为相似。LY2型传感器响应值较低(大多数位于-0.3~0),这可能与其大多数均对有毒有害气体敏感有关[12](如苯胺、硫化氢等),而样品中并不含或含量极低。样品在LY/AA传感器(对有机化合物敏感,如酸性气体、醇类饮料、发酵味等)上差异较小,这可能与红酸汤是众多微生物共同作用产酸,生成醇类、酸类物质有关。4个样品在P30/1(对碳氢化合物、溶剂,如食物的香气、天然香气挥发物敏感)[13]上差异最小,且响应值最高,这可能与样品中各类香味物质的相对含量和种类较为接近有关,需要进一步研究。PA/2(对有机化合物,如乙醇等物质敏感)响应值较高,这可能与4个样品中均含有大量醇类物质有关[14](GC-MS分析4个样品醇类物质差异较小能够印证此结论)。样品在T40/1(对氧化能力较强的气体敏感)上的差异最大,这可能是红酸汤在发酵时产生了大量的氧化气体所致。
2.2 GC-MS检测结果分析
2.2.1 挥发性物质分析
图2为样品挥发性成分总离子流图。图中样品出峰时间主要集中在0~30 min,说明升温程序基本科学合理。表3为4种红酸汤挥发性物质GC-MS检测结果。红酸汤的气味物质是以醇类物质为基础[(A、B、C、D检测出相对含量分别为19.840%、24.082%、21.854%、24.083%,标准偏差较小(1.77)]。这可能是由酵母菌、乳酸菌为红酸汤主要发酵菌群决定[2]。一般认为醇类物质的前体物质是多不饱和脂肪酸[15],他们是酵母菌分解糖代谢以及氨基酸脱氨的代谢产物[16]、stretcher降解产物继续还原生成[17]。酚类物质的含量相对较少(0.32%~3.69%),酚类物质大多具有烟熏香味,一般由酚羧酸的脱羧[18]或酪氨酸降解[19]而来。醛类物质的相对含量在3.29%~19.63%,阈值低[20],对样品气味的贡献较大;醛类物质是酶和微生物氧化不饱和脂肪酸以及Strecker降解[21]形成。4个样品的酸类物质相对含量差异大(标准偏差为10.79),可能是样品差异形成的原因之一。酸类物质是酵母菌、乳酸菌等菌群发酵的产物。酮类物质的相对含量在0.37%~11.57%,一般是脂肪氧化、降解以及美拉德反应[22]等生成;由于其阈值一般高于其同分异构体的醛类[23],因此对风味的贡献相对不大。4个样品的烷烃类物质较少,阈值较高且基本不具有活性[24],对样品香味贡献不大;烯烃类(B、C)较多,且阈值较低,是辣椒中重要的风味物质[25],对样品贡献有一定贡献。酯类物质(4.22%~25.25%)差异较大,其中 B样品含量较低(4.22%),其他含量较高。一般认为酯类物质是酸和醇发生酯化反应的产物[26],也是辣椒发酵的主要反应产物之一[27]。检测到的酯类物质是大多碳原子数<10的低级酯,这类物质一般具有浓郁的芬香气和特殊的水果香[28-29]。硫醚类物质总体含量不高,比较而言B、D含量较高,A、C含量较低,这可能与B、D样品中添加有鸡精[30]和大蒜[31]有关。

A-样品A;B-样品B;C-样品C;D-样品D
图2 样品挥发性成分总离子流图
Fig.2 The total ion chromatogram of volatile components of the sample
表3 四种红酸汤挥发性物质GC-MS检测结果单位:%(相对含量)
Table 3 Detection results of volatile substances of 4 red sore soup by GC-MS

分类序号保留时间/min中文名称分子式相对分子质量ABCD11.50乙醇C2H6O46.0690.84±0.010.26±0.011.43±0.034.54±0.1221.80丙醇C3H8O60.0950.24±0.0132.092-丁醇C4H10O74.1221.29±0.0343.18异丁硫醇C4H10S90.183.67±0.1453.86异戊醇C5H12O88.1481.76±0.020.31±0.0363.903-甲基-1-丁醇C5H12O88.152.39±0.0573.95(±)-2-甲基-1-丁醇C5H12O88.150.24±0.0283.95S-(-)-2-甲基-1-丁醇C5H12O88.150.70±0.022.36±0.0894.63正戊醇C5H12O88.1480.12±0.01105.085-甲基-1-己醇C7H16O116.202.02±0.02115.091,3-丁二醇C4H10O290.120.05±0.01125.092,3-丁二醇C4H10O290.121.91±0.01135.09戊醇C5H12O88.150.06±0.03146.564-甲基-1-戊烯-3-醇C6H12O100.160.11±0.02156.684-甲基-1-戊醇C6H14O102.1750.11±0.031.24±0.05166.973-甲基-1-戊醇C6H14O102.1750.45±0.01177.163-己烯-1-醇C6H12O100.161.17±0.02187.254-己烯-1-醇C6H12O100.160.51±0.03197.25糠醇C5H6O298.101.07±0.00醇类207.30叶醇C6H12O100.160.90±0.01217.76正己醇C6H14O102.1750.94±0.010.38±0.02227.81己醇C6H14O102.170.72±0.04238.943-甲基-2-己醇C7H16O116.2010.18±0.012412.413,5-二甲基环己醇C8H16O128.2120.47±0.032512.503,3-二甲基环己醇C8H16O128.210.24±0.022613.92苯甲醇C7H8O108.141.91±0.020.36±0.032713.99桉叶油醇C10H18O154.250.42±0.012815.45二氢香芹醇C10H18O154.250.04±0.012916.49芳樟醇C10H18O154.2498.89±0.066.24±0.022.91±0.030.31±0.023016.66脱氢芳樟醇C10H16O152.230.31±0.02
续表1
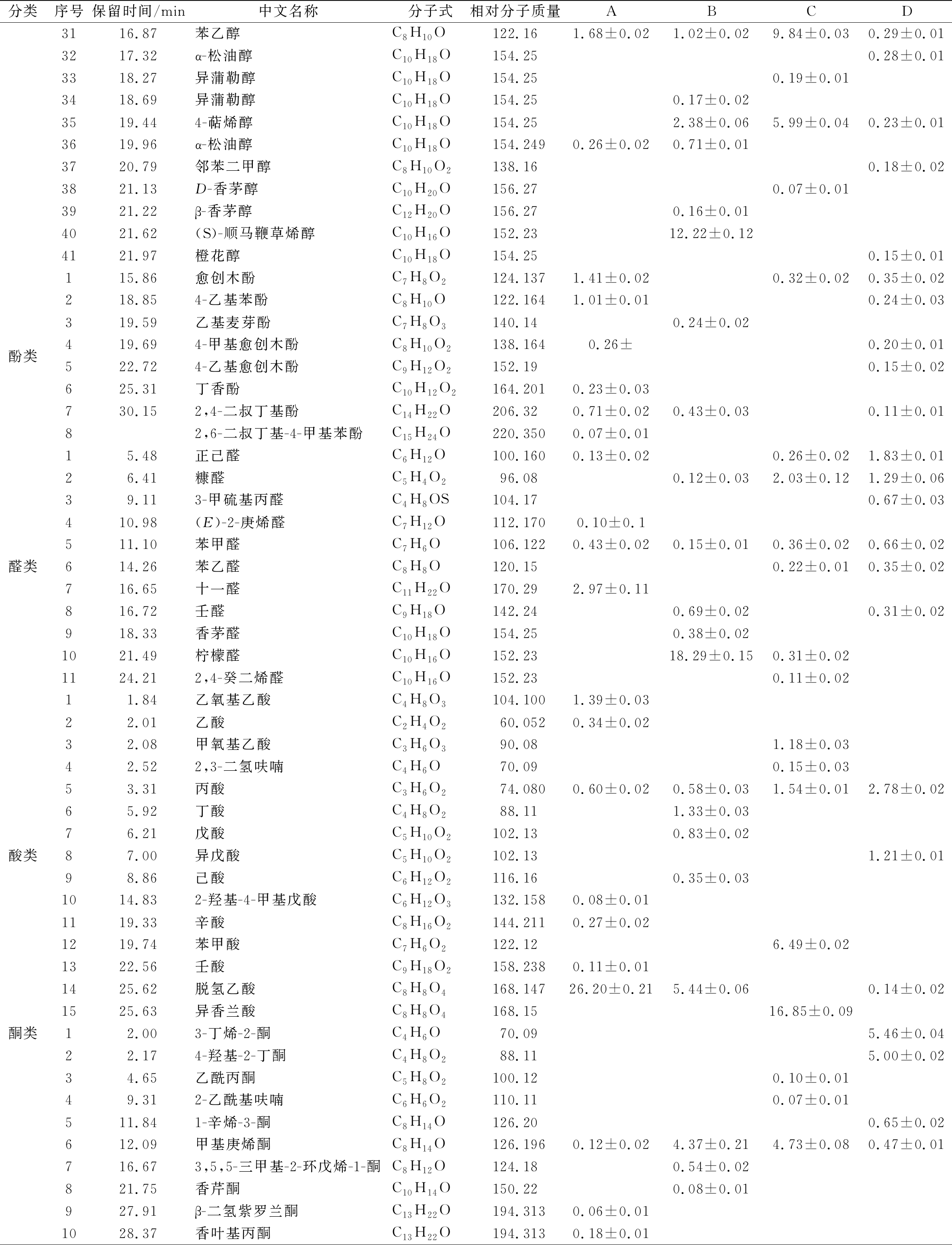
分类序号保留时间/min中文名称分子式相对分子质量ABCD3116.87苯乙醇C8H10O122.161.68±0.021.02±0.029.84±0.030.29±0.013217.32α-松油醇C10H18O154.250.28±0.013318.27异蒲勒醇C10H18O154.250.19±0.013418.69异蒲勒醇C10H18O154.250.17±0.023519.444-萜烯醇C10H18O154.252.38±0.065.99±0.040.23±0.013619.96α-松油醇C10H18O154.2490.26±0.020.71±0.013720.79邻苯二甲醇C8H10O2138.160.18±0.023821.13D-香茅醇C10H20O156.270.07±0.013921.22β-香茅醇C12H20O156.270.16±0.014021.62(S)-顺马鞭草烯醇C10H16O152.2312.22±0.124121.97橙花醇C10H18O154.250.15±0.01115.86愈创木酚C7H8O2124.1371.41±0.020.32±0.020.35±0.02218.854-乙基苯酚C8H10O122.1641.01±0.010.24±0.03319.59乙基麦芽酚C7H8O3140.140.24±0.02酚类419.694-甲基愈创木酚C8H10O2138.1640.26±0.20±0.01522.724-乙基愈创木酚C9H12O2152.190.15±0.02625.31丁香酚C10H12O2164.2010.23±0.03730.152,4-二叔丁基酚C14H22O206.320.71±0.020.43±0.030.11±0.0182,6-二叔丁基-4-甲基苯酚C15H24O220.3500.07±0.0115.48正己醛C6H12O100.1600.13±0.020.26±0.021.83±0.0126.41糠醛C5H4O296.080.12±0.032.03±0.121.29±0.0639.113-甲硫基丙醛C4H8OS104.170.67±0.03410.98(E)-2-庚烯醛C7H12O112.1700.10±0.1511.10苯甲醛C7H6O106.1220.43±0.020.15±0.010.36±0.020.66±0.02醛类614.26苯乙醛C8H8O120.150.22±0.010.35±0.02716.65十一醛C11H22O170.292.97±0.11816.72壬醛C9H18O142.240.69±0.020.31±0.02918.33香茅醛C10H18O154.250.38±0.021021.49柠檬醛C10H16O152.2318.29±0.150.31±0.021124.212,4-癸二烯醛C10H16O152.230.11±0.0211.84乙氧基乙酸C4H8O3104.1001.39±0.0322.01乙酸C2H4O260.0520.34±0.0232.08甲氧基乙酸C3H6O390.081.18±0.0342.522,3-二氢呋喃C4H6O70.090.15±0.0353.31丙酸C3H6O274.0800.60±0.020.58±0.031.54±0.012.78±0.0265.92丁酸C4H8O288.111.33±0.0376.21戊酸C5H10O2102.130.83±0.02酸类87.00异戊酸C5H10O2102.131.21±0.0198.86己酸C6H12O2116.160.35±0.031014.832-羟基-4-甲基戊酸C6H12O3132.1580.08±0.011119.33辛酸C8H16O2144.2110.27±0.021219.74苯甲酸C7H6O2122.126.49±0.021322.56壬酸C9H18O2158.2380.11±0.011425.62脱氢乙酸C8H8O4168.14726.20±0.215.44±0.060.14±0.021525.63异香兰酸C8H8O4168.1516.85±0.09酮类12.003-丁烯-2-酮C4H6O70.095.46±0.0422.174-羟基-2-丁酮C4H8O288.115.00±0.0234.65乙酰丙酮C5H8O2100.120.10±0.0149.312-乙酰基呋喃C6H6O2110.110.07±0.01511.841-辛烯-3-酮C8H14O126.200.65±0.02612.09甲基庚烯酮C8H14O126.1960.12±0.024.37±0.214.73±0.080.47±0.01716.673,5,5-三甲基-2-环戊烯-1-酮C8H12O124.180.54±0.02821.75香芹酮C10H14O150.220.08±0.01927.91β-二氢紫罗兰酮C13H22O194.3130.06±0.011028.37香叶基丙酮C13H22O194.3130.18±0.01
续表1
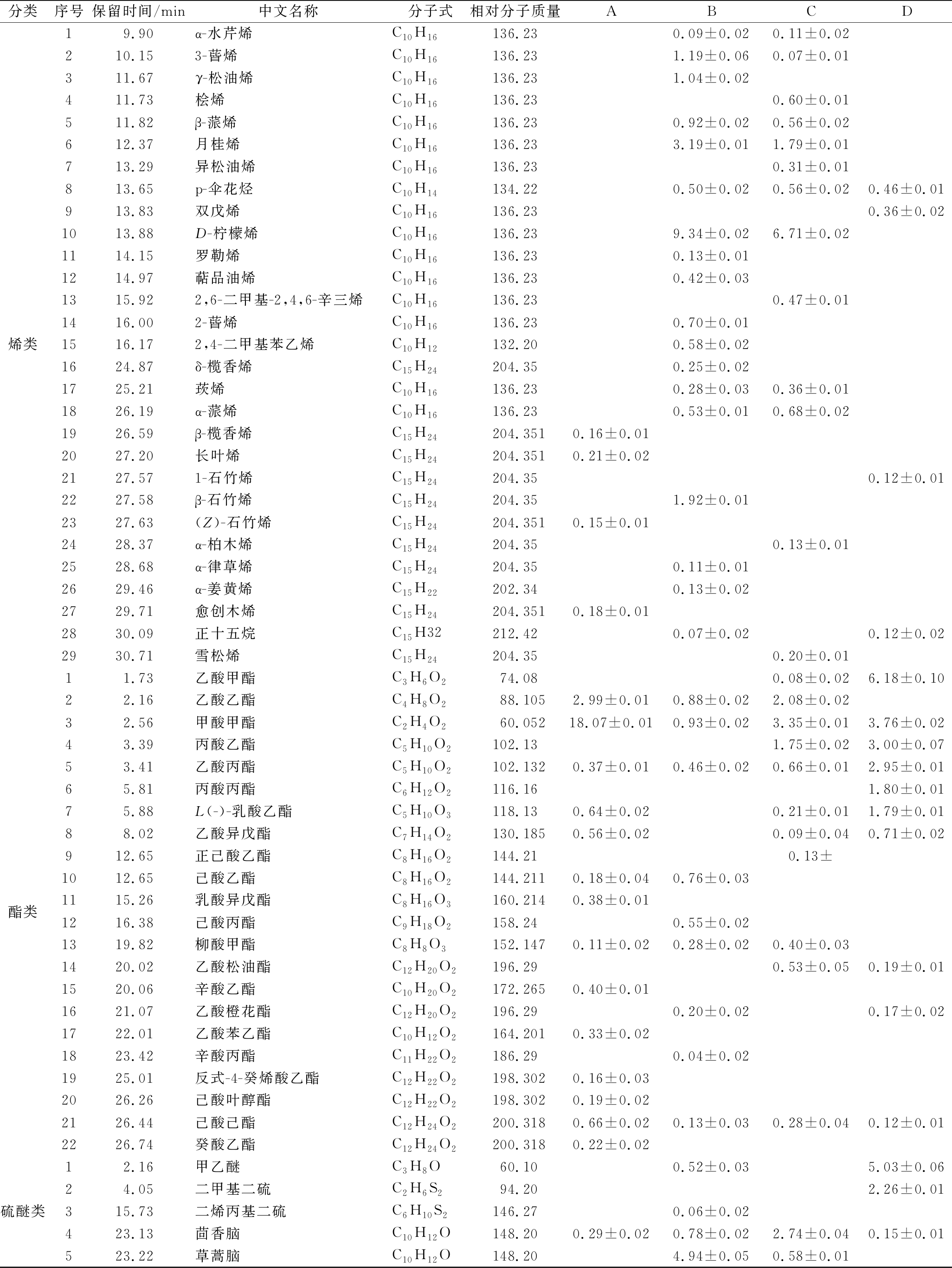
分类序号保留时间/min中文名称分子式相对分子质量ABCD19.90α-水芹烯C10H16136.230.09±0.020.11±0.02210.153-蒈烯C10H16136.231.19±0.060.07±0.01311.67γ-松油烯C10H16136.231.04±0.02411.73桧烯C10H16136.230.60±0.01511.82β-蒎烯C10H16136.230.92±0.020.56±0.02612.37月桂烯C10H16136.233.19±0.011.79±0.01713.29异松油烯C10H16136.230.31±0.01813.65p-伞花烃C10H14134.220.50±0.020.56±0.020.46±0.01913.83双戊烯C10H16136.230.36±0.021013.88D-柠檬烯C10H16136.239.34±0.026.71±0.021114.15罗勒烯C10H16136.230.13±0.011214.97萜品油烯C10H16136.230.42±0.031315.922,6-二甲基-2,4,6-辛三烯C10H16136.230.47±0.011416.002-蒈烯C10H16136.230.70±0.01烯类1516.172,4-二甲基苯乙烯C10H12132.200.58±0.021624.87δ-榄香烯C15H24204.350.25±0.021725.21莰烯C10H16136.230.28±0.030.36±0.011826.19α-蒎烯C10H16136.230.53±0.010.68±0.021926.59β-榄香烯C15H24204.3510.16±0.012027.20长叶烯C15H24204.3510.21±0.022127.571-石竹烯C15H24204.350.12±0.012227.58β-石竹烯C15H24204.351.92±0.012327.63(Z)-石竹烯C15H24204.3510.15±0.012428.37α-柏木烯C15H24204.350.13±0.012528.68α-律草烯C15H24204.350.11±0.012629.46α-姜黄烯C15H22202.340.13±0.022729.71愈创木烯C15H24204.3510.18±0.012830.09正十五烷C15H32212.420.07±0.020.12±0.022930.71雪松烯C15H24204.350.20±0.0111.73乙酸甲酯C3H6O274.080.08±0.026.18±0.1022.16乙酸乙酯C4H8O288.1052.99±0.010.88±0.022.08±0.0232.56甲酸甲酯C2H4O260.05218.07±0.010.93±0.023.35±0.013.76±0.0243.39丙酸乙酯C5H10O2102.131.75±0.023.00±0.0753.41乙酸丙酯C5H10O2102.1320.37±0.010.46±0.020.66±0.012.95±0.0165.81丙酸丙酯C6H12O2116.161.80±0.0175.88L(-)-乳酸乙酯C5H10O3118.130.64±0.020.21±0.011.79±0.0188.02乙酸异戊酯C7H14O2130.1850.56±0.020.09±0.040.71±0.02912.65正己酸乙酯C8H16O2144.210.13±1012.65己酸乙酯C8H16O2144.2110.18±0.040.76±0.03酯类1115.26乳酸异戊酯C8H16O3160.2140.38±0.011216.38己酸丙酯C9H18O2158.240.55±0.021319.82柳酸甲酯C8H8O3152.1470.11±0.020.28±0.020.40±0.031420.02乙酸松油酯C12H20O2196.290.53±0.050.19±0.011520.06辛酸乙酯C10H20O2172.2650.40±0.011621.07乙酸橙花酯C12H20O2196.290.20±0.020.17±0.021722.01乙酸苯乙酯C10H12O2164.2010.33±0.021823.42辛酸丙酯C11H22O2186.290.04±0.021925.01反式-4-癸烯酸乙酯C12H22O2198.3020.16±0.032026.26己酸叶醇酯C12H22O2198.3020.19±0.022126.44己酸己酯C12H24O2200.3180.66±0.020.13±0.030.28±0.040.12±0.012226.74癸酸乙酯C12H24O2200.3180.22±0.0212.16甲乙醚C3H8O60.100.52±0.035.03±0.0624.05二甲基二硫C2H6S294.202.26±0.01硫醚类315.73二烯丙基二硫C6H10S2146.270.06±0.02423.13茴香脑C10H12O148.200.29±0.020.78±0.022.74±0.040.15±0.01523.22草蒿脑C10H12O148.204.94±0.050.58±0.01
4个样品中均检出苯乙醇、芳樟醇、乙醇、苯甲醛、丙酸、甲基庚烯酮、己酸己酯、甲酸甲酯、乙酸丙酯、茴香脑。苯乙醇在A、B、C、D中相对含量分别为1.683%、1.020%、9.837%、0.285%,其具有玫瑰香、茉莉花香,其来源可能是L-苯丙氨酸在酿酒酵母中脱氨酶、脱羧酶和还原酶作用下生产[32]。芳樟醇在A、B、C、D中相对含量分别是8.890%、6.240%、2.910%、0.313%,其具有铃兰与香草香,在果酒[33]、茶叶[34]中均有检出。乙醇相对含量分别为0.835%、0.260%、1.430%、4.536%,其来源于酵母菌在厌氧条件下糖酵解产物,是蔬菜后发酵期重要的呈香物质[35]。甲酸甲酯相对含量分别为18.068%、 0.930%、 3.350%、 3.761%,具有刺激性气味,其在酒类[36]中有检出。
A样品共检出54种物质,相对含量为82.73%;挥发性成分主要以芳樟醇、脱氢乙酸、甲酸甲酯,相对含量分别为8.89%、26.20%、18.07%,脱氢乙酸为红酸汤中添加的防腐剂。B样品中共检出60种挥发性物质,相对含量为89.79%;主要以(S)-顺马鞭草烯醇、芳樟醇、柠檬醛、脱氢乙酸、D-柠檬烯为主,相对含量分别为12.22%、6.24%、18.29%、5.44%、9.34%。(S)-顺马鞭草烯醇可能来源于配料中的木姜子[37],也是葡萄在成熟期形成的品香[38]之一。C样品共检测到51种挥发性物质,相对含量为82.00%;以4-萜烯醇、苯乙醇、苯甲酸、异香兰酸、D-柠檬烯为主,相对含量分别为5.99%、9.83%、6.49%、16.85%、6.71%。4-萜烯醇具有青香、木香和辛香,存在于松节油、薰衣草中,但其阈值较高,对样品香味贡献不大。苯甲酸可能为红酸汤中添加的防腐剂。D-柠檬烯具有鲜橙子香气及柠檬香气[39]。D样品共检测到54种物质,相对含量为75.11%;以3-丁烯-2-酮、甲乙醚为主,相对含量为5.46%、5.03%。表3为红酸汤样品挥发性物质相对含量及种类。
表3 红酸汤样品挥发性成分含量与种类
Table 3 The groups and amounts of volatile compounds in red sore soup sample
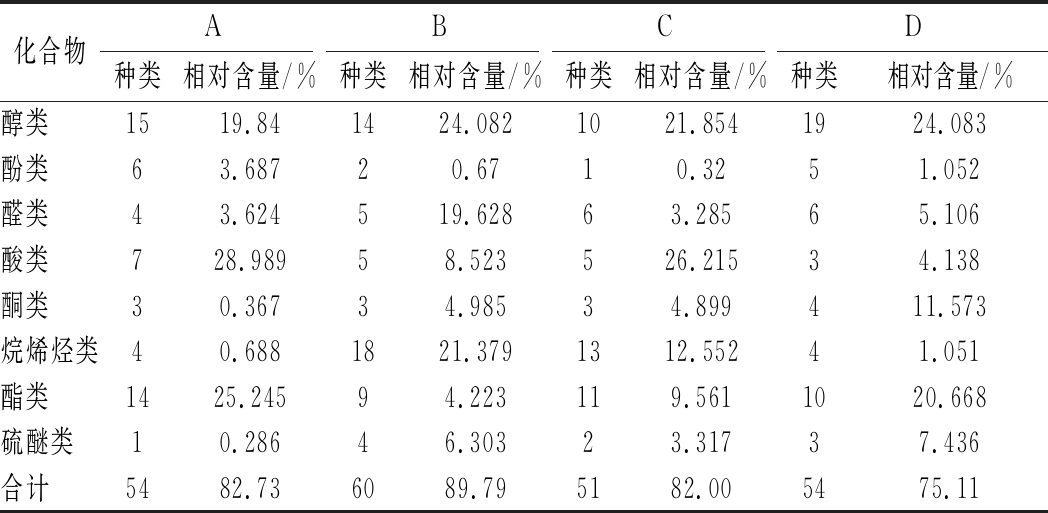
化合物ABCD种类相对含量/%种类相对含量/%种类相对含量/%种类相对含量/%醇类 1519.841424.0821021.8541924.083酚类 63.68720.6710.3251.052醛类 43.624519.62863.28565.106酸类 728.98958.523526.21534.138酮类 30.36734.98534.899411.573烷烯烃类40.6881821.3791312.55241.051酯类 1425.24594.223119.5611020.668硫醚类 10.28646.30323.31737.436合计 5482.736089.795182.005475.11
2.2.2 挥发性物质主成分特征值分析
主成分分析是化学计量学中一种常用的多元统计方法,它通过对原始数据降维处理,将众多相互之间有关联的变量处理成较少的几个不相关的综合指数,提取原始数据最大的几个特征向量作为主成分[40-41]。表4为红酸汤8类挥发性物质主成分特征值及贡献率,表中前3个主成分即可完全反应样品的主要特征信息。
表4 主成分特征值及贡献率
Table 4 Characteristic value and contribution rate of principal components
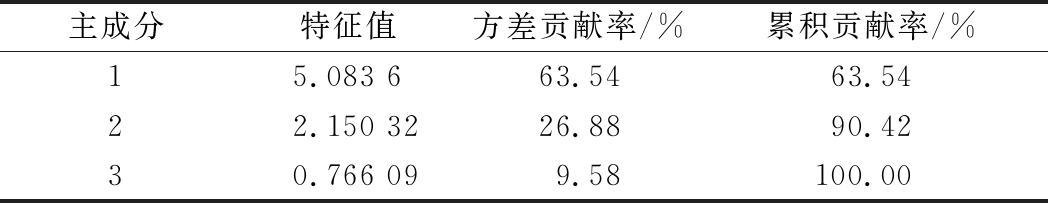
主成分特征值方差贡献率/%累积贡献率/%15.083 663.5463.5422.150 3226.8890.4230.766 099.58100.00
表5为特征向量及载荷分析,载荷分析反映了各类物质对主成分的贡献大小。结合表4、表5分析,第1主成分为63.54%,醇类和硫醚类的载荷系数(分别为0.972、0.933)反映了其对第1主成分的贡献大;第2主成分为26.88%,酮类和烷烯烃类的载荷系数(0.702、0.662)反映了其对第2主成分的贡献,但烷烯烃类与第2主成分呈负相关;酮类和醛类反映了其对第3主成分(9.58%)的贡献。
表5 特征向量及载荷分析
Table 5 Eigenvector and load analysis
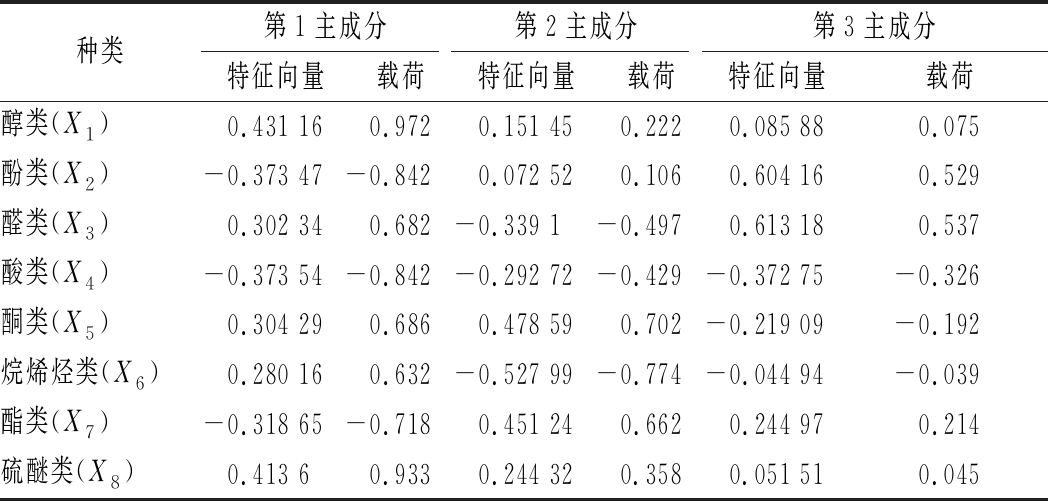
种类第1主成分第2主成分第3主成分特征向量载荷特征向量载荷特征向量载荷醇类(X1)0.431 160.9720.151 450.2220.085 880.075酚类(X2)-0.373 47-0.8420.072 520.1060.604 160.529醛类(X3)0.302 340.682-0.339 1-0.4970.613 180.537酸类(X4)-0.373 54-0.842-0.292 72-0.429-0.372 75-0.326酮类(X5)0.304 290.6860.478 590.702-0.219 09-0.192烷烯烃类(X6)0.280 160.632-0.527 99-0.774-0.044 94-0.039酯类(X7)-0.318 65-0.7180.451 240.6620.244 970.214硫醚类(X8)0.413 60.9330.244 320.3580.051 510.045
2.2.3 建立风味物质分类模型
根据主成分与萃取的特征向量之间的关系,可以得到3个主成分与原变量之间的线性关系,即主成分评分,用T1、T2和T3表示。
T1=0.431 16X1-0.373 47X2+0.302 34X3-0.373 54X4+0.304 29X5+0.280 16X6-0.318 65X7+0.413 6X8;
T2=0.151 45X1+0.072 52X2-0.339 1X3-0.292 72X4+0.478 59X5-0.527 99X6+0.451 24X7+0.244 32X8;
T3=0.085 88X1+0.604 16X2+0.613 18X3-0.372 75X4-0.219 09X5-0.044 94X6+0.244 97X7+0.051 51X8。
以第1、2、3主成分的方差贡献率为权重系数,引入综合评价函数建立红酸汤风味物质识别评价模型。得到T=0.635 4T1+0.268 8T2+9.58T3为综合识别评价模型。表6为综合评分结果。
表6 红酸汤综合评分得分及分类
Table 6 Scores and classification of red sore soup

样品T1T2T3T判别A-10.177 2 4.831 4051.435 586-3.792 65<0B21.651 31-10.911 510.637 7421.015 19>0C3.836 48-4.612 61-4.811 58-3.411 66<0D10.294 4416.907 747.155 5917.940 94>0
由表6可知,B、D综合得分均>0,A、C综合得分均<0。这与电子鼻分析结果一致(B、D较为相似, A、C较为相似)。说明通过对红酸汤挥发性物质种类进行主成分综合评分,可以有效识别4种红酸汤。
3 结论
对4种红酸汤进行电子鼻和气质联用检测,电子鼻检测结果的雷达图与气质联用结合综合评分模型识别结果一致。GC-MS检测结果共鉴定出4种红酸汤141种挥发性物质,主要包括醇类、酚类、醛类、酸类、酮类、烷烯烃类、酯类、硫醚类。A、B、C、D分别检测出54、60、51、54种物质。4个样品均检出的物质有苯乙醇、芳樟醇、乙醇、苯甲醛、丙酸、甲基庚烯酮、己酸己酯、甲酸甲酯、乙酸丙酯、茴香脑,共计10种。GC-MS检测结果结合主成分建立综合评分模型可将样品分成两大类,即A、C为一类,B、D为一类,与电子鼻检测结果一致。不同品牌的红酸汤在气味上差异较大,即使同一产地不同品牌的红酸汤气味也有差异。红酸汤的气味形成是复杂的,这可能与原材料、发酵方式和使用菌种等因素有关。论文从红酸汤的整体风味轮廓和具体风味物质进行了差异分析,建立了红酸汤识别模型,可为不同红酸汤的风味分析提供参考,也可为其他风味食品的鉴别提供参考。
[1] 张璇. 贵州“红酸汤”半成品中微生物区系的研究[D].重庆:西南大学,2011.
[2] 张东亚. 红酸汤发酵工艺优化及品质控制研究[D].贵阳:贵州大学,2018.
[3] 鲁杨. 凯里红酸汤成分及其对大鼠血脂调节作用研究[D]. 贵阳:贵州医科大学,2019.
[4] 邹大维.凯里红酸汤营养成分分析与研究[J].中国调味品,2015,40(5):129-132.
[5] HARTMAN T G, ROSEN R T. Determination of ethyl carbamate in commercial protein based condiment sauces by gas chromatography-mass spectrometry[J]. Journal of Food Safety, 2010, 9(3):173-182.
[6] MURGIA A, SCANO P, CONTU M, et al. Characterization of donkey milk and metabolite profile comparison with human milk and formula milk[J]. LWT - Food Science and Technology, 2016, 74:427-433.
[7] WELDEGERGIS B T,DE VILLIERS A, CROUCH A M. Chemometric investigation of the volatile content of young South African wines [J]. Food Chemistry,2011, 128(4): 1 100-1 109.
[8] QIN Zihan, PANG Xueli,CHEN Dong,et al. Evaluation of Chinese tea by the electronic nose and gas chromatography-mass spectrometry: Correlation with sensory properties and classification according to grade level[J]. Food Research International,2013,53(2):864-874.
[9] KIM H, CADWALLADER K R,KIDO H, et al.Effect of addition of commercial rosemary extracts on potent odorants in cooked beef [J]. Meat Science,2013,94(2):170-176.
[10] XU L, SUN P, YU X, et al. Optimization of processing conditions for five-spice condiment oil based on electronic nose analysis[J]. Food Science, 2014, 35(20): 308-313.
[11] WANG B, XU S Y, SUN D W.Application of the electronic nose to the identification of different milk flavorings[J]. Food Research International, 2010, 43(1):255-262.
[12] LU Lin, SHAO Ping. Classification of rice by combining electronic tongue and nose[J]. Food Analytical Methods, 2015,8(8):1 893-1 902.
[13] 崔琳琳,赵燊,周一鸣,等.基于GC-MS和电子鼻技术的大米挥发性风味成分分析[J].中国粮油学报,2018,33(12):134-141.
[14] 赵阿丹,胡志全,刘友明,等.米茶焙炒挥发性气味的形成与特征研究[J].中国粮油学报,2016,31(3):1-6.
[15] MISHARINA T A, MUKHUTDINOVA S M, ZHARIKOVA G G, et al. Formation of flavor of dry champignons (Agaricus bisporus L.)[J]. Prikl Biokhim Mikrobiol, 2010,46(1):119-124.
[16] ZHANG Shujuan,PETERSEN M A,LIU J, et al. Influence of pre-fermentation treatments on wine volatile and sensory profile of the new disease tolerant cultivar solaris[J]. Molecules, 2015, 20(12): 21 609-21 625.
![]() CARBONELL M, GAYA P, et al. Evolution of the volatile components of ewes raw milk Zamorano cheese. Seasonal variation[J]. International Dairy Journal, 2004, 14(8):701-711.
CARBONELL M, GAYA P, et al. Evolution of the volatile components of ewes raw milk Zamorano cheese. Seasonal variation[J]. International Dairy Journal, 2004, 14(8):701-711.
[18] FSHAHIDI. Flavor of Meat,Meat Products and Seafoods[M]. London:Blackie Academic & Professional,1998:159-190.
[19] WHITFIELD F B. Volatiles from interactions of MailIard reactions and lipids[J]. Critical Reviews in Food Science and Nutrition, 1992, 31(1-2):1-58.
[20] WIDJAJA R, CRASKE J D, WOOTTON M. Comparative studies on volatile components of non-fragrant and fragrant rices[J]. Journal of the Science of Food and Agriculture, 1996, 70(2):151-161.
[21] VENTANAS J, C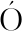 RDOBA J J, ANTEQUERA T, et al. Hydrolysis and Maillard reactions during ripening of Iberian ham[J]. Journal of Food Science, 2010, 57(4):813-815.
RDOBA J J, ANTEQUERA T, et al. Hydrolysis and Maillard reactions during ripening of Iberian ham[J]. Journal of Food Science, 2010, 57(4):813-815.
[22] RANNOU C, TEXIER F, MOREAU M, et al. Odour quality of spraydried hens’ egg powders: The influence of composition, processing and storage conditions[J]. Food Chemistry, 2013, 138(2-3): 905-914.
[23] TOMAC A, COVA M C, NARVAIZ P, et al. Texture, color, lipid oxidation and sensory acceptability of γ-irradiated marinated anchovy fillets[J]. Radiation Physics and Chemistry, 2015, 106: 337-342.
[24] 徐丹萍,过雯婷,郑振霄,等.干贝的营养评价与关键风味成分分析[J].中国食品学报,2016,16(12):218-226.
[25] 陆宽, 王雪雅, 孙小静,等. 电子鼻结合顶空SPME-GC-MS联用技术分析贵州不同品种辣椒发酵后挥发性成分[J]. 食品科学, 2018,39(4):199-205.
[26] KEENAN D F, BRUNTON N P, MITCHELL M, et al. Flavour profiling of fresh and processed fruit smoothies by instrumental and sensory analysis[J]. Food Research International, 2012, 45(1): 17-25.
[27] 唐鑫, 夏延斌, 吴灿. 辣椒汁发酵过程中挥发性成分的变化[J].食品科学, 2014,35(16): 197-201.
[28] 韩江雪, 丁筑红, 李仲军, 等. 不同乳酸菌强化接种发酵辣椒挥发性风味成分分析[J]. 食品科学, 2012, 33(10): 179-183.
[29] 曹雪丹, 方修贵, 赵凯. 椪柑果醋液态发酵工艺及香气成分的GC-MS分析[J]. 中国食品学报, 2015, 15(5):105-112.
[30] 田怀香,吴譞,秦蓝,等.基于GC-MS和GC-O的调味品鸡精特征风味物质研究[J].现代食品科技,2016,32(9):287-294;185.
[31] 李婷婷, 郑炯. 顶空-固相微萃取-气质联用分析泡蒜中的挥发性成分[J]. 食品与发酵工业, 2014,40(5):206-209;215.
[32] 范文来,徐岩.酒类风味化学[M].北京中国轻工业出版社, 2014:110-119.
[33] RIBEREAU-GAYON P, BOIDRON J N, TERRIER A. Aroma of Muscat grape varieties[J]. Journal of Agricultural and Food Chemistry, 1975, 23(6):1 042-1 047.
[34] 刘盼盼, 许勇泉, 尹军峰, 等.主要水质因子对清香型黄山毛峰茶挥发性成分的影响[J].中国食品学报,2016,16(1):245-257.
[35] ATANASOVA-GORANOVA V K, DIMOVA P I, PEVICHAROVA G T. Effect of food products on endogenous generation of N-nitrosamines in rats[J]. British Journal of Nutrition, 1997, 78(2):335-345.
[36] SAVCHUK S A, KOLESOV G M. Chromatographic techniques in the quality control of cognacs and cognac spirits[J]. Journal of Analytical Chemistry, 2005, 60(8):752-771.
[37] 董钟. 木姜子精油成分分析及生物活性研究[D].武汉:武汉轻工大学,2017.
[38] 陈芳, 张晓旭, 杨晓, 等. 威代尔葡萄成熟及后熟过程中游离态萜烯类香气的变化[J]. 中国食品学报, 2010, 10(6):187-192.
[39] DHARMAWAN J, KASAPIS S, CURRAN P. Characterization of volatile compounds in selected citrus fruits from Asia. Part I: freshly squeezed juice[J]. Flavour and Fragrance Journal, 2007, 42(22):228-232.
![]() M, LOJEN S, et al. Determination of geographical origin of commercial tomato through analysis of stable isotopes, elemental composition and chemical markers[J]. Food Control, 2018, 89: 133-141.
M, LOJEN S, et al. Determination of geographical origin of commercial tomato through analysis of stable isotopes, elemental composition and chemical markers[J]. Food Control, 2018, 89: 133-141.
[41] MARENGO E, ROBOTTI E, RIGHETTI P G, et al. Study of proteomic changes associated with healthy and tumoral murine samples in neuroblastoma by principal component analysis and classification methods[J]. Clinica Chimica Acta, 2004, 345(1-2): 55-67.