冠突散囊菌[1-2]又称金花菌,因其在茯砖茶中可形成颗粒饱满的子囊果[3-5],类似金花而得名。冠突散囊菌的生长状况是评价茯砖茶品质的理化指标之一,已列入国家标准。且前研究表明,茯砖茶具有多种功效,包括抗氧化、降血脂和降血糖等[6-11]。在茯砖茶发花过程中,冠突散囊菌大量生长[12-14],其他微生物受到一定的抑制,提示冠突囊菌在生长阶段产生具有抑菌活性的物质;同时长期保存的茯砖茶较少出现杂菌污染的情况,提示茯砖茶中的金花可持续提供抑菌物质。目前已证实金花菌发酵液有一定的抑菌活性[15-16],其提取物对金黄色葡萄球菌、大肠杆菌、沙门氏杆菌、枯草芽孢杆菌与白色链霉菌有抑制作用。现有文献大都集中在金花菌发酵液和茯砖茶[17-20]的抑菌效果研究,但对冠突散囊菌的繁殖体(子囊果、子囊孢子和分生孢子)提取物抑菌活性的研究较少。本论文采用玻璃珠振摇法破碎金花菌繁殖体,获得相应提取物,探讨其对金黄色葡萄球菌、藤黄微球菌、大肠杆菌、枯草芽孢杆菌、白色链霉菌和白色念珠菌的抑菌活性,同时为茯砖茶较难染菌,金花菌天然抗菌剂的开发和利用提供数据参考。
1 材料与方法
1.1 菌种来源
冠突散囊菌(JH1205)由黑茶金花湖南省重点实验室提供。
1.2 设备与试剂
BBS-DDC超净工作台,山东博科;HWS-100F恒温培养箱,上海丙林;R-3001旋转蒸发仪,郑州长城科工;YKW-303台式恒温振荡器,上海程造;BKQ-Z30I立式压力蒸汽灭菌锅,山东博科。
琼脂(不含抗生素)、蔗糖、NaCl、蛋白胨、土豆等(除蛋白胨,土豆外均为分析纯)。
1.3 实验方法
1.3.1 冠突散囊菌中子囊果与分生孢子的获得
子囊果的获得:分别将制备好的金花散茶和储存6年的金花散茶过100目筛,筛选分离获得。
参照刘作易等的研究[21],微调冠突散囊菌产分生孢子的条件,在高渗液体培养基中接种金花菌孢子悬液,于36 ℃静置培养4 d,再用无菌水冲洗菌膜上的分生孢子,获得冠突散囊菌分生孢子悬液;高渗培养基为添加10%(质量分数)NaCl和20%(质量分数)蔗糖的PDA培养基。
1.3.2 冠突散囊菌中子囊果、子囊孢子与分生孢子中抑菌物质的提取
子囊果中抑菌物质的提取:称2 g子囊果装入锥形瓶中,加30 mL 蒸馏水和玻璃珠若干(玻璃珠铺满瓶底),置于180 r/min摇床中振摇120 min。将破碎后的子囊果溶液在4 000 r/min的条件下离心10 min,保留上清液(此为子囊果提取物);将沉淀物用蒸馏水清洗后,加蒸馏水溶解制成悬浊液,再用4层纱布过滤获得子囊孢子悬浊液,调节子囊孢子浓度为10-7个/mL,加入玻璃珠后置于-18 ℃冰箱冷冻1 d,再60 ℃水浴加热1.5 h,取出置于180 r/min摇床中振摇10 h,4 000 r/min离心10 min,保留上清液(此为子囊孢子提取物)。
分生孢子中抑菌活性物质的提取:提取方法和子囊孢子中活性物质的提取一致。
所有提取物浓缩至100 mg/mL进行抑菌实验。
1.3.3 抑菌实验
将灭菌后的滤纸片浸入浓缩后的提取物中,浸泡15 min,沥干,置于涂布有0.3 mL供试菌(新鲜培养菌种,OD值为0.4)的BL(基础培养基)平板中,恒温培养24 h后测量抑菌圈的大小,平行测定3次。供试菌为金黄色葡萄球菌、藤黄微球菌、大肠杆菌、枯草芽孢杆菌,此4种菌培养温度为37 ℃;白色念珠菌和白色链霉菌,此2种菌培养温度为30 ℃。
1.3.4 稳定性实验
1.3.4.1 温度稳定性
取适量子囊果提取物,分别置于室温(25 ℃)、40、60、80、100、121 ℃下分别处理1 h,冷却至室温后,以未处理的样品为对照,以金黄色葡萄球菌和大肠杆菌作为供试菌,用1.3.3中方法验证其抑菌活性的变化,每个处理重复3次,将平板置于37 ℃恒温培养24 h后测量抑菌圈半径。
1.3.4.2 pH值稳定性
取适量子囊果提取物,采用1 mol/L HCl溶液和NaOH溶液分别调pH值至2、4、6、8、10,放置2 h,以未处理的样品为对照,以金黄色葡萄球菌和大肠杆菌作为供试菌,用1.3.3方法验证其抑菌活性的变化,每个处理重复3次,将平板置于37 ℃恒温培养24 h后测量抑菌圈半径。
1.3.4.3 紫外光稳定性
取适量子囊果提取物,置于30 W紫外灯下,距离30 cm,照射发酵液浓缩液1、2、3、4、5 h,以未处理的样品为对照,以金黄色葡萄球菌和大肠杆菌作为供试菌,用1.3.3中方法验证其抑菌活性的变化,每个处理重复3次,将平板置于37 ℃恒温培养24 h后测量抑菌圈半径。
1.3.5 冠突散囊菌子囊果提取物不同浓度下的抑菌实验
按1.3.3中所述实验方法,将浸泡不同浓度子囊果提取物的滤纸片,置于涂布有0.3 mL供试菌的BL培养基平板中,37 ℃恒温培养24 h后测量抑菌圈的大小,平行测定3次。供试菌为金黄色葡萄球菌和大肠杆菌。
2 结果与分析
2.1 冠突散囊菌观察
按1.3.1中实验方案分离得到冠突散囊菌的子囊果、子囊孢子和分生孢子,并进行观察,结果如图1所示。冠突散囊菌的繁殖方式分为无性繁殖和有性繁殖2种方式,有性繁殖时产生大量黄色闭囊壳(子囊果),外表缠绕有大量营养菌丝,子囊果破裂,释放子囊孢子;无性繁殖时只产生分生孢子。在普通培养基中,冠突散囊菌进行有性繁殖,形成表面粗糙而致密的金黄色菌膜(图1-a);在高渗液体培养基中,冠突散囊菌进行无性繁殖,生成紧致而细密的灰白色菌膜,表面相对有性型较为光滑(图1-b)。冠突散囊菌在茶叶基质中,以有性繁殖为主,在茶叶基质表面形成大量的金黄色颗粒,此为冠突散囊菌的子囊果(图1-c)。从液体培养基上的菌膜颜色,即可区分冠突散囊菌的繁殖方式。光镜观察下,子囊孢子与分生孢子形态基本一致,均为球形或椭球形(图1-d、图1-e)。
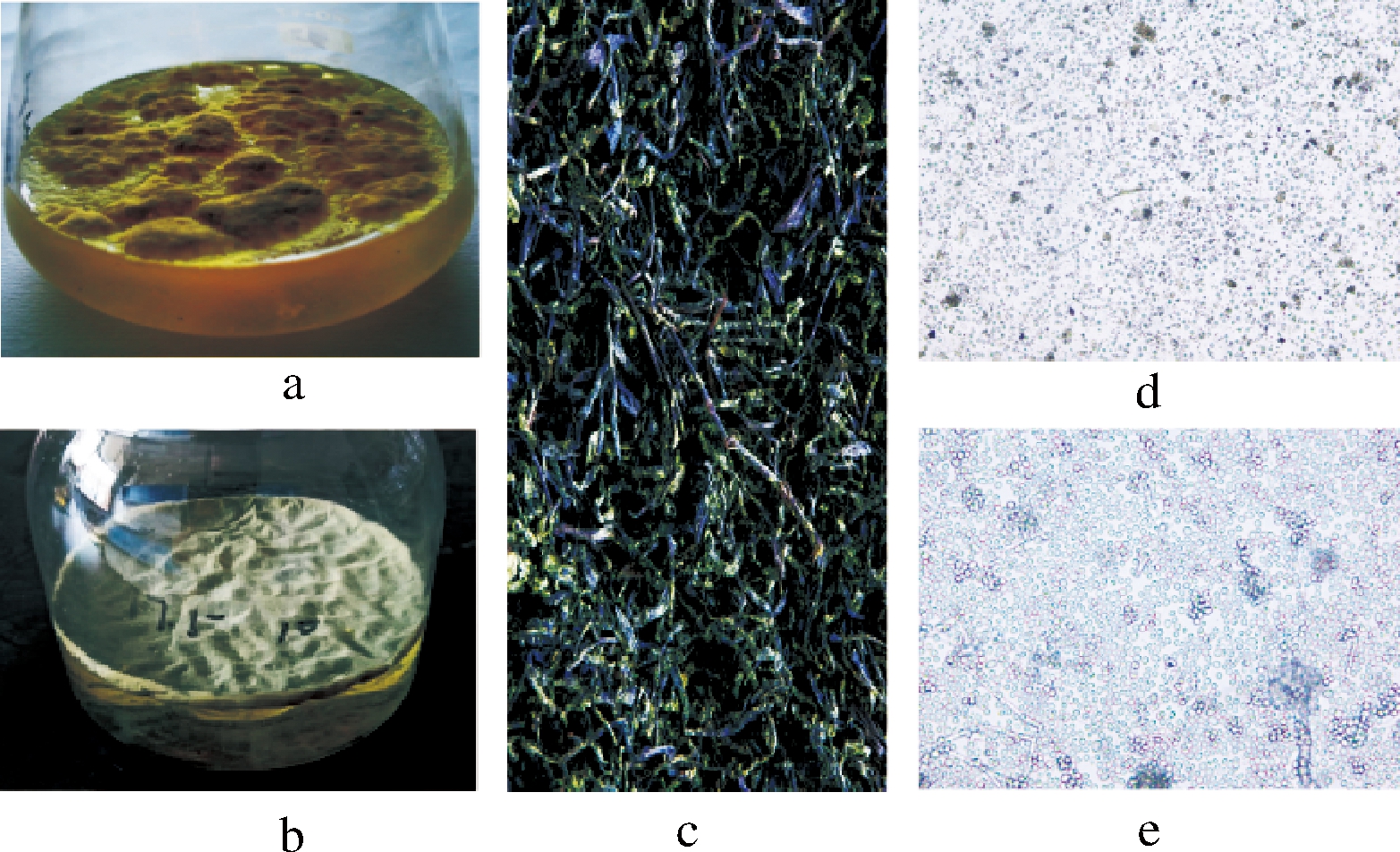
a-有性菌体(子囊果);b-无性菌体(分生孢子);c-长满子囊果的散茶;d-光镜下子囊孢子;e-光镜下分生孢子
图1 冠突散囊菌不同繁殖体图片
Fig.1 The picture of eurotium cristatum propagule
2.2 冠突散囊菌子囊果、子囊孢子和分生孢子提取物的抑菌活性
由表1可知,冠突散囊菌的无性繁殖体和有性繁殖体的提取物表现出截然不同的抑菌活性,无性繁殖体(分生孢子)提取物对6种供试菌均未检测到抑菌活性,而有性繁殖体子囊果和子囊孢子提取物,具有明显的抑菌活性。子囊果提取物和子囊孢子提取物对6种供试菌的抑菌能力有所差别,其中子囊果提取物的抑菌效果更好,例如子囊果提取物对金黄色葡萄球菌的抑菌全半径最大可达到5.8 mm,子囊孢子对其抑菌圈半径为2.7 mm。
表1 子囊果、子囊孢子及分生孢子提取物对供试菌的抑菌圈半径 单位:mm
Table 1 Antibacterial activities of ascocarp, ascospore and conidium extract
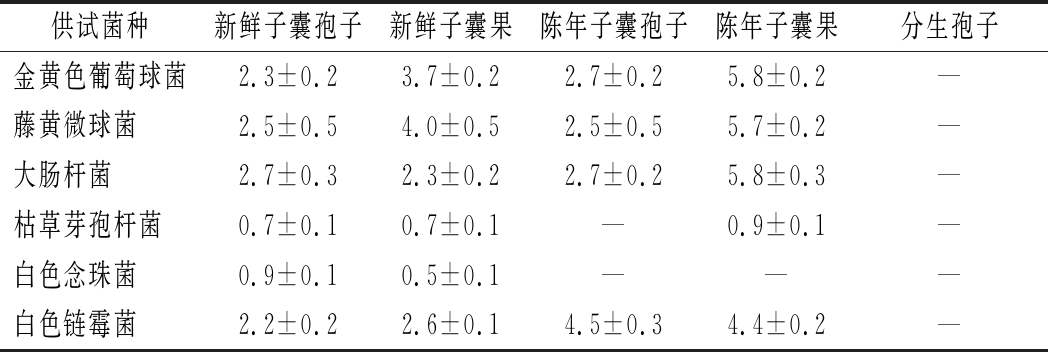
供试菌种新鲜子囊孢子新鲜子囊果陈年子囊孢子陈年子囊果分生孢子金黄色葡萄球菌2.3±0.23.7±0.22.7±0.25.8±0.2—藤黄微球菌 2.5±0.54.0±0.52.5±0.55.7±0.2—大肠杆菌 2.7±0.32.3±0.22.7±0.25.8±0.3—枯草芽孢杆菌 0.7±0.10.7±0.1—0.9±0.1—白色念珠菌 0.9±0.10.5±0.1———白色链霉菌 2.2±0.22.6±0.14.5±0.34.4±0.2—
注:“—”代表未检测到抑菌圈
子囊果和子囊孢子提取物对不同微生物的抑制作用有很大区别,对金黄色葡萄球菌、藤黄微球菌、白色链霉菌和大肠杆菌的抑制效果最好;对枯草芽孢杆菌和白色念珠菌的抑制效果较弱。金黄色葡萄球菌、藤黄微球菌和枯草芽孢杆菌均为革兰氏阳性菌,枯草芽孢杆菌的抑菌圈半径最大为0.9 mm,而金黄色葡萄球菌和藤黄微球菌的抑菌圈半径最大为5.8 mm;大肠杆菌为革兰氏阴性菌,其最大抑菌圈半径可达5.8 mm,这说明子囊果和子囊孢子提取物的抑菌作用不依赖于微生物细胞壁的组成。
冠突散囊菌子囊果储存时间对其抑菌活性有显著影响。随着储存时间(6年)的延长,子囊孢子提取物对金黄色葡萄球菌、藤黄微球菌和大肠杆菌的抑制作用基本不变,但对白色链霉菌的抑制作用增强了2倍(抑菌圈半径从2.2 mm增加至4.5 mm),对枯草芽孢杆菌和白色念珠菌的抑制作用则消失。除了白色念珠菌,陈年子囊果的提取物对其余5种供试菌的抑菌活性均比新鲜子囊果提取物的抑菌活性更强,这说明在长时间的储存过程中,子囊果中积累了更多或更有效的抑菌活性物质。
2.3 冠突散囊菌子囊果中抑菌物质的稳定性
2.3.1 热稳定性
由表2可知,经不同温度处理的金花菌子囊果提取物仍对金黄色葡萄球菌和大肠杆菌有抑制作用;随着处理温度的升高,其对金黄色葡萄球菌的抑制作用逐渐降低,且降低幅度较大,当121 ℃处理1 h后,其抑菌圈半径从6.0 mm降低到1.5 mm,降低幅度为75%。随着温度的升高,子囊果提取物对大肠杆菌的抑制作用也有所降低,但相对于金黄色葡萄球菌,其降低幅度更小(抑菌圈半径从4.7 mm降低到2.4 mm,降低幅度为49%),这说明金花菌子囊果中可抑制大肠杆菌的物质具有更好的热稳定性。
表2 金花菌子囊果提取物的热稳定性 单位:mm
Table 2 Effect of temperature on the antimicrobial activities of ascocarp extract

组别25 ℃(对照)40 ℃60 ℃80 ℃100 ℃121 ℃对金黄色葡萄球菌抑菌圈6.0±0.55.2±0.23.5±0.52.5±0.32.2±0.21.5±0.5对大肠杆菌抑菌圈 4.7±0.23.0±0.12.5±0.22.4±0.22.7±0.22.7±0.3
2.3.2 酸碱稳定性
金花菌子囊果提取物初始 pH值为6,其对金黄色葡萄球菌的抑菌圈直径为5.7 mm,对大肠杆菌的抑菌圈直径为3.5 mm,由表3可知,经过不同pH值的酸碱处理后,金花菌子囊果提取物仍对大肠杆菌有抑制作用;仅在酸性条件下,对金黄色葡萄球菌有抑制作用。pH值为4 时,对金黄色葡萄球菌和大肠杆菌的抑菌圈直径均为最大,说明在pH 值低于原液的酸性条件下,其中的抑菌物质作用随pH 值降低而明显增强。金花菌子囊果提取物中对金黄色葡萄球菌有抑制作用的物质具有一定的耐酸能力,耐碱能力弱。
表3 金花菌子囊果提取物的酸碱稳定性 单位:mm
Table 3 Effect of pH value on the antimicrobial activities of ascocarp extract

组别246(对照)810对金黄色葡萄球菌抑菌圈10.5±0.513.5±0.55.7±0.2——对大肠杆菌抑菌圈 4.5±0.54.7±0.43.5±0.52.2±0.22.5±0.5
注:“—”表示未检测到抑菌圈
pH为2的子囊果提取物对大肠杆菌的抑菌圈直径为对照组的1.29倍,pH为4的子囊果提取物对大肠杆菌的抑菌圈直径为对照组的1.34 倍,说明在pH 值低于原液的酸性条件下,其中对大肠杆菌的抑菌物质作用有所增强,当pH 值<4 时,抑菌作用亦随pH 值降低而减弱;在碱性条件下,其抑菌作用减弱,由此可见,金花菌子囊果提取物中对大肠杆菌有抑制作用的物质具有一定的耐酸碱能力,有较强的耐酸能力。
2.3.3 紫外光稳定性
由表4可知,金花菌子囊果提取物经过不同时间紫外光照射后,其对金黄色葡萄球菌和大肠杆菌的抑制作用的变化有所不同。对于金黄色葡萄球菌,在紫外线照射子囊果提取物2 h后,其抑菌活性开始下降,但随着照射时间继续延长至5 h,其抑菌活性无明显的降低,表明子囊果提取物中能抑制金黄色葡萄球菌生长的物质具有一定的紫外线稳定性。
表4 金花菌子囊果提取物的紫外光稳定性 单位:mm
Table 4 Effect of ultraviolet light on the antimicrobial activities of ascocarp extract

组别0 h(对照)1 h2 h3 h4 h5 h对金黄色葡萄球菌抑菌圈3.5±0.54.5±0.22.8±0.12.3±0.12.2±0.22.5±0.5对大肠杆菌抑菌圈 4.1±0.24.5±0.15.2±0.25.0±0.13.7±0.23.5±0.3
对于大肠杆菌,在紫外线照射子囊果提取物4 h后,其抑菌活性开始下降,再继续延长照射时间至5 h,其抑菌活性基本不变,表明子囊果提取物中能抑制大肠杆菌生长的物质比抑制黄色葡萄球菌生长的物质,具有更好的紫外线稳定性。
2.3.4 冠突散囊菌子囊果提取物不同质量浓度下的抑菌效果
图2为冠突散囊菌子囊果提取物不同质量浓度时,对金黄色葡萄球菌和大肠杆菌的抑制作用,由图2可知,随着提取物质量浓度的降低,所测得抑菌圈半径越来越小,说明抑菌效果越来越差。当提取物质量浓度降低至20 mg/mL,抑菌圈消失,这说明用冠突散囊菌子囊果提取物做抑菌剂时,需调节其质量浓度>20 mg/mL。
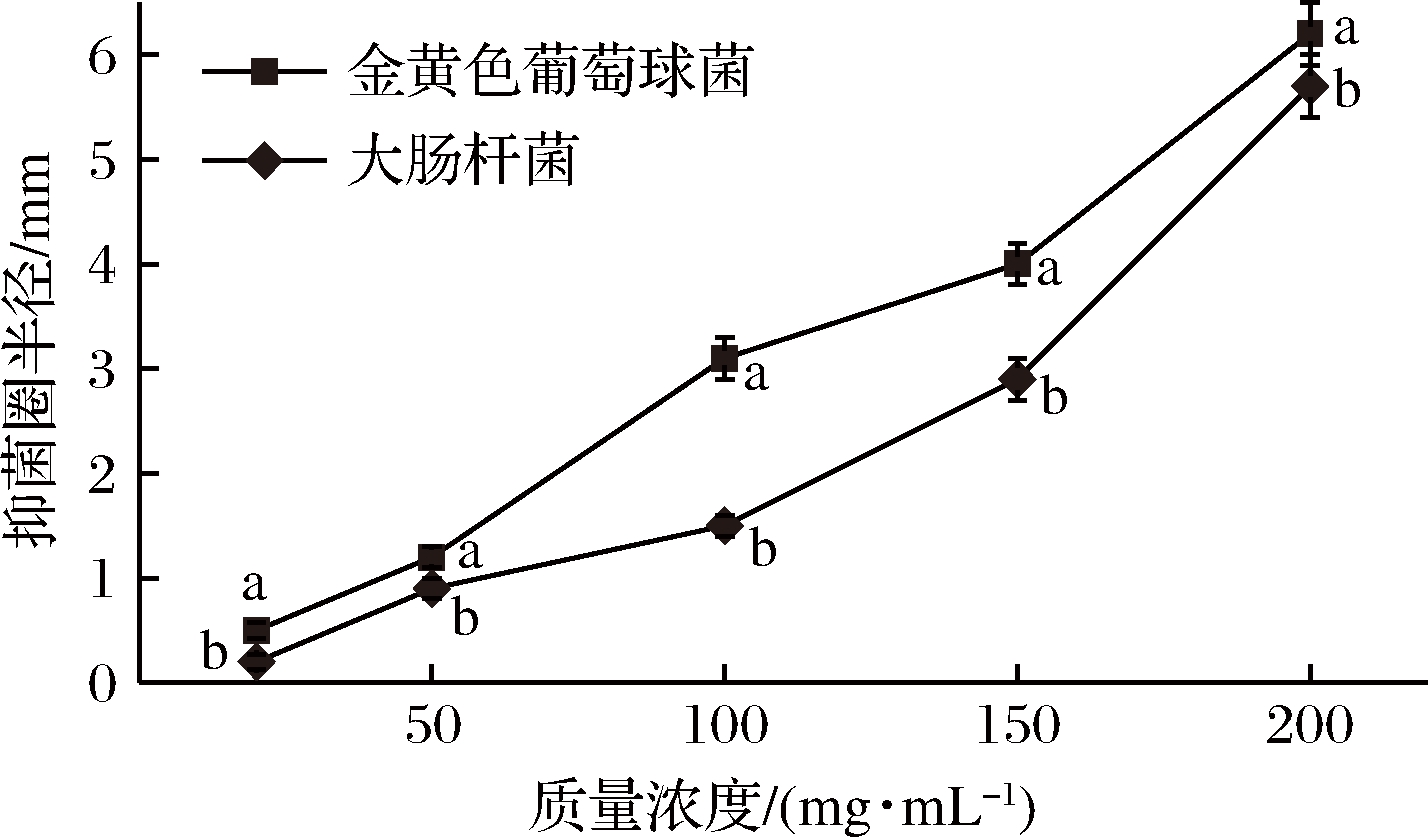
图2 冠突散囊菌子囊果提取物对金黄色葡萄糖球菌和大肠杆菌的抑菌圈半径
Fig.2 The radius of inhibition cycle of Eurotium cristatum extract on Escherichia coli and Staphylococcus aureus
3 结论
本文研究了冠突散囊菌繁殖体中提取物质的抑菌活性,发现其有性繁殖体(子囊果和子囊孢子)提取物对细菌、真菌、放线菌有抑制作用,其中对金黄色葡萄球菌、藤黄微球菌和大肠杆菌的抑制效果最好;无性繁殖体(分生孢子)提取物未检测到抑菌活性。子囊果提取物的抑菌活性强于子囊孢子提取物;随着储存时间的增加,子囊果中提取物的抑菌活性得到增强,子囊孢子中提取物的抑菌活性基本不变。研究还表明,抑菌物质有良好的紫外线稳定性和一定的热稳定性,在酸性条件下抑菌物质的抑菌活性保持不变,甚至增强,这有利于抑菌物质添加在果汁等酸性饮料中,有利于用于酸性饮料的冠突散囊菌天然防腐剂应用开发。
[1] 张海艳. 冠突散囊菌在发酵茶中的应用研究进展[J]. 黑龙江科学, 2018, 9(22): 30-31.
[2] 郑梦霞, 李会娟, 陈淑娜, 等. 冠突散囊菌发酵对茶汤香气成分的影响[J]. 食品科学, 2019, 40(18): 223-228.
[3] 叶聿程. 茯砖茶中冠突散囊菌的研究进展[J]. 生物技术世界, 2014 (9): 64.
[4] 王玉臣, 谭玉梅, 刘作易, 等. 冠突散囊菌有性产孢相关基因的生物信息学分析[J]. 贵州农业科学, 2014, 42(10): 32-36.
[5] 陈桂梅. 冠突散囊菌研究进展[J]. 西北农林科技大学学报(自然科学版), 2012, 40(3): 179-184.
[6] 曾桥, 韦承伯, 缑会莉, 等. 杜仲叶茯砖茶多糖提取工艺优化及抗氧化降血脂活性[J]. 食品科技, 2018, 43(8): 184-192.
[7] 韩卓潇, 黄亚亚, 梁艳, 等. 茯砖茶降脂功能及主要降脂活性物质研究进展[J]. 广东茶业, 2017 (4): 6-11.
[8] 王茹茹, 肖孟超, 李大祥, 等. 黑茶品质特征及其健康功效研究进展[J]. 茶叶科学, 2018, 38(2): 113-124.
[9] 吴凯为, 杨立娜, 朱力杰, 等. 冠突散囊菌在发酵茶中应用的研究进展[J]. 食品研究与开发, 2018, 39(1): 189-193.
[10] 覃金球, 罗美玲, 张旋, 等. 冠突散囊菌医药价值研究进展[J]. 食品工业科技, 2018, 39(24): 336-339.
[11] 刘婷, 李颂, 张赓, 等. 冠突散囊菌和茯砖茶的健康功效[J]. 食品研究与开发, 2016, 37(5): 208-212.
[12] 吕嘉枥, 杨柳青, 孟雁南. 茯砖茶中金花菌群的研究进展[J]. 食品科学,2020,41(9):316-322.
[13] 孟雁南. 陕西茯砖茶优势菌群及其功能性研究[D]. 西安:陕西科技大学, 2019.
[14] 张亚, 黄亚亚, 韩卓潇, 等. 微型茯砖茶加工及“金花”菌鉴定[J]. 食品科技, 2018, 43(7): 116-122.
[15] 张芳芳, 刘飞, 袁超, 等. 冠突散囊菌发酵产物的抑菌作用及特性研究[J]. 食品与药品, 2019, 21(1): 62-65.
[16] 李佳莲, 胡博涵, 赵勇彪, 等. 冠突散囊菌发酵液的抑菌作用[J]. 食品科学, 2011, 32(11): 157-160.
[17] 傅冬和, 余智勇, 黄建安, 等. 不同年份茯砖茶水提取物的抑菌效果研究[J]. 中国茶叶, 2011, 33(1): 10-12.
[18] AMY C K, TIFFANY L W, COREY D B, et al. Antibacterial activity and phytochemical profile of fermented Camellia sinensis (fuzhuan tea)[J]. Food Research International, 2013, 53(2): 945-949.
[19] 许靖逸, 崔修丹, 陈昌辉, 等. 六大茶类对部分肠道致病菌抑菌效果的研究[J]. 食品工业科技, 2013, 34(16): 140-142.
[20] 彭影琦, 龙军, 林玲, 等. 相同加工原料下六大茶类抑菌效果比较[J]. 食品与机械, 2017, 33(7): 47-50;76.
[21] 刘作易, 秦京,李乃亮. 茯砖茶“金花”菌—谢瓦氏曲霉间型变种的孢子产生条件[J]. 西南农业学报, 1991(1):75-79.