张家口坝上地区因其优越的地理位置成为我国重要的夏秋错季蔬菜生产基地之一,蔬菜种植面积广,种类多,产量大,出口多,营养价值高,口感好[1-4]。然而无论是外销还是内供蔬菜,大多为毛菜,不但浪费严重,而且食用品质与安全性也较差,净菜加工是解决该问题的有效途径。净菜加工中除机械损伤、生理性衰老、微生物污染、农药残留超标等可导致净菜产品质量下降外,质构劣变以及营养物质损失也是影响净菜产品质量的原因。
清洗是净菜加工的关键环节之一,对蔬菜的品质至关重要[5]。清洗方式可分为水流式、气泡式、超声波、超静压等物理方式,以及用弱酸性的消毒剂或碱性化学试剂等的化学方式,常用清洗剂有NaClO、ClO2、CH3COOOH、H2O2、NaOH、NaCl、O3等[6-10]。以上清洗方式在去除蔬菜表面有害杂质的同时,会不同程度地影响净菜产品的感官与营养品质,部分化学试剂残留还会对人体健康造成危害[11-12]。梁东妮等[13]研究表明,经过过氧化氢处理,大白菜感官品质较差,维生素C(VC)流失严重;侯田莹等[14]研究发现,次氯酸钠清洗效果较好,但由于有余氯,不仅会有残留的臭气,还可能形成“三致”物质。
电生功能水(electrolyzed functional water,EFW)又称电解水或离子水,是将水在一种特殊装置中经电场处理后,使水的pH值、氧化还原电位(oxidation-reduction potential,ORP)、有效氯含量(available chlorine content,ACC)等指标发生改变而产生的具有特殊功能的酸性离子水(acid electrolyzed water,AcEW)和碱性离子水(alkaline electrolyzed water,AlEW)的总称[15-18]。近年来,EFW清洗技术被应用于净菜加工的相关研究,EFW可有效去除蔬菜表面大部分农药残留,无毒无副作用,而且易制取、成本低,且有利于保持蔬菜的质构和营养品质[19-25]。
在前期对EFW去除张家口坝上地区甘蓝、西兰花、彩椒3种特色蔬菜中甲拌磷、毒死蜱、高效氯氟氰菊酯、氟氯氰菊酯、腐霉利、百菌清6种农药残留规律研究的基础上,本实验继续探究EFW对甘蓝、西兰花、彩椒质构特性以及营养成分含量的影响,以确定EFW净菜加工清洗条件,为提高净菜产品安全、营养、感官品质提供理论依据与技术支撑。
1 材料与方法
1.1 材料与试剂
无水乙醇(95%)、冰乙酸,分析纯,天津市大茂化学试剂厂;磷酸(98%,分析纯),西陇科学股份有限公司;草酸(分析纯),天津市化学试剂供销公司;盐酸(分析纯),永飞化学试剂有限公司;无水CuSO4、酒石酸钾钠、乙酸锌、亚铁氰化钾、甲基红指示剂,分析纯,天津市风船化学试剂科技有限公司;NaOH(分析纯),天津市天力化学试剂有限公司;Na2CO3(分析纯),天津市永大化学试剂有限公司;2,6-二氯靛酚钠(分析纯),天津市光复精细化学研究所;G-250考马斯亮蓝,上海榕柏生物技术有限公司;牛血清白蛋白(纯度≥99.0%),武汉纯度生物科技有限公司;抗坏血酸标准品(纯度≥99%),上海甄准生物科技有限公司;葡萄糖标准品(纯度≥99%),青岛捷世康生物科技有限公司;亚甲基蓝指示剂,天津市天新精细化工开发中心;甘蓝、西兰花、彩椒,均购自超市;试验用水,如未特殊说明,均为超纯水。
1.2 仪器与设备
Texture Exponent 32 TA.XT plus质地分析仪,英国Stable Micro System公司;XYS-C-12电生功能灭菌水生成器,宝鸡新宇光机电有限责任公司;舜科2000潜水泵,广州世承五金机电有限公司;LE225D精密电子天平,德国sartorius;SHH.W21.600智能恒温水箱,北京市长风仪器仪表公司;Thermo Scientific Heraeus Multifuge X1R离心机,美国Thermo Fisher Scientific公司;Lambda 365紫外可见分光光度计,美国PerkinElmer公司;KQ-500DE数控超声波清洗器,昆山市超声仪器有限公司;XYJ-H帕恩特实验室中央超纯水系统,北京湘顺源科技有限公司;SX721 pH/ORP电位计,上海三信仪表厂。
1.3 实验方法
1.3.1 电生功能水的制备
以0.5 g/L NaCl溶液为电解质,电生功能灭菌水生成器通10.0 V交流电压,电流变化范围为2.8~4.3 A,时间为10 min,制得pH值为(2.9±0.1)、ORP为(1160±10)mV、ACC为(100±10)mg/L的AcEW和pH为(11.4±0.1)、ORP为(-890±10)mV的AlEW。pH值和ORP值用pH/ORP氧化还原电位计检测,ACC采用碘量法滴定测定。低温避光保存,现制现用。
1.3.2 清洗工艺参数
对甘蓝、西兰花、彩椒均分别作0、5、10、15、20、25 min清洗处理,洗后立即测定每种蔬菜质构和营养成分含量,均以鲜重(m鲜)表示。其中0 min为不对蔬菜进行清洗,即对照组。试验重复3次,工艺参数见表1。其中间歇振荡200 r/min,振荡30 s、静置30 s,循环;连续振荡200 r/min。
表1 清洗工艺参数
Table 1 Cleaning process parameters
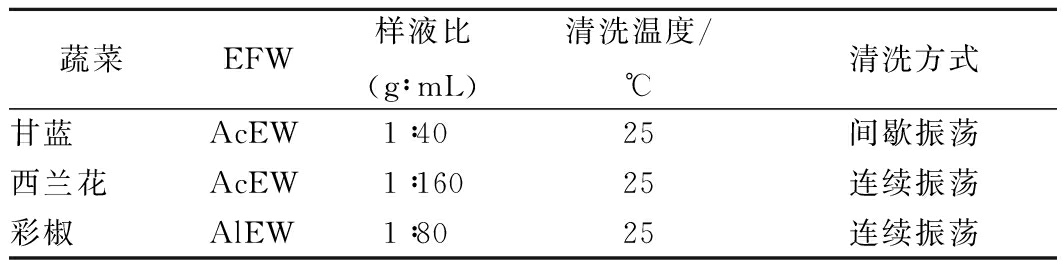
蔬菜EFW样液比(g∶mL)清洗温度/℃清洗方式甘蓝AcEW1∶4025间歇振荡西兰花AcEW1∶16025连续振荡彩椒AlEW1∶8025连续振荡
1.3.3 质构分析与测定
试验中T.A. Settings选择Return To Start模式,采用A/MORS探头,剪切试验模式对甘蓝、西兰花、彩椒进行质构测定,曲线记录方式为Target,测试参数设置见表2。甘蓝测定:分别对叶和茎进行剪切,得平均硬度、紧实度、脆性;西兰花测定:对花、茎进行剪切,得皮硬度、内部平均硬度、紧实度、脆性;彩椒测定:分别对正面(表皮朝上)和反面(表皮朝上)进行剪切,得紧实度、硬度、脆性。试验5次平行,去除偏差较大的数据后取3次平行进行分析,结果以平均值表示。
表2 TA-XT plus 测试参数设置
Table 2 Test parameter of TA-XT plus
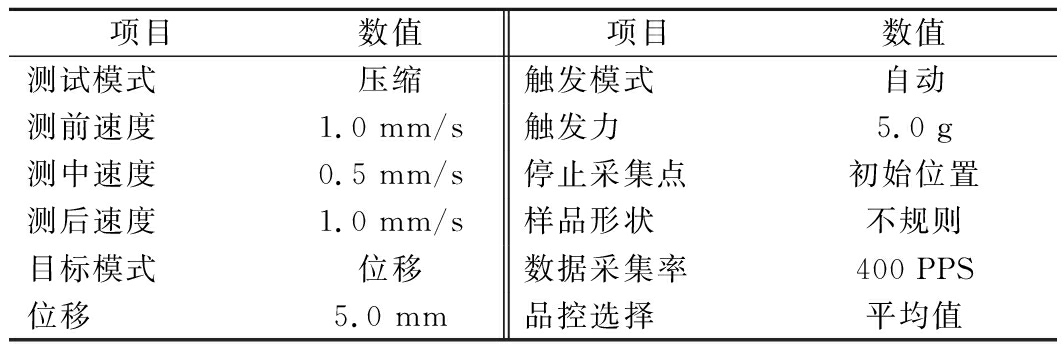
项目数值项目数值测试模式压缩触发模式自动测前速度1.0 mm/s触发力5.0 g测中速度0.5 mm/s停止采集点初始位置测后速度1.0 mm/s样品形状不规则目标模式位移数据采集率 400 PPS位移5.0 mm品控选择 平均值
1.3.4 营养成分含量分析与测定
VC测定参照GB 5009.86—2016《食品安全国家标准 食品中抗坏血酸的测定》中第三法(2,6-二氯靛酚滴定法);可溶性蛋白测定参照SNT 3926—2014《出口乳、蛋、豆类食品中蛋白质含量的测定》(考马斯亮蓝法);可溶性总糖测定参照GB 5009.7—2016《食品安全国家标准 食品中还原糖的测定》中第一法(直接滴定法)。
1.4 数据处理
采用Texture exponent 32软件对质地分析仪测定结果进行图表分析,Microsoft office excel 2010 软件和SPSS 22.0统计软件对试验数据进行分析,使用Origin 9.0 软件绘图。
2 结果与分析
2.1 蔬菜质构特性随时间变化规律
2.1.1 甘蓝质构特性随时间变化规律
2.1.1.1 平均硬度
通过质地分析仪剪切试验对甘蓝叶和茎进行质构测定,由图1可知,甘蓝叶未清洗时的平均硬度为236.46 g,随清洗时间延长,叶的平均硬度先变大后减小,15 min平均硬度最大为256.04 g,相对于未清洗时提高8.28%,25 min时平均硬度为249.24 g,仍大于未清洗时平均硬度,20 min时平均硬度为252.36 g,相对于未清洗时增加5.40%。随清洗时间延长,甘蓝茎的平均硬度缓慢减小, 20、25 min时几乎保持不变;未清洗时茎的平均硬度为495.13 g,20 min时为470.47 g,相对于未清洗时减小4.93%。
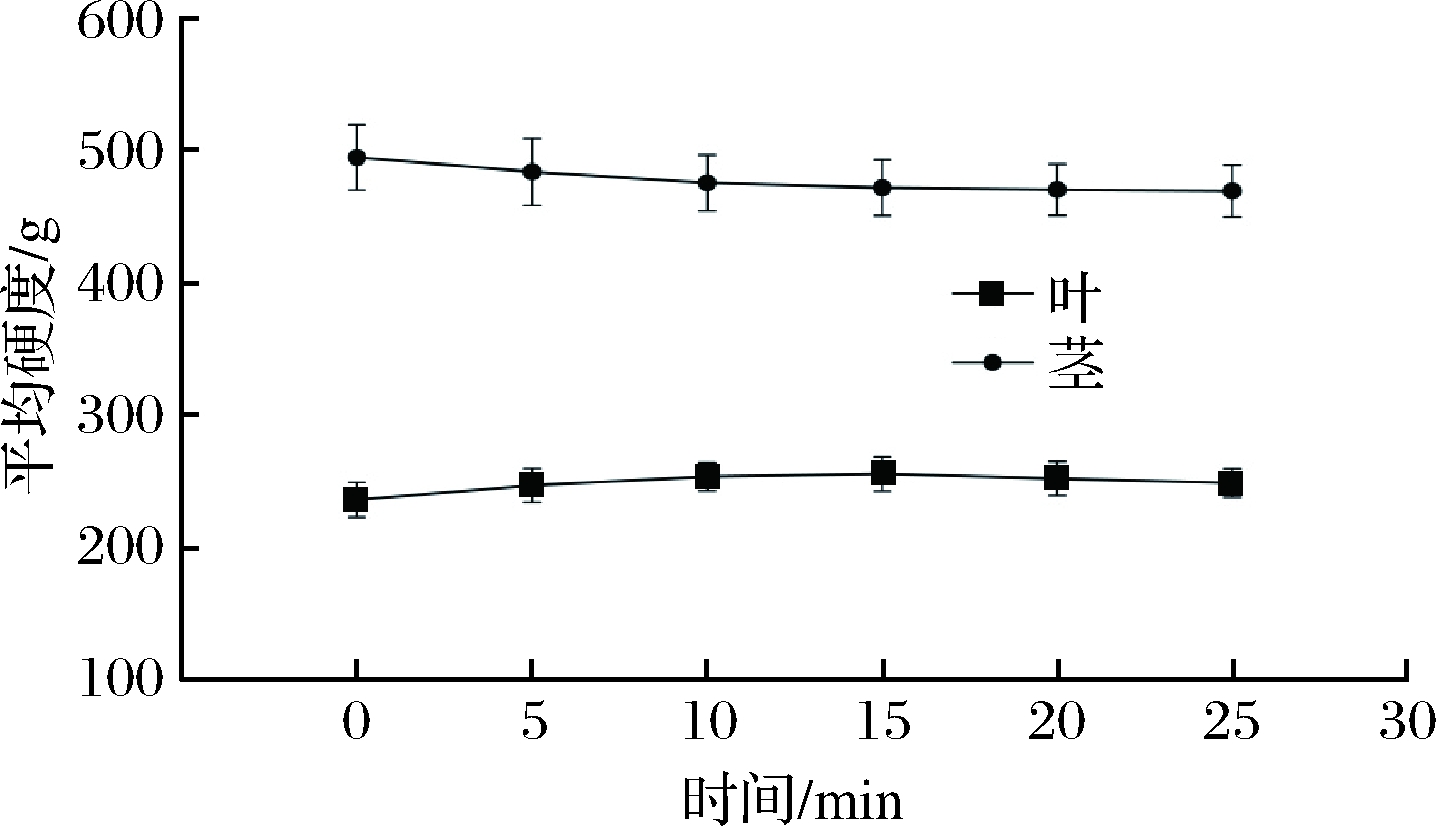
图1 不同清洗时间对甘蓝叶和茎平均硬度的影响
Fig.1 Effect of different cleaning time on the average
hardness of cabbage leaves and stems
2.1.1.2 紧实度
由图2可知,甘蓝茎的紧实度约为叶的3倍,且随清洗时间的延长,叶和茎的紧实度均有稍稍变大。未清洗时,叶的紧实度为123.62 g·s,茎的紧实度为381.77 g·s;清洗20 min时,叶的紧实度为134.21 g·s,相对于未清洗时提高8.57%,茎的紧实度为398.97 g·s,相对于未清洗时提高4.51%。
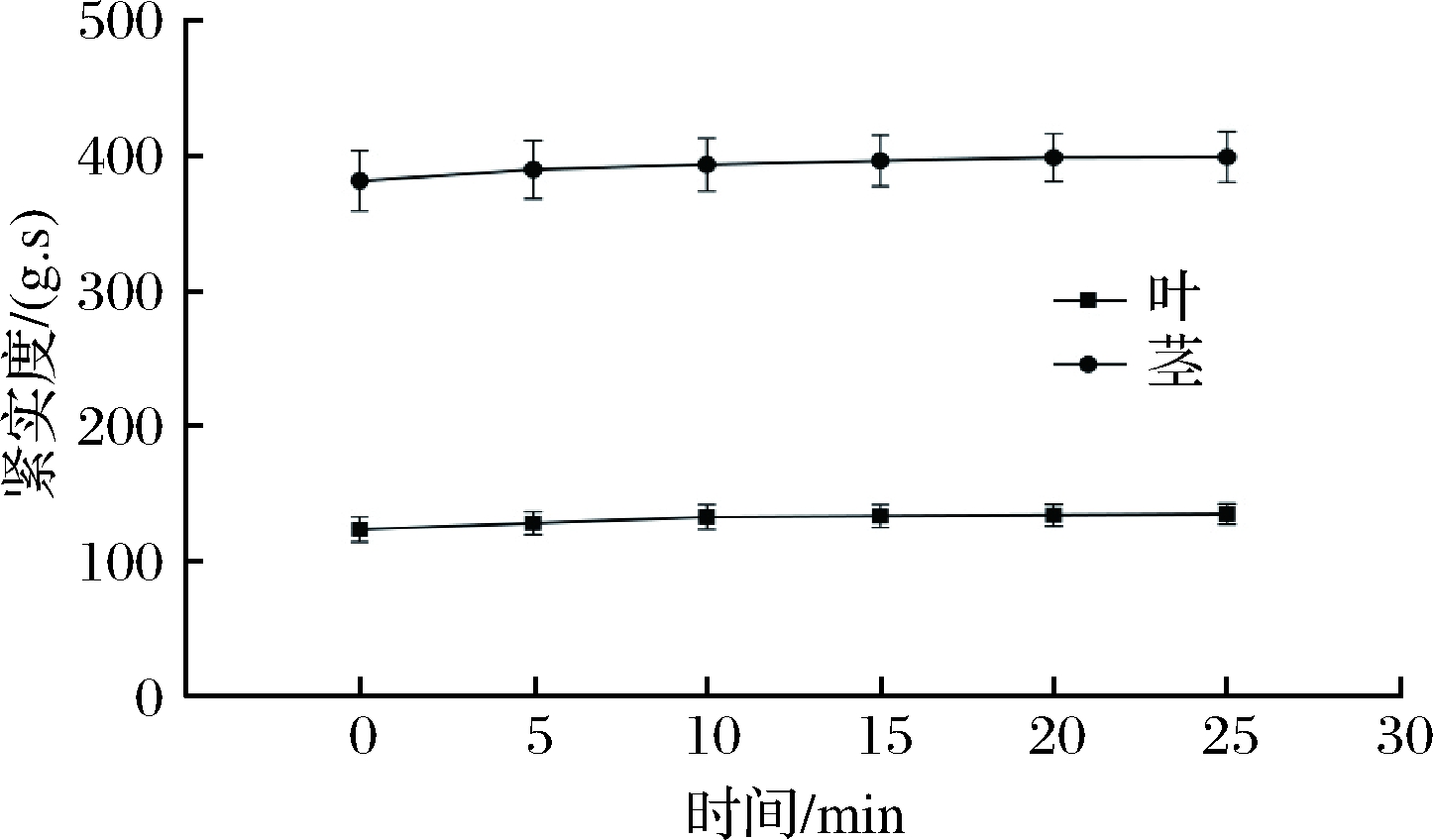
图2 不同清洗时间对甘蓝叶和茎紧实度的影响
Fig.2 Effect of different cleaning time on leaf and stem
compactness of cabbage
2.1.1.3 脆性
由图3可知,甘蓝茎的脆性大于叶的脆性。未清洗时与清洗10、20 min时,叶的脆性值均为2,清洗5、15、25 min时叶的脆性值均为3,清洗后叶的脆性值不低于未清洗时叶的脆性值。未清洗时茎的脆性值为12,清洗5、15、20 min时茎的脆性值均为13,清洗10、25 min时茎的脆性值均为14,清洗后茎的脆性值大于未清洗时茎的脆性值。因此清洗时间长短对甘蓝叶和茎的脆性无明显影响,但清洗可提高甘蓝茎的脆性值1~2。
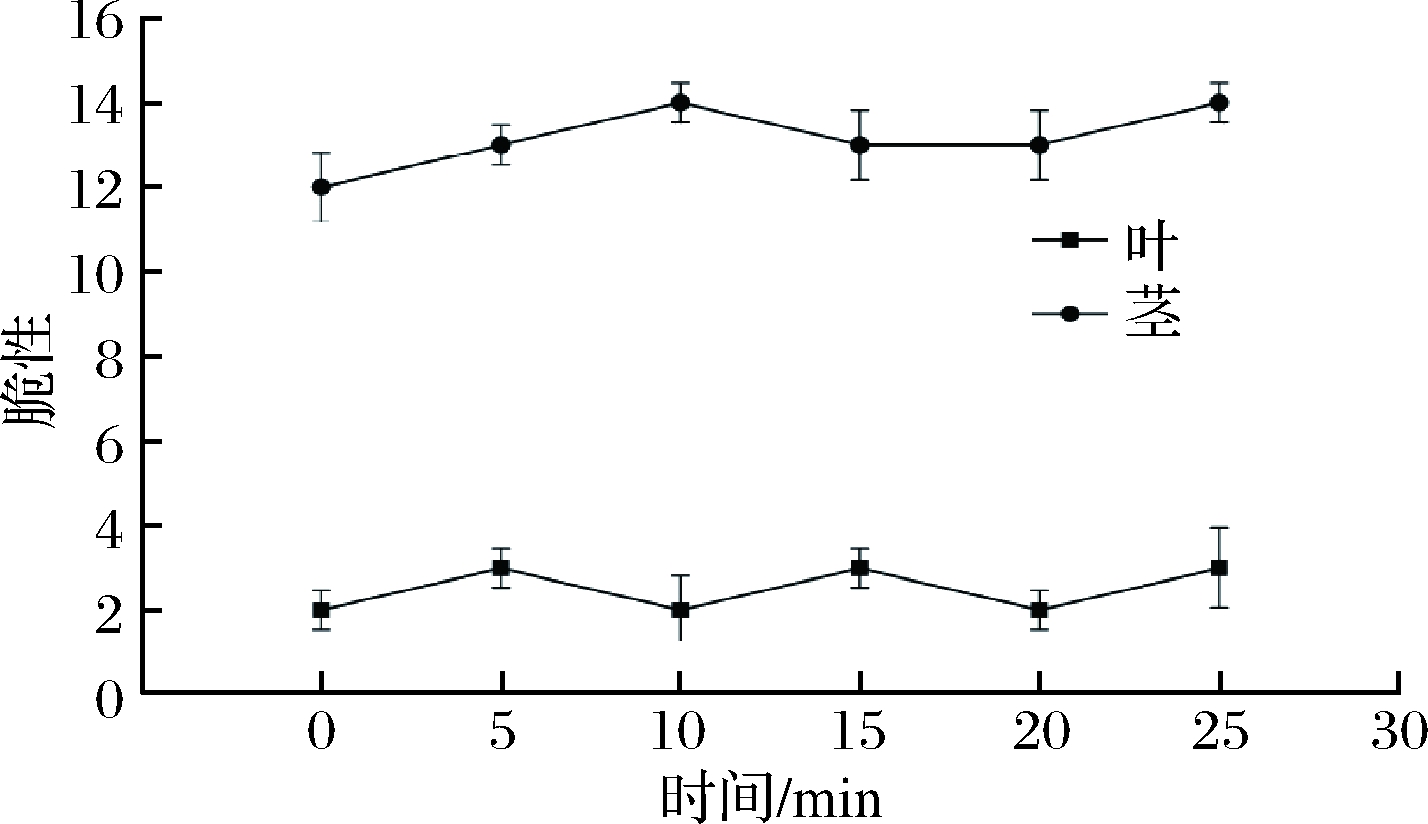
图3 不同清洗时间对甘蓝叶和茎脆性的影响
Fig.3 Effect of different cleaning time on the brittleness of
cabbage leaves and stems
2.1.2 西兰花质构特性随时间变化规律
2.1.2.1 皮硬度
通过质地分析仪剪切试验对西兰花花茎进行质构测定,根据3次平行试验得到的平均值来比较不同清洗时间的质构差异,由图4可知,西兰花花茎的皮硬度随清洗时间的延长而缓慢减小并趋于稳定,清洗15、20、25 min时皮硬度几乎无变化。未清洗时花茎皮硬度为430.30 g,清洗20 min时为401.43 g,相对于未清洗时降低了6.71%。
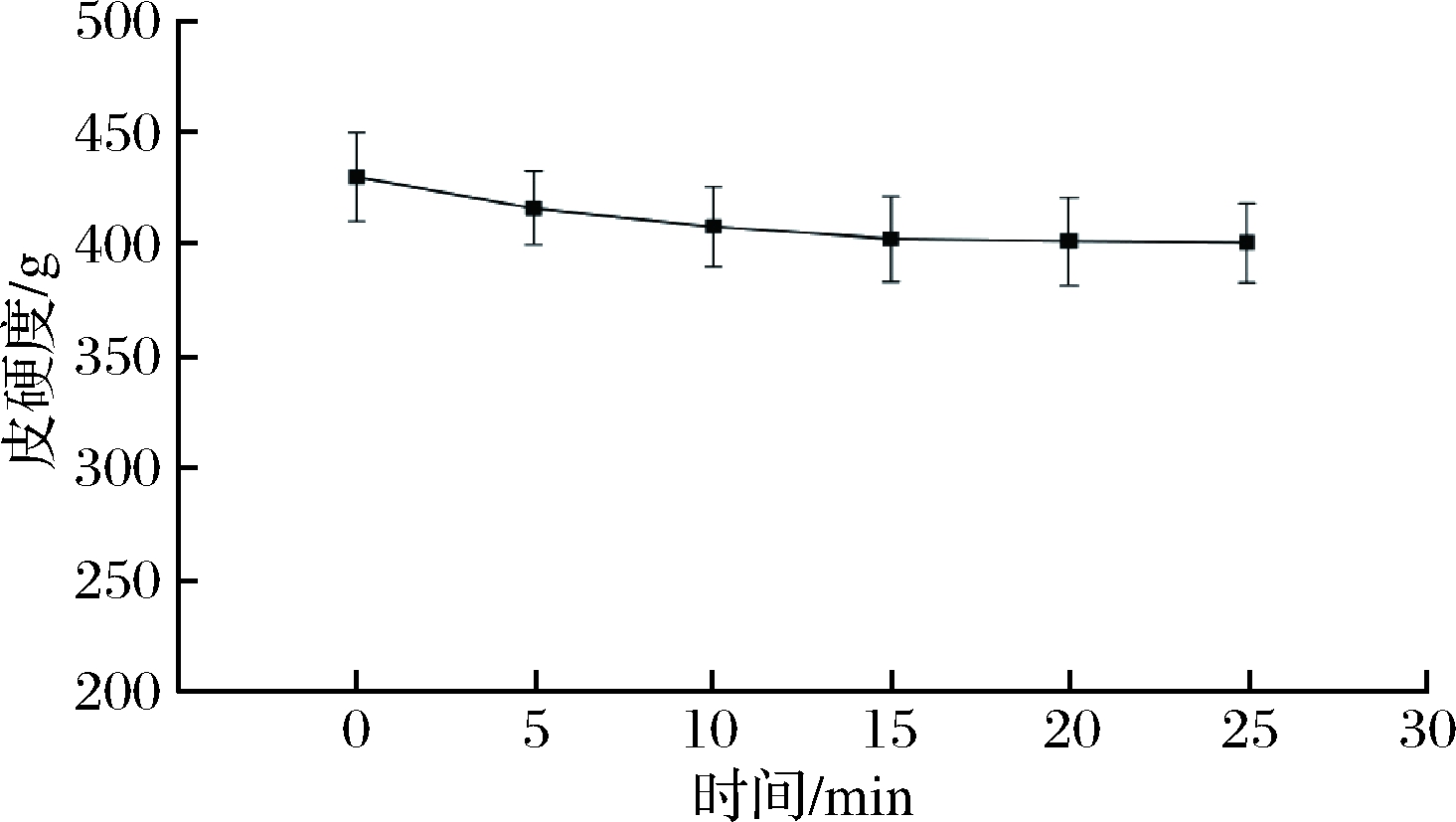
图4 不同清洗时间对西兰花花茎皮硬度的影响
Fig.4 Effect of different cleaning time on the hardness of
broccoli stems
2.1.2.2 内部平均硬度
由图5可知,西兰花花茎的内部平均硬度随清洗时间延长而缓慢增大,5、10 min增大速度较快,10~25 min增大速度较慢,15、20、25 min几乎无变化。未清洗时西兰花花茎的内部平均硬度为343.39 g,清洗20 min时为373.93 g,相对于未清洗时增加了8.89%。
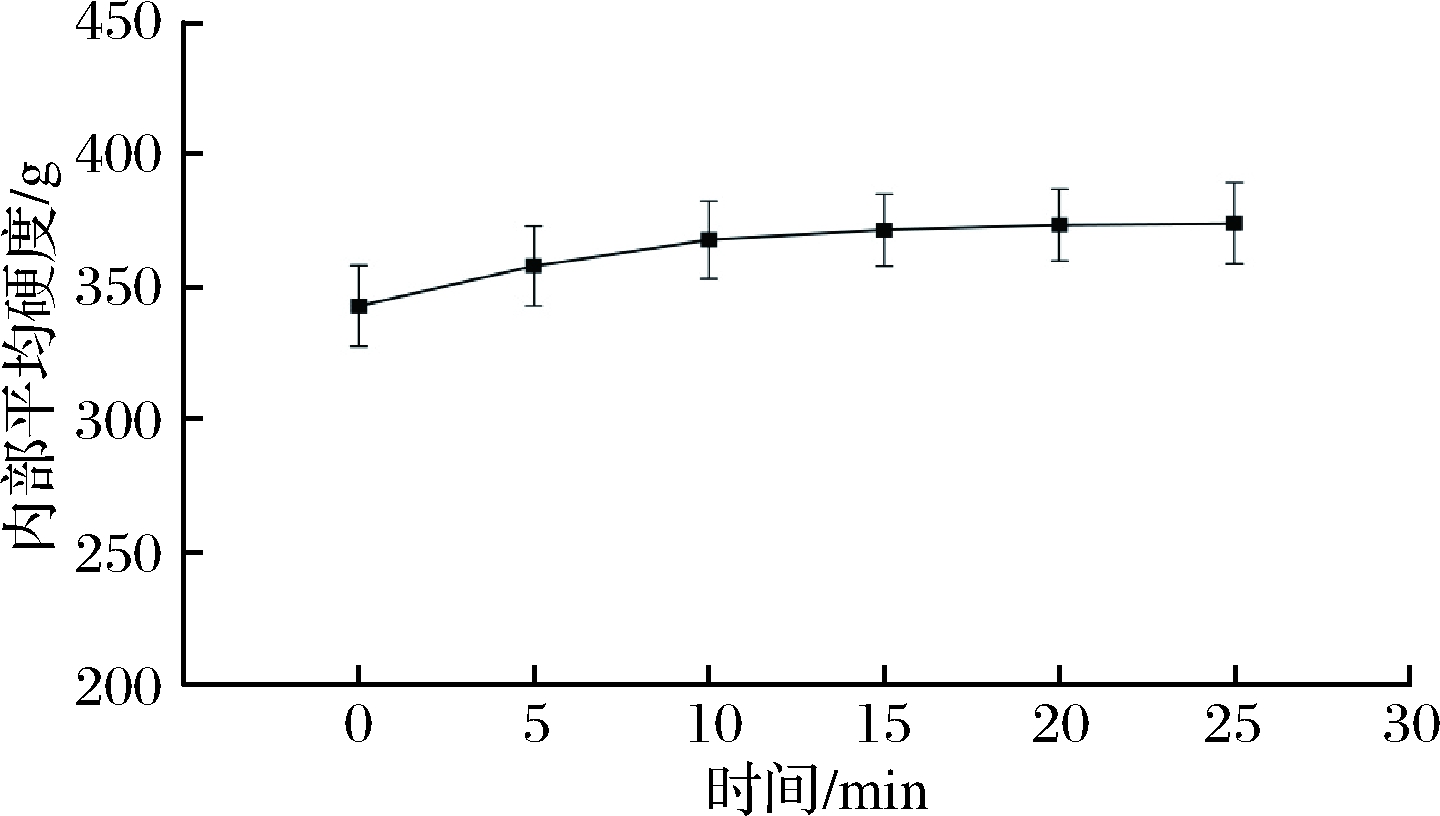
图5 不同清洗时间对西兰花花茎内部平均硬度的影响
Fig.5 Effect of different cleaning time on the average
hardness of broccoli stems
2.1.2.3 紧实度
由图6可知,西兰花花茎的紧实度随清洗时间延长而缓慢减小,0~10 min减小速度较快,10~25 min减小速度较慢, 20、25 min几乎无变化。未清洗时西兰花花茎的紧实度为238.02 g·s,清洗20 min时为210.75 g·s,相对于未清洗时减小了11.46%。
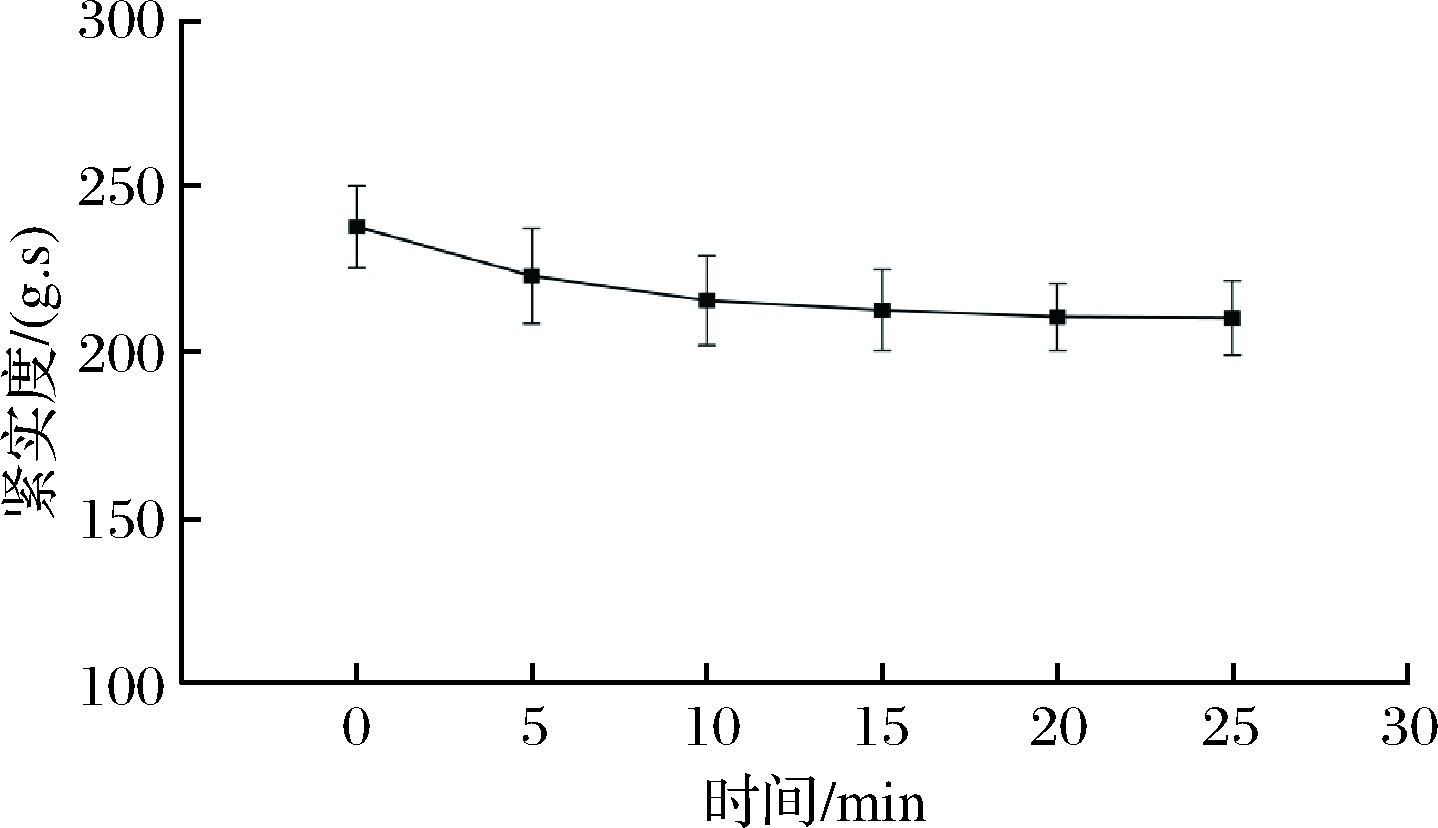
图6 不同清洗时间对西兰花花茎紧实度的影响
Fig.6 Effect of different cleaning time on the compactness
of broccoli stems
2.1.2.4 脆性
由图7可知,在0~25 min的AcEW清洗条件下,未清洗时西兰花花茎的脆性值为11,清洗5、15、20 min时花茎的脆性值为12,清洗10、25 min时花茎的脆性值为13,清洗后花茎的脆性值与未清洗时相比提高1~2,与甘蓝茎的清洗结果趋势一致。
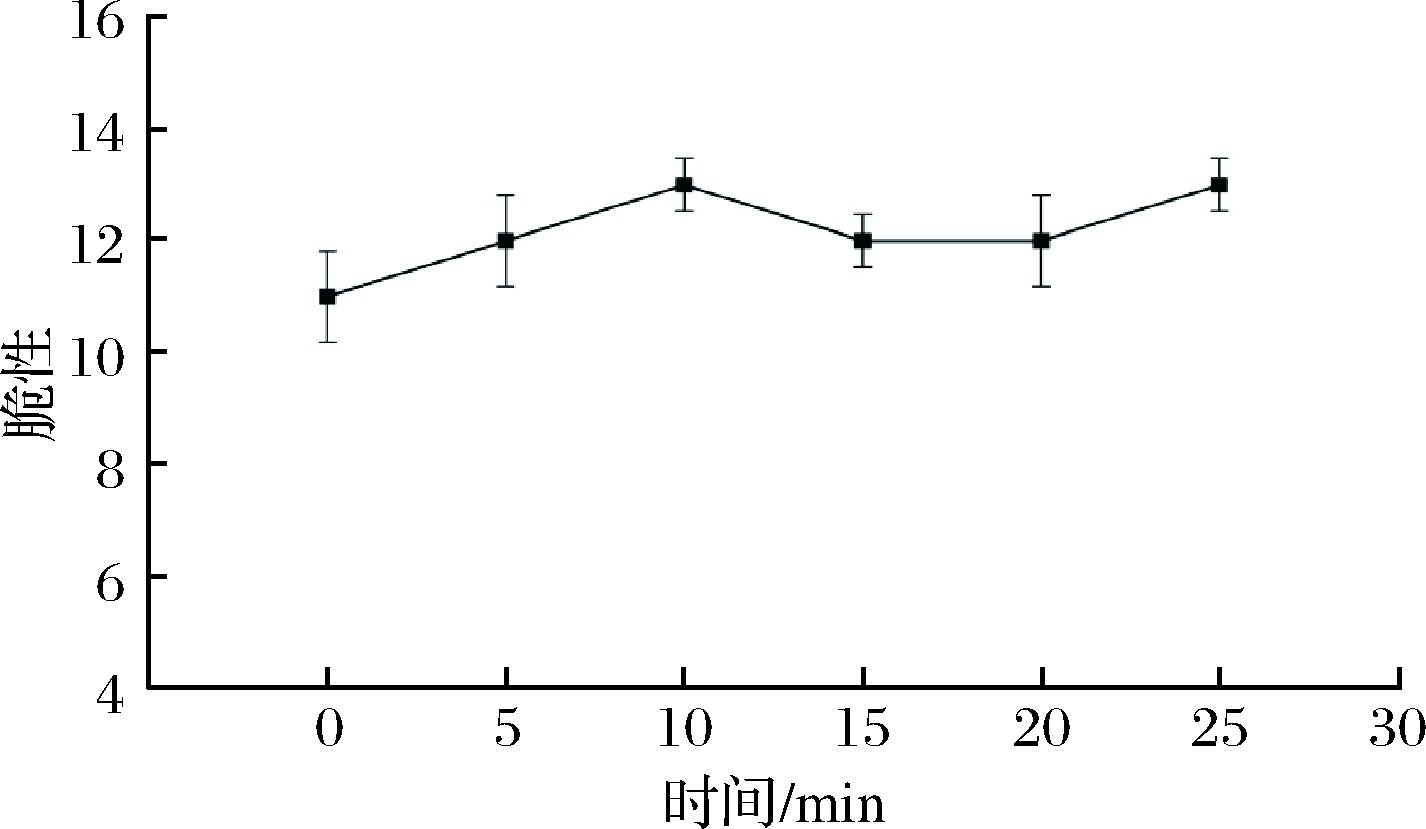
图7 不同清洗时间对西兰花花茎脆性的影响
Fig.7 Effect of different cleaning time on brittleness of
broccoli stems
2.1.3 彩椒质构特性随时间变化规律
2.1.3.1 紧实度
由图8可知,在AlEW清洗条件下,彩椒正面和反面的紧实度随清洗时间延长均呈现出缓慢变大趋势,但清洗20、25 min时,正、反面的紧实度几乎无变化。未清洗时,正、反面的紧实度分别为111.55、18.76 g·s,清洗20 min时,正面、反面的紧实度分别为118.59、22.01 g·s,相对于未清洗时分别增加6.31%、17.32%。
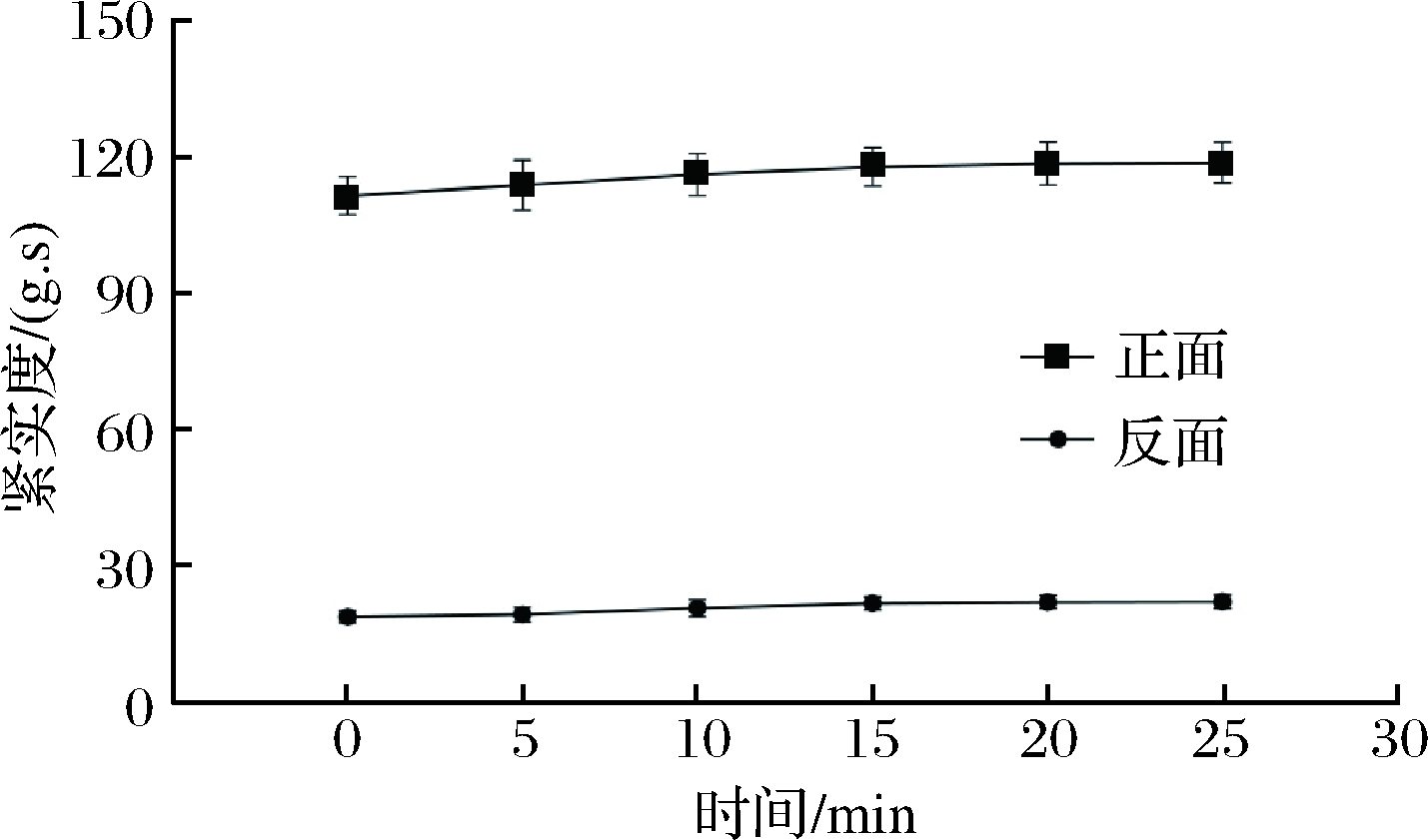
图8 不同清洗时间对彩椒正面和反面紧实度的影响
Fig.8 Effect of different cleaning time on the compactness
of the front and the back of bell pepper
2.1.3.2 硬度和脆性
由图9可知,在AlEW清洗条件下,彩椒正面硬度随着清洗时间的延长呈现出缓慢增大趋势,0~10 min增大趋势较快,10~25 min增大趋势较缓,20、25 min几乎无变化。未清洗时彩椒正面硬度为504.24 g,清洗20 min时正面硬度为532.35 g,相对于未清洗时增加了5.57%。未清洗时彩椒反面的脆性值为9,清洗5、15 min时脆性值为10,清洗10、20、25 min时脆性值为11,清洗后彩椒反面的脆性值与未清洗时相比,提高1~2。
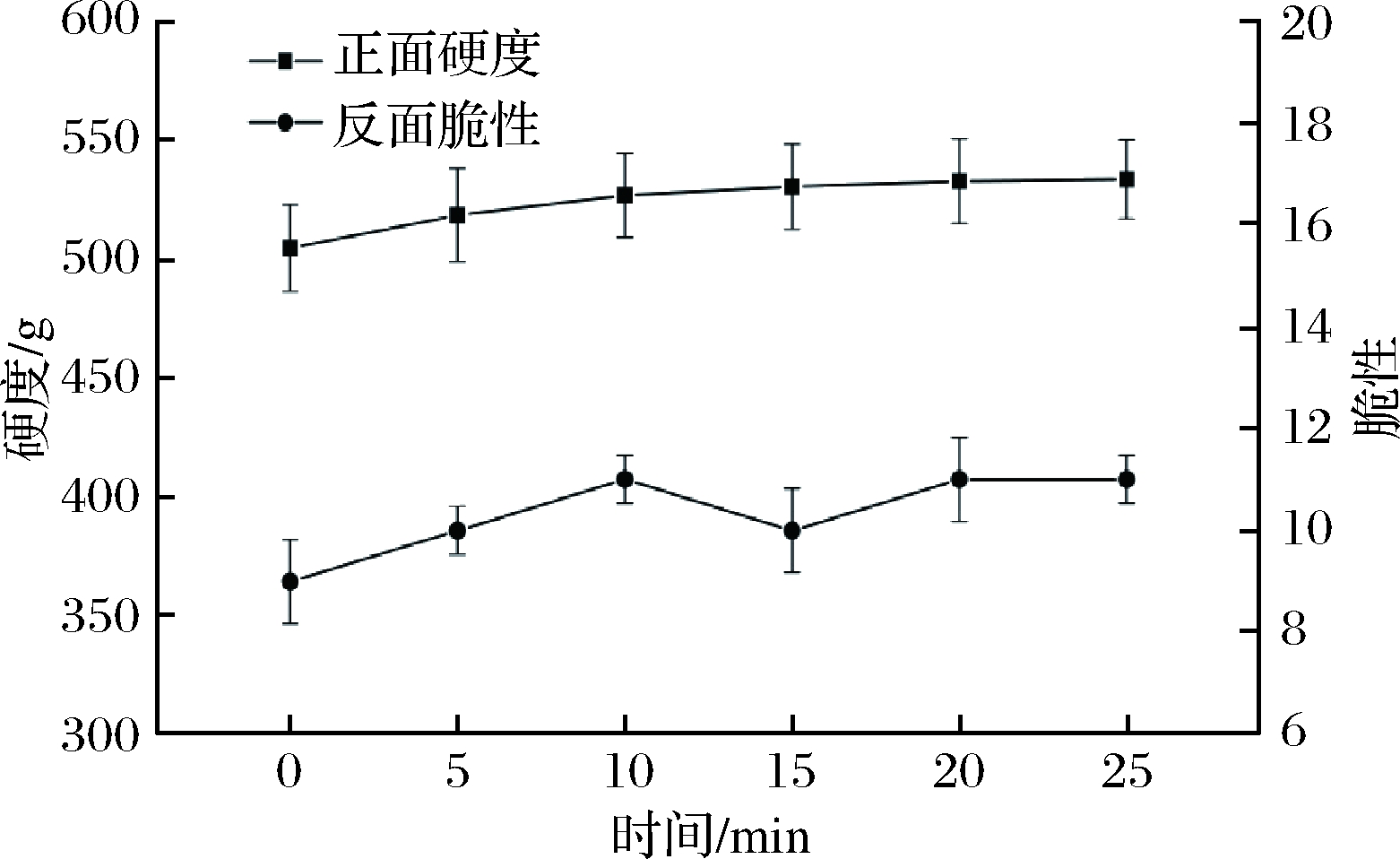
图9 不同清洗时间对彩椒正面硬度和反面脆性的影响
Fig.9 The effect of different cleaning time on the hardness
and brittleness of bell pepper
2.1.4 蔬菜质构检测结果单因素方差分析
由表3、表4和表5可知,甘蓝、西兰花和彩椒3种蔬菜各自质构特性在不同清洗时间均无显著差异(P>0.05),说明各蔬菜在特定清洗条件下,5~25 min清洗时间对3种蔬菜质构特性无显著影响,即用EFW清洗蔬菜,可保持蔬菜质构特性。
2.2 蔬菜营养成分含量随时间变化规律
2.2.1 VC含量测定
由图10可知,未清洗时,VC含量最高,为131.59 mg/100 g,西兰花和甘蓝较为接近,分别为88.49和87.73 mg/100 g。
表3 甘蓝剪切试验结果方差分析表
Table 3 Variance analysis of cabbage shear test results
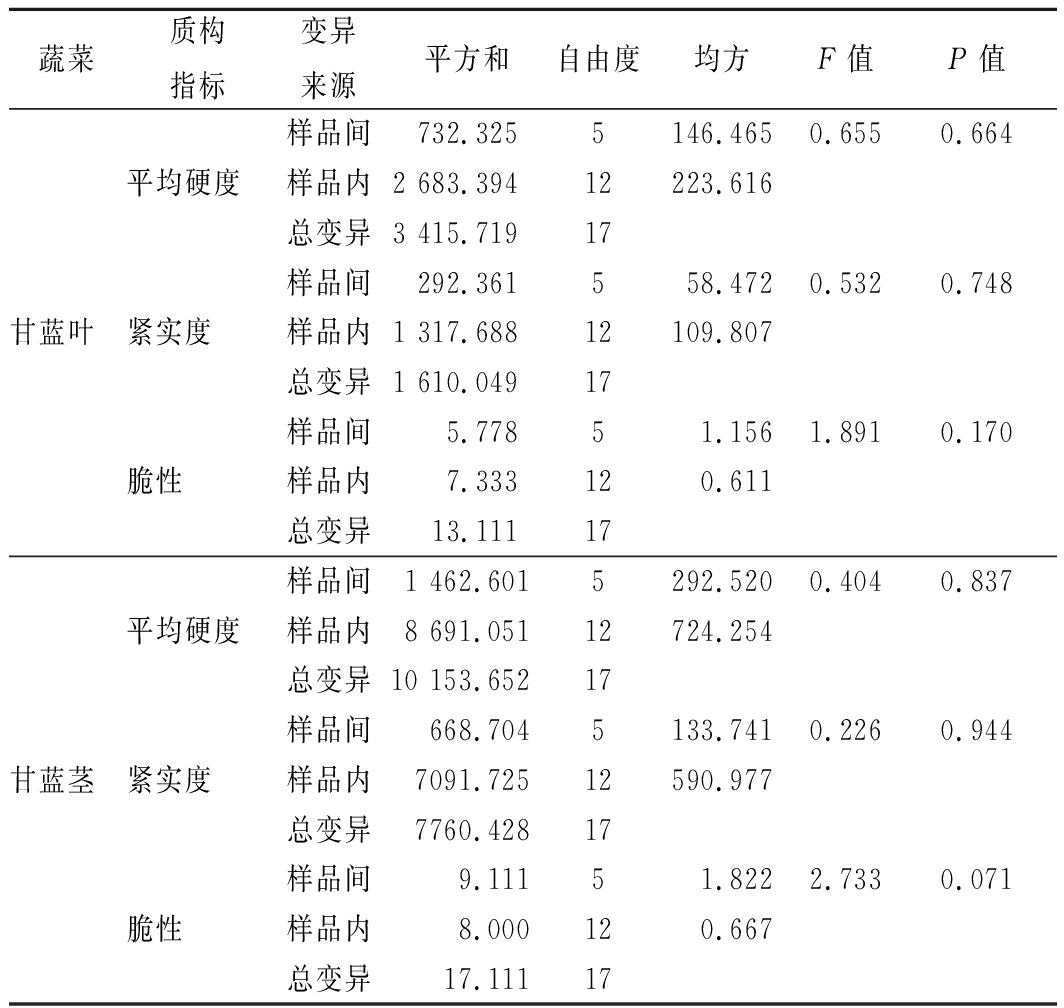
蔬菜质构指标变异来源平方和自由度均方F值P值甘蓝叶样品间732.3255146.4650.6550.664平均硬度样品内2 683.39412223.616总变异3 415.71917样品间292.361558.4720.5320.748紧实度样品内1 317.68812109.807总变异1 610.04917样品间5.77851.1561.8910.170脆性样品内7.333120.611总变异13.11117甘蓝茎样品间1 462.6015292.5200.4040.837平均硬度样品内8 691.05112724.254总变异10 153.65217样品间668.7045133.7410.2260.944紧实度样品内7091.72512590.977总变异7760.42817样品间9.11151.8222.7330.071脆性样品内8.000120.667总变异17.11117
表4 西兰花剪切试验结果方差分析表
Table 4 Variance analysis of broccoli shear test results
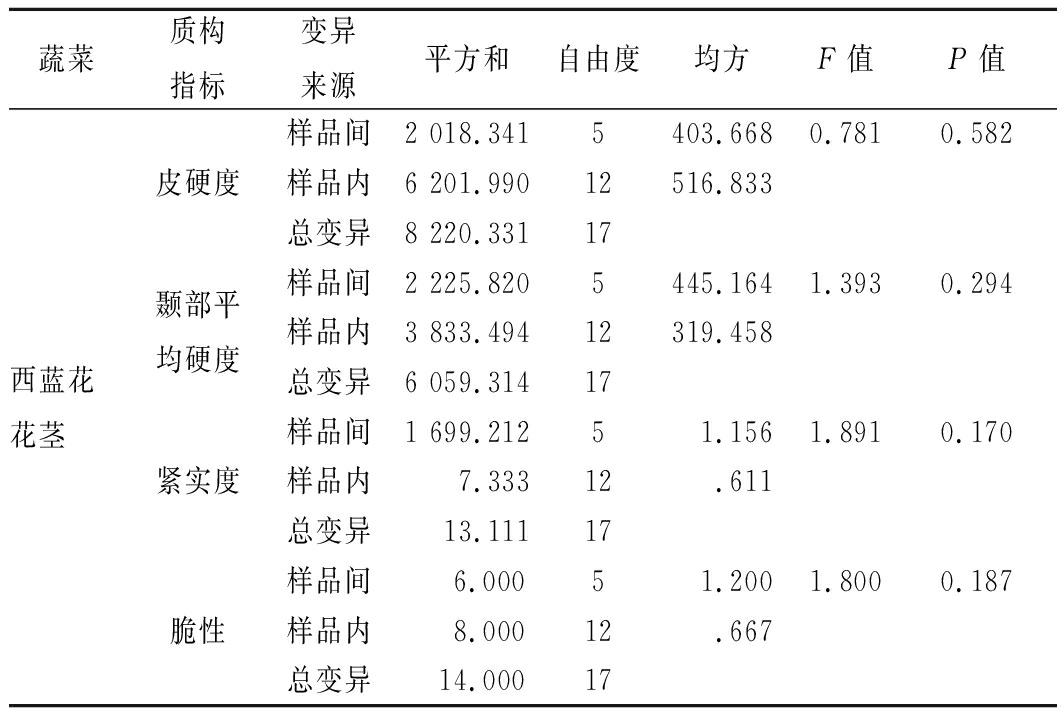
蔬菜质构指标变异来源平方和自由度均方F值P值西蓝花花茎皮硬度样品间2 018.3415403.6680.7810.582样品内6 201.99012516.833总变异8 220.33117颞部平均硬度样品间2 225.8205445.1641.3930.294样品内3 833.49412319.458总变异6 059.31417紧实度样品间1 699.21251.1561.8910.170样品内7.33312.611总变异13.11117脆性样品间6.00051.2001.8000.187样品内8.00012.667总变异14.00017
表5 彩椒剪切试验结果方差分析表
Table 5 Variance analysis of bell pepper shear test results

蔬菜质构指标变异来源平方和自由度均方F值P值彩椒正面样品间1 861.6095372.3220.7700.589硬度样品内5 805.74412483.812总变异7 667.35317样品间127.001525.4000.7840.581紧实度样品内388.9111232.409总变异515.91217彩椒反面样品间10.27852.0563.0830.051脆性样品内8.00012.667总变异18.27817样品间31.26156.2521.7590.196紧实度样品内42.662123.555总变异73.92217
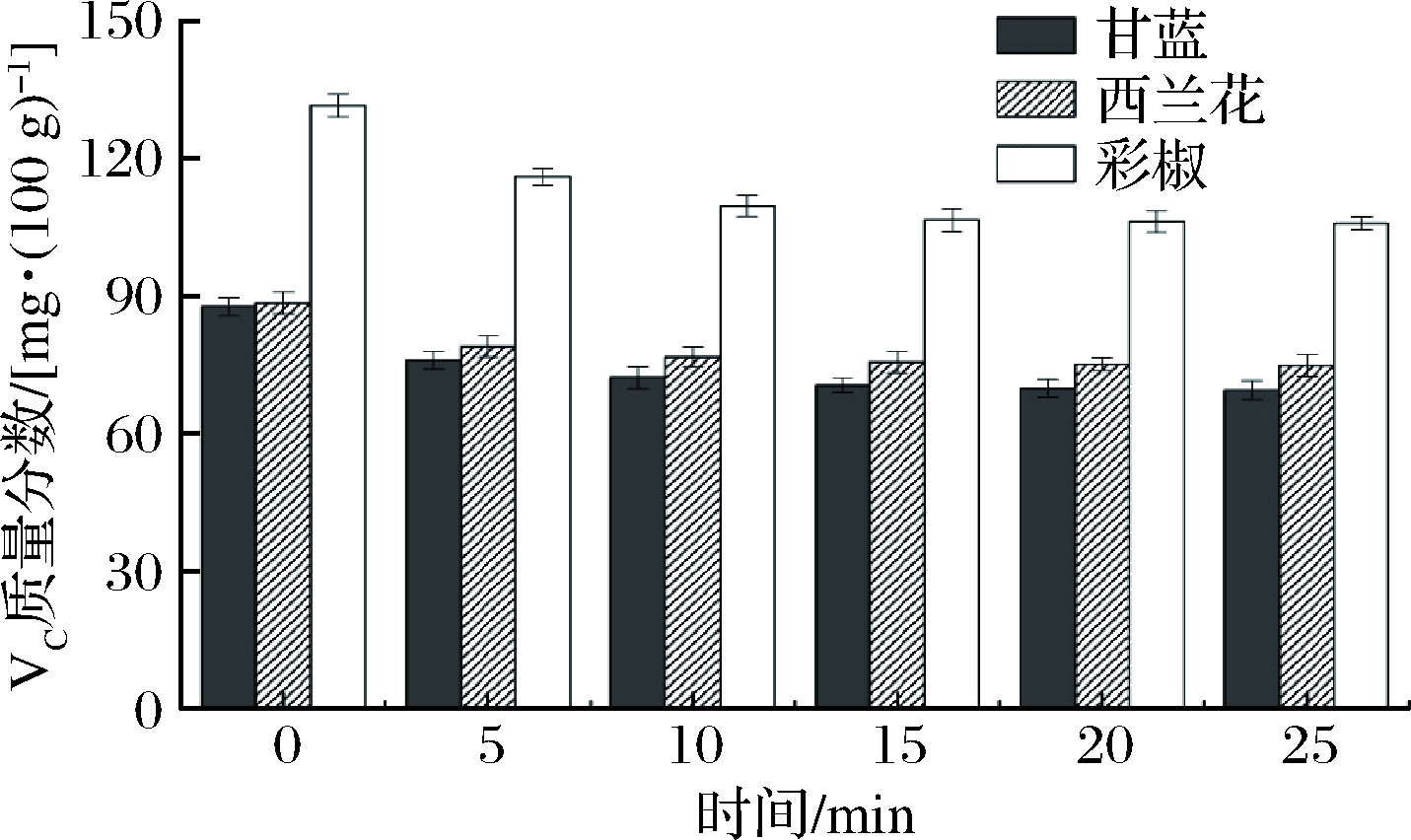
图10 不同清洗时间对甘蓝、西兰花和彩椒中VC含量
的影响
Fig.10 Effect of different cleaning time on vitamin C content
of cabbage,broccoli and bell pepper
在3种蔬菜各自清洗参数条件下,随时间延长,甘蓝、西兰花、彩椒3种蔬菜VC含量整体均呈现出不同下降趋势,VC均有不同程度地损失。清洗5 min时,甘蓝、西兰花、彩椒VC含量分别为76.01、79.03、116.09 mg/100 g,相对于未清洗时分别降低了13.36%、10.68%、11.78%。3种蔬菜在清洗15、20、25 min时,各自VC含量变化微小,20 min时,甘蓝、西兰花、彩椒VC含量分别为69.96、75.18、106.26 mg/100 g,相对于未清洗时分别降低了20.26%、15.04%、19.25%。
果蔬中的VC比较脆弱,水、光、热、氧气、碱和盐都会造成其损失。本试验中3种蔬菜中VC损失的原因可能是:①试验过程中,3种蔬菜均在切分状态下进行清洗,由于机械损伤,蔬菜的细胞壁被严重破坏,细胞液外流,其中VC也随之外流损失;②由于切面使蔬菜内部直接暴露,致VC更易被EFW洗去;③蔬菜中VC与空气以及酸性EFW中的氧气接触,发生氧化反应从而导致损失;④彩椒中VC还可能因为碱性EFW的碱性环境使VC被破坏;⑤VC被EFW中未被完全电解的NaCl破坏等。
2.2.2 可溶性蛋白含量测定
在595 nm波长下,以牛血清白蛋白(bovine serum albumin,BSA)为横坐标、吸光值为纵坐标绘制标准曲线。标准曲线方程为y=0.008 2x+0.002(R2=0.998 5)。
由图11可知,西兰花可溶性蛋白含量丰富,甘蓝、彩椒较少。3种蔬菜可溶性蛋白含量随清洗时间延长均减少,说明清洗均造成蔬菜中可溶性蛋白损失,但甘蓝和彩椒损失较少,而西兰花损失较大。清洗5 min时,甘蓝、西兰花、彩椒可溶性蛋白含量相对于未清洗时分别降低了10.84%、17.44%、5.50%。甘蓝在清洗15、20、25 min时,可溶性蛋白含量变化微小;彩椒在清洗10、15、20、25 min时,可溶性蛋白含量几乎无变化;不同清洗时间,西兰花可溶性蛋白含量变化明显。清洗20 min时,甘蓝、西兰花、彩椒可溶性蛋白相对于未清洗时分别降低了17.07%、32.23%、9.51%。
3种蔬菜可溶性蛋白损失的原因可能是:①机械损伤使可溶性蛋白随细胞汁液外流;②溶解在EFW中从而被洗去;③蛋白质在EFW的酸性或碱性环境下发生变性等。
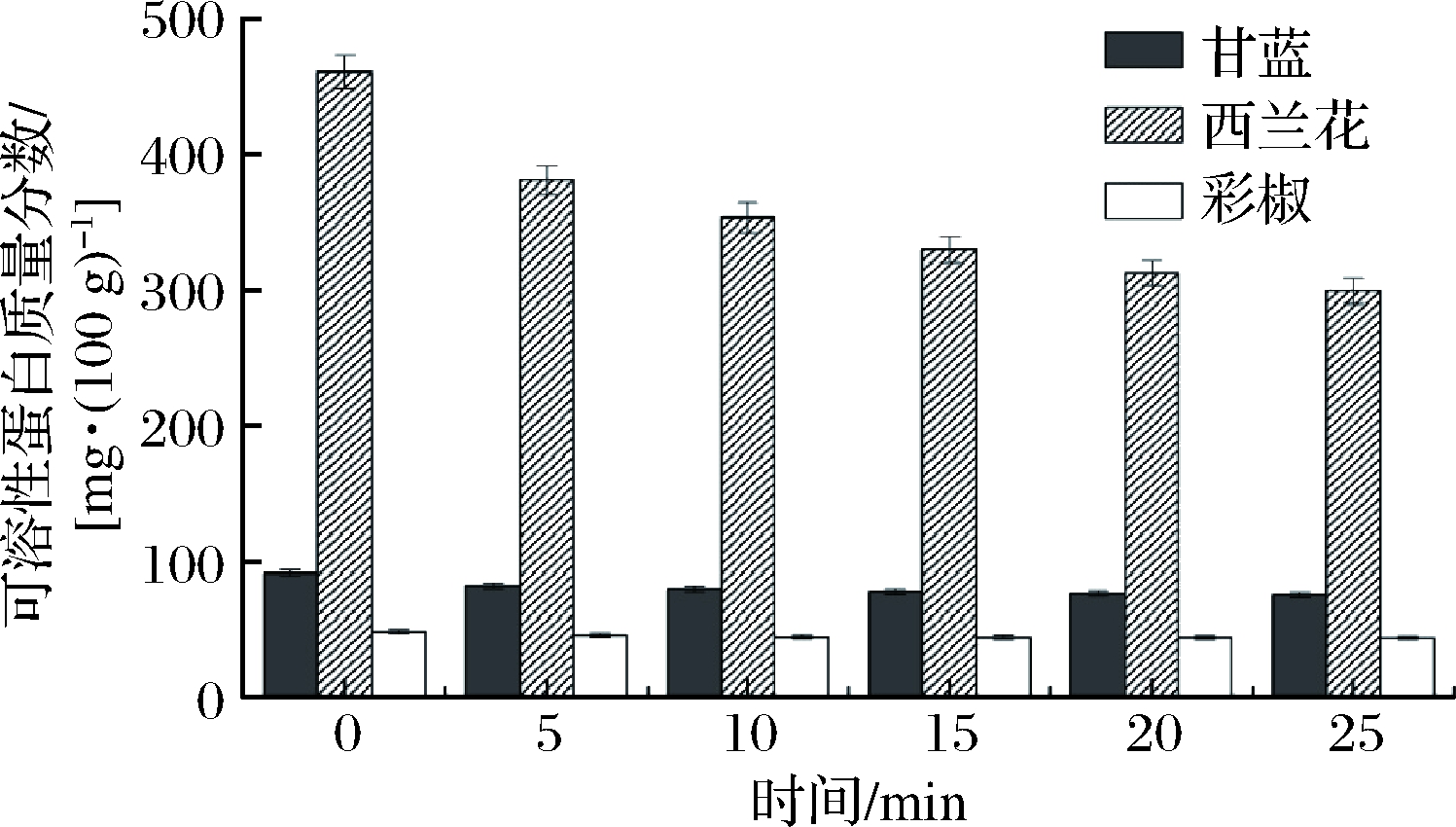
图11 不同清洗时间对甘蓝、西兰花和彩椒可溶性
蛋白含量的影响
Fig.11 Effect of different cleaning time on soluble protein
content of cabbage,broccoli and bell pepper
2.2.3 可溶性总糖含量的测定
由图12可知,3种蔬菜中,甘蓝和彩椒可溶性总糖含量极为接近,且均高于西兰花。未清洗时,甘蓝、西兰花、彩椒可溶性总糖质量分数分别为4.24、2.98、4.13 g/100 g。整体来看,3种蔬菜可溶性总糖含量在各自清洗参数条件下,随时间延长均呈现出下降趋势,说明清洗过程均造成蔬菜中可溶性总糖的损失。清洗5 min时,甘蓝、西兰花、彩椒可溶性总糖含量相对于未清洗时分别降低了6.54%、4.10%、5.17%。3种蔬菜在清洗15、20、25 min时,各自可溶性总糖含量变化微小,20 min时,甘蓝、西兰花、彩椒可溶性总糖含量相对于未清洗时分别降低了13.11%、10.88%、11.66%。由此可看出,20 min的清洗时间对3种蔬菜可溶性总糖质量分数影响较小。
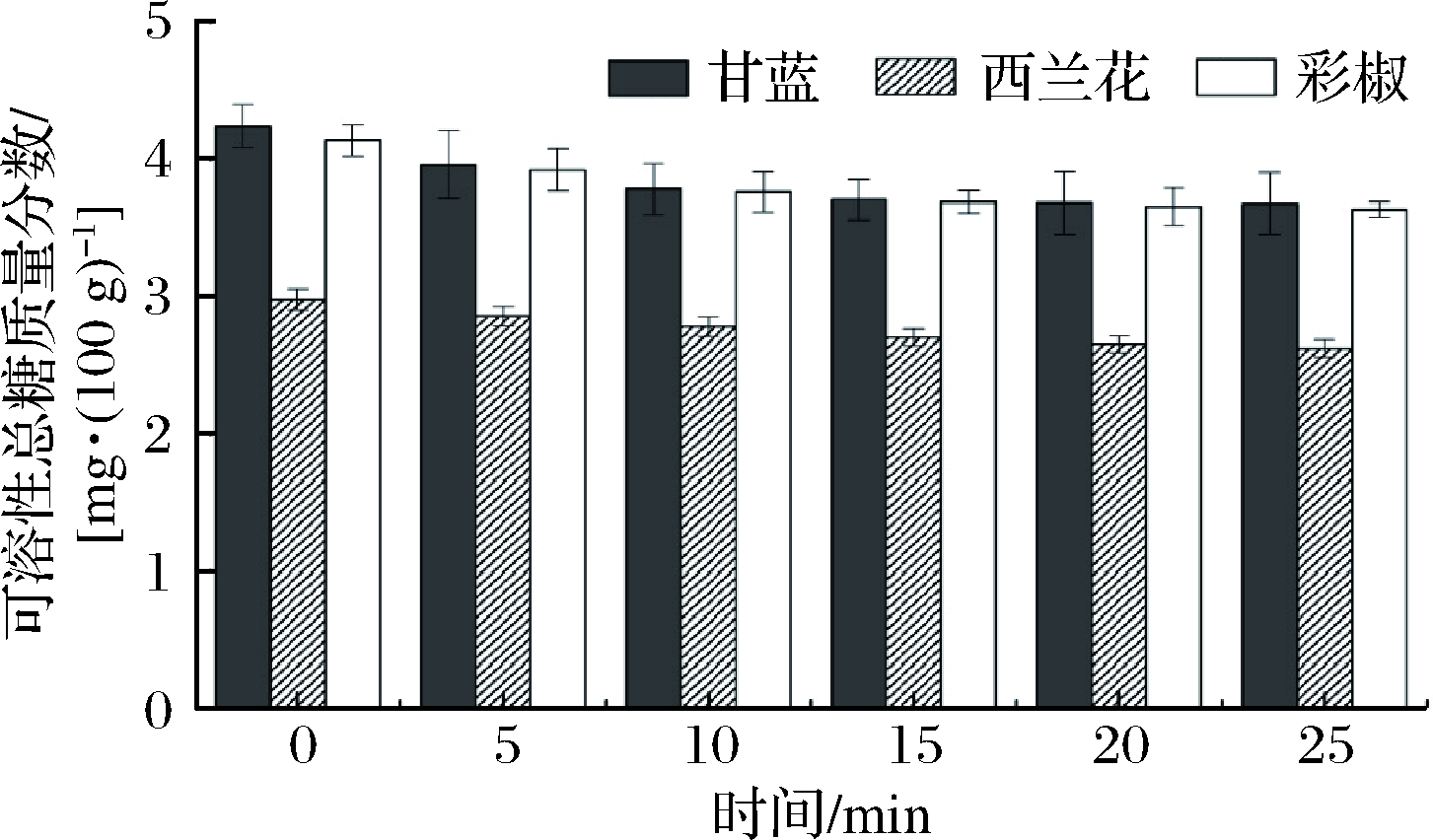
图12 不同清洗时间对甘蓝、西兰花和彩椒可溶性
总糖含量的影响
Fig.12 Effect of different cleaning time on total soluble sugar
content of cabbage,broccoli and bell pepper
3种蔬菜可溶性糖损失的原因可能是:①机械损伤使可溶性糖随细胞汁液外流;②溶解在EFW中从而被洗去等。
3 结论
在5~25 min清洗时间内,甘蓝、西兰花和彩椒各自质构特性参数与未清洗时无显著差异(P>0.05),即EFW清洗过程对3种蔬菜质构特性无显著不良影响。
EFW清洗过程对甘蓝、西兰花和彩椒中VC、可溶性蛋白、可溶性总糖造成不同程度损失,除西兰花的可溶性蛋白和甘蓝的VC损失较为严重外,其余损失较小,清洗20 min损失量均在20%以下。
基于以上结果与分析,采用EFW清洗甘蓝、西兰花、彩椒3种蔬菜,能保持蔬菜质构特性及大部分营养物质,表明该清洗方式具有良好的应用潜力和推广价值。
[1] 张倩,鲁建斌,于峰,等. 河北省张家口市蔬菜生产变化趋势及优势品种分析[J]. 中国蔬菜,2018,4: 15-18.
[2] 苏沛然. 张家口市蔬菜出口竞争力分析[J]. 河北北方学院学报(社会科学版),2018,5(34): 70-73.
[3] 刘尚金. 浅谈张家口市的蔬菜产业化[J]. 农业与技术,2017,37(9): 34-38.
[4] 杨万军,苏浴源. 张家口市蔬菜产业发展现状与分析[J]. 农业科技通讯,2017(6): 17-20.
[5] TOIVONEN P M A,BRUMMELL D A. Biochemical bases of appearance and texture changes in fresh-cit fruit and vegetable[J]. Postharvest Biology and Technology,2008,48(1): 1-14.
[6] 唐偲雨,曾顺德,刁源,等. 不同清洗方式对净菜微生物污染的控制研究进展[J]. 南方农业,2015,9(1): 6-39.
[7] HWANG E S,CASH J N,ZABIK M J. Postharvest treatments for the reduction of mancozeb in fresh apples[J]. Journal of Agricultural and Food Chemistry,2001,49(6): 3 127-3 132.
[8] MILLER F A,SILVA C L M,BRAND O T R S. A review on ozone-based treatments for fruit and vegetables preservation[J]. Food Engineering Reviews,2013,5(2): 77-106.
O T R S. A review on ozone-based treatments for fruit and vegetables preservation[J]. Food Engineering Reviews,2013,5(2): 77-106.
[9] 李淑艳. 氢氧化钠对果蔬中有机磷农药残留降解效果探究[J]. 农业与技术,2016,36(24): 34-36.
[10] ONG K C,CASH J N,ZABIK M J,et al. Chlorine and ozone washes for pesticide removal from apples and processed apple sauce[J]. Food Chemistry,1996,55(2): 153-160.
[11] 茅林春,方雪花. 净菜加工关键工艺及其保鲜技术应用现状与发展趋势[J]. 保鲜与加工,2003,3(4): 1-3.
[12] 乔永祥,谢晶. 新鲜蔬菜清洗技术研究进展[J]. 包装工程,2017(3): 60-66.
[13] 梁东妮. 鲜切蔬菜清洗、护色和包装技术的研究[D]. 南京: 南京农业大学,2003.
[14] 侯田莹,赵园园,郑淑芳. 次氯酸钠在蔬菜加工中循环利用的杀菌效果评价[J]. 食品科学,2010,31(13): 27-30.
[15] JIA G L,SHI J Y,SONG Z H,et al. Prevention of enzymatic browning of Chinese yam (Dioscorea spp.) using electrolyzed oxidizing water[J]. Journal of Food Science,2015,80(4): 718-728.
[16] WANG J J,LIN T,LI J B,et al. Effect of acidic electrolyzed water ice on quality of shrimp in dark condition[J]. Food Control,2014,35(1): 207-212.
[17] ZHANG C L,LU Z H,LI Y Y,et al. Reduction of Escherichia coli O157:H7 and Salmonella enteritidison mung bean seeds and sprouts by slightly acidic electrolyzed water[J]. Food Control,2011,22(5): 792-796.
[18] 贾国梁,石晶盈,李法德. 电生功能水抑制微生物及其产生毒素研究进展[J]. 食品科学,2015,36(3): 265-271.
[19] AREVALOS-SANCHEZ M,REGALADO C,MARTIN S E,et al. Effect of neutral electrolyzed water on lux-tagged L. monocytogenes EGDe biofilms adhered to stainless steel and visualization with destructive and non-destructive microscopy techniques[J]. Food Control,2013,34(2): 472-477.
[20] MONNIN A,LEE J,PASCALL M A. Efficacy of neutral electrolyzed water for sanitization of cutting boards used in the preparation of foods[J]. Journal of Food Engineering,2012,110(4): 541-546.
[21] SAKURAI Y,NAKATSU M,SATO Y,et al. Endoscope contamination from HBV and HCV positive patients and evaluation of a cleaning/disinfecting method using strongly acidic electrolyzed water[J]. Digestive Endoscopy,2003,15(1): 19-24.
[22] SHIMMURA S,MATSUMOTO K,YAGUCHI H,et al. Acidic electrolysed water in the disinfection of the ocular surface[J]. Experimental Eye Research,2000,70(1): 1-6.
[23] 胡朝晖,吴彤娇,万阳芳,等. 微酸性电解水对韭菜中乐果和毒死蜱去除效果的研究[J]. 食品工业科技,2016,37(1): 49-52.
[24] 朱军伟,谢晶,林永艳,等. 清洗条件对切割黄瓜贮藏品质和安全性的影响[J]. 食品工业科技,2012,33(20): 320-323.
[25] LI H Z,ZHENG S F,SONG S H,et al. Study on steri-lization and preservation of fruits and vegetables using acidic electrolyzed oxidizing water[J]. Modern Food Science and Technology,2011,27(3): 361-365.