纳豆激酶是枯草芽孢杆菌发酵大豆制备纳豆过程中产生的一种丝氨酸蛋白酶[1],因其具有多种溶栓功效[2]而备受关注,但是纳豆的特有不良风味一直是其产业推广的瓶颈。纳豆风味改良主要通过菌种选育、工艺优化、辅料添加等[3-5]措施以适度降低或掩盖其特有不良风味,但要从根本上解决风味问题还需明确其主要挥发性成分。不同学者对纳豆风味物质的解析鉴定因大豆品种、发酵条件和检测方法的不同而有所差异:TANAKA等[6]研究表明,丙酮、异丁酸甲酯、氨、2,5-二甲基吡嗪(2,5-dimethylpyrazine,2,5-DMP)、2-甲基丁酸是纳豆的主要风味物质。LIU等[7]和黄璇等[8]研究表明,2,5-DMP、2,3,5-三甲基吡嗪(2,3,5- trimethylpyrazine,2,3,5-TMP)和川芎嗪等物质对纳豆风味有很大贡献。刘野等[9]认为酸类及以2,5-DMP为主的吡嗪类物质含量高低对整体风味的影响很大。KEITAROU等[10]研究表明,异戊酸、三甲基吡嗪、1-辛烯-3-醇和1-己醇等是枯草芽孢杆菌发酵食品中主要特征风味物质。然而,对于枯草芽孢杆菌发酵豆制品风味物质的变化规律和产生机制尚不明确,有待开展深入的研究。
前期研究发现,枯草芽孢杆菌BSNK-5通过液体深层发酵豆乳富集的纳豆激酶活性显著高于固体发酵[11],更适合纳豆激酶类产品的大规模工业化生产,然而,该过程产生的不良风味也更为突出。因此,本研究对BSNK-5发酵豆乳的感官和风味物质进行了跟踪鉴定,同时通过生化方法对其产生机制进行初步探索。具体为电子鼻监测发酵过程中的风味变化,气相色谱-质谱(gas chromatography-mass spectrometry,GC-MS)检测不同时间点挥发性成分,理化方法研究发酵过程中蛋白质的代谢变化规律。本研究将为发酵豆乳及纳豆的风味改良奠定理论基础。
1 材料与方法
1.1 材料与仪器
大豆,市售;菌种:纳豆枯草芽孢杆菌BSNK-5,实验室筛选保存[12];KH2PO4、乙醇、NaOH等试剂均购于国药集团化学试剂有限公司。
电子鼻(PEN3),德国Airsense公司;气相色谱质谱联用仪(GCMS-QP2010 Plus),日本岛津公司;酶标仪(spectra MAX190),美谷分子仪器(上海)有限公司;凯氏定氮仪(YQ205-09),意大利VELP公司。
1.2 实验方法
1.2.1 发酵豆乳的制备
1.2.1.1 种子液制备
-80 ℃保存的纳豆枯草芽孢菌BSNK-5经LB固体培养基过夜活化后,取单菌落至20 mL LB液体培养基中,200 r/min过夜培养,取1 mL菌液转接至100 mL LB液体培养基中,培养6~8 h后作为种子液备用。培养温度均为37 ℃。
1.2.1.2 工艺流程
大豆清洗→浸泡(40 ℃水浴6 h)→沥干→煮制豆乳(豆水比1∶8(g∶mL))→加400 mL豆乳于2 L摇瓶中(装液量20%)→接菌量1%→发酵(同种子液培养条件)
分别于24、48、84 h取样,以未发酵豆乳为对照(CK)。
1.2.2 发酵豆乳挥发性成分检测
1.2.2.1 电子鼻感官分析
样品预处理:取1 mL样品于20 mL顶空瓶中,瓶盖上用聚四氟乙烯隔垫密封。每个样品平行3次。
检测条件:采用顶空抽样的方法,传感器(种类详见表1)清洗时间为180 s,检测时间为60 s,自动调零时间为10 s,内部流量为300 mL/min,进样流量为300 mL/min。
表1 电子鼻传感器信息
Table 1 Sensor information of electronic nose
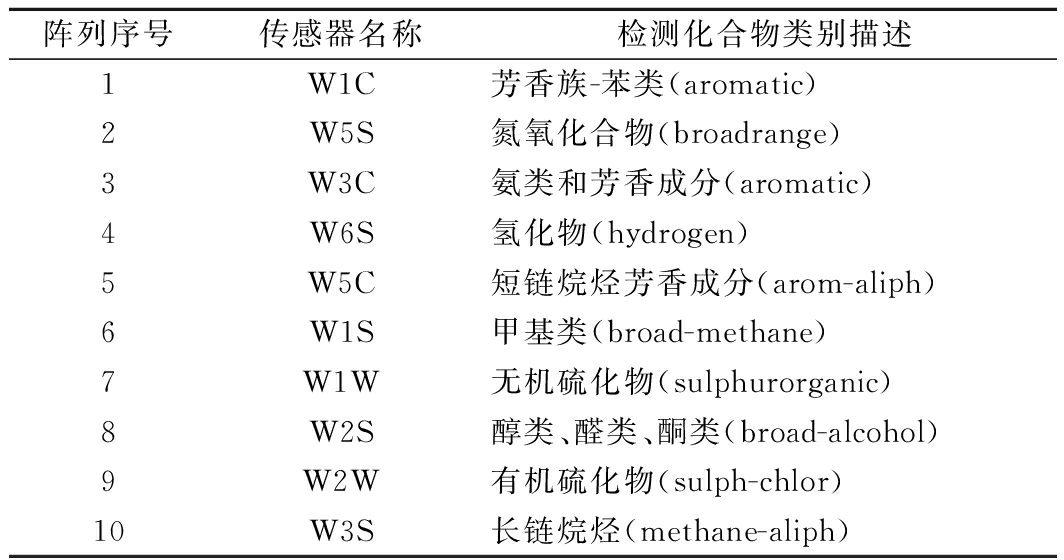
阵列序号传感器名称检测化合物类别描述1W1C芳香族-苯类(aromatic)2W5S氮氧化合物(broadrange)3W3C氨类和芳香成分(aromatic)4W6S氢化物(hydrogen)5W5C短链烷烃芳香成分(arom-aliph)6W1S甲基类(broad-methane)7W1W无机硫化物(sulphurorganic)8W2S醇类、醛类、酮类(broad-alcohol)9W2W有机硫化物(sulph-chlor)10W3S长链烷烃(methane-aliph)
1.2.2.2 GC-MS分析
样品预处理:参考黄璇等[8]的方法。取1 mL样品于15 mL顶空瓶中,在磁力搅拌器上60 ℃加热平衡后,通过隔垫插入已活化好的固相微萃取(solid-phase microextraction,SPME)萃取装置(270 ℃活化30 min),顶空吸附40 min 后,插入GC进样口解析5 min。每个样品平行6次。
色谱(GC)条件:柱型采用DB-5 ms毛细管柱(30 m×0.25 mm,0.25 μm);升温程序:柱温40 ℃保持3 min,以5 ℃/min升至150 ℃,接着以10 ℃/min 升至250 ℃,保持10 min,再以20 ℃/min升至270 ℃,保持1 min;进样口温度为250 ℃,采用不分流方式,载气(He)流量为1.0 mL/min。
质谱(MS)条件:离子源温度200 ℃,电离方式EI,电子能量70 eV,灯丝电流150 μA,扫描质量范围m/z 33~500。
1.3 理化分析
1.3.1 蛋白质含量的测定
参考GB 5009.5—2016《食品安全国家标准 食品中蛋白质的测定》第一法凯氏定氮法进行测定。
1.3.2 氨基酸态氮含量的测定
参考GB 5009.235—2016《食品安全国家标准 食品中氨基酸态氮的测定》比色法进行测定。
1.3.3 游离氨基酸含量的测定
参考GB/T 8314—2013《茶游离氨基酸总量的测定》进行测定。
1.3.4 挥发性盐基氮含量的测定
参考GB 5009.228—2016《食品安全国家标准 食品中挥发性盐基氮的测定》第二法自动凯氏定氮仪法进行测定。
1.4 数据处理
电子鼻:48~52 s数据较稳定,可进行分析。将所测得的数据使用其自带的Winmuster 软件进行主成分分析(principal component analysis,PCA)。
GC-MS:通过NIST谱库检索匹配定性,且相似度≥80(最大值为100)初步判定为目标化合物。数据以峰面积归一化法定量,得到目标化合物在样品风味物质中的相对含量,结果以![]() 的形式表示,数据用Excel处理并作饼状图。
的形式表示,数据用Excel处理并作饼状图。
理化指标:采用GraphPad Prism 7 进行作图。
2 结果与分析
2.1 BSNK-5发酵豆乳挥发性风味物质分析
前期研究证实BSNK-5通过液体发酵豆乳大量富集纳豆激酶的同时,其感官风味也发生了严重劣变[11]。如图1所示,12~36 h,发酵豆乳呈乳白色,风味口感优良;36~60 h,其颜色逐渐变黄,口感略苦,不良风味逐渐增加;60~96 h,其颜色由黄变棕,口感苦涩味加重,风味极差。

图1 不同发酵时间的BSNK-5发酵豆乳
Fig.1 BSNK-5-fermented soymilk at different fermentation time
根据BSNK-5发酵豆乳的风味变化规律,本研究以未发酵豆乳为参照,选取3个时间点取样,采用电子鼻分析风味变化规律,GC-MS鉴定不同时间点的风味物质。3个取样时间点为:24、48、84 h,结果表明,发酵豆乳24 h无不良风味、48 h不良风味较轻、84 h不良风味较重。
2.1.1 电子鼻分析BSNK-5发酵豆乳的风味变化规律
采取PCA对电子鼻检测不同时间点发酵豆乳气味信号进行分析,结果如图2-a所示,主成分1(PC1)和主成分2(PC2)的累积方差为99.60%(>85%),说明可以很好地代表传感器的主要信息特征,并准确反映样品信息。由图2-a可知,沿着PC1轴,未发酵豆乳(CK)及24、48和84 h发酵豆乳样品信息之间互不重叠,且从右到左呈现一定的变化趋势。结果表明BSNK-5发酵豆乳随着发酵时间的延长,在嗅觉上呈现一定的变化规律,这与实验过程中嗅觉闻到不良风味越来越浓郁的感官变化相一致。同时,由图2-b可知,与气味变化最密切的是氮氧化合物,整个发酵过程中其含量明显降低,其次是无机硫化物含量轻微降低,而其他类别化合物含量并无明显变化。
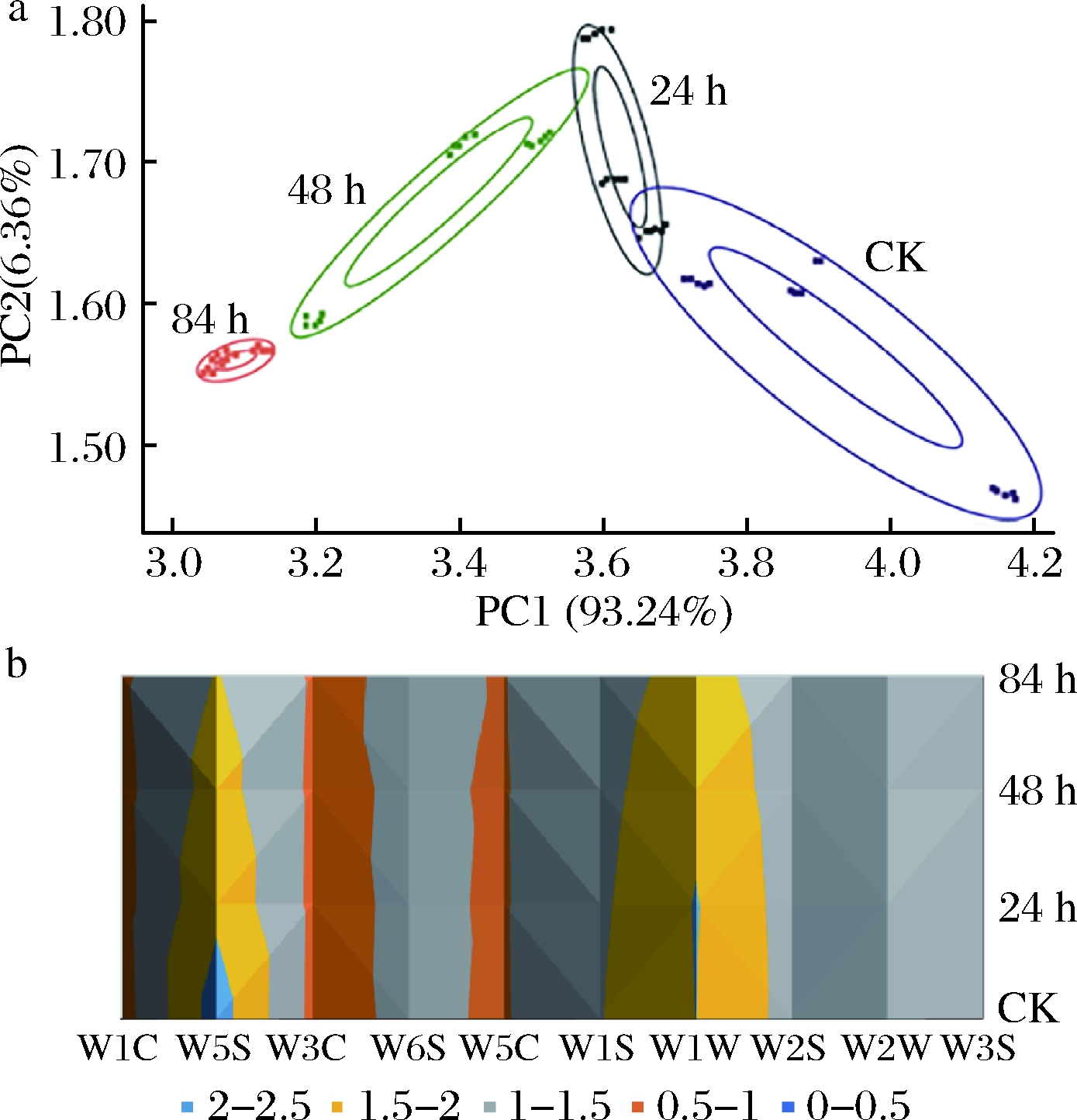
a-PCA图;b-传感信号三维图
图2 电子鼻数据分析
Fig.2 Analysis of electronic nose
2.1.2 GC-MS鉴定BSNK-5发酵豆乳挥发性物质
以上电子鼻感官分析结果表明,随着发酵时间的延长,BSNK-5发酵豆乳在风味上呈现一定的变化趋势。为了进一步探明其呈味特征,本研究采用GC-MS对上述时间点样品的挥发性化合物进行鉴定。结果如表2和图3所示,GC-MS共检测到60种风味物质,主要包括烷烃类(6种)、醇类(7种)、醛类(5种)、酮类(8种)、有机酸酯类(18种)、杂环类(10种)及未做归属的其他类化合物(6种)。未发酵豆乳及24、48和84 h样品中分别检测到26、41、54和49种挥发性化合物,分别占挥发性总成分的71.18%、83.61%、97.46%、95.72%。由此可见,发酵可以显著增加挥发性成分的种类。
表2 不同时间发酵豆乳挥发性成分
Table 2 Volatile components in fermented soy milk at different times

序号保留时间/min化合物名称相对含量(x±S)/%CK24 h48 h84 h烷烃类(6种)3.32 1.66 2.38 129.109环己烷(1-十六烷基十七烷基)0.49±0.370.48±0.271.6±0.08226.378正十九烷0.58±0.50.22±0.04323.976正十四烷1.86±0.160.49±0.04431.014正二十烷0.33±0.060.11 0.03±0.01518.4162-癸基十二烷基-环己烷0.31±0.49613.325正三十三烷0.64±0.730.22±0.05醇类(7种)25.35 15.03 20.93 6.02 129.133壬-3,5-二烯-2-醇0.43 5.65 3.03 211.4541-辛烯-3-醇24.44±0.8612.83±1.514.01±10.122.47±0.46315.663苯乙醇0.91±0.630.42±0.10.29±0.08413.162苯甲醇0.26 0.17±0.010.09±0.03514.2712-辛烯-1-醇0.68±0.750.08 630.9321-十六烷醇0.24±0.020.06 712.017辛醇0.67±0.020.6±0.04醛类(5种)9.47 0.90 2.44 7.41 110.459苯甲醛0.41 2.26±1.66.2±1.22215.484壬醛8.08 0.63 313.498苯乙醛0.65±0.210.55 431.946 顺-7-十四烯醛0.13±0.020.04±0.21 513.986反-2-辛烯醛0.85±0.250.25 0.18±0.11酮类(8种)6.19 7.32 6.26 115.0312-壬酮2.15±0.792.08±0.441.64±0.2528.4732-庚酮1.65±0.861.89±1.780.93±0.19317.1852-十一酮0.27±0.160.73±0.100.82±0.27427.6253-十五烷酮0.08±0.010.97±0.220.76±0.34530.5322-十九烷酮0.40±0.290.41±0.100.75±0.44617.039甲基辛基甲酮0.18±0.120.40±0.110.68±0.29726.2462-十三烷酮0.82±0.960.41±0.090.40 817.1932-十二烷酮0.64±0.060.43±0.150.28±0.31酸酯类(18种)2.05 34.59 8.42 9.35 18.0382-甲基丁酸9.51±0.171.05±0.451.88±2.39210.474醋酸2.34±0.761.25±0.701.18±0.2737.752异戊酸5.73±4.120.92±0.50.71 429.188花生四烯酸酯0.11±0.010.13 521.4554-癸烯酸甲酯1.19±0.231.8±1.26621.879癸酸甲酯 0.53±0.110.67±0.461.26±0.97725.566丙酸癸内酯0.36±0.060.40 831.952顺式-8,11,14-二十碳三烯酸甲酯0.04 0.39 916.058辛酸甲酯0.09±0.030.28±0.171031.715 邻苯二甲酸酯0.57±0.060.17 0.15±0.040.26±0.161130.021肉豆蔻酸甲酯0.19±0.090.23±0.11232.775 邻苯二甲酸二丁酯0.43±0.10.11 0.05±0.030.15±0.081317.817三异辛酸甘油酯0.07±0.010.07±0.031410.617环氧乙烷-2-羧酸乙酯14.34±2.230.85 1527.624Diethylmalonic acid, di(2-(3,3-dimethyl-2,4-ox-acyclopentyl)ethyl) ester0.48±0.200.29±0.060.451628.083Hydroxy-bis(4-trifluoromethyl-phenyl)acetic acid, 1-methylpiperidin-4-yl ester1.05±0.830.19 0.18±0.020.16±0.081814.076Propanoic acid, 2-methyl-, propyl ester1.19±0.40.96±0.72杂环类(10种)5.23 10.92 48.91 60.70 111.7742-正戊基呋喃5.23±0.172.57 0.95±0.140.7±0.1129.1892,5-二甲基吡嗪2.19±0.8630.69±13.3746.53±1.37
续表2

序号保留时间/min化合物名称相对含量(x±S)/%CK24 h48 h84 h312.0922,3,5-三甲基吡嗪1.83±0.377.69±0.539.71±0.7421.1792-异戊基-6-甲基吡嗪0.45±0.271.39±0.78514.5213-乙基-2,5-二甲基吡嗪2.31±1.726.88±2.910.89±1.04621.1832-甲基-3-丙基吡嗪0.46±0.070.73 715.1922-甲基-6-(1-丙烯基)吡嗪0.49±0.010.63 813.8452-甲基-3-异丙基吡嗪0.24±0.060.07 919.9092-丁基-3,5-二甲基吡嗪0.14±0.080.05 1014.708 4-Hexen-1-ol,(4E)-, acetate2.02±0.100.92±0.57其他(6种)25.76 14.32 6.82 5.32 114.797愈创木酚1.72±0.93.47±2.561.66±0.26215.511甲基麦芽酚2.81±0.620.38±0.070.68±0.12311.348苯酚0.45±0.230.33±0.2148.922甲氧基苯肟23.08±5.188.37±3.032.31±0.322.65±0.97523.97713-甲基三萜1.18±0.730.18±0.05618.7374-(2,4-Dichloro-7,8,9,10-tetrahydro-6H-5-oxa-cyclohepta[b]naphthalen-5a-yl)-morpholine1.5±0.640.97±0.690.48±0.25
注: 相对含量无标准差数据的化合物表示6组平行中只检测到1次
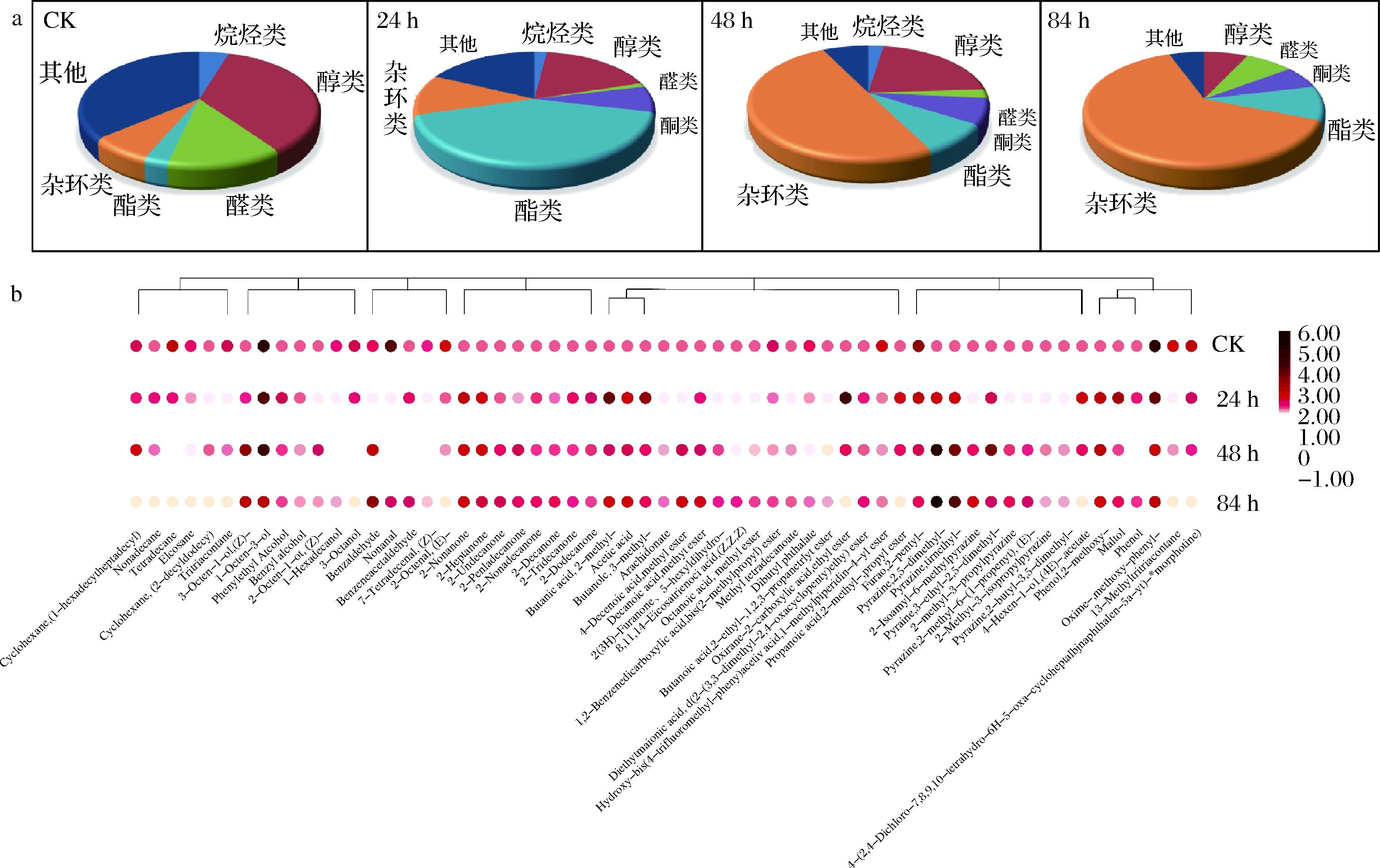
a-饼图;b-热图
图3 不同发酵时间豆乳发挥性成分含量比较
Fig.3 Comparison of active components in soy milk at different fermentation times
就整体变化趋势而言,挥发性化合物相对含量变化“从高到低”的化合物有烷烃类、醇类;“从高到低,再到高”的化合物为醛类;“从低到高,再到低” 的化合物为有机酸酯类,且在发酵24 h时达到峰点;“从低到高”的化合物为酮类、杂环类,除2-正戊基呋喃外,均从未发酵豆乳中“无”到发酵豆乳中合成。酮类化合物在3个发酵时间点几乎保持不变。杂环类化合物中2-正戊基呋喃为豆腥味物质[13],随着发酵时间的延长,其含量有所降低,说明BSNK-5有助于降解豆腥味物质;吡嗪类化合物含量在整个发酵过程中显著增加,84 h时在总挥发性成分中占比达到60.70%,其中以2,5-DMP和2,3,5-TMP为主,二者在总挥发性成分中占比分别为46.53%和9.71%,在杂环化合物中占比分别为76.65%和16.00%,说明吡嗪类化合物为BSNK-5发酵豆乳的主要呈味物质,侧面解释了电子鼻感官分析结果中氮氧化合物含量明显减少的现象,极可能转为只含氮原子的吡嗪类化合物。
2.2 理化方法分析BSNK-5发酵豆乳的蛋白质代谢变化
多数纳豆的风味研究表明2,5-DMP是引起纳豆特有风味的主要成分。吡嗪是由美拉德反应或微生物发酵产生,均与蛋白质代谢有关[14-15]。因此,本研究进一步分析了豆乳中蛋白质的代谢变化,具体测定了不同时间点发酵豆乳中蛋白质、氨基酸态氮、游离氨基酸和挥发性盐基氮的含量变化,氨基酸态氮可侧面反映小分子肽和游离氨基酸的变化,挥发性盐基氮也可表明氨基酸代谢的发生。由图4可知,随着发酵时间的延长,蛋白质含量下降;氨基酸态氮、游离氨基酸和挥发性盐基氮的含量均呈上升趋势。48与84 h相比,除挥发性盐基氮的含量明显增加外,其他指标含量差异较小,说明2个时间点的样品在蛋白质、肽和氨基酸等营养品质上差异不大,但在风味上发生了显著变化。

a-蛋白质含量变化;b-氨基酸态氮含量变化;c-游离氨基酸含量变化;d-挥发性盐基氮含量变化
图4 不同时间发酵豆乳蛋白质变化规律
Fig.4 Changes of protein in fermented soy milk at different times
注:**表示差异极显著(P<0.01);***表示差异高度显著(P<0.001)
3 讨论
本研究旨在明确BSNK-5发酵豆乳中特有风味物质,通过对不同时间点发酵豆乳的风味分析和理化检测以反映整个发酵过程中感官和挥发性成分的动态变化及其产生机制,研究发现主要是以2,5-DMP和2,3,5-TMP为主的吡嗪类化合物贡献了其特有风味,与黄璇等[8]的研究一致,同时也与本研究电子鼻感官分析结果中氮氧化合物含量的改变、蛋白质代谢中游离氨基酸等指标的显著变化相呼应,进一步加深了“吡嗪类物质与枯草芽孢杆菌发酵豆制品特有风味相关”的猜测。
吡嗪类化合物是BSNK-5发酵豆乳新增化合物,在不良风味出现时,其含量显著增加。吡嗪类化合物的阈值较低,天然发酵食品中因其含量较低多呈现优良风味,气相色谱-闻香器(gas chromatography-dfactometry,GC-O)技术分析中对2,5-DMP的风味描述为“焙烤味、坚果味、霉味和泥土味”[16],因此,在纳豆或本研究的发酵豆乳中可能因其合成量过多而引起不愉快的气味。有研究表明,枯草芽孢杆菌可代谢产生2,5-DMP和四甲基吡嗪(tetramethylpyrazine,TTMP)等吡嗪类物质[17],已知2,5-DMP的前体物质为苏氨酸,在酶催化下产生氨基丙酮,进而通过非酶促反应合成2,5-DMP[18]。但是培养基在不添加任何前体物质(苏氨酸、乙酰丙酮)的前提下,主要存在2,5-DMP和2,3,5-TMP,几乎没有TTMP[19],这与本研究中GC-MS 结果一致。而TTMP是白酒中主要香气成分,其代谢途径为糖酵解产生丙酮酸,以其为原料合成α-乙酰乳酸,再脱羧产生乙偶姻,进而分泌到胞外联合氨基酸代谢产生的游离氨合成TTMP[20],因此,推测2,5-DMP代谢干扰了TTMP的前体物质乙偶姻的合成,或者乙偶姻的竞争合成物质乙酸过量合成使TTMP合成受阻[21]。同时,BSNK-5发酵豆乳相对纳豆固体发酵氧气利用率高,也可引起吡嗪类化合物的过量合成[19]。然而,2-甲基丁酸、异戊酸等短链脂肪酸[22]作为大豆发酵制品中不良风味物质在整个发酵过程中却呈现出降低的趋势,可能由于发酵而转为“酯”,但是在一定程度上也为2,5-DMP的合成提供碱性环境[19]。蛋白质代谢的理化分析表明大豆中优质蛋白质降解为小分子肽及游离氨基酸,而挥发性盐基氮作为氨基酸进一步的代谢产物,可参与下游吡嗪等特有风味物质的合成,且BSNK-5产生蛋白酶系复杂,可能加速了“蛋白质→肽→氨基酸→游离氨→挥发性盐基氮”或“苏氨酸→2,5-DMP”等代谢过程。
本研究中未能明确特有风味物质的主要来源和合成机制,需要进一步对BSNK-5发酵豆乳中2,5-DMP、2,3,5-TMP等特有风味物质展开定量分析,并通过代谢组学和转录组学联合分析,在全面阐释发酵豆乳代谢产物谱的基础上,明确BSNK-5发酵豆乳过程中的基因表达变化,进而明确其产生机制。
4 结论
本研究以未发酵豆乳为对照,对 24、48和84 h的BSNK-5发酵豆乳开展了电子鼻和GC-MS的感官及风味分析,并结合理化指标初步研究其特有风味物质的合成机理。结果表明,发酵豆乳的风味体系因时间点不同而有显著差异,其中杂环类化合物中的吡嗪类物质是主要呈味组分,并推测2,5-DMP为发酵豆乳的特征风味物质,而引起发酵豆乳风味劣变的主要原因可能是蛋白质的分解代谢促成了2,5-DMP的大量合成,引起发酵豆乳整体的风味变化。本研究将为枯草芽孢杆菌发酵豆制品的风味改良和产业化推广奠定理论基础。
[1] 杨溢,王雅南,王雪梅,等. 纳豆激酶研究现状及展望[J]. 现代食品,2018(16):36-38.
[2] WENG Y Q,YAO J,SAWYER S,et al. Nattokinase: An oral antithrombotic agent for the prevention of cardiovascular disease[J]. International Journal of Molecular Sciences,2017,18(3):523.
[3] 邓永建,刘健,高泽鑫,等. 碳源对纳豆腐乳风味及营养成分的影响[J]. 中国酿造,2016,35(9):51-54.
[4] 张杰,赵志峰,靳岳,等. 改善纳豆风味与营养特性工艺的对比研究[J]. 中国调味品,2019,44(4):11-15;22.
[5] 付文静,王家林,张杰. 赤小豆纳豆发酵工艺的研究[J]. 食品研究与开发,2018,39(2):109-113.
[6] TANAKA T,MURAMATSU K,KIM H,et al. Comparison of colatile compounds from chungkuk-jang and itohiki-natto[J]. Bioscience Biotechnology and Biochemistry,1998,62(7):1 440-1 444.
[7] LIU Y,SONG H L,LUO H Z. Correlation between the key aroma compounds and gDNA copies of Bacillus during fermentation and maturation of natto[J]. Food Research International,2018,112:175-178.
[8] 黄璇,廖卢艳,范琳,等. 固相微萃取法分析纳豆挥发性成分[J]. 食品工业科技,2012,33(10):58-61.
[9] 刘野,苏杭,宋焕禄,等. 8种纳豆挥发性香气成分的比较研究[J]. 食品工业科技,2016,37(5):302-307.
[10] KEITAROU,KIMURA,SATOSHI Y. Trends in the application of Bacillus in fermented foods[J]. Current Oopinion in Biotechnology,2018,56:36-42.
[11] 倪楠,辛志宏,许斌,等. 纳豆激酶豆乳液体发酵条件优化[J]. 生物技术通报,2019,35(10):212-219.
[12] 赵仲麟,李淑英,聂莹,等. 纳豆激酶生产菌株分离筛选与热稳定性分析[J]. 生物技术进展,2013,3(4):277-280.
[13] STEPHANY M,KAPUSI K,BADER-MITTERMAIER S,et al. CarleOdour-active volatiles in lupin kernel fibre preparations (Lupinus angustifolius L.): Effects of thermal lipoxygenase inactivation[J]. European Food Research and Technology,2016,242(7):995-1 004.
[14] GUSTAVO L,LEONARDO S,PRABIN L,et al. Impact of different enzymatic hydrolysates of whey protein on the formation of pyrazines in Maillard model systems[J]. Food Chemistry,2019,278:533-544.
[15] SILBERSACK J,JURGEN B,HECKER M,et al. An acetoin-regulated expression system of Bacillus subtilis[J]. Applied Microbiology and Biotechnology,2006,73(4):895-903.
[16] GUSTAVO L,LEONARDO S,ANGELOS G,et al. Impact of whey protein hydrolysates on the formation of 2,5-dimethylpyrazine in baked food products[J]. Food Reaearch International,2020: 132.
[17] 汤丹丹. 枯草芽孢杆菌产吡嗪发酵条件的研究[D].济南:齐鲁工业大学,2015.
[18] ZHANG L,CAO Y,TONG J,et al. An alkylpyrazine synthesis mechanism involving L-threonine-3-dehydrogenase describes the production of 2,5-dimethylpyrazine and 2,3,5-trimethylpyrazine by Bacillus subtilis[J]. Applied and Environmental Microbiology,2019,85(24):1 807-1 819.
[19] LARROCHE C,BESSON I,GROS J B. High pyrazine production by Bacillus subtilis in solid substrate fermentation on ground soybeans[J]. Process Biochemistry,1999,34(6-7):667-674.
[20] 徐岩,吴群,范文来,等. 中国白酒中四甲基吡嗪的微生物产生途径的发现与证实[J]. 酿酒科技,2011(7):37-40.
[21] 李欣. 枯草芽孢杆菌芽孢形成阻断及碳流调控对乙偶姻合成的影响[D].无锡:江南大学,2017.
[22] HONG C L,CHEN Y Y,LI L,et al. Identification of a key gene involved in branched-chain short fatty acids formation in natto by transcriptional analysis and enzymatic characterization in Bacillus subtilis[J]. Journal of Agricultural and Food Chemistry,2017,65(8): 1 592-1 597.