多环芳烃(polycyclic aromatic hydrocarbons,PAHs)是一类由2个或多个芳香环(碳和氢原子)组成的物质,有机物质的不完全燃烧和高温分解可以产生大量的多环芳烃[1]。多环芳烃是100多种多环化学结构式的总称,其中有16种物质是高致癌的物质,是目前国际上比较关注的高危物质,它们分别为萘 (Nap)、苊烯(Any)、苊(Ana)、芴 (Flu)、菲(Phe)、蒽(Ant)、荧蒽(Flt)、 芘(Pyr)、苯并(a)蒽(Baa)、屈(Chr)、苯并(B)荧蒽(Bbf)、苯并(k)荧蒽(Bkf)、苯并(A)芘(Bap)、茚苯(1,2,3-Cd)芘(Ipy)、 二苯并(A, N)蒽(Dba)、苯并(Ghi)北(二萘嵌苯)(Bpe),很多国家对这16种多环芳烃在食物和水中的含量都做了严格的规定[2-3]。食品中的多环芳烃一方面来源于煤、煤气等不完全燃烧,另一方面来源于食品中的脂肪的不完全吸收等因素[4-8]。联合国欧洲经济委员会规定 PAHs为《长距离越境空气污染物公约》污染物之一,并且联合国环境规划署化学品处公布的《持久性有毒污染物区域评价报告》也提出,PAHs 是包括中国在内的中亚和东北亚地区需要格外关注的污染物[9-11]。但是对于这类规定在法律上是有效的,因为在界定多环芳烃这类复杂化合物的安全性上存在困难。
食品级接触材料塑料(polyethylene,PE)因其广泛的适用性而被大量的使用于食品的包装,特别是高脂食品接触材料,食品接触材料法规中一般都有材料生产中允许使用的单体及添加剂清单,某些风险物质更涉及用量和最大迁移量的要求,生产者按照此要求选择合适的原料及配比进行生产[12-14]。原料配比及工艺复杂的塑料材料,是欧美市场监管的关注重点,尤其是聚碳酸酯(polycarbonate,PC)、聚氯乙烯(polyvinyl chloride,PVC)、橡胶、涂层等。若长期食用含塑料类包装的食品势必会对人体产生潜在的危害,造成食品的潜在安全问题[15-17]。本文以16种多环芳烃为研究对象,建立多环芳烃的快速、灵敏的检测方法。同时利用4种不同基质的食品模拟物(含脂类食品模拟物、含醇类食品模拟物以及酸性和纯水机食品模拟材料)进行迁移实验研究,研究分析各类食品模拟物中多环芳烃存在的问题与原因及各种多环芳烃的暴露量,提高风险管理能力,以期为政府制定相关控制措施和政策提供技术支持。
1 材料与方法
1.1 材料与仪器
16种PAHs标准品:萘(Nap)、苊烯(Acy)、苊(Ace)、芴(Flu)、菲(Phe)、蒽(Ant)、荧蒽(Fla)、芘(Pyr)、苯并[a]蒽(Baa)、![]() (Chr)、苯并[b]荧蒽(Bbf)、苯并[k]荧蒽(Bkf)、苯并[a]芘(Baf)、茚苯[1,2,3-cd]芘(Icdp)、二苯并[a, n]蒽(Daha)、苯并[g,h,i]芘(二萘嵌苯)(Bghip)均购于德国 Dr.Ehrenstorfer GmbH公司;正己烷、异辛烷、乙醇、乙腈、甲醇(均为色谱纯)等,德国 Meker公司;冰乙酸、无水乙酸铵(均为分析纯),国药集团化学试剂公司。
(Chr)、苯并[b]荧蒽(Bbf)、苯并[k]荧蒽(Bkf)、苯并[a]芘(Baf)、茚苯[1,2,3-cd]芘(Icdp)、二苯并[a, n]蒽(Daha)、苯并[g,h,i]芘(二萘嵌苯)(Bghip)均购于德国 Dr.Ehrenstorfer GmbH公司;正己烷、异辛烷、乙醇、乙腈、甲醇(均为色谱纯)等,德国 Meker公司;冰乙酸、无水乙酸铵(均为分析纯),国药集团化学试剂公司。
气相色谱-质谱联用仪,日本岛津公司; GRE-4 氮吹仪,上海科电科技有限公司。
1.2 仪器分析条件
色谱柱HP-5MS(30 m×0.32 mm×0.25 μm);载气:氮气,流速1.0 mL/min;进样口温度: 260 ℃;程序升温:初始柱温90 ℃,保持1 min;以20 ℃/min升温至220 ℃,保持1 min;再以5 ℃/min升温至320 ℃,保持2 min。载气高纯氦(纯度>99.999%),流速1.0 mL/min。进样方式不分流进样;进样量1 μL,质谱接口温度250 ℃,离子源温度230 ℃,电离方式EI,溶剂延迟3.5 min,16种PAHs质谱参数见表1。
表1 16种PAHs保留时间、定性和定量离子
Table 1 16 PAHs retention time, qualitative and quantitative ions
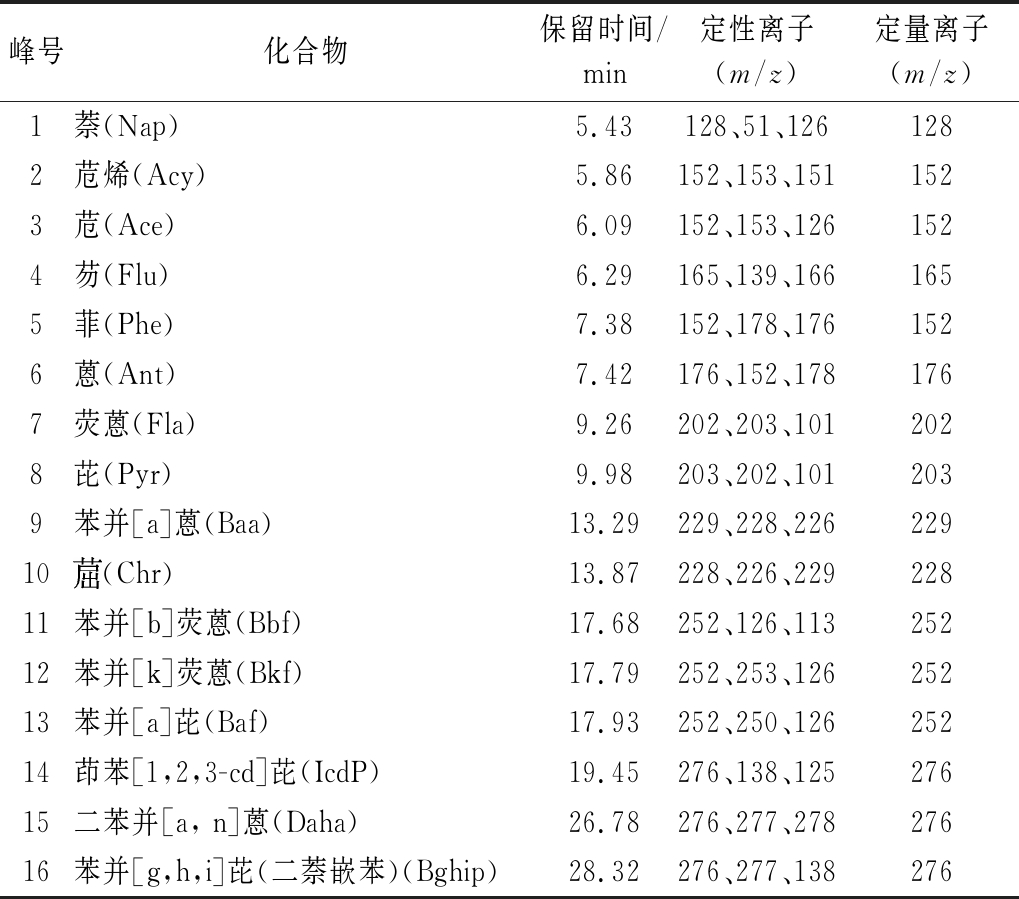
峰号化合物保留时间/min定性离子(m/z)定量离子(m/z)1萘(Nap)5.43128、51、1261282苊烯(Acy)5.86152、153、1511523苊(Ace)6.09152、153、1261524芴(Flu)6.29165、139、1661655菲(Phe)7.38152、178、1761526蒽(Ant)7.42176、152、1781767荧蒽(Fla)9.26202、203、1012028芘(Pyr)9.98203、202、1012039苯并[a]蒽(Baa)13.29229、228、22622910(Chr)13.87228、226、22922811苯并[b]荧蒽(Bbf)17.68252、126、11325212苯并[k]荧蒽(Bkf)17.79252、253、12625213苯并[a]芘(Baf)17.93252、250、12625214茚苯[1,2,3-cd]芘(IcdP)19.45276、138、12527615二苯并[a, n]蒽(Daha)26.78276、277、27827616苯并[g,h,i]芘(二萘嵌苯)(Bghip)28.32276、277、138276
1.3 实验方法
1.3.1 样品制备
多环芳烃的产生随其用量的提高(到饱和极限)而增加,一般情况下多环芳烃相对于基质而言使用量影响较大,且对人体危害较大。本实验选择各按0.03%的比例在PE粉中加入上述16 种多环芳烃标品, 搅拌均匀后,委托某塑料薄膜生产企业制作成厚度为0.17 mm的PE塑料薄片,且PE塑料薄片中所以目标物均匀分布于塑料薄片内,作为多环芳烃迁移规律研究样品。
1.3.2 16种多环芳烃迁移规律前处理
根据GB 5009.156—2016《食品接触材料及制品迁移试验预处理方法通则》[18],在食品接触材料中加入相应的食品模拟物,模拟实际使用场景,在选定迁移条件下进行迁移实验。同时参照GB 31604.1— 2015 《食品接触材料及制品迁移试验通则》[19]的检验方法进行检测,仪器条件及参数同上。
1.3.3 食品介质对16种多环芳烃迁移的影响
准确吸取迁移实验中获得的纯水基质、乙酸基质和乙醇基质食品模拟物各20.0 mL,经50 mL正己烷萃取后,氮吹尽干,用1.0 mL乙腈定容后,过0.22 μm有机滤膜过滤,供气相色谱-质谱联用仪(gas chromatograph-mass spectrometer,GC-MS)检测用。对于油基食品模拟物:精确移取迁移实验中得到油基异辛烷食品模拟物20.0 mL于50 mL具塞离心管中,净化液于氮吹仪中45 ℃氮气吹干,用1.0 mL 乙腈互溶,过膜后,供GC-MS检测用。
1.3.4 乙醇体积分数对16种多环芳烃迁移的影响
分别配制体积分数为5%、10%、20%、30%、40%、50%、60%、70%、80%、90%的乙醇溶液作为醇类食品模拟物,常温下分别进行迁移实验,取迁移实验中得到的样液20.0 mL,经正己烷提取氮吹尽干后,用1.0 mL乙腈定容后,过0.22 μm滤膜过滤,供GC-MS仪器测定用。
1.3.5 乙酸质量浓度对16种多环芳烃迁移的影响
分别配制质量浓度为10、20、40、60、80、100、120、140、180、200、300和400 g/L的乙酸溶液作为酸性食品模拟物,其余步骤同1.3.3。
1.3.6 接触温度对16种多环芳烃迁移的影响
分别选取5、10、20、30、40、50、60、70、80 、90、100 ℃11种不同的接触温度条件下进行迁移实验,选用100 g/L乙酸溶液为食品模拟物,接触时间为4 h,其余步骤同1.3.3。
1.3.7 食品模拟物浸泡时间对16种多环芳烃迁移的影响
选用100 g/L乙酸溶液为食品模拟物,常温下进行食品,分别浸泡1、2、4、6、8、12、24、48、72 h进行迁移实验,其余步骤同1.3.3。
2 结果与分析
2.1 不同基质食品模拟物对多环芳烃迁移规律的影响
本实验选用蒸馏水、50%(体积分数)乙醇、200 g/L 乙酸和异辛烷进行迁移实验研究,这些食品模拟物分别模拟纯水基质食品、含醇类食品、酸性食品和含脂类食品4种不同的基质,且根据国内外的相关报道具有代表性。上述4种基质模拟物在常温下浸泡24 h,并对16种多环芳烃的迁移规律进行研究,每种食品基质模拟物平行测定6 次,取平均值,结果见表2。
表2 不同基质食品模拟物中PAHs迁移量检测结果
Table 2 Results of determination of PAHs migration in different matrix food simulants

注:ND表示未检出
多环芳烃蒸馏水200 g/L乙酸溶液50%(体积分数)乙醇异辛烷迁移量/(mg·L-1)RSD/%迁移量/(mg·L-1)RSD/%迁移量/(mg·L-1)RSD/%迁移量/(mg·L-1)RSD/%NapNDND0.065.870.124.56AcyNDND0.033.450.093.21AceNDND0.062.130.213.76FluND0.025.670.084.650.125.45PheND0.014.430.122.340.261.21Ant0.032.350.044.530.132.870.326.78Fla0.043.130.063.590.095.900.153.67Pyr0.053.220.083.160.082.670.177.87BaaND0.022.980.073.690.274.54CfrND0.031.560.091.340.182.34BbfND0.034.650.091.980.236.78BkfND0.023.570.132.321.214.13Baf0.032.980.082.560.104.540.892.34Icdp0.022.160.054.120.241.460.951.56DahaND0.043.230.103.120.872.97BghipND0.061.270.234.980.534.65
由表2可以看出,PAHs的迁移量受不同模拟物基质影响不同,差别较大。蒸馏水基质模拟物除对Ant、Fla、Pyr、Baf、Icdp五种PAHs有一定溶出外,对其余的11种PAHs都没有溶出,表明纯水基质食品模拟物对PAHs的溶出迁移量不大。酸性食品模拟物相比于纯水基质食品模拟物有更强的溶解性,除了Nap、Acy、Ace三种PAHs未有溶出外,其余的13种PAHs化合物均有不同浓度的溶出;含醇类食品模拟物和脂肪类食品模拟物对16种PAHs均有不同程度的溶出,且溶出值较大。
2.2 乙酸质量浓度对PAHs迁移规律的影响
选择在常温条件下考察乙酸质量浓度为10~400 g/L时PAHs的迁移规律,本实验采用不同浓度乙酸溶液浸泡食品接触塑料材质24 h,不用乙酸浓度下PAHs的迁移规律见图1。
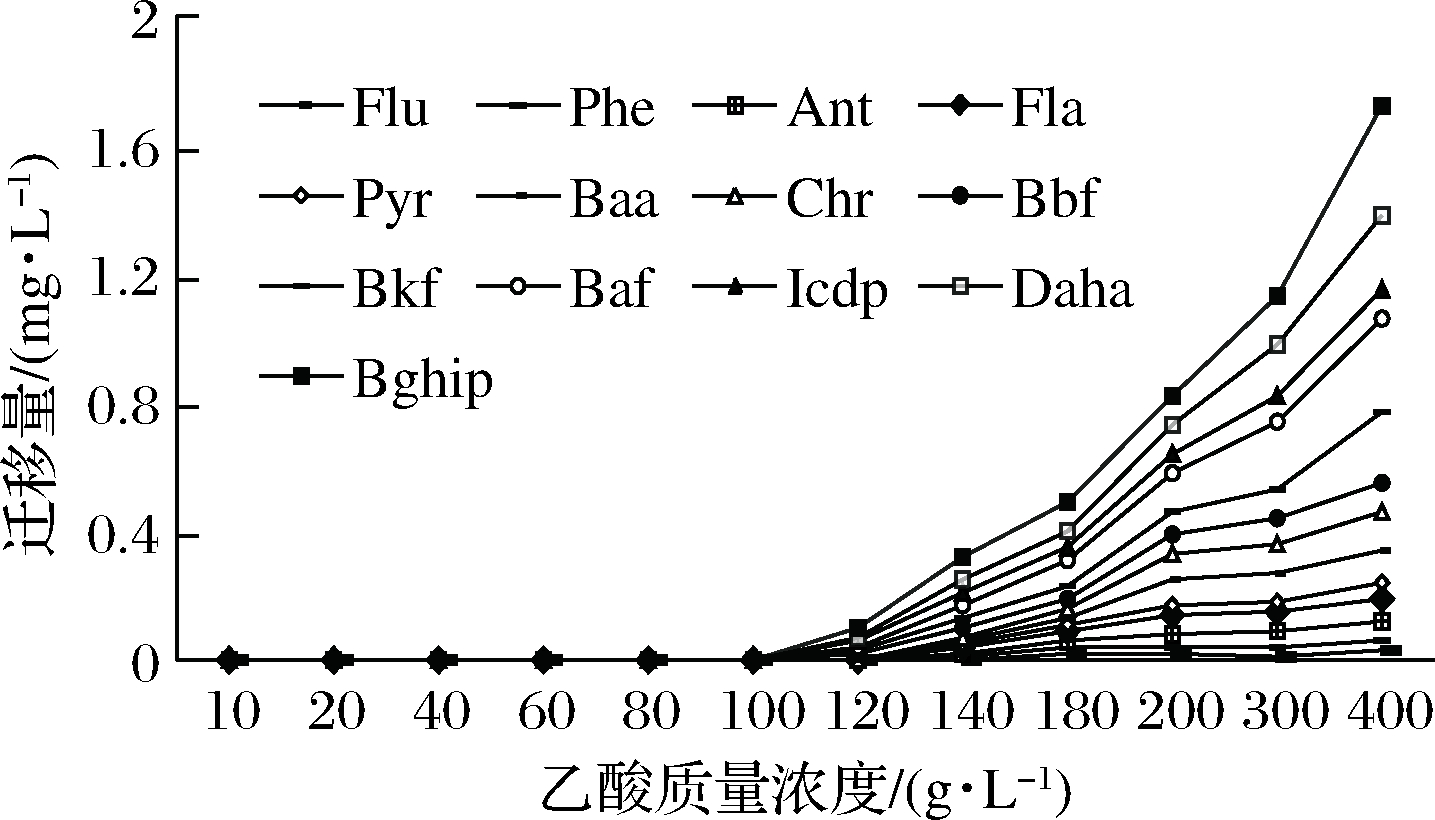
图1 乙酸质量浓度对PAHs迁移情况的影响
Fig.1 Effect of acetic acid concentration on the migration of PAHs
由图1可以看出,除了Nap、Acy、和Ace三种多环芳烃没有溶出外,其余13种PAHs均有溶出,且随着乙酸质量浓度的升高而增加,在乙酸溶液质量浓度为10~100 g/L时13种PAHs溶出结果为0,而到120 g/L时,溶出物质的含量随乙酸溶液质量浓度的升高而不断增加,同时Bghip的溶出浓度要明显高于另外几种PAHs。
2.3 乙醇体积分数对PAHs迁移情况的影响
选择在30 ℃接触条件下,用体积分数为5%~90%乙醇溶液分别浸泡食品接触材料24 h,考察不同的乙醇体积分数下PAHs的迁移情况,结果见图2。
由图2可以看出,随着乙醇溶液浓度的增加,16种PAHs的迁移量增大,且乙醇体积分数为80%时,PAHs的迁移量最大,为浓度为20%乙醇溶液的30倍,同时每种PAHs都有不同程度的溶出,由此可以看出不同乙醇溶液对16种PAHs的迁移具有较大影响,且随着浓度的增加迁移量增大。
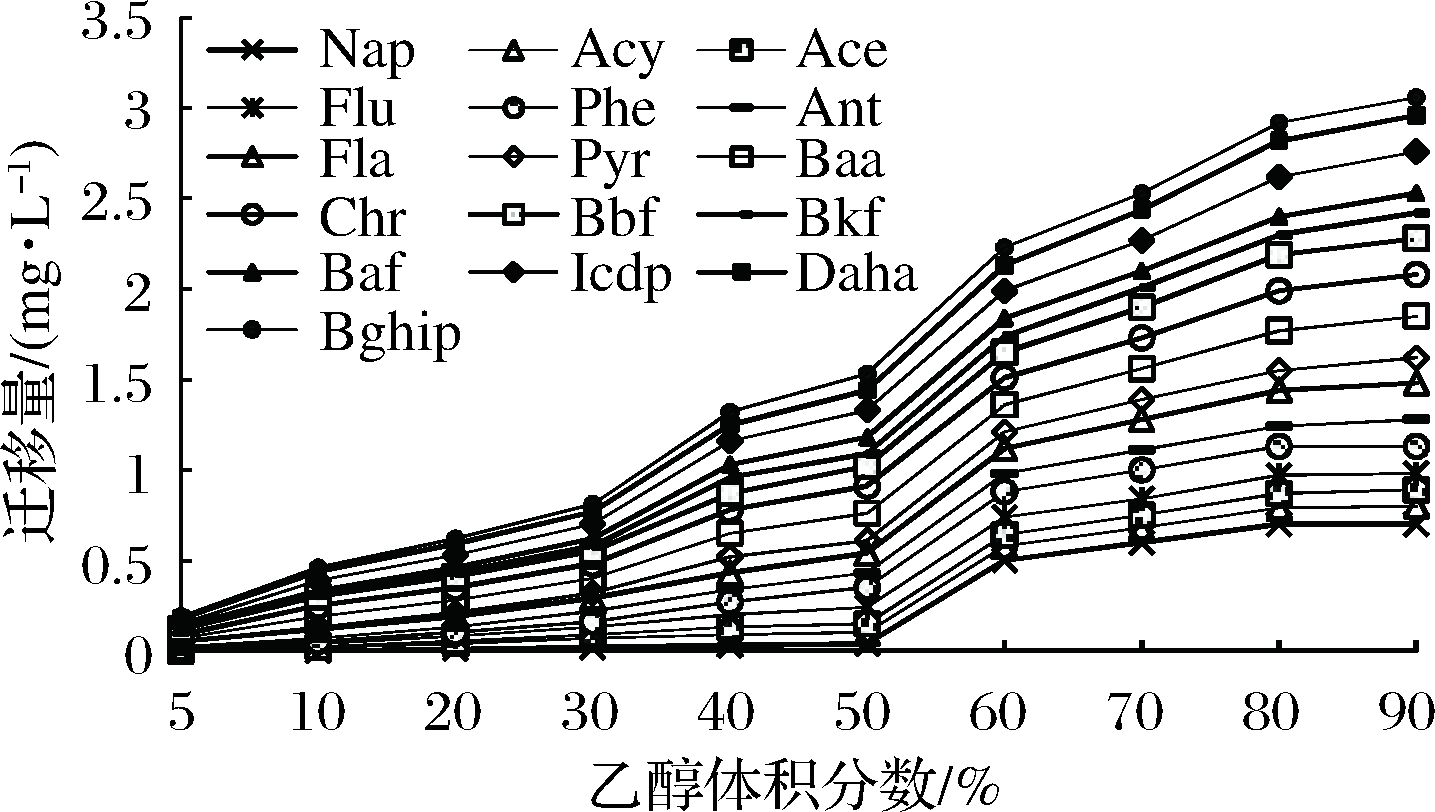
图2 乙醇体积分数对PAHs迁移情况的影响
Fig.2 Effect of ethanol concentration on the migration of PAHs
2.4 接触温度对PAHs迁移情况的影响
为了了解不同食品接触材料塑料在不同接触温度下释放出多环芳烃的迁移量,实验选用100 g/L的乙酸为食品接触模拟物,考察温度在5~100 ℃条件下,接触时间为24 h时,16种多环芳烃的迁移规律,根据自由体积理论学说,当化合物温度升高时,不同体积分子的活化能较大,化合物就越容易迁移[20-21],不同接触温度下的PAHs迁移结果见图3。

图3 接触温度对PAHs迁移情况的影响
Fig.3 Effect of contact temperature on the migration of PAHs
由图3可以看出,塑料包装PE材料中PAHs的迁移量随着温度的升高而增大,在100 ℃时BghiP的最大迁移量达到5 ℃时的25倍,在低温(5~40 ℃)条件下PAHs的迁移量变化较小但是随着接触温度的升高, PAHs的迁移量也随之增大。当温度高于70 ℃时,PAHs的迁移量骤然增大,且随着温度的升高,迁移量增幅变大,由此可以看出温度的增加对PAHs化合物的迁移具有显著影响。
2.5 接触时间对PAHs迁移情况的影响
通常情况下,随着食品在塑料包装材料中的接触时间的增长,PAHs化合物在接触材料中的迁移溶出率会变大。为了了解食品PE塑料材料在不同接触时间下PAHs的迁移情况,实验选用乙醇体积分数为50%的醇类物质为模拟物,在常温条件下进行接触实验,考察食品包装塑料材质在不同时间段的迁移变化规律,结果见图4。

图4 接触时间对PAHs迁移情况的影响
Fig.4 Effect of exposure time on PAHs migration
由图4可以看出,随着接触时间的延长,PAHs的迁移量也随之增加,但到达最大值后迁移量不在增加,在48 h内,各种PAHs的含量都呈增长状态,但在第48 h迁移量出现峰值后,PAHs迁移量变化不大,表明PAHs随着时间的延长迁移量不会逐渐增多。由于本实验中使用体积分数50%乙醇溶液具有一定的挥发性,随着实验时间的不断延长,乙醇溶液不断挥发,乙醇含量逐渐降低,这可能是导致PAHs迁移量不再增加的一个重要原因。
3 结论
本实验采用已建立的食品接触塑料材料中PAHs的检测方法,采用4种具有代表性的食品模拟物包括有异辛烷、体积分数为50%乙醇溶液、质量浓度为200 g/L乙酸溶液和蒸馏水,对不同基质食品模拟物的PAHs进行迁移规律研究,同时考察不同乙醇体积分数、乙酸质量浓度和不同接触时间和温度对PAHs迁移规律的影响。结果表明,纯水基质食品模拟物对PAHs有一定溶解性但迁移量不明显,酸性食品模拟物则具有更强的溶解性,而含醇类食品和脂肪类食品模拟物对大部分PAHs都具有较好的溶解效果;对16种PAHs进行不同温度、时间等的迁移实验研究,结果显示PAHs的溶出量随着乙酸质量浓度和乙醇体积分数的增加而增加;对不同温度下的PAHs溶出情况的实验表明,较高的温度对塑料包装材料中PAHs的迁移溶出具有显著影响,并且随着接触时间的延长,塑料包装材料中的PAHs向食品中迁移的可能性也不断加大。
[1] 邓棋霏,郭欢,张晓敏,等.多环芳烃的健康损害及其健康监护[J].中华劳动卫生职业病杂志,2014,32(2):149-151.
[2] 段小丽,陶澍,徐东群,等.多环芳烃污染的人体暴露和健康风险评价方法[M].北京:中国环境科学出版社,2011:49.
[3] 毛明英,刘守琼,宋磊,等.塑料食品包装制品中多环芳烃的分析及检测[J].包装工程,2009,30(1):43-45.
[4] 乌日娜.多环芳烃在食用植物油加工工艺中的污染特征研究[D].北京:中国农业科学院,2016.
[5] 张云,吕水源,张信仁,等.食品包装PE材料中荧光增白剂迁移规律的分析[J].食品科学,2018,39(2):298-302
[6] RICHARD J L. Some major mycotoxins and their mycotoxicoses:An overview[J]. International Journal of Food Microbiology, 2007,119(1-2): 3-10.
[7] SCHATZMAYR G, ZEHNER F, T UBEL M et al. Microbiologicals for deactivatingmycotoxins[J].Molecular Nutrition & Food Research, 2006, 50(6): 543-551.
UBEL M et al. Microbiologicals for deactivatingmycotoxins[J].Molecular Nutrition & Food Research, 2006, 50(6): 543-551.
[8] BHAT R, REDDY K R N. Challenges and issues concerningmycotoxins contamination in oil seeds and their edible oils: updates from last decade[J]. Food Chemistry, 2017,215:425-437.
[9] CARVAJAL-MORENO M. Metabolic changes of aflatoxin B1 to becomean active carcinogen and the control of this toxin[J]. Immunome Research, 2015, 11(3): 2-14.
[10] ABRAR M, ANJUM F M, BUTT M S, et al. Aflatoxins: Biosynthesis, occurrence, toxicity, and remedies[J].Critical Reviews in Food Science and Nutrition, 2013, 53(8): 862-874.
[11] WILLIAMS J H, PHILLIPS T D, JOLLY P E, et al. Human aflatoxicosis in developing countries: A review of toxicology, exposure, potential health consequences, and interventions[J]. The American Journal of Clinical Nutrition, 2004, 80(5): 1 106-1 122.
[12] WU F, GROOPMAN J D, PESTKA J J. Public health impacts of foodborne mycotoxins[J]. Annual Review of Food Science and Technology, 2014, 5(1): 351-372.
[13] CHEN C, MITCHELL N J, GRATZ J, et al. Exposure to aflatoxin and fumonisin in children at risk of growth impairment in rural Tanzania[J]. Environment International, 2018, 115: 29-37.
[14] 曹梦思,王君,张立实,等.我国食用油脂中欧盟优控15+1种多环芳烃的污染状况分析[J].中国食品学报,2016,16(12):198-205.
[15] MANSOUR M,JAVAD M,MIR-MICHAEL M,et al. Application of the microwave-assisted extraction and dispersive liquid-liquid microextraction for the analysis of PAHs in smoked rice [J]. Food Analytical Methods, 2017,10:277-286.
[16] 李进伟,王兴国,金青哲.食用油中苯并芘的来源、检测和控制[J].中国油脂,2011,36(6): 7-11.
[17] 王珍,王琳琳,陈小鹏,等.超声波辅助-DMC萃取食用油中苯并[a]芘及其GC/MS分析[J].广西大学学报, 2013,38(3):538-543.
[18] 国家卫生和计划生育委员会.GB 5009.156—2016食品接触材料及制品迁移试验预处理方法通则[S].北京:中国标准出版社,2016.
[19] 国家卫生和计划生育委员会. GB 31604.1—2015食品接触材料及制品迁移试验通则[S].北京:中国标准出版社,2015.
[20] 钟秋,何茂刚,张颖.基于自由体积理论和摩擦理论的流体自扩散系数预测模型[J].高校化学工程学报,2012,26(6): 9 923-9 928.
[21] 吕宏凌,王保国.高分子聚合物中溶剂扩散系数的预测[J].化工学报,2006,57(1): 6-12.