The effect of cyclic irradiation of low-intensity UV-A combined with ε-Polylysine on the preservation of fresh-cut spinach at 4 ℃
ABSTRACT In order to investigate the effect of UV-A illumination combined with ε-polylysine on fresh-cut spinach, the optimum preservation concentration of ε-polylysine solution was determined by sensory indicators, water loss, microbiological indicators, antioxidant enzyme indicators and nutritional indicators. The results indicated that 0.05 g/L ε-polylysine solution had the best preservation effects on fresh-cut spinach combined with UV-A (0.588 kJ/m2) illumination, which was conducted at an interval of 8 h. And it can extend shelf life of spinach to 12 d. 0.02 g/L ε-polylysine solution treatment could extend shelf life of spinach to 10 d with the radiation of UV-A (0.588 kJ/m2), which was conducted at an interval of 8 h. However, 0.08 g/L ε-polylysine solution showed no obvious preservation effect on spinach with the radiation of UV-A (0.588 kJ/m2), which was conducted at an interval of 8 h. In conclusion, appropriate intensity UV-A light combined with ε-polylysine solution could not only slow down the growth of spoilage bacteria but also maintain the good antioxidant properties of spinach. It could provide a new development direction on the preservation of spinach for supermarkets, and attention should also be paid to the appropriate dosage in practical application.
Key words fresh-cut spinach; UV-A lillumination; ε-polylysine; compoumd preservation; antioxidant activity
菠菜是一种常见的可食用蔬菜,其叶片和茎为主要食用部分,人们常常将其鲜切后进行烹饪或置于4 ℃下贮藏,其因膳食纤维丰富、营养全面受到不同年龄人群的青睐[1],但鲜切后的菠菜易发生汁液流失且愈伤呼吸剧烈[2],同时菠菜鲜切部分易受到腐败菌侵染,一旦微生物进入植物机体内部会加快作物腐败[3],这些特点都加剧了鲜切菠菜相关代谢酶的降解进程及微生物对其的侵染,因此应探寻适宜的保鲜方式,提高菠菜的商品价值。
紫外线波长介于320~400 nm的光被称长波紫外线,是紫外辐射中危害最小的部分[4],相比UV-B、UV-C能量较低,处理叶菜类作物较为温和,同时UV-A光照对植物抗氧化能力有一定程度的强化作用。SURJADINATA等[5]的研究中指出,通过UV-A光照处理不仅可以显著提升阿魏酸、绿原酸、异香豆素等酚类物质的含量,还对超氧化物歧化酶(superoxide dismutase,SOD)、过氧化物酶(peroxidase,POD)等氧化代谢酶等活性有一定的增强作用。在可推广性上,目前市场上大部分UV-A灯管材质为LED灯珠,具有波长稳定、寿命长、产热小、造价低廉等优势,具有极大的应用潜力,郁杰等[6]将UV-A光应用于鲜切菠菜,其结果表明,在420 s(1.764 kJ/m2)的照射条件下,可将鲜切菠菜货架期延长至10 d,UV-A光照能够显著提升鲜切菠菜的抗氧化能力,延缓衰老,但采后叶菜本身极易失水,因此应选择适宜的光照强度和频率以及其他辅助手段,避免叶菜失水。
ε-聚赖氨酸(ε-polylysine,ε-PL)属于天然防腐剂,由多个赖氨酸残基聚合而成,ε-PL 已于2003年10月被美国FDA 批准为安全的食品保鲜剂[7],其摄入人体内可降解成赖氨酸被人体吸收。通常ε-PL以其优异的抑菌性能常与其他保鲜剂协同应用于果蔬保鲜[8-9]。还有文献指出ε-PL具有一定光敏性,经一定波长的光照会在体外产生活性氧,从而达到更强的抑菌的效果[10]。因此,本实验以不同浓度的ε-PL溶液协同UV-A光照应用于鲜切菠菜,探究保鲜效果,为商超物流、贮运等过程中鲜切菠菜保鲜工艺的改良提供新的发展方向。
1 材料与方法
1.1 材料、试剂及仪器
1.1.1 实验材料
菠菜样品来源:于3月份采摘,大棚种植环境温度为12~15 ℃、相对湿度为80%,菠菜为有刺种,要求大小统一、叶片均匀、无病虫害,采摘后立即于20 min内送达实验室进行预处理。
1.1.2 实验试剂
丙酮、石英砂、碳酸钙粉、HCl(分析纯),国药集团化学试剂有限公司;KNO3,上海阿拉丁生化科技股份有限公司;超氧化物歧化酶测试盒,南京建成生物科技有限公司;三氯乙酸(>99%),上海生工生物工程有限公司;革兰氏阴性菌培养基(G-)、假单胞菌琼脂培养基(CFC),青岛海博生物技术有限公司。
1.1.3 仪器与设备
高速冷冻离心机(H-2050R-1型),长沙湘仪离心机有限公司;微型计算机(D30D),戴尔公司;高温高压灭菌锅(HVE-50),日本Hi-rayama制造有限公司;超净工作台(VS-1300L-U),上海康福特环境科技有限公司;冰箱(BCD-252MHV型),苏州三星电子有限公司;植物紫外线UV辅助补光灯(9 W/0.6 m),山东贵翔光电有限公司;光强测定仪(ST-513),先驰光电股份有限公司;紫外可见分光光度计(UV-1102型),上海天美仪器有限公司;色差计(CR-400型),KONICA MINOLTA公司。
1.2 实验方法
1.2.1 样品的鲜切处理及分组
以自来水冲洗去泥污,直至洗涤后的废水仍为澄清,代表清洗完成;10 min内晾干,随后距菠菜叶片茎部约4 cm处鲜切。将鲜切后的菠菜分为四大组,每大组分为8小组,每小组分装60 g/盒。
1.2.2 ε-PL溶液的保鲜处理
将鲜切菠菜分别浸泡于0.02、0.05、0.08 g/L的ε-PL溶液,分别标为A组、B组、C组,对照组使用无菌蒸馏水浸泡,标为CK组;30 s后取出通风晾干,分装放入无菌盒,并用无菌PE高透光防雾膜包好。
1.2.3 UV-A照射与参数确定
在前期的实验中根据不同光照总量和频率筛选得出最佳照射方式即:灯管垂直距离受照鲜切菠菜为30 cm,单次光照间隔8 h,光照持续140 s(0.588 kJ/m2)[10]。光参数用光强测定仪(ST-513)测定,灯下垂直30 cm处透过防雾膜的光照强度为4.2 W/m2,峰值波长399 nm,半波宽16.6 nm,主波长430.32 nm,色纯度98.2%,光量子通量密度9.82 μmol/(m2·s),将A、B、C实验组置于该条件下进行实验。
1.3 指标测定
1.3.1 感官评定
评定小组由10名专业感官评定人员组成,每人评定3次。评定参照PAILLART等[11]的标准,评定后所得分数越高代表品质越好,满分为10分,隔天评价1次。
1.3.2 色度变化值
参考ERICK等[12]的方法,参照公式(1)计算色度变化值ΔE*:
(1)
式中:![]() 为样品初始(第0天)色度值,
为样品初始(第0天)色度值,![]() 为样品贮藏后的色度值。
为样品贮藏后的色度值。
1.3.3 光合色素含量
参照NY/T 3082—2017[13]标准,参照公式(2)计算总叶绿素的含量,使用分光光度法测定总叶绿素、叶绿素a、叶绿素b的含量,并计算脱镁叶绿素、类胡萝卜素的含量。
(2)
式中:G,1 g样品中叶绿素的含量,mg/g;A645,在645 nm处测得的提取液的吸光度值;A663,在663 nm处测得的提取液的吸光度值;VT,提取液的总体积,mL;n,提取液为稀释倍数;m,鲜切菠菜鲜质量,g。
1.3.4 失重率
根据公式(3)计算失重率:
失重率![]()
(3)
式中:M0,第0天的鲜切菠菜的初始质量,g;M1,每隔1 d称量1次鲜切菠菜的质量,g。
1.3.5 革兰氏阴性菌的计数
参考郁杰等[14]的实验方法进行计数。
1.3.6 假单胞菌的计数
参考郁杰等[14]的实验方法进行计数。
1.3.7 亚硝酸盐含量
参照GB 5009.33—2016[15]标准测定。
1.3.8 丙二醛(malondialdehyde,MDA)含量
参照GB 5009.181—2016[16]标准测定。
1.3.9 超氧化物歧化酶(superoxide dismutase,SOD)含量
参照超氧化物歧化酶测试盒中的羟胺法。
1.3.10 可溶性固形物含量
将样品充分研磨后,在4 000 r/min的条件下离心10 min,取上清液滴加至检测镜上,合上盖板防止产生气泡,水平对准光源准确读取刻度尺读数,以质量分数(%)表示,重复3次。
1.3.11 VC含量
参照GB 5009.86—2016[17]标准测定。
1.4 数据处理及分析
所有指标设3次平行,取平均值后用Origin 8.5软件绘图,并使用SPSS Statistics 24软件对组间数据进行Duncan氏新复极差法显著性分析(P<0.05即存在显著差异)。
2 结果与分析
2.1 表观指标
2.1.1 感官评定
消费者们通过感官可以直观地了解到商品的属性及状态,是影响购买意向的直接因素。由图1可知,新鲜菠菜表观呈墨绿色,叶片较大,质地挺拔,具有固有香气。随着贮藏时间的增加,各组分值呈下降趋势,具体依次表现为固有气味的消失、叶片质地发软萎焉、叶片发黄。在第4天,B、C组差异不明显,打开包装仍有固有香气,叶片轻微失水,但未见萎焉,消费者接受度最好,其次为A组,之后C组品质劣变较快,在第8天打开包装带有臭味,叶片发生软腐,和CK组一样,货架期都为8 d,而A组货架期为10 d,B组为最长达12 d。
2.1.2 色度变化值
通过色度值ΔE*可以量化叶片颜色的变化,由图2可知,随着贮藏时间的延长,ΔE*呈先上升后下降的趋势,这表明随着贮藏时间的延长,叶片出现黄化、发白,到了贮藏后期叶片出现冷害发黑,故颜色加深,ΔE*下降,在所有组别中,B组颜色变化幅度最小,能有效控制叶片黄化,其次为A组,C组变化幅度最大且大于CK组,这是因为相对高剂量的ε-PL溶液处理使得外界逆境强度增加,加剧了体内活性氧的产出,使得鲜切菠菜衰老。
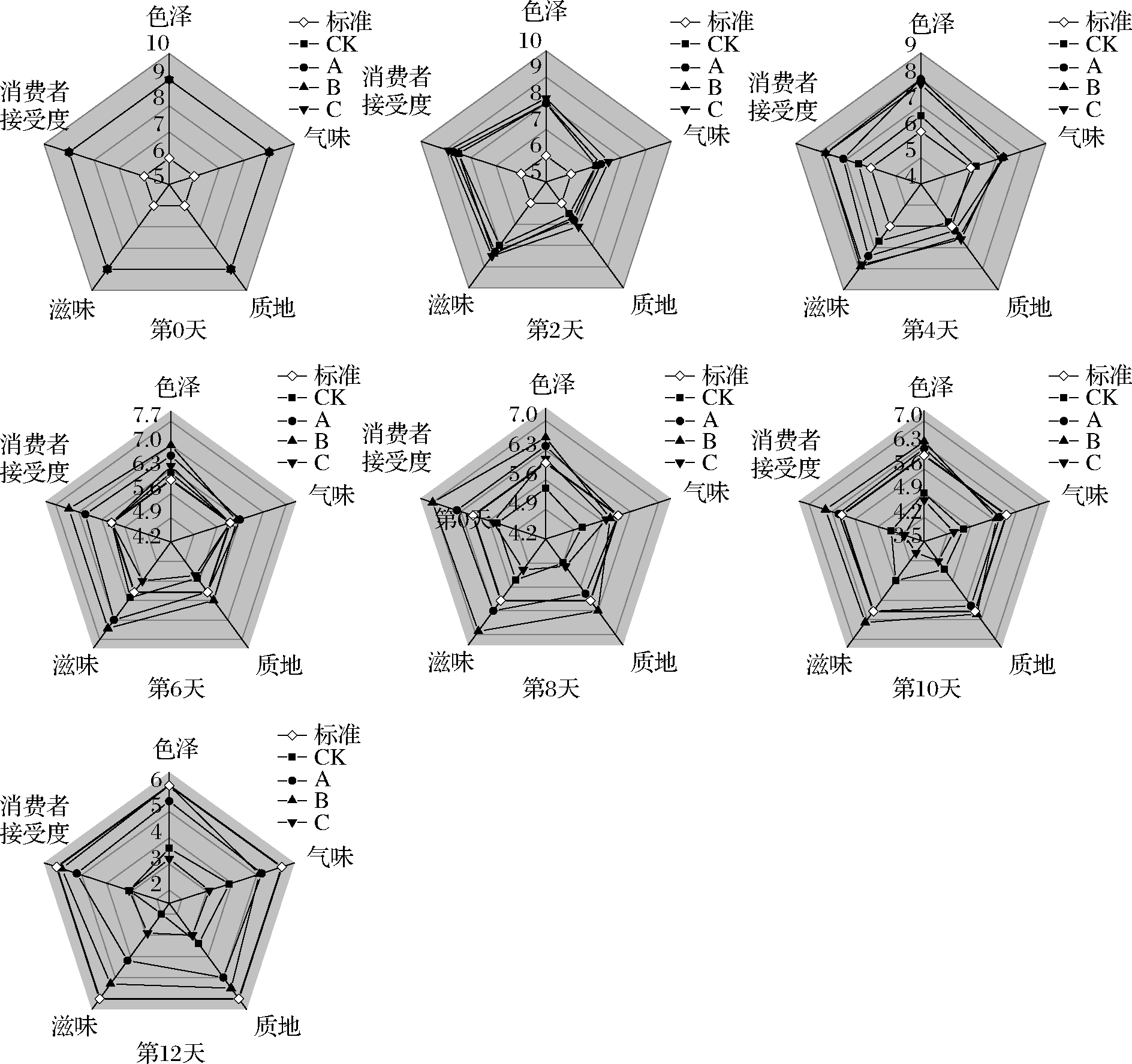
图1 不同处理方式对鲜切菠菜感官品质的影响
Fig.1 Effects of different treatments on sensory quality of
fresh-cut spinach
注:图中白色方块表示消费者最低感官接受度,即:标准
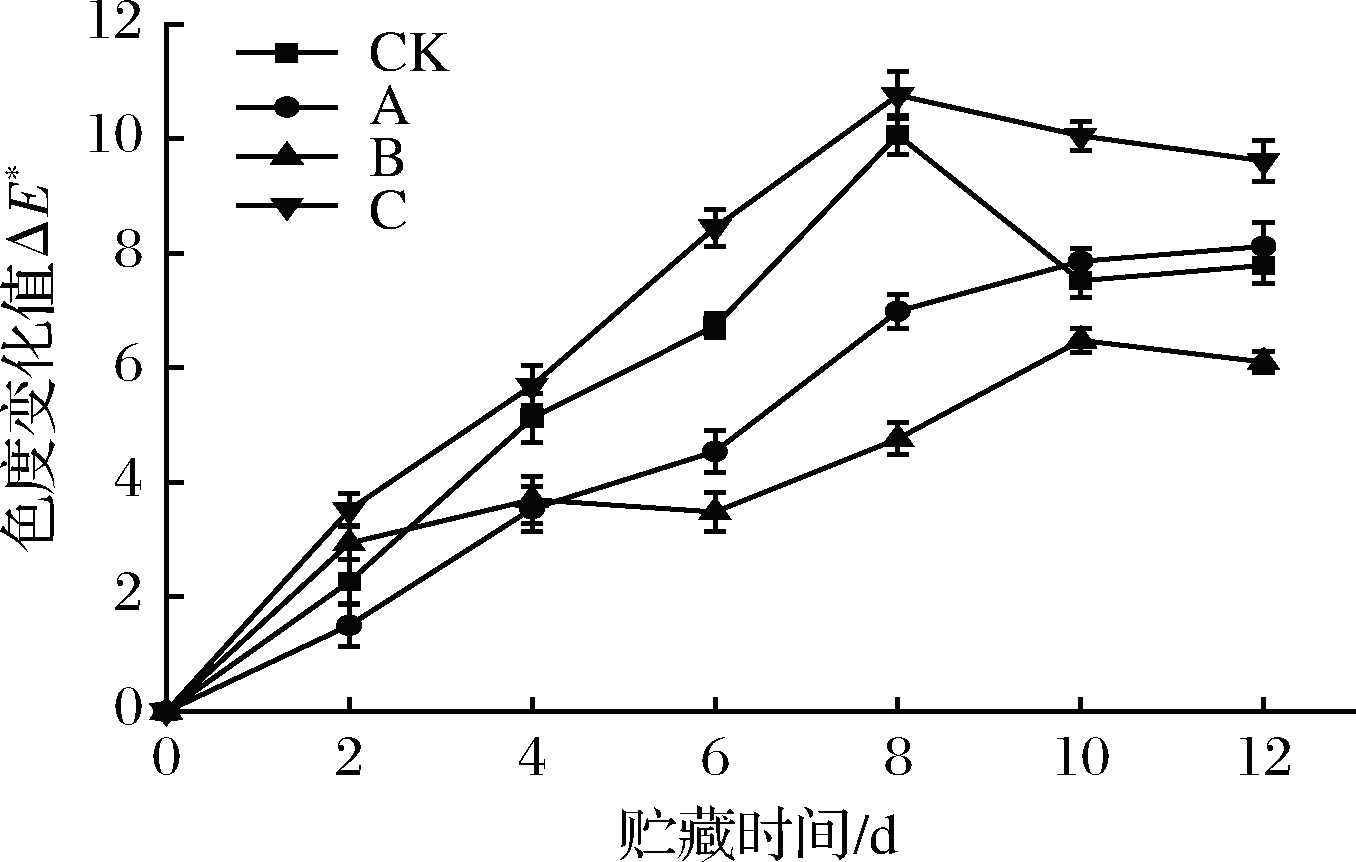
图2 不同处理方式对鲜切菠菜ΔE*的影响
Fig.2 Effects of different treatments on ΔE* of
fresh-cut spinach
2.1.3 叶绿素含量
在高等植物中,叶绿素分子结构上是以镁原子为中心的卟啉环,主要功能是捕捉光量子,但随着贮藏时间的延长,表观上叶片会发生褐变,主要因为当镁原子被氢原子取代后形成脱镁叶绿素,呈棕褐色,因此测定两者的含量可以反映叶片的褪绿情况[18]。由图3-a可知,从总体趋势来看叶绿素含量均呈下降趋势,这是因为:(1)采摘后菠菜失去母体营养,光反应速率大幅放缓,而暗反应在4 ℃的冷藏条件下酶促反应速率降低导致光合作用不活跃。(2)光合系统Ⅰ中铁氧蛋白受体很容易将分子态氧还原成对生物膜有害的活性氧![]() 假单胞菌属在贮藏过程中大量繁殖产酸,叶绿素分子对外界环境的pH值十分敏感。因此,在以上因素的综合作用下导致叶绿素分子被破坏降解形成脱镁叶绿素。在前4 d,各组含量差异不大(P>0.05);在6~8 d时,A、B、C组间差异不明显,但CK组含量显著低于实验组。8 d后,B组含量最高,其次为A组,C组叶绿素含量最低且低于CK组,这是因为A、B组凭借良好的抑菌性能限制腐败菌增殖产酸从而控制pH值的变化,C组ε-PL浓度最高且贮藏过程中失水严重,故叶片组织液浓度也随之上升,加剧酶促反应,使得代谢失衡。由图3-b可知,脱镁叶绿素呈先上升后下降再上升的趋势,之后UV-A光照射短暂激活了叶绿素分子光代谢途径,使得叶绿素分子降解放缓。由图3-b可知,在前2 d,CK、A、C组含量上升不明显,B组脱镁叶绿素含量最早达到最高值显著高于其他组,之后缓慢下降,这与图3-a得变化趋势相符。到了第6天,A、C组达到最高值,之后剧烈降低,表明菠菜即将抵达贮藏终点,叶绿素被完全破坏。到了第10天,各组含量呈上升趋势,C组含量最高,其次为CK组,最低为B组。
假单胞菌属在贮藏过程中大量繁殖产酸,叶绿素分子对外界环境的pH值十分敏感。因此,在以上因素的综合作用下导致叶绿素分子被破坏降解形成脱镁叶绿素。在前4 d,各组含量差异不大(P>0.05);在6~8 d时,A、B、C组间差异不明显,但CK组含量显著低于实验组。8 d后,B组含量最高,其次为A组,C组叶绿素含量最低且低于CK组,这是因为A、B组凭借良好的抑菌性能限制腐败菌增殖产酸从而控制pH值的变化,C组ε-PL浓度最高且贮藏过程中失水严重,故叶片组织液浓度也随之上升,加剧酶促反应,使得代谢失衡。由图3-b可知,脱镁叶绿素呈先上升后下降再上升的趋势,之后UV-A光照射短暂激活了叶绿素分子光代谢途径,使得叶绿素分子降解放缓。由图3-b可知,在前2 d,CK、A、C组含量上升不明显,B组脱镁叶绿素含量最早达到最高值显著高于其他组,之后缓慢下降,这与图3-a得变化趋势相符。到了第6天,A、C组达到最高值,之后剧烈降低,表明菠菜即将抵达贮藏终点,叶绿素被完全破坏。到了第10天,各组含量呈上升趋势,C组含量最高,其次为CK组,最低为B组。
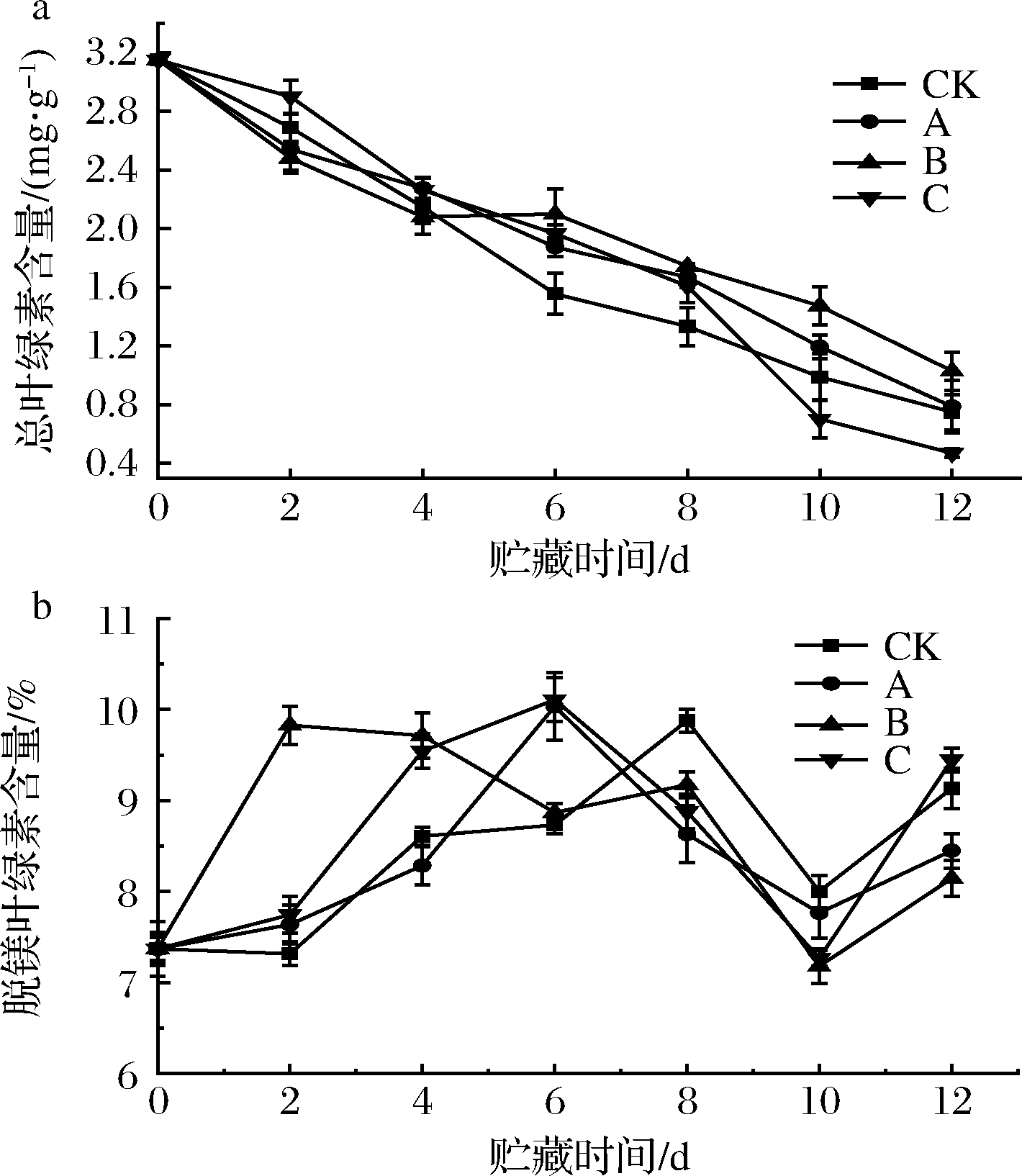
a-总叶绿素含量;b-脱镁叶绿素含量
图3 不同处理方式对鲜切菠菜叶绿素的影响
Fig.3 Effects of different treatments on chlorophyll
contents of fresh-cut spinach
2.2 失水情况
前4 d,各组失水严重,水分含量差异不明显(P>0.05)。在整个贮藏期间CK、C组失水程度严重,组间差异不明显,在第8天,CK、C组失水程度显著高于A、B组(P<0.05),这是因为高浓度ε-PL处理加剧了呼吸作用和蒸腾作用,使得失水严重。10 d后,B组水分含量高于A组,这表明B组能在整个贮藏期间较好地控制鲜切菠菜的失水,这可能是因为ε-PL具有一定成膜性,抑制水分损失。
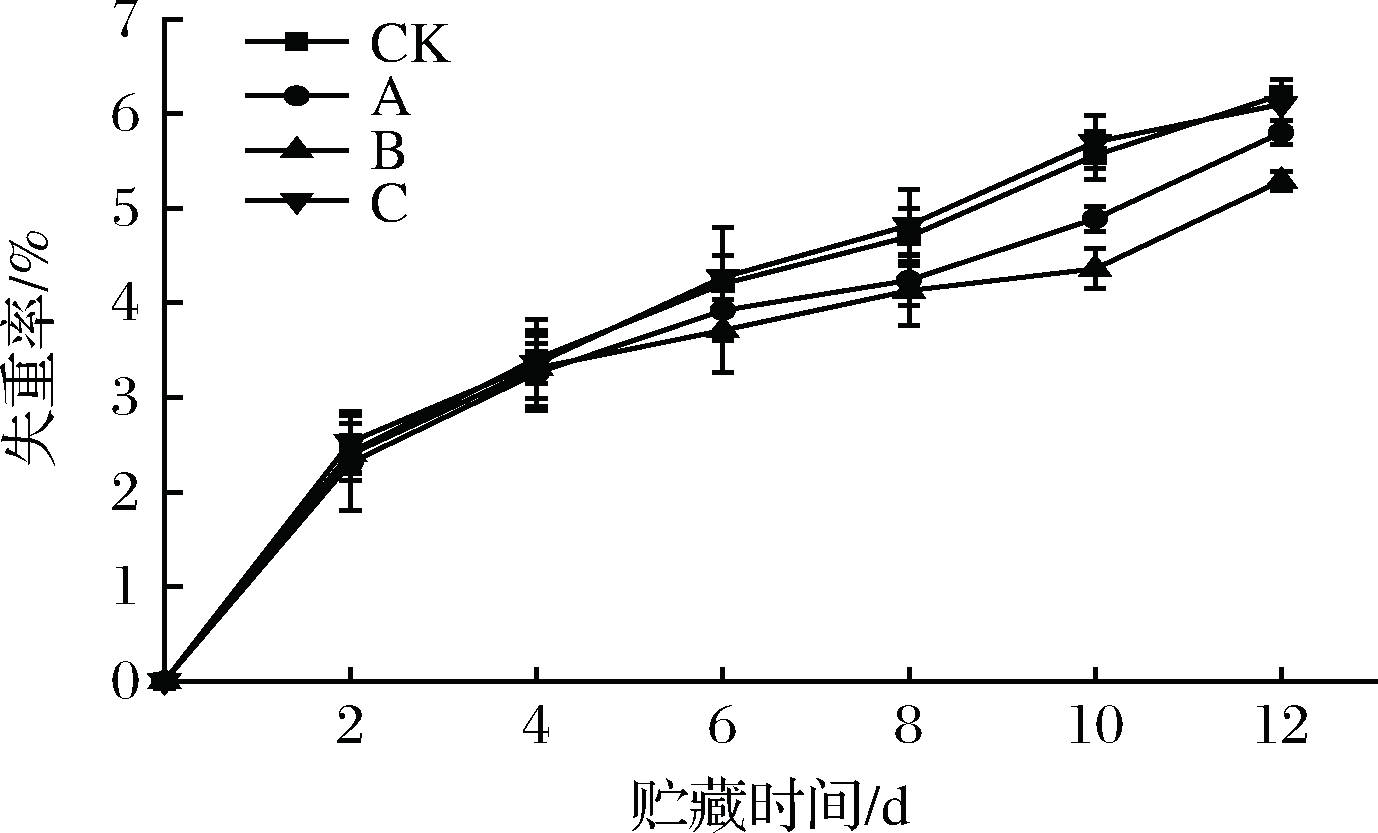
图4 不同处理方式对鲜切菠菜水分损失的影响
Fig.4 Effects of different treatments on water
loss rate of fresh-cut spinach
2.3 微生物指标
2.3.1 革兰氏阴性菌和假单胞菌数量
有文献显示,革兰氏阴性菌是鲜切菠菜表面依附的主要菌群,占比高达90%以上,其中又以假单胞菌为主[14],假单胞菌增殖到一定数量会引起菠菜叶片的软腐、发酸。由图5-a和图5-b可知,在整个贮藏期间,各组革兰氏阴性菌呈增长趋势,假单胞菌呈相同趋势。在前4 d,CK组增长最快,A、B组次之,C组最慢,各组增长趋势同ε-PL溶液浓度呈反比关系。6 d后,C组革兰氏阴性菌的数量陡然上升,这是因为随着贮藏时间的推移,鲜切菠菜本身抵抗不住UV-A光照和高浓度ε-PL的刺激且贮藏过程中失水严重,故叶片组织液浓度也随之上升,加剧了酶促反应,代谢失衡。
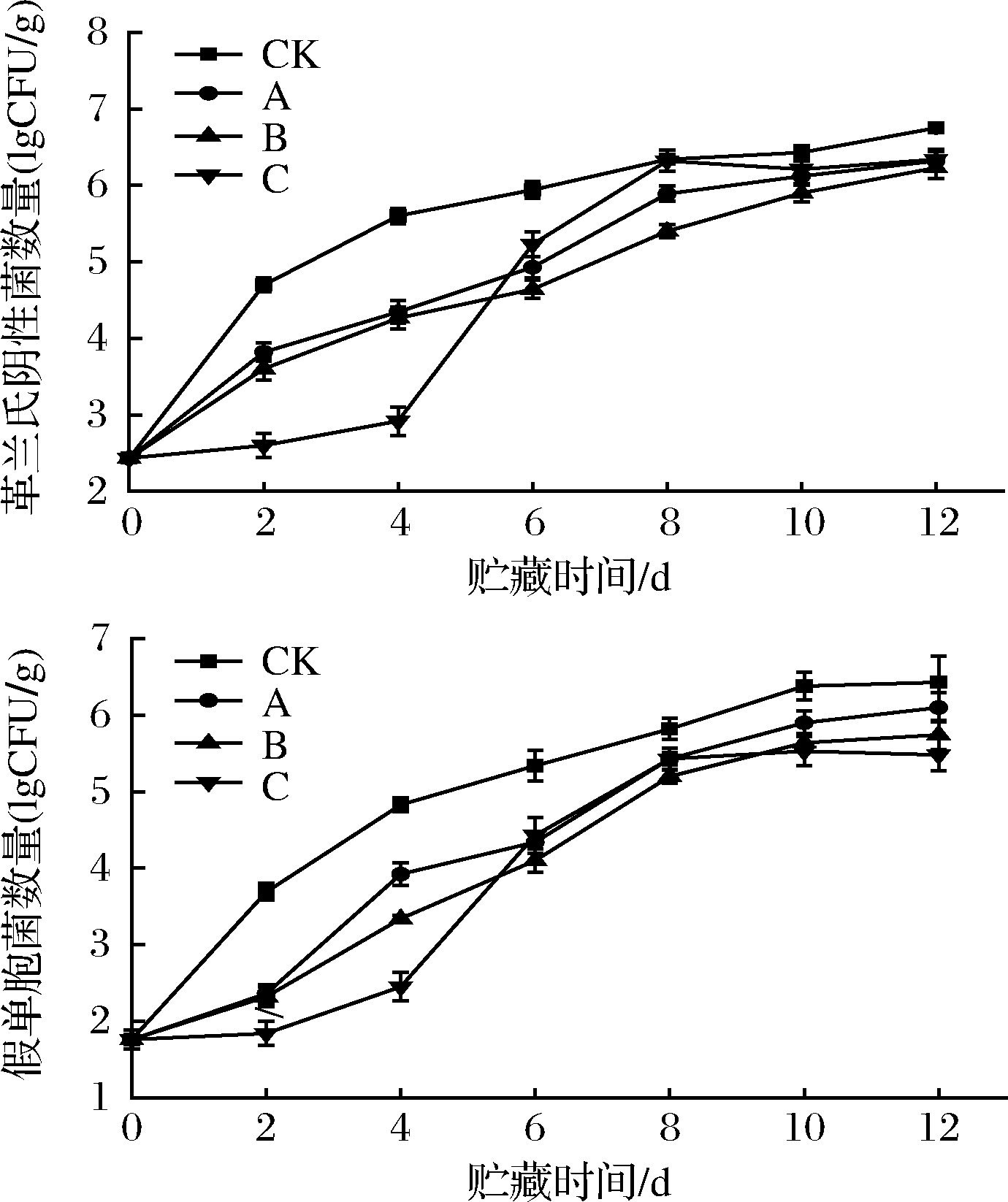
a-革兰氏阴性菌数量;b-假单胞菌数量
图5 不同处理方式对鲜切菠菜表面G-菌和
假单胞菌的影响
Fig.5 Effects of different treatments on the surface
of G- bacteria and Pseudomonas of fresh cut spinach
2.3.2 亚硝酸盐含量
据统计人体摄入的亚硝酸盐80%以上来自蔬菜[19],而亚硝酸盐本身会使人体的血红蛋白的携氧能力大大降低,造成组织缺血从而引起一系列疾病,根据GB 2762—2017标准[20],在蔬菜中亚硝酸盐的限量指标为20 mg/kg。如图6所示,同其他叶菜类相比,新鲜菠菜的亚硝酸盐初始含量较低,这是作物的生物特性决定的[21],各组在前4 d均保持较低水平,但是在6~10 d,CK、C组亚硝酸盐含量迅速上升,这是因为腐败菌迅速增长产生硝基还原酶,将植物中得硝酸盐转换为亚硝酸盐,且2组含量差别不大(P>0.05),大约为A、B组的2~3倍,到了第12天,B组含量仍为最低,其次为A组,CK、C组含量最高,这与图5-a和图5-b实验结果一致。
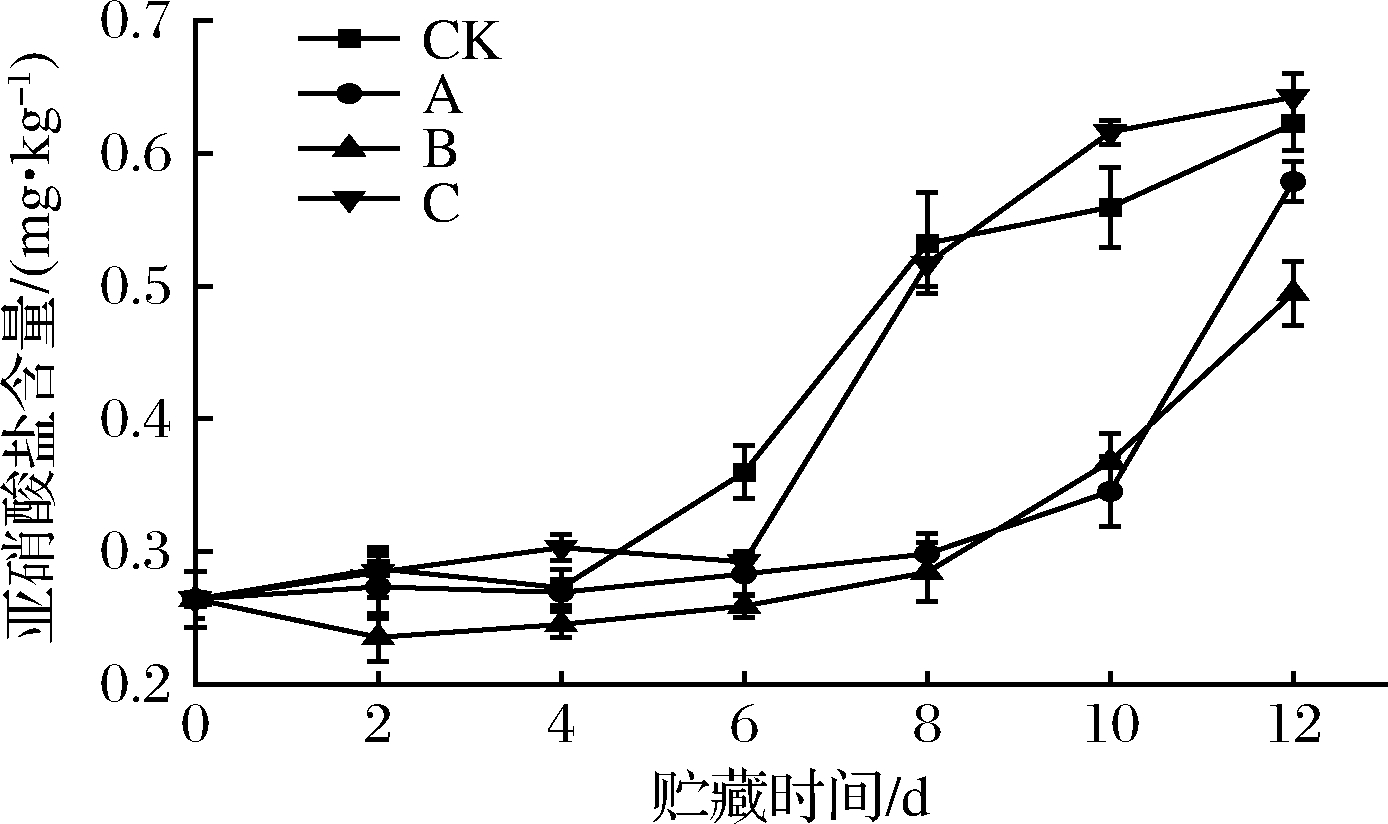
图6 不同处理方式对鲜切菠菜亚硝酸盐含量的影响
Fig.6 Effects of different treatments on nitrite
content of fresh-cut spinach
2.4 抗氧化指标
2.4.1 MDA含量
采摘后的菠菜仍为活体状态,又经过鲜切工艺导致组织愈伤,呼吸作用明显,微观来看,植物细胞中线粒体的呼吸加速,内膜电子呼吸链上传递更多的电子,而有一部分电子和氧气发生了电子还原从而产生了超氧阴离子![]() 同时在内质网膜进行混功能氧化酶的反应中,细胞色素P-450会同空气接触又致使一部分电子与氧气接触产生
同时在内质网膜进行混功能氧化酶的反应中,细胞色素P-450会同空气接触又致使一部分电子与氧气接触产生![]() 本身不仅带有毒性,还会同细胞器膜结构中的不饱和脂肪酸结合产生MDA引起膜损伤,因此MDA含量可判断膜脂过氧化程度[23]。由图7可知,前4 d A、B组MDA含量差异不明显,均显著低于CK、C组,这表明通过适当剂量的UV-A光照和ε-PL处理能够减少
本身不仅带有毒性,还会同细胞器膜结构中的不饱和脂肪酸结合产生MDA引起膜损伤,因此MDA含量可判断膜脂过氧化程度[23]。由图7可知,前4 d A、B组MDA含量差异不明显,均显著低于CK、C组,这表明通过适当剂量的UV-A光照和ε-PL处理能够减少![]() 的产生,保护细胞器膜结构,高剂量的处理方式破坏植物自身的氧化代谢反而加快了细胞衰老。6 d后,B组MDA含量始终保持最低,其次A组,CK、C组保持相对高含量的MDA,2组差异不明显(P>0.05),值得注意的是,C组到了第12天MDA含量降低,结合感官、假单胞菌数量指标推测可能是因为菠菜叶片已腐败,细胞膜结构被破坏,叶片pH值发生改变降解了部分MDA。
的产生,保护细胞器膜结构,高剂量的处理方式破坏植物自身的氧化代谢反而加快了细胞衰老。6 d后,B组MDA含量始终保持最低,其次A组,CK、C组保持相对高含量的MDA,2组差异不明显(P>0.05),值得注意的是,C组到了第12天MDA含量降低,结合感官、假单胞菌数量指标推测可能是因为菠菜叶片已腐败,细胞膜结构被破坏,叶片pH值发生改变降解了部分MDA。
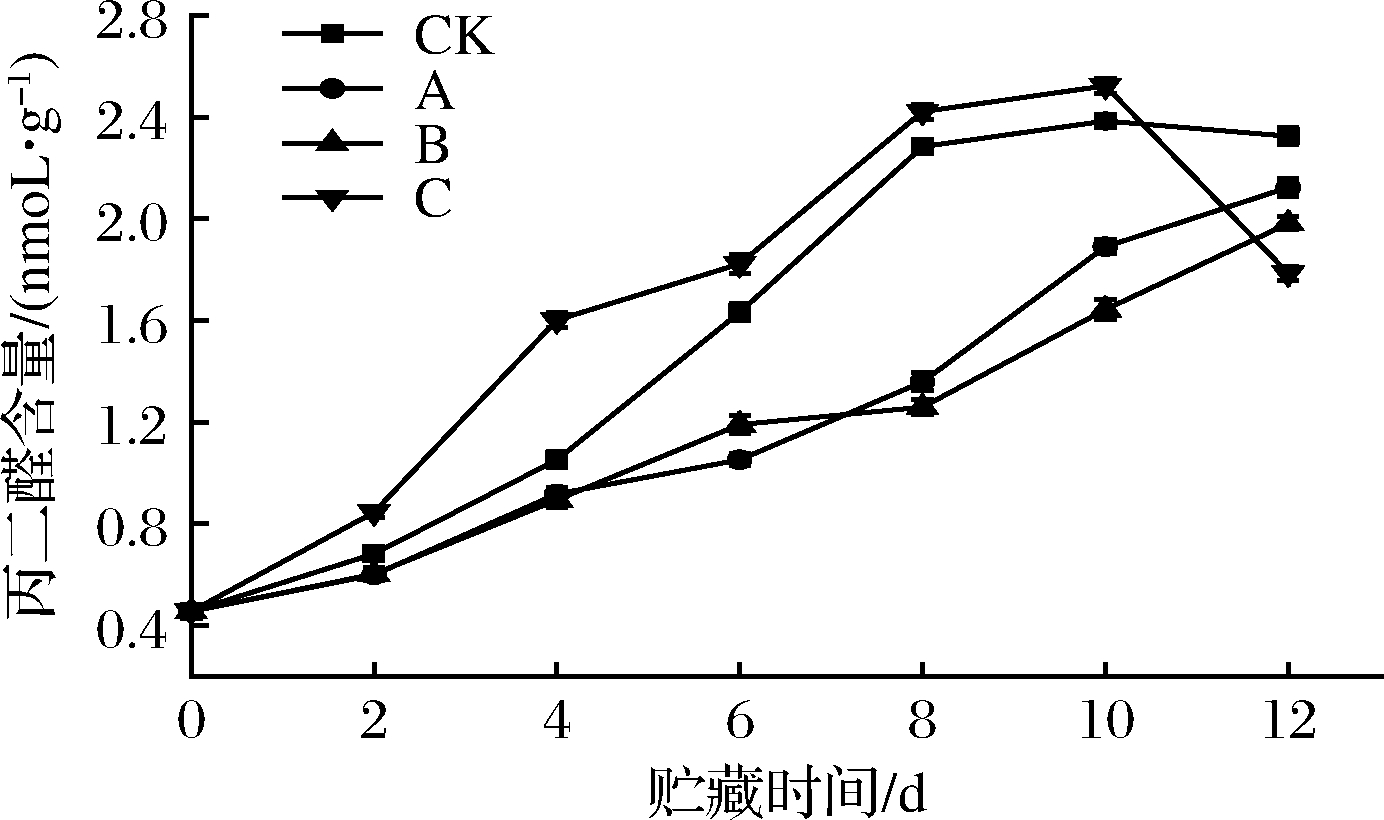
图7 不同处理方式对鲜切菠菜MDA的影响
Fig.7 Effects of different treatments on MDA content
of fresh-cut spinach
2.4.2 SOD含量
SOD是植物氧化代谢中最重要的一种抗氧化酶,其特异底物为![]() 通过发生歧化反应最大限度地清除
通过发生歧化反应最大限度地清除![]() 线粒体内SOD含量直接影响
线粒体内SOD含量直接影响![]() 从线粒体向外扩散的频率[24]。由图8可知,SOD含量都呈先上升后下降的趋势,且上升的时间短于下降时间,这是因为菠菜脱离了养分又经过鲜切,本身抗氧化能力有限,A组在2 d后即开始缓慢下降,在第4天,CK、C组SOD含量达到最高,之后开始下降,且幅度较大,这表明机体内
从线粒体向外扩散的频率[24]。由图8可知,SOD含量都呈先上升后下降的趋势,且上升的时间短于下降时间,这是因为菠菜脱离了养分又经过鲜切,本身抗氧化能力有限,A组在2 d后即开始缓慢下降,在第4天,CK、C组SOD含量达到最高,之后开始下降,且幅度较大,这表明机体内![]() 的动态平衡被打破,即将抵达贮藏终点,B组在8 d内能将SOD含量维持在相对较高的水平,且下降相对缓慢,结合图7得,B组在UV-A光照的刺激下,在整个贮藏过程中抗氧化进程缓和、持久有利于保鲜,且该浓度下的ε-PL溶液不会破坏植物的氧化代谢,其次为A组,而C组浓度过高不利于调节鲜切菠菜的抗氧化能力。
的动态平衡被打破,即将抵达贮藏终点,B组在8 d内能将SOD含量维持在相对较高的水平,且下降相对缓慢,结合图7得,B组在UV-A光照的刺激下,在整个贮藏过程中抗氧化进程缓和、持久有利于保鲜,且该浓度下的ε-PL溶液不会破坏植物的氧化代谢,其次为A组,而C组浓度过高不利于调节鲜切菠菜的抗氧化能力。
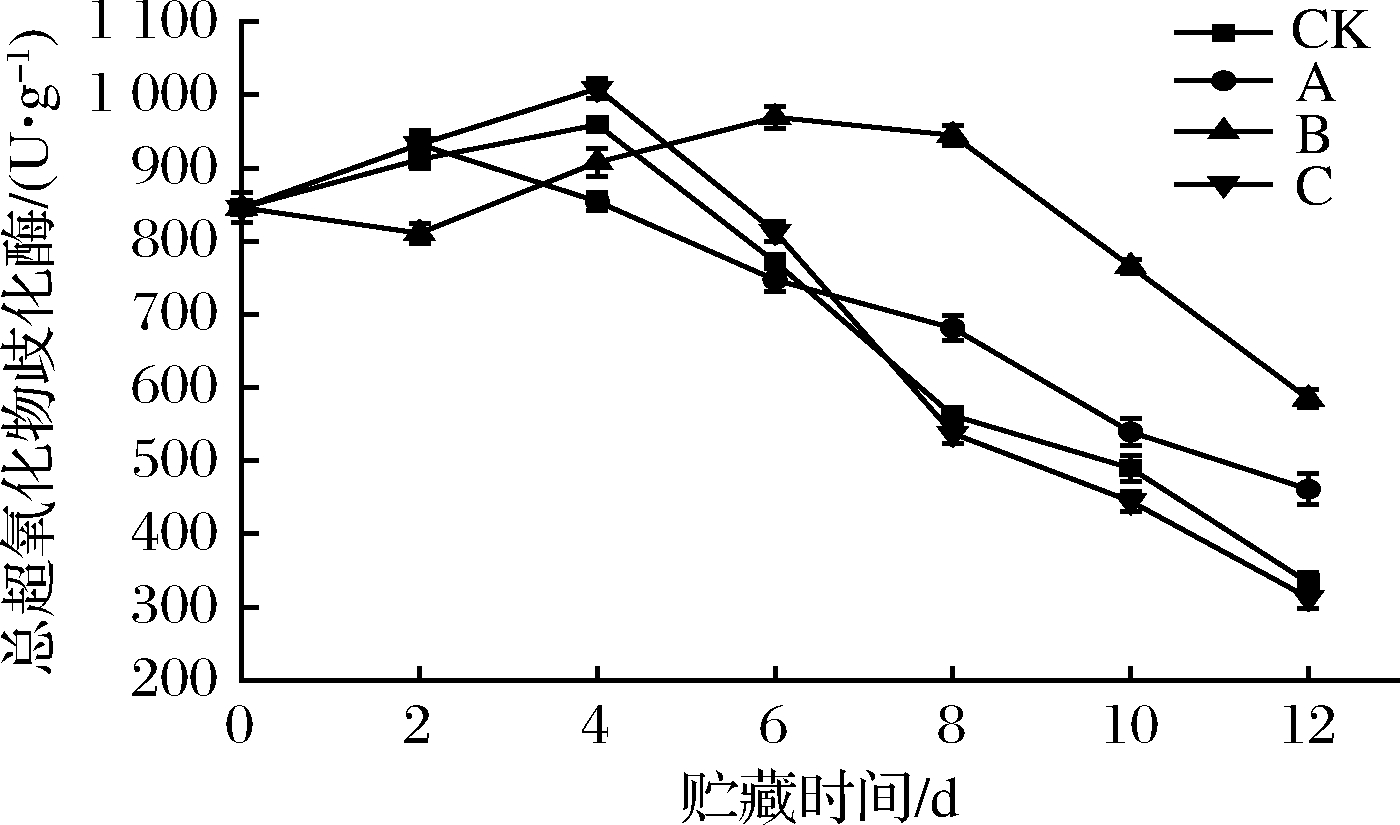
图8 不同处理方式对鲜切菠菜SOD的影响
Fig.8 Effects of different treatments on SOD
activity of fresh-cut spinach
2.5 营养指标
2.5.1 可溶性固形物
在鲜切菠菜中,可溶性固形物包括:糖类物质、水溶性维生素、微量元素等物质,能够较好地反映菠菜中营养成分的变化[25]。由图9可知,随着贮藏时间的延长,各组可溶性固形物被消耗减低,这是因为离体后的植物为了维持本身的生命活动消耗糖分。前4 d各组含量差异不明显(P>0.05),之后B组含量始终为最高,其次为A组,CK和C组差异不显著(P>0.05),这是因为C组体内氧化代谢平衡被打破,组织破裂,营养成分溢出即加速了腐败进程又助于细菌的繁殖。以上现象表明,B组可较好的减缓鲜切菠菜营养流失,有利于保鲜,其次为A组,C组无明显效果。

图9 不同处理方式对鲜切菠菜可溶性固形物的影响
Fig.9 Effects of different treatments on soluble
solids content of fresh-cut spinach
2.5.2 VC含量
VC在人体中参与多种必要的生命活动,如神经递质、蛋白质合成以及多种氨基酸代谢,但人体本身无法合成VC,需要依靠外界摄取,鲜切菠菜富含VC以及多种膳食纤维,是一种可靠的来源,同时,VC也可调节植物自身的氧化代谢平衡延缓衰老,因此VC含量的高低既可以反映营养成分的变化还可以间接反映抗氧化水平。由图10可知,C组的VC含量在第2天短暂地到达最高点,推测相对UV-A光协同高浓度的ε-PL处理可以上调VC合成基因如BO-VTC2、BO-GLDH的表达,这2种基因可以促进VC前体物质的合成从而使得VC含量的增加,这里突出了ε-PL溶液还具有一定的光敏性增强光照对氧化代谢的刺激[26-27],之后VC便开始迅速下降,这是因为相对高浓度的处理方式对鲜切菠菜氧化代谢的刺激程度过高,鲜切菠菜转而开始衰老,从MDA、SOD指标中可以印证这个观点。A、B组均呈缓慢下降的趋势,且B组对减缓VC降解的效果优于A组。
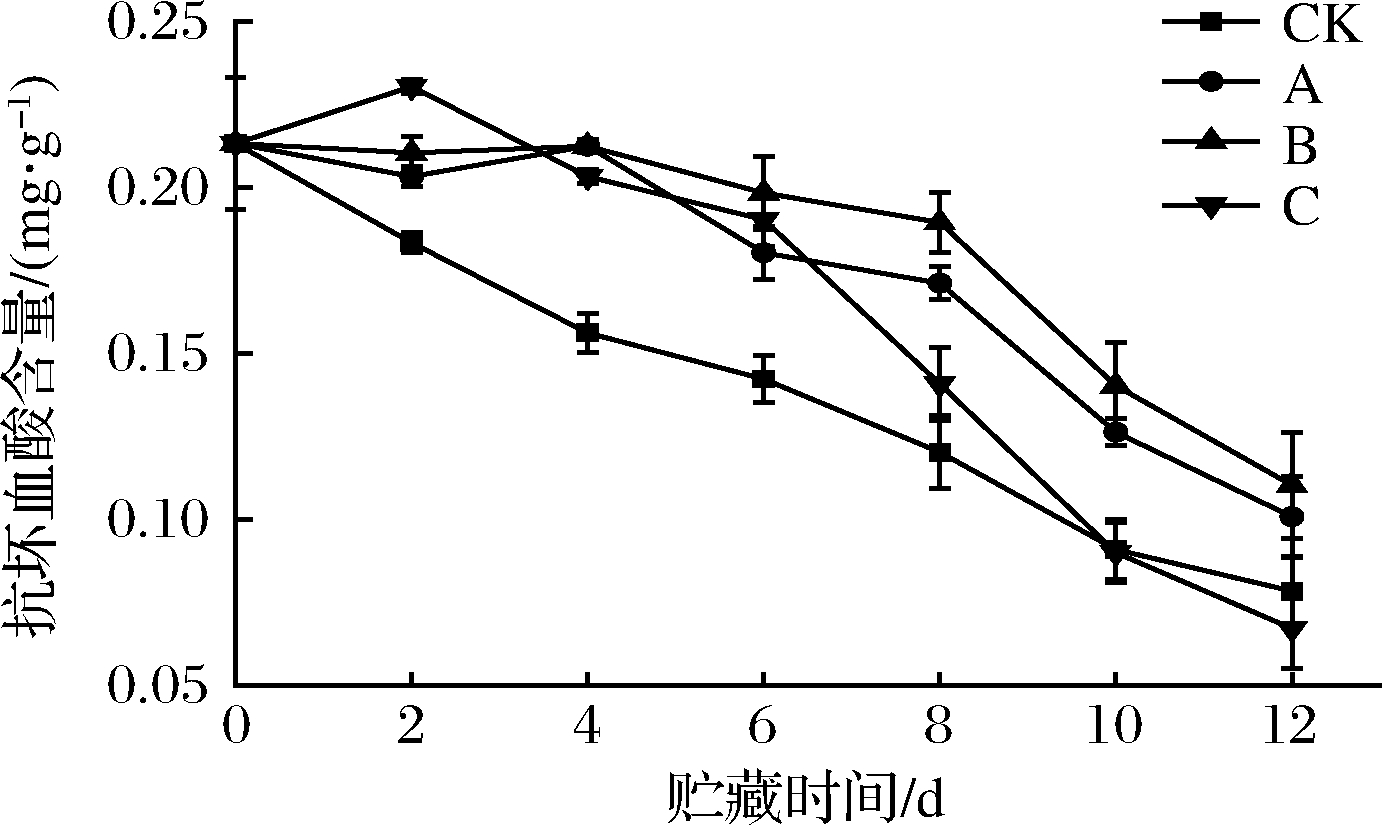
图10 不同处理方式对鲜切菠菜VC的影响
Fig.10 Effects of different treatments on VC
content of fresh-cut spinach
3 结论
UV-A光照结合0.05 g/L ε-PL溶液保鲜效果最好,可有效控制鲜切菠菜颜色发生改变以及腐败菌的增长,极大地减缓褪绿速度和营养成分的损耗,同时又保持良好的抗氧化能力,货架期可达12 d。UV-A光照结合0.02 g/L ε-PL溶液具有一定保鲜效果,但在控制腐败菌的增长和减缓营养流失方面不如前者,货架期可达10 d。UV-A光照结合0.08 g/L ε-PL溶液虽然在贮藏前期能够有效抑制腐败菌的增长,但之后各个指标表明鲜切菠菜劣变较快,货架期同对照组一致为8 d,故判断无明显保鲜效果。
[1] UFUK KASLM M, KASLM R. Yellowing of fresh-cut spinach (Spinacia oleracea L.) leaves delayed by UV-B applications[J]. Information Processing in Agriculture, 2017, 4(3): 214-219.
[2] 姜福星, 黄远祥, 周鹏, 等. 植物叶片再生的探究[J]. 分子植物育种, 2018, 16(20): 6 832-6 839.
[3] PUERTA-GOMEZ A F, KIM J, MOREIRA R G, et al. Quantitative assessment of the effectiveness of intervention steps to reduce the risk of contamination of ready-to-eat baby spinach with Salmonella[J]. Food Control, 2013, 31(2): 410-418.
[4] F Hollsy. Effects of ultraviolet radiation on plant cells[J]. Micron, 2002, 33(2): 179-197.
[5] SURJADINATA, BERNADETH B, JACOBO-VELAZQUEZ, et al. UVA, UVB and UVC Light enhances the biosynthesis of phenolic antioxidants in fresh-cut carrot through a synergistic effect with wounding[J]. Molecules, 2017, 22(4): 1-13.
[6] 郁杰, 张雨宸, 谢晶.低强度UV-A光循环辐照对4 ℃下鲜切菠菜品质及抗氧化能力的影响[J].食品与发酵工业,2019,45(21): 139-146.
[7] 倪清艳, 李燕, 张海涛. ε-聚赖氨酸的抑菌作用及在保鲜中的应用[J]. 食品科学, 2008, 29(9): 102-105.
[8] 刘硕, 王礼群, 张欣怡, 等. 抗坏血酸钙和ε-聚赖氨酸对鲜切甘薯保鲜护色效果的影响[J]. 食品与机械, 2018,34(7):132-136;142.
[9] 姚昕, 秦文. ε-聚赖氨酸和臭氧处理对石榴果实贮藏品质影响的多变量分析 [J]. 食品与发酵工业, 2017, 43(8): 254-261.
[10] 邓静泽, 黄明东, 陈卓, 等. 水溶性寡聚赖氨酸锌酞菁的合成及其光动力学活性[J]. 沈阳药科大学学报, 2018, 35(11): 936-942.
[11] PAILLART M J M, VAN DER VOSSEN J M B M, LEVIN E, et al. Bacterial population dynamics and sensorial quality loss in modified atmosphere packed fresh-cut iceberg lettuce[J]. Postharvest Biology and Technology, 2017, 124: 91-99.
[12] ERICK FALC ODE OLIVEIRA, ROHANTIKEKAR, NITIN NITIN. Combination of aerosolized curcumin and UV-A light for the inactivation of bacteria on fresh produce surfaces [J]. Food Research International, 2018, 114: 133-139.
ODE OLIVEIRA, ROHANTIKEKAR, NITIN NITIN. Combination of aerosolized curcumin and UV-A light for the inactivation of bacteria on fresh produce surfaces [J]. Food Research International, 2018, 114: 133-139.
[13] NY/T 3082—2017 水果、蔬菜及其制品中叶绿素含量的测定, 分光光度法[S]. 北京: 中国标准出版社, 2017.
[14] 郁杰, 谢晶. 高通量测序结合传统方法分析4℃下鲜切菠菜的菌群变化[J]. 食品与发酵工业, 2019, 45(9): 183-189.
[15] 国家食品药品监督管理总局.GB 5009.33—2016 食品中亚硝酸盐与硝酸盐的测定[S]. 北京: 中国标准出版社, 2016.
[16] 国家卫生和计划生育委员会.GB 5009.181—2016 食品安全国家标准 食品中丙二醛的测定[S]. 北京: 中国标准出版社, 2016.
[17] 国家卫生和计划生育委员会.GB 5009.86—2016 食品安全国家标准 食品中抗坏血酸的测定[S]. 北京: 中国标准出版社, 2016.
[18] 朱东兴, 刘天鹤, 仲伟, 等. 不同处理方法对小松菜冻藏期保鲜品质的影响[J]. 北方园艺, 2016(10):131-134.
[19] 张美月, 杨容. 贮存方法和时间对蔬菜中硝酸盐和亚硝酸盐的影响 [J]. 保定学院学报, 2008, 21(4): 4-6.
[20] 国家食品药品监督管理总局.GB 2762—2017 食品安全国家标准 食品中污染物限量[S]. 北京:中国标准出版社, 2017.
[21] JAWORSKA G Y. Nitrates, nitrites, and oxalates in products of spinach and New Zealand spinach: Effect of technological measures and storage time on the level of nitrates, nitrites, and oxalates in frozen and canned products of spinach and New Zealand spinach [J]. Food Chemistry, 2005, 93(3): 395-401.
[22] 刘占才, 牛俊英. 超氧阴离子自由基对生物体的作用机理研究 [J]. 焦作教育学院学报, 2002(4): 48-51.
[23] FOYER C H, NOCTORT G. Oxidant and antioxidant signalling in plants: A re-evaluation of the concept of oxidative stress in a physiological context [J]. Plant Cell & Environment, 2005, 28(8): 1 056-1 071.
[24] ROBSON C A R A, ZHAO D Y Z Y. Interactions between mitochondrial electron transport, reactive oxygen [J]. Botany-botanique, 2008, 86: 278-290.
[25] MAMAJAN B, SINGH R. Effect of packaging films on shelf life and quality of kinnow fruits packed in consumer packages [J]. International Journal of Farm Sciences, 2014, 4(1): 92-98.
[26] D′SOUZA C, YUK H G, KHOO G H, et al. Application of light-emitting diodes in food production, postharvest preservation, and microbiological food safety[J]. Comprehensive Reviews in Food Science & Food Safety, 2015, 14(6): 719-740.
[27] ZHAN Lijuan, HU Jinqiang, AI Zhilu. Light exposure during storage preserving soluble sugar and L-ascorbic acid content of minimally processed romaine lettuce (Lactuca sativa L.var. longifolia) [J]. Food Chemistry, 2013, 136(1): 273-278.