腺嘌呤核苷三磷酸(adenosine triphosphate, ATP)是高能磷酸化合物,由1分子核糖、1分子腺嘌呤和3个相连的磷酸基团构成的核苷酸,广泛存在于各种动物、植物和微生物的活体细胞中。当活体细胞裂解或死亡后,在胞内酶的作用下,游离的ATP分子数量会迅速下降或消失[1]。1983年,日本学者MOYER等[2]首次提出细胞内源性ATP的含量可以反映细胞活性和活细胞数量,主要原理是ATP在虫荧光素酶的催化作用下,与荧光素在有氧环境及Mg2+作用下反应释放出荧光,荧光强度与ATP数量在一定范围内呈线性关系[3]。20世纪80年代,英国人率先研制出ATP荧光检测系统,随后发展到欧洲、美国和日本,应用领域涉及食品加工、超市和饮食行业,检测内容包括微生物和食品残渣[4]。2018年我国颁布标准GB/T 36004—2018《食品接触表面清洗消毒效果实验方法 三磷酸腺苷生物发光法》,规定采用ATP生物发光方法评价食品接触面清洗消毒效果,为生产企业执行危害分析与关键控制点(hazard analysis and critical control point,HACCP)提供快速有效的技术手段。目前,该方法已在乳品发酵[5]、面粉生产[6]、啤酒行业[7]领域引入,应用于食品企业生产原料、过程控制、设备表面清洁及微生物污染情况的检验。
啤酒是一种发酵饮料,营养丰富,素有“液体面包”之称,其酿造过程中始终伴随着微生物污染的风险,机械设备、人员及其装备表面附着微生物和原位清洗(cleaning in place,CIP)不当均可造成外源微生物的侵入,导致啤酒浊度的增加、香气和风味的改变。平板计数法是对细菌总数进行检测的国标方法[8],但该方法检测周期长,不适合现场实时检测。因此,为加强对啤酒污染微生物的管理与控制,本研究引入便携式ATP快速检测系统分别对人工污染短乳杆菌(Lactobacillus brevis)的物体表面、水质和有机质残留进行检测,并以此建立预测模型,快速定量评价啤酒酿造过程中关键控制点的短乳杆菌及有机质污染情况。
1 材料与方法
1.1 实验材料
1.1.1 菌株
短乳杆菌,公司菌种保藏中心提供。
1.1.2 主要仪器与试剂
MVP ICONTM ATP型快速检测仪,德国默克公司;BX53型普通光学显微镜,日本OLYMPUS公司;A49474型手持糖度计,日本爱拓公司;MVP ICON型电导率探针、MVP型ATP表面检测棒、MVP型ATP水质检测棒,默克化工技术(上海)有限公司。
NBB-A/B培养基,德国德乐公司;10 °P纯生啤酒,包装车间提供。
1.2 实验方法
1.2.1 表面细菌总数检测及标准曲线的建立
从试管中挑取短乳杆菌1环,接入NBB-B培养基进行活化,36 ℃恒温培养48 h,10 000 r/min离心5 min收集菌体,无菌水洗涤2~3次。使用无菌水将短乳杆菌悬浮液连续梯度稀释,稀释至可以得到单菌落的浓度梯度为101~103个/mL为止,用倾注平板法向NBB-A培养基注入1 mL稀释的混合菌液,每个稀释梯度做2个平行,在28 ℃恒温培养箱中厌氧培养72 h后,对平板上形成的单菌落进行计数。同时,分别吸取1 mL悬浮菌液均匀涂布于无菌培养皿中,超净工作台中静置至风干,表面检测棒涂抹采集后,检测对应梯度菌液相对荧光单位(relative luciferase unit,RLU)值。以RLU为横坐标、菌落总数对数值lg CFU为纵坐标建立表面细菌总数预测模型。
1.2.2 水质细菌浓度检测及标准曲线的建立
高速离心法富集短乳杆菌菌体,无菌水洗涤2~3次后使用无菌水进行重悬浮,使用血球计数板进行显微计数。使用无菌水将短乳杆菌悬浮液连续梯度稀释至100个/mL,25 ℃静置48 h后,使用水质检测棒取样,检测对应梯度菌悬液的RLU值。并以RLU为横坐标、细菌浓度对数值lg(个/mL)为纵坐标建立预测模型。
1.2.3 啤酒有机质残留检测及标准曲线的建立
使用无菌水进行10 °P纯生啤酒2倍梯度稀释,稀释后的各组样品用糖度计进行糖度检测,同时采用ATP快速荧光检测系统进行各组稀释样品的RLU值检测,做啤酒稀释倍数与RLU值变化曲线并建立预测模型。
2 结果与分析
2.1 表面细菌总数与ATP荧光值的相关性分析
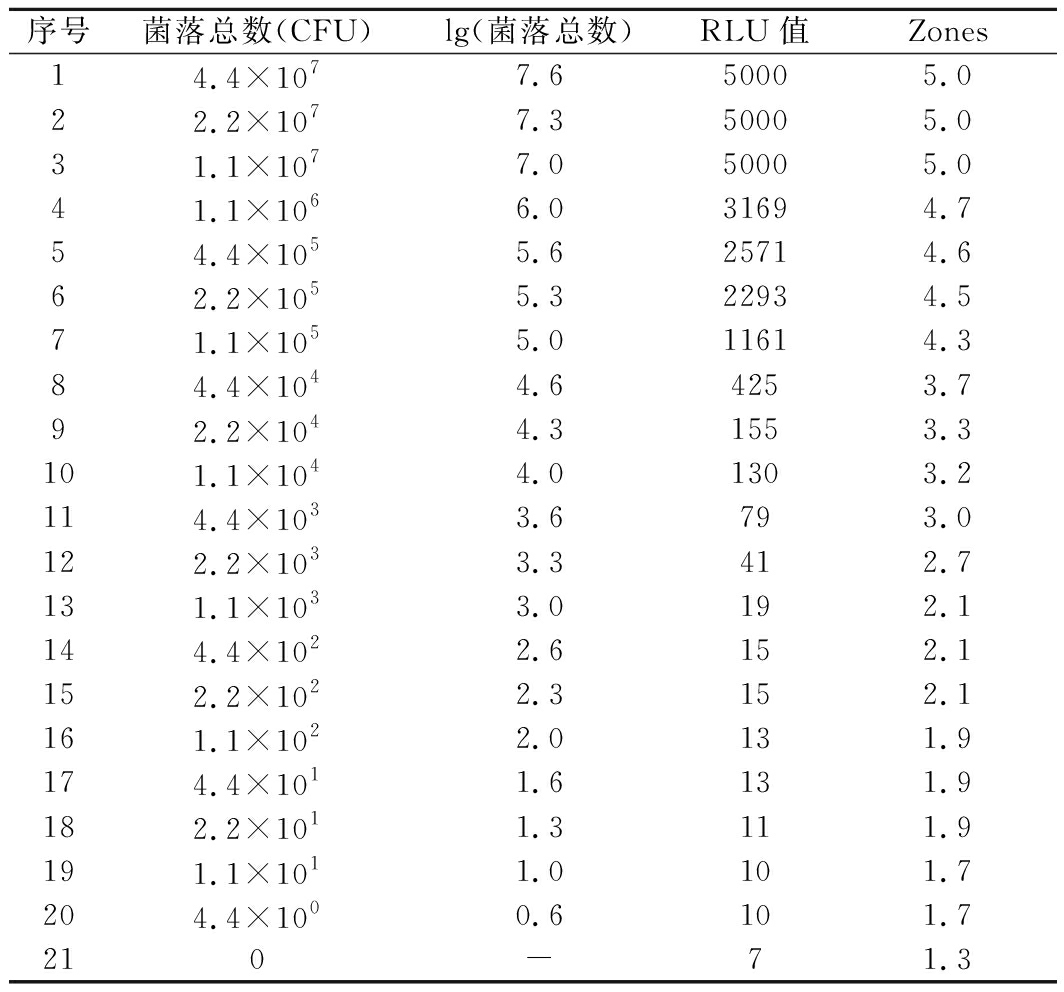
由于ATP生物发光法无法定性鉴别细菌种类,因此不同细菌ATP含量的差异可能直接影响对菌落总数的快速检测。田雨等[9]对比分析了枯草芽孢杆菌、大肠埃希氏菌、蜡状芽孢杆菌、乳酸片球菌、乳酸链球菌等6种常见细菌中ATP含量的差异性,结果显示当细菌总数相同时,ATP生物发光法检测的荧光值无明显差异。因此,本实验以引起啤酒腐败最多的短乳杆菌进行表面菌落总数与ATP荧光值的相关性研究。短乳杆菌菌落总数控制在100~107 CFU,以未污染的洁净表面为阴性对照,共获得21组检测数据,检测结果如表1所示。在该组数据中,RLU值最高为5 000,对应的菌落总数为1.1×107 CFU;最低为无菌阴性对照,RLU值为7。当菌落总数大于2.2×103 CFU时,即Zone值位于“预警”区域范围,RLU值呈指数增长趋势,预示检测表面存在大量微生物残留。
表1 表面细菌总数与RLU值检测结果
Table 1 Detection results of total surface bacteria
and RLU value
序号菌落总数(CFU)lg(菌落总数)RLU值Zones14.4×1077.650005.022.2×1077.350005.031.1×1077.050005.041.1×1066.031694.754.4×1055.625714.662.2×1055.322934.571.1×1055.011614.384.4×1044.64253.792.2×1044.31553.3101.1×1044.01303.2114.4×1033.6793.0122.2×1033.3412.7131.1×1033.0192.1144.4×1022.6152.1152.2×1022.3152.1161.1×1022.0131.9174.4×1011.6131.9182.2×1011.3111.9191.1×1011.0101.7204.4×1000.6101.7210-71.3
注:Zones为清洁区域,Zones<2.5表示“通过”;3.0>Zones≧2.5表示“预警”;Zones>3.0表示“警告”
以lg(菌落总数)为横坐标、RLU值为纵坐标建立预测模型,如图1所示。由图1可知,lg(菌落总数)与RLU值存在正相关,可拟合为指数增长的数学预测模型,指数方程为y=2.103 9e1.120 9x(R2=0.906 4,P<0.05),拟合效果较好,可对危害分析和关键控制点进行表面微生物总数预测。然而,使用台式ATP荧光快速检测仪检测的ATP荧光值与菌落总数常拟合为线性相关方程[10-11],这可能是由于便携式和台式ATP荧光检测仪的检测灵敏度存在差异,但并不影响本实验中表面菌落总数预测模型的建立。
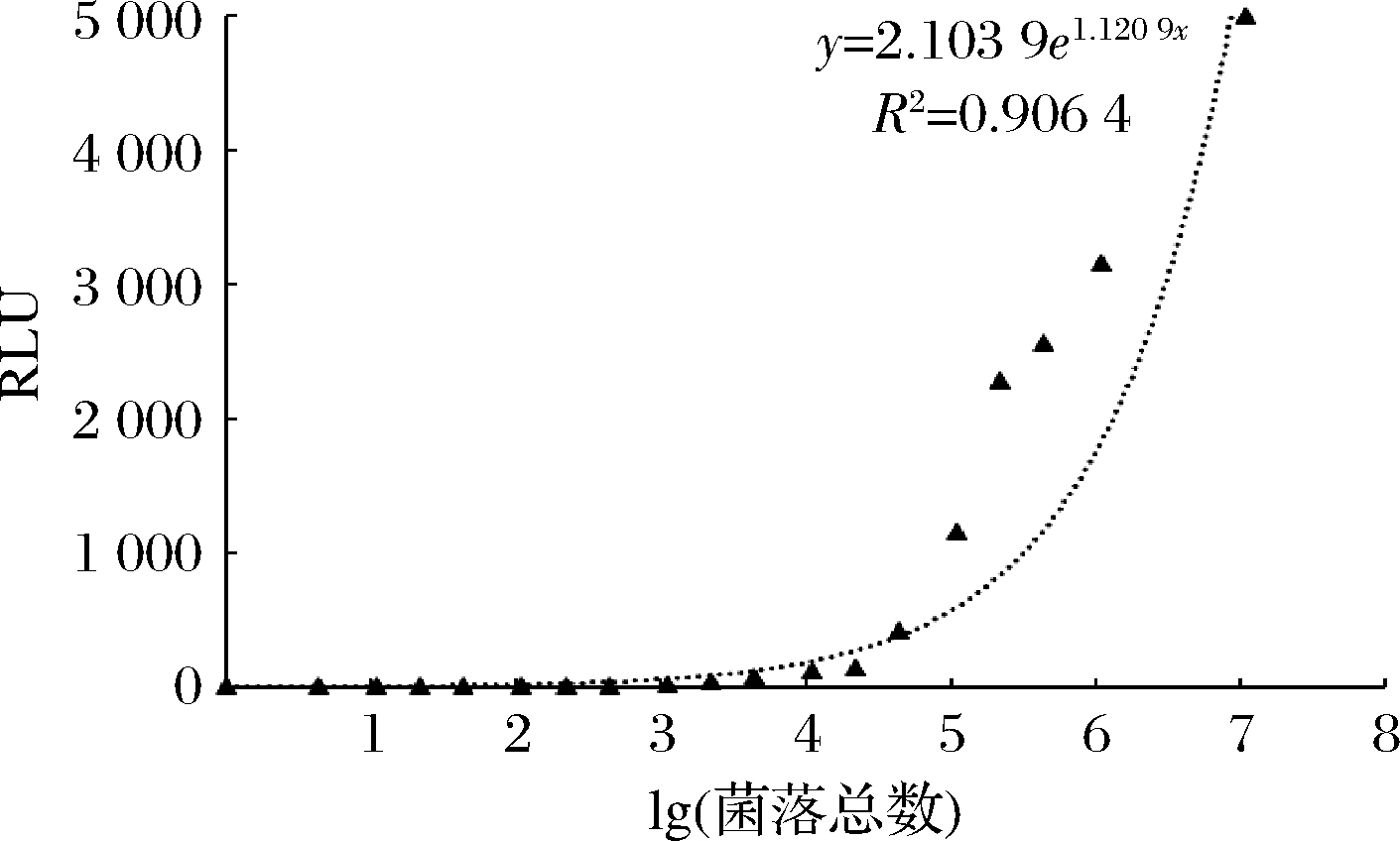
图1 表面细菌总数预测模型
Fig.1 Prediction model of number of bacteria on the surface
2.2 细菌浓度与ATP荧光值的相关性分析
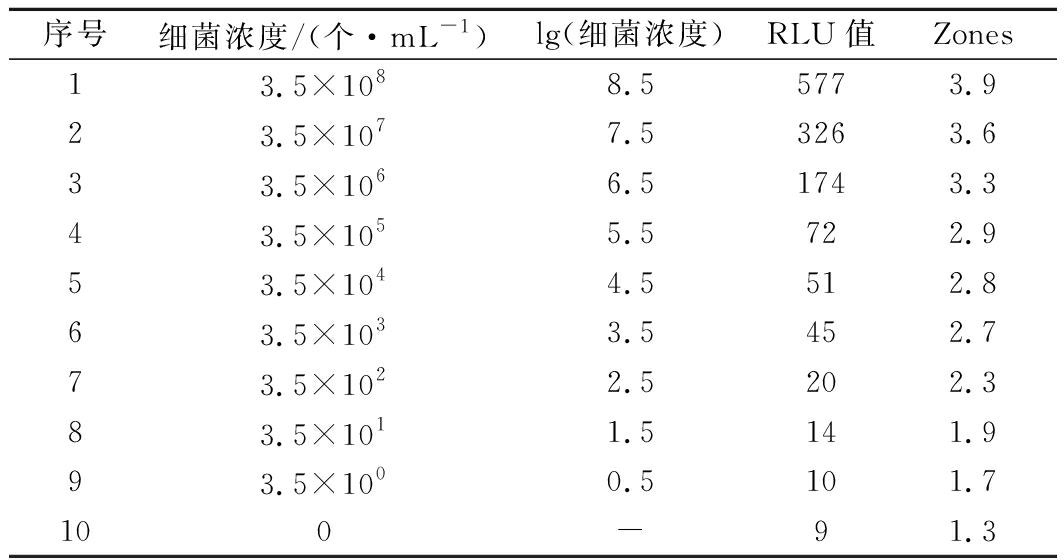
啤酒生产企业绝大多数酿造用水是深井水,能在深井水中生存的微生物一般不耐酸、不耐酒精,因此不能在啤酒中生长,但啤酒在运输经过管道、蓄水池、储水罐及接触空气时就会被微生物污染,会在啤酒酿造过程中产生污染[12]。实验室无菌水经人工污染短乳杆菌后,室温静置48 h,短乳杆菌浓度控制在3.5×100~3.5×108 个/mL,采用便携式ATP快速荧光检测仪进行检测,共获得10组数据,检测结果见表2。当短乳杆菌浓度为3.5×108个/mL,RLU值最高为577;当检测无菌水时,RLU值最低为9。
表2 细菌浓度与RLU值检测结果
Table 2 Detection results of bacterial concentration
and RLU value
序号细菌浓度/(个·mL-1)lg(细菌浓度)RLU值Zones13.5×1088.55773.923.5×1077.53263.633.5×1066.51743.343.5×1055.5722.953.5×1044.5512.863.5×1033.5452.773.5×1022.5202.383.5×1011.5141.993.5×1000.5101.7100-91.3
以lg(细菌浓度)为横坐标、RLU值为纵坐标建立预测模型,如图2所示。lg(细菌浓度)和RLU值呈正相关,数据可拟合为指数方程为y=6.250 3e0.507 7x(R2=0.98,P<0.05),拟合效果较好。当水质检测RLU值>10时,即可证明水质中有微生物存在,与电化学阻抗法[13]、常规PCR法[14]和免疫学法[15]等相比,极大地缩短了检测时间和成本。
2.3 啤酒有机质残留与ATP荧光值的相关性分析
啤酒在灌装过程中应保证灌装设备清洁干净,所使用的灌装容器必须经过严格检查和清洗,如不及时清洗,再加上较长时间不用,其中残留的酒液就会腐败发臭,严重影响啤酒的质量安全。因此,本部分研究建立啤酒残留量的快速检测方法,表3为不同稀释梯度的纯生啤酒对应的RLU值和残留糖度。10 °P纯生啤酒原液RLU检测值为74,当稀释至32倍时,稀释样品检测与无菌水相同,RLU值为9。

图2 水质污染微生物预测模型
Fig.2 Prediction model of microorganism in water
表3 啤酒梯度稀释样品RLU值检测结果
Table 3 RLU value of serial dilution of beer

稀释梯度原样1/2稀释1/4稀释1/8稀释1/16稀释1/32稀释无菌水RLU值743827141199糖度/°Bx5.02.61.30.70.40.20
以酒样稀释梯度为横坐标,RLU值为纵坐标,建立啤酒残留量的预测模型,绘制标准曲线如图3所示,并拟合线性回归方程为y=66.525x+7.005(R2=0.994,P<0.005)。RLU值和啤酒稀释倍数线性关系良好,利用此模型可对CIP或移动清洗(clean out of place,COP)程度进行评价。
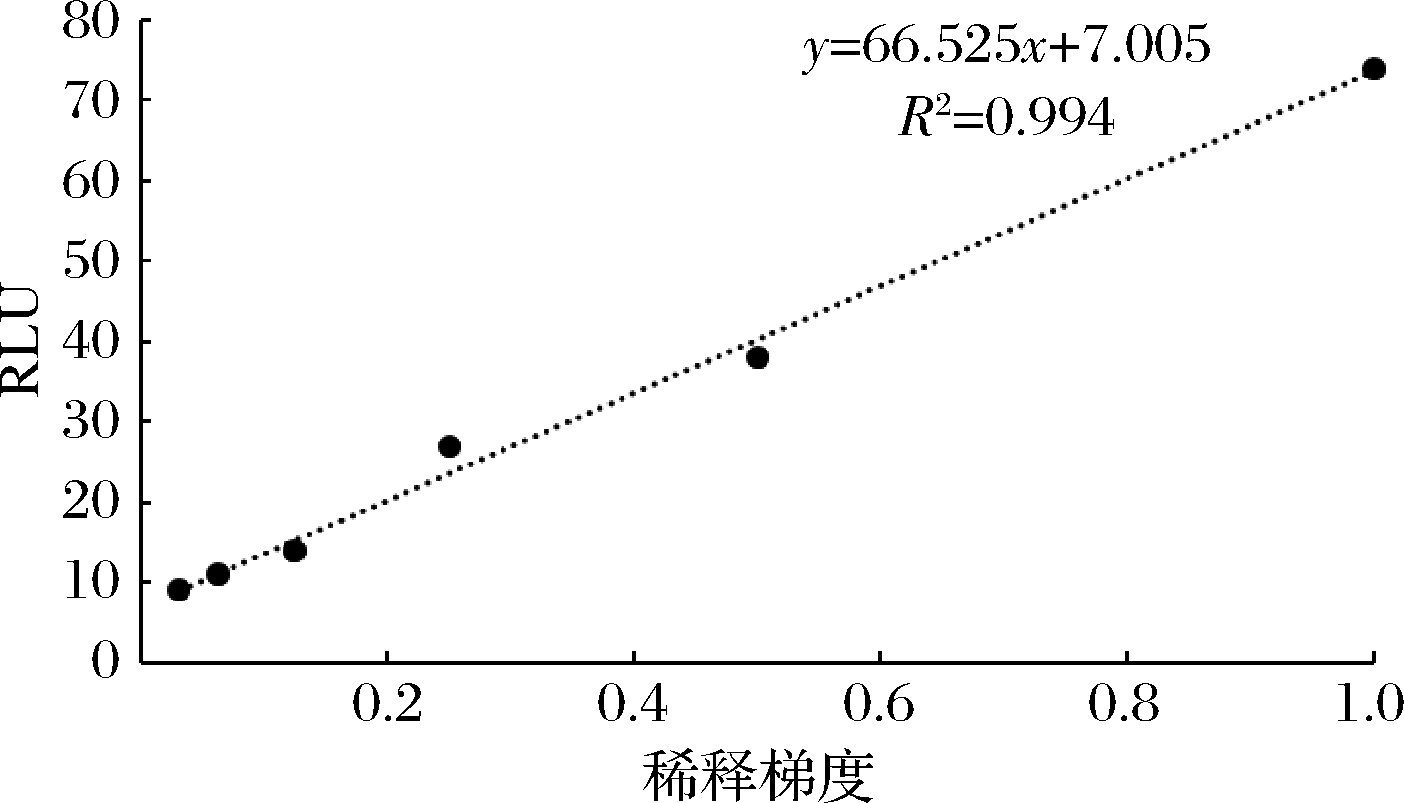
图3 啤酒有机质残留预测模型
Fig.3 Prediction model of organic matter residue from beer
3 结论
便携式ATP生物发光法监测系统应用十分广泛,在生产设备清洁、消毒效果检测、原辅料污染细菌总数检测、HACCP、卫生学监测等方面均可发挥很好的实时监控的作用。本试验基于便携式ATP生物发光快速检测系统,在实验室条件下分别建立表面短乳杆菌总数、水质短乳杆菌浓度和啤酒有机质残留预测模型,其中,当表面短乳杆菌总数>1.1×102 CFU、水质短乳杆菌浓度>3.5×101 个/mL时可使用该检测系统进行快速实时监测,并进行细菌总数或浓度的预测,此外,也可对啤酒包装车间啤酒残留(残留糖度>0.2 °Bx)进行预测。与传统的平板计数法相比,ATP生物发光法具有操作简单、快速灵敏、绿色环保等优点,但该方法检测RLU值的稳定性极易受到食品添加剂种类和周围环境的影响,因此,目前该方法只作为食品加工企业自我卫生监控系统,可极大地提高环境清洁检测的时效性和准确性,降低生产安全隐患发生的可能性。
[1] 侯英,吴雪琼,王兴华. ATP生物发光原理及应用研究[J].中国医药导报, 2010,7(12):12-13;18.
[2] MOYER J D, HENDERSON J F. Nucleoside triphosphate specificity of firefly luciferase[J].Analytical Biochemistry,1983,131(1): 187-189.
[3] VIVIANI V R, OEHLMEYER T L, AMOLDI F G C, et al. A new firefly luciferase with bimodal spectrum: Identification of structural determinants of spectral pH-sensitivity in firefly luciferases[J].Photochemistry and Photobiology,2007,81(4):843-848.
[4] SELAN L,BERLUTTI F,PASSARIELLO C,et al. Reliability of a bioluminescence ATP assay for detection of bacteria[J].Journal of Clinical Microbiology,1992,30(7):1 739-1 742.
[5] 李春艳,霍贵成,王德国,等. ATP生物发光法快速测定生乳中微生物总数的研究[J].东北农业大学学报,2008,29(7):103-106.
[6] 李利霞,伍金娥,常超,等.优化的ATP生物发光法快速检测面粉中细菌总数[J].安徽农业科学,2011, 39(7):4 55-4 057.
[7] 胡雪莲,韩芳,侯玉柱,等. ATP生物发光法测定啤酒酿造过程中污染微生物变化规律的研究[J].啤酒科技,2012(5):24-26.
[8] 程金权,胡继贵.食品中菌落总数快速检测研究进展[J].食品与发酵科技,2014,50(6): 1-5.
[9] 田雨, 侯玉柱, 柯润辉,等.采用ATP生物发光法分析6株常见细菌ATP含量差异[J].食品与发酵工业,2015, 41(1):220-224.
[10] 侯玉柱,田雨,柯润辉,等. ATP生物发光法快速测定物体表面的菌落总数[J].食品与发酵工业,2015,41(2):217-220.
[11] LEE S J, PARK J S, IM H T, et al. A microfluidic ATP-bioluminescence sensor for the detection of airborne microbes[J].Sensors and Actuators B chemical, 2008, 132(2):443-448.
[12] 叶子豪.啤酒酿造过程中有害微生物污染因素及防治策略[J].现代农业科技,2011(9):370-371;376.
[13] NISHIKAWA S, SAKAI S, KARUBE I, et al. Dye-Coupled electrode system for the rapid determination of cell populations in polluted water[J].Applied and Environmental Microbiology, 1982, 43(4): 814-818.
[14] TENOVER F C. Rapid detection and identification of bacterial pathogens using novel molecular technologies: Infection control and beyond[J].Clinical Infectious Diseases, 2007, 44(1):418-423.
[15] VIALETTE M, PINON A, LEPORD B, et al. Meta-analysis of food safety information based on a combination of a relational database and a predictive modeling tool[J].Risk Analysis, 2010, 25(1):75-83.