2001年,联合国粮农组织/世界卫生组织(FAO/WHO)联合专家委员会提出了益生菌的科学定义:益生菌系指活的微生物,当摄取足够数量时,对宿主健康有益[1]。在“健康中国”国家战略的推动下,益生菌的市场规模快速扩大,到2018年已形成近千亿元的庞大市场规模[2]。
益生菌粉(固体饮料类)是益生菌应用的主要产品形式之一,特别是近几年的益生菌市场,益生菌粉的种类和数量如雨后春笋般增长,在市场火爆的同时,益生菌自主产权以及产品稳定性也是人们关注的深层问题,这也是衡量一个企业能否长久发展和参与国际竞争的核心因素。
本文所研究的2株益生菌动物双歧杆菌A6和长双歧杆菌BBMN68均是分离自广西巴马长寿老人肠道[3-4]。已有研究证明,动物双歧杆菌A6具有降低胆固醇、增强机体免疫力和缓解小鼠便秘等多种益生功能[5],还有较强的耐酸耐胆盐能力[6],有助于在肠道内存活和定植;长双歧杆菌BBMN68是1株具有较低耐氧能力的益生菌[7],有多篇研究报道长双歧杆菌BBMN68具有改善小鼠肠道消化功能[8-9]、增强小鼠免疫调节能力[10-11]和提高线虫抗衰老功能等作用[12]。
目前,动物双歧杆菌A6和长双歧杆菌BBMN68的工业生产技术已经完全成熟,能够分别稳定生产出活菌数在1.0×1012和1.0×1011 CFU/g以上的菌粉,这2株益生菌已完全具备产业化应用的基础,但为了进一步提高2株双歧杆菌菌粉的稳定性,降低菌粉的储运成本,需要在包装及贮藏方式方面开展系统研究,以期找到保持产品稳定性的最优方式。
1 材料与方法
1.1 实验材料
1.1.1 菌株
动物双歧杆菌A6和长双歧杆菌BBMN68均由教育部-北京市共建功能乳品重点实验室提供,其菌种专利保藏号分别为CGMCC 9273和 CGMCC 2265。
1.1.2 主要原辅料
益生菌冻干粉:动物双歧杆菌A6菌粉(活菌数1.2×1012 CFU/g)、长双歧杆菌BBMN68菌粉(活菌数5.2×1010 CFU/g),三河福成生物科技有限公司。
辅料:低聚果糖,95型,山东百龙创园生物科技有限公司;乳清粉,D40型,Lactear S.A.;菊粉,NanoST P90型,丰宁平安高科实业有限公司;低聚半乳糖,GOS-700-P型,云浮市新金山生物科技有限公司。辅料在使用前进行烘干处理。
包材:宽度58 mm,厚度8丝,铝箔复合膜材质,四川中金医药包装有限公司。包材符合GB/T 28118—2011《食品包装用塑料与铝箔复合膜、袋》规定。
N2:标准气,纯度≥99.9%。
1.1.3 培养基
活菌计数培养基:MRS培养基,北京路桥技术股份有限公司。培养基按照说明配制,添加质量浓度0.5 g/L半胱氨酸盐酸盐,121 ℃灭菌15 min后置于48 ℃水浴锅内备用。
1.1.4 主要仪器与设备
LabSwift-aw便携式水分活度仪,瑞士Novasina公司;CheckMate 3残氧检测仪,丹麦Dansensor公司;GZX-9070MBE电热鼓风干燥箱,上海博讯实业有限公司医疗设备厂;DXDFZ60F全自动粉剂包装机,北京华清三丰科技有限公司。
1.2 实验方法
1.2.1 样品制备
益生菌粉配方(g/L):低聚果糖350,乳清粉300,菊粉200,低聚半乳糖100,菌粉50。
将A6菌粉和BBMN68菌粉按照配方与辅料进行混合,以充氮和普通包装工艺制备2种菌种的样品,分别记为A6益生菌粉和BBMN68益生菌粉,样品规格2 g/袋,每组样品数量≥200袋。充氮样品残氧控制依据GB/T 26993—2011《奶粉定量充填包装机》,残氧量≤3%。包装完成后,将样品放置于-20、4、25和37 ℃的温度下进行储藏实验,分别在0、3、6、9和12个月取样进行检测。
1.2.2 水分含量测定
水分含量依据GB 5009.3—2016《食品安全国家标准 食品中水分的测定》第一法(直接干燥法)进行测定。检测样品在每个取样点分别做3次平行测定,结果取平均值。
1.2.3 水分活度测定
将待检样品和水分活度仪放置于22~25 ℃、空气相对湿度30%~40%的测定室平衡1~2 h。根据水分活度仪使用说明进行测定,检测样品在每个取样点分别做3次平行测定,结果取平均值。
1.2.4 活菌数测定
菌落计数依据 GB 4789.34—2016《食品安全国家标准 食品微生物学检测 双岐杆菌检验》中食品样品双歧杆菌计数方法,略作修改。称取待检样1.0 g,置于装有9.0 mL灭菌生理盐水的离心管内,旋涡振荡1~2 min,制成10倍稀释度样品匀液,然后做10倍系列梯度稀释,选取2~3个适宜稀释梯度,分别吸取1.0 mL样品匀液于无菌平板内,每个稀释度做3个平皿,及时将冷却至46 ℃的计数培养基倾注平皿,并单方向转动混合。待平板凝固后,倒置于厌氧培养盒内,(36±1)℃培养(48±2)h后计数。
2 结果与分析
2.1 益生菌粉储藏过程中水分含量的变化
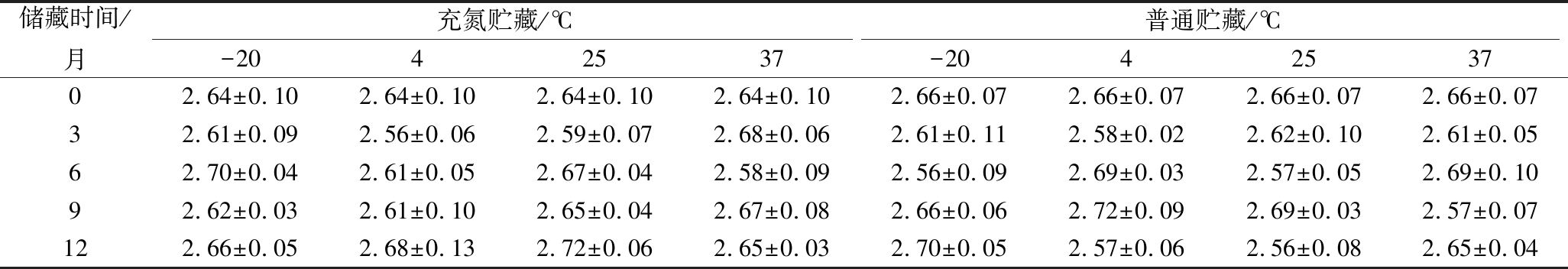
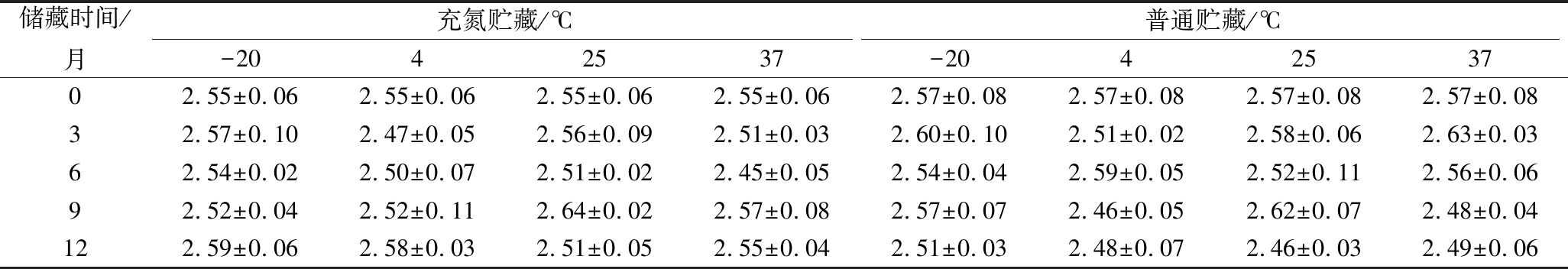
由表1和表2可知,2种益生菌粉随着储藏时间的延长,水分含量(质量分数)无明显变化,数值均小于4%,这有助于益生菌粉的储藏[13]。对比所有组别的水分含量,均无显著性差异(P>0.05),说明2种益生菌粉在储藏过程中可保持其水分含量稳定,且不受包装方式和储藏温度的影响。
表1 A6益生菌粉储藏过程中水分含量 单位:%
Table 1 Moisture content of A6 probiotics powder during storage
储藏时间/月充氮贮藏/℃普通贮藏/℃-2042537-204253702.64±0.102.64±0.102.64±0.102.64±0.102.66±0.072.66±0.072.66±0.072.66±0.0732.61±0.092.56±0.062.59±0.072.68±0.062.61±0.112.58±0.022.62±0.102.61±0.0562.70±0.042.61±0.052.67±0.042.58±0.092.56±0.092.69±0.032.57±0.052.69±0.1092.62±0.032.61±0.102.65±0.042.67±0.082.66±0.062.72±0.092.69±0.032.57±0.07122.66±0.052.68±0.132.72±0.062.65±0.032.70±0.052.57±0.062.56±0.082.65±0.04
表2 BBMN68益生菌粉储藏过程中水分含量 单位:%
Table 2 Moisture content of BBMN68 probiotics powder during storage
储藏时间/月充氮贮藏/℃普通贮藏/℃-2042537-204253702.55±0.062.55±0.062.55±0.062.55±0.062.57±0.082.57±0.082.57±0.082.57±0.0832.57±0.102.47±0.052.56±0.092.51±0.032.60±0.102.51±0.022.58±0.062.63±0.0362.54±0.022.50±0.072.51±0.022.45±0.052.54±0.042.59±0.052.52±0.112.56±0.0692.52±0.042.52±0.112.64±0.022.57±0.082.57±0.072.46±0.052.62±0.072.48±0.04122.59±0.062.58±0.032.51±0.052.55±0.042.51±0.032.48±0.072.46±0.032.49±0.06
2.2 益生菌粉储藏过程中水分活度的变化
由图1和图2可知,当储藏温度为-20和4 ℃时,2种益生菌粉水分活度无明显变化;当温度为25 ℃时,水分活度在储藏过程中开始缓慢上升;当储藏温度为37 ℃时,水分活度变化显著,A6和BBMN68益生菌粉2种包装方式分别在第3和6个月出现显著性差异。因此,储藏温度对益生菌粉水分活度的影响较大,贮藏温度越高,水分活度变化越大,而充氮包装可降低水分活度的波动,更好地维持产品稳定,这与贾宏信[14]的研究结果相似。同时从结果可知,储藏条件一致时,2种益生菌粉之间无显著性差异。
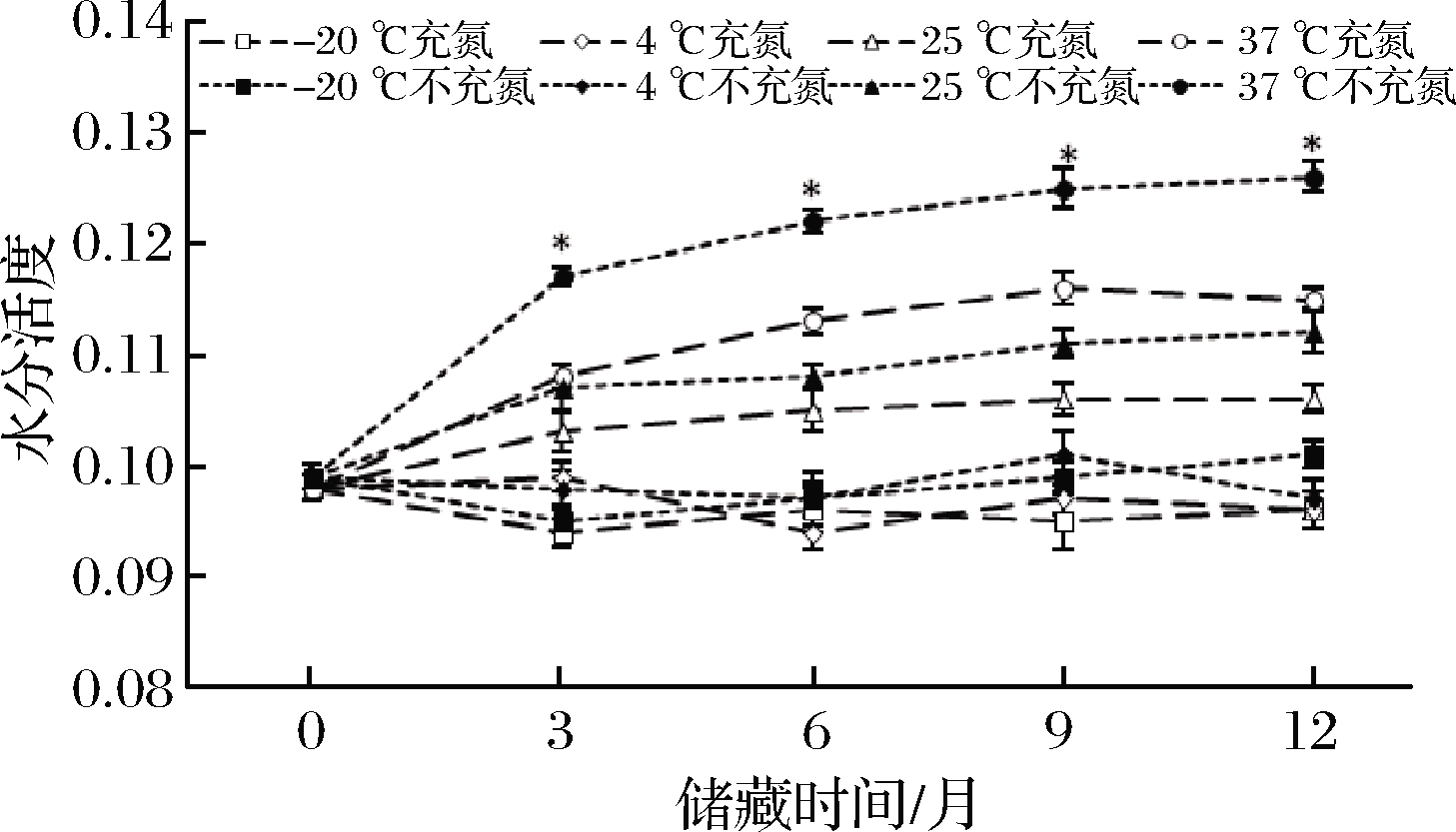
图1 A6益生菌粉储藏过程中水分活度的变化
Fig.1 Water activity change of A6 probiotics powder during storage 注:* 表示在相同储藏温度下,相同储藏时间普通包装与充氮 包装结果呈显著性差异(P>0.05)(下同)

图2 BBMN68益生菌粉储藏过程中水分活度的变化
Fig.2 Water activity change of BBMN68 probiotics powder during storage
对于益生菌类粉剂产品而言,一般要求水分活度<0.25[15-16],在低水分活度下可减少菌体的代谢活动,延长保质期,但水分活度不是越低越好,菌体仍需要一定量的水分来维持细胞结构,水分活度<0.1时,细胞膜上的磷脂更容易被氧化,造成细胞损伤[17]。KURTMANN等[18]和VESTERLUND等[19]分别研究了嗜酸乳杆菌La-5和鼠李糖乳杆菌在不同水分活度的食品中的贮藏稳定性,得到了相同的结果,当水分活度为0.11时,菌体存活率最高。本文研究的2种益生菌粉水分活度均维持在0.1~0.13,可较好维持产品的稳定性。
2.3 益生菌粉贮藏过程中活菌数的变化
由图3、图4可知,在-20和4 ℃下,活菌数保持稳定,存活率维持在85%以上;当温度为25 ℃时,活菌数随着储藏时间延长逐渐下降,储藏期结束,A6和BBMN68益生菌粉充氮包装活菌存活率分别为40.2%和32.7%,而普通包装仅为28.0%和17.3%,差异显著;当温度为37 ℃时,活菌数急剧降低,储藏12个月,充氮和普通包装的A6益生菌粉存活率分别为0.14%和0.033%,BBMN68益生菌粉为0.094%和0.013%。因此,温度对益生菌粉的活菌稳定性影响较大,即使在常温下储藏,活菌数仍会大幅度下降。

图3 A6益生菌粉储藏过程中的活菌数
Fig.3 Survival of A6 in probiotics powder during storage
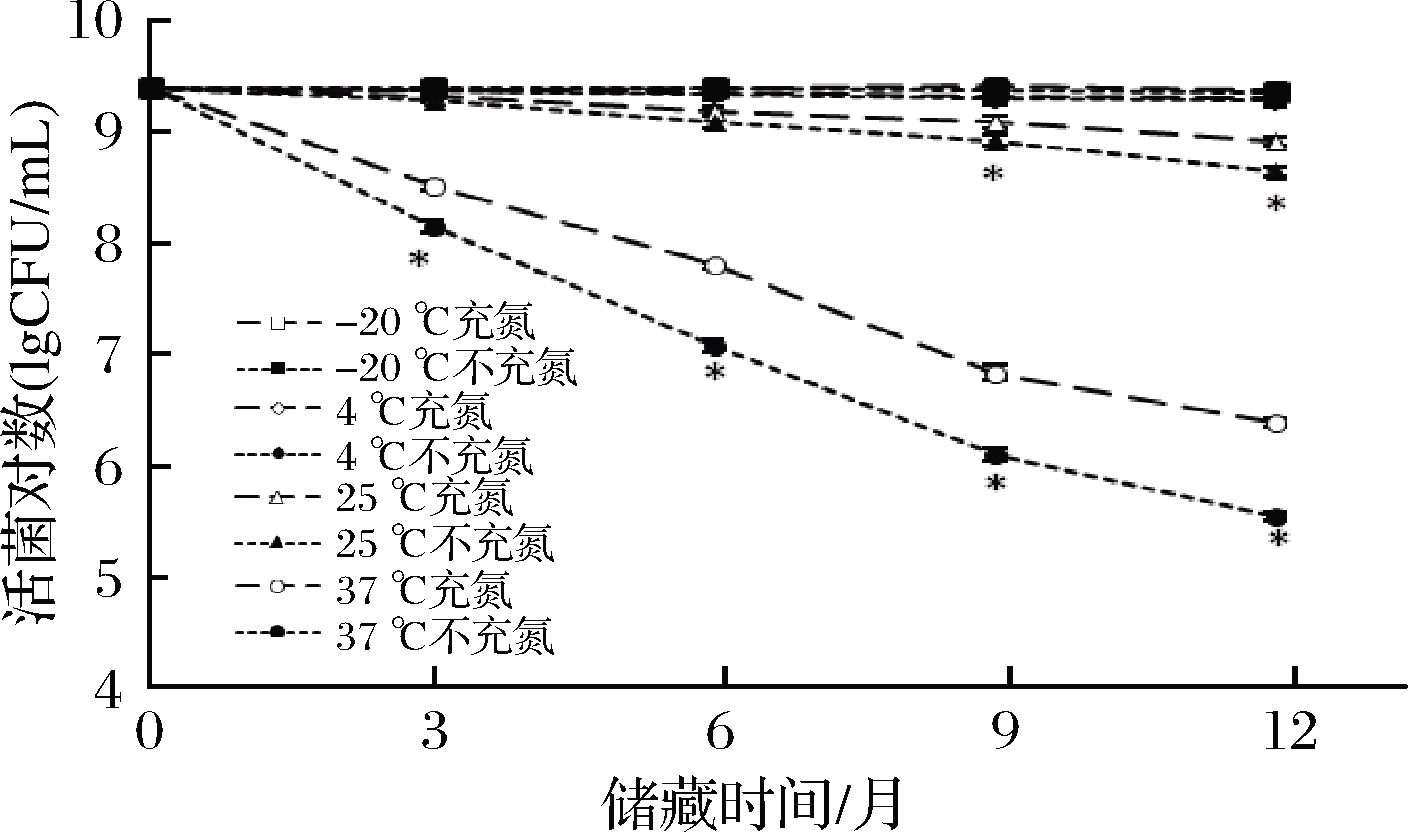
图4 BBMN68益生菌粉储藏过程中的活菌数
Fig.4 Survival of BBMN68 in probiotics powder during storage
益生菌是活的生命体,对温度极为敏感[20-23]。在较低温度下,菌体处于休眠状态,较为稳定,高温则导致菌体内蛋白等物质变性,功能丧失。而且不同菌株性状差异较大,导致其对高温的耐受能力不同[24-25]。由图3和图4结果可知,同样在25和37 ℃储藏下,A6益生菌粉的存活率普遍高于BBMN68益生菌粉,说明A6菌株具有更好的耐高温性能。
此外,细胞膜氧化反应也是影响菌体稳定性的重要因素,细胞膜主要是由磷脂双分子层构成,而磷脂易与O2发生氧化反应,使细胞膜不完整,高温则会加速氧化速率,促使菌体死亡。ISHIBASHI等[26]证实了益生菌在有氧条件下存活率下降,TEIXEIRA等[20]研究了益生菌粉中添加抗氧化剂有利于益生菌活菌数的保持,因此,针对含有益生菌的产品,应做到无氧包装或增加除氧能力,以保证产品质量。图3和图4结果表示,在37 ℃储藏下,不同包装的2种益生菌粉活菌数均在第3个月出现显著性差异,储藏期结束时,充氮包装使A6和BBMN68益生菌粉存活率分别提升4.2和7.2倍,保护效果极为显著。
3 结论与展望
综上所述,储藏温度是影响益生菌粉稳定性的关键因素,冷冻和冷藏条件可较好维持产品品质,当储藏温度升高至常温及以上时,产品稳定性则随温度的升高显著降低。通过改变包装方式,证明了充氮包装有利于益生菌粉储藏,特别是对耐氧性较差的长双歧杆菌,可有效改善该类益生菌在产品中的应用限制,促进益生菌粉市场的发展。
从本文研究结果可知,益生菌粉最佳储藏条件是冷冻或冷藏,然而这在实际操作中很难实现,特别是运输环节,不能保证全程冷链,且低温运输也意味着需要更高的成本,不利于益生菌粉市场的发展。充氮包装方式虽可改善益生菌粉稳定性,但却不能完全阻止益生菌死亡。所以如何提高常温及更高温度下益生菌粉的稳定性依旧是关注的热点,还需深入研究。
[1] FAO/WHO Experts’ Report.Health and nutritional properties of probiotics in food including powder milk with live lactic acid bacteria[R].2001.
[2] 王薇.科技与产业结盟成就千亿元益生菌市场[N].中国食品报,2019-5-27(001).
[3] ZHAO L, QIAO X, ZHU J, et al. Correlations of fecal bacterial communities with age and living region for the elderly living in Bama, Guangxi, China[J]. The Journal of Microbiology, 2011, 49(2): 186-192.
[4] ZHAO L, XU W, IBRAHIM S A, et al. Effects of age and region on fecal microflora in elderly subjects living in Bama, Guangxi, China[J]. Current Microbiology, 2011, 62(1): 64-70.
[5] 刘治麟,白海林,张建铭,等.动物双歧杆菌A6缓解小鼠便秘作用的研究[J].中国奶牛, 2015(15):32-35.
[6] SUN E, ZHAO L, REN F, et al. Complete genome sequence of Bifidobacterium animalis subsp. lactis A6, a probiotic strain with high acid resistance ability[J]. Journal of Biotechnology, 2015, 200: 8-9.
[7] XIAO M, XU P, ZHAO J, et al. Oxidative stress-related responses of Bifidobacterium longum subsp. longum BBMN68 at the proteomic level after exposure to oxygen[J]. Microbiology, 2011, 157(6): 1 573-1 588.
[8] YANG H, LIU A, ZHANG M, et al. Oral administration of live Bifidobacterium substrains isolated from centenarians enhances intestinal function in mice[J]. Current Microbiology, 2009, 59(4): 439-445.
[9] 赵亮.长寿老人源双歧杆菌延缓线虫衰老及其作用机制研究[D].北京:中国农业大学, 2011.
[10] YANG H, LIU S, IBRAHIM S A, et al. Oral administration of live Bifidobacterium substrains isolated from healthy centenarians enhanced immune function in BALB/c mice[J]. Nutrition Research, 2009, 29(4): 281-289.
[11] ZHU J, ZHAO L, GUO H, et al. Immunomodulatory effects of novel Bifidobacterium and Lactobacillus strains on murine macrophage cells[J]. African Journal of Microbiology Research, 2011, 5(1): 8-15.
[12] 丁圣,蒋菁莉,刘松玲,等.长双歧杆菌BBMN68对便秘模型小鼠的通便作用[J].食品科学,2011,32(3):195-198.
[13] ANANTA E, BIRKELAND S E, CORCORAN B, et al. Processing effects on the nutritional advancement of probiotics and prebiotics[J]. Microbial Ecology in Health and Disease, 2004, 16(2-3): 113-124.
[14] 贾宏信.充氮包装对乳粉贮存过程中水分、水分活度及益生菌活菌数变化的影响[J].中国乳品工业,2019,47(1):27-30.
[15] CH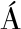 VEZ B E, LEDEBOER A M. Drying of probiotics: optimization of formulation and process to enhance storage survival[J]. Drying Technology, 2007, 25(7-8): 1 193-1 201.
VEZ B E, LEDEBOER A M. Drying of probiotics: optimization of formulation and process to enhance storage survival[J]. Drying Technology, 2007, 25(7-8): 1 193-1 201.
![]() V A, KAILASAPATHY K, et al. Encapsulation of probiotics for use in food products[M].New York: Encapsulation Technologies for Active Food Ingredients and Food Processing. Springer, 2010: 269-302.
V A, KAILASAPATHY K, et al. Encapsulation of probiotics for use in food products[M].New York: Encapsulation Technologies for Active Food Ingredients and Food Processing. Springer, 2010: 269-302.
[17] VIERNSTEIN H, RAFFALT J, POLHEIM D. Stabilisation of probiotic microorganisms[M].Dordrecht, Applications of Cell Immobilisation Biotechnology, Springer, 2005: 439-453.
[18] KURTMANN L, CARLSEN C U, RISBO J, et al. Storage stability of freeze-dried Lactobacillus acidophilus (La-5) in relation to water activity and presence of oxygen and ascorbate[J]. Cryobiology, 2009, 58(2): 175-180.
[19] VESTERLUND S, SALMINEN K, SALMINEN S. Water activity in dry foods containing live probiotic bacteria should be carefully considered: A case study with Lactobacillus rhamnosus GG in flaxseed[J]. International Journal of Food Microbiology, 2012, 157(2): 319-321.
[20] TEIXEIRA P C, CASTRO M H, MALCATA F X, et al. Survival of Lactobacillus delbrueckii ssp. bulgaricus following spray-drying[J]. Journal of Dairy Science, 1995, 78(5): 1 025-1 031.
[21] GARDINER G E, BOUCHIER P, O'SULLIVAN E, et al. A spray-dried culture for probiotic Cheddar cheese manufacture[J]. International Dairy Journal, 2002, 12(9): 749-756.
[22] DESMOND C, ROSS R P, O'CALLAGHAN E, et al. Improved survival of Lactobacillus paracasei NFBC 338 in spray-dried powders containing gum acacia[J]. Journal of applied microbiology, 2002, 93(6): 1 003-1 011.
[23] WANG Y C, YU R C, CHOU C C. Viability of lactic acid bacteria and Bifidobacteria in fermented soymilk after drying, subsequent rehydration and storage[J]. International Journal of Food Microbiology, 2004, 93(2): 209-217.
[24] GARDINER G E, O'SULLIVAN E, KELLY J, et al. Comparative survival rates of human-derived probiotic Lactobacillus paracasei and L.salivarius strains during heat treatment and spray drying[J]. Appl. Environ. Microbiol., 2000, 66(6): 2 605-2 612.
[25] CORCORAN B M, ROSS R P, FITZGERALD G F, et al. Comparative survival of probiotic Lactobacilli spray-dried in the presence of prebiotic substances[J]. Journal of Applied Microbiology, 2004, 96(5): 1 024-1 039.
[26] ISHIBASHI N, SHIMAMURA S. Bifidobacteria: Research and development in Japan[J]. Food Technology (Chicago), 1993, 47(6): 126-136.