樱桃番茄(Lycopersicon esculentum Mill. var. cerasiforme)又名圣女果、小番茄,既可作蔬菜又可作水果,口感好,营养价值高,风味独特,深受广大消费者青睐。樱桃番茄果实皮薄汁多,采后易受到机械损伤和微生物侵染,贮藏期间易腐烂变质[1],其中因微生物侵染导致的水果病害最为严重和普遍[2]。青霉(Penicillium spp.)、链格孢(Alternaria spp.)、镰刀菌(Fusarium)等是引起果蔬贮藏期病害的重要病原真菌,在引水果发腐烂的同时还能积累真菌毒素,如扩展青霉(Penicillium expansum)在低温贮藏条件下也可侵染果实产生棒曲霉素、桔霉素等潜在致癌物质[3-4]。
目前,采用化学合成杀菌剂是控制果蔬采后病害的主要方法,但由于化学杀菌剂的频繁使用,导致病原菌产生抗药性,造成环境污染,危害人类健康[5]。因此,开发安全、有效、绿色环保的天然杀菌剂替代化学合成杀菌剂已成为当前农产品采后贮藏与保鲜研究的一个热点。黄柏(Phellodendron chinense Schneid.)又名黄檗,芸香科(Rutaceae)植物,具有抗菌、抗滴虫、治疗肝炎、抗溃疡、抗氧化、抗癌等多种药理活性[6]。研究表明,黄柏提取物对稻瘟病菌、小麦纹枯病菌、稻纹枯病菌、小麦赤霉病菌、玉米小斑病菌、番茄枯萎病菌等多种植物病原真菌具有较强抑制作用[6-8]。但关于黄柏提取物对果蔬采后主要致病菌的抑制效果研究较少,尤其是对扩展青霉抑菌效果的研究未见报道。本试验以2种重要的樱桃番茄采后病原菌为靶标,系统研究黄柏提取物的抑菌活性,并对其粗提物的最佳萃取剂进行筛选,以期为新型天然果蔬保鲜剂的开发奠定基础。
1 材料与方法
1.1 材料
1.1.1 黄柏
中药黄柏,购于山西省运城市中药市场,使用枝皮部位。
1.1.2 供试菌种和培养基
链格孢(Alternatia alternata)、扩展青霉(Penicillium expansum),中国科学院微生物研究所,由马铃薯葡萄糖琼脂(PDA)培养基28 ℃下继代培养,在4 ℃冰箱保存备用。
1.2 方法
1.2.1 黄柏提取物的制备
采用超声波辅助醇提取法制备黄柏提取物。将阴干的黄柏枝皮在45 ℃恒温电热鼓风干燥箱中吹干至发脆,经粉碎后过80目筛备用。称取样品干粉100 g,用体积分数为70%的乙醇按6∶1(mL∶g)的液固比浸泡,充分搅拌使溶剂完全浸没中草药材料,置于避光处静置24 h后,在45 ℃,80 Hz的条件下超声辅助提取30 min,减压抽滤得滤液,残渣再次采取同样方法进行处理,重复提取3次,合并3次滤液。将滤液用旋转蒸发仪于40 ℃条件下减压浓缩至无溶剂蒸出(呈浸膏状),然后用50%的乙醇定容至1 000 g/L,密封标记后置于4 ℃冰箱中保存备用[6]。
1.2.2 黄柏提取物抑菌活性的测定
1.2.2.1 黄柏提取物对链格孢和扩展青霉的抑菌效果测定
采用菌丝生长速率法测定抑菌活性。取一定量上述提取液于PDA培养基中混合均匀,制成质量浓度为10 g/L的带药培养基,倒入培养皿中,待培养基凝固后,用内径6 mm的打孔器在菌落边缘生长旺盛区域打取菌饼,然后用接种针挑至培养皿中心处,每皿1个菌饼,每处理重复3次。以混有50%乙醇的PDA培养基作为对照,置于28 ℃恒温培养箱中培养。当对照组菌落生长至充满培养皿约80%时,采用十字交叉法测量供试病菌的菌落直径,按公式(1)计算生长抑制率。
抑菌率![]()
(1)
1.2.2.2 黄柏提取物对链格孢和扩展青霉最小抑菌浓度和最小杀菌浓度的测定
菌悬液的制备:无菌条件下,将病原菌接种到PDA培养基上,于28 ℃恒温培养箱中培养4~5 d后,用无菌水冲洗至瓶中,经过滤后充分振荡均匀形成孢子悬浮液,采用血球计数法,使孢子浓度控制在106 CFU/mL。
采用二倍稀释法,将黄柏提取液稀释成1.95~1 000 g/L共10个质量浓度梯度,然后按体积比1∶9的比例与融化的PDA培养基混合,制成提取液终质量浓度为0.195~100 g/L含药培养基,采用平板涂布法,取20 μL供试菌悬液均匀涂于含药培养基上,以50%乙醇处理作为空白对照,每处理重复3次,置于28 ℃的培养箱中培养。2 d后观察,以无菌生长的最低含药浓度为最小抑菌浓度(minimum inhibitory concentration,MIC),将无菌生长的培养皿继续培养7 d后观察,以无菌生长的最低含药浓度为最小杀菌浓度(minimum fungicidal,MFC)[9-10]。
1.2.2.3 黄柏提取物对链格孢和扩展青霉抑菌活性的室内毒力测定
将1 000 g/L的黄柏提取液与PDA培养基混合,制成最终质量浓度为12、6、3、1.5和0.75 g/L的含药培养基,按照“1.2.2.1”所述方法,采用菌丝生长速率法测定不同浓度黄柏提取物对病原菌生长的抑制率,每处理重复3次,以混有50%乙醇的PDA培养基作为对照。使用SPSS 21.0软件,以黄柏提取液浓度的对数值为横坐标,平均抑制率的机率值为纵坐标,计算毒力回归方程、相关系数(r)、半抑制浓度(half maximal inhibitory concentration,EC50)和置信区间[11]。
1.2.2.4 黄柏提取物对链格孢和扩展青霉孢子萌发的影响
采用稀释平板计数法测定提取液对病原菌孢子萌发的抑制作用[6]。取黄柏提取物,制成终质量浓度为12、6、3、1.5和0.75 g/L的含药培养基,制备106 CFU/mL的病原菌孢子悬浮液,并稀释成浓度约100 CFU/mL,吸取20 μL菌悬液均匀涂布于培养基上,28 ℃恒温培养箱中培养4 d,每处理重复3次,以混有50%乙醇的PDA培养基作为对照;按公式(2)计算抑制率:
抑制率![]()
(2)
式中:N0,对照组菌落数;N,涂布提取物平板菌落数。
1.2.3 黄柏不同极性萃取物的抑菌活性测定
称取黄柏枝皮干粉100 g,按照“1.2.1”所述方法提取,旋转蒸发浓缩为浸膏,用100 mL超纯水溶解后,依次用等体积石油醚、氯仿、乙酸乙酯、正丁醇分别萃取。各级萃取液经减压浓缩形成浸膏,分别用50%乙醇溶解,定容至质量浓度为400 g/L,最终得到石油醚相、氯仿相、乙酸乙酯相、正丁醇相和水相,4 ℃保存备用。以50%乙醇为对照,按照“1.2.2.1”所述方法,采用菌丝生长速率法测定不同萃取相对病原菌生长的抑制率,每处理重复3次。
1.2.4 黄柏提取物对樱桃番茄采后黑斑病和青霉果腐病的保护和治疗作用
挑选新鲜、大小均一、成熟度一致、无机械损伤和微生物侵染的樱桃番茄,洗净后在质量分数0.1%次氯酸钠溶液中浸泡1~2 min,清水冲洗,室温晾干备用。
保护作用试验:配制质量浓度为MIC的黄柏提取物,均匀喷洒于樱桃番茄表面,12 h后用病原菌孢子悬浮液(106 CFU/mL)均匀地喷洒于樱桃番茄表面,待菌液晾干后,置于一次性聚乙烯盒中,用打孔的聚乙烯保鲜袋包装。治疗作用试验:用病原菌孢子悬浮液(106 CFU/mL)均匀地喷洒于樱桃番茄表面,12 h后用质量浓度为MIC的黄柏提取物均匀地喷洒于樱桃番茄表面,果实自然晾干,置于一次性聚乙烯盒中,用打孔的聚乙烯保鲜袋包装。
将处理好的樱桃番茄置于25 ℃条件下放置,每隔3 d测定其发病率。以无菌水处理的果实为对照,对照和处理各设置3个平行,每个平行30个樱桃番茄,试验重复3次,通过公式(3)和(4)计算发病率和统计防治效果。
发病率![]()
(3)
防治效果![]()
(4)
2 结果与分析
2.1 黄柏提取物对链格孢、扩展青霉的抑制作用
如图1所示,黄柏提取物对链格孢和扩展青霉的菌丝生长均表现出较强的抑制作用,抑菌圈均达到50 mm以上(表1),抑菌率均达到70%以上,这可能与黄柏提取物中含有黄酮类和生物碱类等具有抑菌作用的化合物有关[12],且黄柏提取物对扩展青霉的抑菌活性较强,抑菌率达到84.5%。

a-c为链格孢:a-对照;b-10 g/L黄柏提取物处理; c-12 g/L正丁醇萃取相处理;d-f为扩展青霉:d-对照; e-10 g/L黄柏提取物处理;f-12 g/L正丁醇萃取相处理
图1 黄柏提取物及其正丁醇萃取相对链格孢、 扩展青霉菌丝生长的抑制
Fig.1 Inhibitory effect of P. chinense Schneid. extracts and n-buthanol extracts against mycelia growth of A. alternata and P. expansum
表1 黄柏提取物对链格孢、扩展青霉的抑菌效果
Table 1 Antifungal activity of P.chinense Schneid. extracts against A.alternata and P.expansum

供试菌种抑菌圈直径/mmMIC/(mg·mL-1)MFC/(mg·mL-1)毒力回归方程相关系数(r)EC50/(mg·mL-1)置信区间链格孢56.33±0.892550y=3.154+2.356x0.9936.0764.462~8.274扩展青霉65.73±0.8112.525y=3.607+2.190x0.9914.3233.316~5.636
此外,链格孢和扩展青霉对黄柏提取物的敏感性有所不同,如表1所示,黄柏提取物对链格孢、扩展青霉的MIC分别是25、12.5 g/L,MFC分别是50、25 g/L,因此扩展青霉对黄柏提取物的敏感性高于链格孢。
2.2 黄柏提取物对链格孢、扩展青霉的室内毒力测定
不同质量浓度黄柏提取物对链格孢、扩展青霉菌丝生长的抑制效果具有显著差异。如表2所示,当黄柏提取液质量浓度为0.75 g/L时,对链格孢、扩展青霉的抑制率分别为2.11%和5.83%,随着提取物质量浓度的增大,抑菌效果明显提高,当提取物质量浓度为6 g/L时,抑制率均达到50%左右,当提取物质量浓度增加至12 g/L时,提取物对链格孢、扩展青霉的抑制率分别为80.54%和87.45%,抑菌效果最显著。
以链格孢、扩展青霉为供试菌进行毒力试验,以黄柏提取液浓度的对数值为横坐标,平均抑制率的机率值为纵坐标,利用SPSS 21.0软件绘制标准曲线,求得毒力回归方程。由表1可知,毒力回归方程的相关系数均大于0.99,说明黄柏提取物的质量浓度与相对应的抑制率之间存在良好的线性关系,且均呈正相关。黄柏提取物对链格孢、扩展青霉的EC50值分别为6.076和4.323 g/L,因此,黄柏提取物对扩展青霉的反应更灵敏,抑制效果更好,这与抑菌活性的测定结果一致。
2.3 黄柏提取物对链格孢、扩展青霉孢子萌发的抑制作用
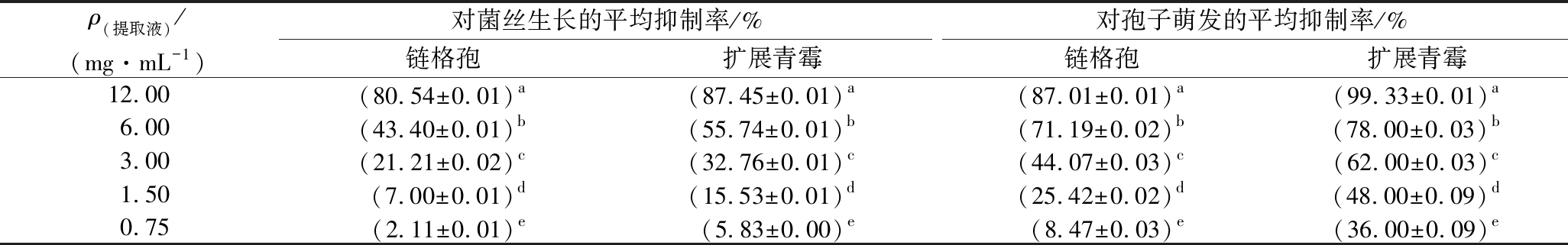
相同质量浓度下,黄柏提取物对链格孢、扩展青霉孢子萌发表现出不同的抑制作用,如表2所示,当质量浓度为12 g/L时,对链格孢、扩展青霉孢子萌发的抑制率分别为87.01%和99.33%,对扩展青霉孢子萌发的抑制作用更强,几乎完全抑制扩展青霉孢子的萌发。随着提取液质量浓度的降低,抑制作用均显著减弱,当质量浓度为0.75 g/L时,对扩展青霉孢子萌发的抑制率在30%以上,而对链格孢的抑制率不到10%。
表2 不同浓度黄柏提取物对链格孢、扩展青霉菌丝生长和孢子萌发的抑制作用
Table 2 Inhibitory effect of different concentrations of P.chinense Schneid. extracts against mycelia growth and spore germination of A.alternata and P.expansum
ρ(提取液)/(mg·mL-1)对菌丝生长的平均抑制率/%对孢子萌发的平均抑制率/%链格孢扩展青霉链格孢扩展青霉12.00(80.54±0.01)a(87.45±0.01)a(87.01±0.01)a(99.33±0.01)a6.00(43.40±0.01)b(55.74±0.01)b(71.19±0.02)b(78.00±0.03)b3.00(21.21±0.02)c(32.76±0.01)c(44.07±0.03)c(62.00±0.03)c1.50(7.00±0.01)d(15.53±0.01)d(25.42±0.02)d(48.00±0.09)d0.75(2.11±0.01)e(5.83±0.00)e(8.47±0.03)e(36.00±0.09)e
注:表中数据为3次重复的平均值,每列数据后不同小写字母表示在5%水平有显著性差异(下同)
2.4 黄柏不同极性萃取物对链格孢、扩展青霉的抑菌效果
黄柏提取物经分步萃取后,依次得到5个萃取相,不同萃取相对链格孢和扩展青霉的抑菌效果见图1和表3。与粗提液相比,正丁醇相的抑菌效果最好,对链格孢和扩展青霉的抑菌圈直径分别为70.58和75.35 mm,抑菌率均达到90%以上。氯仿、石油醚、乙酸乙酯和水相对链格孢的抑菌率均在60%左右,抑菌效果显著低于正丁醇相和粗提液;氯仿相对扩展青霉的抑菌率为64.97%,抑菌效果次于正丁醇相、粗提液,石油醚、乙酸乙酯和水相的抑菌效果均不到5%,几乎没有抑菌作用。粗提液经正丁醇萃取后抑菌效果显著增强,说明黄柏提取物的抑菌活性物质主要存在于正丁醇萃取部位,且经正丁醇萃取可有效富集黄柏的抗菌活性物质。
表3 黄柏提取物不同萃取相对链格孢、扩展青霉的抑菌效果
Table 3 Antifungal activity of different polarity fractions of P.chinense Schneid. extracts against A.alternata and P.expansum

萃取相链格孢扩展青霉抑菌圈直径/mm平均抑制率/%抑菌圈直径/mm平均抑制率/%石油醚相(45.68±1.68)c(58.82±0.02)b(0.97±0.20)d(1.22±0.00)c氯仿相(47.65±1.22)c(61.35±0.02)b(51.47±1.01)c(64.97±0.01)b正丁醇相(70.58±0.13)a(90.88±0.00)a(75.35±0.32)a(95.12±0.00)a乙酸乙酯相(45.08±1.22)c(58.05±0.02)b(2.05±0.12)d(2.59±0.00)c水相(44.72±1.07)c(57.58±0.01)b(0.95±0.34)d(1.20±0.00)c黄柏粗提液(56.33±0.89)b-(65.73±0.81)b-50%乙醇(对照)----
2.5 黄柏提取物对樱桃番茄黑斑病和青霉果腐病的防治效果
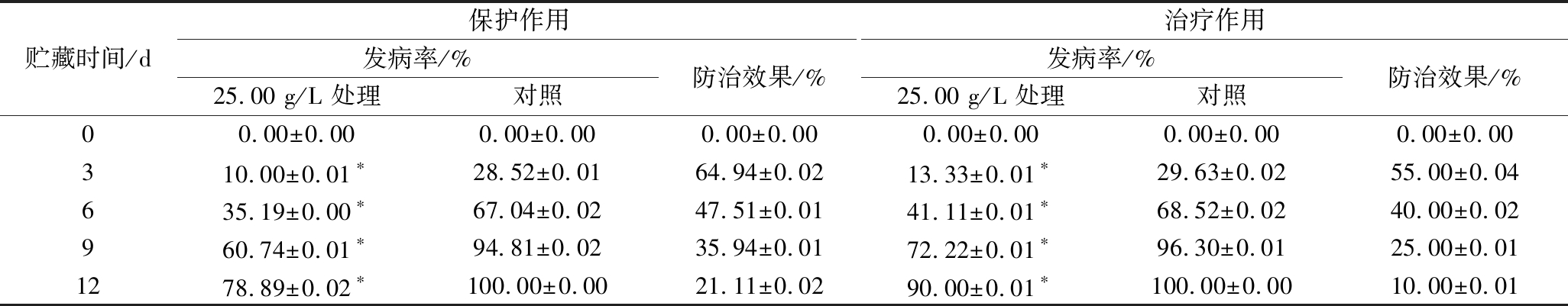
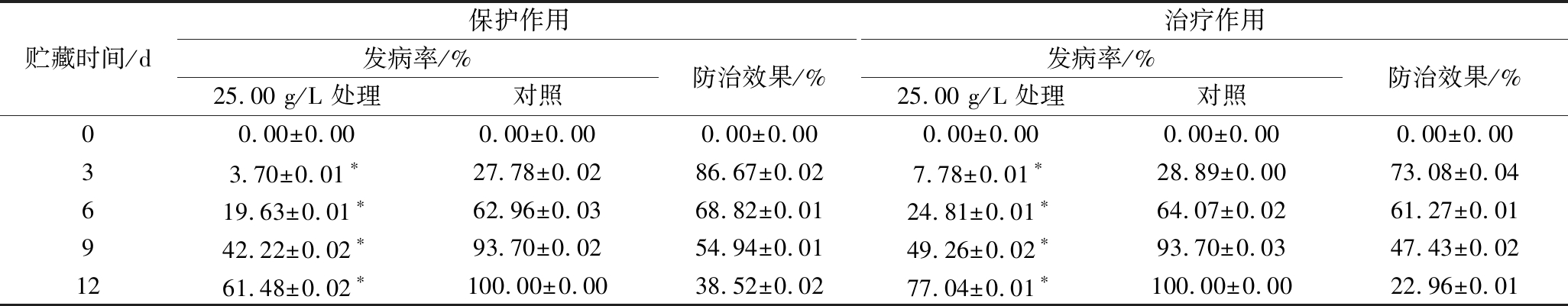
樱桃番茄是典型的呼吸跃变型果实,采后很快进入呼吸跃变期出现呼吸高峰,之后呼吸强度逐渐下降,因此果实极易腐烂变质。番茄黑斑病和青霉果腐病是樱桃番茄采后主要病害,对2种病害的保护作用试验表明(表4、表5),在相同的贮藏时间和贮藏条件下,处理组果实发病率均显著低于对照组。贮藏3 d时,处理组对番茄黑斑病和青霉果腐病的防治效果分别为64.94%和86.67%;贮藏6 d时,防治效果分别为47.51%和68.82%;随着贮藏时间的延长,发病率均呈逐渐上升的趋势,对照组的发病率增加速度较快,贮藏9 d时,对照组2种病害的发病率都已超过90%,而处理组的发病率仍然显著低于对照组,分别为60.74%和42.22%。治疗作用试验表明(表4、表5),在相同的贮藏时间和贮藏条件下,经提取物处理的果实发病率均显著低于对照组,且随着贮藏时间的延长,果实的发病率逐渐增大。但在相同贮藏时间下,黄柏提取物对2种病害的治疗防治效果均低于保护防治效果。说明质量浓度为MIC的提取物表现了显著的保护和治疗作用,且保护防治效果更好,黄柏提取物可显著减缓樱桃番茄果实的腐烂速度,且对青霉果腐病的抑制效果更好,这一结果与提取物抑菌活性的离体测定结果一致。
表4 黄柏提取物对樱桃番茄采后黑斑病的保护及治疗作用
Table 4 Protective and therapeutic effects of P.chinense Schneid. extracts on black rot disease in postharvest cherry tomato
贮藏时间/d保护作用治疗作用发病率/%25.00 g/L 处理对照防治效果/%发病率/%25.00 g/L 处理对照防治效果/%00.00±0.000.00±0.000.00±0.000.00±0.000.00±0.000.00±0.00310.00±0.01∗28.52±0.0164.94±0.0213.33±0.01∗29.63±0.0255.00±0.04635.19±0.00∗67.04±0.0247.51±0.0141.11±0.01∗68.52±0.0240.00±0.02960.74±0.01∗94.81±0.0235.94±0.0172.22±0.01∗96.30±0.0125.00±0.011278.89±0.02∗100.00±0.0021.11±0.0290.00±0.01∗100.00±0.0010.00±0.01
注:表中数据为3次重复的平均值,*表示处理样品与对照样品在0.05水平有显著性差异
表5 黄柏提取物对樱桃番茄采后青霉果腐病的保护及治疗作用
Table 5 Protective and therapeutic effects of P.chinense Schneid. extracts on blue mold fruit rot disease in postharvest cherry tomato
贮藏时间/d保护作用治疗作用发病率/%25.00 g/L 处理对照防治效果/%发病率/%25.00 g/L 处理对照防治效果/%00.00±0.000.00±0.000.00±0.000.00±0.000.00±0.000.00±0.0033.70±0.01∗27.78±0.0286.67±0.027.78±0.01∗28.89±0.0073.08±0.04619.63±0.01∗62.96±0.0368.82±0.0124.81±0.01∗64.07±0.0261.27±0.01942.22±0.02∗93.70±0.0254.94±0.0149.26±0.02∗93.70±0.0347.43±0.021261.48±0.02∗100.00±0.0038.52±0.0277.04±0.01∗100.00±0.0022.96±0.01
注:表中数据为3次重复的平均值,*表示处理样品与对照样品在0.05水平有显著性差异
3 结论与讨论
新型、高效的天然杀菌剂是近年来国内外研究领域的一大热点,本试验以黄柏为材料,研究了其对樱桃番茄主要采后病原菌——链格孢和扩展青霉的抑菌作用。研究结果表明,黄柏提取物对这2株病原真菌均有良好的抑菌效果,当提取物质量浓度为12 g/L时,对链格孢和扩展青霉的菌丝生长抑制率和孢子萌发抑制率均达到80%以上,而吴振宇等[13]报道当提取物质量浓度为60 g/L,黄柏对链格孢的抑菌率才能达到80%以上,抑菌浓度远远高于本试验结果,这可能与提取物制备方法不同有关,与水提法相比,超声波辅助醇提取法所制备的提取物抑菌活性更强,利用超声波振动增加溶剂进入植物细胞的渗透性,强化被提取物在植物细胞与提取介质间的传质速率[14],同时,提取液中除了水溶性的成分外,还有不溶于水的有效成分存在,可大大提高抑菌作用。研究还发现,相同浓度下,黄柏提取物对扩展青霉的抑制作用高于链格孢,当提取物质量浓度为12 g/L时,对扩展青霉孢子萌发抑制率接近100%,且MIC、MFC以及EC50值均相对较小,说明扩展青霉对黄柏提取物的反应更敏感。
在室内活体防效测定试验中,黄柏提取物对樱桃番茄果实黑斑病和青霉果腐病均表现出显著的保护和治疗作用,且保护作用更强,在果实贮藏12 d后,对照组全部腐烂,保护作用试验处理组黑斑病和青霉果腐病的发病率分别降低了21.11%和38.52%,这与黄柏提取液本身具有抑菌作用密切相关,在樱桃番茄采后贮藏期间能有效减少病原真菌的侵染和病害的发生。因此,黄柏可以作为开发天然防腐保鲜剂的材料,具有较好的开发潜力和应用前景。有研究表明,黄柏的主要化学成分为黄酮类和生物碱类,此外还含有易挥发的萜类化合物[8],但具体有效抑菌活性成分仍不清楚,本试验采用溶剂萃取对黄柏提取物进行了初步分离,研究发现,正丁醇萃取物对链格孢和扩展青霉的抑菌率均达到90%以上,这一结果与万春鹏等的研究结果一致[16],说明黄柏提取物的抑菌活性物质主要存在于正丁醇萃取部位,本研究为进一步分离、纯化和鉴定抑菌活性成分奠定基础,同时也为开发新型、天然、经济、有效果蔬保鲜剂提供了线索和依据。
[1] 宋姝婧,王晓拓,王志东,等.5种植物精油对樱桃番茄常温保鲜效果的影响[J].核农学报,2015,29(5):932-939.
[2] MU OZ Z.Sensitivity of botrytis cinerea to chitosan and acibenzolar-S-methyl[J].Pest Management Science,2010,66(9):974-979.
OZ Z.Sensitivity of botrytis cinerea to chitosan and acibenzolar-S-methyl[J].Pest Management Science,2010,66(9):974-979.
[3] 王瑶,姜冬梅,王刘庆,等.拮抗酵母控制果蔬采后真菌病害研究进展[J].食品工业科技,2018,39(8):309-317.
[4] MIEDES E,LORENCES E P.The Implication of xyloglucan endotransglucosylase hydrolase (XTHs) in tomato fruit infection by Penicillium expansum Link.A.[J].Journal of Agricultural and Food Chemistry,2007,55(22):9 021-9 026.
[5] WEI Yingying,MAO Shubo,TU Kang.Biological control of postharvest diseases of fruits and vegetables by microbial antagonists [J].Journal of Nanjing Agricultural University,2012,40(4):411-441.
[6] 马欣,霍蓉,乔俊卿,等.黄柏提取物对番茄枯萎病的生物防治效果[J].江苏农业科学,2016,44(5):178-180.
[7] 潘波,蔡丽丽,关丽杰.22种中草药提取物的抑菌活性研究[J].沈阳化工学院学报,2007,21(4):257-260.
[8] 唐静,周立刚,周亚明,等.黄柏果实提取物对植物病原真菌的抑制作用[J].天然产物研究与开发,2008(20):505-507.
[9] 刘琼,张新龙,黄琦,等.茼蒿粗提物对西瓜枯萎病菌的抑菌活性[J].江西农业大学学报,2015,37(5):832-835.
[10] 周梦娇,万春鹏,陈金印.桂枝提取物抑菌活性研究[J].食品工业科技,2014,35(12):96-98.
[11] 孙昊,张万萍,孟繁博,等.番茄采后灰霉病原对几种抑菌剂的敏感性研究[J].食品与机械,2014,30(1):165-168,175.
[12] 李嘉诚,吴岚,蔡同凯,等.黄柏化学成分及其药理作用研究进展[J].药学实践杂志,2018,36(5):389-391,398.
[13] 吴振宇,艾启俊,王燕,等.中草药提取物对链格孢菌抑制作用增效组合的研究[J].食品科学,2009,30(3):36-38.
[14] 李景华,王超,王黎明,等.超声波辅助提取关黄柏中巴马汀的研究[J].吉林医药学院学报,2016,37(3):187-190.
[15] 万春鹏,周梦娇,刘洋,等.桂枝抑制柑橘采后两种病原菌活性物质研究[J].江西农业大学学报,2014,36(2):319-325.