牦牛是生长在高海拔、缺氧、严寒的青藏高原地带且以天然放牧为主的特有牛种,其肉中富含多种氨基酸及矿物质,蛋白质含量高,脂肪含量较低[1]。如今,人们的食品安全意识不断提高,消费者对食品的天然性、安全性、绿色性有越来越多的关注,由于牦牛肉具备以上优点,逐渐受到广大消费者的青睐。
评价肉食用品质的指标主要有嫩度、色泽、保水性等,而这些指标都会受到外界诸多因素的影响,其中宰后胴体冷却温度是影响肌肉成熟进程和食用品质的关键控制点[2]。宰后冷却的目是为了尽快降低胴体温度,抑制胴体表面微生物的生长繁殖,从而保证肉品安全,最大限度地延长货架期。HOFFMAN等[3]研究表明,宰后在37 ℃条件下放置3 h后再于4 ℃冷库中冷却的牛胴体肌肉嫩度显著高于普通冷却处理的肉样。MUELA等[4]提出将宰后羊胴体分别放置在0~2 ℃、2~4 ℃和4~6 ℃进行冷却排酸,其肉色、消费者整体满意度、贮藏过程中汁液损失等评价指标上均存在很大差异。FERN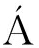 NDEZ等[5]研究指出延迟冷却导致早期钙激活酶的失活率降低,提高了钙激活酶参与宰后肌肉嫩化的速度。惠小洋等[6]研究发现快速冷却能显著降低肌肉冷收缩程度同时能够提高牛肉的保水性。以上研究均说明宰后不同温度下的冷却方式确实对肉的成熟机理及品质产生影响。
NDEZ等[5]研究指出延迟冷却导致早期钙激活酶的失活率降低,提高了钙激活酶参与宰后肌肉嫩化的速度。惠小洋等[6]研究发现快速冷却能显著降低肌肉冷收缩程度同时能够提高牛肉的保水性。以上研究均说明宰后不同温度下的冷却方式确实对肉的成熟机理及品质产生影响。
目前市场上销售的鲜肉主要分为三类——热鲜肉、冷冻肉和冷却肉。冷却肉被认为是最科学,高品质的生鲜肉,具有营养、卫生、安全、鲜嫩等特点,将会逐渐成为我国鲜肉消费领域的主流[7]。但是,传统冷却肉在0~4 ℃贮运销售,不能够完全抑制嗜冷微生物的生长繁殖,存在货架期较短、表面褐变严重及保水性差等问题,不能满足广大消费者的实际需求。因此,本研究选取青海牦牛为研究对象,对宰后牦牛背最长肌分别进行常规冷却和快速冷却方式处理,以探究2种冷却方式对牦牛肉贮藏过程中品质变化的影响,并客观评价2种冷却方式处理肉品质变化的差异性,为优化现有的冷却工艺,延长牦牛肉保鲜期提供理论依据。
1 材料与方法
1.1 材料与试剂
试验材料:选取自然放牧条件下,生长发育良好、体重均匀[(300±20) kg]、公母各半的4~6岁牦牛10头,宰前24 h禁食禁水,进行标准化屠宰。
试验试剂:KCl、HCl、NaN3、KI、MgCl2、CuSO4、NaOH、EDTA、K3PO4、酒石酸钾钠、三氯乙酸,天津市北辰方正试剂厂;甲基红,天津市光复精组化工研究所;无水Na2CO3、无水乙醇、浓H2SO4、溴甲酚,以上试剂均为分析纯。
1.2 仪器与设备
XHF-DY型高速分散器,宁波新芝生物科技股份有限公司;C-LM3B型肌肉嫩度仪,东北农业大学工程学院;GT16-3型高速台式离心机,上海卢湘仪离心机仪器有限公司;SG8-B型便携式pH计,深圳市鑫航兴科技有限公司;CR-10型色差仪,柯尼美能达有限公司;YYW-2型应变式控制式无侧限压力仪,南京土壤仪器厂有限公司;DHG-9140型电热恒温鼓风干燥箱,山东博科生物产业有限公司;GM1311X型电子数显食品温度计,衡水盛杰仪器仪表有限公司;DKS28型恒温水浴锅,上海精宏实验设备有限公司;SP-765P型紫外可见分光光度计,上海光谱仪器责任有限公司。
1.3 试验方法
1.3.1 样品采集与处理
宰后45 min内迅速取出牦牛左右两侧背最长肌作为试验对象,随后从每头牦牛背最长肌取约30 g肉样,重复3~5次,然后用耐低温锡纸包装后投入到液氮罐中,作为0 h的肉样。其余肉样中同一头牦牛左右两侧背最长肌随机分成2组,其中第1组按照常规冷却(conventional chilling, CC)工艺处理;第2组按照快速冷却(rapid chilling, RC)工艺处理。常规冷却组的肉样置于4 ℃冷库中贮藏;快速冷却组的肉样首先置于-18 ℃环境的冷库中,当其中心温度降至4 ℃后立即转移至4 ℃冷库中继续贮藏。在此过程中,分别在宰后成熟时间点0、3、6、12、24、72、120、168、216 h测定2组肉样pH、色度、剪切力等指标。对于总挥发性盐基氮(total volatile base nitrogen,TVB-N)等不便于立即测定的指标,应准时在设计时间点采集肉样后置于液氮中暂时保存并迅速运回至实验室转移到-80 ℃的超低温冰箱冻藏待测。
1.3.2 指标测定方法
1.3.2.1 pH
采用便携式酸度计对肉样pH值进行测定,测定时先对酸度计进行校准,然后将酸度计的探头插入肉样中深度约2 cm,当酸度计的读数稳定之后立即记录显示的数据,每组各个时间点肉样重复测定3次,取平均值。
1.3.2.2 色度
采用色差仪对肉色进行测定。测定前先对仪器进行校准,设置光源为D65,测量直径8 mm,标准视角10°,并将肉样新切横断面氧合30 min,测定时使肉样尽量平整并将探头完全覆盖于肉样表面,每块肉样选取3处测定。
1.3.2.3 剪切力
将质量约50 g规则整齐且表面无脂肪和筋膜的肉样装入蒸煮袋中,在预先恒温的80 ℃水浴锅中加热至中心温度达到75 ℃,恒温保持5 min后从水浴锅中取出并冷却至室温,然后将肉样切成1 cm×1 cm×5 cm的长条,用肌肉嫩度仪测定剪切力值,每组平行测定3次,取平均值,单位为牛顿(N)。
1.3.2.4 加压损失
采用经FAROUK[8]改进的加压滤纸法对肉样的加压损失进行测定。沿垂直于肌原纤维方向用取样器取厚度为1 cm肉样,精确称量其质量,记为m1,然后将肉样用双层纱布包裹并在其上下各垫18层滤纸并置于压力仪平台上加压至1 283.80 N,保持5 min,立即称量其质量,记为m2,按公式(1)计算加压损失率:
加压损失![]()
(1)
式中:m1,加压前肉样质量,g;m2,加压后肉样质量,g。
1.3.2.5 蒸煮损失
参照贾娜等[9]方法并对其稍作修改,取肉样质量为w1(g),放入塑料蒸煮袋中并置于80 ℃的恒温水浴锅中,当待肉样中心温度上升至75 ℃后恒温保持20 min,取出后冷却至室温,称重,计为w2(g),按公式(2)计算蒸煮损失率:
蒸煮损失![]()
(2)
式中:w1,蒸煮前肉样质量,g;w2,蒸煮后肉样质量,g。
1.3.2.6 挥发性盐基氮
参照GB 5009.228—2016《食品安全国家标准食品中挥发性盐基氮的测定》[10],采用半微量定氮法对挥发性盐基氮进行测定。
1.3.2.7 硫代巴比妥酸反应产物(thiobarbituric acid reactant substances,TBARS)
参考张宏博等[11]的方法,并对其略作修改。准确称量肉样2.0 g,并用绞肉机绞碎,置于100 mL三角瓶中,之后在其中加入三氯乙酸混合溶液(含0.1% EDTA)20 mL,充分振摇30 min,用离心机在1 600 r/min的条件下离心5 min,离心结束后用双层滤纸对其进行2次过滤,准确移取上述滤液5 mL置于25 mL比色管内,加入5 mL氯仿,摇匀,待其静置分层后,取上清液分别在532 nm和600 nm处比色(同时做空白试验),记录吸光度值,按公式(3)计算TBARS值:
TBARS/(mg·kg-1)=7.91×(A1-A2)+0.010 3
(3)
式中:A1,532 nm处的吸光度值;A2,600 nm处的吸光度值。
1.3.2.8 感官评价
参考黄彩燕等[12]的方法,并略作修改。感官评定由本实验室经过专业训练的10名同学组成,对2种不同冷却方式处理的2种牦牛肉在贮藏过程中肉的感官性状的5个方面进行评分,评定标准如表1所示。
表1 牦牛肉感官评分标准
Table 1 Sensory evaluation standard of yak meat

评分感官指标颜色气味弹性组织状态总体可接受性10色泽鲜红,颜色均匀,有光泽具有牛肉特有的气味,无任何异味弹性好,指压后凹陷立即恢复没有出水,牛肉表面不发黏接受性非常高8色泽较鲜红,颜色均匀,有光泽具有牛肉气味,无异味弹性较好,指压后凹陷可恢复稍有出水,牛肉表面不发黏接受性高6色泽暗红,切面尚有光泽,新切面湿润香味差或无鲜味弹性一般,指压后凹陷缓慢恢复出水较多,牛肉表面不发黏可接受4色泽较暗红,切面无光泽有异味,比较明显无弹性,指压后凹陷不能恢复出水较多,牛肉表面发黏较能接受2色泽暗褐色,切面呈深灰色有异味,不可接受弹性完全丧失,指压后凹陷明显出水较多,牛肉表面发黏严重不可接受
1.4 数据处理与统计分析
采用Microsoft Office Excel 2016对所得数据进行统计,并用SPSS 22.0软件进行Duncan显著性检验。试验结果用 “平均值±标准差”表示,用Origin 9.1进行绘图。
2 结果与分析
2.1 冷却方式对肌肉pH值的影响
由图1可知,2种冷却方式处理的牦牛肉在贮藏过程中pH值均逐渐下降,在达到极限pH后又缓慢上升。常规冷却组pH在宰后72 h内显著降低(P<0.05),并于宰后72 h达到极限pH 5.56;120~216 h,牦牛肉pH维持在5.65左右,无明显差异(P>0.05);快速冷却组在宰后120 h内pH显著下降(P<0.05),于120 h达到极限pH 5.57;贮藏至216 h,牦牛肉pH为5.62,较120 h稍有上升但差异不显著(P>0.05)。在整个贮藏过程中,宰后3 h与6 h,快速冷却组牦牛肉pH极显著高于常规冷却组(P<0.01);宰后 72 h,快速冷却组pH显著高于常规冷却组(P<0.05)。72 h之后,常规冷却组pH高于快速冷却组,但两者之间无显著差异(P>0.05)。同时,2组极限pH差异也不显著(P>0.05)。
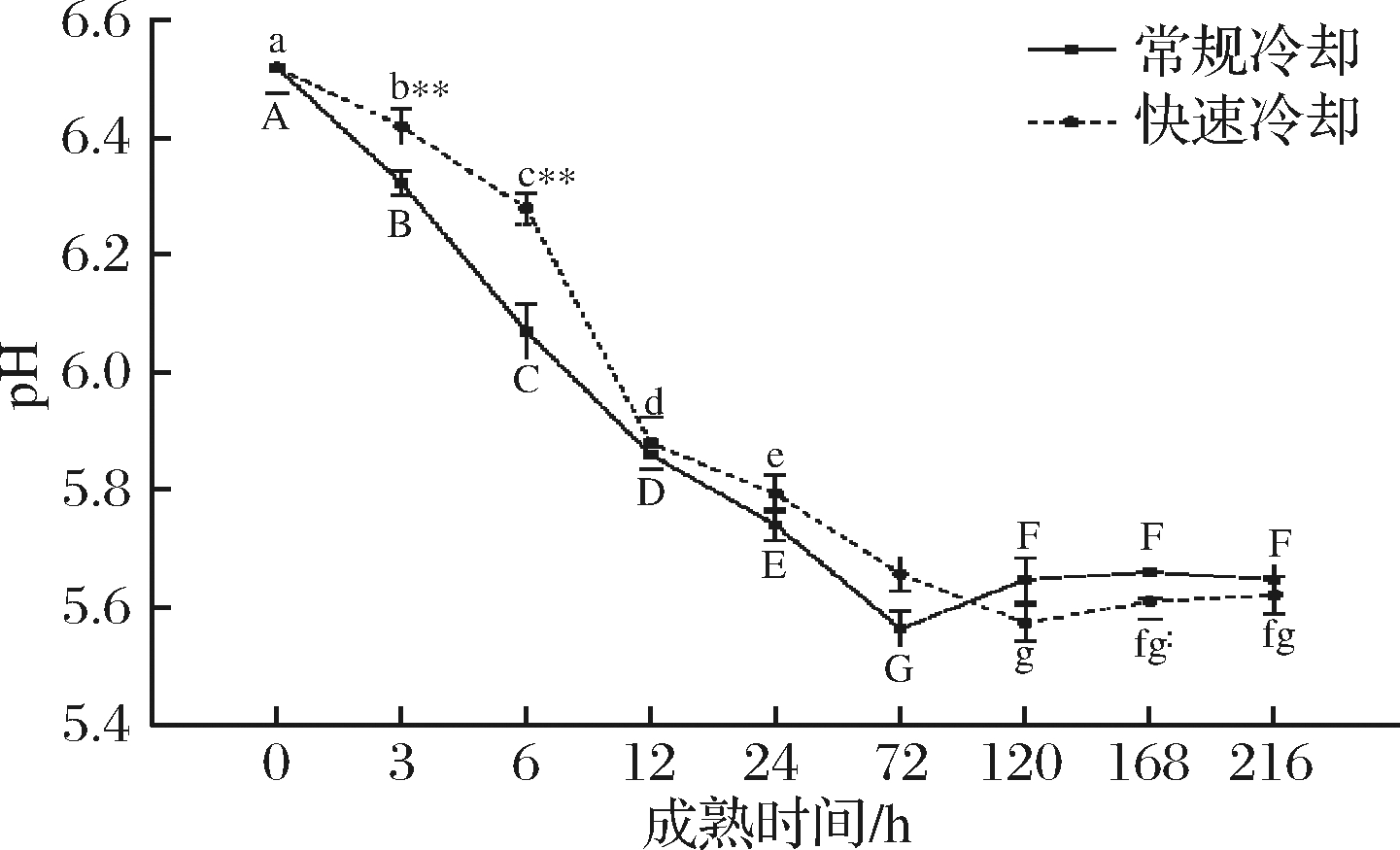
图1 冷却方式对肌肉pH值的影响
Fig.1 Effect of chilling methods on pH value of muscle
注:图中大、小写字母分别表示常规冷却和快速冷却组在贮藏
过程中指标变化差异显著(P<0.05);常规冷却组和快速冷却组
在同一成熟时间点指标变化差异显著用“*”表示(P<0.05),
差异极显著用“**”表示(P<0.01)(下图、下表同)
2.2 冷却方式对肌肉肉色的影响
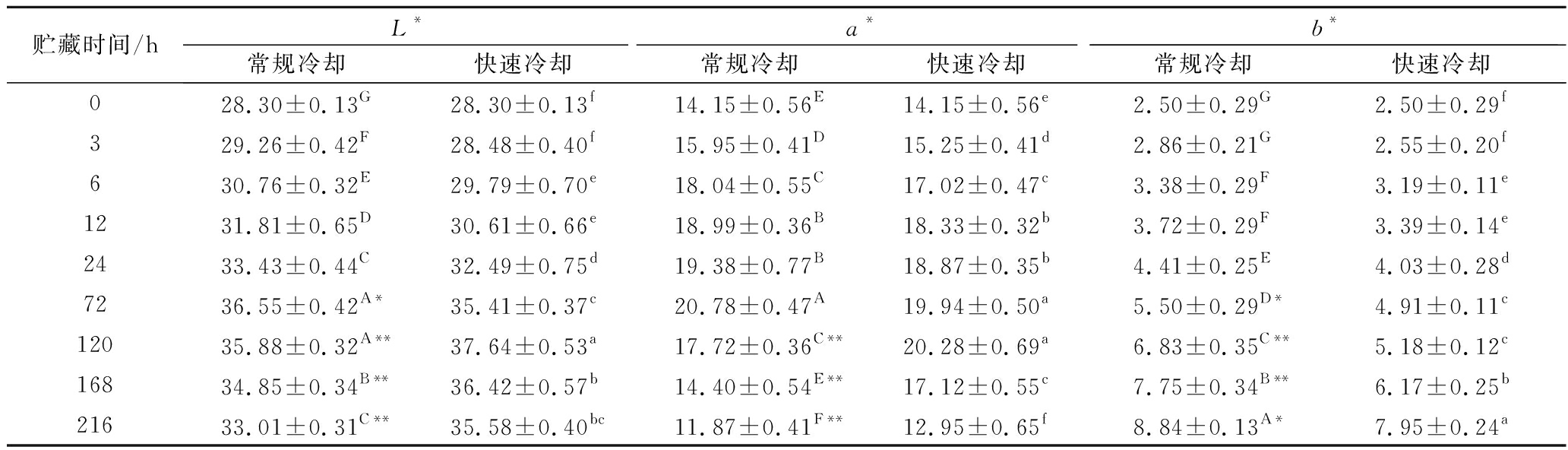
表2所示为牦牛肉在2种冷却方式处理下宰后贮藏过程中肉色的变化情况。由表2可知,2种不同冷却方式下牦牛肉L*值均呈先上升后下降的变化趋势。常规与快速2组L*值分别于宰后72、120 h达到最大值36.55、37.64,随后开始显著下降(P<0.05)。在整个贮藏阶段,常规冷却组L*值在0~24 h虽高于快速冷却组,但差异不显著。贮藏至120~168 h时,快速冷却组L*值极显著高于常规冷却组(P<0.01)。不同冷却方式下牦牛肉a*值呈现先上升后下降的趋势。宰后初期,常规冷却组a*上升较快,于72 h达到最大值20.78,随后显著下降(P<0.05),贮藏至216 h时降至最低。而快速冷却组a*值在宰后初期上升较慢,在贮藏至120 h时达到最大值20.28,之后显著下降(P<0.05)。整个贮藏过程中,快速冷却组a*值在0~72 h内高于常规冷却组,但2个处理组a*值差异不明显,宰后120~216 h,快速冷却组a*值极显著(P<0.01)高于常规冷却组。随贮藏时间的推移,2种冷却方式下的牦牛肉其b*值均呈现上升的趋势。宰后0~24 h,常规冷却组b*值虽高于快速冷却组,但差异不明显,贮藏至24 h以后,常规冷却组b*值明显高于快速冷却组(P<0.01)。
表2 冷却方式对肌肉色度的影响
Table 2 Effect of chilling methods on L*、a*、b*of muscle
贮藏时间/hL*a*b*常规冷却快速冷却常规冷却快速冷却常规冷却快速冷却028.30±0.13G28.30±0.13f14.15±0.56E14.15±0.56e2.50±0.29G2.50±0.29f329.26±0.42F28.48±0.40f15.95±0.41D15.25±0.41d2.86±0.21G2.55±0.20f630.76±0.32E29.79±0.70e18.04±0.55C17.02±0.47c3.38±0.29F3.19±0.11e1231.81±0.65D30.61±0.66e18.99±0.36B18.33±0.32b3.72±0.29F3.39±0.14e2433.43±0.44C32.49±0.75d19.38±0.77B18.87±0.35b4.41±0.25E4.03±0.28d7236.55±0.42A*35.41±0.37c20.78±0.47A19.94±0.50a5.50±0.29D*4.91±0.11c12035.88±0.32A**37.64±0.53a17.72±0.36C**20.28±0.69a6.83±0.35C**5.18±0.12c16834.85±0.34B**36.42±0.57b14.40±0.54E**17.12±0.55c7.75±0.34B**6.17±0.25b21633.01±0.31C**35.58±0.40bc11.87±0.41F**12.95±0.65f8.84±0.13A*7.95±0.24a
2.3 冷却方式对肌肉剪切力的影响
剪切力值越低,肌肉嫩度越好,因而剪切力被用来评价肉的嫩度。图2显示,随着贮藏时间的延长,牦牛肉的剪切力值在两种冷却方式处理下,均呈先上升后降低的变化趋势。贮藏过程中,快速冷却组剪切力值高于常规冷却组,且在宰后120、168 h时极显著高于常规冷却组(P<0.01)。常规冷却组剪切力值升高较慢,于72 h达到最大值,随后显著下降(P<0.05)并逐渐趋于稳定,而快速冷却组升高较快,贮藏至120 h达到最大值,随后显著下降(P<0.05)。
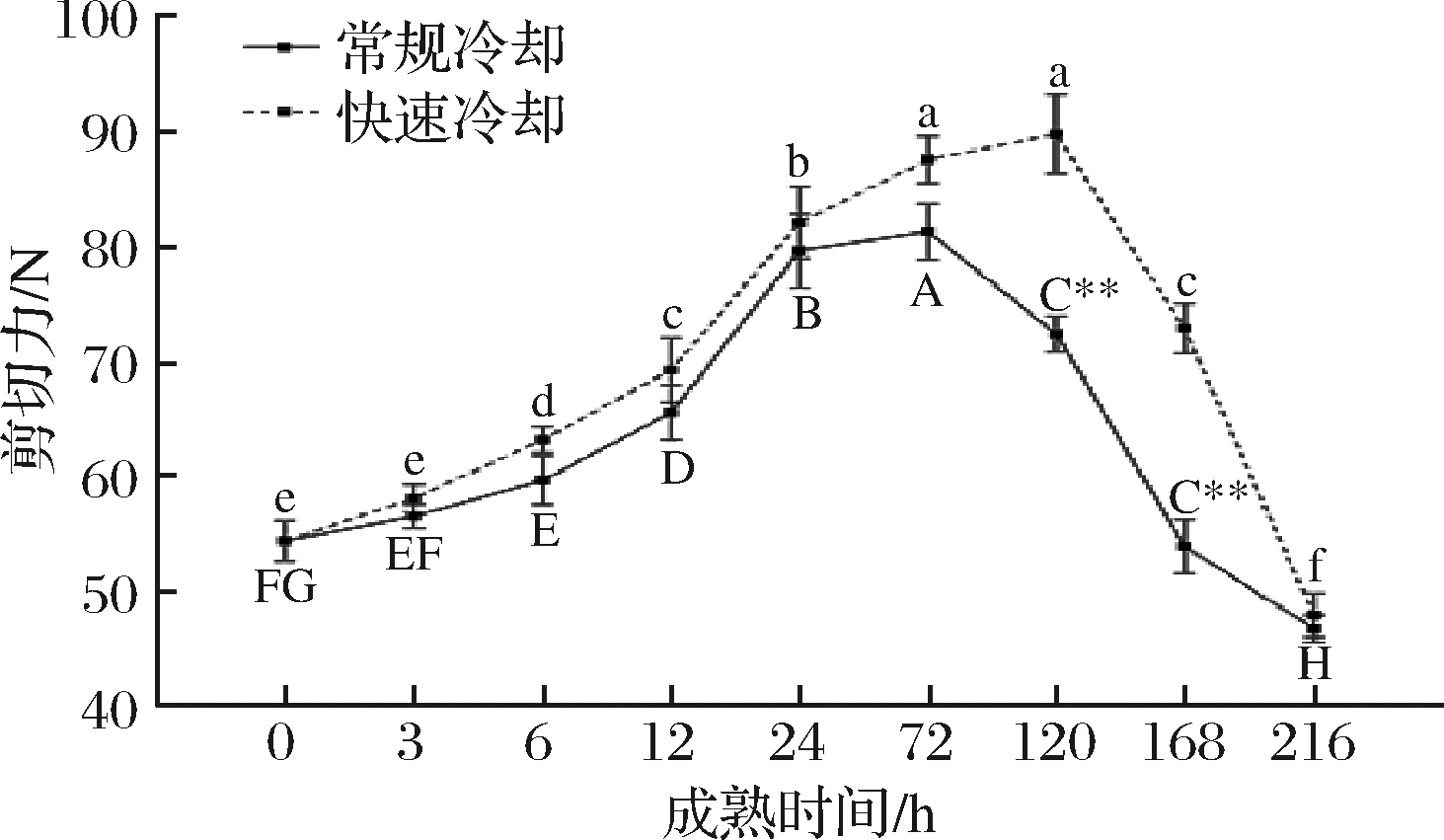
图2 冷却方式对肌肉剪切力的影响
Fig.2 Effect of chilling methods on shear force of muscle
2.4 冷却方式对肌肉加压损失的影响
由图3可知,在宰后贮藏过程中,两处理组肉样加压损失均呈先上升后下降的变化趋势。在宰后0~72 h,常规与快速2组加压损失逐渐增加,并于72 h 达到最大值35.74、31.84,差异显著(P<0.05),且在成熟至6、12、24 h时,常规冷却组加压损失显著(P<0.05)或极显著(P<0.01)高于快速冷却组。同时,在宰后6、12、24、72 h,快速冷却组加压损失比常规冷却组加压损失分别减少了14.84%、17.33%、13.66%、10.91%。宰后成熟72 h之后,两处理组加压损失均呈下降趋势,但2组差异不显著(P>0.05)。
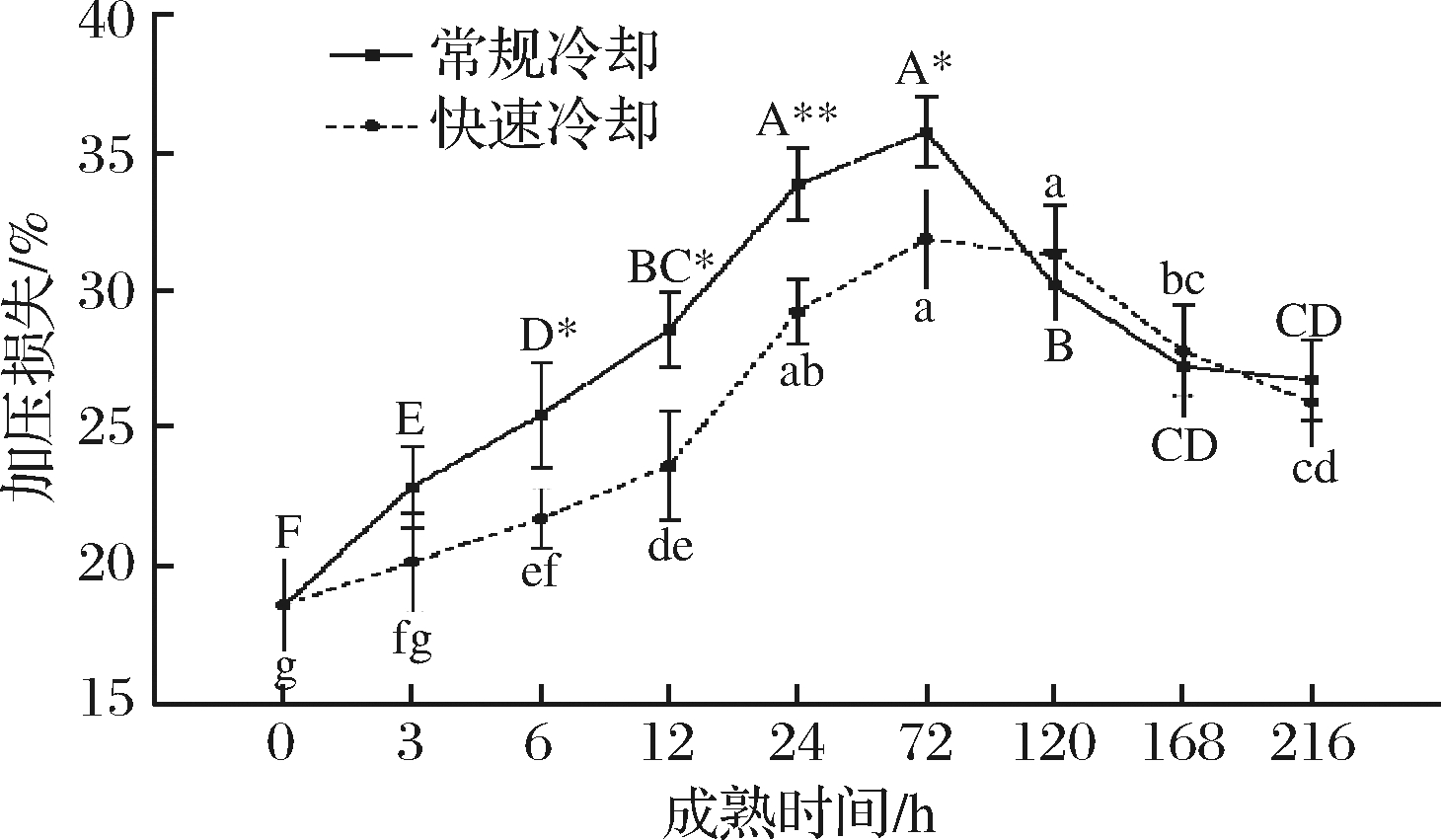
图3 冷却方式对肌肉加压损失的影响
Fig.3 Effect of chilling methods on pressure loss of muscle
2.5 冷却方式对肌肉蒸煮损失的影响
由图4可知,随着贮藏时间的延长,两处理组肉样蒸煮损失均呈先上升后趋于稳定的变化趋势,且在0~72 h常规冷却组升高较快,72 h时常规与快速两组蒸煮损失较0 h时分别增加了50.66%、34.69%,差异显著(P<0.05)。同时在宰后12、24 h,快速冷却组蒸煮损失极显著低于常规冷却组(P<0.01),120~216 h,两处理组蒸煮损失虽出现波动,但两者间无显著差异(P>0.05)。
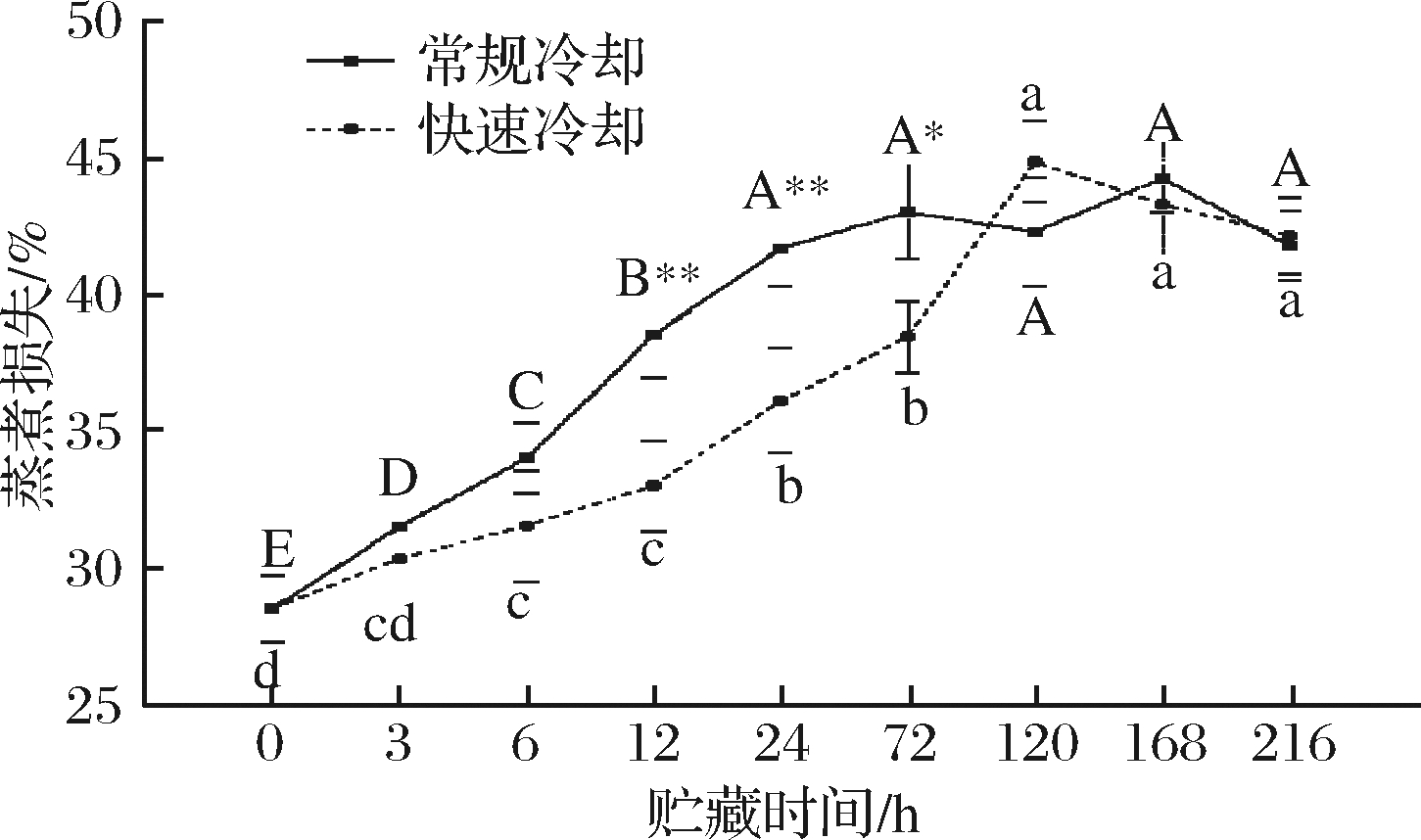
图4 冷却方式对肌肉蒸煮损失的影响
Fig.4 Effect of chilling methods on cooking loss of muscle
2.6 冷却方式对肌肉TVB-N的影响
宰后贮藏过程中挥发性盐基氮的变化如图5所示。由图5可以看出,2种冷却方式处理的牦牛肉背最长肌中TVB-N值在贮藏期间均呈逐渐增长的趋势。越到贮藏后期TVB-N值增长越迅速。常规冷却组TVB-N值在成熟3 h后显著增加(P<0.05),在宰后168 h时率先超过25 mg/100g。快速冷却组TVB-N值在宰后6 h之后开始显著增加(P<0.05),且在整个成熟阶段TVB-N值的变化速度明显小于常规冷却组。同时在宰后成熟中后期快速冷却组在各时间点的TVB-N值显著(P<0.05)或极显著(P<0.01)低于常规组。
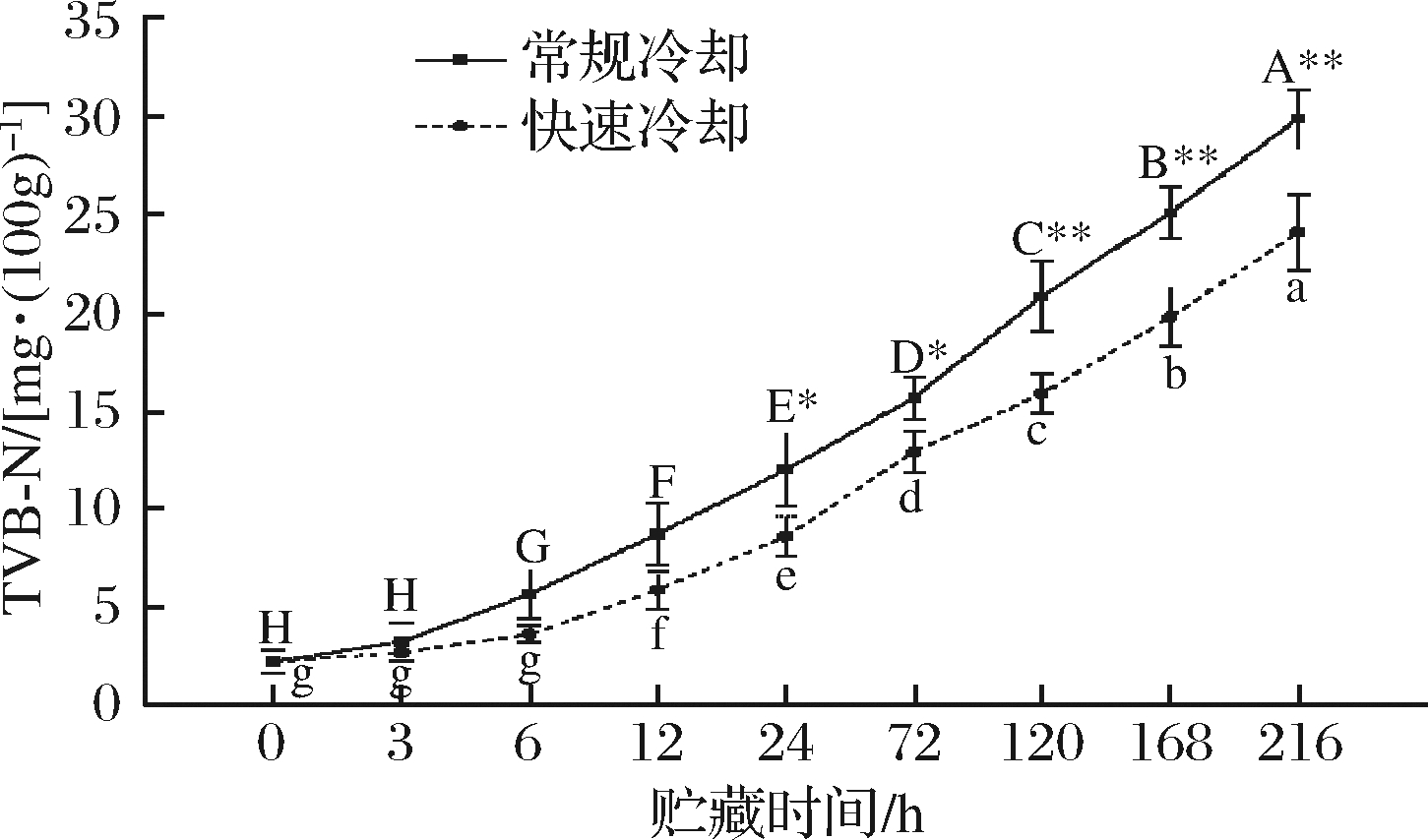
图5 冷却方式对肌肉TVB-N的影响
Fig.5 Effect of chilling methods on TVB-N of muscle
2.7 冷却方式对肌肉TBARS的影响
由图6可以看出,随着贮藏时间的延长,2种冷却方式处理的牦牛背最长肌中TBARS的含量均呈逐渐升高的趋势。在0 h时,肉样的TBARS含量为0.2 mg/kg,两处理组宰后初期TBARS含量上升缓慢,成熟6 h之后开始显著升高(P<0.05),且常规冷却组上升速率较快,于宰后168 h时TBARS含量已接近1.0 mg/kg。在宰后120、168、216 h,两处理组TBARS含量差异极显著(P<0.01),其中常规冷却组比快速冷却分别增加了16.92%、16.05%、18.37%。
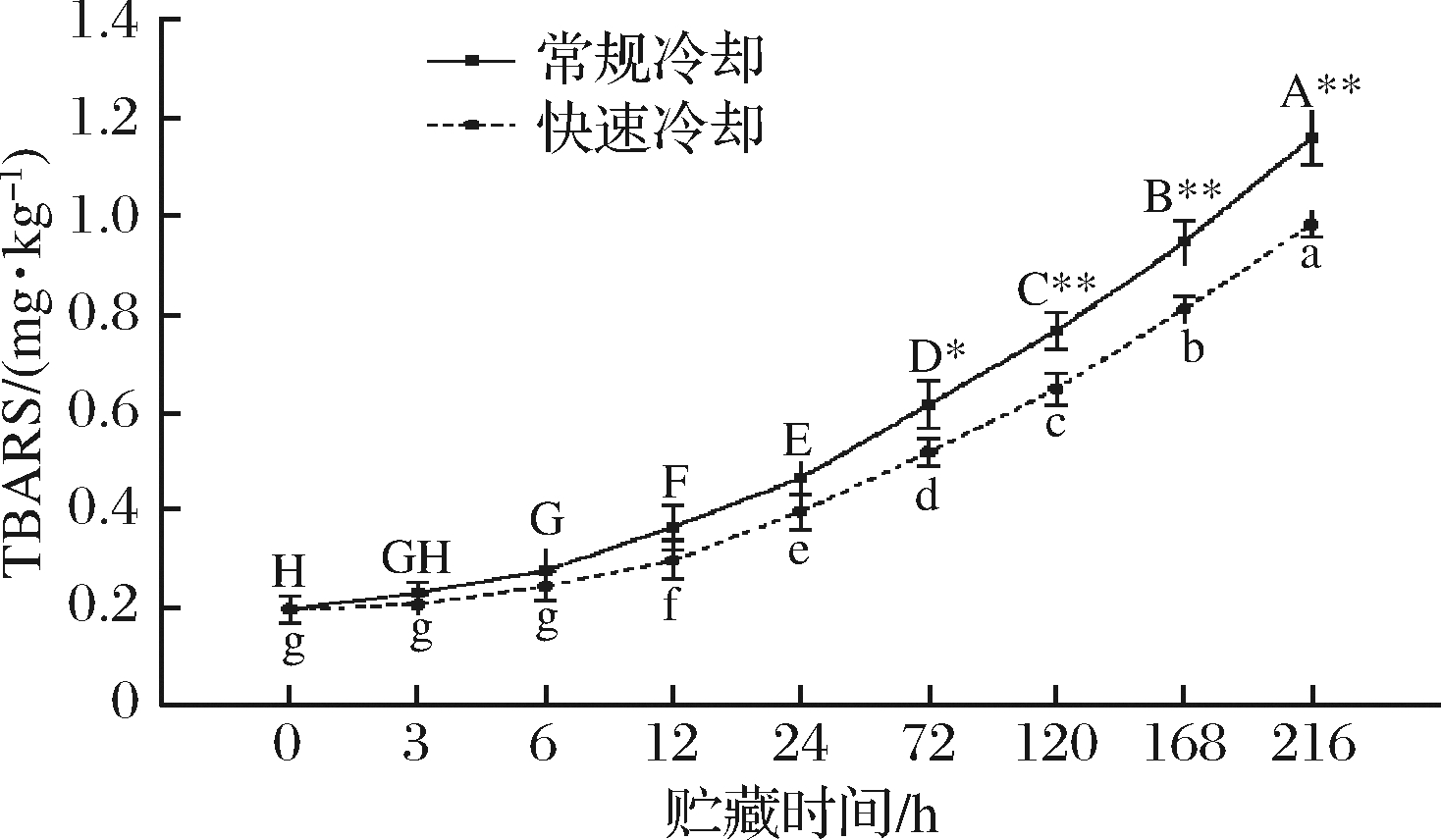
图6 冷却方式对肌肉TBARS值的影响
Fig.6 Effect of chilling methods on TBARS value of muscle
2.8 冷却方式对肌肉感官指标的影响
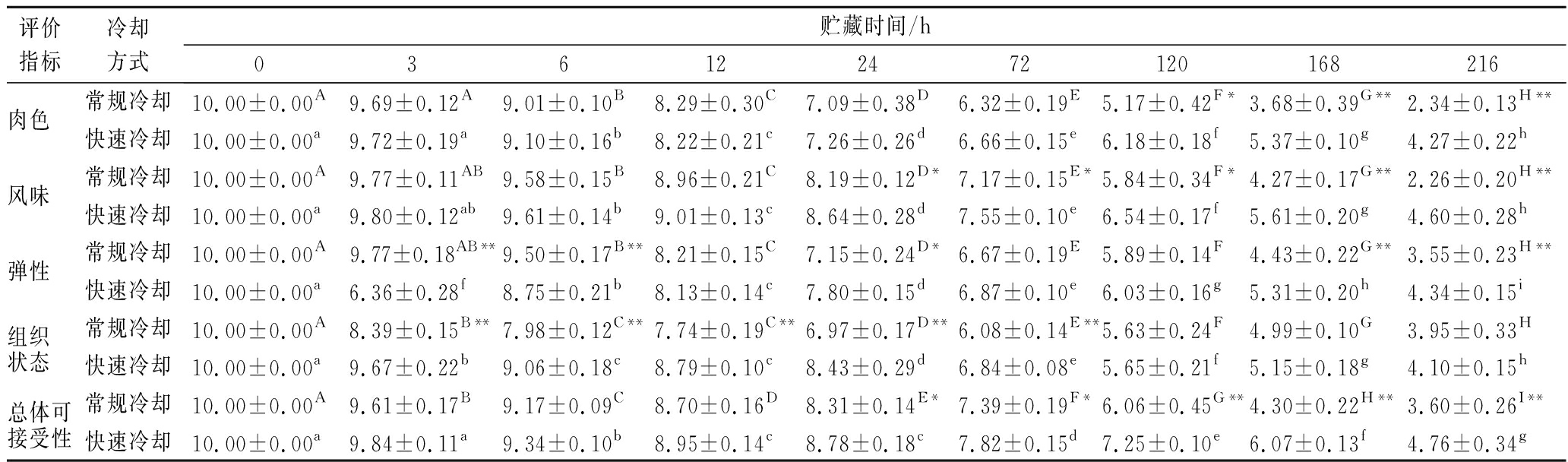
由表3可以看出,随着贮藏时间的延长,两处理组牦牛肉贮藏期间整体感官指标评分逐渐降低。贮藏初期,两处理组肉样在颜色、气味、表面渗水性和总体可接受性的感官评分差异不显著(P>0.05)。24 h 之后,2组感官评分差异显著增加。快速冷却组肉色在宰后168~216 h极显著高于常规组(P<0.01);肉的风味在24 h开始出现显著差异(P<0.05),且随着贮藏时间的延长,差异显著(P<0.01);快速冷却组在宰后初期3~6 h时,弹性极显著低于常规冷却组(P<0.01),在贮藏至168~216 h时弹性极显著高于常规冷却组(P<0.01);两处理组肉样组织状态的感官评分在贮藏前期差异极显著(P<0.01),后期这种差异逐渐降低,常规组在贮藏至168 h时,肉色深暗、有明显异味、弹性几乎消失、表面发黏严重且水分较多,在总体感官上已不能接受,而快速组肉样在216 h时才出现这种情况。
表3 冷却方式对牦牛肉贮藏过程中感官评价指标的影响
Table 3 Effect of chilling methods on sensory evaluation index of yak meat during storage
评价指标冷却方式贮藏时间/h036122472120168216肉色 常规冷却10.00±0.00A9.69±0.12A9.01±0.10B8.29±0.30C7.09±0.38D6.32±0.19E5.17±0.42F*3.68±0.39G**2.34±0.13H**快速冷却10.00±0.00a9.72±0.19a9.10±0.16b8.22±0.21c7.26±0.26d6.66±0.15e6.18±0.18f5.37±0.10g4.27±0.22h风味 常规冷却10.00±0.00A9.77±0.11AB 9.58±0.15B8.96±0.21C8.19±0.12D*7.17±0.15E*5.84±0.34F*4.27±0.17G**2.26±0.20H**快速冷却10.00±0.00a9.80±0.12ab9.61±0.14b9.01±0.13c8.64±0.28d7.55±0.10e6.54±0.17f5.61±0.20g4.60±0.28h弹性 常规冷却10.00±0.00A9.77±0.18AB**9.50±0.17B**8.21±0.15C7.15±0.24D*6.67±0.19E5.89±0.14F4.43±0.22G**3.55±0.23H**快速冷却10.00±0.00a6.36±0.28f8.75±0.21b8.13±0.14c7.80±0.15d6.87±0.10e6.03±0.16g5.31±0.20h4.34±0.15i组织 常规冷却10.00±0.00A8.39±0.15B**7.98±0.12C**7.74±0.19C**6.97±0.17D**6.08±0.14E**5.63±0.24F4.99±0.10G3.95±0.33H状态 快速冷却10.00±0.00a9.67±0.22b9.06±0.18c8.79±0.10c8.43±0.29d6.84±0.08e5.65±0.21f5.15±0.18g4.10±0.15h总体可常规冷却10.00±0.00A9.61±0.17B9.17±0.09C8.70±0.16D8.31±0.14E*7.39±0.19F*6.06±0.45G**4.30±0.22H**3.60±0.26I**接受性快速冷却10.00±0.00a9.84±0.11a9.34±0.10b8.95±0.14c8.78±0.18c7.82±0.15d7.25±0.10e6.07±0.13f4.76±0.34g
3 讨论
影响肉品质最关键的指标是pH,其与保水性、嫩度和色度等评价指标共同决定着肉的食用品质的优劣,同时各个品质评价指标之间也存在很强的关联性[13]。本研究中,肌肉pH值随着宰后贮藏时间的延长呈现先降低后升高的变化趋势,这主要是因为动物在被屠宰放血之后,呼吸作用停止,从而使得机体长期处于无氧状态,破坏了肌肉组织和细胞的正常新陈代谢,肌肉中的肌糖原在无氧呼吸链中的糖酵解过程中被不断分解,最终产生乳酸,使得宰后肌肉pH下降。之后由于肌肉本身以及肉表面存在的各种微生物分泌的蛋白酶对机体蛋白质起到了一定的降解作用,使其空间结构破坏肽键水解为多肽和氨基酸等,随之释放出碱性物质,从而引起肌肉pH值回升。宰后贮藏前期,常规冷却组pH下降速率显著高于快速冷却组,这主要是因为胴体温度与机体内的生化反应速率呈正相关[14]。快速冷却方式下,低温减缓了糖原的酵解速度,使肌肉进入僵直期需要更长的时间。同时,两处理组分别在宰后72、120 h达到极限pH,但2种冷却方式下极限pH之间无显著差异,这说明快速冷却虽减缓了pH的下降速率但未引起极限pH的变化。
肉的色泽是最能直观反映肉品质的指标[15]。目前对色泽的测定多采用色度计,结果表示为L*、a*、b*值。L*、a*值与肌红蛋白的状态有显著相关性[16]。此研究结果显示,牦牛肉在宰后贮藏过程中,两处理组L*、a*值均随着贮藏时间的延长呈现先上升后下降的趋势。这可能是由于宰后肌肉进入僵直期导致肌纤维缩短硬化,使处于肌纤维间隙中的水分溢出并附着于肌肉表面,从而肌肉对光的反射能力得以加强,L*值表现出升高趋势。随后肌肉中肌红蛋白周围的水分不断蒸发减少,逐渐增大了氧气和肌红蛋白的接触面积,使得肌红蛋白被氧化为高铁肌红蛋白肉色呈现出褐色。与此同时,贮藏后期肌肉pH值呈现缓慢上升趋势,由于高于肌原纤维蛋白的等电点,使得肌原纤维和水分子结合更为紧密,导致肌肉吸收了更多的光,肌肉L*开始显著下降[17]。常规冷却组较快速冷却组肌肉L*值升高快,并提前达到最大值,这可能是由于常规冷却组肌肉提前进入僵直期,且4 ℃下失水率更高,使得外渗水对光的反射能力更强,L*值较高。本试验中,宰后贮藏至216 h时,肉样a*值较0 h显著降低且快速冷却组 a*值在贮藏后期显著高于常规冷却组,这主要是因为快速冷却处理下较低温度减缓了肌肉的成熟进程,导致肌红蛋白合成高铁肌红蛋白的速度和数量降低。b*值的大小主要反映的是肌肉脂质氧化的程度和微生物的增值多少情况[18]。贮藏过程中快速冷却组b*值在贮藏后期显著低于常规冷却组,这说明快速冷却处理能较好抑制肉表面微生物的生长繁殖,同时减缓了脂肪氧化的速率,使得快速冷却组肌肉未发生剧烈氧化。
嫩度是消费者在选择和购买肉时最为关注的衡量指标之一,通常用剪切力值的大小来评价,剪切力值越低相应的肉的嫩度就越好[19]。本研究结果显示,随着宰后贮藏时间的延长,两处理组牦牛背最长肌剪切力值总体呈先增加后降低的变化规律,这与HWANG等[20]研究结果类似。其原因主要是宰后肌肉贮藏过程中会很快进入僵直阶段,这时肌肉中一些重要的蛋白质会随pH降低至极限pH的过程中发生沉降,使得肌肉收缩硬化,水分流失增加,嫩度变差,剪切力增加;僵直期结束后,肌肉进入解僵阶段,肌原纤维蛋白和细胞骨架蛋白在机体内源蛋白酶的作用下进行降解,使肉的嫩度得到改善,剪切力降低。常规冷却组于宰后72 h率先达到最大剪切力值,这是因为4 ℃下肌肉进入僵直期较快,而在宰后72 h时快速冷却组仍处于僵直期,所以剪切力值依旧在升高。常规冷却组在贮藏72 h之后,肌原纤维蛋白被内源蛋白酶不断降解,且降解速度较快,剪切力值开始显著下降后逐渐趋于稳定。快速冷却组由于前期低温使糖酵解过程中的关键酶和内源酶活性受到抑制,导致糖酵解和肌原纤维蛋白的降解速率减缓,宰后120 h才达到剪切力最大值[21]。贮藏后期,内源酶活性恢复,对肌原纤维蛋白的降解加速,于宰后216 h时,两处理组剪切力值已无明显差异。纵观整个贮藏过程,快速冷却组剪切力值虽然在120~168 h时极显著高于常规冷却组,但随后显著下降,可通过贮藏时间的延长得到改善。
保水性是生鲜肉重要的品质评价指标之一,直接关系着肉品加工企业的经济效益。蒸煮损失是模拟由生肉加工成食用肉的过程中水分蒸发等原因而造成肉质量减少的程度。而加压损失则反映了施加外部压力情况下生肉保持其水分的能力。在此试验中,两种冷却方式处理下,加压损失和蒸煮损失在宰后0~72 h均逐渐上升,这种情况极可能的原因是在宰后呼吸停止的情况下,肌肉进行无氧糖酵解,产生乳酸引起机体pH值降低,同时使得肌肉蛋白质净电荷减少,从而减弱了蛋白质之间排斥力,使得其相互靠近,分子间间隙缩小,将水分从其间挤出,从而肌肉失水率升高,保水性下降[22]。宰后贮藏至72 h以后,2种冷却方式下肌肉的加压损失开始下降,蒸煮损失逐渐趋于稳定,这主要是由于随着宰后成熟的继续进行,肌肉进入解僵阶段,内源蛋白酶的作用使得肌原纤维蛋白发生降解,导致细胞骨架蛋白体积增大,肌纤维间的间隙也增大[23]。同时在空间位移的作用下,细胞外的水分倒流重新进入细胞内部,从而增加了肌肉的保水性。李婉竹等[24]研究表明,肌肉保水性与pH有关,pH下降速度越快,保水性越差。本试验中在宰后0~72 h时,快速冷却由于前期低温处理减缓了肌肉pH值的下降速率,同时低温也有效地抑制了肌肉内环境中相关代谢酶的活性,使代谢速率得到控制,从而使得宰后贮藏至72 h时快速冷却组加压损失和蒸煮损失低于常规冷却组。贮藏后期,由于肌肉进入解僵阶段,pH出现缓慢回升,但两处理组pH上升速率差异不明显,所以两处理组的加压损失和蒸煮损失在贮藏后期开始缓慢下降并趋于稳定。此外,由于快速冷却组进入解僵期的时间滞后于常规冷却组,其更低的肌肉中心温度使得肉中生成小晶体,进行热处理时,会加剧温度对肌肉的影响程度,同时对蒸煮损失产生一定的影响。也正因此,常规冷却组的加压损失和蒸煮损失略低于快速冷却组。综上可知,快速冷却在一定程度上可以明显提高肉的保水性。
脂肪氧化是肉在贮藏过程中普遍存在的一种现象。脂肪氧化的程度与肉的风味、色泽及营养价值等有关。目前被用于评价肉品脂肪氧化程度的指标有很多,而硫代巴比妥酸反应产物就是其中之一,随着肉的氧化程度升高其值逐渐升高。油脂中硫代巴比妥酸反应生成的产物和不饱和脂肪酸被氧化分解后产生的丙二醛的多少直接决定了TBARS值的大小[25]。通常情况下,人们感官能感知到的最低酸败值为1.0 mg/kg。本试验结果显示,宰后0~6 h内两处理组TBARS值上升缓慢,这表明在肉样贮藏前期,牦牛肉中并未有过多的氧化作用发生,或者说这种氧化作用产生的影响微乎其微。12 h之后,TBARS值显著上升,说明牦牛肉开始进入了氧化阶段。同时在贮藏时间增加的情况下,脂肪氧化的速度也逐渐加快。整个贮藏期间,常规冷却组的硫代巴比妥酸反应产物值在贮藏初期虽高于快速冷却组,但两者差异并不明显。但是,在72~216 h时常规冷却组TBARS值显著或极显著高于快速冷却组,且在168 h时TBARS值已接近1.0 mg/kg,而快速冷却组TBARS值在216 h时还未达到1.0 mg/kg。这说明快速冷却处理的牦牛肉至少在216 h后肉品质才会开始变质,而常规冷却处理的牦牛肉在贮藏168 h之后肉品质就已开始变质。由此可见,快速冷却组由于温度相对较低,减缓了牦牛肉脂肪氧化速度。
TVB-N是肉及肉制品由于受到外界微生物污染,并且在贮藏过程中微生物大量繁殖而不断侵入到肌肉深层组织,导致蛋白质分解所形成的产物。TVB-N值越大,蛋白氧化越严重[26]。TVB-N作为目前用于评价肉的新鲜度最主要的指标之一。依据GB 2707—2016《食品安全国家标准 鲜(冻)畜、禽产品》中规定:鲜肉的挥发性盐基氮(TVB-N)值不超过15 mg/100g;当挥发性盐基氮值大于25 mg/100g为腐败肉。本次试验研究发现,随着贮藏时间的延长,两处理组牦牛背最长肌中挥发性盐基氮的含量均呈逐渐上升的趋势,且越到贮藏中后期挥发性盐基氮含量增长速率越快。其原因可能是因为宰后无氧糖酵解途径中产生的乳酸以及ATP磷酸化过程中生成的酸性物质会使得细胞内环境酸化,导致肌节因受到刺激而收缩,肌肉呈现僵直收缩状态。此时,因肌肉收缩而产生的力会损坏部分肌纤维,而使得肌浆中的蛋白酶被释放出来,催化蛋白质水解为肽等中间产物[27]。同时在蛋白酶催化水解蛋白质的过程中,也会产生一定量的胺、氮等盐基氮类含氮物质,并随着酶促作用渐增。随着时间的延长,宰后肌肉进入成熟阶段,机体内环境中的蛋白酶会继续水解蛋白质产生肽类等物质,为肉表面的微生物大量繁殖提供了营养物质。此外,机体内存在的某些特殊性蛋白质还会分解细菌,同时产生胞外蛋白酶,进而对蛋白质进行进一步降解。所以,肌肉在内外环境因素的共同作用下,其所含的蛋白质会产生大量的伯胺、仲胺和叔胺等盐基氮类含氮物[28]。微生物代谢所产生的一些含氮物质会使得挥发性盐基氮含量在贮藏后期大幅度增高[18]。常规冷却组挥发性盐基氮含量在整个贮藏阶段均高于快速冷却组。常规组于宰后3 h,挥发性盐基氮含量开始显著上升,而快速冷却组在宰后6 h才开始显著升高。这可能是由于快速冷却前期的温度较低,对微生物生长和蛋白酶的活性起到了抑制作用,从而使得挥发性盐基氮含量的增长时间推迟。常规冷却组在在贮藏至168 h时挥发性盐基氮含量已高于25 mg/100g的标准,成为腐败肉,而快速冷却组牦牛肉贮藏至216 h时挥发性盐基氮含量仍低于25 mg/100g的标准,说明此时的牦牛肉仍属于次级鲜肉。因此,快速冷却可以明显降低牦牛肉的蛋白氧化作用,从而提高牦牛肉的货架期。
感官评价主要从肉色、风味、弹性、组织状态等方面进行[29]。试验结果表明,2种冷却方式处理的牦牛肉在贮藏期间各项感官评分值均随着时间的延长而逐渐降低,这是因为随着贮藏时间的延长,机体自身生理生化反应的发生和微生物的生长繁殖,导致肉色变暗、结构松散、弹性变差并出现异味,这与黄彩燕等[12]对湿热地区不同季节市售鲜牛肉贮藏期间新鲜度变化的感官评价结果相似。贮藏初期,两处理组肉色、风味、总体可接受性差异不明显,而到后期,2组间的差异越来越大,其原因主要是快速冷却方式下,低温抑制了宰后牦牛肉贮藏过程中关键酶的活力,同时也减缓了肉表面微生物的生殖代谢活动。随着贮藏时间的延长,前期温度对酶的抑制作用解除,宰后机体适应环境温度后生化反应开始进行,但反应时间也相应地延长,从而导致在贮藏后期同一时间点两处理组间的差异逐渐增大。两处理组肉样组织状态在贮藏3~72 h内差异极显著,随后这种差异逐渐消失。这主要是因为前期pH的下降引起蛋白质间引力增强使得分子间水分被溢出,导致肉表面水分增加,之后由于贮藏过程中水分蒸发损失,蛋白降解使细胞间间隙变大,2组间差异又逐渐缩小[23]。此外,快速冷却组肉样组织状态的总体评分高于常规冷却组的原因是因为快速冷却的低温使得pH下降速率小于常规组,肌肉pH下降速率越快,失水率就越高。
4 结论
常规与快速两组牦牛肉在贮藏至216 h时剪切力值均显著低于0 h的剪切力值,牦牛肉嫩度得到改善。快速冷却显著降低了72 h内加压损失率和蒸煮损失率,且在120~216 h两组L*、a*、b*值差异极显著,提高了肉的整体保水性和色度。此外,快速冷却在贮藏0~6 h能够明显减缓脂肪氧化和蛋白质氧化作用,使牦牛肉保鲜期延长48 h左右。
[1] 韩玲.白牦牛产肉性能及肉质测定分析[J].中国食品学报,2002(4):30-35.
[2] WHITE A,O'SULLIVAN A,TROY D J,et al.Effects of electrical stimulation,chilling temperature and hot-boning on the tenderness of bovine muscles[J].Meat Science,2006,73(2):196-203.
[3] HOFFMAN L C,CLOETE S W P,SCHALKWYK S J V,et al.Effect of bleeding method and low voltage electrical stimulation on meat quality of ostriches[J].South African Journal of Animal Science,2009,39(3):206-213.
[4] MUELA E C,SA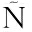 UDO,CAMPO M M,et al.Effects of cooling temperature and hot carcass weight on the quality of lamb[J].Meat Science,2010,84(1):101-107.
UDO,CAMPO M M,et al.Effects of cooling temperature and hot carcass weight on the quality of lamb[J].Meat Science,2010,84(1):101-107.
[5] FERN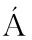 NDEZ A M,VIEIRA C.Effect of chilling applied to suckling lamb carcasses on hygienic, physicochemical and sensory meat quality[J].Meat Science,2012,92(4):569-574.
NDEZ A M,VIEIRA C.Effect of chilling applied to suckling lamb carcasses on hygienic, physicochemical and sensory meat quality[J].Meat Science,2012,92(4):569-574.
[6] 惠小洋,余群力,曹晖,等.两种冷却方式对宰后成熟过程中牛肉保水性的影响[J].食品与发酵工业.2018,44(11):193-199.
[7] 孙京新,周光宏,徐幸莲,等.冷却猪肉加工过程卫生标准操作程序[J].肉类工业,2003(3):34-41.
[8] FAROUK M M,WIELICZKO K J,MERTS I.Ultra-fast freezing and low storage temperatures are not necessary to maintain the functional properties of manufacturing beef[J].Meat Science,2004,66(1):170-179.
[9] 贾娜,李博文,孔保华.盐水注射及食用胶对酱牛肉品质的影响[J].食品与发酵工业,2015,41(3):96-99.
[10] 中华人民共和国国家卫生和计划生育委员会.GB 5009.228―2016食品中挥发性盐基氮的测定[S].北京:中国标准出版社,2017.
[11] 张宏博,王贵印,袁倩,等.巴美羊肉脂肪氧化的研究[J].肉类工业,2013(11):29-34.
[12] 黄彩燕,孙宝忠,韩玲,等.不同贮藏温度市售热鲜牛肉新鲜度变化研究[J].中国畜牧兽医,2018,45(4):1 106-1 113.
[13] 毛衍伟.快速冷却和电刺激对牛肉品质的影响及其机理研究[D].泰安:山东农业大学,2011.
[14] BERTRAM H C,DØNSTRUP S,KARLSSON A H,et al.Post mortem energy metabolism and pH development in porcine M.longissimus dorsi as affected by two different cooling regimes.A(31)P-NMR spectroscopic study[J].Magnetic Resonance Imaging,2001, 19(7):993-1 000.
[15] SUMAN S P,HUNT M C,NAIR M N,et al.Improving beef color stability:Practical strategies and underlying mechanisms[J].Meat Science,2014,98(3):490-504.
[16] 马秀利.CaCl2处理对不同品种牛肉成熟过程中品质及能量代谢的影响[D].兰州:甘肃农业大学, 2018.
[17] 巨晓军,屠云洁,邹剑敏,等.不同货架期对冷鲜鸡肉品质的变化及相关性分析[J].中国畜牧杂志,2017(11):106-109.
[18] 金文刚.冷却方式对羊胴体成熟期间主要理化性质及食用品质的影响[D].银川:宁夏大学,2008.
[19] 刘璐,苏玉虹,王军,等.猪肉嫩度相关QTL整合定位与基因关联分析研究[J].中国农学通报.2012,28(20):37-42.
[20] HWANG I H,PARK B Y,CHO S H,et al.Effects of muscle shortening and proteolysis on Warner-Bratzler shear force in beef longissimus and semitendinosus[J].Meat Science,2004,68(3):497-505.
[21] 马晓冰,苏琳,林在琼,等.不同品种肉羊肌肉的糖酵解潜力及其与肉品质的相关性[J].食品科学,2015,36(15):1-4.
[22] 余小领.冷冻和解冻工艺对猪肉保水性和组织结构的影响研究[D].南京:南京农业大学, 2007.
[23] AGYARE K K,ADDO K,XIONG Y L.Emulsifying and foaming properties of transglutaminase-treated wheat gluten hydrolysate as influenced by pH,temperature and salt[J].Food Hydrocolloids,2009,23(1):72-81.
[24] 李婉竹,梁琪,张炎,等.不同冻融次数下牦牛肉蛋白质氧化与保水性的关系[J].食品科学,2018,39(2):14-19.
[25] 马骋,文鹏程,梁琪,等.不同含氧包装方式对牦牛肉保鲜效果的影响[J].食品与发酵工业,2016,42(6):187-192.
[26] 李苗云,张秋会,高晓平,等.冷却猪肉贮藏过程中腐败品质指标的关系研究[J].食品与发酵工业,2008,34(7):168-171.
[27] 熊国远.致昏、禁食方式和贮藏温度对獭兔肉品质的影响研究[D].南京:南京农业大学,2006.
[28] 彭勇.冷却猪肉常见腐败微生物致腐能力的研究[D].北京:中国农业大学,2005.
[29] 石丽敏,黄岚,梁志宏.冷鲜猪肉的新鲜度评价研究进展[J].肉类研究,2011(12):40-43.